Efecto antitumoral de nanopartículas de sílice mesoporosa dirigidas anti-VEGFR2 marcado con 131I en el cáncer de tiroides anaplásico
Resumen
El cáncer de tiroides anaplásico (ATC) comprende aproximadamente el 2% de todos los cánceres de tiroides y su tasa de supervivencia media sigue siendo baja debido a su resistencia a la terapia convencional. Las nanopartículas de sílice mesoporosas cargadas terapéuticamente con receptor del factor de crecimiento endotelial vascular (VEGFR) representan un avance importante para la obtención de imágenes de angiogénesis y la inhibición en cánceres letales. En el presente estudio, nuestro objetivo era evaluar si 131 Las nanopartículas de sílice mesoporosas dirigidas anti-VEGFR2 marcadas con I tendrían eficacia antitumoral en un modelo de ratón desnudo portador de tumor ATC. Utilizando estudios in vitro e in vivo, investigamos el aumento de la capacidad de direccionamiento y el tiempo de retención en el grupo dirigido anti-VEGFR2 utilizando microscopía confocal y un contador γ. La radiactividad del tejido tumoral del grupo dirigido anti-VEGFR2 a las 24 y 72 h después de la inyección intratumoral fue significativamente mayor que la de los grupos no dirigidos (todos P <0,05). Además, descubrimos que la acumulación radiactiva era obvia incluso 3 semanas después de la inyección en el grupo objetivo anti-VEGFR2 mediante tomografía computarizada / tomografía computarizada por emisión de fotón único, que no se observó 3 días después de la inyección en el grupo de Na 131 Yo agrupo. Mientras tanto, en comparación con el grupo no dirigido, el crecimiento tumoral en el grupo dirigido se inhibió significativamente, sin causar efectos tóxicos sistémicos aparentes. Además, el tiempo medio de supervivencia en el grupo objetivo (41 días) se prolongó significativamente en comparación con el del grupo no objetivo (34 días) o Na 131 I (25 días) grupos (ambos P < 0,01). Nuestros datos respaldan la opinión de que el 131 desarrollado Las nanopartículas de sílice mesoporosas dirigidas anti-VEGFR2 marcadas con I mostraron resultados prometedores en el modelo de ratón portador de tumores ATC y tal enfoque podría representar una nueva opción terapéutica para ATC.
Antecedentes
El cáncer de tiroides anaplásico (ATC) solo representa aproximadamente el 2% de todos los cánceres de tiroides; sin embargo, es un tipo de tumor localmente agresivo que tiene una alta tasa de metástasis a distancia. Generalmente, la mediana de supervivencia de los pacientes con ATC es de aproximadamente 6 meses, y solo el 20% de los pacientes sobreviven 1 año después del diagnóstico debido a una catástrofe vascular y al colapso de las vías respiratorias causado por una enfermedad regional agresiva que invade los tejidos del cuello y los ganglios linfáticos y / o metástasis pulmonar [1 , 2]. Yodo radiactivo-131 ( 131 I) juega un papel importante en el diagnóstico y tratamiento de las metástasis del cáncer de tiroides diferenciado (CDT) [3, 4, 5]. Sin embargo, el 131 convencional I La modalidad de tratamiento no es apropiada para ATC debido a su característica de no concentrar yodo [6].
La angiogénesis es un factor importante que contribuye a la supervivencia, el crecimiento, la migración y la metástasis de las células cancerosas. El factor de crecimiento endotelial vascular (VEGF) es una citocina reguladora crucial en la angiogénesis y juega un papel importante en el desarrollo de ATC. El papel bien establecido de VEGF en la angiogénesis significa que los ligandos radiomarcados, como el bevacizumab, que se dirige al receptor de VEGF (VEGFR), se han desarrollado con éxito para la detección temprana y sensible de lesiones mediante tomografía por emisión de positrones (PET) y tomografía computarizada por emisión de fotón único ( SPECT) técnicas de imagen. El VEGFR-2 ejerce la mayoría de las funciones del VEGF en las células endoteliales de los vasos sanguíneos y es responsable de la proliferación a través de la activación de la vía de la proteína quinasa activada por mitógenos, la migración de los vasos endoteliales y la promoción de la angiogénesis y el crecimiento vascular [7, 8 ]. La expresión de VEGF está regulada al alza en las células ATC de origen epitelial en comparación con la del tejido tiroideo normal [9,10,11]. Se han desarrollado estrategias anti-VEGF para inhibir el crecimiento de nuevos vasos sanguíneos y privar a los tumores del oxígeno y los nutrientes necesarios. Varios estudios preclínicos han desarrollado fármacos que se dirigen al VEGFR2 en ATC con diferentes grados de éxito [12,13,14,15]. Sin embargo, uno de los principales desafíos relacionados con estos medicamentos contra el cáncer es su baja biodisponibilidad y su entrega ineficaz al sitio objetivo. Muchos medicamentos contra el cáncer son hidrófobos y necesitan sistemas de administración de medicamentos biocompatibles para mejorar su biodisponibilidad y facilitar la administración intravenosa.
Se pueden usar nanopartículas, incluidas nanopartículas a base de metales, polímeros y lípidos, para combinar un agente terapéutico con un agente de formación de imágenes. Los ligandos / fracciones dirigidas, tales como péptidos, anticuerpos, radionúclidos o fragmentos de anticuerpos, se pueden unir a nanopartículas para mejorar su eficacia terapéutica. Para el tratamiento del cáncer, las nanopartículas podrían acumularse en el área del tumor a través de un efecto mejorado de permeabilidad y retención, con la capacidad de administrar agentes terapéuticos de una manera más localizada. Durante muchos años, en las ciencias de los materiales y la ingeniería, la sílice se ha considerado un material versátil y relativamente seguro debido a la variedad de modificaciones físicas y químicas disponibles que ofrece, así como a su buena biocompatibilidad [16]. La Administración de Drogas y Alimentos de los Estados Unidos (FDA) reconoce la sílice como "generalmente segura" [17, 18]. Entre los diversos materiales a base de sílice, las nanopartículas de sílice mesoporosa (MSN) se destacan como una clase de nanomateriales con muchas ventajas distintivas, como su naturaleza no tóxica, buena permeabilidad superficial, alta área de superficie, estructuras de poros sintonizables, excelente estabilidad fisicoquímica, y superficies químicamente modificables, todas las cuales las convierten en huéspedes potenciales de diversos agentes químicos y / o fármacos terapéuticos [19]. De manera similar, se ha demostrado que los nanomateriales de carbono mesoporosos son excelentes nanoportadores en la administración de fármacos [20, 21, 22]. En los últimos años, los esfuerzos en el campo de las MSN se han centrado en combinar capacidades terapéuticas y de imágenes. El etiquetado de nanopartículas con sondas de imagen es una herramienta valiosa para permitir su seguimiento in vitro e in vivo. Actualmente, las modalidades de tratamiento dirigidas representan una estrategia alentadora para el tratamiento con ATC [23, 24].
Inspirados por el papel fundamental de la terapia dirigida y las imágenes moleculares contra el VEGFR en la investigación del cáncer y las ventajas que ofrecen los MSN, en este estudio, desarrollamos una nanoplataforma potencialmente teranóstica dirigida contra el VEGFR2 basada en la ingeniería de superficies de los MSN para obtener imágenes SPECT simultáneas no invasivas y una 131 mejorado in vivo Yo efecto terapéutico. Nuestro objetivo era determinar si 131 Los MSN dirigidos a anti-VEGFR2 marcados con I tendrían eficacia antitumoral en un modelo de ratón desnudo portador de tumores ATC, seguido de estudios exhaustivos in vivo, in vitro y ex vivo.
Materiales y métodos
Materiales
El medio Eagle modificado de Dulbecco (DMEM), tripsina-EDTA al 0,25% y suero bovino fetal (FBS) se adquirieron de Gibco (CA, EE. UU.). Los antibióticos (penicilina G, estreptomicina y nistatina) se adquirieron de Dingguo Biotechnology Co. Ltd. (Beijing, China). Bromuro de hexadeciltrimetilamonio (CTAB), ortosilicato de tetraetilo (TEOS), 3-aminopropiltrietoxisilano (APTES), dimetilsulfóxido (DMSO), 1- (3-dimetilaminopropil) -3-etilcarbodiimida clorhidrato (EDC) -hidroxisuccinimida (NHS) e isotiocianato de fluoresceína (FITC) se adquirieron de Sigma-Aldrich (Alemania). Na 131 Me compró en Atomic Hitech (Beijing, China). Los anticuerpos anti-VEGFR2 se adquirieron de Abcam Co. Ltd. (Reino Unido).
Caracterizaciones
Las nanopartículas se dispersaron en etanol, formando una suspensión, se depositaron sobre una rejilla de cobre recubierta de carbono y se secaron durante al menos 24 h. La morfología de las nanopartículas se determinó mediante microscopía electrónica de transmisión (TEM) (JEOL-100CXII, Japón) a un voltaje de aceleración de 200 kV. Los potenciales zeta y los diámetros hidrodinámicos de las muestras se midieron usando dispersión de luz dinámica (DLS) usando un Zetasizer (Nano ZS90, Reino Unido). Las distribuciones del tamaño de los poros y las áreas superficiales de los MSN se caracterizaron mediante análisis de Brunauer-Emmett-Teller (BET) y Barrett-Joyner-Halenda (BJH) (ASAP2020M, EE. UU.).
Cultivo celular
La línea celular ATC humana FRO [25] (comprada en Cell Resource Center, Instituto de Ciencias Médicas Básicas, Peking Union Beijing Medical College en Beijing, República Popular de China) se cultivó a 37 ° C en una incubadora humidificada con una mezcla de 5% CO 2 y 95% de aire y suplementado con 10% de FBS y 1% de penicilina-estreptomicina. El medio se reemplazó cada dos días, y las células se pasaron por tripsina después de que se alcanzó la confluencia. Las células se precultivaron hasta que se logró aproximadamente un 80% de confluencia antes de cada experimento.
Preparación y modificación de la superficie de nanopartículas de sílice
Síntesis de MSN y aminación
Los MSN se sintetizaron como se informó anteriormente [26]. Brevemente, se agregaron 50 mg de CTAB a una mezcla de 25 mL de agua, 5 mL de etanol y 100 μL de solución de NaOH 2 M en un matraz de fondo redondo con agitación continua a 70 ° C. Luego, se agregaron 200 μL de TEOS a la mezcla y se hizo reaccionar durante 1 h. Después, la solución de reacción se centrifugó y se lavó con etanol cinco veces a 10.000 rpm. A continuación, los productos se resuspendieron en 10 mL de etanol. Después de eliminar la plantilla de CTAB, el producto se volvió a suspender en 5 ml de DMSO y 100 μl de APTES, que se añadió gota a gota a la mezcla resultante para modificar la superficie de sílice por aminación. Después de agitar durante toda la noche, los precipitados se separaron por centrifugación, se lavaron con etanol cinco veces y luego el MSNs-NH 2 fueron obtenidos.
Síntesis de BSA-MSNs-Anti-VEGFR2
Se agregaron cinco miligramos de albúmina de suero bovino (BSA) y 50 μL de anticuerpos anti-VEGFR2 al producto anterior (MSNs-NH 2 , 50 mg) y se hizo reaccionar con agitación durante 2 h. La mezcla se lavó con agua cinco veces, después de lo cual se añadieron 1,1 mg de NHS y 1,6 mg de EDC a la mezcla y se agitó durante la noche a temperatura ambiente en 5 ml de agua. Los precipitados se separaron por centrifugación, se lavaron con agua cinco veces, con lo que se obtuvo con éxito el BSA-MSNs-anti-VEGFR2.
131 I Radiomarcaje de nanopartículas
Las nanopartículas producidas se marcaron radiactivamente con 131 Utilizo el método Cloramina-T (indicado como 131 I-BSA-MSN y 131 I-BSA-MSNs-anti-VEGFR2, respectivamente) [27]. En resumen, se diluyeron aproximadamente 100 μg de BSA-MSN o BSA-MSN-anti-VEGFR2 con 100 μL de tampón de fosfato (PB) y 74 MBq de 131 Fui agregado. Luego se añadió a la mezcla Cloramina-T (100 μL; 5 mg / mL en PB). Después de 60 s de agitación e incubación, la reacción se detuvo agregando 100 μL de metabisulfito de sodio (5 mg / mL en PB). El tubo de centrífuga se usó para separar BSA-MSN marcados y BSA-MSN-anti-VEGFR2 de compuestos de bajo peso molecular. La tasa de marcado y la pureza radioquímica de 131 Las nanopartículas marcadas se determinaron mediante cromatografía de capa fina.
Captación celular in vitro:estudio de microscopía confocal
En primer lugar, los MSN-anti-VEGFR2 y los MSN se marcaron con FITC [28]. Brevemente, MSNs-NH 2 (100 mg) a 1 ml de solución de alcohol FITC (1 mg / ml), con reposo durante 4 h con agitación. Los MSN marcados con FITC (FITC-MSN) se obtuvieron por centrifugación y se secaron al vacío. También se podría obtener FITC-MSNs-anti-VEGFR2 usando el mismo método.
Las células FRO se sembraron en placas de 6 pocillos durante la noche y luego 5 × 10 5 las células por pocillo se incubaron con FITC-MSN y FITC-MSN-anti-VEGFR2 durante 1 y 6 ha 37 ° C, respectivamente. Las células se lavaron tres veces con solución salina tamponada con fosfato (PBS) y luego se fijaron con etanol al 70% durante 20 min. Además, las células se lavaron tres veces con PBS y los núcleos se tiñeron con 4,6-diamidino-2-fenilindol (DAPI) durante 45 min y luego se fijaron con paraformaldehído (4% en PBS). Las imágenes de microscopía confocal se adquirieron mediante una microscopía de barrido láser confocal (CLSM) (Zeiss LSM 510, EE. UU.).
Captación celular dependiente del tiempo
Para medir la absorción celular de yodo-131 dependiente del tiempo de las nanopartículas, 1 × 10 5 las células por pocillo se cultivaron con 3,7 MBq / ml de Na 131 libre Yo, 131 I-BSA-MSN o 131 I-BSA-MSNs-anti-VEGFR2, respectivamente. Luego, las células se lavaron lo más rápido posible con 1 ml de solución tampón de solución salina equilibrada de Hanks (HBSS), se separaron con tripsina y se resuspendieron en 1 ml de HBSS durante 1, 2, 3, 5, 7 y 9 h. La radiactividad se midió usando un contador γ (LKB gamma 1261, Australia). Todos los experimentos se realizaron tres veces para obtener datos exactos.
Modelo animal
Se compraron ratones desnudos Balb / c (hembras, de aproximadamente 4 semanas de edad, con un peso de 15 a 20 g) del Centro de Investigación Animal Experimental de Beijing en el Peking Union Medical College y se mantuvieron en condiciones específicas libres de patógenos, con una humedad relativa (30-70 %) y ambiente de temperatura controlada (20–24 ° C) en el Centro de Animales de Laboratorio, Universidad Médica de Tianjin, China. Todos los procedimientos de manipulación de animales se realizaron de acuerdo con un protocolo aprobado por el Comité de Ética del Hospital General de la Universidad Médica de Tianjin. Se indujeron xenoinjertos de tumor FRO mediante inyección subcutánea de 5 × 10 6 Células FRO en 50 μL de PBS en el hombro derecho de los ratones.
Imágenes en vivo
Cuando los ratones desnudos portadores de tumores se alimentaron durante 1 a 2 semanas y el volumen del tumor había alcanzado aproximadamente 10 mm de diámetro, los ratones se dividieron al azar en tres grupos (Na 131 Yo, 131 I-BSA-MSN y 131 I-BSA-MSNs-anti-VEGFR2). Cada grupo recibió 7,4 MBq 131 I mediante inyección intratumoral para evaluar la localización de órganos de 131 Nanopartículas etiquetadas con I. Se realizaron imágenes gammagráficas 1, 2, 3, 7, 14 y 21 días después de la inyección del fármaco respectivo. Los ratones desnudos se anestesiaron con hidrato de cloral al 4% (150 μL) antes de cada escaneo, se colocaron en una posición prona y luego se tomaron imágenes con un escáner SPECT / CT (Discovery NM / CT 670, EE. UU.). Para evitar la exposición del tejido tiroideo a radiación e imágenes no deseadas, se añadió perclorato de sodio (0,05 mg / ml) al agua potable de todos los ratones 1 día antes del experimento y se mantuvo durante 1 semana.
Distribución de tejidos
A las 24 y 72 h después de la inyección intratumoral de 7,4 MBq 131 Nanopartículas etiquetadas con I, los ratones de cada grupo ( n =3 / grupo) se sacrificaron mediante dislocación cervical, y se extrajeron y pesaron el corazón, el bazo, el riñón, el hígado, el intestino, el pulmón y los tejidos tumorales. La radiactividad en varios órganos se midió utilizando un contador γ (LKB gamma 1261, Australia) y la radiactividad se expresó como porcentaje de la dosis inyectada por gramo de tejido (% ID / g).
In Vivo 131 Yo Terapia
De manera similar a las imágenes in vivo, a los ratones de los tres grupos se les inyectó intratumoralmente una dosis de 74 MBq (50 μL) de 131 I-BSA-MSNs-anti-VEGFR2, 131 I-BSA-MSN y Na 131 I, respectivamente, cuando el volumen del tumor había alcanzado unos 10 mm de diámetro. Se administró el mismo volumen de solución salina normal como grupo de control. El volumen del tumor se estimó utilizando la siguiente fórmula:volumen =4π / 3 (1/2 largo x 1/2 ancho x 1/2 alto) [15, 29]. El volumen del tumor y el peso corporal del animal se midieron cada 3 días. Los ratones fueron sacrificados si perdían más del 20% de su peso corporal o estaban moribundos.
Examen histológico
Cuando terminó el experimento, se sacrificaron los ratones y se aislaron el tumor y los tejidos normales de los cuatro grupos, incluidos el corazón, el hígado, el bazo, el riñón y el pulmón, para estudiar su histopatología. Brevemente, se desparafinaron secciones de parafina de 5 mm de espesor usando dos incubaciones con xileno (durante 30 min cada una a 56ºC) y luego se rehidrataron en etanol. A continuación, las secciones se remojaron durante la noche en sacarosa al 10% en agua destilada. A continuación, las secciones se lavaron en PBS 0,1 M, pH 7,4, se incubaron en peróxido de hidrógeno al 1,2% en metanol durante 30 min, y se aclararon en PBS 0,1 M, pH 7,4, durante 15 min. Los portaobjetos de los tumores se incubaron luego en una cámara húmeda durante la noche, a temperatura ambiente, con anticuerpos anti-VEGFR2 diluidos 1:100. Después de lavar tres veces con PBS, los portaobjetos se incubaron con el sistema de detección DAKO-REALTM En-Vision ™ durante 60 minutos, luego se visualizaron usando diaminobencidina y se contratiñeron con hematoxilina de Mayer. Todas las imágenes se adquirieron con un microscopio Olympus.
Análisis estadístico
Todos los datos se presentan como la media ± desviación estándar (DE), y el análisis estadístico se realizó con el paquete estadístico SPSS (Statistical Package for Social Sciences) 12.0 para Windows (SPSS, Chicago, IL, EE. UU.). El análisis de los datos se realizó mediante curvas de Kaplan-Meier y la prueba de rango logarítmico. Todas las pruebas estadísticas fueron de dos colas y una P valor <0.05 se consideró estadísticamente significativo.
Resultados
Las características de las nanopartículas
Las características de las nanopartículas fueron analizadas y determinadas por TEM y DLS (Fig. 1a-c). La imagen TEM demostró que los MSN tenían una morfología esférica uniforme y la imagen DLS mostró que los MSN eran uniformes con un tamaño de 108 ± 5,9 nm. La modificación de BSA y / o el direccionamiento anti-VEGFR2 no cambiaron la morfología de las nanopartículas y solo dieron como resultado una ligera tendencia a agregarse en solución en comparación con los MSN no modificados, lo que puede haber sido causado por el aumento de la superficie de los nanocomplejos. El diámetro de BSA-MSNs-anti-VEGFR2 aumentó ligeramente a 163 ± 4,6 nm, y el potencial zeta medio de los MSN fue de -23,91 mV, que cambió a 28,45 mV para BSA-MSNs-anti-VEGFR2. El cambio en el potencial zeta y el aumento de tamaño después de la modificación de la superficie sugirieron la adición exitosa de BSA y anti-VEGFR2 en la superficie de los MSN en cada paso (Tabla 1). La caracterización de la textura de los MSN fue confirmada por la isoterma de adsorción-desorción de nitrógeno. Los MSN tienen una estructura mesoporosa bien definida con una superficie de 630,2 m 2 / gy un diámetro medio de poro de 2,8 nm (Fig. 1d). La estabilidad de las nanopartículas de BSA-MSNs-anti-VEGFR2 se controló durante varias semanas y no se observó ninguna agregación obvia. La proporción de 131 El etiquetado I fue aproximadamente del 50 al 75%.
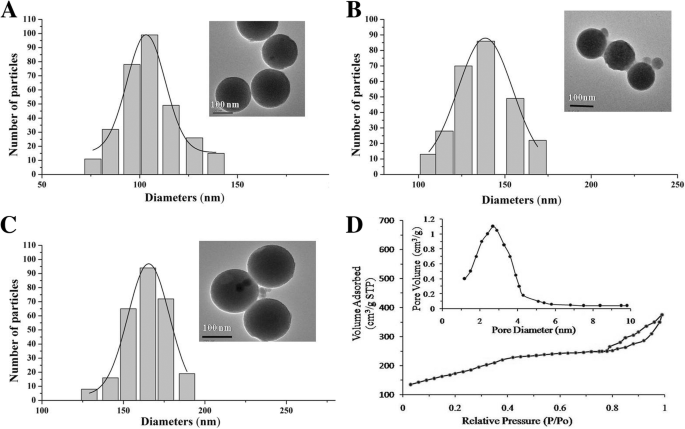
Las características de las nanopartículas. Caracterizaciones de MSN ( a ), BSA-MSN ( b ), BSA-MSNs-anti-VEGFR2 ( c ) e isoterma de adsorción-desorción de nitrógeno y curvas de distribución de tamaño de poro de Barrett-Joyner-Halenda (BJH) de MSN ( d ). Las imágenes de microscopía electrónica de transmisión muestran que todas tenían una morfología regular (esférica uniforme). Las imágenes de dispersión de luz dinámica muestran que todas eran uniformes, con tamaños promedio de 108 nm, 139 nm y 163 nm, respectivamente. Los análisis BET y BJH demostraron isotermas típicas de tipo IV, consistentes con una estructura mesoporosa
Captación de nanopartículas construidas
La unión de BSA-MSN y BSA-MSN-anti-VEGFR2 a células FRO de la línea celular ATC humana diana se ensayó usando microscopía confocal (Fig. 2). La inmunofluorescencia mostró que tanto los MSN dirigidos como los no dirigidos podían unirse eficazmente a las células FRO. Después de 1 h de incubación con BSA-MSNs o BSA-MSNs-anti-VEGFR2, la fluorescencia visible estaba presente en las células, la cual se mantuvo y fortaleció después de 6 h de incubación. En comparación con BSA-MSN-anti-VEGFR2, BSA-MSN también podrían unirse a las células, pero encontramos que la retención de células tumorales era mínima y la señal de fluorescencia verde era débil. Este resultado sugirió que la capacidad de direccionamiento de las nanopartículas se mejoró mediante la modificación con el anticuerpo anti-VEGFR2.
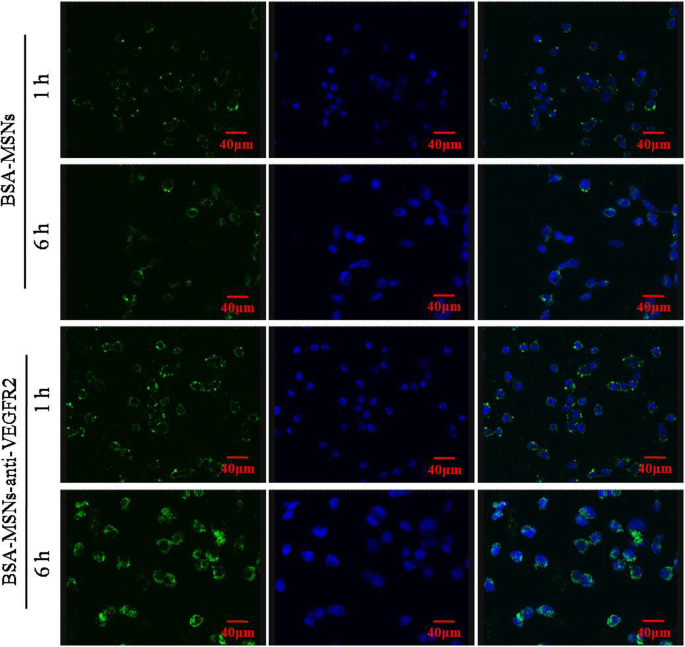
Captación de nanopartículas construidas. Imágenes de microscopio de escaneo láser confocal mostraron internalización celular de diferentes formulaciones a 1 y 6 h para BSA-MSN y BSA-MSN-anti-VEGFR2. La señal fluorescente a 1 h se incrementó a las 6 h para ambos grupos. Además, la fluorescencia verde de unión en el grupo dirigido al anti-VEGFR2 fue más fuerte que en el grupo no dirigido en ambos puntos de tiempo
Captación celular dependiente del tiempo
Para determinar la captación de yodo radiactivo de Na 131 Yo, 131 I-BSA-MSN y 131 I-BSA-MSNs-anti-VEGFR2 a medida que pasaba el tiempo, 131 Se obtuvieron mediciones de la actividad cronometrada en células FRO. Como se muestra en la Fig. 3a, el 131 La absorción en esta línea celular alcanzó su nivel máximo después de 3 h de incubación con 131 I-BSA-MSN y después de 5 h con 131 I-BSA-MSNs-anti-VEGFR2. Además, la captación de yodo radiactivo de 131 I-BSA-MSNs-anti-VEGFR2 fue más alto que el de 131 I-BSA-MSN.
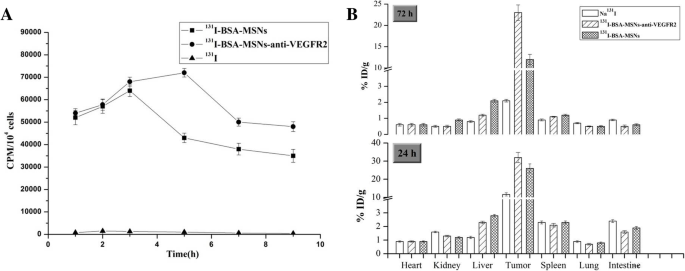
Captación celular dependiente del tiempo y distribución tisular. un Los datos sobre la captación celular dependiente del tiempo se presentan como la media ± DE de tres grupos. b Comparación de los datos sobre la biodistribución de 131 I en el tumor y órganos principales de ratones portadores de tumor ATC a las 24 y 72 h después de la inyección intratumoral de Na 131 Yo, 131 I-BSA-MSN y 131 I-BSA-MSNs-anti-VEGFR2. La radiactividad del tejido tumoral del grupo objetivo anti-VEGFR2 a las 24 y 72 h después de la inyección intratumoral (32,2 ± 2,8% ID / gy 23,0 ± 1,8% ID / g, respectivamente) fue significativamente mayor que la del grupo no objetivo (26,1 ± 2,5% ID / gy 12,3 ± 1,2% ID / g, respectivamente) (todos P <0,05). Los datos también se presentan como la media ± DE para los tres grupos
Distribución de tejidos
La distribución tisular de 131 La I en ratones desnudos se midió con un γ contador a las 24 y 72 h después de la inyección intratumoral con los respectivos fármacos (Fig. 3b). Los resultados revelaron que los tres grupos tenían una acumulación similar de radiación en los tejidos normales a las 24 y 72 h. La radiactividad para todos los grupos disminuyó gradualmente con el tiempo y se acumuló principalmente en el tumor. Además, la acumulación en el tejido tumoral a las 24 y 72 h después de la inyección en los dos grupos con 131 Las nanopartículas marcadas con I eran mucho más altas que las de Na 131 I grupo, que fue 11,6 ± 0,9% DI / ga 24 h y disminuyó drásticamente a 2,1 ± 0,08% DI / g a las 72 h. Sin embargo, la concentración en el tumor del grupo diana anti-VEGFR2 a las 24 y 72 h después de la inyección fue 32,2 ± 2,8% ID / gy 23,0 ± 1,8% ID / g, respectivamente, que fue significativamente mayor que la de los no- grupo objetivo (26,1 ± 2,5% ID / gy 12,3 ± 1,2% ID / g, respectivamente, todos P <0.05).
Imágenes en vivo
Para determinar el 131 Capto y distribuyo nanopartículas y observo el tiempo de residencia de 131 I en el tejido tumoral in vivo, se adquirieron imágenes SPECT / CT representativas de ratones portadores de tumores FRO en diferentes puntos de tiempo después de la inyección intratumoral con los fármacos respectivos (Fig. 4a). Los resultados mostraron que la acumulación radiactiva en el Na 131 El grupo I se excretó rápidamente del tumor 2 días después de la inyección y no se observó 3 días después de la inyección. Por el contrario, los dos grupos con 131 Las nanopartículas marcadas con I tenían un aclaramiento sanguíneo más lento y una mayor acumulación en el tejido tumoral incluso 2 semanas después de la inyección, especialmente en el grupo dirigido anti-VEGFR2. En particular, a las 3 semanas después de la inyección, la radiactividad en el grupo objetivo era obviamente más fuerte que en el grupo no objetivo.
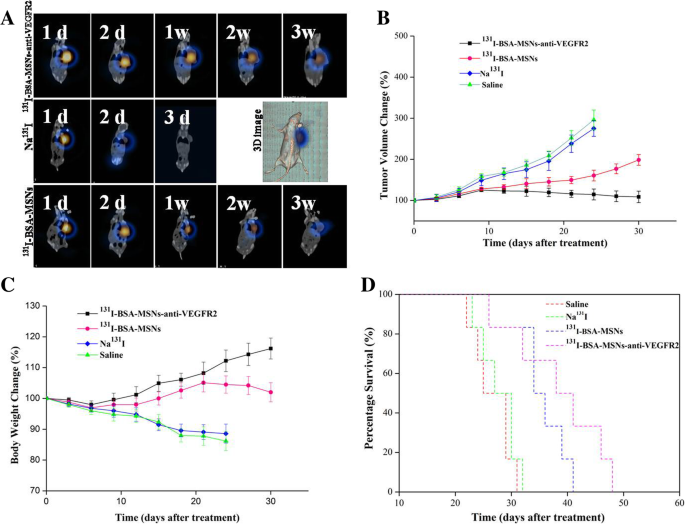
Imágenes in vivo, in vivo 131 Terapia y análisis de supervivencia. un Imágenes SPECT / CT fusionadas y tridimensionales de ratones portadores de tumores ATC obtenidas en diferentes puntos de tiempo después de la inyección intratumoral con los fármacos respectivos. La acumulación radiactiva en el Na 131 El grupo I no se vio a los 3 días después de la inyección, pero fue obvio incluso a las 3 semanas después de la inyección en el grupo objetivo anti-VEGFR2. Volumen del tumor ( b ), peso corporal ( c ) cambios y curvas de supervivencia de Kaplan-Meier ( d ) en los modelos de xenoinjerto FRO ATC ( n =6 / grupo). El crecimiento del tumor y la pérdida de peso corporal en el grupo objetivo se inhibieron significativamente en comparación con los del grupo no objetivo, Na 131 I, o grupo salino, respectivamente. Los datos se presentan como la media ± DE de tres grupos y todos fueron P < 0,05. Además, el tiempo medio de supervivencia en el grupo objetivo (41 días) se prolongó significativamente en comparación con el del grupo no objetivo (34 días) o Na 131 I (25 días) grupo (todos P < 0,01)
In Vivo 131 Yo Terapia
La Figura 4b muestra el volumen tumoral medio a lo largo del tiempo en los cuatro grupos. El volumen del tumor antes de la inyección se utilizó como referencia inicial. Excepto en el 131 I-BSA-MSNs-anti-VEGFR2, los tumores crecieron gradualmente en todos los grupos, especialmente en el Na 131 I y grupos salinos. El día 24, el volumen tumoral medio en el Na 131 I y los grupos de solución salina fue 296,6 ± 24,2% y 278,3 ± 19,3%, respectivamente, en comparación con 198,7 ± 13,2% en el 131 Grupo I-BSA-MSN el día 30. Curiosamente, observamos que el volumen en el grupo objetivo anti-VEGFR2 se redujo lentamente después del día 9 después de la inyección y casi se redujo a la referencia inicial al final de la observación.
La figura 4c muestra los cambios en el peso corporal de los cuatro grupos. El peso corporal disminuyó gradualmente en el Na 131 I y grupos salinos durante el período de observación. Sin embargo, los otros dos grupos perdieron peso solo en la primera semana, que se recuperó en momentos posteriores, especialmente para el grupo objetivo anti-VEGFR2.
Análisis de supervivencia
En este estudio, usamos la probabilidad de supervivencia como otra métrica para evaluar los efectos terapéuticos de 131 Nanopartículas etiquetadas con I. La Figura 4d muestra las curvas de supervivencia de Kaplan-Meier después de tratamientos con solución salina, Na 131 Yo, 131 I-BSA-MSN o 131 I-BSA-MSNs-anti-VEGFR2 en el modelo de ratón desnudo portador de tumor ATC. Los tumores progresaron rápidamente en la solución salina y Na 131 I grupos, y la mediana del tiempo de supervivencia fue de 27 y 25 días, respectivamente. El análisis con una prueba de rango logarítmico reveló que la mediana del tiempo de supervivencia en el 131 El grupo de I-BSA-MSN (34 días) se prolongó significativamente en comparación con el del Na 131 Yo grupo ( P < 0,001). Además, encontramos que el tratamiento en el grupo objetivo anti-VEGFR2 (tiempo medio de supervivencia, 41 días) resultó en resultados de supervivencia significativamente mejores que los del grupo no objetivo ( P <0.01).
Análisis histopatológico
Evaluar el efecto antitumoral de 131 Se recolectaron nanopartículas marcadas con I y se evaluó la toxicidad potencial de los MSN en ratones, los principales órganos y tumores para la tinción con hematoxilina y eosina después de la radioterapia. No se observaron cambios patológicos significativos en los órganos vitales en los ratones portadores de tumores después del tratamiento con 131 Nanopartículas marcadas con I (Fig. 5a). Esto indicó que no se había producido ninguna toxicidad sistémica aparente durante el período de observación. Además, los tumores tratados con 131 I-BSA-MSNs-anti-VEGFR2 mostró degeneración y necrosis masiva de las células tumorales, que era más obvia que en el 131 Grupo I-BSA-MSNs. Sin embargo, el tumor tratado con Na 131 El grupo I o solución salina estaba lleno de células tumorales viables. El análisis inmunohistoquímico del tumor reveló una expresión visible de VEGFR (Fig. 5b).
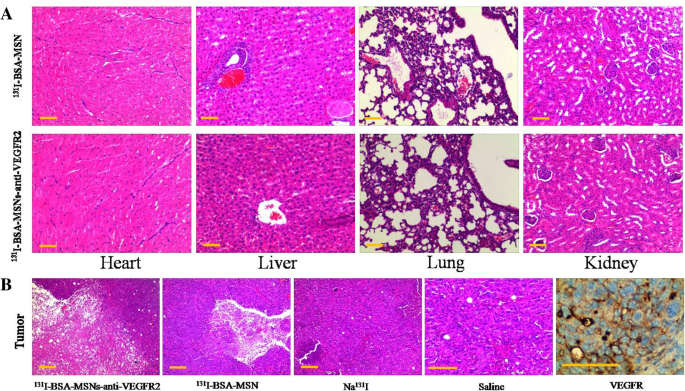
Análisis histopatológico. un Análisis histopatológico de los principales órganos de ratones portadores de tumores FRO ATC después del tratamiento con 131 Nanopartículas etiquetadas con I. No se observaron cambios patológicos significativos en el corazón, hígado, pulmón y riñón. b Exámenes patológicos (tinción H &E) y análisis inmunohistoquímico de tumores en ratones. Grandes fragmentos de la degeneración y necrosis de las células tumorales en el grupo dirigido a anti-VEGFR2 y pequeños fragmentos de necrosis de baja densidad en el 131 Se muestra el grupo I-BSA-MSN. Por el contrario, solo se observaron células tumorales viables en el Na 131 I y grupos salinos. La microfotografía del análisis inmunohistoquímico mostró una expresión visible de VEGFR. Bar =200 μm
Discusión
El pronóstico del ATC sigue siendo malo y hasta ahora no existen opciones de tratamiento eficaces [1, 2, 6]. La terapia molecular dirigida, como terapia novedosa, ha mejorado la morbilidad y la mortalidad de muchos cánceres [23, 24]. VEGFR is crucial to microvascular formation, which facilitates the growth of most malignancies, and allows continued tumor expansion [9, 10]. In this study, we evaluated the efficacies of Na 131 I, 131 I-BSA-MSNs, and 131 I-BSA-MSNs-anti-VEGFR2 for the treatment of ATC in tumor-bearing nude mouse models. The results demonstrated that both anti-VEGFR2 targeted and non-targeted nanoparticles labeled with 131 I were effective in delaying the tumor growth of ATC and that the 131 I-labeling anti-VEGFR2 targeted MSNs was the most effective agent to inhibit the tumor growth in nude mice and prolonging median survival. This treatment modality might represent a novel therapeutic option for ATC.
VEGFR targeting with nanoparticles is rarely reported in the literature. Goel S et al. [19] confirmed that VEGFR targeting using VEGF121 conjugated, anti-VEGFR therapeutics-loaded MSNs represented a major advance for angiogenesis imaging and inhibition in human glioblastoma. A study performed by Gule indicated that inhibition of epidermal growth factor receptor (EGFR) and VEGFR2 in ATC using vandetanib causes significant tumor growth inhibition in vivo in an orthotopic xenograft model [15]. In the present study, using confocal microscopy, we found that both targeted and non-targeted nanoparticles could efficiently bind to the cytoplasm and cytoplast of FRO cells, and further confirmed that the targeting ability of the nanoparticles was enhanced via modification with the anti-VEGFR2 antibody, which result was consistent with that of the time-dependent cellular uptake experiment. Additionally, after intratumoral injection with the respective drugs, we compared data on the tissue distribution of 131 I in the tumor-bearing nude mice at 24 and 72 h for the different groups. The radioactivity for all groups was mostly accumulated in the tumor and gradually decreased with time. Moreover, we found that the radioactivity in anti-VEGFR2 targeted group could be retained for longer time in the tumor in comparison with non-targeted group, which was also consistent with the results observed by confocal microscopy.
SPECT/CT is a powerful tool to provide both structural and functional imaging information for diseases, and can monitor the metabolism of radioactive drugs at different times post injection [30,31,32]. In the present study, we compared data on the tissue distribution of 131 I using SPECT/CT. The results showed that radioactive accumulation in the Na 131 I group was not seen at 3 day post-injection. However, higher accumulation in the tumor tissue was observed at 2 weeks post-injection for the two groups with 131 I-labeled nanoparticles, and at 3 weeks the radioactive signal in the anti-VEGFR2 targeted group was apparently stronger than that in the non-targeted group. We hypothesized that the passive tumor targeting of MSNs, which relies on unpredictable tumor extravasation and enhanced permeability retention effect, and positive targeting linked with anti-VEGFR-2, associated with VEGFR2 overexpression in ATC, played a key role in enhancing the retention of the nanoparticles in the tumors. This finding revealed that anti-VEGFR2 modification prolonged the retention time of 131 I in the tumor tissue compared with that of free Na 131 I and 131 I-BSA-MSN, which was also similar to the tissue biodistribution of 131 I measured by γ counter.
In the present study, we monitored the body weight change of nude mice after intratumoral injection with a single dose of 2 mCi 131 I, which showed that the body weight in the 131 I-labeled nanoparticle groups gradually increased at 1 week post-injection, especially for the anti-VEGFR2 targeted group. Similarly, we also observed the changes in tumor volume and found that the tumors in the Na 131 I or saline group grew rapidly, while the volume in 131 I-BSA-MSNs group increased slowly. Interestingly, the tumors in anti-VEGFR2 targeted group gradually decreased after 1 week post-injection, which was contrary to the body weight change. These results indicated that the anti-VEGFR2 modification could effectively inhibit the increase in tumor volume and thereby enhanced the efficiency of 131 I therapy. We considered that the tumor necrosis was caused by the beta rays emitted from 131 I, which resulted in tumor shrinkage and indirectly led to an increase in body weight. This effect, we speculated, began to appear mainly 1 week after injection of 131 I.
Our findings indicated that the treatment mediated by intratumorally injected 131 I-BSA-MSNs-anti-VEGFR2 resulted in significant tumor growth delay, which was confirmed increased structural damage and massive necrosis in tumor tissue compared with that in the 131 I-BSA-MSNs group. Significantly, this higher antitumor activity was achieved without causing apparent systemic toxic effects, as indicated by the lack of significant pathological changes in the vital organs observed in tumor-bearing nude mice. Although further studies are needed to document both the acute and chronic toxicological effects, 131 I-BSA-MSNs-anti-VEGFR2 exhibited several properties that made them a promising candidate for minimally invasive therapy for ATC.
In our pre-experiment, injection into the tail vein was performed and the results showed that the radioactivity was mainly distributed in the phagocytosis system. Intratumoral injection was used in some studies [29, 33, 34], and the operation is more convenient. Therefore, we used intratumoral injection as the injection method and also achieved better results. MSNs offer a promising approach to overcome the insolubility issue and deliver large payloads of hydrophobic small molecule drugs. Currently, we are investigating the potential for loading targeted anti-cancer drugs using MSNs. We will provide the results in the future publication.
Conclusions
In the present study, we successfully synthesized BSA-MSNs-anti-VEGFR2, with uniform spherical morphology, and which were radiolabeled with 131 I using the Chloramine-T method. The results showed that both targeted and non-targeted MSNs could efficiently bind to the cytoplasm and cytoplast of FRO cells. The radioactivity in ATC tumor-bearing nude mouse model was mostly accumulated in the tumor and could be retained a longer time in the 131 I-BSA-MSNs-anti-VEGFR2 group. Additionally, the tissue distribution of 131 I could be also imaged and validated using SPECT/CT. Moreover, tumor growth in the ATC tumor-bearing nude mouse model was significantly inhibited by the anti-VEGFR2 targeted MSNs compared with that achieved using non-targeted MSNs and the 131 I treatment with anti-VEGFR2 targeting MSNs significantly prolonged the survival of ATC tumor-bearing mice. Our data supported the view that such an approach may represent a more effective means to treat ATC.
Abreviaturas
- APTES:
-
Aminopropyltriethoxysilane
- ATC:
-
anaplastic thyroid cancer
- BSA:
-
Albúmina de suero bovino
- CLSM:
-
Microscopía de escaneo láser confocal
- CTAB:
-
Bromuro de hexadeciltrimetilamonio
- DAPI:
-
4,6-Diamidino-2-phenylindole
- DLS:
-
Dispersión de luz dinámica
- DMEM:
-
Dulbecco’s modified Eagle medium
- DMSO:
-
Dimetilsulfóxido
- EDC:
-
1-(3-Dimethylaminopropyl)-3-ethylcarbodiimide hydrochloride
- FBS:
-
Suero fetal bovino
- FITC:
-
Fluorescein isothiocyanate
- HBSS:
-
Hanks’ balanced salt solution
- MSNs:
-
Mesoporous silica nanoparticles
- NHS:
-
N -hydroxysuccinimide
- PBS:
-
Phosphate buffer saline
- TEM:
-
Microscopio electrónico de transmisión
- TEOS:
-
Ortosilicato de tetraetilo
- VEGFR:
-
Vascular endothelial growth factor receptor
Nanomateriales
- Nanopartículas para la terapia del cáncer:avances y desafíos actuales
- Nanopartículas como bomba de eflujo e inhibidor de biopelícula para rejuvenecer el efecto bactericida de los antibióticos convencionales
- Nanopartículas de quitosano cargadas con genisteína y bioflavonoides dirigidas al receptor de folato para un efecto anticancerígeno mejorado en los cánceres de cuello uterino
- Nanopartículas de sílice para la administración intracelular de proteínas:un nuevo enfoque de síntesis que utiliza proteína verde fluorescente
- Efecto del método de síntesis de nanopartículas de manganita La1 - xSr x MnO3 en sus propiedades
- Efecto de nanopartículas de ingeniería en la liberación de sustancias exopoliméricas del fitoplancton marino
- Toxicidad de nanopartículas de CoFe2O4 recubiertas de PEG con efecto de tratamiento de curcumina
- Efecto del agente peptizante ácido sobre la relación anatasa-rutilo y el rendimiento fotocatalítico de nanopartículas de TiO2
- Nanopartículas de oro de forma redonda:efecto del tamaño de partícula y la concentración sobre el crecimiento de la raíz de Arabidopsis thaliana
- Evaluación de la toxicidad de las nanopartículas de PEG-PCCL e investigación preliminar sobre su efecto antitumoral de la carga de paclitaxel
- El efecto de apoptosis en las células de cáncer de hígado de nanopartículas de oro modificadas con ácido litocólico



