Efecto de nanopartículas de ingeniería en la liberación de sustancias exopoliméricas del fitoplancton marino
Resumen
Las nanopartículas diseñadas (ENP), productos de las nanotecnologías modernas, pueden tener un impacto potencial en el medio ambiente marino y plantear serias amenazas a los ecosistemas marinos. Sin embargo, las respuestas celulares del fitoplancton marino a los ENP aún no están bien establecidas. Aquí, investigamos cuatro especies de diatomeas diferentes ( Odontella mobiliensis , Skeletonema grethae , Phaeodactylum tricornutum , Thalassiosira pseudonana ) y un alga verde ( Dunaliella tertiolecta ) para su liberación de sustancias poliméricas extracelulares (EPS) bajo tratamientos modelo ENP:dióxido de titanio de 25 nm (TiO 2 ), Dióxido de silicio de 10 a 20 nm (SiO 2 ) y dióxido de cerio de 15 a 30 nm (CeO 2 ). Encontramos SiO 2 Los ENP pueden estimular significativamente la liberación de EPS de estas algas (200-800%), mientras que TiO 2 La exposición a ENP indujo la liberación más baja. Además, el aumento de Ca 2+ intracelular La concentración puede ser provocada por los ENP, lo que sugiere que el proceso de liberación de EPS está mediado por Ca 2+ Vías de señal. Con una mejor comprensión del mecanismo celular mediado por la liberación de EPS inducida por ENP, se pueden desarrollar posibles medidas preventivas y de seguridad para mitigar el impacto negativo en el ecosistema marino.
Antecedentes
Las nanopartículas de ingeniería (ENP), que varían en tamaño entre 1 y 100 nm (en al menos una dimensión), se utilizan en la fabricación de numerosos bienes de consumo, incluidas tintas y pinturas para impresoras, detergentes, bactericidas, recubrimientos, cosméticos, lociones de protección solar, neumáticos, construcción de computadoras y administración de medicamentos. Dada la prometedora aplicación de las PEV, la financiación de la Iniciativa Nacional de Nanotecnología (NNI) en los EE. UU. Se acercó a los 1.400 millones de dólares en 2017 [1, 2, 3]. El establecimiento de conocimientos fundamentales a nanoescala fue el enfoque principal de la comunidad de investigación en nanotecnología en la primera fase. En 2009, este nuevo conocimiento sustentaba alrededor de un cuarto de billón de dólares en el mercado mundial, de los cuales alrededor de $ 91 mil millones correspondían a productos estadounidenses que incorporan componentes a nanoescala [4]. Con el rápido desarrollo de la nanotecnología, es inevitable que los ENP finalmente encuentren su camino hacia los sistemas acuáticos. La principal preocupación de los ENP en términos de su potencial toxicidad (por ejemplo, el potencial de producir especies reactivas de oxígeno, ROS) en el medio ambiente está relacionada con su gran y única reactividad de superficie. Sin embargo, el impacto real en el ecosistema marino sigue siendo en gran parte desconocido debido a los complejos factores ambientales y biológicos de las aguas naturales y la variedad de ENP [1, 5, 6]. Estudios anteriores han demostrado que los ENP pueden causar un daño significativo al ecosistema marino basado en algas [7, 8]. Se ha demostrado que los organismos marinos (en particular el fitoplancton) interactúan con los ENP, lo que genera repercusiones negativas [9,10,11]. Con el aumento potencial de la utilización de la nanotecnología en diversos campos, más y más ENP pueden ingresar a ambientes acuáticos, por lo que las respuestas celulares del fitoplancton marino a los ENP merecen mayor atención [12,13,14,15,16,17,18,19,20, 21].
La mayoría de los microbios marinos, ya sean autótrofos o heterótrofos, generalmente son capaces de producir sustancias exopoliméricas (EPS), que tienen diversas funciones funcionales y propiedades físicas en el ecosistema marino, actuando como inhibidores del crecimiento, promotores del crecimiento, toxinas, captadores de metales o como sustratos para el ciclo heterotrófico [22,23,24,25,26]. Los EPS liberados del fitoplancton y las bacterias en el océano son biopolímeros coloidales aniónicos ricos en polisacáridos que son críticos para la formación de geles marinos, nieve marina y biopelículas, así como para la captación de coloides y oligoelementos y para brindar protección contra diversas amenazas ambientales. incluidas las PEV [7, 15, 19, 20, 25, 27]. Además, se cree que la secreción de EPS es una respuesta natural cuando el fitoplancton experimenta diversos tipos de estrés [8].
Ca 2+ es un segundo mensajero común involucrado en una multitud de vías de señalización intracelular. Se ha demostrado que Ca 2+ es necesario para la quimiotaxis, la motilidad y la adhesión en la diatomea Amphora coffeaeformis [28]. Ca 2+ libre intracelular mejorado Se sabe que los niveles conducen a la activación de la proteína quinasa C, que participa en muchas vías de señalización intracelular [29]. Dado que la liberación de EPS está estrechamente relacionada con la motilidad y la adhesión de las diatomeas, se propuso que un Ca 2+ El proceso de secreción mediado controla la liberación de EPS de las diatomeas [30] y la evidencia directa que verifica Ca 2+ señalización, exocitosis y correlación de Ca 2+ La señalización con exocitosis se ha informado en nuestro estudio anterior [31]. Estudios anteriores también han demostrado que las interacciones con los ENP pueden alterar el Ca 2+ intracelular vías, que son esenciales para la señalización celular [29, 32,33,34]. Ca 2+ intracelular específico los cambios de concentración son importantes en los procesos de secreción y señalización celular; sin embargo, no hay informes de dióxido de titanio (TiO 2 ), dióxido de silicio (SiO 2 ), o dióxido de cerio (CeO 2 ) para alterar el Ca 2+ intracelular nivel en fitoplancton.
En 2013, Quigg et al. [8] resumió los efectos tóxicos directos e indirectos de los PE en las algas. En nuestros experimentos anteriores, se demostró que los ENP facilitan la agregación de EPS [35]. En este sentido, el EPS puede exacerbar o reducir la toxicidad directa inducida por ENP hacia los organismos acuáticos [7, 15, 36]. Sin embargo, nunca se ha informado de la medición directa de la liberación de EPS del fitoplancton bajo estrés de ENP. En este estudio, el objetivo es estudiar la liberación de EPS de cuatro especies de diatomeas diferentes ( Odontella mobiliensis , Skeletonema grethae , Phaeodactylum tricornutum , Thalassiosira pseudonana ) y un alga verde ( Dunaliella tertiolecta ) bajo tratamientos ENP. Al comprender los mecanismos subyacentes de la liberación de EPS inducida por ENP en el fitoplancton, la implementación de medidas preventivas y de seguridad puede mitigar los efectos potencialmente perjudiciales para los organismos marinos.
Resultados y discusiones
Caracterización de ENP
La dispersión dinámica de láser (DLS) se utilizó para caracterizar las métricas de tamaño de los siguientes ENP suspendidos en agua pura:TiO 2 , SiO 2 y CeO 2 . La distribución del tamaño de partícula osciló entre 7 y 66 nm en TiO 2 , 9 a 66 nm en SiO 2 y de 12 a 70 nm en CeO 2 . Algunos tamaños más grandes podrían deberse a agregación o aglomeración, mientras que el tamaño predominante para TiO 2 es 25 nm, SiO 2 es de 10 a 20 nm, y CeO 2 es de 15 a 30 nm, lo que coincide con la información del fabricante (Fig. 1).
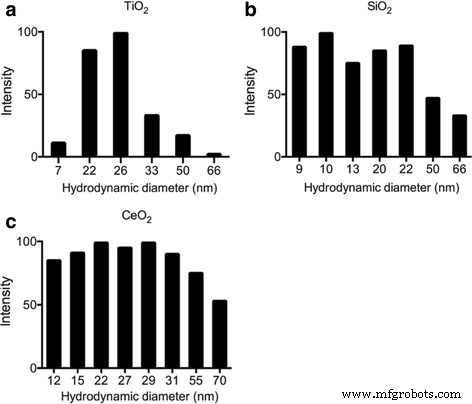
Caracterización de ENP mediante evaluación DLS de a TiO 2 , b SiO 2 y c Director ejecutivo 2 en medio L1 después de la sonicación mostrando su distribución de tamaño. La concentración final de ENP en la muestra de DLS es de 1 μg / ml, el tiempo de medición es de 3 minutos inmediatamente después de la sonicación
Los ENP inducen Ca intracelular 2+ Concentración en fitoplancton
Investigar si los ENP podrían inducir un aumento del Ca intracelular 2+ concentración, las células de fitoplancton (DO 600 =0,8) se cargaron con tinte Fluo-4AM y se expusieron a 1 mg / ml de TiO 2 de 25 nm , 10–20 nm SiO 2 y 15–30 nm CeO 2 ENPs respectivamente. El cambio en el Ca 2+ intracelular La concentración, representada por la intensidad de fluorescencia dentro de las células de fitoplancton, se controló durante 150 s. Las figuras 2a-e muestran que 1 mg / ml de tres ENP respectivos aumentaron el Ca 2+ concentración en SiO 2 en aproximadamente un 50–300%, TiO 2 en aproximadamente un 40%, y el director ejecutivo 2 en aproximadamente un 150-200%, mientras que las condiciones de control (medio L1) permanecieron sin cambios. Los resultados muestran que los ENP pueden inducir una cantidad significativa de Ca 2+ intracelular respuestas en el fitoplancton y sugieren que el fitoplancton responde a distintos ENP a través de Ca 2+ vías de señalización. Nuestros datos indican solo cambios menores en el Ca 2+ intracelular niveles cuando TiO 2 está presente, potencialmente atribuido a la muerte sustancial de células de fitoplancton por TiO 2 -toxicidad inducida [37, 38]. En nuestro estudio anterior, TiO 2 aumento provocado en el Ca intracelular 2+ concentración [34] junto con apoptosis celular significativa [39]. Sin embargo, SiO 2 mostró sorprendentemente el Ca 2+ intracelular más obvio aumento para todas las especies de fitoplancton, mientras que CeO 2 solo puede desencadenar un Ca 2+ intracelular intermedio aumento de concentración. Investigaciones anteriores sugirieron el potencial de un alto director ejecutivo 2 concentraciones (> 50 mg / ml) para inducir estrés oxidativo intracelular y elevación del Ca 2+ intracelular niveles, aunque los efectos fueron pequeños, y apoyaron nuestro hallazgo [40]. También medimos el potencial zeta de cada ENP en agua de mar artificial para abordar el efecto potencial que puede causar la carga superficial; sin embargo, el valor fue bajo. La medición indicó que los ENP se consideran aproximadamente neutrales [41] (Archivo adicional 1:Datos suplementarios). Este sirvió como el primer informe en el que se encontró que los ENP dispares inducían Ca 2+ intracelular cambios de concentración en fitoplancton específico, lo que finalmente allana una nueva vía para la investigación futura.
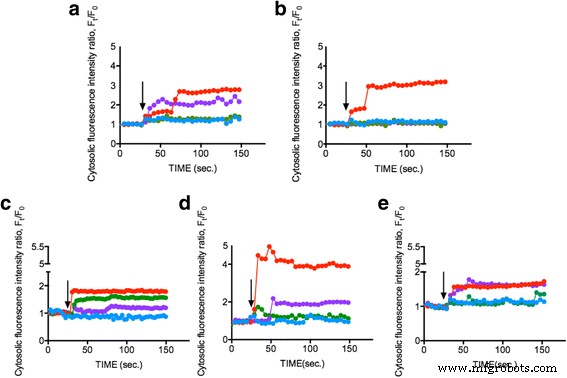
Medición de Ca 2+ intracelular concentración después de la estimulación por diferentes ENP. Diferentes células de fitoplancton a Dunaliella tertiolecta , b Thalassiosira pseudonana , c Skeletonema grathae , d Phaeodactylum tricornutum y e Odontella mobiliensis fueron tratados con TiO 2 25 nm (verde), SiO 2 10-20 nm (rojo), director ejecutivo 2 15–30 nm (violeta) con una concentración de 1 mg / ml y control (azul). La flecha negra indica el momento en el que se aplicaron las EPN (30 s). Las mediciones muestran datos representativos de un promedio de 20 celdas individuales
Lanzamiento de EPS inducido por ENP en fitoplancton
Se utilizó el ensayo de lectina unida a enzimas (ELLA) para evaluar la cantidad de liberación de EPS de las células de fitoplancton cuando se estimulan con TiO 2 , SiO 2 y CeO 2 NEP, rango de concentración de 1 μg / ml a 5 mg / ml según estudios previos para TiO 2 [42, 43] y director ejecutivo 2 [44,45,46]. La secreción de EPS se normalizó a la cantidad total de ADN de fitoplancton (archivo adicional 1:datos del suplemento) para tener una base igual para la comparación. En comparación con el control, encontramos que 10–20 nm SiO 2 puede aumentar la liberación de EPS hasta en un 550% en Dunaliella , 500% en Thalassiosira , 1000% en Skeletonema , 400% en Odontella y 900% en Phaeodactylum (Fig. 3). Cuando las especies de fitoplancton fueron expuestas a TiO 2 , no hubo un efecto fuerte sobre la secreción de EPS, ya que solo Skeletonema y Phaeodactylum mostró cambios significativos. Por lo tanto, los datos de liberación de EPS son consistentes con nuestro Ca 2+ intracelular resultados de concentración. TiO 2 no presentó un impacto significativo en la producción de EPS, similar al hecho de que el Ca +2 intracelular las concentraciones mostraron cambios muy límites debido a la toxicidad del TiO 2 al fitoplancton. La producción y los residuos de ROS pueden dar lugar a muchas complicaciones, como la apoptosis en el fitoplancton [47,48,49]. En el CeO 2 tratamiento, los resultados mostraron un efecto menor en Dunaliella , Skeletonema , Odontella y Phaeodactylum . Sin embargo, SiO 2 mostró la inducción de EPS más significativa en Thalassiosira pseudonana (alrededor del 600%) y Skeletonema grethae (alrededor de 1000-1500%). Estos datos indican que diferentes ENP pueden inducir la liberación de EPS específicos del fitoplancton y Ca 2+ intracelular los cambios también coinciden con los resultados de la versión EPS. Evaluando los cambios en el Ca 2+ intracelular concentración, es evidente que existe una conexión directa en el Ca 2+ Vías celulares en las que los ENP evocan la secreción de EPS del fitoplancton. La observación aquí está de acuerdo con nuestros estudios anteriores basados en Phaeocystis Lanzamiento de EPS [31]. Los resultados proporcionan evidencia directa de que el fitoplancton puede detectar y distinguir los ENP que responden con diferentes liberaciones de EPS reguladas por Ca 2+ vías celulares.
El uso de ELLA nos permitió determinar la liberación de EPS a través de las interacciones del fitoplancton con los ENP. Nuestros resultados indican que la secreción de EPS aumentó significativamente cuando el fitoplancton interactuó con SiO 2 para Dunaliella tertiolecta , Thalassiosira pseudonana y Skeletonema grethae . Parece que estas diatomeas están preparadas para reconocer SiO 2 partículas. Sin embargo, en Phaeodactylum tricornutum , no se encontró una fuerte secreción de EPS. Esta diferencia representa la liberación de EPS desencadenada por los ENP que dependen de la especie de fitoplancton y la concentración de ENP (Fig. 3). En un estudio anterior, los derrames de petróleo provocaron grandes liberaciones de EPS microbianos marinos que se propuso para contrarrestar las consecuencias negativas de los derrames de petróleo [50]. Además, Boglaienko y Tansel encontraron que SiO 2 partículas fue capaz de eliminar los agregados de aceite de manera eficiente [51]. Nuestro hallazgo proporciona un nuevo mecanismo potencial en el que el SiO 2 de baja toxicidad las partículas pueden inducir la liberación de EPS de un fitoplancton específico, lo que potencialmente facilita la eliminación de los derrames de petróleo al promover la agregación de EPS. Nunca se ha informado que el dióxido de cerio perturbe los ecosistemas marinos basados en el fitoplancton. Los resultados aquí mostraron CeO 2 Los ENP pueden afectar a todo el fitoplancton aquí excepto a Thalassiosira pseudonana. Director ejecutivo 2 Los ENP pueden, como SiO 2, tienen la capacidad de impulsar la liberación de EPS de un fitoplancton particular para aplicaciones de mitigación de petróleo.
Conclusiones
La interacción ENP-medio ambiente marino es cada vez más crítica debido a las descargas actuales y futuras de nanomateriales. Aquí, demostramos una mayor secreción de EPS como uno de los principales efectos de los ENP en el fitoplancton. También proporcionamos evidencia de que diferentes fitoplancton pueden responder de manera diferente a varios estreses de ENP regulando Ca 2+ caminos. Sin embargo, una evaluación completa de las PE en el ecosistema marino necesitaría más investigaciones para proporcionar un conocimiento y una comprensión detallados de las interacciones entre los nanomateriales y los organismos marinos.
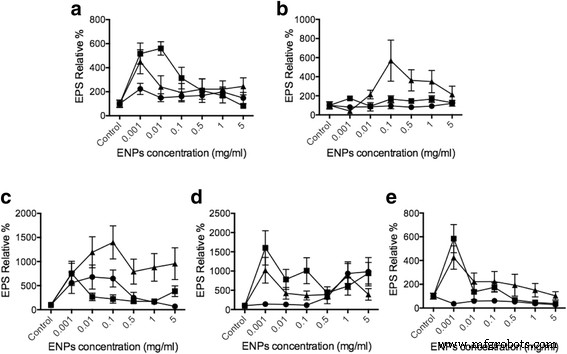
Lanzamiento de EPS desencadenado por varios ENP. Diferentes células de fitoplancton a Dunaliella tertiolecta , b Thalassiosira pseudonana , c Skeletonema grathae , d Phaeodactylum tricornutum y e Odontella mobiliensis fueron tratados con TiO 2 (círculos), SiO 2 (triángulos), director ejecutivo 2 (cuadrados), respectivamente, con concentraciones de 5 mg / ml y 1 mg / ml, 0,5 mg / ml, 0,1 mg / ml, 10 μg / ml, 1 μg / ml ( n =3)
Métodos
Cultura de fitoplancton
Cultivos por lotes de Odontella mobiliensis (CCMP597), Dunaliella tertiolecta (UTEX999), Skeletonema grethae (CCMP775), Phaeodactylum tricornutum (UTEX646), Thalassiosira pseudonana (Colección de cultivo de fitoplancton marino Provasoli-Guillard, West Boothbay Harbor, MN, EE. UU.) Se cultivaron en medio marino L1 (Sigma, MO, EE. UU.) En un ciclo 14:10 (luz:oscuridad) a 100 μmol m -2 s −1 y 24 ° C en condiciones axénicas. La fase de crecimiento del cultivo se determinó mediante recuento celular con un hemocitómetro.
Nanopartículas y caracterización
Todos los ENP, TiO 2 , SiO 2 , Director ejecutivo 2 (Sigma-Aldrich, MO, EE. UU.), Se sonicaron en agua pura antes de su uso. Los ENP se reconstituyeron con medio L1 filtrado (Sigma, MO, EE. UU.) Antes de ser analizados. El tamaño de los ENP se confirmó de forma independiente utilizando dispersión láser de dinámica homodina (DLS). Brevemente, las muestras de agua de mar se volvieron a filtrar a través de una membrana Millipore de 0,22 μm (prelavada con HCl 0,1 N) y se vertieron directamente en cinco celdas de dispersión de 10 ml que luego se colocaron en el goniómetro de un espectrómetro láser Brookhaven BI-200SM (Brookhaven Instruments, Nueva York, EE. UU.). La función de autocorrelación de las fluctuaciones de intensidad de dispersión detectadas en un ángulo de 45 ° se procesó en línea mediante un autocorrelacionador Brookhaven BI 9000AT, y la distribución del tamaño de partículas se calculó mediante el método CONTIN (Provencher, 1982). Los resultados de cada muestra se recogieron por triplicado inmediatamente después de la sonicación. La calibración del espectrómetro DLS se realizó utilizando suspensiones estándar de microesferas de látex monodispersas (Polysciences, PA, EE. UU.).
Tratamiento ENP
Las células de fitoplancton se cultivaron en una placa de 96 pocillos con medio L1 durante 24 h. Las células se trataron con reservas de ENP:5 mg / ml y 1 mg / ml, 0,5 mg / ml, 0,1 mg / ml, 10 μg / ml, 1 μg / ml del TiO 2 , SiO 2 y CeO 2 (Sigma-Aldrich, MO, EE. UU.) O medio L1 (control) durante 48 h. Se recogió el sobrenadante que contenía EPS secretado y se centrifugó brevemente a 4000 rpm para eliminar los ENP residuales. Este protocolo fue adaptado de nuestra publicación anterior [34]. El rango de concentración utilizado aquí no pretende representar ni imitar los niveles actuales de ENP en el medio ambiente, sino que tiene como objetivo evaluar el impacto potencial total de los ENP en el fitoplancton marino e investigar los mecanismos celulares asociados. Como nanomaterial emergente prometedor, los ENP aún no han alcanzado su plena capacidad comercial. Es muy necesaria una evaluación detallada de sus impactos ecológicos completos antes de que las ENP ingresen al mercado de productos comerciales y domésticos para introducir más ENP en el océano.
Ensayo de lectina ligada a enzimas (ELLA)
El sobrenadante que contenía el polisacárido secretado se recogió y se centrifugó brevemente a 1700 rcf (Megafuge 1.0R) para eliminar los ENP residuales. A continuación, se incubó el sobrenadante en una placa de 96 pocillos (Nunc MaxiSorp, VWR, CA, EE. UU.) Durante la noche a 4ºC. Posteriormente, la placa de 96 pocillos se lavó con PBST (PBS + Tween-20 al 0,05%) y PBS y luego se bloqueó con BSA al 1%. La placa de 96 pocillos se lavó nuevamente con PBST y PBS y se incubó con lectina (Concanavalin A, ConA) (Sigma-Aldrich, MO, EE. UU.), Conjugada con peroxidasa de rábano picante (HRP; 5 mg / ml) (Sigma-Aldrich, MO, EE. UU.) , EE. UU.), A 37 ° C durante 1 h. El sustrato, 3,39,5,59-tetrametilbencidina (TMB; Sigma-Aldrich, MO, EE. UU.), Se añadió a cada pocillo a temperatura ambiente seguido de H 2 SO4 (Sigma-Aldrich, MO, EE. UU.) Para terminar la reacción. La densidad óptica se midió a 450 nm por PerkinElmer VICTOR3 (MA, EE. UU.). Este protocolo fue adaptado de nuestra publicación anterior [34, 52].
Determinación de ADN
Se recogió el sedimento que contenía fitoplancton y se obtuvo el kit ZR-96 Quick-gDNA (ZYMO Research, CA, EE. UU.). En resumen, se usó tampón de lisis 4X para romper las células de fitoplancton y fluir a través de la columna de unión al ADN, eluido por el tampón de elución al final. Las concentraciones de ADN se midieron con NanoDrop ND-1000 (Thermo, CA, EE. UU.). El protocolo se adaptó del protocolo del kit fabricado.
Mediciones de Ca intracelular 2+ Concentraciones inducidas por ENPs
A continuación, las células de fitoplancton se cargaron con un colorante Fluo-4AM (1 mM) (Kd =335 nM, λEx =494 nm y λEm =506 nm, ThermoFisher, CA, EE. UU.) Durante 60 min [31]. Después de la carga de tinte, las células de fitoplancton se enjuagaron, se incubaron con medio L1 y se trataron con 1 mg / ml de TiO 2 , SiO 2 y CeO 2 respectivamente. Todos los experimentos de señalización de calcio se llevaron a cabo en un microscopio Nikon (Nikon Eclipse TE2000-U, Tokio, Japón). El protocolo y las condiciones se adaptaron de publicaciones anteriores [31, 34].
Potencial Zeta de la medición de ENP
Para medir las cargas superficiales de los ENP, se midió el potencial zeta (ζ) de los ENP con un Zetasizer Nano ZS, Malvern, en presencia de agua de mar artificial a 25 ° C. Después de recopilar los datos de cada muestra, se promediaron los valores registrados.
Análisis estadístico
Los datos se expresan como medias ± DE. Cada experimento se realizó de forma independiente al menos tres veces. Los histogramas fueron hechos por GraphPad Prism 6.0. (GraphPad Software, Inc., San Diego, CA, EE. UU.).
Nanomateriales
- Nanopartículas semiconductoras
- Nanopartículas plasmónicas
- El efecto del pH en los tintes amarillos del jardín
- Mecanismo de formación de superredes de nanopartículas bien ordenadas y empaquetadas densamente depositadas de la fase gaseosa en superficies sin plantillas
- Nanopartículas como bomba de eflujo e inhibidor de biopelícula para rejuvenecer el efecto bactericida de los antibióticos convencionales
- Nanopartículas de quitosano cargadas con genisteína y bioflavonoides dirigidas al receptor de folato para un efecto anticancerígeno mejorado en los cánceres de cuello uterino
- Nanotecnología:del sistema de imágenes in vivo a la administración controlada de fármacos
- Efecto del método de síntesis de nanopartículas de manganita La1 - xSr x MnO3 en sus propiedades
- Toxicidad de nanopartículas de CoFe2O4 recubiertas de PEG con efecto de tratamiento de curcumina
- Efecto del agente peptizante ácido sobre la relación anatasa-rutilo y el rendimiento fotocatalítico de nanopartículas de TiO2
- Nuevas nanopartículas dirigidas al receptor CD44 y mitocondrial dual para liberación activada por estímulos redox



