Efecto de la no estequiometría de los reactivos iniciales sobre las propiedades morfológicas y estructurales de las perovskitas CH3NH3PbI3
Resumen
Las propiedades de las películas de perovskitas orgánico-inorgánicas CH 3 NH 3 PbI 2.98 Cl 0.02 dependiendo de la proporción de reactivos de partida en soluciones (PbI 2 :{CH 3 NH 3 I + CH 3 NH 3 Cl}) ha sido investigado. Se encontró que la formación de la estructura de perovskita con la proporción de los reactivos iniciales PbI 2 :CH 3 NH 3 I =1:1 ocurre a 70-80 ° C, y con el aumento de la temperatura del tratamiento térmico a 120 ° C, comienza la destrucción térmica de la perovskita. Cuando la proporción de los reactivos iniciales PbI 2 :CH 3 NH 3 I =1:2, la formación de la estructura de perovskita se produce a través del compuesto intermedio (CH 3 NH 3 ) 2 PbI 4 , y cuando la proporción es 1:3— (CH 3 NH 3 ) 3 PbI 5 y (CH 3 NH 3 ) 2 PbI 4 . Independientemente de la proporción de los componentes iniciales (CH 3 NH 3 I:PbI 2 ), la relación entre el contenido de plomo y yodo en las películas permanece sin cambios, por lo que una diferencia significativa en las propiedades de la película podría explicarse por la anisotropía de la forma de la partícula, lo cual es consistente con los datos de microscopía electrónica y X- difractometría de rayos.
Antecedentes
Hoy en día, la energía solar está emergiendo como fuentes alternativas de energía y el desarrollo de tecnologías para transformar la energía renovable en electricidad es esencial para el avance social [1]. Las células solares más comercializadas basadas en silicio cristalino o multicristalino y semiconductor CuIn, GaSe 2 - x S x , CdTe [2]. En la práctica, la mayoría de las células solares se basan en silicio (85-90%) [3]. Las eficiencias teóricas de conversión de energía (PCE) de estos módulos solares son tan altas como 28-19,9%. Sin embargo, para los módulos solares comercializados, el PCE es solo del 18% para las células solares de silicio cristalino y del 12-14% para el Si policristalino. La principal desventaja de las células solares basadas en silicio y semiconductores es el estrecho rango espectral de sensibilidad a la radiación solar y su banda prohibida indirecta [4]. Esto hace que el uso de un gran espesor (~ 100 μm) de la capa activa aumente la cantidad de absorción de la radiación solar y, en consecuencia, conduce a un costo relativamente alto.
La nueva clase prometedora de célula solar es la de perovskita, que ha atraído un interés considerable de los investigadores debido al notable crecimiento rápido de su PCE. Las perovskitas orgánico-inorgánicas (OIP) son una clase de sustancias con fórmula química típica ABX 3 , donde A es un catión orgánico (a menudo metilamonio CH 3 NH 3 + , formamida CH (NH 2 ) 2 + ), B es un catión inorgánico (generalmente Pb 2+ ), y X es un anión haluro (I - , Cl - o Br - ) [5, 6]. La síntesis de estos compuestos es relativamente fácil y tienen altas características fotoeléctricas, en particular, la gran longitud de difusión de los portadores de carga [7]. Un aumento impresionante de PCE para células solares basadas en OIP de ~ 3.4% en 2004 a 23.3% (22.6% certificado) a principios de 2018 [8,9,10] ha generado un interés considerable en el estudio de sus propiedades. Se obtuvieron logros significativos gracias al desarrollo de una nueva tecnología para la formación de estos compuestos, que permiten la producción de capas activas suaves y densas de dispositivos fotovoltaicos de alto rendimiento [11, 12]. El proceso de formación de una película lisa sin poros requiere un control cuidadoso de la química de las soluciones de precursores y las condiciones para su deposición [13,14,15]. En particular, la deposición de una cantidad estequiométrica de yoduros de metilamonio y plomo (MAI:PbI 2 =1:1) sobre un sustrato de vidrio no permite la preparación de una película densa de perovskitas de yoduro de metilamonio y plomo (MAPbI 3 ), ya que en este caso crecen los cristales en forma de aguja. Esta morfología de la película reduce significativamente el PCE. Al mismo tiempo, se puede preparar una película densa utilizando una cantidad adicional (súper estequiométrica) de MAI [16, 17].
Varias propiedades fundamentales hacen que el OIP sea extremadamente prometedor para aplicaciones fotovoltaicas, incluyendo baja densidad de defectos, larga vida útil del portador de carga y longitud de difusión, baja velocidad de recombinación y alto coeficiente de absorción óptica debido a la banda prohibida directa [18, 19]. Sin embargo, hasta la fecha, muchas de las propiedades fundamentales de OIP aún no se han estudiado en detalle. Se sabe que uno de los principales inconvenientes de esta clase de materiales es su baja estabilidad. La exposición incluso a condiciones atmosféricas ambientales provoca una grave degradación de OIP y, en consecuencia, sus propiedades optoelectrónicas únicas disminuyen. Numerosos trabajos han establecido los efectos de la humedad y el oxígeno, el tratamiento térmico en T > 100 ° С, y la acción de la entrada de radiación UV en MAPbI 3 películas, y se entiende bien que a medida que el MAI se evapora, el PbI sólido 2 permanece en la película [20,21,22,23,24,25,26]. Esta inestabilidad no solo complica la implementación exitosa de células solares basadas en MAPbI 3 , sino también el estudio de las propiedades de este material. En particular, el análisis de difracción de rayos X, Raman y estudios de fotoluminiscencia (PL) con un gran tiempo de exposición (> 6 s) conduce a la destrucción de la perovskita. Por lo tanto, es importante tener en cuenta estas características en el estudio de OIP y distinguir los espectros de los materiales y productos de su descomposición en los factores antes mencionados. Cabe señalar que a pesar de la degradación de este material bajo la influencia de factores externos, el número de trabajos dedicados al estudio de sus propiedades aumenta significativamente cada año [27,28,29]. Esto puede indicar que la comunidad científica cree en la posibilidad de utilizar perovskitas en células solares.
Como se señaló anteriormente, la perovskita MAPbI 3 fue investigado extensamente por varios métodos, pero hoy en día, hay pocos datos sobre la influencia de cantidades no estequiométricas de reactivos en las propiedades de los cristales sintetizados. Al mismo tiempo, la presencia de varios complejos (PbI 3− , PbI 4 2− ) en la solución utilizada para la síntesis de perovskitas orgánico-inorgánicas afecta la microestructura de la película resultante [30, 31]. En particular, el cambio en la proporción de CH 3 NH 3 I:PbI 2 de 1:1 a 1:3 en las soluciones iniciales conduce a cambios significativos en la microestructura y propiedades de las películas [16, 32]. La investigación de los parámetros de dispositivos basados en perovskitas orgánico-inorgánicas CH 3 NH 3 PbI 3-x Cl x mostró que al aumentar el exceso de MAI en la solución inicial en el rango de 1 a 3, los valores de voltaje de circuito abierto (Voc) aumentan, y la densidad de corriente de cortocircuito (Jsc), factor de llenado (FF) y eficiencia de conversión de potencia (PCE ) pasan por un máximo en exceso de MAI de ~ 2-2,6 [33]. Por tanto, el estudio de los mecanismos químicos y físicos, que, con la no estequiometría de los reactivos de partida, afectan significativamente sus propiedades morfológicas y estructurales, es muy importante tanto desde el punto de vista fundamental como para la aplicación práctica de las perovskitas.
Para estudiar la influencia de la no estequiometría de los reactivos de partida sobre las propiedades de la OIP sintetizada, se ha utilizado la espectroscopia Raman y la difractometría de rayos X. La espectroscopia Raman es un método sensible y rápido para diagnosticar varios compuestos tanto en forma de soluciones como en sólidos. La investigación de OIP por espectroscopia Raman y métodos de difractometría de rayos X puede ampliar significativamente la comprensión existente de los procesos de su formación, las características de la estructura cristalina y su efecto en la morfología de la película.
En este artículo, nuestro objetivo es estudiar la formación de películas de perovskita orgánico-inorgánica CH 3 NH 3 PbI 2.98 Cl 0.02 y la influencia de diferentes proporciones de los reactivos de partida (CH 3 NH 3 I:PbI 2 ) en su microestructura.
Métodos
Métodos de síntesis
Yoduro de plomo (PbI 2 ), cloruro de metilamonio CH 3 NH 3 Cl y yoduro de metilamonio presintetizado CH 3 NH 3 Fui utilizado como material de partida. Para estabilizar la estructura de la perovskita, se realizó la sustitución parcial de yodo por cloro mediante la adición de cloruro de metilamonio CH 3 NH 3 Cl [16, 34]. Se utilizó dimetilformamida seca (DMF) como disolvente.
Para la deposición de CH 3 NH 3 PbI 2.98 Cl 0.02 películas (MAPbI 3-x Cl x ), los reactivos de partida PbI 2 , CH 3 NH 3 I y CH 3 NH 3 Cl en proporciones de 1:0,98:0,02 (en adelante 1:1); 1:1,98:0,02 (1:2); 1:2,98:0,02 (1:3) se disolvió en DMF y se agitó a 70ºC durante 1 h. Las películas se depositaron en una caja seca. La solución transparente obtenida previamente se depositó en el sustrato de vidrio purificado y en los sustratos de FTO (óxido de estaño dopado con flúor) mediante recubrimiento por rotación a 1200 rpm durante 30 s. El tratamiento térmico de las películas se llevó a cabo en una placa calefactora precalentada a temperaturas de 70 a 180 ° C durante 30 min.
Caracterización
La microestructura de los reactivos de partida (PbI 2 en CH 3 NH 3 I) y OIP (CH 3 NH 3 PbI 3 ) se estudió utilizando un microscopio electrónico de barrido SEC miniSEM SNE 4500 MB. La composición elemental de las películas se determinó mediante un espectrómetro EDAX Element PV6500 / 00 F, que se incluye en el conjunto de este microscopio.
La composición de fase de las películas se identificó mediante difractometría de rayos X en polvo (XRPD) usando un difractómetro DRON-4-07 (radiación CuKα, 40 kW, 18 mA) sobre 2Θ =10-120 °, un paso de 0.04 °, y un tiempo de recuento de 4 s. Los parámetros estructurales se determinaron mediante el método de análisis de perfil de Rietveld utilizando datos XRPD. Los espectros Raman fueron excitados por líneas de láser de estado sólido de 532 y 671 nm y adquirieron el uso de monocromador de una sola etapa equipado con detector de dispositivo de carga acoplada (CCD) (Andor). La potencia del láser excitante se mantuvo lo más baja posible, para evitar el daño de las moléculas bajo investigación debido al calentamiento o reacciones fotoquímicas.
Resultados y discusión
Investigación de soluciones
La Figura 1 a, b muestra los espectros Raman de DMF pura (curva 1) y compuestos disueltos como PbI 2 (curva 2), CH 3 NH 3 I (curva 3), PbI 2 y CH 3 NH 3 I en la proporción 1:1 (curva 4), PbI 2 y CH 3 NH 3 I en la proporción 1:2 (curva 5), PbI 2 y CH 3 NH 3 I en la proporción 1:3 (curva 6) y PbI 2 y CH 3 NH 3 Cl en la relación 1:1 (curva 7) obtenida por excitación láser en λ =532 nm a temperatura ambiente. Cabe señalar que las soluciones tanto de PbI 2 y CH 3 NH 3 Yo en DMF soy prácticamente transparente. En la disolución simultánea de PbI 2 y CH 3 NH 3 En DMF, la coloración de una solución cambia de amarillo claro en una proporción de componentes (1:1) a amarillo oscuro (1:3). La coloración de la solución muestra que existe una interacción química entre los componentes de PbI 2 y CH 3 NH 3 I.
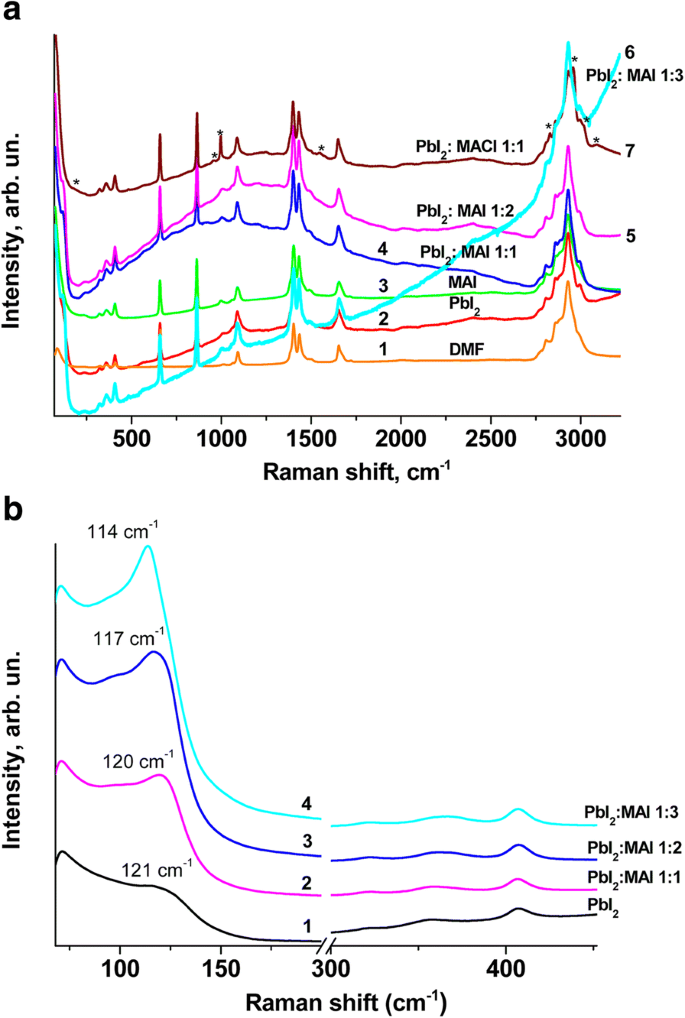
un Espectros Raman de un disolvente DMF (curva 1) y compuestos disueltos en él:2 - PbI 2 , 3 - CH 3 NH 3 I, 4 - PbI 2 y CH 3 NH 3 I (1:1), 5 - PbI 2 y CH 3 NH 3 I (1:2), 6 - PbI 2 y CH 3 NH 3 I (1:3), 7 - PbI 2 y CH 3 NH 3 Cl (1:1). b Espectros Raman de soluciones:1- PbI 2 , 2 - PbI 2 y CH 3 NH 3 I (1:1), 3 - PbI 2 y CH 3 NH 3 I (1:2), 4 - PbI 2 y CH 3 NH 3 I (1:3) en DMF en el rango de baja frecuencia. Todos los espectros se obtuvieron con λ exc =532 nm a temperatura ambiente
Aparecen bandas suficientemente intensas en la región espectral de 50 a 3500 cm −1 en el espectro Raman de DMF (curva 1). Casi todas las mismas bandas ocurren en el espectro de la solución de PbI 2 en DMF (curva 2), excepto uno, que es una manifestación del modo de vibración de Pb-I con una frecuencia de ~ 114 cm −1 y algunas características en la región de 475 cm −1 . Solo las bandas Raman de DMF (curva 3) aparecen en el espectro de la solución de CH 3 NH 3 Yo en DMF.
En los espectros de soluciones en las que tanto PbI 2 y CH 3 NH 3 Los compuestos I se agregaron en una proporción de 1:1 y 1:2, a excepción de las bandas con frecuencias de 114 cm −1 , aparecen bandas anchas con máximos a 1000 y 1250 cm −1 (Fig. 1a, curvas 4, 5), respectivamente. Para el espectro de la solución en la que el PbI 2 y CH 3 NH 3 Los compuestos I se añadieron en una proporción de 1:3, los cambios máximos a una región de onda larga (Fig. 1a, curva 6). Lo más probable es que todos ellos aparezcan debido a la contribución de la fotoluminiscencia del compuesto formado CH 3 NH 3 PbI 3 porque cuando los espectros Raman se excitan con radiación λ =671 nm, no aparecen en los espectros (los espectros se muestran en el archivo adicional 1).
Como se señaló anteriormente, la banda de vibración característica Pb-I aparece en el rango de 114-121 cm −1 (Fig. 1b) en todos los espectros Raman de soluciones con diferentes proporciones de PbI 2 y CH 3 NH 3 Yo compuestos. Su intensidad relativa aumenta y el máximo de las bandas se desplaza hacia el lado de baja frecuencia con un aumento en CH 3 NH 3 Me contento en la solución (Fig. 1b). Este cambio del pico Raman se correlaciona con el cambio del borde de absorción óptica de 2,54 eV para PbI 2 en DMF hasta 2,24 eV para la mezcla de PbI 2 y CH 3 NH 3 Mezclé en una proporción de 1:3 (los espectros se agregan al archivo adicional 1:Figuras S1 y S2). Estos cambios espectrales indican que la adición de CH 3 NH 3 I aumenta la probabilidad de formar poliyoduros de plomo, como [PbI 3 ] −1 , [PbI 4 ] −2 , [PbI 5 ] −3 y [PbI 6 ] −4 . Nuestros resultados se correlacionan con el resultado del trabajo [31], donde se demostró la influencia de los precursores en las propiedades estructurales y ópticas de las perovskitas. La diferente composición de los poliyoduros puede provocar la diferente morfología de las películas de perovskita, incluidas las observadas en nuestro trabajo. Dado que una pequeña fracción de CH 3 NH 3 Cl (2% en relación con CH 3 NH 3 I) se añadió a la solución junto con CH 3 NH 3 Yo, era necesario establecer la posible contribución de este compuesto a los espectros Raman. Para ello, el espectro Raman de CH 3 NH 3 Se registró Cl en DMF (Fig. 1a, curva 7). Muestra una serie de bandas adicionales con las siguientes frecuencias:178, 953, 997, 1547, 2829, 2957, 3020 y 3092 cm −1 , que en la Fig. 1a, la curva 7 están marcadas con asteriscos. De hecho, las frecuencias de estas bandas están cerca de las frecuencias de las bandas Raman del compuesto CH 3 NH 3 PbICl 2 , obtenido en [35]. Sin embargo, las bandas mencionadas anteriormente no se manifiestan en los espectros Raman de CH 3 NH 3 PbI 2.98 Cl 0.02 soluciones debido a una pequeña fracción de átomos de cloro.
Investigación de películas
La Figura 2 muestra imágenes de las películas de los reactivos iniciales depositadas sobre la superficie de los sustratos de vidrio.

Imágenes de CH 3 NH 3 Yo ( un , b ) y PbI 2 ( c , d ) películas sin calentar ( a , c ) y después del tratamiento térmico a 90 ° С ( b , d ), depositado sobre sustratos de vidrio. Insertar en a —Aumento de la imagen de heterogeneidad de SEM-BSE
La microestructura del CH 3 NH 3 Parece un vidrio con pequeñas heterogeneidades de cierta forma en la superficie (Fig. 2a). Los estudios de espectroscopía de rayos X microscópicos y de dispersión de energía (EDX) han demostrado que las películas son más delgadas en el área de heterogeneidades El análisis de la EEB (electrones de retrodispersión) sugiere que esto se debe al aumento del nivel de superficie en estos lugares (consulte los espectros EDX en el archivo adicional 1). Estas áreas probablemente se forman debido a la rápida evaporación del solvente de la película. El aumento significativo en el número de tales heterogeneidades con el aumento de temperatura a 90 ° C confirma este hecho (Fig. 2b).
Cuando PbI 2 La solución se deposita a temperatura ambiente (sin calentar), los granos grandes alargados (en forma de alambre [36]) crecen en todas las direcciones (Fig. 2c). A 90 ° C, inicialmente, los granos en forma de alambre crecen a partir de un pequeño número de centros de cristalización. Además, se forma la solución sobresaturada y los granos crecen en régimen sobresaturado [37, 38] con los granos en forma de alambre inicialmente formados como partículas de semillas (Fig. 2d).
La Figura 3 muestra la superficie de las películas de perovskitas orgánico-inorgánicas que se depositaron sobre el sustrato de vidrio y FTO / vidrio. Cuando los reactivos iniciales (CH 3 NH 3 I:PbI 2 ) se tomaron en la proporción 1:1, la microestructura de la película de perovskita orgánico-inorgánica depositada sobre el sustrato de vidrio y FTO / vidrio prácticamente no difiere:hay películas estructuradas con una anisotropía significativa de la forma de la partícula (en forma de aguja) . En el caso de una proporción de reactivos iniciales 1:2, las partículas en forma de hoja de arce son visibles en el vidrio. El crecimiento de este último se produce desde el centro de cristalización en 5-6 direcciones. Entre las partículas grandes, aparecen partículas pequeñas en forma de hojas (ver el inserto en la Fig. 3b). Al mismo tiempo, después de la deposición de la película sobre la superficie de vidrio / FTO, las partículas se vuelven más isotrópicas en la forma. Esto coincidió con los datos de Ref. [39], donde se observa una fuerte diferencia en las microestructuras para películas depositadas sobre diferentes sustratos policristalinos y amorfos. En el caso de la proporción de reactivos iniciales 1:3, el tamaño de las partículas se reduce significativamente y se forma una película más densa.

Imágenes de películas de perovskitas orgánico-inorgánicas depositadas sobre sustratos de vidrio ( a - c ) y FTO / vidrio ( d - f ). Insertar en b —La imagen ampliada del área entre granos
La Figura 4 muestra los resultados del análisis XRPD de películas después del tratamiento térmico en el rango de temperatura de 70 a 180 ° C.
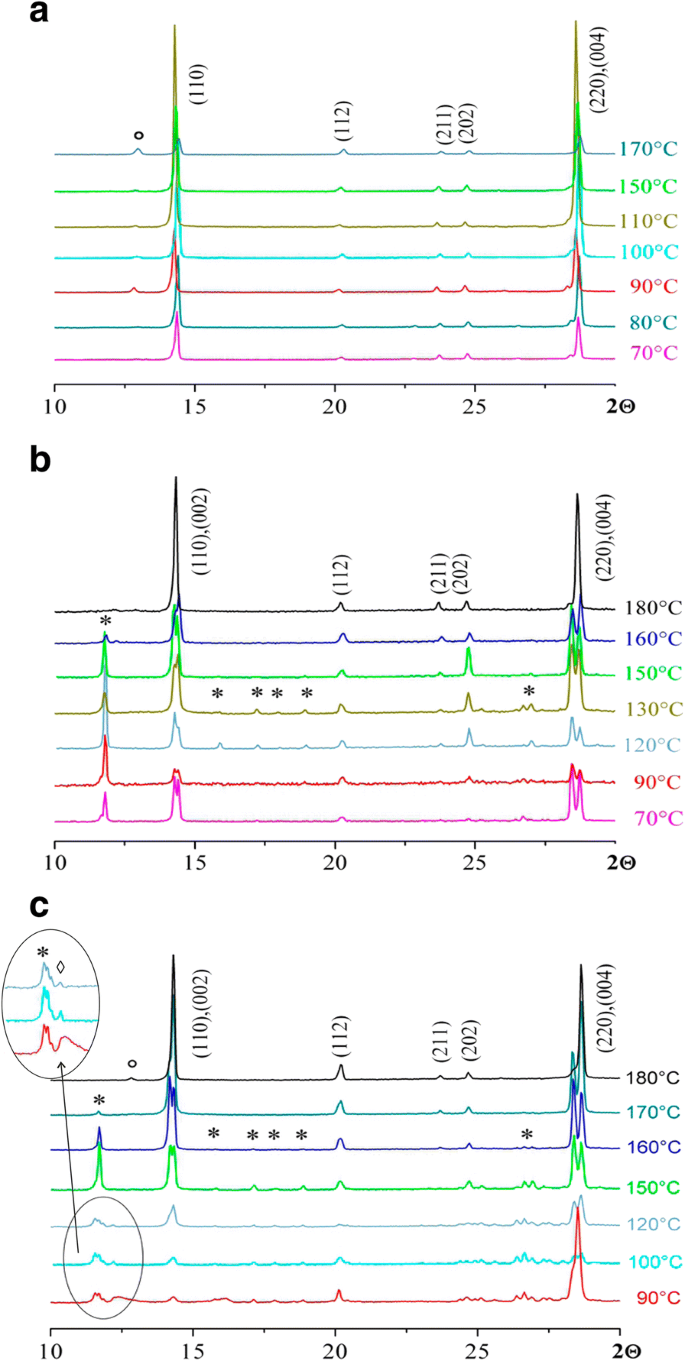
Patrón de difracción de rayos X de CH 3 NH 3 PbI 3 películas obtenidas con diferentes proporciones de los reactivos de partida PbI 2 y CH 3 NH 3 Yo: un 1:1. b 1:2. c 1:3, asterisco denota (CH 3 NH 3 ) 2 PbI 2 ; diamante denota (CH 3 NH 3 ) 3 PbI 5
Para el sistema con la proporción de los reactivos iniciales PbI 2 :CH 3 NH 3 I =1:1, se encontró que el producto monofásico se forma a 70-80 ° С por la reacción:
$$ \ mathrm {PbIz} + \ mathrm {CH} 3 \ mathrm {NH} 3 \ mathrm {I} \ overset {70-80 {} ^ {\ circ} \ mathrm {C}} {\ to} \ mathrm {C} \ mathrm {H} 3 \ mathrm {NH} 3 \ mathrm {PbI} 3. $$ (1)La síntesis de CH 3 NH 3 PbI 3 películas se llevó a cabo en una caja de guantes, es por eso que la formación de fases de mono y dihidratos (CH 3 NH 3 PbI 3 · H 2 O, (CH 3 NH 3 ) 4 PbI 6 · 2H 2 O), que son típicos de la síntesis en una atmósfera húmeda, no se observó (Fig. 4a) [40, 41].
El aumento de las temperaturas conduce a la aparición de PbI 2 picos (2Θ =12,8 °), lo que puede explicarse por la descomposición parcial de la perovskita. Se ha demostrado que otros posibles productos de la descomposición de perovskita CH 3 NH 3 PbI 3 , a excepción de la fase de PbI 2 , son CH 3 NH 2 y HI [42, 43]. Los autores [44] han demostrado que en los espectros de espectroscopía infrarroja por transformada de Fourier (FTIR) de los productos, hay bandas que indican la presencia de un enlace C-I. Por lo tanto, la reacción de descomposición de la perovskita orgánico-inorgánica se puede escribir como:
$$ \ mathrm {CH} 3 \ mathrm {NH} 3 \ mathrm {PbI} 3 \ overset {> 80 {} ^ {\ circ} \ mathrm {C}} {\ to} \ mathrm {PbI} 2+ \ mathrm {CH} 3 \ mathrm {I} \ uparrow + \ mathrm {NH} 3 \ uparrow $$ (2)Para los sistemas, donde los reactivos de partida estaban en la proporción PbI 2 :CH 3 NH 3 I =1:2, después de la evaporación del solvente, la formación de la fase adicional (CH 3 NH 3 ) 2 PbI 4 se ha observado (Fig. 4b). Con el aumento de la temperatura del tratamiento térmico hasta 180 ° C, se ha observado la disminución de la intensidad de este pico. A 180 ° C, las películas resultantes eran monofásicas. El esquema de la reacción de formación de perovskita, donde los reactivos de partida se tomaron en las proporciones PbI 2 :CH 3 NH 3 I =1:2, se puede escribir como:
$$ \ mathrm {Pb} {\ mathrm {I}} _ 2 + 2 \ \ mathrm {C} {\ mathrm {H}} _ 3 \ mathrm {N} {\ mathrm {H}} _ 3 \ mathrm {I} \ \ overset {20-120 {} ^ {\ circ} \ mathrm {C}} {\ to} {\ left (\ mathrm {C} {\ mathrm {H}} _ 3 \ mathrm {N} {\ mathrm {H }} _ 3 \ right)} _ 2 \ mathrm {Pb} {\ mathrm {I}} _ 4 \ overset {> 180 {} ^ {\ circ} \ mathrm {C}} {\ to} $$$$ \ overset {> 180 {} ^ {\ circ} \ mathrm {C}} {\ to} \ mathrm {C} {\ mathrm {H}} _ 3 \ mathrm {N} {\ mathrm {H}} _ 3 \ mathrm {Pb} {\ mathrm {I}} _ 3+ \ kern0.5em \ mathrm {C} {\ mathrm {H}} _ 3 \ mathrm {I} \ uparrow + \ mathrm {N} {\ mathrm {H}} _ 3 \ uparrow $$ (3)Cuando los reactivos iniciales estaban en la proporción PbI 2 :CH 3 NH 3 I =1:3, la fase intermedia (CH 3 NH 3 ) 3 PbI 5 se formó, así como una fase (CH 3 NH 3 ) 2 PbI 4 (Figura 4c). Fases intermedias (CH 3 NH 3 ) 3 PbI 5 y (CH 3 NH 3 ) 2 PbI 4 fueron descritos en [44, 45]. Con el aumento de la temperatura del tratamiento térmico hasta 170 ° C, se forma una estructura de perovskita monofásica. El esquema de la reacción de formación de perovskita se puede escribir como:
$$ \ mathrm {Pb} {\ mathrm {I}} _ 2 + 3 \ \ mathrm {C} {\ mathrm {H}} _ 3 \ mathrm {N} {\ mathrm {H}} _ 3 \ mathrm {I} \ desbordado {20-120 {} ^ {\ circ} \ mathrm {C}} {\ to} {\ left (\ mathrm {C} {\ mathrm {H}} _ 3 \ mathrm {N} {\ mathrm {H} } _3 \ right)} _ 3 \ mathrm {Pb} {\ mathrm {I}} _ 5 \ overset {> 120 {} ^ {\ circ} \ mathrm {C}} {\ to} $$$$ \ overset {> 120 {} ^ {\ circ} \ mathrm {C}} {\ to} {\ left (\ mathrm {C} {\ mathrm {H}} _ 3 \ mathrm {N} {\ mathrm {H}} _ 3 \ right )} _ 2 \ mathrm {Pb} {\ mathrm {I}} _ 4+ \ mathrm {C} {\ mathrm {H}} _ 3 \ mathrm {I} \ uparrow + \ mathrm {N} {\ mathrm {H}} _ 3 \ uparrow \ overset {> 170 {} ^ {\ circ} \ mathrm {C}} {\ to} $$$$ \ overset {> 170 {} ^ {\ circ} \ mathrm {C}} {\ to} \ \ mathrm {C} {\ mathrm {H}} _ 3 \ mathrm {N} {\ mathrm {H}} _ 3 \ mathrm {Pb} {\ mathrm {I}} _ 3+ \ kern0.5em \ mathrm {C} { \ mathrm {H}} _ 3 \ mathrm {I} \ uparrow + \ mathrm {N} {\ mathrm {H}} _ 3 \ uparrow $$ (4)Con el aumento de la temperatura del tratamiento térmico hasta 180 ° C, se ha observado la descomposición térmica de la perovskita de acuerdo con la reacción química (2).
Se sabe que las perovskitas de CH 3 NH 3 PbI 3 puede tomar tres fases diferentes:ortorrómbica a temperaturas por debajo de - 111 ° С [46], tetragonal en el rango de temperatura de - 110 a 51 ° C, y cúbica a temperaturas superiores a 51 ° C [47]. En todos nuestros sistemas (1:1, 1:2, 1:3) se ha observado simetría tetragonal (grupo espacial I4 / mcm), que se confirma con la división de picos (220) / (004) (Fig. . 5).
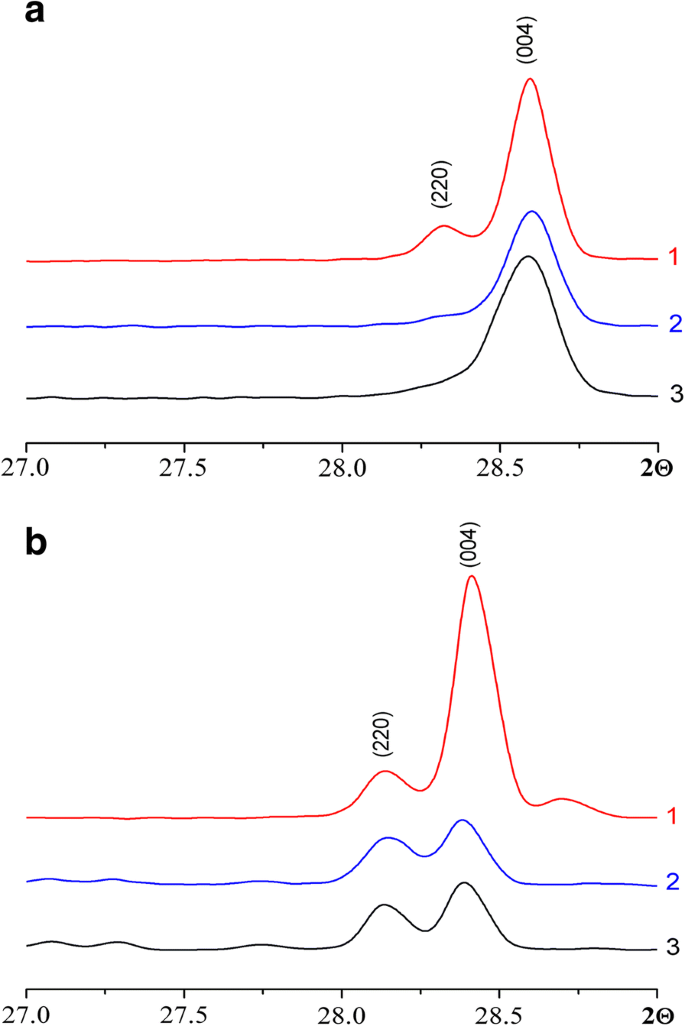
Patrón XRPD de picos 220 y 004 de CH 3 NH 3 PbI 3 películas depositadas sobre el sustrato de vidrio ( a ) y en la FTO ( b ) a 85 ° C en diferentes proporciones de los reactivos de partida PbI 2 y CH 3 NH 3 Yo:1:1 (1); 1:2 (2); 1:3 (3)
La Figura 5 muestra la difracción XRPD en un rango estrecho de 2Θ (27–29 °) para picos (220) y (004), para películas que se depositaron sobre vidrio y sustratos de vidrio / FTO. La relación de las intensidades de estos picos depende de varios factores:composición química, ocupación de posiciones en la estructura y anisotropía de la forma de las partículas. Anteriormente, hemos demostrado que independientemente de la proporción de los componentes iniciales (CH 3 NH 3 I:PbI 2 =1:1, 1:2, 1:3), la relación entre el contenido de plomo y yodo en las películas permanece invariable [20]. Como han demostrado los cálculos, la mayor contribución a la intensidad da el elemento más pesado:el plomo (en la proporción 1:2). Pero para una muestra sintetizada en una proporción de los reactivos de partida 1:1, la proporción de las intensidades de los picos es significativamente mayor que en el caso del sistema 1:2. Una diferencia tan significativa en la intensidad de los picos (220) y (004) podría explicarse solo por la anisotropía de la forma de la partícula, que es consistente con los datos de microscopía electrónica (Fig. 3). De forma adecuada, la forma de las partículas para la muestra PbI 2 :CH 3 NH 3 I =1:1 depositado sobre el sustrato de vidrio es fuertemente anisotrópico (ver Fig. 3a). Para muestras sintetizadas en una relación de los reactivos iniciales 1:2 y 1:3, las relaciones de las intensidades de los picos (220) y (004) prácticamente iguales, lo que es consistente con la pequeña anisotropía de las partículas o su ausencia. (ver Fig. 3 b, c respectivamente). Se observan resultados similares para las muestras, donde las películas se depositan sobre el sustrato de vidrio / FTO.
Para un estudio más detallado de la influencia de la relación de reactivos iniciales PbI 2 :CH 3 NH 3 I y la temperatura de cristalización de la película sobre la formación de la estructura de perovskitas, se llevó a cabo la espectroscopía Raman.
Figura 6, curva 1 muestra el espectro Raman del CH 3 NH 3 PbI 3 película formada a partir de la solución de PbI 2 y CH 3 NH 3 I compuestos en la proporción (1:1) en DMF y se registra a una potencia suficientemente pequeña de excitación de radiación láser (~ 5 × 10 2 W / cm 2 ). Los espectros de CH 3 NH 3 PbI 3 películas, formadas a partir de la solución de PbI 2 y CH 3 NH 3 I en DMF que se toman en la proporción 1:1, 1:2 y 1:3, son similares y no se muestran para las dos últimas películas (los espectros se muestran en el archivo adicional 1). Esto sugiere que a pesar de la diferente morfología de la película [32], sus unidades estructurales son la red cristalina de la perovskita tetragonal. Como se señaló anteriormente, las películas de perovskita son bastante sensibles a factores externos (humedad, rayos X intensos y radiación láser). Cuando las películas se irradiaron con radiación láser excitante durante 200 s, el espectro Raman cambia significativamente (Fig. 6, curva 2). Se produce un cambio similar en los espectros cuando la densidad de potencia de la radiación láser excitante aumenta unas cinco veces. Con este efecto de la radiación láser, el CH 3 NH 3 PbI 3 la película se transforma en un estado metaestable, que es un estado de transición de la perovskita al PbI 2 . De hecho, la radiación láser intensa puede provocar la destrucción de enlaces químicos en el CH 3 NH 3 PbI 3 , ya la excitación del subsistema electrónico de unidades estructurales individuales, lo que contribuye a la formación de una estructura metaestable. En particular, tal estado puede ser el resultado de la intercalación del compuesto formado debido a la destrucción parcial de la perovskita en PbI 2 [44]. El cambio en la forma de los espectros Raman de las películas en tal estado metaestable se observa directamente en el proceso de sus mediciones. En particular, después de una irradiación adicional de la película por radiación láser durante 200 s, el espectro Raman ha cambiado significativamente (Fig. 6, curva 2). En la Fig.6, a modo de comparación, los espectros de las películas formadas por la deposición de la solución de DMF con PbI 2 (curva 4) y CH 3 NH 3 También se dan los compuestos I (curva 5). Mayor aumento del tiempo de irradiación del CH 3 NH 3 PbI 3 La película por radiación láser con el mismo poder conduce a la destrucción completa del CH 3 NH 3 PbI 3 . Como resultado, el espectro es similar a la curva 4, en la Fig.3, que corresponde a los espectros vibracionales del PbI 2 compuesto. Cabe señalar que la destrucción del CH 3 NH 3 PbI 3 perovskita durante su interacción con la humedad es mucho más lenta [48].
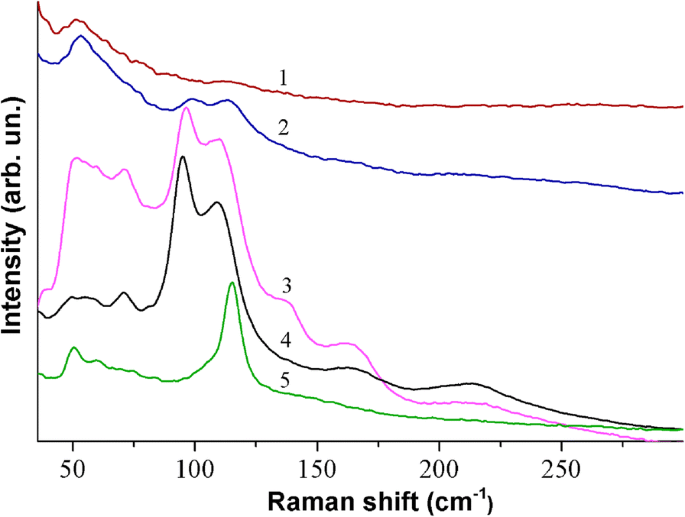
Espectros Raman de CH 3 NH 3 PbI 3 películas formadas por la mezcla 1:1 de PbI 2 y CH 3 NH 3 I en DMF:directamente después de la deposición sobre un sustrato de vidrio en T =90 ° C (1); después de la irradiación con luz láser durante 200 s (2); después de la irradiación durante 400 s (3). Espectros Raman de películas formadas a partir de la solución de PbI 2 puro (4) y CH 3 NH 3 I (5) en DMF. Todos los espectros se obtuvieron con λ exc =532 nm a temperatura ambiente
Los resultados del análisis de difracción de rayos X mostraron que cuando la proporción de los reactivos iniciales PbI 2 :CH 3 NH 3 I =1:2 y 1:3, la formación de la estructura de perovskita ocurre a través de intermedios (CH 3 NH 3 ) 3 PbI 5 y (CH 3 NH 3 ) 2 PbI 4 . En los espectros Raman, es difícil detectar estos compuestos, ya que las frecuencias de los modos vibracionales de CH 3 NH 3 PbI 3 , (CH 3 NH 3 ) 3 PbI 5 y (CH 3 NH 3 ) 2 PbI 4 en la región de baja frecuencia del espectro están bastante cerca [49].
También llevamos a cabo estudios Raman de películas de perovskita formadas a partir de soluciones de PbI 2 y CH 3 NH 3 I compuestos (1:3) en DMF, que se recocieron en el intervalo de temperatura de 100 a 180 ° C (Fig. 7). Los espectros de las películas que se trataron a temperaturas de hasta 180 ° C son bastante similares al espectro 1, que se muestra en la Fig. 6. Sin embargo, el espectro Raman de la película que se trató en T =180 ° C ya corresponde al espectro de la fase metaestable (curva 3 en la Fig. 6). Estos resultados se correlacionan con los datos del análisis de difracción de rayos X.
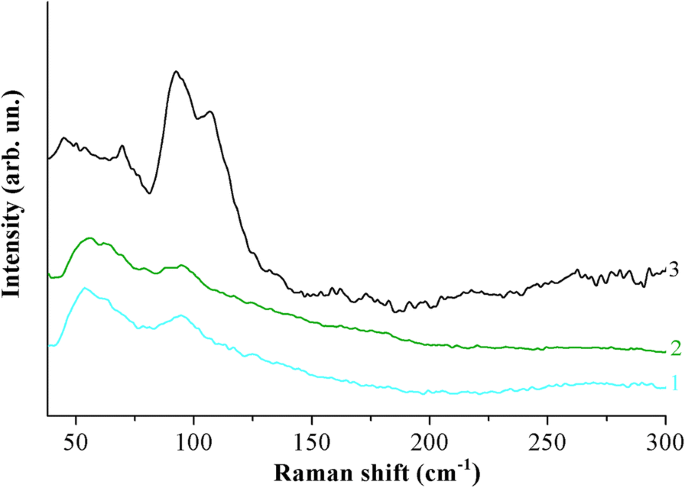
Raman spectra of the films formed of the solution of PbI2 and CH3 NH 3 I compounds in DMF in the ratio (1:3) at temperatures of 100 (1), 150 (2), and 180 °C (3). All spectra were obtained with λ exc = 532 nm at room temperature
Conclusiones
Therefore, the possibility to control morphology, structural, and optical properties of CH3 NH 3 PbI 3 films by variation of the ratio of initial compounds, of PbI2 and CH3 NH 3 I in DMF solvent, was found. X-ray diffraction analysis has shown that the formation of the perovskite structure with the ratio of the initial reagents PbI2 :CH3 NH 3 I = 1:1 occurs at 70–80 °C, and with the increase of the temperature of thermal treatment to 120 °C, the thermal destruction of the perovskite begins. When the ratio of the starting reagents PbI2 :CH3 NH 3 I = 1:2, the formation of the perovskite structure occurs through the intermediate compound (CH3 NH 3 ) 2 PbI4 , and when the ratio is 1:3—(CH3 NH 3 ) 3 PbI5 and (CH3 NH 3 ) 2 PbI4 . Independent on the ratio of the initial components (CH3 NH 3 I:PbI2 ), the ratio between the content of lead and iodine in the films remains unchanged, that is why a significant difference in the film properties could be explained by the anisotropy of the particle shape, which is consistent with the data of electron microscopy, as well as with X-ray diffractometry (change in the ration of peaks (220) and (004) intensity). By using Raman spectroscopy, it was shown that films are sensitive to laser radiation, which leads to destruction, the final product of which is PbI2 . When illuminated with laser radiation with low power density, they may be in a metastable state for some time, which is a transition from perovskite to PbI2 .
Abreviaturas
- BSE:
-
Backscattering electrons
- CCD:
-
Charge-coupled device
- DMF:
-
Dimethylformamide, C3 H 7 NO
- EDX:
-
Espectroscopia de rayos X de dispersión de energía
- FTIR:
-
Espectroscopía infrarroja por transformada de Fourier
- FTO:
-
Óxido de estaño dopado con flúor
- MAI:
-
Methylammonium iodide
- MAPbI 3 :
-
Methylammonium lead iodide perovskites, CH3 NH 3 PbI 3
- MAPbI3-x Clx :
-
Methylammonium lead iodide chloride perovskites, CH3 NH 3 PbI2.98 Cl0.02
- OIP:
-
Organic-inorganic perovskites
- PCE:
-
Power conversion efficiencies
- XRPD:
-
X-ray powder diffractometry
Nanomateriales
- Preparación y propiedades magnéticas de nanopartículas de espinela de FeMn2O4 dopadas con cobalto
- El reordenamiento atómico de múltiples pozos cuánticos basados en GaN en gas mixto H2 / NH3 para mejorar las propiedades estructurales y ópticas
- Hacia los nanofluidos de TiO2:Parte 1:Preparación y propiedades
- Efecto de la distribución de nanopartículas de oro en TiO2 sobre las características ópticas y eléctricas de las células solares sensibilizadas por colorante
- Efecto del confinamiento en las propiedades fotofísicas de las cadenas P3HT en la matriz de PMMA
- El efecto del plasma de no equilibrio por contacto sobre las propiedades estructurales y magnéticas de Mn Х Fe3 - X О4 Espinelas
- Propiedades paramagnéticas de nanomateriales derivados del fullereno y sus compuestos poliméricos:efecto de bombeo drástico
- Efectos del espesor de la bicapa en las propiedades morfológicas, ópticas y eléctricas de los nanolaminados de Al2O3 / ZnO
- Síntesis de nanocristales de ZnO y aplicación en células solares de polímero invertido
- Efecto sinérgico del grafeno y los MWCNT en la microestructura y las propiedades mecánicas de los nanocompuestos de Cu / Ti3SiC2 / C
- Propiedades ópticas del infrarrojo cercano visible y estructural del TiO2 dopado con Cr para pigmentos fríos coloreados



