Efectos antimicrobianos y citotóxicos de las nanopartículas de plata sintetizadas del extracto de piel de Punica granatum
Resumen
Para abordar los crecientes desafíos de los microbios resistentes a los medicamentos y la incidencia de tumores, se están adoptando enfoques para fitosintetizar nanopartículas de metal, particularmente nanopartículas de plata, para obtener medidas correctivas. En este estudio, se ha intentado utilizar un importante producto de residuos biológicos, la cáscara de la granada ( Punica granatum ), para sintetizar nanopartículas de plata. Las nanopartículas de plata (AgNP) se sintetizaron utilizando el extracto acuoso de piel de granada. La formación de AgNP sintetizados se confirmó mediante espectroscopía UV-Vis, difracción de rayos X (XRD), microscopía electrónica de transmisión (TEM), microscopía electrónica de barrido (SEM) y espectroscopía de rayos X de dispersión de energía (EDX), así como mediante el cambio de la solución acuosa incolora a una solución de color marrón oscuro. Usando espectroscopía UV-Vis, la solución de color marrón oscuro mostró un pico de banda de resonancia de Plasmon a 378 nm en espectroscopía UV-Vis después de reaccionar durante 24, 48 y 72 h. El informe XRD reveló que los AgNP tenían una estructura cúbica. El informe TEM y SEM mostró que las nanopartículas estaban distribuidas por igual en la solución, con una forma esférica y un tamaño que variaba de 20 a 40 nm y con un tamaño de partícula promedio de 26,95 nm. Las imágenes EDX también confirmaron la presencia de AgNP. Se encontró que los AgNP sintetizados exhiben buenos efectos antimicrobianos sobre bacterias Gram negativas y Gram positivas, particularmente los patógenos Escherichia coli (ATCC 25922), Pseudomonas aeruginosa (ATCC 27584), Proteus vulgaris (ATCC 8427), Salmonella typhi (ATCC 14028), Staphylococcus aureus (ATCC 29213), Staphylococcus epidermidis (MTCC 3615) y neumonía por Klebsiella . Los efectos citotóxicos de los AgNP también se probaron contra una línea celular de cáncer de colon (RKO:ATCC® CRL-2577 ™), y se observó que las viabilidades fueron 56% y 61% en los días 3 y 5, respectivamente, con exposición a 12,5 μg de AgNP. Este método simple, económico y ecológico sugiere que los AgNP biosintetizados con extracto de cáscara de granada pueden ser una solución novedosa y potente para el desarrollo de un fármaco para el cáncer de colon que también tiene actividad antibacteriana.
Antecedentes
En las últimas décadas, ha habido una cantidad creciente de investigación sobre nanotecnología, particularmente en lo que respecta a la síntesis y caracterización verde de nanopartículas, ya que las nanopartículas de menos de 100 nm de tamaño son agentes ideales para la administración de fármacos y aplicaciones biomédicas [1]. La síntesis de nanopartículas juega un papel influyente en varios campos, que incluyen la nanotecnología, la biotecnología, el procesamiento químico, la metodología física, la ingeniería de sistemas, los motores moleculares, los nanocristales y los nanobiomateriales [2]. Actualmente existen tres métodos de producción de nanopartículas:rutas químicas, físicas y "verdes", y la ruta verde implica el empleo de agentes reductores biológicos, incluidos extractos de plantas y filtrados microbianos. Los dos primeros métodos suelen ser costosos y generan subproductos tóxicos, pero el método de nanosíntesis verde ha sido reconocido como un proceso económico y ecológico [3, 4, 5].
En la síntesis verde de NP, se utilizan componentes vegetales, incluidas proteínas, enzimas y carbohidratos, para formular nanopartículas que pueden interactuar fácilmente con biomoléculas diana [6]. Este enfoque de la síntesis de nanopartículas de plata puede desempeñar un papel importante en futuros tratamientos para diversas formas de cáncer u otras dolencias que pueden ser controladas por fito-nanotecnología [7, 8]. Bacterias gramnegativas, como Escherichia coli , Pseudomonas aeruginosa y Proteus vulgaris y patógenos grampositivos, como Staphylococcus aureus y S. epidermidis , son responsables de la mayoría de las infecciones adquiridas en el hospital [9]. De hecho, las infecciones quirúrgicas, incluidas la neumonía y las infecciones del torrente sanguíneo, también se deben a la presencia de bacterias Gram positivas y Gram negativas [10]. La síntesis de AgNP mediada por plantas puede ayudar en el desarrollo de agentes antibacterianos eficaces contra patógenos microbianos de importancia para la salud pública. Recientemente, se ha observado que los AgNP sintetizados pueden tener una relación sinérgica con el antibiótico levofloxacino, aumentando la actividad antimicrobiana total [11]. Muchos investigadores han informado de que los AgNP sintetizados contienen propiedades antimicrobianas bien conocidas contra patógenos Gram-positivos y Gram-negativos, así como efectos citotóxicos en diferentes líneas celulares cancerosas y normales [12,13,14]. Además, los AgNP son altamente eficientes debido a una alta proporción de área de superficie a volumen, pueden romperse fácilmente y tienen la capacidad de penetrar en las células bacterianas en comparación con los iones de plata solos [13].
El estudio actual se centra en la síntesis verde de AgNP utilizando el extracto acuoso de Punica granatum pelar y en la investigación de sus propiedades antimicrobianas mediante el uso de placas de rayas y mediciones de concentración mínima de inhibición (MIC) después de 24 h de incubación a 37 ° C. Las bacterias Gram-negativas E. coli (ATCC 25922), P. aeruginosa (ATCC 27584), P. vulgaris (ATCC 8427) y Salmonella typhi (ATCC 14028) así como las bacterias Gram positivas Staphylococcus aureus (ATCC 29213), S. epidermidis (MTCC 3615) y K. pneumoniae se estudiaron para probar la inhibición potencial del crecimiento por los AgNP sintetizados. Además, se probaron los efectos citotóxicos en una línea celular de cáncer de colon (RKO:ATCC® CRL-2577 ™) y mostraron una tasa de viabilidad celular del 56% el día 3 y del 61% el día 5 con una dosis de 12,5 μg de AgNP.
Métodos
Preparación del extracto de cáscara
Un kilogramo de frutos de granada saudí ( Punica granatum (Cultivado en la región de Taif del Reino de Arabia Saudita) se compró en el supermercado de Riad, Arabia Saudita. Los frutos se lavaron varias veces con agua del grifo y luego con agua bidestilada (DDH 2 O). Después del lavado, la cáscara se retiró con cuidado. La cáscara de granada se enjuagó a fondo con DDH 2 O para evitar cualquier contaminación de la superficie y dejar secar completamente a temperatura ambiente. Finalmente, la cáscara se molió hasta obtener una fina potencia. Se remojaron diez gramos del polvo fino en 100 mL de DDH 2 O durante 24 ha temperatura ambiente. La mezcla resultante se filtró usando papel de filtro Whatman No. 1 para adquirir el extracto acuoso. Todo el proceso se realizó en condiciones esterilizadas.
Proceso de síntesis de AgNPs
Nitrato de plata (AgNO 3 ; 0,1 mM) se mezcló con 250 ml de DDH2O. Luego, se agregaron diez mililitros de extracto acuoso de cáscara de granada y la solución se mezcló completamente usando una incubadora con agitación durante 5 min. Se encontró que la mezcla de reacción cambiaba su color de una solución incolora a una solución de color marrón después de 24 h, lo que indica la reducción de los iones de plata en nanopartículas de plata. A continuación, la solución de nanopartículas se centrifugó a 15.000 rpm durante 15 minutos y el proceso se repitió cuatro veces. Finalmente, se recolectaron los AgNP purificados y se realizaron más ensayos para analizar las características y actividades biológicas de los NP sintetizados. El exceso de extracto de cáscara se almacenó a 4 ° C para su posterior análisis.
Caracterización de los AgNPs
La reducción de iones de plata por el extracto acuoso de cáscara de granada se controló utilizando un espectrofotómetro Perkin Elmer Lambda 950 UV / Vis / NIR 24, 48 y 72 h después del inicio de la reacción de 200 a 800 nm y a una resolución de 1 nm. . Los patrones de XRD se obtuvieron mediante un difractómetro de rayos X PANalytical capaz de velocidades de escaneo que van desde 20 a 50 con 2 θ y se utilizaron para determinar la estructura cristalina de las nanopartículas de plata.
Los análisis topográficos y de composición de la superficie de los AgNP se realizaron utilizando análisis TEM realizado en un JEOL JEM-1230 (JEOL, Tokio, Japón) y JSM 6380 LA SEM, con una resolución de 3,0 nm. El análisis elemental de los AgNP se realizó mediante espectroscopia de rayos X de dispersión de energía (EDX) utilizando una serie JED 2200 (Jeol).
Estudios antibacterianos
Preparación de la suspensión bacteriana
Cepas bacterianas E. coli (ATCC 25922), P. aeruginosa (ATCC 27584), P. vulgaris (ATCC 8427), S. typhi (ATCC 14028), S. aureus (ATCC 29213), S. epidermidis (MTCC 3615) y K. pneumoniae se obtuvieron del King Khalid Hospital, Riyadh, Reino de Arabia Saudita. Se realizó una identificación rápida de las células bacterianas de acuerdo con métodos publicados anteriormente [15]. Todos los cultivos identificados se transfirieron a medios de agar y se almacenaron a -20 ° C hasta que se necesitaron para el estudio. En ese momento, cada cepa bacteriana se inoculó en agar nutritivo estéril y se incubó a 37 ° C durante 24 h. La suspensión (10 6 UFC / mL) se preparó transfiriendo un asa de inóculo del cultivo incubado de 24 h en 5 mL de caldo nutritivo e incubándolo a 37 ° C durante 2 h.
Ensayos antimicrobianos
Los ensayos de actividad antimicrobiana se llevaron a cabo utilizando un método de difusión de pozos de agar [16]. Se humedeció un hisopo estéril con suspensión bacteriana reciente y se extendió sobre una placa de agar Muller-Hinton estéril y sólida. Los pocillos se hicieron en la placa de agar utilizando un taladro de corcho. Se vertieron diferentes concentraciones (25, 50, 75 y 100 μL) de suspensión de nanopartículas sintetizadas en cada pocillo consecutivo. Todas las placas se incubaron a 37 ° C durante 24 h. Se midió una zona de inhibición (mm) alrededor de cada pocillo en cada placa incubada. Para cada experimento, se realizaron tres réplicas [17].
Análisis de proliferación celular
El efecto de los AgNP sobre la proliferación celular se evaluó mediante un ensayo Alamar Blue como se describió anteriormente [12].
En resumen, 0,005 × 10 6 células / pocillo se sembraron en placas de 96 pocillos con diferentes concentraciones (100–0,3 μg / mL) de AgNP y se incubaron durante 2 a 5 días a 37 ° C. El medio, DMEM, se complementó con 4500 mg / L de d-glucosa, l-glutamina 4 mM, 110 mg / L de piruvato de sodio, suero bovino fetal al 10% (FBS), 1 x penicilina-estreptomicina y aminoácidos no esenciales (todos adquiridos de Gibco-Invitrogen, EE. UU.). Los pocillos de control se trataron solo con medio y se midió la proliferación celular el día 3 y el día 5. En estos momentos, se añadió azul Alamar (1:10) a cada pocillo y las placas se incubaron a 37 ° C durante 4 h.; luego, las placas se leyeron utilizando un lector de microplacas espectrofotométrico (Biotek Synergy 2; Biotek Instruments, EE. UU.), y se registró la unidad de fluorescencia relativa (RFU).
Análisis de apoptosis / necrosis celular
Para determinar la apoptosis / necrosis, las células se trataron con AgNP a diferentes concentraciones (25 a 1,5 μg / ml). El día 5, las células se tiñeron con una solución de tinción fluorescente dual (1 μL) que contenía 100 μg / mL de AO (naranja de acridina) y 100 μg / mL de EtBr (bromuro de etidio) (AO / EtBr, Sigma, St. Louis, MO ). Las células teñidas se expusieron a una solución de colorante AO / EtBr (1:100) durante 1 min y se observaron usando un microscopio de fluorescencia Nikon Eclipse Ti. Los resultados se compararon con el control experimental. AO / EtBr, una combinación de dos tintes, ayuda a visualizar las células con una organización de cromatina aberrante. La captación diferencial de AO / EtBr permite la identificación de células viables y no viables. En particular, el AO se utilizó para visualizar el número de células que habían sufrido apoptosis.
Análisis estadístico
Se realizaron análisis estadísticos y gráficos utilizando Microsoft Excel 2010 y el software GraphPad Prism 6.0 (GraphPad, San Diego, CA, EE. UU.). P Los valores se calcularon utilizando comparaciones múltiples ANOVA de una vía. Se probó el análisis de datos antimicrobianos para diferentes concentraciones con un nivel de significancia de P <0.05.
Resultados y discusión
Los AgNP se sintetizaron con éxito utilizando el extracto acuoso de piel de granada como fuente de agente reductor. La figura 1a muestra nitrato de plata 0,1 mM disuelto en 250 ml de DDH 2 O para hacer una solución incolora. Luego, se agregaron 10 ml de extracto de cáscara acuoso y se mezcló bien, y la mezcla de reacción cambió lentamente a un color marrón oscuro durante 24 h, como se ve en la Fig. 1b. El cambio de color observado durante la síntesis de AgNP se ha informado para reacciones similares cuando se utilizan varios tipos de extractos de partes de plantas, como hojas, flores, cáscaras, semillas y frutos. El cambio de color se debió a AgNO 3 interactuando con fuentes vegetales y reduciéndose de nitrato de plata a plata elemental [18,19,20,21,22].

un 0,1 mM de nitrato de plata. b El color cambia después de P. granatum extracto de cáscara añadido
La Figura 2 muestra el espectro UV-Vis de AgNPs sintetizados usando extracto acuoso de piel de granada. Como se muestra en la Fig. 2, la banda de absorbancia tiene un pico a 378 nm en tiempos de reacción de 24, 48 y 72 h con intensidades de 0,96, 1,08 y 1,16, respectivamente. La intensidad aumentó con el tiempo, ya que la reacción tuvo más tiempo para ocurrir, lo que condujo a concentraciones más altas de AgNP. Los datos de resonancia del plasmón de superficie mostraron que el aumento de las concentraciones de AgNP condujo a un aumento de los picos de AgNP, coincidiendo con mayores cantidades de plata reducida a lo largo del tiempo. Como AgNO 3 reaccionó para formar AgNP debido a la liberación de electrones del extracto de granada, una reacción concurrente comenzó a oxidar los radicales ascorbato. Un espectro de absorción UV-Vis similar se observó en un estudio diferente que produjo AgNP a partir del extracto de cáscara de granada, con un pico de absorbancia a 371 nm [23].
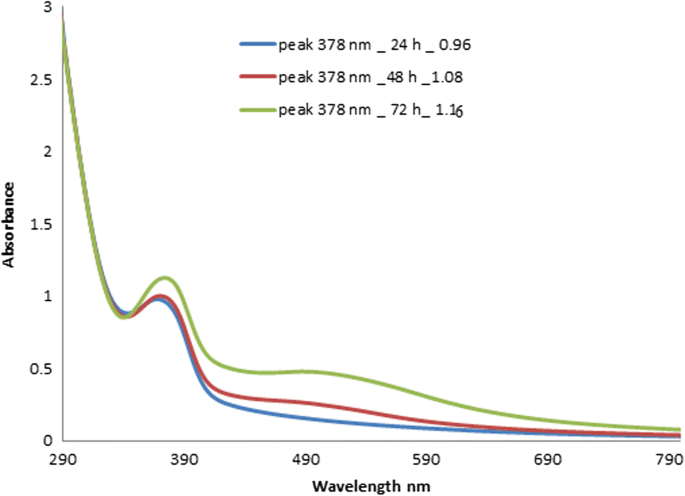
Espectros de absorbancia UV-Vis de AgNP sintetizados en 48 a 72 h en intervalos de tiempo
El patrón XRD de los AgNP sintetizados en verde se muestra en la Fig. 3. Se observan seis picos de difracción intensos a 2 θ valores que van de 0 a 90, lo que indica que podríamos asignar los planos 111, 200, 220 y 311 de un cubo enfrentado con un ion Ag central. El espectro XRD sugiere que los AgNP sintetizados se formaron en una estructura cristalina. Este resultado concuerda con los patrones XRD previamente publicados en la base de datos JCPDS (No. 04-0783). Los picos cristalinos no identificados (*) observados corresponden a óxidos de plata [24]. En la Fig. 4 se muestra una imagen TEM de NP de piel acuosa de granada 0,1 mM. Esta imagen mostró partículas de forma esférica con un diámetro que variaba de 20 a 40 nm, siendo el tamaño medio de partícula 26,95 nm. Se han realizado informes similares sobre la nanosíntesis de NP utilizando Actinidia deliciosa extracto de fruta [25]. Las observaciones SEM de los AgNP sintetizados (Fig. 5) muestran una distribución equitativa de nanopartículas de plata en la superficie de las células de la cáscara de granada. A partir de esta imagen, se determinó que las nanopartículas son de forma esférica, con diámetros que van de 20 a 40 nm, lo que es similar a un informe anterior de AgNP de forma esférica que van desde 34 a 50 nm de diámetro producidos con Raphanus sativus. L. extracto de piel [26].
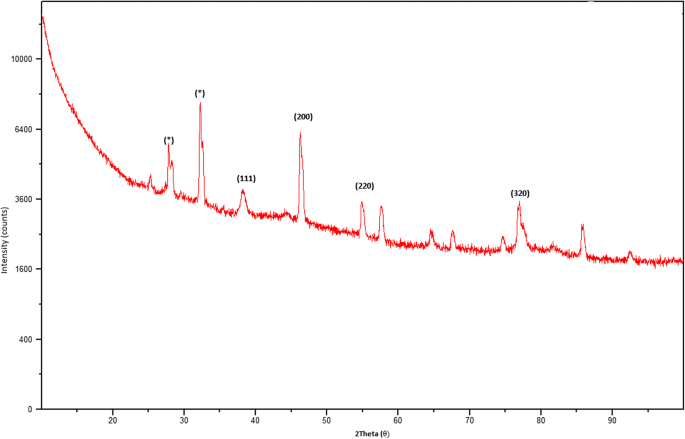
Patrón XRD de AgNP sintetizados de P. granatum extracto de cáscara

Imagen TEM de AgNP sintetizados de P. granatum extracto de cáscara

Imagen SEM de AgNP sintetizados de P. granatum extracto de cáscara
En la fitosíntesis de nanopartículas de plata utilizando el extracto de cáscara de granada presentado aquí, el tamaño de las nanopartículas obtenidas es bastante prometedor para la administración de fármacos. Se informa que el tamaño de las nanopartículas de menos de 100 nm desempeña un papel en el desarrollo de sistemas inteligentes, mejorando los valores terapéuticos y de imagen y la administración de fármacos a tejidos específicos para proporcionar una terapia de liberación controlada [27]. El tamaño y la forma de las nanopartículas influyen en la biodisponibilidad del fármaco en los tejidos diana. Se informa que las nanopartículas de 100 nm exhiben una absorción 2,5 veces mayor en comparación con las partículas de 1 µm de diámetro [28, 29]. El tamaño de las nanopartículas juega un papel clave en la función de las partículas, como la degradación, la dinámica vascular, la focalización, el aclaramiento y los mecanismos de captación [30]. Además, la naturaleza nanocristalina de los AgNP sintetizados mejora la biodistribución y la farmacocinética, como se informó [31, 32]. La utilización de residuos biológicos de granada será un enfoque novedoso para la utilización de residuos, como se informó anteriormente [33].
Los datos del estudio EDX proporcionaron un análisis cualitativo y cuantitativo de los elementos encontrados en las nanopartículas sintetizadas, como se muestra en la Fig. 6. El estudio EDX proporcionó un desglose elemental del contenido de los NP sintetizados y estimó que los NP consistían en un 70% Ag por peso. Otros elementos y enlaces identificados en los resultados fueron C-K, O, C-U, Cu y K, cada uno de los cuales correspondía a un pequeño porcentaje de la masa total. El informe EDX proporciona evidencia de que la baja concentración de AgNO 3 0,1 mM dio como resultado un gran número de AgNP sintetizados. Se informaron resultados similares para AgNO 3 0,3 mM que se vertió en agua destilada durante 3 hy se calentó a 300 ° C, y durante 1, 2 y 3 g de extracto de cáscara de granada se mezcló con 30 mL de agua destilada y se calentó a 80 ° C [34].
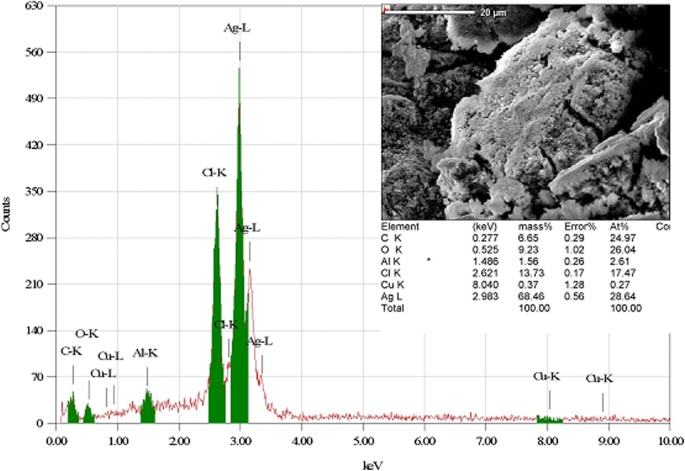
Imagen EDX de AgNP sintetizados de P. granatum extracto de piel con análisis cuantitativo
Las propiedades antibacterianas de los AgNP sintetizados en granada se investigaron utilizando muestras de 25, 50, 75 y 100 μg / ml contra bacterias Gram positivas y Gram negativas mediante la prueba de difusión de pocillos de agar. Placas de agar con bacterias Gram-negativas E. coli , S. typhi , y P. aeruginosa y las zonas de inhibición se muestran en la Fig. 7a-c. Las bajas concentraciones de AgNP sintetizados en granada (25 y 50 μL) mostraron actividad inhibidora contra P. aeruginosa y E. coli pero no contra S. typhi. Se han informado anteriormente efectos antimicrobianos similares de los productos de granada, donde se observaron las inhibiciones más fuertes para E. coli , S. aureus y P. aeruginosa [35,36,37].
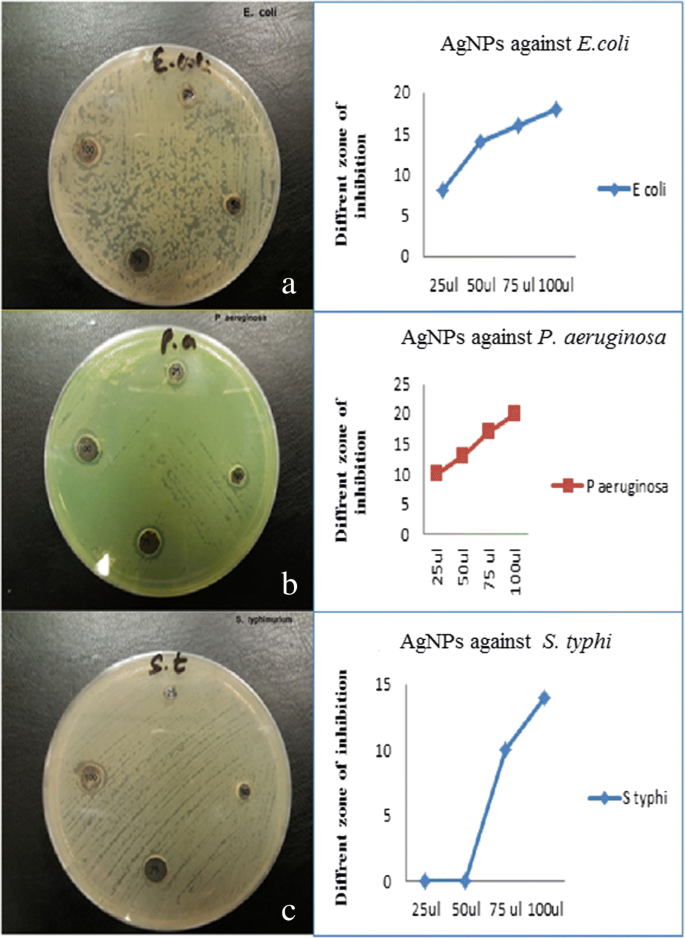
Efectos antimicrobianos y zona de inhibición de los AgNP de patógenos gramnegativos ( a - c )
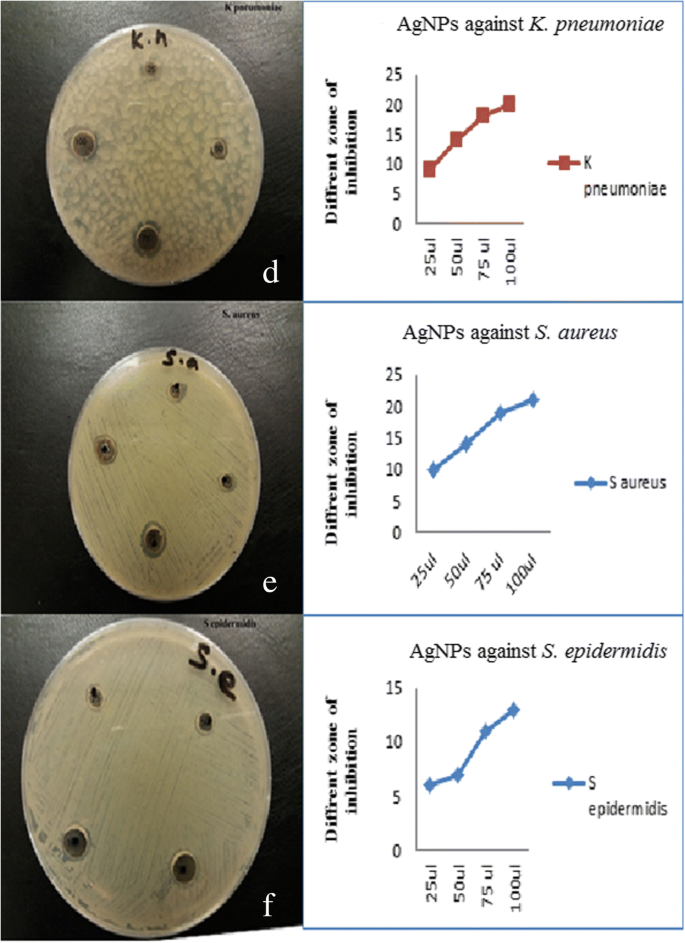
Efectos antimicrobianos y zona de inhibición de los AgNP de patógenos grampositivos ( d - f )
La Figura 8a-c muestra la actividad antimicrobiana de los AgNP sintetizados contra los patógenos Gram-positivos K. pneumoniae , S. aureus y S. epidermidis . Se observó actividad antimicrobiana incluso a concentraciones bajas de AgNP (25 y 50 μL) para K. pneumoniae, con zonas de inhibición de 9 y 14 nm, respectivamente, y contra S. aureus , con zonas de inhibición de 6 y 14 nm, respectivamente. Estudios anteriores también confirmaron la inhibición del crecimiento de bacterias Gram-positivas tratadas con NP sintetizadas [35,36,37,38]. La actividad antibacteriana evaluada después de la exposición a los AgNP sintetizados mostró zonas de inhibición en el rango de 7 a 21 mm. La Figura 9 presenta los efectos inhibidores de diferentes concentraciones (25 a 100 μL) de P. granatum pelar los AgNP en E. coli , P. aeruginosa , S. typhi , K. pneumoniae , S. aureus y S. epidermidis . Incluso a bajas concentraciones de AgNP, se observó una buena actividad antibacteriana para todos los microbios, excepto S. typhi , como se informó anteriormente [38].
Para analizar los efectos citotóxicos de los AgNP, se utilizó una línea celular de cáncer de colon (RKO:ATCC® CRL-2577 ™). El día 3, encontramos una viabilidad del 56% con un tratamiento de 12,5 μg y una viabilidad del 61% el día 5. Las reducciones significativas generales en la proliferación se observaron en> 12,5 μg (Fig. 10a), y fue consistente en día 5. Además, las imágenes teñidas con AO / EtBr confirmaron la reducción de la proliferación visualizando las colonias y el número de células (Fig. 10b). Curiosamente, pudimos observar células con vacuolas citoplásmicas perinucleares a 12,5 μg (Fig. 10b, c); este proceso podría ser una ruta de degradación en los lisosomas en el proceso de autofagia para mejorar la muerte celular programada. Sin embargo, se necesitan más estudios para confirmar el efecto de AgNP en las funciones de autofagia. En nuestro estudio anterior sobre AgNP sintetizados con Pimpinella anisum semillas, también encontramos que 12 μg de AgNPs era tóxico para las células HCT116 al mejorar la apoptosis o la necrosis [12]. También se informó que una concentración baja de AgNP puede inducir la apoptosis [39]. Los experimentos actuales con AgNP sintetizados con Punica granatum el extracto de cáscara también mostró una toxicidad del 55 al 62% con 12,5 μg. Además, la tinción AO / EtBr reveló una imagen clara de la muerte celular programada mediante autofagia.
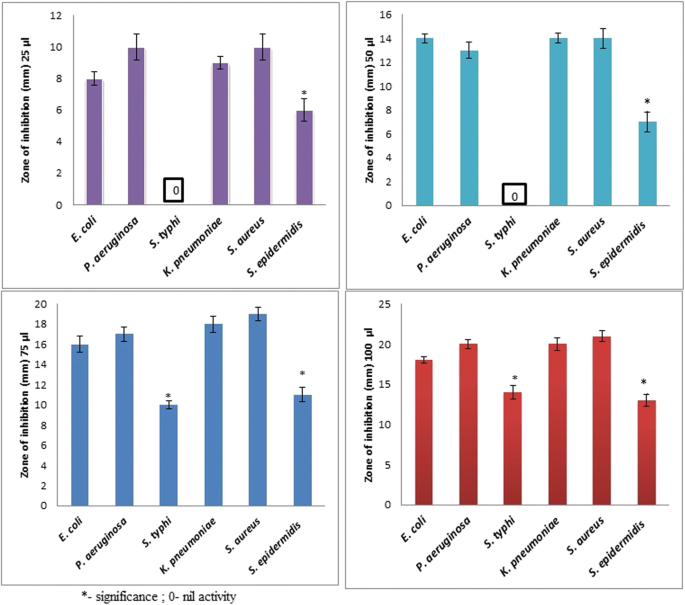
Actividad antimicrobiana de los AgNP contra patógenos gramnegativos y grampositivos
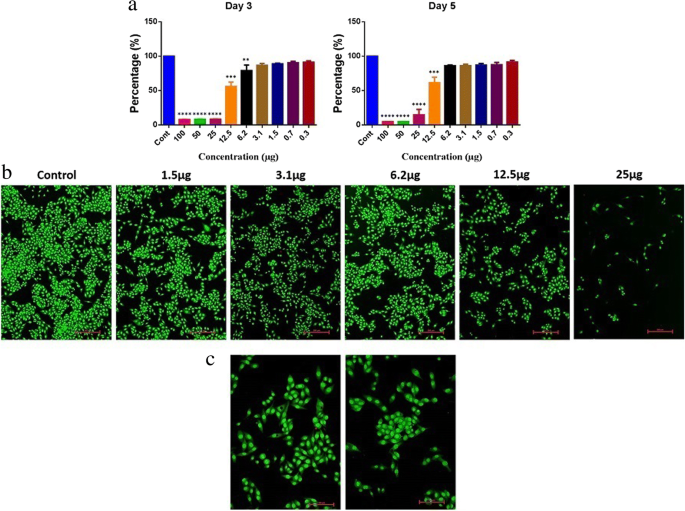
Citotoxicidad de los AgNP. un Análisis de viabilidad y proliferación celular en células RKO. Comparaciones múltiples de ANOVA unidireccional, *** P <0,0005. b Análisis de apoptosis / necrosis en células RKO. c Células RKO expuestas a diferentes dosis de AgNP
Conclusiones
El resultado del presente estudio mostró que el extracto de cáscara de granada es un buen agente reductor para sintetizar nanopartículas de plata con un rango de tamaño de 20 a 40 nm (tamaño medio, 26,95 nm), un requisito previo ideal para la administración eficaz de fármacos y para una mayor biodisponibilidad a sitio de destino. La actividad antibacteriana de los AgNP sintetizados en los organismos probados, incluso a bajas concentraciones de AgNP (25-100 μL), confirma aún más la eficacia antibiótica de los AgNP sintetizados en verde para el desarrollo de nuevos agentes antibacterianos para el tratamiento contra Gram-negativos y Gram. -patógenos positivos. Además, los efectos citotóxicos observados de los AgNP en las líneas celulares de cáncer de colon y las reducciones en la proliferación celular a un nivel de dosis> 12,5 μg promueven aún más los AgNP como tratamiento de primera línea para los tumores.
Abreviaturas
- EDX:
-
Espectroscopia de rayos X de dispersión de energía
- SEM:
-
Microscopio electrónico de barrido
- TEM:
-
Microscopía electrónica de transmisión
- XRD:
-
Difracción de rayos X
Nanomateriales
- Síntesis biogénica, caracterización y evaluación del potencial antibacteriano de nanopartículas de óxido de cobre contra Escherichia coli
- Efectos de interacción en el ensamblaje de nanopartículas magnéticas
- Fabricación, caracterización y citotoxicidad de nanopartículas de carbonato de calcio derivadas de concha de oro-berberecho conjugado de forma esférica para aplicaciones biomédicas
- Aptitud ecológica en la síntesis y estabilización de nanopartículas de cobre:actividades catalíticas, antibacterianas, citotóxicas y antioxidantes
- Profundos efectos interfaciales en CoFe2O4 / Fe3O4 y Fe3O4 / CoFe2O4 Core / Shell Nanoparticles
- Avances recientes en métodos sintéticos y aplicaciones de nanoestructuras de plata
- Saponinas Platycodon de Platycodi Radix (Platycodon grandiflorum) para la síntesis verde de nanopartículas de oro y plata
- Evaluación de las propiedades antimicrobianas, apoptóticas y de administración de genes de células cancerosas de nanopartículas de oro cubiertas con proteínas sintetizadas a partir del hongo mic…
- Sobreenfriamiento de agua controlado por nanopartículas y ultrasonido
- Propiedades microestructurales, magnéticas y ópticas de las nanopartículas de perovskita manganita La0.67Ca0.33MnO3 sintetizadas mediante el proceso Sol-Gel
- Efectos del tamaño y la agregación / aglomeración de las nanopartículas en las propiedades interfaciales / interfásicas y la resistencia a la tracción de los nanocompuestos poliméricos



