Carbón poroso jerárquico con poros ordenados interconectados de residuos biológicos para electrodos supercondensadores de alto rendimiento
Resumen
El uso de residuos biológicos como precursores para la preparación de nanomateriales de valor agregado es fundamental para el desarrollo sostenible de dispositivos. Los lignosulfonatos son subproductos de las industrias de fabricación de pulpa y papel y, por lo general, se descartan como desechos. En el presente estudio, el lignosulfonato se utiliza como precursor para preparar carbono poroso ordenado jerárquicamente con poros interconectados para la aplicación de almacenamiento de energía electroquímica. La estructura molecular y las propiedades únicas del lignosulfonato garantizan la adquisición de carbono poroso de alta calidad con una estructura de poros controlable y propiedades físicas mejoradas. Como resultado, el carbono poroso de orden jerárquico tal como se preparó muestra un excelente rendimiento de almacenamiento de energía cuando se usa para ensamblar el supercondensador simétrico, que exhibe una capacitancia específica alta de 289 F g −1 a una densidad de corriente de 0,5 A g −1 , con una densidad de energía de 40 Wh kg −1 a la densidad de potencia de 900 W kg −1 . El presente estudio proporciona una estrategia prometedora para la fabricación de dispositivos de almacenamiento de energía de alto rendimiento a bajo costo.
Introducción
Los supercondensadores son prometedores como dispositivos de almacenamiento de energía para sistemas de respaldo y diversos componentes electrónicos debido a su alta densidad de potencia, ciclo de vida prolongado y peso ligero en comparación con las baterías y los condensadores convencionales [1, 2, 3, 4, 5, 6]. Los nanomateriales a base de carbono son conocidos por su excelente rendimiento de almacenamiento de energía como materiales de electrodos activos en supercondensadores que almacenan electricidad a través de la doble capa electroquímica. Su capacidad de almacenamiento de energía está determinada por las propiedades físicas de los materiales activos de los electrodos, especialmente la estructura porosa [7,8,9]. Los macroporos (mayores de 50 nm) sirven como reservorios de amortiguación de iones, los mesoporos (2-50 nm) como canales de transporte de iones de electrolito y los microporos generalmente como sitios de almacenamiento de carga [10]. Nuestro trabajo previo basado en la investigación de correlación lineal indica que la capacitancia específica y la capacidad de velocidad están altamente relacionadas con el volumen de microporos y mesoporos [11, 12], respectivamente. Se espera que los supercondensadores basados en nanomateriales de carbono tengan una estructura porosa jerárquica con una distribución equilibrada de macroporos, mesoporos y microporos que están interconectados.
Se han realizado considerables esfuerzos para preparar carbono poroso jerárquico para un mejor rendimiento de almacenamiento de energía [13,14,15,16]. Los investigadores han desarrollado varias plantillas duras que incluyen zeolita, MCM-41, MCM-48, SBA-15, SBA-16 y KIT-6 para preparar carbono poroso con mesoporos ordenados [17, 18]. Los tratamientos de activación química y física también se emplean ampliamente, que generalmente dan como resultado poros cerrados distribuidos aleatoriamente [13] y, por lo tanto, muestran poca capacidad de control sobre la estructura de los poros.
La biomasa y los residuos biológicos se han activado química y físicamente a temperaturas elevadas para la preparación de carbón poroso [19]. Pocos de ellos se han utilizado en los métodos de plantilla para la síntesis de carbono poroso con estructura de poros ordenada [11, 12, 20]. Muchos carbonos porosos se preparan a partir de tensioactivos y copolímeros de bloque costosos y no renovables. La lignina es el segundo material orgánico más abundante y el polímero aromático más abundante que existe en las especies vegetales [21]. En la industria de fabricación de papel, la lignina se convierte en lignosulfonatos durante el proceso de fabricación de pasta y, por lo general, se desecha como residuo, lo que genera graves problemas medioambientales [22]. Los lignosulfonatos son típicamente moléculas pequeñas con un anillo aromático y grupos que contienen oxígeno. Por lo general, tienen un peso molecular mucho menor que la lignina y exhiben una excelente solubilidad en agua debido a los grupos que contienen oxígeno [23]. Estos méritos hacen que los lignosulfonatos sean los precursores ideales que se pueden emplear en el método de la plantilla para la síntesis de carbono poroso de valor agregado con estructura de poros ordenada.
En el presente estudio, utilizamos KIT-6 como plantilla dura por su buena interconectividad de poros ordenados y capacidad de control sobre el tamaño de los poros para preparar carbono mesoporoso ordenado combinado con la activación química posterior para crear microporos en la estructura mesoporosa. Se ha empleado lignosulfonato de sodio como precursor. El carbono poroso ordenado jerárquicamente preparado (HOPC) se utilizó para ensamblar el supercondensador simétrico que muestra un excelente rendimiento de almacenamiento de energía.
Métodos
Preparación del KIT-6
La plantilla de sílice mesoporosa ordenada (KIT-6) se sintetizó de acuerdo con la referencia [24]. En un procedimiento modificado, 5,53 g de Pluronic P123 (EO 20 PO 70 EO 20 , PM =5800, Aldrich) se disolvió en primer lugar en 200 g de agua desionizada que contenía 10,9 g de HCl concentrado (35%) en una botella de vidrio de 250 ml. Luego se agregaron 5,53 g de butanol a la botella con agitación a 35 o C. Después de agitar durante 1 h, se añadieron 11,9 g de TEOS (tetraetil ortosilicato, Aldrich) a la solución anterior, y luego la mezcla se agitó durante 24 ha 35 o C. Posteriormente, la botella se envejeció durante otras 24 ha 100 o C en condiciones estáticas. El producto sólido se recogió mediante filtración y se secó a 100 o C sin lavar. El residuo orgánico se eliminó mediante extracción en la mezcla de etanol y HCl, seguido de calcinación a 550 o C durante 6 h.
Preparación de carbono mesoporoso ordenado
El carbono mesoporoso ordenado (OMC) se preparó utilizando el KIT-6 tal como se sintetizó como plantilla dura y lignosulfonato de sodio como fuente de carbono. Se utilizó la plantilla de sílice KIT-6 sintetizada anteriormente para cargar lignosulfonato. Normalmente, se disolvieron 0,6 g de lignosulfonato de sodio adquirido en Lanyi Reagent (Beijing, China) en 15 ml de agua desionizada, seguido de la adición de 0,6 g de molde KIT-6. La mezcla se mantuvo en agitación durante 24 ha temperatura ambiente, seguido de secado a 70 o El compuesto seco que contiene sílice y lignosulfonato de sodio se utilizó como precursor de la carbonización. El proceso de carbonización se realizó a las 900 o C durante 2 h en Ar con un caudal de gas de 30 sccm. Después de la carbonización, se eliminó la plantilla de sílice sumergiendo el material compuesto en una solución acuosa de NaOH 2,5 M durante 12 ha temperatura ambiente. Después de un tratamiento de lavado usando una solución diluida de HCl y agua desionizada, se obtuvo carbono ordenado mesoporoso (abreviado como OMC) y se registró como OMC-900 (el número digital se refiere a la temperatura de carbonización). OMC-700, OMC-800 y OMC-1000 se refieren a las muestras obtenidas carbonizadas a 700 o C, 800 o C y 1000 o C, respectivamente.
Preparación de carbono poroso ordenado jerárquicamente
Para preparar el carbono poroso ordenado jerárquicamente (abreviado como HOPC), se empleó un proceso de activación química posterior. Brevemente, el OMC-900 tal como se preparó se mezcló homogéneamente con ZnCl 2 solución con una relación en peso de carbono a ZnCl 2 de 1:1 y secado a 110 o C durante 6 h. El tratamiento de activación se llevó a cabo calentando los composites a 900 o C durante 3 h en Ar con un caudal de gas de 30 sccm. Para investigar el efecto de la temperatura de carbonización, las plantillas de KIT-6 impregnadas con lignosulfonato de sodio también se carbonizaron a 700 o C y 800 o C, marcado como OMC-700 y OMC-800. A modo de comparación, el lignosulfonato de sodio puro sin ningún tratamiento se carbonizó directamente en las mismas condiciones y el carbono obtenido se registró como lignina-carbono.
Caracterización
La morfología de la plantilla KIT-6 sintetizada y las muestras de carbono poroso se caracterizaron utilizando un microscopio electrónico de barrido (SEM) Hitachi SU8020. La estructura porosa fina se examinó adicionalmente en un microscopio electrónico de transmisión (TEM) JEOL 2100F. El patrón de difracción XRD de ángulo bajo se registró en un difractor de rayos X de polvo avanzado XD-2 / XD-3. La estructura química se investigó utilizando una espectroscopia de fotoelectrones de rayos X (XPS) ESCALAB250Xi. La caracterización Raman se realizó utilizando una espectroscopía HORIBA Science Raman. Los espectros de infrarrojos transformados de Fourier (FTIR) se registraron usando una espectroscopía NEXUS 670 FTIR. Las características porosas de la plantilla KIT-6 y el carbono poroso fueron analizadas por N 2 experimentos de adsorción / desorción a 77 K usando un Micromeritic ASAP2020 V3.02 H. El área de superficie específica se midió de acuerdo con el método Brunauer-Emmett-Teller (BET), y la distribución del tamaño de los poros se calculó usando una densidad no local de poros de hendidura modelo de teoría funcional (NLDFT).
Medición electroquímica
Se examinó el comportamiento electroquímico de las muestras de carbono poroso preparadas utilizando una configuración de tres electrodos. El HOPC optimizado finalmente se investigó utilizando una configuración de dos electrodos. El electrodo de trabajo en el sistema de tres electrodos se fabricó mezclando físicamente el carbono poroso preparado y el PVDF que se disolvió en disolvente NMP de antemano con una relación en peso de carbono a PVDF de 9:1. La suspensión homogénea se vertió sobre una lámina de níquel con un área de cobertura de aproximadamente 1 cm 2 , seguido de secado a 80 o C durante 12 h para eliminar el disolvente residual. En la prueba de tres electrodos, una placa de platino (1 cm 2 ) y Ag / AgCl se utilizaron como contraelectrodo y electrodo de referencia, respectivamente. El electrodo de trabajo en el sistema de dos electrodos se preparó mediante el mismo procedimiento mientras se reemplazaba la lámina de níquel con espuma de níquel. Se usaron espumas de níquel con la misma cantidad de carga de materiales de electrodo activo para ensamblar el supercondensador simétrico en el que se usó el papel de filtro como separador. Tanto en las configuraciones de tres electrodos como de dos electrodos, se emplearon soluciones acuosas de KOH 6 M como electrolito.
La voltamperometría cíclica (CV), la espectroscopia de impedancia electroquímica (EIS) y la carga / descarga galvanostática constante se realizaron en un instrumento Gamry de referencia 3000. La medición de CV en la configuración de tres electrodos se realizó en una ventana de potencial de - 1 a 0 V frente a Ag / AgCl, mientras que la ventana de potencial en el supercondensador simétrico fue de 0 a 1 V. La caracterización EIS se llevó a cabo en la amplitud de CA de 5 mV en el rango de frecuencia de 1 MHz a 0.01 Hz. La capacitancia específica de las curvas CV recopiladas de la prueba de tres electrodos se calculó mediante la ecuación C =ʃ Yo dt / mV . La capacitancia específica derivada de la curva CV en la prueba de dos electrodos y la prueba galvanostática se determinó mediante C =4ʃ yo dt / MV y C =v4 I t / MV , respectivamente, donde I es la corriente de descarga, t es el tiempo de descarga, V es la ventana de voltaje de trabajo, m es la masa del material activo en el electrodo de trabajo en la configuración de tres electrodos, y M es la masa total del material activo en los dos electrodos del supercondensador simétrico. La densidad de energía ( E ) y la densidad de potencia ( P ) se calcularon a partir de pruebas de carga / descarga galvanostática a través de E = CV 2 / 2 y P = E / t , respectivamente, donde C es la capacitancia específica de la prueba de dos electrodos y t es el tiempo de descarga.
Resultados y discusión
La muestra de HOPC se sintetizó mediante cinco pasos, como se ilustra en la Fig. 1. (a) La plantilla de sílice KIT-6 se preparó mediante un método modificado en la literatura [24]; (b) se impregnó lignosulfonato de sodio en la plantilla KIT-6 sumergiendo la plantilla de sílice KIT-6 en la solución acuosa de lignosulfonato de sodio; (c) el KIT-6 cargado con lignosulfonato de sodio se carbonizó durante 2 h en gas Ar. Para optimizar el proceso de carbonización, realizamos la carbonización a 700 o C, 800 o C, 900 o C y 1000 o C. (d) después de la carbonización, la plantilla de sílice KIT-6 se eliminó en una solución caliente de NaOH 2,5 M para obtener el carbono mesoporoso ordenado (OMC); (e) la muestra de carbón de OMC se activó químicamente con ZnCl 2 al 900 o C durante 3 h para preparar HOPC.
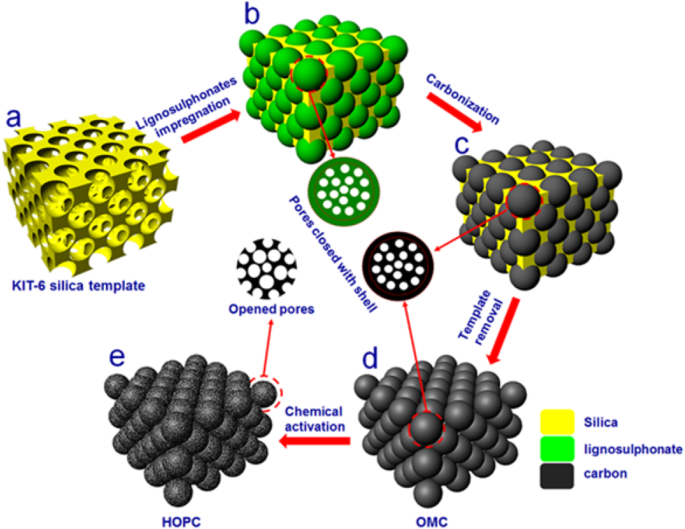
Ilustración de los procesos sintéticos de carbono poroso ordenado jerárquicamente (HOPC) utilizando el método de plantilla dura combinado con la activación química posterior
La plantilla de sílice KIT-6 preparada se analizó en primer lugar usando un patrón de difracción de rayos X de polvo de ángulo bajo (XRD) como se muestra en la Fig. 2a. La sílice KIT-6 sintetizada pertenece a la Ia3d cúbica con dos picos de difracción característicos a 1 o y 1.2 o de los planos (211) y (220) de la estructura mesoporosa ordenada cúbicamente [24]. Los resultados del N 2 El análisis de adsorción / desorción muestra que la plantilla de sílice KIT-6 está compuesta mayoritariamente por mesoporos y pocos microporos, con buena interconectividad (Fig. 2b). La distribución del tamaño de los poros se centra en 2,5 nm y 7,5 nm (Fig. 2c). La superficie BET (Brunauer-Emmett-Teller) es de 1481 m 2 g −1 y el volumen total de poros es de 2,62 cm 3 g −1 . Además, investigamos la micromorfología y la estructura de los poros de la plantilla KIT-6 sintetizada mediante microscopía electrónica de transmisión (TEM), como se muestra en la Fig. 2d. Los puntos brillantes representan los poros y el área oscura de las paredes (sílice). El grosor de la pared y el tamaño medio de los poros se miden en 3,1 nm y 6,4 nm, respectivamente. La imagen de inserción del patrón FFT en la Fig. 2d confirma la estructura de poros ordenada periódicamente.
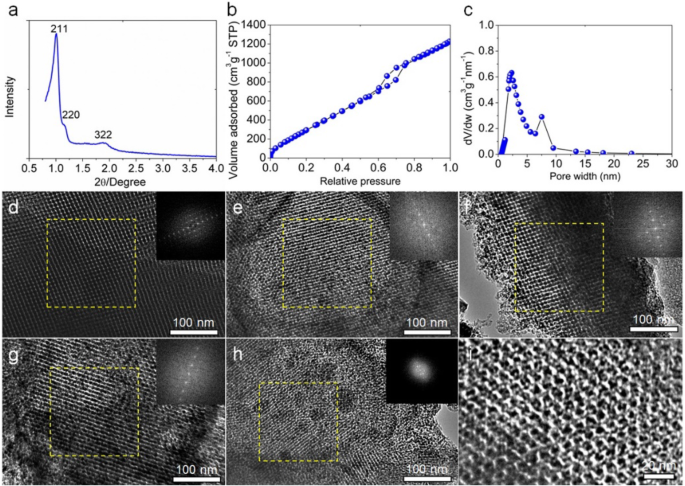
Caracterización de la plantilla de sílice KIT-6 preparada, a Patrón XRD de ángulo bajo de la plantilla de sílice KIT-6. b N 2 isoterma de adsorción / desorción de la plantilla KIT-6. c La distribución de tamaño de poro correspondiente para N 2 calculado utilizando un modelo NLDFT de poro con rendija. Imágenes TEM de ( d ) Sílice KIT-6, las muestras de carbono OMC preparadas en ( e ) 700 o C, ( f ) 800 o C y ( g ) 900 o C, y la muestra de HOPC ( h - yo ). Las imágenes insertadas son los correspondientes patrones de Transformada Rápida de Fourier de las áreas seleccionadas
Las muestras de carbono de OMC se caracterizaron por SEM y TEM. En la Figura S1, las muestras de carbono OMC preparadas a diferentes temperaturas de carbonización muestran la morfología en forma de panal con poros ordenados. Además, utilizamos TEM para investigar la estructura microporosa como se muestra en la Fig. 2e-g. Las imágenes TEM muestran nanodominios ordenados. Las partes oscuras son el carbón aislado y las partes brillantes poros interconectados. Las imágenes FFT muestran puntos nítidos y brillantes para todas las muestras de carbono OMC, lo que confirma aún más la estructura ordenada de los poros. El tamaño de los poros es de 2,9 nm, 2,1 nm y 2,4 nm para OMC-700, OMC-800 y OMC-900, respectivamente, que está muy cerca del grosor de la pared de la plantilla de sílice. Por el contrario, la muestra preparada a partir de la carbonización de lignosulfonato de sodio sin el uso de la plantilla de sílice no muestra estructura porosa (Figura S2). Se concluye que el carbono mesoporoso ordenado se prepara con éxito mediante el uso de lignosulfonato de sodio y la plantilla de sílice KIT-6 a las temperaturas de carbonización seleccionadas.
Se llevaron a cabo experimentos de adsorción / desorción de nitrógeno para investigar las propiedades físicas y químicas de las muestras de carbono de OMC sintetizadas, como se muestra en la Figura S3. Todas las curvas de isoterma tienen un intermedio similar y el volumen adsorbido aumenta a una presión relativa muy baja y aumenta rápidamente con la presión relativa, lo que sugiere la coexistencia de microporos y mesoporos con el volumen de poros alto para todas las muestras de OMC preparadas. La distribución del tamaño de los poros para las muestras de OMC se centra en 0,6 nm y 2,3 nm. Aumentamos aún más la temperatura de carbonización a 1000 o C y la curva de isoterma de la muestra de OMC-1000 que se muestra en la Figura S4 muestra un perfil similar, lo que indica una estructura de poros similar. La Figura 3a muestra el área de superficie específica, el volumen total de poros, el volumen de microporos y el volumen de mesoporos como función de la temperatura de carbonización. El aumento de la superficie específica está relacionado con el aumento del volumen total de poros. Aumentando aún más la temperatura de carbonización a 1000 o C, la superficie específica disminuye a 1948 m 2 g −1 , con disminución del volumen de microporos y aumento del volumen de mesoporos. Se sugiere que la temperatura óptima de carbonización sea 900 o C. La Tabla S1 resume las propiedades físicas de las muestras de carbono OMC preparadas. Se encuentra que la muestra OMC-900 muestra el área de superficie específica más alta de 2201 m 2 g −1 y un volumen total de poros de 3,74 cm 3 g −1 .
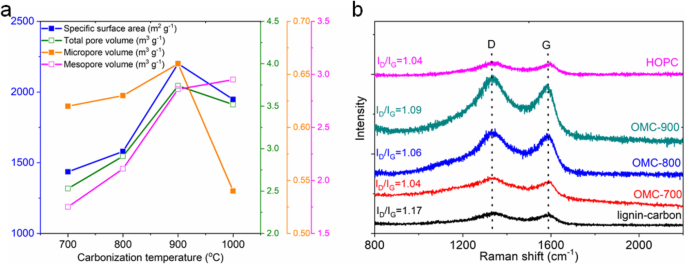
Caracterización del carbono OMC preparado y de las muestras de HOPC. un El área de superficie específica, el volumen total de poros, el volumen de microporos y el volumen de mesoporos como función de la temperatura de carbonización. b Espectros Raman
Por lo tanto, realizamos la activación química utilizando ZnCl 2 como reactivo de activación utilizando la muestra OMC-900 para crear aún más una estructura porosa jerárquica. Como se ve en la imagen SEM en la Figura S5, la red de poros tridimensional ordenada se destruyó parcialmente después de la activación química para formar numerosas nanopartículas aisladas. La imagen TEM en la Fig. 2e muestra claramente poros ordenados y el patrón FFT correspondiente muestra puntos brillantes, lo que indica la existencia de nanodominios ordenados. La imagen HRTEM en la Fig. 2f muestra que se forman microporos en las paredes de los mesoporos después de la activación química. Los resultados de N 2 adsorción / desorción indican que después de la activación química, la muestra de HOPC muestra un área de superficie específica significativamente aumentada de 2602 m 2 g −1 , con un volumen de microporos de 1,03 cm 3 g −1 y volumen de mesoporos de 3,49 cm 3 g −1 (Tabla S1 y Figura S6a yb).
Las propiedades de los lignosulfonatos facilitan la formación de carbono mesoporoso ordenado. La Figura S7 muestra la estructura molecular representativa del lignosulfonato, y los grupos hidroxilo permiten que las moléculas de lignosulfonato tengan lugar una reacción de reticulación [25]. En el presente estudio, se propone que las moléculas de lignosulfonato se adsorban en las paredes de sílice hidrófila a través de los grupos hidroxilo y se reticulan entre sí mediante enlaces de hidrógeno para formar redes tridimensionales. Los espectros FTIR de la plantilla KIT-6, el lignosulfonato de sodio y los lignosulfonatos impregnados con la plantilla KIT-6 se muestran en la Figura S8. Los picos de lignosulfonato de sodio ubicados a 3429 cm −1 , 2950 cm −1 , 1635 cm −1 , 1514 cm −1 , 1041 cm −1 puede asignarse a estiramiento O – H, estiramiento C – H, estiramiento C =O, estiramiento C – C y estiramiento C – O [26], respectivamente. Los picos de la plantilla de sílice KIT-6 ubicados a 463 cm −1 , 802 cm −1 y 1090 cm −1 se asignan al balanceo de Si – O – Si. El pico ubicado a 967 cm −1 se debe a la vibración del Si – O de los silanoles superficiales [27]. En el espectro de lignosulfonato-sílice coexisten los picos característicos de lignosulfonato y sílice, lo que confirma la impregnación del lignosulfonato en la plantilla de sílice. Además, el pico ubicado a 3429 cm −1 en lignosulfonato-sílice se ensancha, lo que indica la formación de enlaces de hidrógeno entre moléculas de lignosulfonato a través de una reacción de reticulación. Las moléculas de lignosulfonato adsorbidas y orientadas se convierten en capas sólidas de carbono durante el proceso de carbonización, lo que puede inducir numerosos poros cerrados, como se ilustra en los pasos byc de la Fig. 1. La activación química ayuda a abrir estos poros cerrados para mejorar aún más las propiedades físicas. .
Se utilizó la caracterización Raman para investigar el grado de grafito de las muestras de carbono preparadas y los resultados se muestran en la Fig. 3b. Todos los espectros Raman muestran la banda D y la banda G características ubicadas a 1340 cm −1 y 1590 cm −1 , respectivamente. La relación de intensidad de la banda D (el carbono desordenado) y la banda G (carbono ordenado) para las muestras de OMC y la muestra de HOPC es alrededor de 1.06, menor que 1.17 de la muestra de carbón preparada por la carbonización de lignosulfonato sin el uso de sílice. plantilla. Este resultado indica que las muestras de carbono de OMC tienen un mayor grado de grafito que la muestra de carbono de la carbonización directa de lignosulfonato. La razón probablemente se atribuye a la reacción de reticulación antes mencionada entre las moléculas de lignosulfonato que ayuda a la orientación de los anillos aromáticos. El resultado del análisis XPS en la Figura S9 muestra que todas las muestras contienen principalmente carbono y oxígeno. No hay señal detectable de impureza en los productos finales de carbono. La descomposición del lignosulfonato de sodio puede dar lugar a la formación de CO 2 y Na 2 CO 3 [28], que puede eliminarse completamente durante el tratamiento de lavado posterior con agua desionizada. El nivel de núcleo C1s se puede descomponer en cuatro componentes para todas las muestras de carbono preparadas. Es decir, C – O (286,7 eV), C =O (288,0 eV) [29], el sp 2 carbono (284,8 eV, carbono ordenado) y el sp 3 carbono (285,4 eV, carbono desordenado) [30].
El rendimiento electroquímico de las muestras de carbón OMC preparadas y la muestra de HOPC activada se evaluó mediante una configuración de tres electrodos en un electrolito acuoso de KOH 6 M. La muestra de carbono de la carbonización directa de lignosulfonato muestra un rendimiento de almacenamiento de energía insignificante (Figura S10). Las muestras de carbono OMC muestran perfiles CV rectangulares que indican el rendimiento electroquímico mejorado (Figura S11 y Figura 4a). A 2 mV s −1 , la capacitancia específica es 59 F g −1 , 93 F g −1 , 130 F g −1 y 120 F g −1 para OMC-700, OMC-800, OMC-900 y OMC-1000 (Fig. 4b). El electrodo OMC-900 muestra el mejor rendimiento electroquímico entre todas las muestras de carbono OMC. Después de la activación química, la capacitancia específica aumenta aún más a 243 F g −1 para la muestra de HOPC, casi dos veces más alto que el de la muestra OMC-900 antes de la activación. La capacitancia específica de HOPC en este estudio es mucho mayor que la del carbono derivado de hongos (196 F g −1 a 5 mV s −1 ) [31], y también más alto que el del carbono mesoporoso basado en aerogel de grafeno preparado a partir de una plantilla de sílice dura (226 F g −1 a 1 mV s −1 ), que disminuye a 83 F g −1 a 100 mV s −1 [32]. Para el carbono derivado de hongos, la capacitancia específica disminuye a 90 F g −1 a 100 mV s −1 . Sin embargo, la capacitancia específica de HOPC sigue siendo tan alta como 128 F g −1 a la misma velocidad de escaneo.
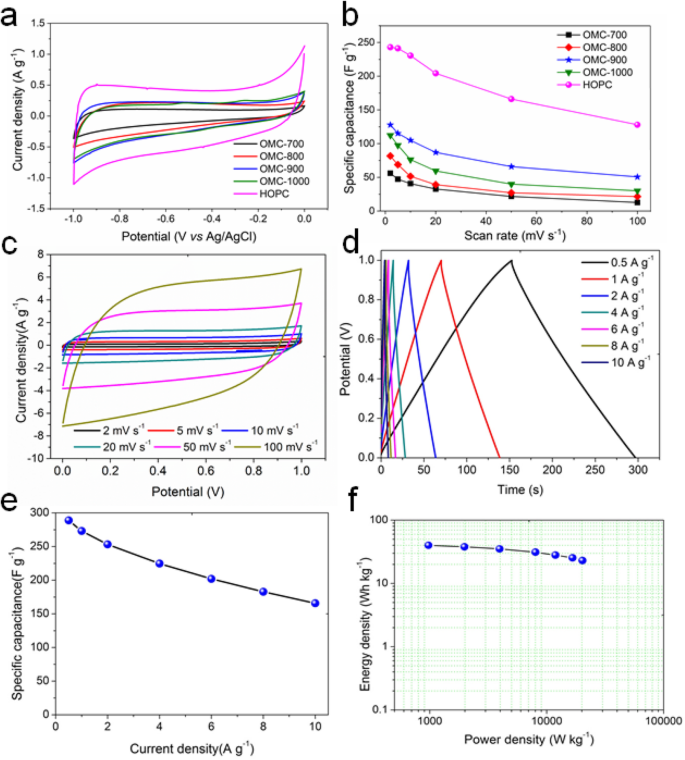
un Perfiles de voltamperometría cíclica (CV) de los electrodos OMC-700, OMC-800, OMC-900, OMC-1000 y HOPC a una velocidad de exploración de 2 mV s −1 usando la configuración de tres electrodos y b capacitancia específica correspondiente. c Perfiles CV del electrodo HOPC en el supercondensador simétrico de dos electrodos a velocidades de barrido que varían de 2 mV s −1 a 100 mV s −1 en electrolito acuoso de KOH 6 M. d Curvas de carga-descarga a diferentes densidades de corriente de 0,5 A g −1 hasta 10 A g −1 . e Capacitancia específica calculada a partir de las curvas de descarga de la prueba de carga-descarga. f Gráficos de Ragone que muestran la densidad de energía en función de la densidad de potencia
Se realizaron mediciones de impedancia para investigar la conductividad de las muestras. La Figura S12 revela los espectros de impedancia de Nyquist en el rango de frecuencia de 1 MHz – 0.01 Hz, y el circuito equivalente correspondiente que consiste en la resistencia en serie equivalente ( R s ), resistencia de transferencia de carga ( R ct ) y la capacitancia electroquímica de doble capa. La resistencia en serie equivalente R s es 0,7 Ω cm −2 para todos los electrodos, lo que indica la alta conductividad eléctrica de las muestras y la alta calidad de los electrodos. Los gráficos de Nyquist indican que el electrodo HOPC muestra la resistencia de transferencia de carga más baja de 5 Ω.
La energía entregable y la densidad de potencia están muy relacionadas con la capacitancia dependiente de la frecuencia [33, 34], que se puede expresar de la siguiente manera
$$ C =\ frac {1} {jwZ} =\ frac {- {Z} _ {\ mathrm {imagen}}} {W {\ left | Z \ right |} ^ 2} -j \ frac {- { Z} _ {\ mathrm {real}}} {W {\ left | Z \ right |} ^ 2} ={C} _ {\ mathrm {real}} - j {C} _ {\ mathrm {imagen}} $$donde C y Z son la capacitancia y la resistencia, respectivamente. Z real y Z imagen referirse a las partes reales e imaginarias de Z . C real es la parte real de la capacitancia que representa la capacitancia entregable de los materiales del electrodo, y C imagen es la capacitancia imaginaria relacionada con la pérdida de resistividad irreversible en el dispositivo. La Figura S13a muestra que la muestra de HOPC tuvo la respuesta más rápida. La frecuencia ƒ es la frecuencia de caracteres a la que C imagen alcanza el máximo, y t =1 / ƒ es la constante de tiempo del supercondensador. Ambos f y t son la capacidad de tasa característica. Los supercondensadores de alta densidad de potencia suelen tener una alta frecuencia de caracteres ƒ y pequeña t . La Figura S13b muestra las gráficas de C imagen en función de la frecuencia. La frecuencia de caracteres de la muestra OMC-700, OMC-800, OMC-900, OMC-1000 y HOPC es 0.01 Hz, 0.1 Hz, 0.01 Hz, 0.01 Hz y 0.5 Hz, y la constante de tiempo correspondiente es 100 s, 10 s, 100 s, 100 sy 2 s. La muestra HOPC muestra la frecuencia de carácter más alta y la constante de tiempo más baja, lo que indica la respuesta más rápida a la salida de potencia.
Se ha demostrado que HOPC presenta un alto rendimiento electroquímico. Sin embargo, para aplicaciones prácticas, las pruebas de configuración de tres electrodos no pueden revelar la capacidad real de almacenamiento de energía [33, 35]. Por lo tanto, usamos una muestra de HOPC para preparar electrodos para ensamblar supercondensadores simétricos. La Figura 4c ilustra las curvas CV del electrodo HOPC. Los perfiles CV presentan una forma casi rectangular con buena simetría en todas las velocidades de escaneo desde 2 mV s −1 a 100 mV s −1 , lo que indica las buenas propiedades electroquímicas y la estabilidad de velocidad del electrodo HOPC. Las mediciones de carga-descarga galvanostática a densidades de corriente constantes también se realizaron en el supercondensador simétrico ensamblado y los resultados se muestran en la Fig. 4d. Los perfiles de voltaje lineal frente al tiempo durante el proceso de carga y descarga muestran una forma de triángulo ideal con buena simetría, lo que representa la excelente capacidad de almacenamiento de energía del electrodo HOPC. Cuando la densidad de corriente era de 0,5 A g −1 , el tiempo de descarga es tan largo como 150 s, que corresponde a la capacitancia específica de aproximadamente 289 F g −1 . La capacitancia específica de HOPC de lignosulfonato a 10 A g −1 sigue siendo tan alto como 166 F g −1 , como se muestra en la Fig. 4e. El rendimiento del HOPC en este estudio es mejor que los valores de las muestras de carbono en la literatura [3, 36,37,38,39].
La alta capacitancia específica de HOPC contribuye a la baja resistencia óhmica y la resistencia de transferencia de carga, que es de aproximadamente 0,6 Ω cm −1 y 2,4 Ω cm −1 , respectivamente, como se muestra en la Figura S14. El ángulo de fase del supercondensador simétrico a la frecuencia más baja de 0,01 Hz es de aproximadamente 81,7 o (Figura S15), que está muy cerca del valor del supercondensador ideal (90 o ). La frecuencia del carácter es de aproximadamente 0,2 Hz, correspondiente a la constante de tiempo de 5 s. Esto significa que el electrodo HOPC tiene una buena capacidad de suministro de energía. La capacitancia entregable es tan alta como 290 mF (Figura S16). La Figura 4f ilustra la gráfica de Ragone del supercondensador simétrico. La densidad de energía está en el rango de 40 Wh kg −1 hasta 23 Wh kg −1 con una densidad de potencia de aproximadamente 0,9 kW kg −1 hasta 20 kW kg −1 .
La alta capacitancia específica y la densidad de energía de HOPC pueden contribuir a la estructura de poros optimizada. La muestra de HOPC contiene un alto volumen de poros tanto de microporos como de mesoporos. Como se demostró en la literatura anterior mediante análisis de correlación [40, 41], los microporos están muy relacionados con el almacenamiento de energía y los mesoporos están muy relacionados con la retención de capacitancia, ya que los mesoporos son los principales responsables del transporte de iones. También se concluye que los mesoporos tienen contribuciones al almacenamiento de carga. Tenga en cuenta las instrucciones anteriores, empleamos con dedicación el método de plantilla dura y la activación química para preparar la muestra de HOPC. Los presentes resultados no solo demuestran las conclusiones anteriores, sino que también muestran el diseño para la preparación de materiales de almacenamiento de energía de alto rendimiento. Para medir la capacidad de ciclo, el supercondensador simétrico de usar HOPC como material de electrodo se carga y descarga repetidamente a 2 A g −1 durante 3000 ciclos (Figura S17). Se encuentra que después de 3000 ciclos, la capacitancia específica es 218 F g −1 con una ligera disminución de 253 F g −1 iniciales con retención de capacitancia del 86,2%. La capacitancia específica de nuestra muestra de HOPC del sistema de dos electrodos es superior y comparable después de 3000 ciclos con los valores informados en la Tabla S2. Por lo tanto, el presente estudio proporciona una ruta potencial para el desarrollo de materiales activos de electrodo de supercondensador de alto rendimiento a partir de desechos industriales.
Conclusión
En este estudio, hemos preparado con éxito materiales de carbono mesoporosos ordenados utilizando lignosulfonato de residuos biológicos como fuente de carbono utilizando la técnica de fundición en molde basada en la plantilla KIT-6. During the mold casting process, lignosulphonate can easily be cast into the pores of KIT-6. The crosslinking reaction of lignosulphonate molecules not only increases the pore volume, but also bridges the aromatic rings to promote the graphitization. The as-synthesized ordered mesoporous carbons exhibit high electrical conductivity, high-specific surface area, and pore volume, which are highly dependent on the carbonization temperature. The results of Raman analysis and N2 adsorption/desorption experiments show that the OMC-900 sample has the best physical properties. The pore structure of OMC-900 was further optimized through ZnCl2 chemical activation to prepare HOPC. The specific capacitance of HOPC in the symmetric supercapacitor was about 289 F g −1 with the energy density as high as 40 Wh kg −1 . The present study indicates lignosulphonate is very suitable to prepare hierarchical ordered porous carbon at low cost with high-performance supercapacitors.
Disponibilidad de datos y materiales
All data generated or analyzed in this study are included in the manuscript and the supplementary information files. All the materials are available from the corresponding author on request.
Abreviaturas
- HOPC:
-
Hierarchical ordered porous carbon
- KIT-6:
-
The ordered mesoporous silica template
- OMC:
-
The ordered mesoporous carbon
- NMP:
-
N-methyl pyrrolidone
- PVDF:
-
Fluoruro de polivinilideno
- CV:
-
Voltamperometría cíclica
- EIS:
-
Espectroscopia de impedancia electroquímica
- AC:
-
Corriente alterna
Nanomateriales
- Compuestos de grafeno y polímeros para aplicaciones de supercapacitores:una revisión
- Fibras de carbón activado con nanoestructura jerárquica derivada de guantes de algodón usados como electrodos de alto rendimiento para supercondensadores
- Síntesis fácil de nanocables de plata con diferentes relaciones de aspecto y utilizados como electrodos transparentes flexibles de alto rendimiento
- Nanoesferas de carbono monodispersas con estructura porosa jerárquica como material de electrodo para supercondensador
- Microesferas de carbono magnéticas como adsorbente reutilizable para la eliminación de sulfonamidas del agua
- Un enfoque simple para sintetizar puntos cuánticos de carbono fluorescente de aguas residuales de tofu
- Evaluación de estructuras de grafeno / WO3 y grafeno / ceO x como electrodos para aplicaciones de supercondensadores
- Compuesto de aerogel / azufre de carbón activado recubierto de polianilina para batería de litio-azufre de alto rendimiento
- Síntesis y rendimiento del supercondensador de compuestos de carbono mesoporoso ordenados con polianilina / dopado con nitrógeno
- Microarreglos mesoporosos de VO2 bidimensionales para supercondensadores de alto rendimiento
- Nanoesferas de caolinita de estructura jerárquica con propiedades de adsorción notablemente mejoradas para el azul de metileno



