Influencia de la modificación de grupo en los bordes de los puntos cuánticos de carbono en las emisiones fluorescentes
Resumen
Presentamos una investigación detallada sobre el efecto de la modulación del grupo funcional en los bordes de los puntos cuánticos de carbono (CQD) sobre la fluorescencia de los CQD. Los CQD unidos por los elementos N, S y P se sintetizan mediante pirólisis de una mezcla de ácido cítrico y NH 3 H 2 O, H 2 SO 4 y H 3 PO 4 , respectivamente. Por lo tanto, parte de –COOH en los bordes de los CQD se puede convertir en –C =O y grupos funcionales como –NH 2 , –SO 2 , –HSO 3 y –H 2 PO 4 puede conectarse a los enlaces de carbono. Encontramos que la formación de N / S / P-CQD puede reducir la cantidad de –COOH que se adhiere a los bordes de sp 2 -conjugado π -dominios ubicados en los centros de estos CQD. Este efecto puede resultar en la reducción de la recombinación no radiativa para la transición electrónica en estos CQD. Como resultado, el rendimiento cuántico (QY) para la fluorescencia de los CQD se puede mejorar de manera eficiente. Demostramos experimentalmente que los QY para N / S / P-CQD pueden alcanzar hasta 18,7%, 29,7% y 10,3%, respectivamente, en comparación con el 9% para estos sin modulación de grupo funcional. Este trabajo puede proporcionar un enfoque experimental práctico para mejorar las propiedades ópticas de los CQD fluorescentes.
Antecedentes
Los puntos cuánticos de carbono (CQD) son nanomateriales emergentes [1] con propiedades fluorescentes superiores [2] y propiedades químicas, electrónicas y ópticas únicas [3]. A diferencia de las moléculas de colorante tradicionales y los puntos cuánticos basados en semiconductores, los CQD no solo presentan una buena resistencia a la luz y al blanqueamiento por luz de centelleo [4], sino también características importantes como baja toxicidad, biocompatibilidad, bajo coste, alta fotoestabilidad [5 ], etc. Por lo tanto, los CQD se han propuesto como materiales electrónicos y optoelectrónicos avanzados para su aplicación en áreas tales como dispositivos optoelectrónicos [6], conversión de energía [7], fotocatálisis [8], sensores [9], bioimagen [ 10], marcadores celulares [11, 12] y administración de fármacos [13], por mencionar solo algunos. En los últimos años, la investigación de CQD se ha convertido en un campo de investigación de rápido crecimiento en las comunidades científicas y de la industria.
En la actualidad, el método experimental más utilizado para la síntesis química de los CQD es mediante un enfoque ascendente que se puede aplicar para producir CQD fluorescentes de forma sencilla, económica y en grandes cantidades. En este método, pequeñas moléculas de compuestos orgánicos o polímeros se toman como fuentes de carbono y se deshidratan y carbonizan para realizar las CQD. Durante la preparación de los CQD, la superficie y el borde de los CQD a menudo están unidos por algunos grupos químicos como OH, COOH, C =O, etc. La presencia de estos grupos químicos puede afectar en gran medida las propiedades electrónicas y ópticas de los CQD. En particular, las características fluorescentes de los CQD dependen sensiblemente de la presencia de estos grupos [14]. Desde un punto de vista de la física, los grupos químicos adheridos a la superficie y al borde de los CQD pueden inducir nuevos tipos de estados de superficie y borde en los sistemas CQD y, por lo tanto, pueden modificar la estructura electrónica y los canales de transición electrónicos y ópticos correspondientes en el CQD. En este caso, la fotoluminiscencia (PL) de los CQD se puede lograr mediante la transición electrónica entre estados de borde y estados de carbono, como el conjugado π estados (o sp 2 área). Por lo tanto, el mecanismo de emisión de PL de los CQD es muy similar al de la emisión de luz fotoinducida de estados de impureza en un semiconductor dopado [15] de la siguiente manera:(i) los fotones pueden ser absorbidos a través de transiciones electrónicas desde y estados electrónicos de carbono ocupado a estados más altos y vacíos bajo la acción del bombeo óptico, (ii) los electrones fotoexcitados pueden relajarse en los estados electrónicos en los estados de borde a través de eventos de transición electrónica no radiativa, y (iii) el PL La emisión se puede lograr a través de transiciones electrónicas desde los estados de borde a los estados electrónicos con bajo contenido de carbono acompañadas de la emisión de fotones. Por lo tanto, los estados electrónicos de los bordes juegan un papel como los estados de impurezas radiativas en un semiconductor y los electrones se pueden combinar con los huecos para la luminiscencia. Generalmente, el sp 2 -conjugado π -se considera que los dominios son los centros inherentes para la emisión de PL [16] y los aromáticos sp 2 el área de carbono de un CQD está rodeada por sp 3 estados de carbono (C – OH). Por lo tanto, la recombinación de pares de electrones y huecos en el sp 2 El área y las transiciones electrónicas entre los estados de borde y carbono pueden promover la emisión de PL de los CQD [17, 18].
El rendimiento cuántico fluorescente (QY) es un parámetro clave para medir la eficiencia de la emisión de luz fotoinducida de un material o un dispositivo, que se define por el número de fotones emitidos en relación con el número de fotones absorbidos. En los primeros años, cuando se descubrieron los CQD, el QY para los CQD preparados químicamente era bastante bajo (incluso menos del 2%) [1]. Cómo mejorar la QY fluorescente para CQDs ha sido un problema central para la investigación fundamental y para la aplicación de materiales. En general, el QY para CQD obtenido químicamente a través de un enfoque ascendente depende de la elección de la fuente de carbono, la técnica de síntesis y la modulación de bordes. Más específicamente, la intensidad y frecuencia de la emisión de PL de los CQD son las consecuencias de los parámetros de muestra de los CQD, la presencia de los grupos funcionales o estados de borde, la interacción entre estados electrónicos en sp 2 -conjugado π -dominios y en grupos químicos, y las propiedades del fluoróforo en los CQDs [19]. En los últimos años, la QY fluorescente para CQD se ha mejorado en gran medida [20]. En particular, Lingam et al. examinó el efecto de los estados de borde inducidos en la síntesis de CQD sobre la emisión de PL. Descubrieron que si los bordes de los CQD se dañan, la emisión de PL cae bruscamente hasta ser incluso inconmensurable [21]. Un trabajo similar de Kumar et al. También ha demostrado que la presencia de los estados de borde es el factor clave para PL de CQD, y el origen de PL heterogéneo sintonizable es amino funcionalizado para CQDs [22]. Tang y col. informaron de una síntesis hidrotermal asistida por microondas simple de los CQD utilizando glucosa como única fuente de carbono [23]. Simplemente extendiendo el tiempo de reacción de 1 minuto a 9 minutos, pudieron ajustar el tamaño de los CQD de 1,65 nm a 21 nm. Curiosamente, encontraron que el PL de los CQD era independiente del tamaño de los CQD, donde los CQD con los tamaños de 9,6 nm y 20 nm muestran aproximadamente los mismos comportamientos de absorción y emisión de luz. Los resultados obtenidos a partir del trabajo de investigación adicional de Lin et al. también indican que la emisión de PL de los CQD depende débilmente del efecto del confinamiento cuántico de la sp 2 -conjugado π -dominios [24] y la presencia de los grupos funcionales de superficie unidos a los CQD es el factor clave para la emisión de PL. Dong y col. realizó los CQD fluorescentes azules con las nanohojas en forma de disco (el tamaño de 15 nm y el grosor de 0,5 a 2,0 nm) ajustando el grado de carbonatación del ácido cítrico. Descubrieron que el PL de los CQD es independiente de la longitud de onda de excitación y el QY fluorescente puede llegar hasta el 9,0% [25]. Cabe señalar que de acuerdo con la relación entre el tamaño de un CQD y la longitud de onda de la emisión PL para un CQD desnudo [26], los CQD con un tamaño de aproximadamente 2,25 nm pueden emitir la fluorescencia azul, mientras que los CQD con el El tamaño de 15 nm solo puede emitir fluorescencia de longitud de onda más larga. La fuerte emisión de PL azul de los CQD con un tamaño de 15 nm [25] sugiere una vez más que la presencia de los estados de borde inducidos por grupos químicos unidos a los CQD es principalmente responsable de la emisión de PL de los CQD. Por lo tanto, la funcionalidad de borde de los CQD puede afectar no solo a la fluorescencia de los CQD, sino también a las propiedades físicas y químicas de los CQD en general [19].
Cabe señalar que, en la actualidad, la frecuencia de la emisión fluorescente de los CQD no se puede controlar y modificar artificialmente fácilmente. Además, el QY fluorescente correspondiente aún no ha alcanzado los requisitos para la aplicación como dispositivos prácticos. Los resultados obtenidos de investigaciones experimentales [27, 28, 29] y teóricas [30, 33] han confirmado que la pasivación de bordes puede mejorar eficazmente las propiedades ópticas electrónicas de los CQD. Los agentes de pasivación se utilizan ampliamente para ajustar las propiedades fluorescentes de las CQD [21,22,23]. Jing Liu y col. desarrolló una preparación en un solo paso de puntos cuánticos de carbono dopado con nitrógeno y pasivado en la superficie [27]. Descubrieron que el QY de los CQD sin pasivación superficial suele ser bastante bajo (QY <10%), los CQD pasivados muestran un QY del 37,4%. Un trabajo similar de Shen et al. investigaron que los CQD pasivados con PEG tienen un QY del 28% [28], y Kwon et al. informó que la hexadecil amina (HDA) pasivada produce un 19-35% [29]. Dimos y colaboradores también descubrieron que la pasivación de los bordes puede inducir eficazmente los electrones en la banda de conducción y aumentar la energía superficial de las CQD para evitar la degradación de la fluorescencia o la extinción causada por la agregación de las CQD [30]. Además, la generación de fluorescencia a partir de CQD fabricados mediante una reacción química o un enfoque ascendente es inducida principalmente por la presencia de los grupos funcionales radiativos o fluoróforo unido al borde de los CQD [31]. Químicamente, estos grupos funcionales se pueden modificar poniendo los CQD en diferentes soluciones químicas. La fluorescencia de estos CQD modificados químicamente se puede lograr mediante la emisión excitónica acompañada de recombinación electrónica y separación de pares de electrones y huecos atrapados en el borde de los CQD [32]. Por lo tanto, la frecuencia de la emisión PL se puede sintonizar seleccionando diferentes grupos de bordes para formar los estados de borde requeridos.
La principal motivación de este estudio es explorar cómo las propiedades fluorescentes de los CQD se pueden modificar en diferentes soluciones químicas para su pasivación o funcionalidad de borde. Recientemente, habíamos producido CQD a partir de aguas residuales de tofu sin agregar ninguna sustancia tóxica y revelamos el mecanismo de luminiscencia [33]. Descubrimos que se pueden lograr diferentes colores de la emisión fluorescente de estos CQD colocando estos materiales de puntos en agua o en una solución de NaOH [33]. También habíamos fabricado los CQD a partir de jugo de limón fresco y los aplicamos para obtener imágenes celulares [34]. Se descubrió que la presencia de grupos que contienen oxígeno en la superficie y el borde de las CQD es la principal responsable de la fluorescencia de las CQD [34]. Nuestra atención del presente estudio se centra principalmente en cómo lograr una forma eficaz de mejorar el rendimiento cuántico de fluorescencia de los CQD.
Método
Síntesis de N-, S- y P-CQD
En este trabajo, el ácido cítrico (C 6 H 8 O 7 , 99,5%), hidróxido de sodio (NaOH, 96%), solución de amoniaco (NH 3 H 2 O, 25-28%), solución de ácido sulfúrico (H 2 SO 4 , 98%), solución de ácido fosfórico (H 3 PO 4 , 85%), y se utilizó agua desionizada para fabricar los CQD y modificar los estados de los bordes.
Los B-CQD se sintetizaron mediante pirólisis de ácido cítrico como única fuente de carbono. Los N / S / P-CQD se fabricaron mediante pirólisis de amoníaco, ácido sulfúrico y ácido fosfórico junto con ácido cítrico, respectivamente. El principio y los procesos experimentales para la realización de los CQD y los N / S / P-CQD correspondientes se muestran en la Fig. 1. A través de la pirólisis del ácido cítrico, los B-CQD se pueden fabricar mediante deshidratación intermolecular, carbonización y reacción de condensación. Este enfoque puede formar (i) la estructura aromática (es decir, el sp 2 estados de carbono con enlaces C – C y C =C) con el área conjugada como núcleo de los CQD, (ii) los bordes de los CQD unidos por hidroxilo (OH) y carboxilo (COOH / –O – C =O), y (iii) el sp 3 área de carbono (C – C – OH / –C – O) que puede pasivarse, por ejemplo, en una solución de NaOH. Los N-CQD se pueden lograr mediante el proceso de pirólisis de la solución mixta de ácido cítrico y NH 3 H 2 O. En tal caso, la reacción de deshidrogenación entre grupos adyacentes con carboxilo puede promover la formación de N pirrólico en el esqueleto de grafeno de las CQD. Los bordes de los N-CQD se unen luego con grupos químicos adicionales como –C – N y –NH 2 [35]. Similar a la realización de los N-CQD, S-CQD y P-CQD se pueden fabricar mediante la pirólisis de la solución mixta de ácido cítrico y H 2 SO 4 y H 3 PO 4 , respectivamente. La reacción de deshidratación, carbonización y condensación intermolecular puede formar el esqueleto de grafeno de los CQD con la conexión a grupos químicos como –SO 2 , –HSO 3 y –H 2 PO 4 . Además, es probable que los átomos de S y P se unan al borde de sp 2 área de conjugado de carbono para formar los defectos de los bordes. Las estructuras de los materiales de N / S / P-CQD se muestran en la Fig. 1. En el presente estudio, N / S / P-CQD se dispersan en una solución de NaOH a temperatura ambiente para hacerlos pasivación. Por lo tanto, podemos convertir parte de –COOH en el borde de los CQD en –COONa y reducir la cantidad de –COOH en el borde de sp 2 -conjugado π -dominios. En consecuencia, se puede lograr la modificación del grupo en el borde de los CQD.
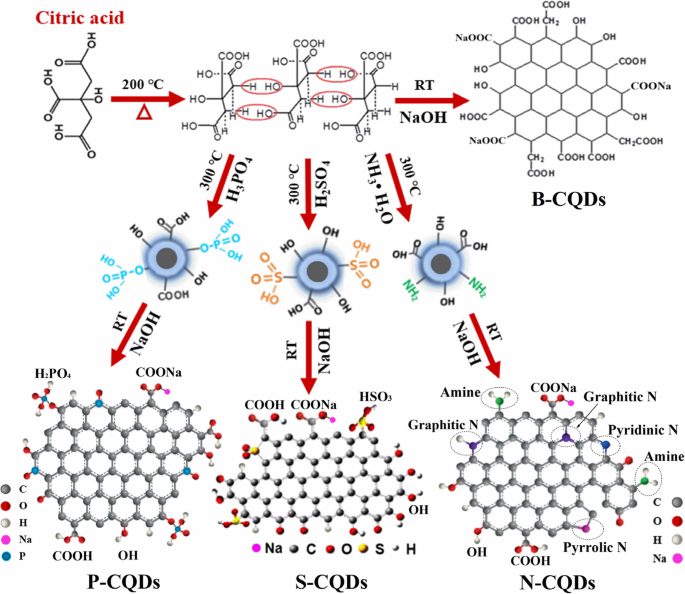
Procesos de síntesis esquemática de CQD y estructuras N-, S- y P-CQD correspondientes
Más específicamente, los N / S / P-CQD fluorescentes se preparan de las siguientes maneras:(i) Se agregaron 2 g de ácido cítrico analíticamente puro en 60 ml de NH 3 H 2 O (pH =7,5), 60 ml H 2 SO 4 (pH =3) y 60 ml de H 3 PO 4 (pH =3), respectivamente. (ii) Colocamos la solución mezclada en la plataforma de calentamiento para un calentamiento constante a 300 ° C, donde el tiempo de calentamiento es de 20 a 30 min. (iii) Se añaden 50 ml de solución de hidróxido de sodio (NaOH) al vaso de precipitados después de que el vaso de precipitados se enfríe de forma natural hasta la temperatura ambiente. (iv) La mezcla se agita magnéticamente durante 10 min y se somete a una descarga ultrasónica durante 10 min y se centrifuga adicionalmente a una velocidad de 12 000 r / min durante 10 a 30 min. Luego, se toma el sobrenadante, en el cual N / S / P-CQDs modificados por soluciones de amoniaco, ácido sulfúrico y ácido fosfórico, respectivamente, y pasivados por grupos como –OH, –COOH, –C =O, –COONa, –NH 2 , –SO 2 , –HSO 3 y –H 2 PO 4 se puede obtener en soluciones de NaOH. En la preparación de N / S / P-CQD, excepto que los N / S / P-CQD fueron modificados por NH 3 H 2 O, H 2 SO 4 y H 3 PO 4 , respectivamente, las otras condiciones experimentales fueron aproximadamente las mismas. Usamos la misma cantidad de ácido cítrico para disolverlo en NH 3 H 2 O, H 2 SO 4 y H 3 PO 4 , respectivamente, para la pirólisis y luego se añadió la misma cantidad y la misma concentración de solución de hidróxido de sodio cuando las sustancias en el vaso de precipitados estaban casi secas. Esto puede garantizar que la densidad de los CQD en la solución de NaOH sea casi la misma.
Medidas
En este trabajo se observó la morfología y microestructura de las CQDs mediante microscopía electrónica de transmisión (TEM, JEM 2100) a un voltaje de aceleración de 300 kV. La espectroscopia de fotoelectrones de rayos X (XPS) se aplicó para caracterizar las muestras, utilizando espectrómetro de fotoelectrones PHI5000 Versa Probe II con Al Kα a 1486,6 eV. El espectro de absorción ultravioleta-visible (UV-Vis) de los CQD se midió mediante un espectrofotómetro UV-Vis (Specord200, Alemania). La emisión de PL de los CQD se midió utilizando un sistema PL estándar (IHR320, Jobin Yvon, EE. UU.) A temperatura ambiente. El QY fluorescente de los CQD se evalúa sobre la base de los datos de PL.
Resultados y discusiones
La caracterización de las muestras
La morfología y las estructuras de las CQD sintetizadas fueron investigadas por TEM. La Figura 2 muestra las imágenes TEM (a) y las distribuciones de diámetro (b) de S-CQD. Puede verse claramente que los S-CQD son láminas circulares y se dispersan uniformemente en una solución de NaOH. A través de un promedio estadístico de las imágenes TEM para los CQD, encontramos que la distribución de tamaño de los S-CQD se ubica principalmente en el rango de 3 a 8 nm y el tamaño promedio de los CQD es de aproximadamente 5,73 nm. Estos resultados se obtienen mediante análisis estadístico de más de 300 partículas CQD utilizando la imagen J software. Los resultados mostrados en la Fig. 2c indican que estos S-CQD están altamente cristalizados con una estructura reticular típica de carbono. Las franjas de celosía de los CQD son claras y el espaciado de celosía correspondiente es de aproximadamente 0.215 nm consistente con la faceta (100) del grafeno [32].
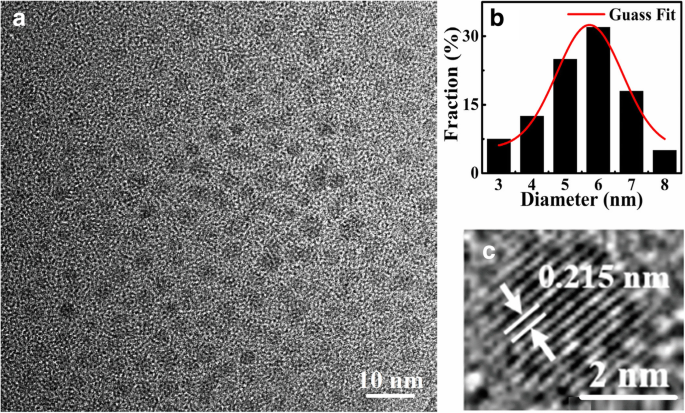
Imágenes TEM de S-CQD en solución de NaOH (pH =12) en a y sus flecos de celosía en c . La distribución de diámetro de los S-CQD se muestra en b
En el presente estudio, aplicamos la espectroscopia de fotoelectrones de rayos X (XPS) para la medición y examen de los grupos funcionales de los bordes adjuntos a los CQD. Usamos láminas de vidrio como sustratos y cubrimos las muestras sobre las láminas de vidrio para las medidas. En la Fig. 3, mostramos los espectros XPS para N-, S- y P-CQD. Como se muestra en la Fig. 3a, el espectro XPS de barrido completo para N-CQD indica que el porcentaje atómico de N1 es del 9,6%. Las figuras 3 byc indican que (i) las CQD S- y P-muestran picos de respuesta para S2 (a 169 eV) y P2 (a 133 eV), respectivamente, en contraste con las CQD preparadas sin modificación del grupo funcional y (ii) los porcentajes atómicos de S2 para S-CQD y de P2p para P-CQD son 2,7% y 0,6%, respectivamente. La razón principal de un contenido más bajo de P en P-CQD que el contenido de S en S-CQD es que P tiene un radio atómico relativamente mayor (el número de protones de núcleos es 15) que S (el número de protones de núcleos es 16). Por lo tanto, es relativamente menos probable que los átomos de P sean absorbidos por los enlaces químicos en la superficie de los CQD que los átomos de S. En comparación con la Fig. 3 ayc para los espectros XPS para N- y P-CQD, la Fig. 3 b muestra que el porcentaje de átomos de C1 en S-CQD es mucho mayor (76,9%) y las proporciones de átomos de O1 ( 20,2%) y los átomos de impurezas (S, Na) son muy bajos. Estos resultados indican que hay menos defectos en el sp 2 área de carbono en S-CQD. En la Fig. 3 d se muestran los espectros de alta resolución de C1 exhibe tres picos típicos, respectivamente, a 284,8 eV, 286,6 eV y 288,5 eV para N-CQD, lo que indica que el sp 2 El área de carbono (C – C / C =C) tiene una buena estructura reticular [14, 25, 36]. Además, sp 3 El carbono (C – O / C – N, 286,4 eV) y el carboxilo (O – C =O / COOH, 288,1 eV) tienen una energía de unión similar [33], lo que sugiere que existen cantidades similares de hidroxilo (C – O / C– OH) y carboxilo (O – C =O / COOH) alrededor de la sp 2 área de carbono. Los correspondientes espectros de alta resolución de C1 para S- y P-CQD se muestran en la Fig. 3 ey f. Como se muestra en la Fig. 3 e, el pico de sp 3 El carbono (C – O) es muy fuerte y el pico de hidroxilo (O – C =O / COOH) es débil para los S-CQD, lo que indica que la cantidad de hidroxilo (C – O / C – OH) es mucho mayor que la del carboxilo. (O – C =O / COOH) alrededor de la sp 2 área de carbono para S-CQD. Además, la Fig. 3 h indica que la cantidad de hidroxilo (C – O / C – OH) es menor que el carboxilo (O – C =O / COOH) alrededor de la sp 2 área de carbono para P-CQD. Comparando con la Fig. 3 d, eyf, encontramos que el pico de hidroxilos (C – O / C – OH) es el más fuerte mientras que el pico de hidroxilos (O – C =O / COOH) es el más débil. para S-CQD. Cuando aumenta la cantidad de grupos hidroxilo, se reduce la cantidad de grupos carboxilo, y viceversa, cuando aumenta la cantidad de grupos carboxilo, disminuye la cantidad de grupos hidroxilo.
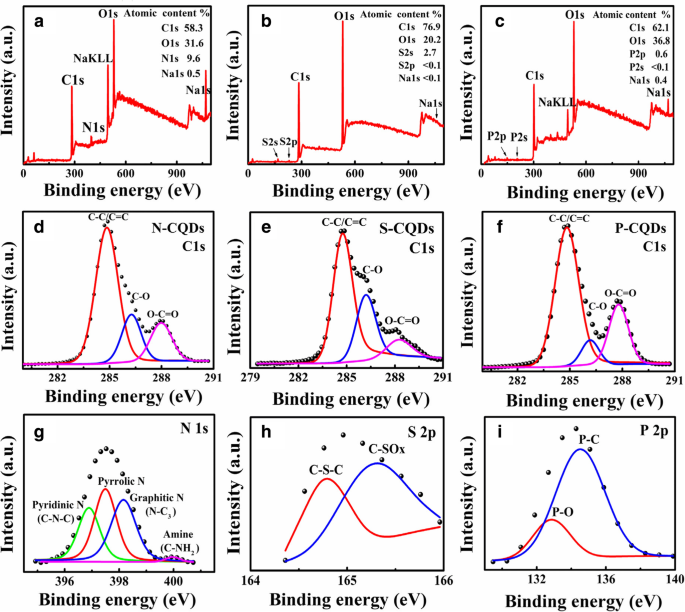
Los espectros XPS de escaneo completo en a / b / c y los espectros de alta resolución de C1 en d / e / f y N1 s / S2p / P2p en g / h / yo para, respectivamente, los N / S / P-CQDs
En la Fig.3 g, los espectros de alta resolución de N1s muestran cuatro picos relacionados con nitrógeno piridínico (N piridínico, 396,9 eV), nitrógeno pirrólico (N pirrólico, 397,6 eV), nitrógeno grafito (N – C 3 , 398.5 eV, ubicado en el centro de sp 2 carbono) y el grupo amida (C – NH 2 , 399,9 eV, ubicado en el borde de sp 2 carbono), respectivamente [22, 37,38,39]. Estos resultados verifican la estructura del material de los N-CQD que se muestran en la Fig. 1. En los N-CQD, los fluoróforos se forman mediante la hibridación de grupos funcionales de borde como C – OH y C – NH 2 con sp 2 -conjugado π -dominios [40], que pueden desempeñar un papel en la mejora de la fluorescencia de N-CQD. El espectro de alta resolución de S2s y P2p correspondiente a los resultados de XPS para S- y P-CQDs se muestran en la Fig.3 h y i, implica que los bordes de S-CQDs y P-CQDs están unidos por algunos enlaces químicos tales como C – S – C (164,8 eV) [41], C – SO X ( X =2, 3, 4, 165,1 eV) [42], P – C (135,0 eV) [43] y PO (132,7 eV) [44]. Por lo tanto, los enlaces químicos como C – SO 2 , –HSO 3 , C – P – C, –H 2 PO 4 , etc. se pueden formar en los bordes de los CQD S y P, como se muestra en la Fig. 1.
La Fig. 4 muestra los espectros de absorción y emisión medidos a partir de las CQD B y N / S / P en soluciones de NaOH. En la Fig. 4a se muestran los espectros de absorción UV-Vis de B / N / S / P-CQD. El espectro de absorción de B-CQD exhibe picos de absorción UV a 278 nm, mientras que el espectro de absorción UV-Vis de N-, S- y P-CQD representa dos bandas de absorción claras. El pico de absorción a 253 nm se atribuye a π - π * transición del enlace aromático C =C y el hombro a 302 nm corresponde a n - π * transición del enlace C =O [40]. Los enlaces C =C provienen de sp 2 -Dominios conjugados en los núcleos de N / S / P-CQD, mientras que los enlaces C =O se originan a partir de los numerosos grupos extractores de electrones que contienen oxígeno, como los grupos carboxilo y carbonilo que existen en los sitios de borde de N / S / P-CQD . Los dos picos de absorción revelan la existencia de sp 2 -Estructuras conjugadas y grupos funcionales que contienen oxígeno (C =O y O – C =O / COOH) en N-, S- y P-CQD.
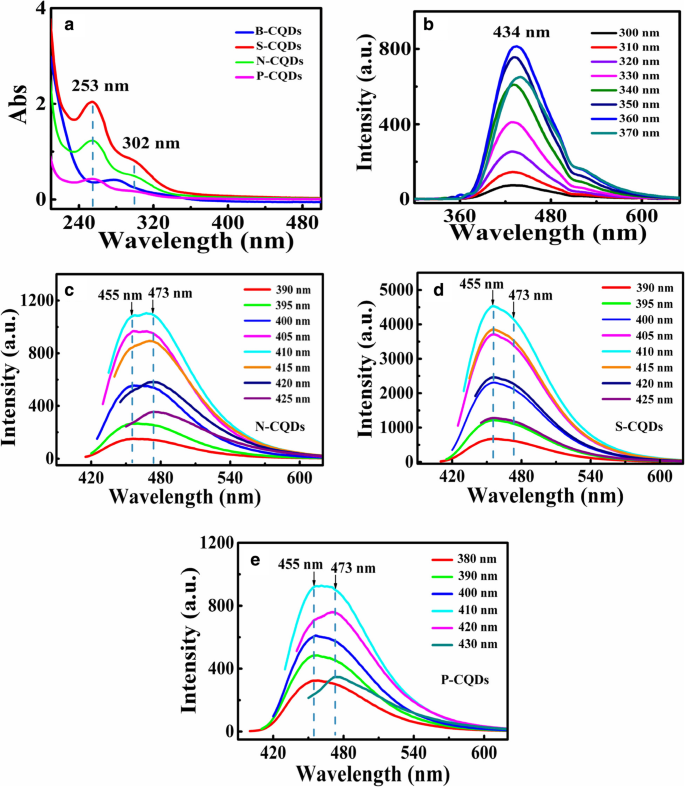
Los espectros de absorción de UV-Vis por B- y N / S / P-CQD en a . Los espectros PL de b B-CQD, c N-CQD, d S-CQD y e P-CQD con diferentes longitudes de onda de excitación como se indica. Estos resultados se obtienen a temperatura ambiente
La Figura 4 b – e muestra los espectros PL de B- y N / S / P-CQD. Como podemos ver, la fuerte emisión de PL se puede observar en estos CQD. Encontramos que la intensidad de la emisión PL primero aumenta y luego disminuye al aumentar la longitud de onda de excitación. Este efecto se ha encontrado en la mayoría de los materiales nanoestructurados (ver, por ejemplo, Ref. [45]). Como ha señalado la Ref. [38], la dependencia de la intensidad de la emisión de PL sobre la excitación de los CQD se origina principalmente debido a los estados de superficie heterogéneos y los tamaños y propiedades electrónicas de los heteroátomos. Para el caso de los CQD con modulación de grupo de superficie, la presencia de los estados de superficie puede alterar la banda prohibida y los estados de energía radiativa de los CQD. Bajo una excitación de longitud de onda relativamente más corta, los electrones se bombean a estados de mayor energía en la banda de conducción más lejos de los estados electrónicos radiativos inducidos por la modulación de la superficie. Por lo tanto, la posibilidad de emisión de fotones de los CQD se reduce mediante una excitación de longitud de onda más corta. Es decir, la intensidad de la emisión de PL aumenta con la longitud de onda de excitación en un régimen de longitud de onda más corta. En un régimen de longitud de onda relativamente larga, la excitación de longitud de onda más larga implica que se pueden bombear relativamente menos electrones a la banda de conducción en los CQD. Como resultado, la intensidad de la emisión de PL disminuye al aumentar la longitud de onda de excitación en un régimen de longitud de onda de excitación larga. Además, las emisiones PL de N / S / P-CQD consisten en dos bandas espectrales superpuestas [25]. Los picos dobles de PL se pueden medir respectivamente a aproximadamente 455 nm y 473 nm mediante excitación de longitud de onda de 410 nm. Esto es una consecuencia de las emisiones de PL de N / S / P-CQD modificadas por diferentes grupos funcionales para afectar la recombinación radiativa de pares electrón-hueco (e-h) formados por sp 2 -conjugado π -Dominios y grupos de estado de borde [32, 40]. El posible mecanismo propuesto aquí es que (i) la fotoexcitación de electrones en N / S / P-CQDs se logra a través de π - π * transiciones de sp 2 -conjugado π -dominios a n - π * transiciones, (ii) los electrones se relajan de n - π * establece niveles de energía C =O a través de canales de transición no radiativos, y (iii) la recombinación radiativa para huecos en sp 2 discretos Los estados relacionados y los electrones en los estados de borde pueden ser inducidos por abundantes grupos funcionales [46].
En la Fig. 4 b-e, bajo las mismas condiciones experimentales, encontramos que la intensidad de fluorescencia de N / P / S-CQD fue significativamente mayor que la de B-CQD. La intensidad de la emisión de PL de los S-CQD es la más fuerte, seguida de los N-CQD, y la emisión de PL de los P-CQD es la más débil. Este hallazgo corresponde a los resultados mostrados en espectros de alta resolución de C1 para N / S / P-CQD (ver Fig. 3d, e, f). La intensidad de la emisión de PL aumenta al aumentar la altura del pico de C – O (C – OH) y al disminuir la altura del pico de O – C =O (COOH). Por lo tanto, es razonable creer que los N / S / P-CQD con varios grupos de bordes, como C – OH, COOH, C =O y C – H, pueden inducir diferentes tipos de estados de borde e influir en la intensidad de su fotoluminiscencia. Lo más interesante es que encontramos que las posiciones de los picos para la emisión de PL de N / S / P-CQD dependen de la longitud de onda de excitación, lo que implica que los estados electrónicos radiativos inducidos por grupos funcionales unidos a los bordes de los CQD son bastante estables.
Como se mencionó anteriormente, sp 2 El área de carbono de los S-CQD tiene menos defectos, por lo que la emisión de luz inherente de los S-CQD es la más fuerte, en comparación con los N- y P-CQD. Después de utilizar la fórmula para evaluar el rendimiento cuántico fluorescente [33], obtenemos que los QY para N / S / P-CQD son 18,7%, 29,7% y 10,3%, respectivamente. Por lo tanto, se puede lograr el mayor QY para S-CQD, seguido de N- y P-CQD. Como sabemos, la QY de los CQD es una consecuencia del proceso competitivo entre la transición electrónica radiativa y las trampas no radiativas [32]. El hidroxilo (C – O / C – OH) en los bordes de los CQD se puede hibridar sinérgicamente con estados electrónicos en sp 2 -conjugado π -dominios para formar los fluoróforos, mientras que los carboxilo (–COOH) pueden desempeñar un papel como centro de recombinación no radiativa en el borde de las CQD [40]. Por lo tanto, el QY de los CQD se ve afectado por los grupos C – O / C – OH y O – C =O / COOH. Además, encontramos que el uso de ácido sulfúrico para la modificación de los grupos funcionales en el borde de S-CQD puede afectar significativamente la mejora de la emisión de PL de S-CQD, en comparación con N- y P-CQD. El QY de 29,7% para S-CQD, realizado en este estudio, es mayor que 18,7% para N-CQD, 10,3% para P-CQD y 9% para CQD [23] preparados sin amoniaco, ácido sulfúrico o ácido fosfórico .
En este trabajo, los N / S / P-CQD se sintetizan mediante pirólisis de estas mezclas de ácido cítrico y NH 3 H 2 O, H 2 SO 4 y H 3 PO 4 , posteriormente dispersado en las soluciones de NaOH. Puede promover la deshidratación intermolecular, la carbonización y la reacción de condensación para el ácido cítrico. El carboxilo (–COOH) en los bordes de los CQD se puede convertir en carbonilo (–C =O) [19], y los bordes de los N / S / P-CQD se pueden unir mediante grupos químicos como –OH, –COOH , –C =O, –NH 2 , –SO 2 , –HSO 3 y –H 2 PO 4 . Por lo tanto, la formación de N / S / P-CQD puede reducir la cantidad de –COOH adherida a los bordes de sp 2 -conjugado π -dominios y puede resultar en la reducción de la recombinación no radiativa [47]. En consecuencia, la QY fluorescente de los CQD se puede mejorar de manera eficiente.
Conclusiones
En este estudio, hemos desarrollado un método experimental eficaz para mejorar el rendimiento cuántico fluorescente de CQD. Los N / S / P-CQD se han sintetizado mediante pirólisis de ácido cítrico y utilizando, respectivamente, amoníaco, ácido sulfúrico y ácido fosfórico para modificaciones de los grupos de bordes. Los resultados han demostrado que la presencia de los grupos funcionales de los bordes puede desempeñar un papel importante en la generación y mejora de la fluorescencia de estos CQD. Especialmente, los grupos hidroxilo (C – O / C – OH) en los bordes de sp 2 -conjugado π Los dominios-pueden afectar significativamente los rendimientos cuánticos fluorescentes de los CQD. Sin embargo, la unión de grupos carboxilo (O – C =O / –COOH) a los bordes de sp 2 -conjugado π -dominios conducen principalmente a centros de recombinación no radiativos, que pueden debilitar la emisión de PL de los CQD. En el presente estudio, los QY para N / S / P-CQD pueden alcanzar hasta 18,7%, 29,7% y 10,3%, respectivamente. Estos valores son mucho más altos que el del 9% para los CQD preparados sin modificación del grupo funcional. La conclusión más importante que sacamos de este estudio es que la modificación del grupo en los bordes de los CQD por el ácido sulfúrico puede afectar fuertemente la emisión de fluorescencia y QY de los CQD.
Disponibilidad de datos y materiales
Los conjuntos de datos generados durante y / o analizados durante el estudio actual están disponibles de los autores correspondientes a solicitud razonable.
Abreviaturas
- CQD:
-
Puntos cuánticos de carbono
- PL:
-
Fotoluminiscencia
- QY:
-
Rendimiento cuántico
- TEM:
-
Microscopio electrónico de transmisión
- UV-Vis:
-
Ultravioleta visible
- XPS:
-
Espectroscopia de fotoelectrones de rayos X
- XRD:
-
Difracción de rayos X
Nanomateriales
- Los nanotubos de carbono superan el límite de la electrónica flexible
- Imagen de carbono oceánico en escala atómica
- Costo de la fibra de carbono:factores que más influyen
- N, N-dimetilformamida reguladora de la fluorescencia de los puntos cuánticos de MXene para la determinación sensible de Fe3 +
- Presentación de la estructura atómica y electrónica de las nanofibras de carbono de copa apilada
- El diseño de la capa de emisión para multiplicadores de electrones
- Síntesis de puntos cuánticos de carbono codopados N, S ricos en piridínicos como imitadores enzimáticos eficaces
- Puntos cuánticos de bismuto en pozos cuánticos de GaAsBi / AlAs recocidos
- Defectos en la superficie del nanofósforo de MgAl2O4 dopado con Ti
- Un enfoque simple para sintetizar puntos cuánticos de carbono fluorescente de aguas residuales de tofu
- Fotoconductividad entre bandas de puntos cuánticos de InAs / InGaAs metamórficos en la ventana de 1,3 a 1,55 μm



