Fabricación de hidrogeles compuestos de poli (ácido acrílico) / nitruro de boro con excelentes propiedades mecánicas y rápida autocuración a través de interacciones jerárquicamente físicas
Resumen
Muchos tejidos vivos poseen excelentes propiedades mecánicas y capacidad de autocuración. Para imitar estos tejidos vivos, una serie de nuevos hidrogeles compuestos, nanohojas de poli (ácido acrílico) / nitruro de boro modificado en la superficie (PAA / BNNS-NH 2 ) se fabricaron simplemente a través de interacciones jerárquicamente físicas:interacción de coordinación de metales a escala molecular entre –COOH de PAA y Fe 3+ y enlace H a nanoescala entre –COOH de PAA y –NH 2 de BNNS-NH 2 . Los hidrogeles compuestos exhiben excelentes propiedades mecánicas (que incluyen mayor tensión de fractura, alargamiento, tenacidad, módulo de Young y energía disipada) y una capacidad de curación rápida sin ningún estímulo externo. Especialmente, el B 0.5 P 70 (el hidrogel con una concentración de BNNS de 0,5 mg mL - 1 , el contenido de agua del 70% en peso) presenta una tensión de fractura de ~ 1311 kPa y una tenacidad de ~ 4,7 MJ m - 3 , casi ~ 3 veces y ~ 8 veces a B 0 P 70 , respectivamente. Las excelentes propiedades, combinadas con el método de preparación simple, dotan a estos hidrogeles compuestos de posibles aplicaciones.
Antecedentes
Los hidrogeles con redes tridimensionales formadas por enlaces covalentes y / o interacciones físicas entrecruzados que contienen una gran cantidad de agua poseen alta hidrofilicidad, capacidad de retención de agua y biocompatibilidad excepcional [1,2,3,4], lo que les permite ser uno de los más biomateriales populares. Sin embargo, la mayoría de los hidrogeles tienen malas propiedades mecánicas, lo que limita en gran medida las aplicaciones. Es bien sabido que muchos tejidos vivos, como músculos, ligamentos y piel, poseen una propiedad mecánica excelente y una capacidad significativa para curar heridas de forma autónoma [5,6,7]. Inspirándose en estos tejidos vivos, se han explorado materiales con altas propiedades mecánicas y capacidad de autocuración para diversas aplicaciones [8, 9], que incluyen ingeniería de tejidos, liberación de fármacos, vendajes para heridas, lentes de contacto, sensores y actuadores [2, 10, 11,12]. Ihsan y col. informó de un hidrogel de polianfolito que se auto-curaba mediante la reformación de los enlaces irónicos en la superficie de la fractura [7]. Zhang y col. diseñó un hidrogel autocurable de PVA con un proceso de autocuración rápido mediante enlaces de hidrógeno [13]. Tao y col. preparó un hidrogel autocurativo resistente al frío reticulado por enlace dinámico de éster catecol-borato que permite autocurarse tanto a temperatura ambiente como a baja temperatura [14]. Sin embargo, todos estos materiales autocurables tienen una debilidad común:las malas propiedades mecánicas [15,16,17,18,19] limitaban en gran medida las aplicaciones.
Para mejorar la propiedad mecánica de los hidrogeles, se han introducido algunos nanomateriales inorgánicos en los sistemas reticulados. Han y col. informó un hidrogel supermolecular mediante el uso de nanohojas de óxido de grafeno para reducir la temperatura para la autocuración [15]. Si y col. explotó un nuevo hidrogeles ensamblados con nanofibras con memoria de forma, súper elásticos y de contenido ultra alto en agua [20]. El flexible SiO 2 Se introdujeron nanofibras para mejorar las propiedades mecánicas y acelerar la memoria de forma y la respuesta a la presión. Especialmente, Duan et al. desarrollaron hidrogeles compuestos de poli (alcohol vinílico) / nitruro de boro (PVA / BNNS) con propiedades mecánicas mejoradas [21]. Gao y col. fabricó un hidrogel nanocompuesto relleno de montmorillonita exfoliada que mejoró drásticamente el alargamiento de la fractura [22]. Zhong y col. diseñaron hidrogeles nanocompuestos de óxido de grafeno (GO) / poli (ácido acrílico) (PAA / GO) que mejoraron significativamente las propiedades mecánicas [23]. Los nuevos hidrogeles compuestos autorreparables con propiedades mecánicas mejoradas todavía son muy buscados, aunque los hidrogeles explotados han avanzado significativamente en los últimos años. Las nanoláminas de nitruro de boro, “grafeno blanco”, exhiben muchas propiedades excelentes, incluidas excelentes propiedades mecánicas, una inercia química extraordinaria y una notable no toxicidad [24, 25, 26]. En particular, las nanoláminas BN de superficie modificada sirvieron como nanorrellenos en los nanocompuestos de hidrogeles que mejoran las propiedades mecánicas y térmicas y se han informado en trabajos recientes [27, 28]. Por lo tanto, el desarrollo de un nuevo hidrogel compuesto con nanoláminas BN de superficie modificada todavía está muy perseguido.
Aquí, los nuevos hidrogeles compuestos se fabrican a partir de poli (ácido acrílico) (PAA) y nanohoja de nitruro de boro de superficie modificada con grupos amino (BNNS-NH 2 ) a través de interacciones jerárquicamente físicas:interacción de coordinación de metales a escala molecular entre –COOH de PAA e iones férricos (Fe 3+ ) y enlace H a nanoescala entre –COOH y BNNS-NH 2 Fue reportado. La introducción de BNNS-NH 2 mejoró la propiedad mecánica y aceleró el proceso de autocuración de los hidrogeles. Este trabajo proporciona una nueva ruta para preparar hidrogeles con excelentes propiedades mecánicas y una rápida capacidad de autocuración.
Método / Experimental
Materiales
Persulfato de potasio (KPS; 99,0%) y FeCl 3 · 6H 2 Se adquirió O (99,0%) de J&K Chemical Technology y ácido acrílico (AA; 98,0%) de Sigma-Aldrich. Todos estos productos químicos se utilizaron tal como se recibieron sin ninguna purificación. La rodamina B (95,0%) se adquirió de Sigma-Aldrich. BNNS-NH 2 fue obtenido por nuestro trabajo anterior [24]. Se utilizó agua desionizada a lo largo de los experimentos.
Preparación de BNNS-NH 2 Dispersión
BNNS-NH 2 fue preparado de acuerdo con nuestro trabajo anterior [24]. Para hacer BNNS-NH 2 dispersos constantemente en la red polimérica, es indispensable preparar el BNNS-NH 2 dispersiones de agua. Para obtener el BNNS-NH 2 estable Se utilizaron dispersiones, agitación magnética y baño de ultrasonidos a temperatura ambiente. El BNNS-NH 2 dispersiones con concentraciones de 1.0, 0.8, 0.5 y 0.1 mg mL - 1 se obtuvieron mediante el siguiente procedimiento. Los 100 mg, 80 mg, 50 mg y 10 mg de BNNS-NH 2 se agregaron en 100 mL de agua desionizada, respectivamente, bajo agitación magnética (1000 rpm) durante 24 ha temperatura ambiente en aire ambiente para obtener mezclas, y luego las mezclas se sonicaron (20 kHz) a temperatura ambiente durante 2 h en aire ambiente para obtener dispersiones estables. Para evitar la pérdida de la solución acuosa, las dispersiones obtenidas se conservaron en recipientes sellados con diferentes marcas para la siguiente preparación de hidrogeles autorreparables.
Preparación de hidrogel autocurativo
El PAA como polímero común con abundantes grupos –COOH permite establecer la cantidad de enlaces de hidrógeno intracatenarios e intercatenarios que otorgan al polímero una elasticidad superior y una resistencia favorable [29]. Además, las interacciones de coordinación de metales se establecen entre –COOH de PAA y el ión férrico (Fe 3+ ). Los dos tipos de enlaces no covalentes reversibles dotaron al hidrogel de propiedades de autocuración. Los hidrogeles reticulados por enlaces no covalentes siempre poseen propiedades mecánicas inferiores. Para mejorar la fuerza del hidrogel, BNNS-NH 2 se introdujo en la red tridimensional del polímero, que estableció enlaces de hidrógeno entre –NH 2 de BNNS-NH 2 y –COOH de PAA. Aquí, el compuesto PAA / BNNS-NH 2 los hidrogeles se abrevian como B x P y , en el que B representa BNNS-NH 2 , x es el contenido del BNNS-NH 2 (mg mL - 1 ), P significa PAA / BNNS-NH 2 hidrogel compuesto, e y se refiere al contenido de agua del PAA / BNNS-NH 2 hidrogel compuesto (fracción de masa,% en peso). Los hidrogeles se prepararon de acuerdo con un procedimiento que se describe a continuación. Normalmente, 10 ml de AA, 0,25 g de FeCl 3 · 6H 2 Se disolvieron O (1,05% en moles de AA) y 0,1 g de KPS (0,25% en moles de AA) en BNNS-NH 2 dispersiones con diferentes concentraciones o agua desionizada bajo agitación magnética (1000 rpm) a temperatura ambiente durante 10 min bajo aire ambiente para formar una mezcla homogénea. Después de eso, N 2 se burbujeó en la mezcla para eliminar el oxígeno (10 min), y luego se llevó a cabo la polimerización a 25 ° C en un baño de agua durante 6 h para formar hidrogeles. Hidrogeles preparados según el procedimiento mencionado anteriormente y los parámetros de BNNS-NH 2 dispersiones con la concentración de 1.0, 0.8, 0.5 y 0.1 mg mL - 1 se indicaron como B 1 P 90 , B 0.8 P 90 , B 0.5 P 90 y B 0.1 P 90 , respectivamente, mientras que los hidrogeles preparados a partir de agua desionizada se denominaron B 0 P 90 .
Es bien sabido que los hidrogeles con diferentes contenidos de agua poseen propiedades mecánicas completamente diferentes. Para caracterizar la influencia del contenido de agua en las propiedades mecánicas de los hidrogeles, se prepararon los hidrogeles con diferentes contenidos de agua como sigue. En primer lugar, la B x P 90 Los hidrogeles se prepararon según el procedimiento y los parámetros antes mencionados. Luego, la B x preparada P 90 los hidrogeles se expusieron al aire a temperatura ambiente durante diferentes tiempos dependiendo del contenido final de agua de los hidrogeles. Allí, los hidrogeles de secado obtenidos con diferentes contenidos de agua se etiquetaron como B x P 70 , B x P 50 y B x P 25 , respectivamente. El contenido de agua se calculó mediante la fórmula:contenido de agua = W w / W t , donde el W w es el peso del agua y W t es el peso total del hidrogel. Por otro lado, las densidades de reticulación de B x P 90 Los hidrogeles se calcularon a partir de los resultados de las mediciones reológicas, y es bien sabido que la mayor densidad de reticulación conduce a una propiedad mecánica más robusta. Para verificar la teoría, es indispensable realizar los ensayos de tracción. Sin embargo, la B x P 90 Los hidrogeles eran tan blandos que la máquina eléctrica universal de ensayo de materiales no puede reconocer la muestra sin carga, por lo que los hidrogeles compuestos con menor contenido de agua eran muy necesarios para fabricar. Los hidrogeles con diferentes contenidos de agua se cortaron en diferentes formas o tamaños para las siguientes pruebas.
Prueba mecánica
Con el fin de caracterizar las propiedades mecánicas de los hidrogeles, los hidrogeles preparados se cortaron en una forma escamosa (50 mm x 2 mm x 2 mm) y se probaron con la máquina eléctrica universal de prueba de materiales con una celda de carga de 200 N a una velocidad de 50 mm mínimo - 1 a 25 ° C y una humedad aproximada del 45%. La tensión de tracción ( σ ) que representa la fuerza se calculó mediante la ecuación: σ = F / ( a × b ), donde F , a y b Fueron la fuerza de carga y el ancho y espesor de los hidrogeles, respectivamente. La cepa ( ε ) que representa la capacidad de estiramiento se definió como el cambio de longitud, ilustrado por la fórmula: ε =( l - l 0 ) / l 0 × 100%, donde l y l 0 representan las longitudes después y antes de la prueba, respectivamente. La rigidez se caracterizó por el módulo de Young que se obtuvo de la pendiente de la curva tensión-deformación en las deformaciones bajas. La tenacidad de las muestras se ilustró como el área bajo las curvas de tensión-deformación. Los ensayos de tracción cíclica se realizaron en la misma condición experimental que tenía como objetivo obtener la energía disipada. La energía disipada se caracterizó por el área entre las curvas de carga y descarga y X -eje.
Caracterización
Los espectros de infrarrojos de transformada de Fourier (FTIR) se llevaron a cabo para registrar los caracteres FTIR de las muestras, que se registraron en un espectrómetro Thermo Scientific Nicolet 6700 en modo de reflexión total atenuada (ATR), con una resolución de 4 cm - 1 dentro del rango 400–4000 cm - 1 . La morfología de los hidrogeles después del proceso de secado por congelación se observó en micrografías electrónicas de barrido (SEM, Carl Zeiss AG, ZEISS EV0 MA15). Para analizar la viscoelasticidad de los hidrogeles y calcular la densidad de reticulación, las medidas reológicas se realizaron utilizando un reómetro (HAAKE MARS III Thermo Fisher Scientific Limited, China) para medir los módulos de almacenamiento (G ') y los módulos de pérdida (G ”). Los ensayos de tracción se llevaron a cabo para analizar las propiedades mecánicas de las muestras, que se realizaron utilizando una máquina de ensayo de materiales eléctrica universal con una celda de carga de 200 N (Instron 2360).
Resultados y discusión
El PAA / BNNS-NH 2 Los hidrogeles compuestos se formaron simplemente mediante la polimerización in situ de AA, con la presencia de Fe 3+ y el BNNS-NH 2 . Las cadenas macromoleculares de PAA así formadas se reticularon mediante interacciones jerárquicamente físicas:interacción de coordinación de metales entre carboxilos (–COOH) de PAA y Fe 3+ en escala molecular, y la interacción del enlace de hidrógeno entre –COOH del PAA y –NH 2 de BNNS-NH 2 en nanoescala, lo que da como resultado la formación de redes tridimensionales (esquema 1).
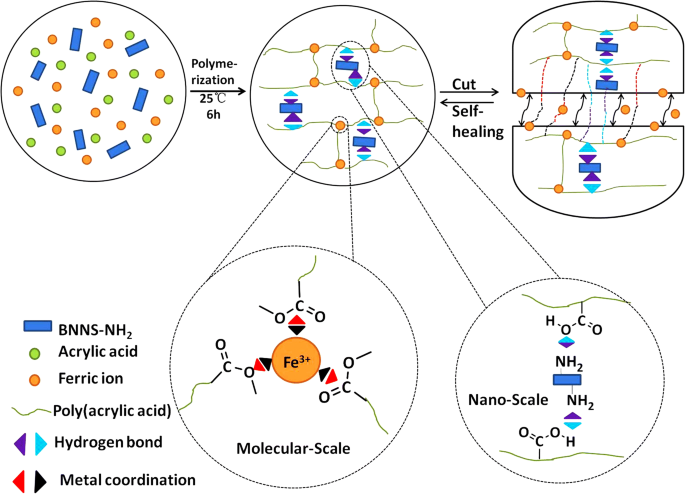
Esquema que ilustra la formación de un PAA / BNNS-NH 2 hidrogel compuesto con capacidad de autocuración
Los dos tipos diferentes de interacciones físicas dentro del PAA / BNNS-NH 2 Los hidrogeles compuestos fueron revelados por espectroscopia FTIR en primer lugar. A partir de los resultados de la Fig. 1, PAA muestra un estiramiento característico (-C =O estiramiento) a 1690 cm - 1 , que ha cambiado a 1620 cm - 1 en el PAA / BNNS-NH 2 hidrogel compuesto. Este cambio indica la existencia de interacciones de enlace de hidrógeno entre –COOH de PAA y –NH 2 de BNNS-NH 2 [30, 31]. La presencia de enlace de hidrógeno se puede verificar por el hecho de que los picos característicos a 3400 cm - 1 porque –COOH se volvió menos obvio en el hidrogel compuesto [32, 33]. El pico a 3230 cm - 1 se puede asignar a la vibración de estiramiento N – H en el hidrogel compuesto. La interacción de coordinación de metales fue revelada por el pico a 620 cm - 1 tanto en el hidrogel PAA como en el hidrogel compuesto, lo que demuestra que la interacción de coordinación de metales entre Fe 3+ y –COO - se formó en el sistema de red [34]. El B – N en el plano se extiende a 1388 cm - 1 y las vibraciones de flexión B-N-B fuera del plano a 1780 cm −1 puede verse en el hidrogel compuesto (Fig. 1a), lo que confirma la presencia de BNNS-NH 2 .
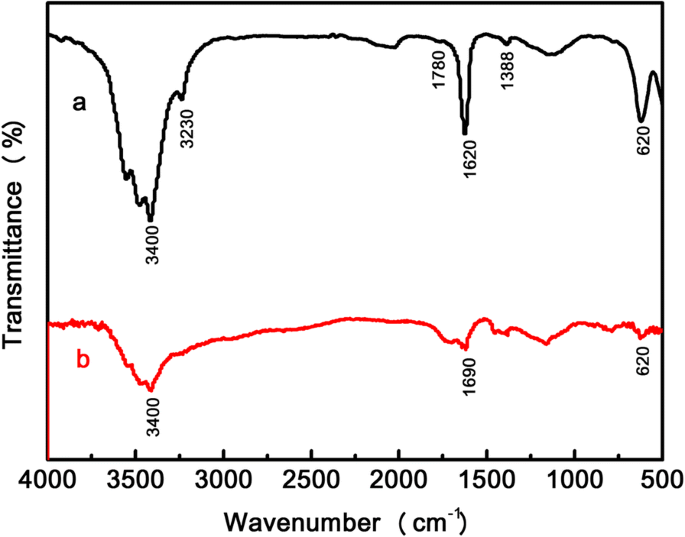
Espectros FTIR de a un hidrogel compuesto y b un hidrogel de PAA
Después del secado, se observaron las morfologías de estos hidrogeles mediante SEM. Se han observado estructuras porosas en hidrogel de PAA (Fig. 2a, b) y B x P y hidrogel compuesto (Fig. 2c). Los poros más grandes tienen un diámetro promedio de alrededor de docenas de micrómetros y los poros más pequeños tienen un diámetro promedio en nanoescala. La presencia de poros puede proporcionar una alta capacidad de estiramiento y compresión de los hidrogeles [35]. En comparación con los hidrogeles de PAA, los poros dentro del hidrogel compuesto son más aislados y de tamaño uniforme (Fig. 2c). Y el BNNSs-NH 2 se puede observar en una imagen SEM (Fig. 2d) de hidrogel que contiene BNNSs-NH 2 y fueron señalados por flechas, y la imagen insertada verificó aún más la presencia de BNNS-NH 2 [34]. Para comprender los efectos de las interacciones de dos tipos, pruebas de tracción de hidrogeles compuestos con diferentes BNNS-NH 2 Se llevaron a cabo concentraciones y los resultados de estos hidrogeles con diferentes contenidos de agua se muestran en la Fig. 3a-c. Sin BNNS-NH 2 , la tensión de fractura de B 0 P 70 hidrogel era de aproximadamente 406 kPa, y la tensión de fractura de B 0.1 P 70 aumentado a 526 kPa mediante la introducción de una pequeña cantidad de BNNS-NH 2 . El B 0.5 P 70 exhibe una tensión de fractura de 1311 kPa, casi tres veces a B 0 P 70 y dos veces a B 0.1 P 70 , como se muestra en la Fig. 3a. El resultado superó con creces los hidrogeles compuestos previos en trabajos publicados [34]. Esto significa que el enlace de hidrógeno formado entre –COOH de PAA y –NH 2 de BNNS-NH 2 mejoró significativamente las propiedades mecánicas [36]. Sin embargo, la tensión de la fractura disminuyó cuando el BNNS-NH 2 la concentración siguió aumentando. La tensión de fractura es incluso menor que la de B 0 P 70 , que indicó que se logró un equilibrio primordial de interacciones de coordinación de metales y enlaces de hidrógeno en el BNNS-NH 2 concentración de 0.5 mg mL - 1 . En consecuencia, las mayores tensiones de fractura también se realizaron en el mismo BNNS-NH 2 concentración (0.5 mg mL - 1 ) dentro de hidrogeles compuestos con un contenido de agua de 50% en peso y 25% en peso (Fig. 3b, c) que fue un factor importante para afectar las propiedades mecánicas del hidrogel [37, 38]. Las tensiones de fractura de los hidrogeles compuestos mejoraron notablemente (archivo adicional 1:Figura S1-S5) cuando el contenido de agua disminuyó al 50% en peso y al 25% en peso, atribuido al estrecho espacio entre cadenas con bajo contenido de agua [35]. En particular, la B x P y los hidrogeles pudieron resistir la tracción, los nudos, la flexión y la torsión incluso bajo un alto grado de deformaciones (Fig. 3d-g, archivo adicional 1:Figura S6). La adición de BNNS-NH 2 podría cambiar ligeramente el pH de la solución debido a la presencia de –NH 2 grupos, lo que lleva a un cambio en la constante de asociación entre –COOH y Fe 3+ . El equilibrio entre las interacciones de coordinación de metales y los enlaces de hidrógeno dependía del BNNS-NH 2 concentración con el contenido constante de Fe 3+ . Los excelentes comportamientos mecánicos del hidrogel compuesto se derivaron del equilibrio óptimo entre la interacción de coordinación de metales a escala molecular y las interacciones de enlace de hidrógeno en nanoescala [36].

Imágenes SEM de a , b Hidrogel de PAA y c , d hidrogel compuesto. El BNNS-NH 2 fue señalado por flechas en ( d ) y la imagen insertada en ( d ) es la imagen ampliada del BNNS-NH 2
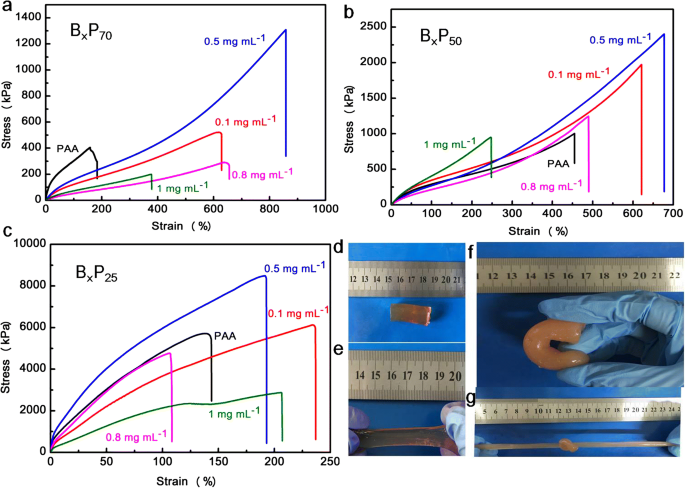
Curvas de tensión-deformación de los hidrogeles compuestos: a B x P 70 , b B x P 50 y c B x P 25 . La fotografía digital de hidrogeles compuestos: d original, e estirado, f doblada y g estirado después de ser anudado
Los efectos de BNNS-NH 2 concentración en las propiedades mecánicas de B x P 90 fueron estudiados por medición reológica (Fig. 4a). Para todas las muestras, sus módulos de almacenamiento (G ’) son siempre más altos que los correspondientes módulos de pérdida (G”) en el rango de frecuencia de 0,1 a 100 rad s - 1 , que indica la formación de redes tridimensionales [34, 36]. Con el aumento de frecuencia, tanto G ’como G” aumentaron, pero el aumento de G ”es más agudo, mostrando sus comportamientos de corte fino [34]. B 0.5 P 90 exhibió el G 'más alto, que es consistente con los resultados de las pruebas de tracción. A partir del módulo de corte de equilibrio ( G e ), densidad de reticulación ( N ) de estos hidrogeles se pueden calcular utilizando la fórmula 1 [39,40,41].
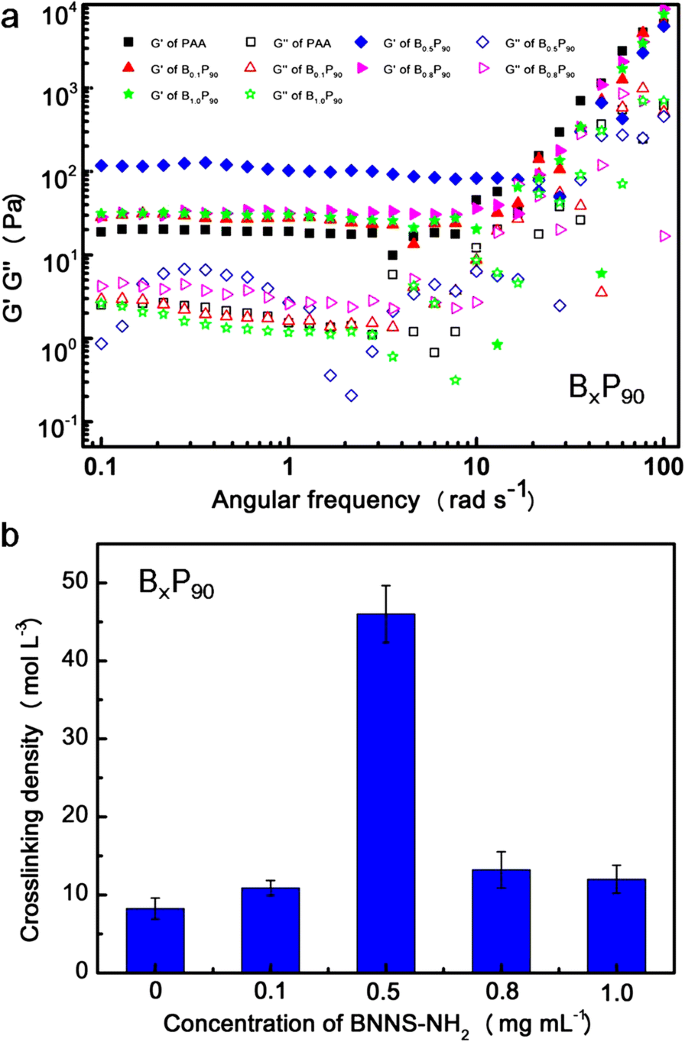
un Dependencia de la frecuencia de los módulos de almacenamiento (G ’) y los módulos de pérdida (G”) de B x P 90 a una deformación del 0,1%. b Densidad de reticulación de B x P 90 calculado por el módulo de corte de equilibrio
$$ N =Ge / (RT) $$ (1)Aquí, G e , R y T son el valor de terraza de G ', la constante de gas y la temperatura absoluta, respectivamente. La densidad de reticulación se muestra en la Fig. 4b. Con aumento de la concentración de BNNS-NH 2 , la densidad de reticulación aumentó, lo que demuestra que BNNS-NH 2 también sirvió como reticulante en los hidrogeles compuestos a través de interacciones de enlace de hidrógeno entre –COOH de PAA y –NH 2 de BNNS-NH 2 . Sin embargo, la densidad de reticulación disminuyó cuando el BNNS-NH 2 la concentración es superior a 0,5 mg mL - 1 que se correspondía con los resultados de las propiedades mecánicas [40]. Se ilustra que el exceso de BNNS-NH 2 conduce a la reunión de las nanohojas, lo que perjudica la mejora de los hidrogeles compuestos como B 0.8 P y y B 1.0 P y [41, 42].
Para obtener hidrogeles con excelentes propiedades mecánicas, se puede lograr el equilibrio óptimo de interacciones de enlace de hidrógeno e interacciones de coordinación de metales ajustando el BNNS-NH 2 concentraciones mientras que el contenido de Fe 3+ es constante. La tenacidad y el módulo de Young que representa la rigidez se muestran en la Fig. 5a y la Fig. 5b, respectivamente [24, 36, 37]. De la Fig. 5a, los hidrogeles se volvieron rígidos con la disminución del contenido de agua o el aumento de BNNS-NH 2 concentración hasta 0.5 mg mL - 1 coherente con los resultados de la prueba de tracción (archivo adicional 1:Figura S7).
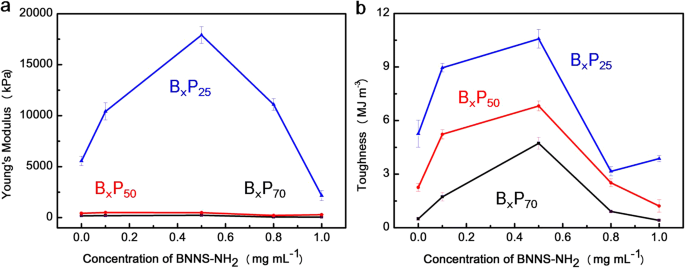
un Módulo de Young y b tenacidad de hidrogeles compuestos con diferentes contenidos de agua y BNNS-NH 2 concentraciones
La tenacidad se observa en la Fig. 5b. Está claro que la tenacidad aumenta con la disminución del contenido de agua, similar a la tendencia del módulo de Young. Sin BNNS-NH 2 , la dureza de B 0 P 70 fue de aproximadamente ~ 0,5 MJ m - 3 y con BNNS-NH 2 , la dureza de B 0.5 P 70 aumentado a ~ 4,7 MJ m - 3 , casi ocho veces superior al de B 0 P 70 . El B 0.5 P 25 exhibió el módulo de Young más alto de ~ 17,9 MPa, la resistencia a la tracción más alta de ~ 8491 kPa y la tenacidad más alta de ~ 10,5 MJ m - 3 , que es mucho más alto que el de B 0 P 25 .
La rigidez de la mayoría de los hidrogeles poliméricos disminuye con el aumento de la correspondiente tenacidad. Según el modelo de Lake-Thomas [42, 43], la tenacidad aumenta pero la rigidez disminuye al disminuir la densidad de reticulación. En este trabajo, un nuevo tipo de hidrogel con alta rigidez y alta tenacidad (B 0.5 P y ) (Fig.5), que es diferente a los hidrogeles convencionales (alta rigidez / baja tenacidad o baja rigidez / alta tenacidad). Las propiedades excepcionales se pueden atribuir a la existencia de interacciones jerárquicas:interacciones de coordinación de metales en escala molecular y enlaces de hidrógeno en nanoescala.
Ensayos cíclicos de tracción de B x P 70 y B x P 50 se realizaron a una deformación del 200% (Fig. 6a, b). Se observaron bucles de histéresis obvios para B x P 70 y B x P 50 y B x P 50 mostraron bucles de histéresis mucho más grandes, lo que indica que el contenido de agua determina la disipación de energía debido a que se establecen más enlaces de hidrógeno entre las cadenas de polímeros debido a las redes encogidas [37]. La energía disipada aumentó con el aumento de BNNS-NH 2 concentración, y el valor máximo se obtuvo a la concentración de 0.5 mg mL - 1 debido al establecimiento de numerosos enlaces de hidrógeno entre BNNS-NH 2 y cadenas PAA [34]. Sin embargo, la energía disipada disminuyó cuando BNNS-NH 2 concentración aumentada a 0,8 y a 1,0 mg mL - 1 , debido a la alta concentración de BNNS-NH 2 lo que lleva a la agregación de las nanohojas [41, 42]. Esta explicación también es adecuada para curvas de tensión-deformación específicas y resultados de reología de B x P y hidrogeles.
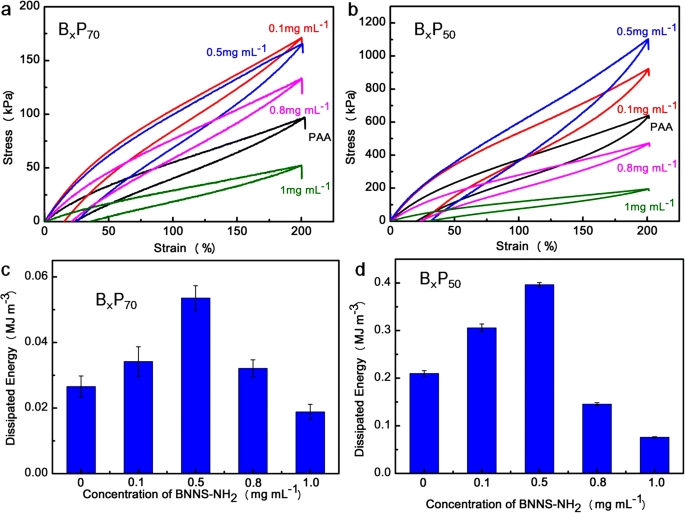
Tracción cíclica de las curvas de carga-descarga de a B x P 70 y b B x P 50 ; la energía disipada de c B x P 70 y d B x P 50
El rápido proceso de autocuración se puede realizar sin ningún estímulo externo basado en las abundantes interacciones físicas:interacciones de coordinación de metales y enlaces de hidrógeno. Como se muestra en la Fig. 7a-c, el hidrogel original se cortó en tres partes (dos partes se tiñeron de rojo con rodamina B para distinguir las cicatrices del hidrogel dañado) y luego se pusieron en contacto con las superficies dañadas. Sin ningún estímulo externo, el hidrogel cortado se puso en contacto durante 10 minutos a temperatura ambiente, el hidrogel curado se puede estirar a cierta tensión. La eficacia de autorreparación se puede calcular a partir de la relación entre la tensión de fractura de los hidrogeles curados y los hidrogeles originales. Original B 0 P 70 exhibió una tensión de fractura de ~ 410 kPa, y el hidrogel curado correspondiente exhibió una tensión de fractura de solo ~ 37 kPa, lo que indica que la eficiencia de autocuración fue solo del 9%. En comparación, la tensión de fractura del B 1 original y curado P 70 eran aproximadamente ~ 203 kPa y ~ 166 kPa, respectivamente, y la eficiencia de autorreparación es de aproximadamente 81%, que es significativamente más alta que los hidrogeles sin el BNNS-NH 2 . De manera similar, como se muestra en la Fig. 7e, la eficiencia de autocuración de B 0 P 50 hidrogel fue del 31,8%, mientras que el B 1 P 50 hidrogel fue del 94,6%. Este resultado indica que la presencia de enlaces de hidrógeno a nanoescala entre BNNS-NH 2 y las cadenas de polímero PAA en nanoescala mejoraron la capacidad de autocuración atribuyendo que el contenido de enlaces reversibles es el factor de influencia clave de la eficacia de autocuración, y es bien sabido que la eficacia de autocuración es proporcional al contenido de la reversible enlaces [16, 21, 36, 42]. Sin embargo, mientras que el contenido de agua se redujo al 25% en peso (archivo adicional 1:Figura S8), la eficiencia de autocuración disminuyó drásticamente debido al movimiento de Fe 3+ se impidió con un contenido de agua tan bajo. Esta suposición fue confirmada por el hecho de que la eficacia de curación de B x P 90 fue mucho mejor que otro contenido de agua, con solo 10 minutos requeridos atribuidos a la razón de que los contenidos de agua más altos hacen que el Fe 3+ para migrar fácilmente y restablecer enlaces de hidrógeno fácilmente [36].
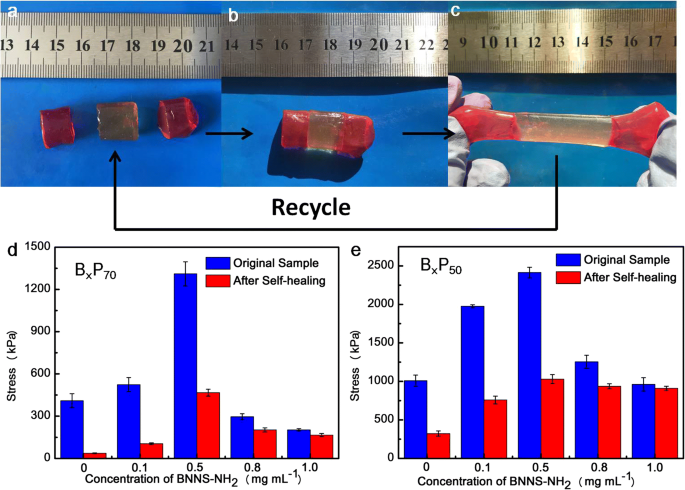
Proceso de autocuración de B 0.5 P 90 ( a ) el hidrogel se cortó en tres partes (las dos partes terminales se tiñeron de rojo con rodamina B). b Ponga estrictamente las tres partes juntas una por una. c Después de 10 minutos de curación, el hidrogel curado se puede estirar. d Las tensiones de fractura del B x original P 70 y sanó a B x P 70 . e Las tensiones de fractura del B x original P 50 y sanó a B x P 50. El tiempo de curación fue de 1 h
Conclusiones
En resumen, los nuevos hidrogeles compuestos se han fabricado a través de interacciones jerárquicamente físicas:la interacción de coordinación de metales en escala molecular y el enlace de hidrógeno en nanoescala. Los hidrogeles exhiben una rigidez mejorada (aproximadamente 17,9 MPa), tenacidad (aproximadamente 10,5 MJ m - 3 ), extensión y capacidad de autocuración. La reversibilidad de la interacción de coordinación de metales y la interacción de enlaces de hidrógeno es responsable de las propiedades mecánicas mejoradas y la eficiencia de autocuración. Combinados con una preparación fácil, propiedades mecánicas mejoradas y capacidad de autocuración hacen que estos hidrogeles compuestos sean adecuados para muchas aplicaciones potenciales.
Abreviaturas
- B x P y :
-
Hidrogel compuesto con BNNS-NH 2 concentración de x mg mL - 1 y contenido de agua de y % en peso
- Fe 3+ :
-
Ión férrico
- FTIR:
-
Infrarrojos por transformada de Fourier
- PAA / BNNS-NH 2 :
-
Nanohojas de poli (ácido acrílico) / nitruro de boro de superficie modificada
- PAA / GO:
-
Óxido de grafeno / poli (ácido acrílico)
- SEM:
-
Escaneo de micrografías electrónicas
Nanomateriales
- Propiedades y aplicaciones del tantalio
- Síntesis y propiedades electroquímicas de materiales de cátodo LiNi0.5Mn1.5O4 con dopaje compuesto Cr3 + y F− para baterías de iones de litio
- Síntesis fácil de compuesto de CuSCN coloreado y conductor recubierto con nanopartículas de CuS
- Fabricación sencilla de un compuesto de polianilina poroso multi-jerárquico como sensor de presión y sensor de gas con sensibilidad ajustable
- Propiedades eléctricas de materiales compuestos con alineación asistida por campo eléctrico de rellenos de nanocarbono
- Estabilidad mejorada de nanopartículas magnéticas de oro con poli (ácido 4-estirenosulfónico-ácido co-maleico):propiedades ópticas personalizadas para la detección de proteínas
- Síntesis de calentamiento de estado sólido de compuesto de poli (3,4-etilendioxitiofeno) / oro / grafeno y su aplicación para la determinación amperométrica de nitrito y yodato
- Fabricación, caracterización y actividad biológica de sistemas de nanoportación de avermectina con diferentes tamaños de partículas
- Dependencia de la toxicidad de las nanopartículas en sus propiedades físicas y químicas
- Morfología, estructura y propiedades ópticas de películas semiconductoras con nanoislinas GeSiSn y capas tensas
- Propiedades de los materiales de ingeniería:generales, físicas y mecánicas



