Películas delgadas de óxido de vanadio amorfo como cátodos de rendimiento estable de baterías de iones de litio y sodio
Resumen
Aquí, informamos óxido de vanadio amorfo prístino libre de aditivos y aglutinantes (a-VOx) para aplicaciones de baterías de iones de litio y sodio. Se cultivan películas delgadas de a-VOx con un espesor de aproximadamente 650 nm sobre un sustrato de acero inoxidable a partir de V 2 cristalino O 5 objetivo utilizando la técnica de deposición por láser pulsado (PLD). Bajo presión parcial de oxígeno variable (pO 2 ) en un entorno de 0, 6, 13 y 30 Pa, las películas tienen relaciones atómicas O / V de 0,76, 2,13, 2,25 y 2,0, respectivamente. Las películas depositadas a 6‑30 Pa tienen un porcentaje más atómico de V 5+ que el de V 4+ con una tendencia a un estado posterior aumentado a medida que pO 2 sube. Películas de VOx amorfa obtenidas a pO 2 moderada los niveles son superiores a otros equivalentes para la aplicación de cátodos en baterías de iones de litio y de sodio con capacidades reversibles de hasta 300 y 164 mAh g −1 a una tasa de corriente de 0,1 C, respectivamente. Al final del ciclo 100, se observa una retención de capacidad del 90% en ambos casos. La tendencia de ciclismo observada sugiere que más es el (V 5+ ) La naturaleza estequiométrica de a-VOx mejor es la electroquímica.
Introducción
Los óxidos de vanadio amorfo (a-VOx) se están volviendo cada vez más populares para la aplicación de dispositivos electrónicos [1, 2], baterías secundarias de iones de litio y post-litio [3,4,5,6,7,8,9,10, 11,12,13]. En comparación con sus homólogos cristalinos, a-VOx podría ofrecer trayectos de difusión más cortos y, a su vez, una cinética de litiación fácil que facilita el logro de capacidades teóricas en condiciones prácticas. Óxidos cristalinos como V 2 O 5 poseer la capacidad teórica de ingesta de litio hasta 441 mAh g −1 (1 C). En la práctica, esta capacidad teórica representa 3 mol de Li que deben descargarse a 1,5 V. Pero la formación de ω-Li x irreversible V 2 O 5 fase cuando se descarga por debajo de 1,9 V limita la capacidad reversible a 2 mol de Li solamente [8]. Por esta razón, el cristalino V 2 O 5 debe ciclarse dentro de una ventana de voltaje de 4.0–2.0 V que corresponde a la capacidad teórica 292 mAh g −1 . Por tanto, a pesar de la enorme capacidad teórica, los óxidos de vanadio cristalinos exhiben menores capacidades experimentales. En este contexto, los materiales a-VOx surgieron como cátodos de alta capacidad que están libres de formaciones de fase irreversibles y, por lo tanto, superan la restricción de voltaje de operación [5, 8]. Por ejemplo, sol-gel sintetizó amorfo V 2 O 5 · x H 2 O ( x =2–2,3) exhibieron una alta capacidad reversible de 410 mAh g −1 a una tasa actual de C / 8 [14]. En un informe reciente, la película a-VOx electrodepositada como cátodo de la batería de iones de sodio (SIB) se desempeñó mejor que su contraparte cristalina con el doble de capacidad (241 mAh g −1 ) [10]. Sin embargo, en estos dos casos, la estabilidad del ciclismo no es buena. A finales de la década de 1990, Zhang et al. y McGraw et al. informó de películas a-VOx preparadas por deposición de láser pulsado (PLD) con una capacidad específica de 346 mAh g −1 en el ciclo 100 en el rango de voltaje de 1,5 a 4,1 V y a una tasa de corriente de 0,1 mA cm −2 [3, 4]. Sin embargo, en estos casos, la contribución colectiva del conductor SnO 2 el sustrato que es electroquímicamente activo a la alta capacidad sigue siendo desconocido. La película de a-VOx de aproximadamente 450 nm de espesor preparada por deposición química de vapor en capa atómica (ALCVD) promocionaba una buena estabilidad cíclica a una velocidad de 0,1 C con una capacidad reversible de 275 mAh g −1 al final del 100º ciclo [6]. Una película a-VOx de 30 nm de espesor cultivada por ALD exhibió un rendimiento cíclico superior que los materiales amorfos antes discutidos con una capacidad de ciclo 100 de 330 mAh g −1 a una tasa de 1 C entre 1,5 y 4,0 V [7]. Se observó un comportamiento cíclico similar para las películas de VOx casi amorfas depositadas por ALD con una capacidad de alrededor de 60 mAh g −1 a una tasa de 1 C en el rango de voltaje de 2,75–3,8 V [14]. En un estudio reciente, a-VOx depositado electroquímicamente en papel de grafito como cátodo para una batería de iones de sodio mostró una ciclabilidad superior que la contraparte cristalina a corrientes específicas más bajas en el rango de 80-320 mA g −1 [11]. Por lo tanto, los óxidos de vanadio amorfos son superiores a los cristalinos para las aplicaciones de almacenamiento de energía electroquímica. Sin embargo, hasta donde sabemos, no existe un estudio completo sobre el funcionamiento catódico de a-VOx prístino que correlacione ampliamente el rendimiento con propiedades fundamentales clave como el grado de amorfización, estequiometría y coordinación de oxígeno a vanadio. Tal estudio fue iniciado por Julien et al. en 1999 para obtener amorfo V 2 O 5 películas delgadas por PLD en pO 2 ~ 13,33 y 19,995 Pa ya una temperatura del sustrato de 300 ° C que es demasiado alta para obtener la fase amorfa [15]. A esta temperatura, V 2 amorfo O 5 La formación de fase probablemente no es posible ya que está muy por encima de 200 ° C, que es un límite de temperatura mínima ampliamente aceptado para obtener la fase cristalina [16,17,18,19,20,21]. El análisis detallado de la composición elemental y química (XPS) del V 2 amorfo así reivindicado O 5 fase necesita ser estudiada. La electroquímica de litiación presentada de V 2 O 5 depositado a 300 ° C sobre sustratos de vidrio o silicio confirma que las películas eran realmente cristalinas al visualizar mesetas claras de intercalación de Li de larga duración (~ 35 h) alrededor de 2.6 V.Además, presentó electroquímica medida sobre vidrio y Si natural aislante perfecto (incluyendo V 2 O 5 película) sustratos sin un colector actual adecuado plantean ambigüedad al considerarlo para compararlo con otras obras similares. Sin embargo, en comparación con el presente estudio PLD a-VOx, no se discutió la electroquímica de litiación o sodiación de la fase amorfa. Por lo tanto, optamos por estudiar películas de a-VOx depositadas con láser pulsado que crecen a diferentes presiones parciales de oxígeno (pO 2 ) para aplicaciones de baterías de iones de litio y de sodio.
La naturaleza física y química de las películas PLD se puede adaptar fácilmente controlando el gas de oxígeno reactivo. Se informará de un estudio sistemático de dichos parámetros de control y de las consecuencias sobre la propiedad final. Este estudio es muy importante para explorar los aspectos fundamentales en función de la estequiometría variable del oxígeno. La deposición por láser pulsado es una de las mejores formas de estudiar las propiedades electroquímicas fundamentales de a-VOx en su estado prístino. Además, no hay necesidad de aditivos como carbón y aglutinantes. Además, las impurezas químicas como las moléculas de agua que ocupan sitios de celosía o los hidroxilos superficiales que emergen durante el proceso de síntesis química húmeda podrían evitarse mediante PLD. Además, las impurezas químicas podrían causar una pérdida considerable de capacidad o plantear ambigüedad en las características electroquímicas exactas. Por ejemplo, electrodepositado a-VOx · n H 2 O [10], a-V 2 O 5 [11] y V 2 templado en estado fundido O 5 · n H 2 Los compuestos de O xero-gel [22] como cátodos de SIB exhibieron características de inserción y deserción de sodio totalmente diferentes y asimétricas que en el presente estudio. Además, a-VOx · n H 2 O [10] y V 2 O 5 · n H 2 Los compuestos de O [22] entregaron altas capacidades iniciales que rápidamente decayeron a las capacidades estables obtenidas a lo largo del ciclo en el presente estudio. Una disminución tan rápida de la capacidad podría surgir plausiblemente de la interacción de especies de hidroxilo con iones de Na y / o con moléculas de electrolito para formar compuestos covalentes irreversibles. Por lo tanto, en el presente estudio, las películas a-VOx preparadas por PLD se investigan por sus propiedades físicas y químicas en correlación con la electroquímica de litiación y sodiación. Los resultados obtenidos se comparan con la literatura disponible así como con V 2 comercial O 5 polvo a granel cuyos electrodos se fabricaron mediante la adición de carbón y aglutinante.
Métodos
Deposición de película delgada
Las películas de óxido de vanadio se depositaron usando V 2 cristalino O 5 como objetivo de PLD. Láser excimer KrF de alta energía ( λ =248 nm) se centró en la superficie de V 2 O 5 objetivo, con una potencia de ~ 200 mJ y repetición de 5 Hz. Las películas de VOx amorfo se cultivaron en un sustrato de acero inoxidable de grado 304 (SS) precalentado a 100 ° C y bajo diferentes presiones parciales de oxígeno (pO 2 ). La distancia entre el sustrato y el objetivo se mantuvo en ~ 5 cm. La deposición se llevó a cabo a alto vacío de 0,6 × 10 −5 mbar al principio, y luego se introdujo gas oxígeno equivalente a pO 2 ~ 6, 13 y 30 Pa. Cada película se depositó durante 44 min que dio como resultado un espesor de aproximadamente 650 nm. Para una próxima discusión, estos cuatro tipos de películas se abrevian como a-VOx-0 Pa, a-VOx-6 Pa, a-VOx-13 Pa y a-VOx-30 Pa.
Caracterización
Las micrografías electrónicas y la composición elemental (EDAX) de las películas se obtuvieron con un microscopio electrónico de barrido por emisión de campo JEOL 7600F (FESEM) que operaba a un voltaje de aceleración de 5 kV. La caracterización estructural y de fase se realizó con Bruker D8 Advance XRD con radiación Cu-Ka ( λ =1,54 Å) que funcionaba a 40 kV y 40 mA. Las imágenes del microscopio de fuerza atómica (AFM) se obtuvieron de un AFM comercial (Asylum Research MFP3D), utilizando puntas Asylum Research AC240TM (recubiertas de Pt / Ti, 70 kHz y 2 N / m). La espectroscopia de fotoelectrones de rayos X (XPS) se realizó con una fuente de radiación de rayos X monocromática de Mg en un espectrómetro Phoibos (SPECS, Alemania). Los espectros de levantamiento de alta resolución se analizaron con el paquete de software Casa XPS.
Caracterización electroquímica
Las películas depositadas se utilizaron como cátodos para fabricar pilas de botón CR2016 con metal de Li y Na como contraelectrodos. Como separador se utilizó papel de filtro de microfibras de vidrio Whatman. Un molar LiPF 6 en carbonato de etileno (EC) y carbonato de dietilo (DEC) (1:1 en volumen) se utilizó como electrolito para baterías de iones de litio (LIB). Un molar de NaClO 4 en carbonato de propileno (PC) con 5% de carbonato de fluoroetileno (FEC) como electrolito para fabricar SIB. La fabricación de pilas de monedas se llevó a cabo dentro de una caja de guantes llena de gas Ar donde los niveles de humedad y oxígeno se limitaron estrictamente a menos de 0,1 ppm.
La prueba de la batería se llevó a cabo a temperatura ambiente después de 8 h de relajación. Las medidas de voltamperometría cíclica (CV) para LIB y SIB se llevaron a cabo en el rango de voltaje de 1,5 a 4,0 V a una velocidad de exploración de 0,1 mV s −1 utilizando equipo SOLARTRON 1470E. Las pruebas de carga-descarga galvanostática (GC) se llevaron a cabo en el mismo rango de voltaje que en el caso de las mediciones de CV y a una tasa de corriente de 0.1 a 10.0 C usando el sistema de prueba de batería NEWARE. Aquí, 1 C =294 y 441 mA g −1 para ventanas de voltaje 2.0–4.0 y 1.5–4.0 V, respectivamente, para LIB. En caso de SIB, 1 C =236 mA g −1 para un rango de voltaje de 1,5–4,0 V. Las mediciones de espectroscopia de impedancia electroquímica (EIS) se llevaron a cabo en el rango de frecuencia de 100.000–0,01 Hz y con una amplitud de voltaje de 10 mV utilizando el Analizador de respuesta de frecuencia, Solartron Analytical 1400 CellTest System.
Resultados y discusión
Caracterización física y química
La morfología física de las películas depositadas observadas bajo FESEM es como se muestra en la Fig. 1. La película a-VOx-0 Pa (Fig. 1a) es suave y continua pero se asemeja al sustrato de acero inoxidable desnudo (Archivo adicional 1:Figura S11) que posee trincheras en la superficie. En la Fig. 1b, también se encuentra que la película a-VOx-6 Pa es continua pero con muchas partículas esféricas acumuladas. Se observan características similares en el caso de la película a-VOx-13 Pa (Fig. 1c) pero es totalmente diferente de las otras dos películas al tener grandes límites de grano de varias decenas de micras de tamaño. En común, estas tres películas son muy transparentes al haz de electrones, ya que las marcas de arañazos en el acero inoxidable desnudo son claramente perceptibles. A diferencia de estas tres películas, a-VOx-30 Pa es opaca y discontinua (Fig. 1d). Posee límites de grano de tamaño submicrónico muy pequeños y partículas de forma aleatoria muy grandes del orden de 10 μm de longitud. En un sistema PLD típico, un láser de alta energía golpea la superficie del objetivo y provoca la evaporación de los materiales del objetivo, que forma la columna activa (es decir, la mezcla de especies energéticas como átomos, moléculas, electrones e iones) y luego el crecimiento de películas delgadas sobre los sustratos. Durante la deposición, pO 2 afecta en gran medida la colisión y la reacción entre la columna y los átomos de oxígeno y, por lo tanto, la forma y el tamaño de la columna. Por lo tanto, el modo de crecimiento, la tasa de deposición y la homogeneidad de la película delgada dependen de pO 2 [23, 24]. En general, pO 2 más alta conduce a la atenuación y ralentización de la pluma, lo que da como resultado un tamaño de grano más grande y una película más áspera [25]. En nuestro caso, cuando pO 2 se fija en 30 Pa, la rugosidad de la película VOx es demasiado grande (no reflectante) y algunos de los granos están aislados, por lo que la película presenta una topografía opaca y no continua. Las composiciones elementales de las películas a-VOx obtenidas mediante la técnica EDAX se enumeran en la Tabla 1. La deposición de la película al vacío dio como resultado una relación atómica O / V muy pobre y, por esta razón, la película a-VOx-0 Pa se omitió del análisis adicional. A continuación, la relación O / V aumenta a 2,135 con la introducción de oxígeno en la cámara de deposición que es equivalente a 6 Pa. Como se muestra en la Tabla 1, no hay un aumento significativo en la relación O / V incluso después de duplicar el oxígeno a 13 Pa. Un aumento adicional de oxígeno a un nivel muy alto de 30 Pa redujo la relación O / V a 2,003. La relación O / V sin cambios o disminuida podría haber tenido lugar de manera plausible a partir de un cambio en la propiedad de transporte, como la reducción en el camino libre medio ( λ ) de las especies de oxígeno con pO 2 en aumento ( λ α 1 / pO 2 ) [26].

Micrografías electrónicas de barrido por emisión de campo de películas a-VOx depositadas en pO 2 ( a ) 0 Pa, ( b ) 6 Pa, ( c ) 13 Pa y ( d ) 30 Pa
Los patrones de XRD de todas las películas son similares y contienen picos correspondientes al acero inoxidable solo como se muestra en el archivo adicional 1:Figura S12. Esto confirma claramente que todas las películas son únicamente amorfas. La topografía de la superficie AFM de las películas a-VOx como se muestra en la Fig. 2 cumple bien con la morfología física observada en las micrografías electrónicas (Fig. 1). Las películas a-VOx-6 Pa (Fig. 2a) y a-VOx-13 Pa (Fig. 2b) tienen características superficiales similares y son lisas de acuerdo con sus respectivas micrografías electrónicas. Por otro lado, la superficie de la película a-VOx-30 Pa (Fig. 2c) es muy rugosa e irregular en contraste con las otras dos películas. La rugosidad media medida en un escaneado de 3 × 3 μm es ~ 8,6, ~ 9,2 y ~ 24 nm para las películas a-VOx-6 Pa, a-VOx-13 Pa y a-VOx-30 Pa, respectivamente. Por lo tanto, un aumento en la presión parcial de oxígeno no solo aumenta la rugosidad de la superficie sino que también induce un cambio en la morfología como se observa en las micrografías de FESEM.
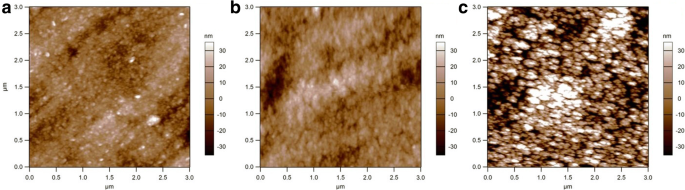
Topografía de superficie AFM de a-VOx-6 Pa ( a ), a-VOx-13 Pa ( b ) y a-VOx-30 Pa ( c )
Los espectros XPS de alta resolución de las películas a-VOx-6, a-VOx-13 y a-VOx-30 Pa que comprenden el doblete V 2p característico y los picos del nivel del núcleo de O 1s se muestran en la Fig. 3. Las características y posiciones de cada pico se superpone entre sí en los tres casos con una ligera variación en los recuentos de intensidad. Los picos de V2p 3/2 , V2p 1/3 y los O 1 se encuentran centrados en 517,30, 524,8 y 530,2 eV, respectivamente, y concuerdan bien con el trabajo informado [6, 10, 11]. Entre las tres películas, la película a-VOx-30 Pa posee una masa ligeramente mayor que las otras dos y, por lo tanto, su espectro mostró recuentos de intensidad más altos (Fig. 3a. Las películas a-VOx-6 Pa y a-VOx-13 Pa tienen mostró los mismos recuentos de intensidad que están en gran acuerdo con la relación atómica V / O casi igual observada en los hallazgos de EDAX. Un examen detallado de V2p 3/2 región reveló una diferencia sustancial en estas tres películas que se enumeran en la Tabla 2. Cada V 2p 3/2 el espectro se deconvoluciona aún más en dos picos correspondientes a V 5+ (verde) y V 4+ (azul) estados de oxidación (Fig. 3b – d). En los tres casos, At% de V 5+ (~ 68–64%) se encuentra mayor que V 4+ (~ 32–36%). Como se indica en la Tabla 2, en% de V 5+ disminuyó continuamente al aumentar la pO 2 . Al% de V 5+ se observa una disminución de aproximadamente 0.35% y 4.7% cuando pO 2 aumentó de 6 a 13 Pa y de 6 a 30 Pa, respectivamente. La tendencia cambiante en At% de V 4+ se encuentra exactamente opuesto e igual a V 5+ estado de oxidación. Por lo tanto, mayor pO 2 el entorno dice que por encima de 13 Pa parece crear más V 4+ estado, es decir, más deficiencia de oxígeno. Estos cambios observados en At% son muy consistentes con las variaciones de la relación atómica O / V observadas en el análisis EDAX. Por lo tanto, el análisis general de XPS se complementa bien con las inferencias de EDAX.
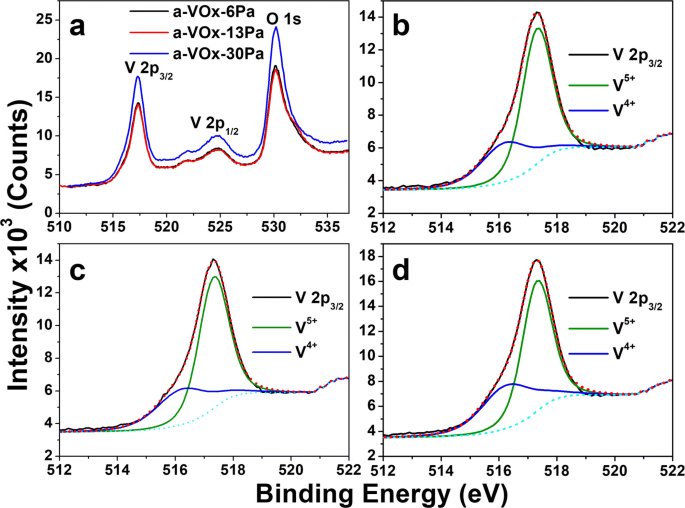
Espectros XPS de alta resolución de películas a-VOx ( a) Nivel de núcleo O 1s y V 2p; V 2p 3/2 de ( b ) a-VOx-6 Pa, ( c ) a-VOx-13 Pa y ( d ) a-VOx-30 Pa
Caracterización electroquímica
Resultados de la batería de iones de litio
Los resultados de la prueba LIB de las películas depositadas a-VOx-6 Pa, a-VOx-13 Pa y a-VOx-30 Pa se muestran en la Fig. 4 y en el archivo adicional 1:Figura S13. Entre las tres, las películas a-VOx-6 Pa demostraron un rendimiento excelente con altas capacidades reversibles y ciclos estables en ambas ventanas de voltaje, 2.0–4.0 y 1.5–4.0 V. Las características CV de a-VOx-6 Pa se asemejaron al comportamiento pseudocapacitivo en ambos ventanas de voltaje (Fig. 4a, c). Las reacciones faradaicas rápidas debidas al proceso de adsorción y desorción de la superficie del litio son las principales responsables del comportamiento pseudocapacitivo [10]. Aquí, los picos de corriente irreversibles observados hasta el quinto ciclo se originan principalmente en el sustrato de acero inoxidable (archivo adicional 1:Figura S14) con la menor contribución de la descomposición de electrolitos que conduce a la formación de interfase de electrolitos sólidos (SEI). Las firmas de (des) intercalación de iones de litio están totalmente ausentes en comparación con el V 2 cristalino a granel O 5 como se muestra en el archivo adicional 1:Figura S15. La ausencia de las características de intercalación confirma la naturaleza amorfa completa en sintonía con las inferencias XRD. Los perfiles de carga-descarga de GC observados obtenidos después de mitigar el efecto del sustrato (Fig. 4b, d) son consistentes con los resultados de CV. Una pequeña meseta de capacidad de carga alrededor de 4 V se desarrolla y desaparece cuando se cicla entre 2.0 y 4.0 V (Fig. 4b) como consecuencia de las modificaciones continuas del ambiente local de vanadio para adquirir más simetría para la litiación [5]. Esta meseta se hizo mucho más pequeña para los ciclos de 1,5–4,0 V, pero el punto medio de las curvas de capacidad se desplazó hacia un voltaje más alto, lo que es una indicación de una mayor ionicidad de la matriz. Tal aumento en la ionicidad podría originarse por la reducción de vanadio a V (III) además de los cambios locales de coordinación de vanadio-oxígeno, es decir, una mayor amorfización [5, 27, 28, 29]. Las características generales de carga-descarga de a-VOx-6 Pa son similares a otros materiales a-VOx sintetizados por diferentes rutas en otros trabajos como se hace referencia en el presente trabajo. Durante el primer ciclo a una tasa de 0.1 C, a-VOx-6 Pa mostró altas capacidades reversibles de 239 y 298 mAh g −1 en ventanas de voltaje 2.0–4.0 y 1.5–4.0 V, respectivamente. Al final del ciclo 100, casi el 90% de la retención de capacidad se nota en ambas ventanas de voltaje (Fig. 5a, b) como se menciona en la Tabla 3. Se observa una eficiencia coulombica del 100% a lo largo del ciclo de la ventana de 1.5 a 4.0 V, mientras que fluctuaba ligeramente alrededor del 100% en el caso de una ventana de 2,0 a 4,0 V como resultado de los cambios continuos en el ambiente local de vanadio-oxígeno [5]. Además, ha mostrado una buena capacidad de velocidad como se muestra en la Fig.6 con capacidades que van desde 300 a 50 mAh g −1 a tasas de corriente de 0.1 y 10.0 C, respectivamente. A 1.0 y 10.0 C, entregó capacidades de más de 150 y 40 mAh g −1 , respectivamente. El ciclo observado es mucho mejor que el cristalino comercial V 2 O 5 polvo que se probó de manera convencional (Fig. 5c, d); retuvo sólo el 38-57% de la capacidad inicial en ambas ventanas de voltaje. Durante el ciclo galvanostático en la ventana de potencial de 1,5 a 4,0 V, a-VOx-6 Pa mostró ~ 15% más de capacidad que el V 2 cristalino O 5 durante el primer ciclo y esa diferencia sube al 63% en la terminación del ciclo. Además, se encuentra que su rendimiento es superior a algunas de las películas de PLD a-VOx depositadas sobre el SnO 2 electroquímicamente activo sustrato como se indica en la Tabla 4. SnO 2 es un material de ánodo conocido para LIB y podría ofrecer una capacidad de alrededor de 150 mAh g −1 entre 1,5 y 3,0 V a una tasa de corriente de 100 mA g −1 [30, 31]. El rendimiento de a-VOx-6 Pa es comparable incluso con las películas ALD avanzadas (3,5 nm) a 1 C, como se muestra en la prueba de capacidad de velocidad (Fig. 6). Pero su rendimiento es ligeramente inferior al de otras películas CVD y ALD. En PLD, las condiciones ambientales muy duras pueden conducir a una coordinación V-O de baja calidad en comparación con los métodos CVD o ALD en los que las condiciones de deposición lentas y constantes a baja temperatura pueden generar coordinaciones V-O de alta calidad. Sin embargo, el rendimiento general de a-VOx-6 Pa es muy superior a c-V 2 O 5 polvo a granel y películas PLD a-VOx reportadas. El rendimiento de las películas a-VOx puede ser más adecuado para aplicaciones con limitaciones de espacio y requisitos de capacidad limitada y comparable a las últimas baterías Li-S [32,33,34,35,36,37], prometiendo sus ventajas únicas, como la ausencia de requisitos de aglutinante, aditivo de carbono, preparación sencilla y prometedor alcance para incorporarlos a todas las baterías de estado sólido. Además, las películas a-VOx están libres de pérdidas de capacidad debido a la formación de compuestos irreversibles, como la interfaz de electrolitos sólidos y las estructuras de anillos de polisulfuro [32,33,34,35,36,37].
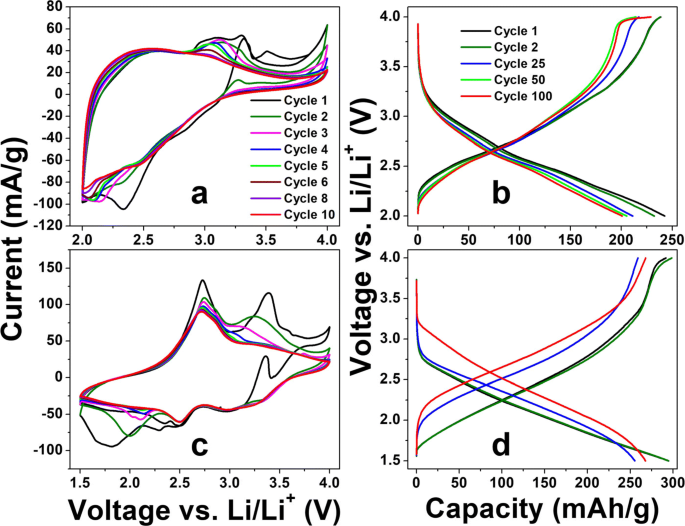
Curvas CV de la batería de iones de litio ( a , c ) y perfiles GC a 0,1 C ( b , d ) de a-VOx-6 Pa
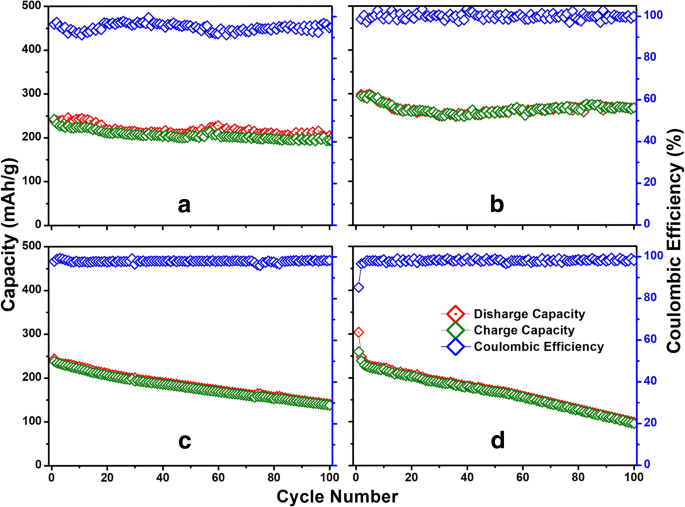
Rendimiento cíclico de la batería de iones de litio de a-VOx-6 Pa ( a , b ) en comparación con el c-V a granel 2 O 5 ( c , d ) en las ventanas de voltaje 2.0–4.0 V ( a , c ) y 1,5–4,0 V ( b , d )
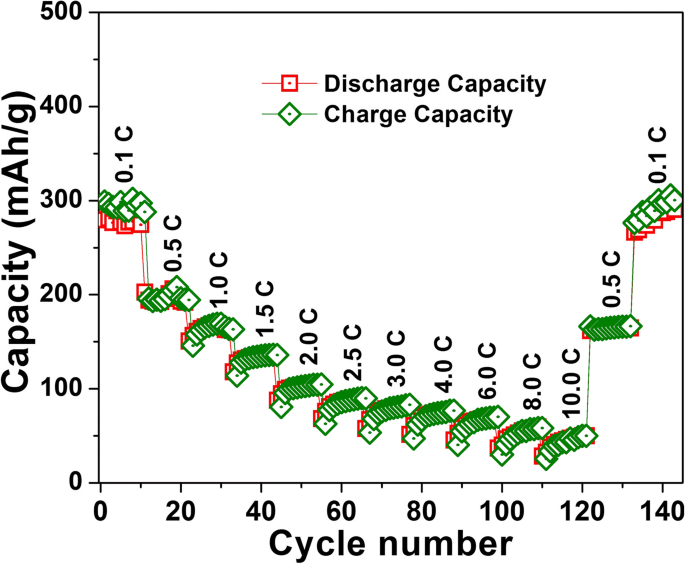
Rendimiento de la tasa de batería de iones de litio de a-VOx-6 Pa
Resultados de la batería de iones de sodio
Las características de la batería de iones de sodio de las películas a-VOx se muestran en la Fig. 7. Las características del perfil GC y CV se encuentran en concordancia entre sí. Especialmente los perfiles CV mostraron características profundas de pseudocapacidad con un área más grande bajo las curvas que los perfiles LIB. Aquí, no aparecieron picos de acero inoxidable, a diferencia del caso LIBs. De las tres películas, a-VOx-30 Pa mostró una disminución continua en la corriente CV mientras que las otras dos se estabilizaron a partir del quinto ciclo en adelante. Incluso después del ciclo 100, la tendencia similar continuó como se muestra en el archivo adicional 1:Figura SI6. La disminución continua de la corriente CV junto con el cambio del punto medio de carga-descarga a un voltaje más alto es una evidencia combinada de la amorfización continua de la película a-VOx-30 Pa [5, 27, 28, 29]. Se encuentra que los perfiles de GC de los tres casos son similares, pero sus puntos de cruce de carga y descarga son ligeramente más altos que las respectivas contrapartes de LIB. Las características de la curva de carga-descarga con pendiente continua son la consecuencia del comportamiento de pseudocapacitancia que se origina a partir de reacciones superficiales faradaicas rápidas que ocurren en las cavidades y trastornos en la matriz del cátodo [10]. Se observa que las capacidades iniciales enumeradas en la Tabla 5 aumentan con el aumento de pO 2 . Especulamos que este efecto podría surgir plausiblemente de un aumento de la porosidad como el aumento de la rugosidad de la superficie observado en los análisis de AFM y FESEM que ingieren más sodio. La ausencia de tal tendencia de capacidad creciente en los ciclos de LIB sugiere que el tipo de cavidades y el entorno poroso formaron los mejores ajustes para la inserción de iones de sodio con la selección actual de electrolitos. Parece que una mayor porosidad conduce a una adsorción-desorción de sodio en la superficie en gran medida, es decir, que se producen reacciones faradaicas muy rápidas, como se ve en la Fig. 7f. Aquí, las curvas CV formaron un perfil casi rectangular que está muy cerca de la naturaleza de un condensador de doble capa eléctrico puro [38]. Este efecto de porosidad aumentada es ventajoso solo para los pocos ciclos iniciales, ya que la capacidad se desvaneció continuamente durante el transcurso del ciclo, como se muestra en la figura 7e y la figura 8c. La formación continua de SEI debido a un entorno de alta deficiencia de oxígeno (> V4 +) podría ser una de las muchas razones del desvanecimiento de la capacidad observada que impone cada vez más una naturaleza aislante a la matriz del electrodo, es decir, la pérdida de contactos eléctricos con el colector de corriente. Por otro lado, las películas depositadas por debajo de pO 2 ~ 13 Pa exhibió una buena estabilidad cíclica con eficiencias de Coulombic que fluctuaron alrededor del 100% como se muestra en la Fig. 8a, prometiendo una buena coordinación V-O como se observa en el análisis EDAX y XPS. Entre estas dos películas, a-VOx-6 Pa mostró una excelente estabilidad cíclica con una capacidad de retención del 90% al final del ciclo 100, aunque su capacidad es menor que a-VOx-13 Pa. La deposición en pO 2 ~ 13 Pa parece ser bueno para una aplicación práctica, ya que permitió que la película ofreciera una capacidad reversible de 162 mAh g −1 que se puede retener hasta un 84% al final de la prueba. Para comparar con los resultados de la presente investigación, hay muy pocos informes disponibles sobre el a-VOx prístino para el almacenamiento de iones de sodio como se indica en la Tabla 4. Por ejemplo, el a-VOx electrodepositado exhibió una alta capacidad de 216 mAh g −1 en primer lugar y eso aumentó a 241 mAh g −1 en el segundo ciclo desde donde se desvaneció continuamente a 140 mAh g −1 en el ciclo 100. Este comportamiento cíclico inferior podría haber resultado de la presencia de restos de agua residual al 12% en peso incluso después del recocido en vacío. En comparación con este caso, a-VOx-13 Pa mostró una estabilidad cíclica mucho mejor al estar libre de moléculas de agua. En otro informe similar, a-VOx electrodepositado sobre papel de grafito exhibió una capacidad de 220 mAh g −1 durante la primera descarga a 1.0 V. En comparación con el corte de 1.5 V, podría entregar aproximadamente 150 mAh g −1 capacidad comparable a a-VOx-13 Pa. Además, no se mencionó información sobre el efecto de las especies de agua que quedaron en a-VOx o en el sustrato de grafito. Por lo tanto, la electroquímica de las películas PLD a-VOx es única y superior a otros materiales de este tipo.
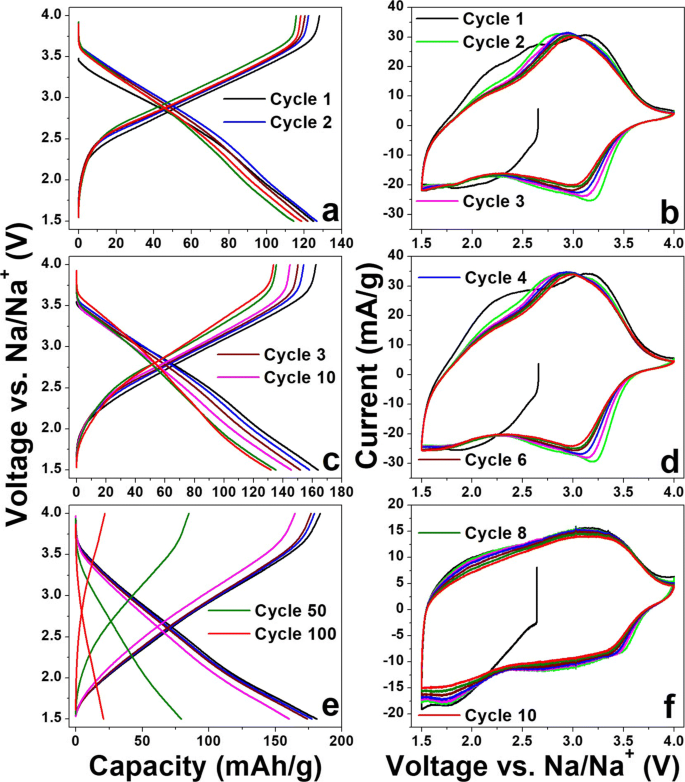
Perfiles GC de batería de iones de sodio de ( a ) a-VOx-6 Pa, ( c ) a-VOx-13 Pa y ( e ) a-VOx-30 Pa a 0,1 C y las respectivas curvas CV mostradas en ( b ), ( d ) y ( f )
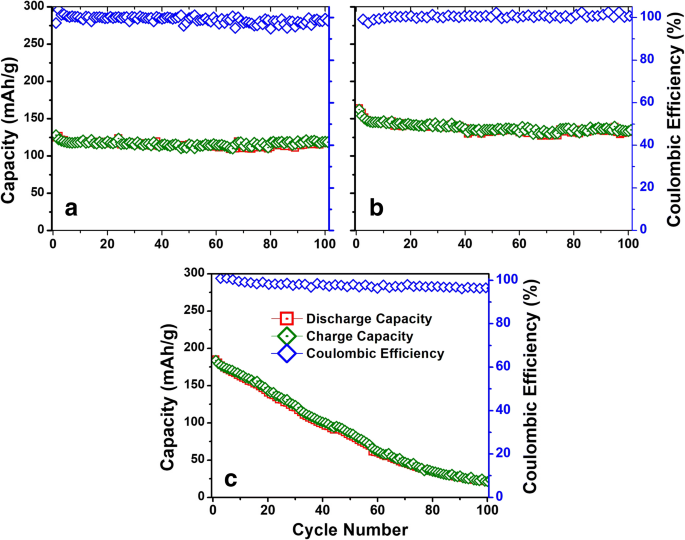
Rendimiento cíclico de la batería de iones de sodio de ( a ) a-VOx-6 Pa, ( b ) a-VOx-13 Pa y ( c ) Películas a-VOx-30 Pa a 0,1 C
Análisis de espectroscopia de impedancia electroquímica
La cinética de litiación y sodiación y las características de impedancia de las películas a-Vox se obtienen a voltaje de circuito abierto (OCV), se descargan a 1,5 V y se cargan en condiciones de 4,0 V. Los resultados de EIS representados como gráficos de Nyquist se muestran en la Fig. 9 para LIB y en la Fig. 10 para SIB. Los valores de varios elementos de circuito que se muestran en los circuitos equivalentes correspondientes se proporcionan en la Tabla 6 para LIB y la Tabla 7 para SIB. Los circuitos que se muestran contienen una resistencia de contacto electrolito-electrodo R e , resistencia debido a la formación de película superficial R sf , resistencia a la transferencia de carga R ct , resistencia a granel (sustrato) R b , componentes de capacitancia debido a la formación de película superficial CPE sf , doble capa de formación de carga CPE dl , fase masiva CPE b e intercalación iónica C i [31, 39,40,41,42,43,44]. En caso de ciclos de LIB, R sf y R ct los valores variaron como 13 Pa <30 Pa <6 Pa mientras que CPE dl El valor varió como 30 Pa <6 Pa <13 Pa. El CPE muy bajo dl valores y disminución de 2,5 veces en C i (after the first charge) of a-VOx-30 Pa can explain its inferior and rapidly decaying capacity values. In all three cases, R b is found greater than R ct that indicates lithiation by fast faradaic surface reactions whose rate seems to be slow down with increasing pO2 as the difference between R b y R ct is decreasing [40, 42]. The decreasing R sf , consistent R ct and very large difference between R b y R ct , i.e. very fast lithiation reactions of a-VOx-6 Pa, enabled it to outperform the other two films. On the other hand, during the SIBs cycling, R ct values varied randomly, but a-VOx-13 Pa film has lower values than the other two films. Further, it possesses similar and consistent R ct , R b , CPEdl , CPEb y C i during the first discharge and charge. Thus, a-VOx-13 Pa film achieved superior capacity stable cycling performance than the other two films. Therefore, the overall impedance analysis is in good agreement with the cycling features.
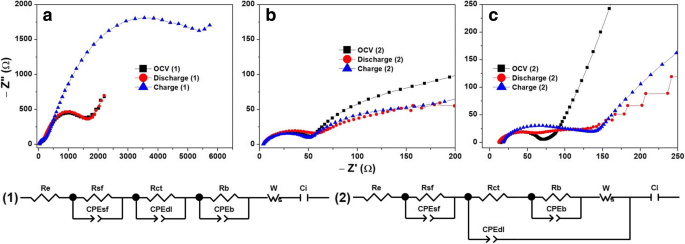
Li-ion battery impedance analysis of a-VOx films deposited at pO2 (a ) 6 Pa, (b ) 13 Pa and (c ) 30 Pa
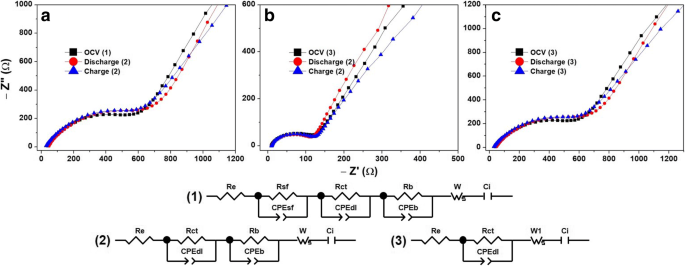
Na-ion battery impedance analysis of a-VOx films deposited at pO2 (a ) 6 Pa, (b ) 13 Pa and (c ) 30 Pa
Conclusions
We successfully investigated the electrochemical properties of pristine a-VOx films as cathodes in Li- and Na-ion batteries. The growth of a-VOx thin films by PLD as a function of varying pO2 is probed systematically with a multitude of characterization techniques. At selected pO2 of 0, 6, 13 and 30 Pa, O/V atomic ratios of the films were found to be 0.76, 2.13, 2.25 and 2.0, respectively. Vanadium in the films a-VOx-6, a-VOx-13 and a-VOx-30 Pa is found in 5+ and 4+ oxidation states with a tendency of later state increased as pO2 rises. Amorphous VOx films obtained at pO2 ~ 6 and 13 Pa found superior to other counterparts for cathode application in Li- and Na-ion batteries with reversible capacities as high as 300 and 164 mAh g −1 at 0.1 C current rate, respectively. High Coulombic efficiencies around 100% are noticed throughout the cycling. At the end of the 100th cycle, nearly 90% of capacity retention is noticed in both cases. The observed cycling trend suggests that the (V 5+ ) stoichiometric nature of a-VOx is better than the electrochemistry. The superior performance of a-VOx-6 Pa vs. Li and a-VOx-13 Pa vs. Na cycling is aided from low-resistance charge transfer and fast faradaic surface reactions.
Abreviaturas
- AFM:
-
Atomic force microscope
- a-VOx:
-
Amorphous vanadium oxide
- CV:
-
Voltamperometría cíclica
- DEC:
-
Diethyl carbonate
- EC:
-
Ethylene carbonate
- FESEM:
-
Field emission scanning electron microscopy
- LIB:
-
Batería de iones de litio
- PC:
-
Propylene carbonate
- PLD:
-
Pulsed laser deposition
- SEI:
-
Solid electrolyte interface
- SIB:
-
Sodium-ion battery
- XPS:
-
X-ray photoelectron spectroscopy
- XRD:
-
Difracción de rayos X
Nanomateriales
- Nanocristales de estaño para futuras baterías
- Nano y ánodo de batería:una revisión
- Nanocables de silicio amorfo cultivados en película de óxido de silicio mediante recocido
- Bioseguridad y capacidad antibacteriana del grafeno y el óxido de grafeno in vitro e in vivo
- Preparación de micromateriales híbridos de MnO2 recubiertos de PPy y su rendimiento cíclico mejorado como ánodo para baterías de iones de litio
- Fabricación de películas delgadas de SrGe2 en sustratos Ge (100), (110) y (111)
- Estudio de la fuerza de adhesión y la transición vítrea de películas delgadas de poliestireno mediante microscopía de fuerza atómica
- Propiedades de las nanopartículas de óxido de zinc y su actividad contra los microbios
- Preparación y propiedades antibiofilm de películas compuestas de óxido de zinc / alúmina anódica porosa
- Síntesis e investigación de nanocables de CuGeO3 como materiales anódicos para baterías avanzadas de iones de sodio
- Microesferas de silicio mesoporosas producidas a partir de la reducción magnetotérmica in situ de óxido de silicio para material anódico de alto rendimiento en baterías de iones de sodio



