Preparación asistida con ácido sulfúrico de puntos poliméricos carbonizados emisores de rojo y la aplicación de imágenes biológicas
Resumen
Se prepararon puntos de polímero carbonizado (CPD) emisores de rojo a partir de p -fenilendiamina ( p -PD) solución acuosa con la ayuda de ácido sulfúrico (H 2 SO 4 ), y en este artículo se estudiaron las propiedades ópticas y la aplicación de bioimágenes. En comparación con otros sistemas asistidos por ácidos fuertes, los SA-CPD (preparados a partir de H 2 SO 4 -sistema asistido, el diámetro medio es de ~ 5 nm) es el más brillante. El rendimiento cuántico de fotoluminiscencia (QY) es del 21,4% (en agua) y el rendimiento del producto es del 16,5%. La solución acuosa de SA-CPD emite a 600 nm cuando se excita con la luz de 300 a 580 nm. La longitud de onda de emisión es independiente de la longitud de onda de excitación. Se calcularon las energías de formación de los CPD de dos formas para mostrar que el crecimiento longitudinal (formación de polímeros) es difícil y el crecimiento transversal (formación de CPD) es fácil. Además, las propiedades de fotoluminiscencia de dos fotones (que se emiten a 602 nm cuando se excitan con un láser de pulso de femtosegundos de 850 nm) de los SA-CPD también se utilizaron en los experimentos para la tinción de células HeLa y se demostró que tienen aplicaciones potenciales en la bioimagen.
Antecedentes
Los puntos de carbono (CD) han atraído mucha atención debido a sus ventajas que incluyen una excelente solubilidad en agua, estabilidad óptica, propiedades de fluorescencia únicas, baja toxicidad, bajo costo, etc. [1]. La mayoría de los CD se estudiaron como candidatos potenciales para diversas aplicaciones, como sensores inmunológicos electroquímicos [2], sensores de imágenes biológicas [3, 4, 5, 6] [7, 8, 9, 10, 11, 12], catálisis [13,14,15], dispositivos emisores de luz [16] y optoelectrónica [17,18,19]. La síntesis de CD juega un papel importante en los estudios sobre las propiedades y aplicaciones ópticas. Los enfoques informados para preparar CD se podrían resumir principalmente como "de arriba hacia abajo" de varios materiales de carbono y "de abajo hacia arriba" de moléculas orgánicas, polímeros o productos naturales [20]. Los métodos "de abajo hacia arriba" son rutas eficientes para la síntesis de CD fluorescentes a gran escala [21]. Grupos en las moléculas aplicadas que incluyen –OH, –COOH, –C =O y –NH 2 se puede deshidratar y carbonizar a temperatura elevada mediante hidrotermia, microondas, combustión, pirólisis, etc.
Los puntos emisores de rojo han despertado un interés considerable debido, es decir, a la mayor profundidad de penetración en el campo de la bioimagen. Especialmente, los puntos de color puro son críticos para una determinada ocasión porque los materiales de luminiscencia independientes de la longitud de onda de excitación pueden proporcionar una luz de fotoluminiscencia (PL) única y estable. La mayoría de las emisiones de CD son dependientes de la longitud de onda de excitación, y los CD generalmente emiten luz azul, verde o amarilla, pocos CD emiten luz roja brillante [22].
Recientemente, los isómeros de fenilendiamina (PD), como o -, m - y p -PD, se han estudiado como fuentes de carbono para preparar CD [8, 9, 23, 24]. Los CD que emiten azul, verde y rojo se pueden preparar a partir de m -, o - y p -PD solución de etanol, respectivamente [23]. Se pueden preparar CD emisores de luz a todo color desde p -PD y solución acuosa de urea [24]. En nuestro trabajo anterior [25], propusimos que se pueden sintetizar fácilmente nuevos puntos de carbono rojo (rendimientos cuánticos =15,8%, en agua) a partir de “ p -PD + HNO 3 ”Sistema acuoso y aplicado en la detección de iones metálicos en agua. Recientemente, el similar " o -PD + H 3 PO 4 ”[26] y“ o -PD + HNO 3 Se informaron [27] sistemas, y Liu et al. [27] cambió el nombre de sus CD (QY =10,8%, en agua) como "puntos de polímero carbonizado (CPD)". A diferencia de los puntos de carbono tradicionales, las longitudes de onda de emisión de los CPD no dependen de la longitud de onda de excitación y, por lo tanto, los "CD" basados en PD deberían denominarse con mayor precisión como CPD.
En este documento, informamos un método fácil y de alta eficiencia de ruta hidrotermal asistida por ácido fuerte para preparar CPD emisores de rojo y la aplicación de imágenes biológicas con propiedades de fotoluminiscencia de dos fotones. Se propone un mecanismo para la formación de CPD utilizando el paquete de programa Gaussian 09.
Métodos
Síntesis de CPD rojos de p asistido por ácido -PD Systems
Basándonos en nuestro trabajo anterior [25], seleccionamos ácido sulfúrico (H 2 SO 4 ), ácido clorhídrico (HCl) y ácido perclórico (HClO 4 ) como asistentes para la preparación de los CPD rojos, los CPD correspondientes fueron etiquetados como SA-CPD, HC-CPD y PA-CPD, respectivamente. Para optimizar las condiciones experimentales de H 2 SO 4 -sistema asistido, seleccionamos varios parámetros, como c (ácido) a c ( p -PD) relación, c ( p -PD), temperatura ( T ) y tiempo de reacción ( t ). Los productos CPD se lavaron con hexano para eliminar el p que no había reaccionado. -PD y por alcohol etílico para eliminar los ácidos, centrifugado a 14000 rpm durante 30 min para eliminar la precipitación del polímero y filtrado a través de una membrana de filtro de 0,22 μm. Si se desea polvo, la solución de CPD purificada se puede evaporar más mediante un evaporador rotatorio hasta un estado casi seco a 80 ° C y en condiciones de bajo vacío (el resto será en forma de polvo).
Caracterización y medición
Se registraron imágenes TEM de alta resolución (HR-TEM) en un microscopio de transmisión JEM-2100 que funcionaba a 200 kV. Los espectros infrarrojos de las soluciones de CPD se recogieron usando el espectrómetro Prestige-21 FT-IR mediante el uso de cortes de ventana KRS-5 (mezcla de TlBr y TlI), típicamente, las fases líquidas se dejaron caer sobre un corte y se secaron. La rebanada se cubrió con la otra rebanada y se fijó en el soporte de prueba. Luego se registraron los espectros infrarrojos.
Los espectros de fluorescencia de los CPD se midieron en un espectrofotómetro de fluorescencia F-2500. Los espectros de absorción de UV-Vis se registraron en un espectrómetro Lambda 950 UV / VIS / NIR. Los espectros de emisión de dos fotones de los CPD se registraron mediante un espectrógrafo de fibra (QE65000, Ocean Optics) en el sistema de microscopio. La solución acuosa de SA-CPD y la solución de polvos redisueltos se centrifugaron en portaobjetos, y luego se midieron las propiedades de fotoluminiscencia de dos fotones.
Los rendimientos cuánticos de fotoluminiscencia (QY) de los CPD se midieron con rodamina B (QY =56% en etanol) como colorante de referencia en el rango de emisión de 580-610 nm excitado por luz UV de 365 nm [25, 28], el procedimiento de Las medidas de QY se muestran en el archivo adicional 1.
Métodos de cálculo
El paquete Gaussian 09 se utilizó para los cálculos de la teoría de la función de densidad (DFT) [29]. Las estructuras de equilibrio se optimizaron mediante el método B3LYP junto con el nivel de conjunto básico 6–311 ++ G (d) [30]. Para investigar el papel de los efectos de los solventes, se utilizó agua en un modelo continuo polarizado (PCM). Se realizaron análisis de frecuencia con el mismo nivel para confirmar que cada estructura optimizada correspondía a un punto estacionario.
Cultivo y tratamiento celular
1,35 ml de células HeLa en medio Eagle modificado de Dulbecco (DMEM; Gibco) a una densidad inicial de 4 × 10 4 Se sembraron células por mililitro en cada placa y se cultivaron a 37 ° C durante 24 h en una atmósfera humidificada que contenía 5% de CO 2 . Los polvos de SA-CPD se volvieron a disolver en agua para preparar la solución de reserva (400 μg mL - 1 ). Se cultivaron 1350 μL de células con 150 μL de solución de reserva de SA-CPD (la concentración final es de 40 μg mL - 1 ) durante 12 hy luego se lavó tres veces con PBS para eliminar los SA-CPD libres. Finalmente, los resultados de las imágenes celulares se recolectaron con un microscopio confocal bajo excitación láser de femtosegundos de 850 nm (30 mW).
Resultados y discusión
Optimización de la preparación para los CPD rojos
En experimentos básicos, se investigaron diferentes sistemas asistidos por ácido con diversas relaciones de concentración, temperaturas de reacción y tiempos (consulte el archivo adicional 1:Figura S1). Descubrimos que los CPD rojos se pueden formar por encima de 180 ° C (reaccionando durante 2 h) para diferentes sistemas ácidos, y las reacciones no se ven afectadas por los aniones en las soluciones. De larga duración (4 a 12 h, 240 ° C para H 3 PO 4 y sistemas de HF, consulte el archivo adicional 1:Figura S1f) la reacción aumentará el tamaño de partícula y la fluorescencia roja se desvanecerá finalmente, mientras que el cambio de fluorescencia no es obvio para el sistema de HCl (2-6 h, 200 ° C, consulte la sección Adicional archivo 1:Figura S2). Teniendo en cuenta el ahorro de energía y el límite superior de temperatura del revestimiento de teflón, la temperatura y el tiempo de reacción óptimos se seleccionan como 200 ° C y 2 h respectivamente. Basado en la estrategia de optimización de p -Sistema PD + HCl (ver archivo adicional 1:Figura S2), optimizamos la p -PD + H 2 SO 4 y p -PD + HClO 4 sistemas y obtuvo los resultados de optimización que se muestran en la Tabla 1.
Los SA-CPD, HC-CPD y PA-CPD se prepararon a partir de p -Solución de PD con la ayuda de H 2 SO 4 , HCl y HClO 4 , respectivamente. El c optimizado (ácido) a c ( p -PD) proporciones de H 2 SO 4 -, HCl- y HClO 4 -los sistemas asistidos son 1, 3 y 3, respectivamente (consulte el archivo adicional 1:Figura S3a). El c adecuado ( p -PD) para la preparación de CPD rojos es amplio (de 0,02 a 0,20 mol L - 1 ). La temperatura optimizada ( T ) y el tiempo de reacción ( t ) son 200 ° C y 2 h. Los SA-CPD son los CPD rojos más brillantes con un QY alto del 21,4% (archivo adicional 1:Figura S3b). Hay dos razones por las que H 2 SO 4 -los puntos de carbono asistido tienen una mejor calidad en comparación con el HCl-, HClO 4 - y HNO 3 -asistidos (publicados en nuestro trabajo anterior [25]). Primero, H 2 SO 4 es un ácido fuerte no volátil que mantiene su acidez en una solución de reacción a alta temperatura y alta presión. En segundo lugar, H 2 SO 4 El sistema asistido es el único que puede formar la precipitación de sal de amonio en el precursor, y los precipitados liberan los reactivos libres lentamente, evitando la formación de precipitación de polímeros de partículas grandes y promoviendo aún más la formación de puntos de carbono de alta calidad. Los HA-CPD y los PA-CPD son soluciones espesas de color rojo oscuro-marrón y emiten PL rojo oscuro bajo irradiación de luz UV de 365 nm, mientras que los SA-CPD preparados son una solución delgada transparente de color rojo brillante y emite luz roja brillante (archivo adicional 1:Figura S3c). Después de ser purificados mediante lavado, concentración, filtrado y evaporación, se obtuvieron polvos de color marrón rojizo oscuro de SA-CPD (Archivo adicional 1:Figura S3d) con un rendimiento de producto del 16,5%. Los polvos se pueden volver a disolver en agua y la solución emite fluorescencia roja y brillante (archivo adicional 1:Figura S3e).
Caracterización TEM y análisis FT-IR
Imágenes TEM de OpPD de muestra (sin H 2 SO 4 ) y SA-CPD (con H 2 SO 4 ) se muestran en la Fig. 1. La muestra de OpPD está compuesta por fragmentos (oligómeros, Fig. 1a) y polímeros (inserto de la Fig. 1a). Los SA-CPD son CPD monodispersos con un tamaño medio de ~ 5 nm (Fig. 1c). Presenta dedos de celosía bien resueltos con un espacio de ~ 0.21 nm (inserto de la Fig. 1b), correspondiente al espaciado de celosía en el plano (100) del grafeno [31, 32].
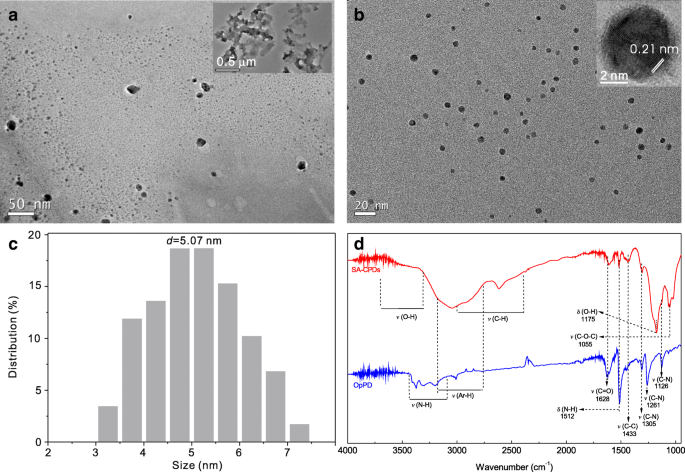
Imágenes TEM de OpPD de muestra (sin H 2 SO 4 ) ( a ) y SA-CPD ( b ). c La distribución de tamaño de SA-CPD. d Los espectros FT-IR de la muestra de OpPD y CPD rojos. Se prepararon muestras de OpPD y SA-CPD a partir de p -PD solución acuosa sin y con H 2 SO 4 -asistido
Los estados de superficie de los CPD pueden afectar las propiedades ópticas. Los grupos químicos de la superficie de las muestras OpPD y SA-CPD se caracterizaron mediante espectros FT-IR (Fig. 1d). Dos muestras tienen varios grupos similares, como Ar-H (2700–3200 cm - 1 [33], pertenece a la vibración aromática de estiramiento C-H), C-C (~ 1433 cm - 1 , pertenece a la vibración aromática de estiramiento del hueso C, revela la presencia de vibraciones de estiramiento aromáticas características de las unidades bencenoides) [34], y C =O (1628 cm - 1 , pertenece a los grupos –COOH). En comparación con la muestra de OpPD, los nuevos grupos, como O-H (3300–3700 cm - 1 y 1175 cm - 1 pertenecen a los grupos –COOH), C-O-C (1055 cm - 1 , existen en ésteres) y C-H (2400–3000 cm - 1 pertenece a los radicales alquilo formados en la reacción de apertura del anillo), se encuentran en los CPD, mientras que el –NH 2 o –NH– grupos relacionados como N-H (3100–3300 cm - 1 y 1512 cm - 1 y C-N (1126, 1261 y 1305 cm - 1 pertenecen a la libre –NH 2 o –NH– grupos de p -PD precursores, se debilitan o desaparecen. La existencia de grupos –OH o –COOH indica que el grado de oxidación de la superficie de los SA-CPD (con H 2 SO 4 adición) es mayor que la de la muestra OpPD (sin adición de ácido).
Mecanismo propuesto para la formación de CD
Las energías de formación se calcularon utilizando el paquete de programa Gaussian 09. Después de ser protonados por ácido asistido, los bi-polímeros se pueden polimerizar de dos formas que se denominan crecimiento longitudinal y transversal. La energía de formación calculada del crecimiento transversal (- 1406.07 kJ mol - 1 ) es significativamente mayor que la del crecimiento longitudinal (- 616,25 kJ mol - 1 ). Muestra que los bipolímeros completamente protonados (pH 3, después de un exceso de H + fue agregado) tienden a polimerizarse de manera transversal para formar una estructura plana (Fig.2). Estas estructuras planas se autoensamblaron luego para formar CPD esféricos.
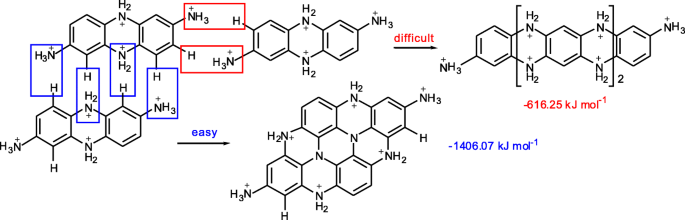
Energías de formación de crecimientos longitudinales y transversales
Propiedades ópticas
Aunque se preparan con la ayuda de diferentes ácidos, todos los CPD tienen propiedades ópticas similares [25]. Para los espectros UV-Vis de la solución acuosa de SA-CPD (Fig.3a), el pico de absorbancia ubicado a ~ 290 nm está asociado a las transiciones en el anillo de benceno, y los picos ubicados a 430 nm y 510 nm podrían asignarse a π -π * transición de fenazina sustituida conjugada a los pares de electrones solitarios en el grupo amina adyacente y la transición de electrones del anillo bencenoide a los anillos quinoides, respectivamente [32]. La curva de excitación describe una tendencia ascendente amplia y gradual en la región visible, y el pico de excitación máximo (~ 580 nm) está cerca del pico de emisión (~ 600 nm). Los CPD emiten en la zona de luz roja (600-700 nm) cuando se excitan de 220 nm a 310 nm, mientras que emiten en luz naranja (~ 600 nm) cuando se excitan de 310 nm a 580 nm (Fig. 3b). Vale la pena señalar que la fluorescencia de este tipo de CPD emisores de rojo es independiente de la longitud de onda de excitación [22, 35].
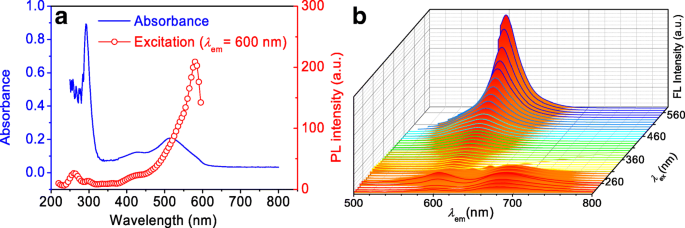
un Absorción UV-Vis, excitación (pico a 600 nm) y b espectros de emisión (excitados 220–580 nm) de SA-CPD
Imagen celular
Las propiedades de fotoluminiscencia de dos fotones de los SA-CPD antes y después del proceso de pulverización se muestran en la Fig. 4a. Hay un cambio de azul de 602 nm (antes del proceso de pulverización) a 529 nm (después del proceso de pulverización) a la misma longitud de onda de excitación de 850 nm por láser de pulso de femtosegundos (30 mW). La intensidad de PL se incrementó después del proceso de pulverización.
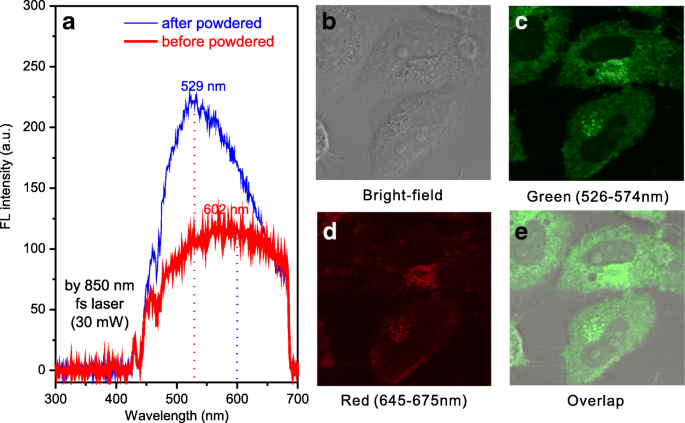
Espectros de fotoluminiscencia de dos fotones de SA-CPD ( a ) e imágenes de microscopía de fluorescencia confocal de células HeLa tratadas con SA-CPD excitadas por láser de pulso de femtosegundo de 30 mW y 850 nm ( b - e )
Los polvos de SA-CPD se volvieron a disolver en PBS (1X) y se aplicaron en imágenes de células HeLa utilizando microscopía de fluorescencia confocal y láser de pulso de femtosegundo de 850 nm (30 mW) (ver Fig. 4b-e). Después de cultivar con células HeLa durante 12 h, las células HeLa se tragaron las SA-CPD y las CPD entraron en el citoplasma. La intensidad de FL del canal rojo (645–675 nm) es débil mientras que el canal verde (526–574 nm) es brillante, es consistente con el cambio de azul en el proceso de pulverización.
Conclusiones
Se informó sobre un método fácil de ruta hidrotermal asistida por ácido para preparar puntos de carbono y la aplicación de imágenes biológicas. Dentro de H 2 SO 4 -, HCl- y HClO 4 -sistemas asistidos, SA-CPD preparados a partir de H 2 SO 4 El sistema asistido es el CPD más brillante con un tamaño promedio de ~ 5 nm, el QY del 21,4% y el rendimiento del producto del 16,5%. La solución acuosa de SA-CPD emite a 600 nm cuando se excita con luz de 300 a 580 nm. La longitud de onda de emisión es independiente de la longitud de onda de excitación. Además, los SA-CPD tienen propiedades de fotoluminiscencia de dos fotones que emiten a 602 nm cuando se excitan con un láser de pulso de femtosegundos de 850 nm (30 mW). El método también se ha utilizado en la obtención de imágenes de células HeLa y tiene el potencial, por ejemplo, en aplicaciones de imágenes biológicas.
Abreviaturas
- CD:
-
Puntos de carbono
- CPD:
-
Puntos de polímero carbonizado
- HC-CPD:
-
Los puntos de carbono se prepararon a partir de p -PD con sistema asistido por HCl
- PA-CPD:
-
Los puntos de carbono se prepararon a partir de p -PD con HClO 4 -sistema asistido
- p -PD:
-
P -fenilendiamina
- QY:
-
Rendimientos cuánticos
- SA-CPD:
-
Los puntos de carbono se prepararon a partir de p -PD con H 2 SO 4 -sistema asistido
Nanomateriales
- Aplicación de tintes ácidos en el mundo de las telas
- El desarrollo y la aplicación de la tela de fibra de vidrio
- Preparación de nanopartículas de mPEG-ICA cargadas con ICA y su aplicación en el tratamiento del daño celular H9c2 inducido por LPS
- Síntesis de puntos cuánticos de tipo II / tipo I de ZnSe / CdS / ZnS con supresión de reabsorción y su aplicación para el ensayo inmunoabsorbente
- Absorbedor perfecto de banda ultra estrecha y su aplicación como sensor plasmónico en la región visible
- Los efectos de la relación Li / Nb en la preparación y el rendimiento fotocatalítico de los compuestos Li-Nb-O
- La preparación de la nanoestructura yema-cáscara de Au @ TiO2 y sus aplicaciones para la degradación y detección del azul de metileno
- Síntesis de nanocristales de ZnO y aplicación en células solares de polímero invertido
- Estudio de la fuerza de adhesión y la transición vítrea de películas delgadas de poliestireno mediante microscopía de fuerza atómica
- Efectos del tamaño y la agregación / aglomeración de las nanopartículas en las propiedades interfaciales / interfásicas y la resistencia a la tracción de los nanocompuestos poliméricos
- Película de condensador:propiedades, construcción y aplicación



