Deposición precisa in situ asistida por campo eléctrico de nanofibras de γ-Fe2O3 / poliuretano electrohiladas para hipertermia magnética
Resumen
Un método de electrohilado facial de fabricación precisa in situ de una membrana fibrosa magnética compuesta de nanofibras de poliuretano (PU) decoradas con γ-Fe superparamagnético 2 O 3 Se reportan nanopartículas con generación de calor simultánea en respuesta al campo magnético alterno (AMF). En este método, se utiliza un electrodo auxiliar de aluminio cónico para regular el campo electrostático y afectar el proceso de electrohilado para la deposición rápida y precisa in situ de γ-Fe 2 electrohilado O 3 / Fibras PU. El electrodo cónico auxiliar puede extender la zona de estabilización del chorro de la solución precursora cuatro veces más que sin electrodo auxiliar, lo que puede lograr el control preciso del área de deposición de fibras. Además, las membranas fibrosas compuestas electrohiladas muestran un rápido aumento de temperatura desde la temperatura ambiente a 43 ° C en 70 s bajo el AMF, que exhibe una velocidad de calentamiento más rápida y una temperatura de calentamiento más alta en comparación con las muestras fabricadas sin la ayuda del electrodo auxiliar. Los presentes resultados demuestran que el electrohilado preciso in situ con la ayuda de un electrodo cónico auxiliar tiene el potencial como un método de manipulación para preparar fibras compuestas magnéticas, así como la hipertermia magnética de la terapia del cáncer.
Antecedentes
La hipertermia es otro tratamiento eficaz después del tratamiento tradicional del tumor, que puede utilizarse en estrategias multimodal, ya que puede potenciar sinérgicamente los efectos antitumorales de la quimioterapia, la radioterapia y la inmunoterapia [1, 2, 3]. El mecanismo de utilizar la hipertermia como medida de tratamiento del cáncer es la sensibilidad de las células cancerosas en el rango de 41 a 45 ° C, en contraste con las células sanas [4, 5]. La aplicación de nanopartículas magnéticas para el diagnóstico y la terapia del cáncer todavía está limitada por una mala orientación, aunque se han realizado muchas estrategias de focalización, como la focalización magnética y la focalización molecular [6, 7]. Si las partículas magnéticas se inyectan directamente en el cuerpo, el sistema reticuloendotelial las elimina rápidamente y se enriquecen en ciertos órganos, como el riñón, el hígado y el bazo, en lugar de en el sitio del tumor [8]. Además, las nanopartículas magnéticas se inyectan localmente en el tejido tumoral y prefieren escaparse del sitio del tumor debido a su pequeño tamaño [9]. Todos estos casos reducen la eficacia de la hipertermia de las nanopartículas magnéticas. En comparación con la hipertermia de las nanopartículas magnéticas, la entrega precisa y local de nanopartículas de óxido de hierro (INOP) a las células cancerosas es la principal ventaja de las fibras compuestas magnéticas, que es un método de tratamiento de hipertermia ideal para tumores de fácil acceso.
En muchos informes, las membranas nanofibrosas compuestas se prepararon a partir de una solución de polímero que contenía una dispersión de nanopartículas magnéticas sintetizadas previamente, que se emplearon en el tratamiento de la hipertermia [10,11,12,13]. Sin embargo, todos tienen algunos inconvenientes evidentes. Por ejemplo, es difícil para las nanofibras previamente preparadas desarrollar un recubrimiento homogéneo y continuo en la superficie del tejido tumoral, que es fácil de romper y directamente adverso a un sello hermético, y luego conduce a la insuficiencia del tejido tumoral complejo. . Como resultado, el electrohilado preciso in situ sobre el tejido tumoral podría ser una buena estrategia no solo para prevenir el desprendimiento de las membranas fibrosas compuestas durante el proceso de hipertermia magnética, sino también para aumentar la posibilidad de calentamiento homogéneo sobre el tejido tumoral.
El electrohilado in situ necesita controlar con precisión el rango de deposición en un tejido tumoral específico, lo que podría evitar causar una adhesión tisular grave, especialmente en la cavidad abdominal [14]. Numerosos investigadores han informado de que el electrohilado preciso in situ se puede aplicar en el campo de la medicina [15]. Estudios recientes demostraron el uso de un dispositivo de electrohilado in situ dirigido por flujo de aire para mejorar la deposición precisa de fibras poliméricas ultrafinas en los sitios de la herida [16]. Sin embargo, el dispositivo de electrohilado in situ dirigido por flujo de aire debe agregar una bomba de aire adicional, un mango adicional hecho en casa con un cabezal de hilera y otro dispositivo asistido por flujo de aire en comparación con el aparato de electrohilado tradicional, y debe coordinar el flujo de aire y la relación entre la velocidad y el voltaje, lo que complica el funcionamiento del aparato. El electrohilado asistido por campo magnético también es una forma eficaz de preparar fibras electrohiladas ordenadas y controlar el rango de deposición de las fibras electrohiladas [17]. Los polímeros macromoleculares que incorporan suficientes partículas magnéticas pueden inducir suficiente susceptibilidad magnética a la solución polimérica. Yang y col. [18] informó de un enfoque para la fabricación de matrices bien alineadas y rejillas multicapa mediante un método llamado electrohilado magnético (MES). En el MES, se agrega una pequeña cantidad de nanopartículas magnéticas para magnetizar la solución de polímero. Se aplica un campo magnético generado por dos imanes permanentes colocados en paralelo durante el electrohilado, y el campo magnético estira las fibras a través del espacio para formar una matriz paralela. Sin embargo, el electrohilado asistido por campo magnético solo se puede utilizar para la preparación de fibras magnéticas, lo que no tiene ningún efecto sobre el proceso de hilado de fibras no magnéticas. En contraste, el uso de un electrodo auxiliar en el electrohilado preciso in situ para lograr las membranas fibrosas compuestas magnéticas es un método más simple, efectivo y universal.
Aquí, desarrollamos una deposición precisa in situ de membranas fibrosas compuestas con γ-Fe 2 incrustado O 3 NP mediante un hilador electrostático portátil que agrega un electrodo auxiliar de aluminio cónico en la ubicación del cabezal giratorio para regular la dirección de deposición y la extensión de las fibras compuestas magnéticas. El presente estudio tiene como objetivo explorar la influencia del electrodo auxiliar en las membranas fibrosas compuestas magnéticas cuya morfología y rendimiento pueden cambiar. En comparación con el enfoque convencional, esta técnica podría depositar fibras nanoestructuradas de manera muy rápida y precisa en tejido tumoral complejo e irregular para formar membranas continuas, compactas y flexibles con una integridad excelente, que actúa como una fuente poderosa para calentar localmente la región del tumor a la temperatura deseada. sin sobrecalentar los tejidos sanos circundantes y para prevenir un posible crecimiento tumoral o mejorar los efectos antitumorales de la quimioterapia, la radioterapia y la inmunoterapia. Los estudios in vitro demostraron que el electrohilado γ-Fe 2 O 3 / Las membranas de fibra magnética de PU tienen una excelente eficacia terapéutica de hipertermia mediada por magnetismo. Además, la estabilidad térmica de γ-Fe 2 O 3 / Las membranas fibrosas compuestas de PU también han sido demostradas por la excitación repetida del campo magnético.
Métodos / Experimental
Materiales
γ-Fe 2 O 3 nanopartículas (γ-Fe 2 O 3 NP, 10 nm, phere, 99.5%, Shanghai Macklin Biochemical Co., Ltd. China), gránulos de poliuretano de grado poliéter de alto peso molecular (PU, WHT-8170, Yantai Wanhua Polyurethanes Co., Ltd., China) y N , N -dimetilformamida (DMF ≥ 99,5%, Pharm Chemical Reagent Co, Ltd., China) se utilizaron tal como se recibieron sin mayor pureza.
Preparación de Electrospun γ-Fe 2 O 3 / Nanofibras magnéticas de PU
Para dispersar γ-Fe 2 O 3 Se agregaron NP en DMF, 0.54 g de nanopolvo a 2.5 g de DMF, después de lo cual la mezcla se expuso a ultrasonidos durante 4 h en una botella de cono. Se preparó una solución pura de poliuretano disolviendo gránulos de PU de 1,8 g en disolvente DMF de 7,5 g y agitando a 40ºC. Luego, la solución de PU se vertió en el γ-Fe 2 O 3 Dispersión de NP y agitado vigorosamente durante 30 min mediante un agitador mecánico casero. Finalmente, la mezcla de la solución se dispersó adicionalmente mediante sonicación durante otras 24 ha 50 ° C antes del electrohilado.
En el proceso de electrohilado, adoptamos una hiladora electrostática portátil para lograr la fabricación de fibras magnéticas. Como se muestra en la figura 1a, la máquina giratoria electrostática portátil tiene un dispositivo giratorio manual con forma de pistola. Como se muestra en la imagen ampliada del cabezal de hilatura, se fijó en la hilera un electrodo auxiliar cónico con un diámetro de 4 cm en la parte inferior, que puede controlar y regular el campo electrostático para la rápida deposición de fibras al espesor ideal. Este dispositivo de electrohilado utilizó una jeringa de plástico de 5 ml (Becton Dichinson), a la que se le colocó una punta de aguja con un diámetro interno de 0,7 mm. La solución del precursor de electrohilado se cargó en la jeringa y se apretó mediante una bomba de jeringa del dispositivo. El electrohilado se llevó a cabo a un voltaje aplicado que variaba entre 10 ~ 15 kV, con una distancia del ápice al colector de 10 cm y una velocidad de alimentación constante de 33 μL / min. El recolector podría ser papel de aluminio, la piel e incluso la superficie del tejido tumoral. Bajo el efecto de la fuerza del campo electrostático, la solución precursora de electrohilado exprimida por una bomba de jeringa se estiró, se cortó en nanofibras en el aire y finalmente se depositó en la superficie del colector. Después de diferentes tiempos de hilado de 5, 10, 15 y 20 min, se obtuvieron diferentes espesores de las membranas de fibra magnética y se denotaron como γ-Fe 2 O 3 / PU-A5, γ-Fe 2 O 3 / PU-A10, γ-Fe 2 O 3 / PU-A15 y γ-Fe 2 O 3 / PU-A20, respectivamente. Además, el γ-Fe 2 O 3 / Las membranas fibrosas compuestas de PU también se prepararon en el mismo tiempo y condiciones de electrohilado pero sin el electrodo auxiliar durante el electrohilado y se denominaron γ-Fe 2 O 3 / PU-5, γ-Fe 2 O 3 / PU-10, γ-Fe 2 O 3 / PU-15 y γ-Fe 2 O 3 / PU-20, respectivamente. Todos los procedimientos se llevaron a cabo de acuerdo con las pautas de los Institutos Nacionales de Salud para el uso de animales de laboratorio y con la aprobación del Comité de Investigación Animal del Canciller de la Universidad.
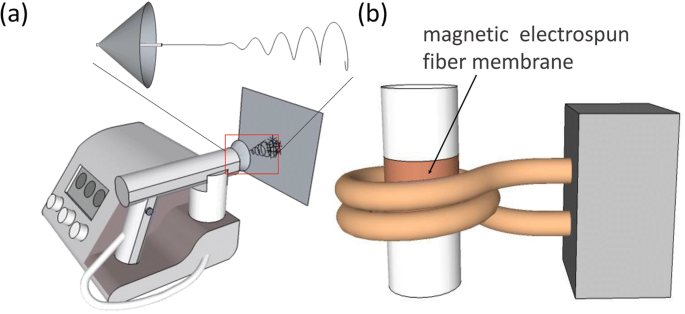
un Diagrama esquemático del dispositivo de giro electrostático portátil y el electrodo auxiliar. b Representación esquemática del generador de campo, bobinas y sistema de adquisición de datos para registrar la temperatura
Caracterización
La estructura morfológica de la superficie y los diámetros del γ-Fe 2 O 3 / Las membranas nanofibrosas compuestas de PU se determinaron mediante microscopía electrónica de barrido (SEM, TM-1000, Hitachi). El tamaño y la distribución de las partículas magnéticas se caracterizaron utilizando un microscopio electrónico de transmisión (TEM, JEM-200EX). El análisis de difracción de rayos X en polvo (XRD, goniómetro de ángel ancho RINT2000) se llevó a cabo usando un difractómetro de rayos X Rigaku. La composición química y la estructura molecular de las membranas de nanofibras se determinaron utilizando un espectrómetro de infrarrojos con transformador de Fourier (FTIR) (Thermo Scientific Nicolet iN10). El análisis termogravimétrico (TGA) de las membranas de la composición se realizó a una velocidad de calentamiento de 10 ° C / min de 30 a 600 ° C bajo la protección del flujo de nitrógeno. Propiedades magnéticas de γ-Fe 2 O 3 / PU se midieron con el magnetómetro de muestra de vibración (VSM, Quantum Design Corporation) de - 15.000 a 15.000 Oe.
Experimento de calentamiento magnético
El AMF excitado utilizado para inducir el tratamiento térmico fue producido por un generador de campo magnético alterno (SP-04AC Shenzhen Shuangping Power Technology Co., Ltd.) cuya potencia nominal era de 3 kW y la bobina de inducción enfriada por agua estaba hecha de cobre, con un bobina de dos sintonización y un diámetro interior de 30 mm (Fig. 1b). La intensidad máxima del campo magnético del generador de AMF y la frecuencia del campo magnético fueron 12,5 Oe y 153 kHz, respectivamente. Las membranas fibrosas en forma cilíndrica se colocaron en el centro de la bobina de cobre [19, 20]. Para medir las características de calentamiento de las membranas fibrosas, se fijó el detector de temperatura por infrarrojos sobre las membranas de fibra y se registró el cambio de temperatura de las películas de nanofibras en tiempo real.
Resultado y discusión
Deposición precisa a través del electrohilado in situ
Se realizó una comparación en el rango de deposición entre el electrohilado con y sin un electrodo auxiliar. Como se muestra en la Fig.2, bajo las mismas condiciones externas (temperatura, voltaje, distancia, humedad, velocidad de hilado, fluido precursor de hilado, diámetro de la aguja de hilado, etc.), el rango de deposición de la membrana fibrosa preparada utilizando el electrodo auxiliar (diámetro de 1,8 cm) era significativamente más pequeña que la de la fibra electrohilada sin el uso del electrodo auxiliar (diámetro de 4,6 cm). En el proceso tradicional de electrohilado, el fluido precursor del hilado se divide, bate y se estira en micro / nanoescala de fibra en el aire, y finalmente se deposita en el colector para formar una membrana de tela no tejida [21]. Sin embargo, en la región inestable del chorro giratorio, la distribución espacial cónica del chorro aumenta el rango de deposición de la fibra y reduce la precisión de la deposición de la fibra. Cuando se modifica con un electrodo auxiliar, la división y el batido del chorro precursor giratorio se suprimen y el rango de la región de estabilización del chorro se vuelve grande y fluctúa en un carril muy estrecho. Como se muestra en la Fig. 2a, b, sin la ayuda del electrodo auxiliar, la zona de estabilización del chorro de la solución precursora fue de 0,96 cm. Y con la ayuda del electrodo auxiliar se amplió 4 cm la zona de estabilización del chorro de la solución precursora, que era cuatro veces más larga que sin el electrodo auxiliar. A la misma distancia de giro, la extensión de la zona de estabilización ayuda a reducir el rango de deposición del giro y lograr un giro preciso in situ. Como se muestra en la Fig. 2c, d, los rangos de deposición de membranas fibrosas compuestas preparadas sin y con la ayuda de un electrodo auxiliar son regiones circulares cuyos diámetros son 4,6 y 1,8 cm, respectivamente. El resultado demuestra que el electrodo auxiliar puede reducir eficazmente el rango de deposición durante el proceso de electrohilado. La Figura 2e muestra la tendencia del grosor de la membrana de fibra electrohilada a lo largo del tiempo. Con la ayuda del electrodo auxiliar, se puede lograr un electrohilado rápido y, después de 30 minutos, el grosor de la membrana compuesta depositada es aproximadamente cuatro veces más grueso que el preparado por otro método de electrohilado. Está claro que bajo la mediación del electrodo auxiliar, el chorro de electrohilado tiene un rango de deposición más preciso y se puede formar una película fibrosa que tiene un cierto espesor en poco tiempo, lo que tiene gran importancia en la ejecución del giro preciso in situ y la realización. el rápido electrohilado en el siguiente experimento de hipertermia magnética.
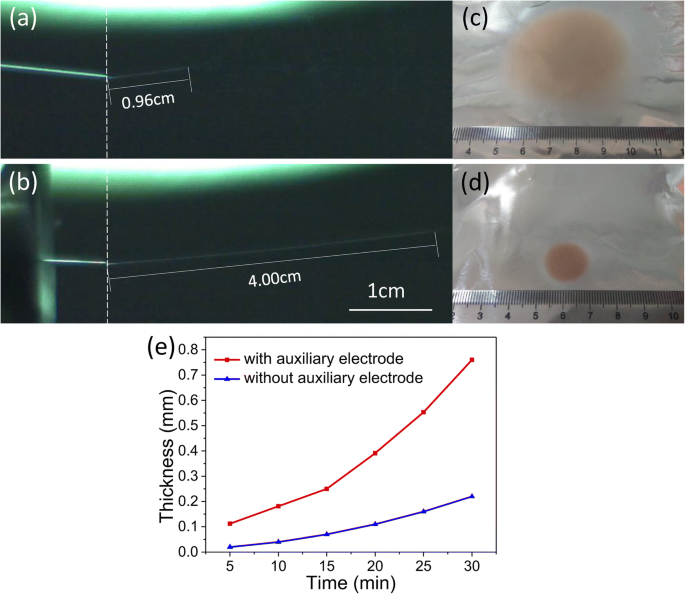
Fotos de cámara de alta velocidad de un chorro electrospinning en zona estable a sin y b con el electrodo auxiliar. Fotografías ópticas de membrana de fibra electrohilada depositada in situ c sin y d con el electrodo auxiliar. e Curvas de espesor de deposición dependientes del tiempo para la preparación in situ de membranas de fibra electrohilada
Propiedades morfológicas, estructurales y magnéticas
Las imágenes SEM de membranas fibrosas de PU y membranas compuestas preparadas con / sin un electrodo auxiliar se muestran en la Fig. 3. Como se desprende de la Fig. 3a, e, byf, las membranas fibrosas de PU con un tamaño submicro, alto la porosidad y la orientación ordenada al azar preparadas con y sin un electrodo auxiliar son las matrices relativamente suaves y sin perlas de fibras entrelazadas. Según los análisis estadísticos que se insertan en las esquinas superiores izquierdas de las imágenes SEM, los rangos de diámetros de las membranas fibrosas de PU que se preparan de dos formas diferentes son 700-1900 nm y 1100-2300 nm, respectivamente, y la fibra media sus diámetros son aproximadamente 1390 y 1670 nm, respectivamente. Evidentemente, los diámetros de fibra de las membranas fibrosas de PU preparadas con un electrodo auxiliar son un poco más gruesos que los del otro, lo que podría atribuirse a la restricción del campo electrostático por un electrodo auxiliar. La adición del electrodo auxiliar restringe el campo eléctrico y limita aún más el batido y elongación de las fibras hiladas, de modo que las fibras hiladas son relativamente más gruesas que las fabricadas en la forma en que no se agregan los electrodos auxiliares. Como se muestra en la Fig. 3c, g, d y h, la adición de γ-Fe 2 O 3 Los NP cambian ligeramente la morfología de la superficie y el diámetro de las fibras, pero no cambia la geometría y la estructura porosa de las membranas fibrosas compuestas en comparación con el PU. Después de la incorporación de γ-Fe 2 O 3 NP, el diámetro de la fibra se redujo a 850 nm y la superficie de las fibras exhibió una mayor rugosidad, lo que podría deberse a la dispersión de γ-Fe 2 O 3 NP en / sobre las fibras de PU debido a su alta relación superficie-volumen [22]. Sin embargo, las membranas fibrosas compuestas preparadas utilizando un electrodo auxiliar se vuelven menos lisas (Fig. 3d). Por lo tanto, además de los efectos de las partículas magnéticas, la adición del electrodo auxiliar durante el proceso de electrohilado inhibe el batido de las fibras y la volatilización del solvente es incompleta, lo que hace que la superficie de la fibra se vuelva más rugosa. Después de la adición de γ-Fe 2 O 3 nanopartículas, además del cambio en la morfología microscópica de las nanofibras, el color de las membranas de nanofibras compuestas también cambió de blanco a marrón claro, y el color se mantuvo sin cambios después de varios lavados.
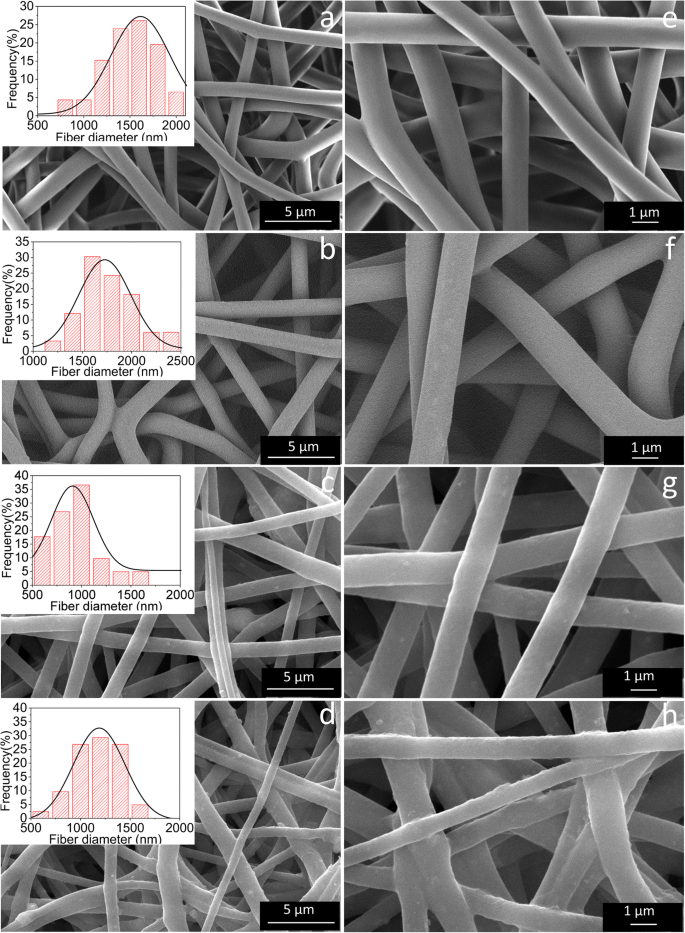
Imágenes SEM de membranas de fibra pura PU preparadas a , e sin y b , f con el uso de un electrodo auxiliar. γ-Fe 2 O 3 / Membranas de fibra compuesta de PU preparadas c , g sin y d , h con el uso de un electrodo auxiliar (las inserciones muestran las distribuciones de diámetro de las membranas de fibra electrohilada)
Para caracterizar aún más la dispersión de γ-Fe 2 O 3 NPs incorporadas en las membranas magnéticas, hemos analizado en detalle la imagen TEM de la membrana de fibra compuesta. Como se puede observar en la Fig.4, el γ-Fe 2 O 3 Las NP están bien dispersas y la mayoría de ellas están encapsuladas firmemente dentro de las nanofibras, evitando así su posible fuga y migración cuando se utilizan como materiales de sustrato para la hipertermia magnética. El γ-Fe 2 O 3 Los NP muestran una buena dispersión y ninguna aglomeración en la fibra, lo que significa que el electrodo auxiliar no interfiere en la distribución uniforme de las partículas magnéticas.

Imágenes TEM de γ-Fe 2 O 3 / Membranas de fibra compuesta de PU preparadas con el uso de un electrodo auxiliar
La Figura 5A muestra los patrones XRD de membranas de fibra de PU ordenadas, γ-Fe 2 O 3 nanopartículas magnéticas y γ-Fe 2 electrohilado O 3 / Membranas fibrosas compuestas de PU. Se encuentra que los espectros XRD del electrohilado γ-Fe 2 O 3 / Las membranas nanofibrosas compuestas de PU y las membranas de fibra de PU ordenadas muestran un pico ancho, señalando un símbolo típico de los materiales de baja cristalinidad. Este resultado prueba que la membrana fibrosa de PU preparada tiene una baja cristalinidad. Sin embargo, las posiciones e intensidades relativas de algunos picos nuevos de la membrana compuesta concuerdan bien con la tarjeta de difracción estándar JCPDS 39-1346, que corresponden a (220), (311), (400), (511) y (440 ) picos característicos de γ-Fe 2 O 3 nanopartículas magnéticas. Comparado con γ-Fe 2 O 3 NP, la disminución significativa de la intensidad del pico de difracción de las membranas fibrosas compuestas se puede atribuir a la combinación física entre γ-Fe 2 O 3 Membranas fibrosas NP y PU sin reacción química.
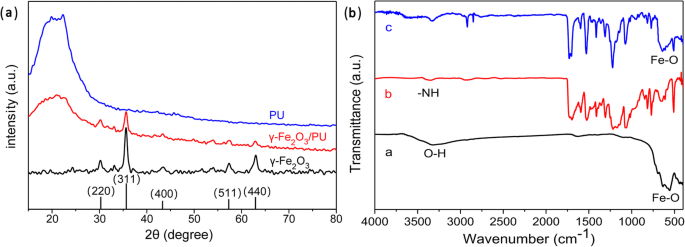
un Patrones de XRD de nanofibras de PU, γ-Fe 2 O 3 / Membranas de fibra compuesta de PU y γ-Fe 2 O 3 NP. b Espectros FTIR de ( a ) γ-Fe 2 O 3 NP, ( b ) Membranas de fibra electrohilada de PU, y ( c ) membranas de fibra compuesta magnética
Para determinar la estructura molecular de las membranas fibrosas compuestas, se analizaron los espectros infrarrojos por transformada de Fourier (FTIR) de las muestras en el rango espectral de 400 a 4000 cm −1 (Figura 5B). Las asignaciones de bandas principales se enumeran en la Tabla 1. La curva a en la Fig. 5B presenta un pico de absorción débil y ancho observado alrededor de 3347 cm −1 , correspondiente a la vibración de estiramiento O-H de H 2 O debido a la absorción de humedad en γ-Fe 2 O 3 NP. Además, una banda fuerte a 557 cm −1 puede asignarse a la frecuencia vibratoria del enlace Fe-O. Como se muestra en la curva b en la Fig. 5B, la fuerte banda de absorción de las membranas de PU electrohiladas a 3328 cm −1 puede atribuirse al estiramiento N-H; la banda a 2919 cm −1 se asigna a la vibración de estiramiento del enlace C-H en PU; las bandas en 1704, 1729, 1529, 1073 y 771 cm −1 surgen de la vibración de flexión asimétrica C-H, vibraciones de estiramiento> C =H, banda amida II, estiramiento C-O y CH 2 balanceo, respectivamente [23,24,25]. Por otro lado, en comparación, la curva c en la Fig. 5B muestra el fenómeno de que cuando γ-Fe 2 O 3 Se incluyeron NP, no se observaron cambios evidentes en el espectro FTIR de las membranas fibrosas compuestas. Por ejemplo, el pico característico del enlace Fe-O también aparece a 557 cm −1 sin un cambio obvio en el espectro. Sin embargo, observamos un ligero cambio a 1073 cm −1 en la membrana de fibra compuesta, lo que significa un aumento en el enlace de hidrógeno entre el PU y γ-Fe 2 O 3 NP [26].
Las curvas de magnetización de γ-Fe 2 O 3 Las NP y las membranas fibrosas compuestas preparadas con / sin un electrodo auxiliar, medidas por VSM a 300 K, revelaron un comportamiento superparamagnético típico sin bucle de histéresis distintivo y valores de magnetización de 58,3, 10,7 y 10,0 emu / ga 15.000 Oe, respectivamente , lo que demuestra que todas las muestras poseen superparamagnetismo (Fig. 6A) [5, 27]. La disminución obvia en el valor de magnetización de los dos tipos de membranas fibrosas compuestas en comparación con γ-Fe 2 O 3 Los NP a 15.000 Oe pueden atribuirse a la existencia de PU no magnético que contiene las nanopartículas magnéticas y la distribución no homogénea de las nanopartículas magnéticas en las membranas fibrosas compuestas [28, 29]. Sin embargo, los valores de magnetización de los dos tipos de membranas fibrosas compuestas preparadas con diferentes electrodos muestran una desviación del valor teórico calculado por la relación de dopaje de γ-Fe 2 O 3 NP. La cantidad de γ-Fe 2 O 3 Las NP incorporadas en las membranas fibrosas compuestas se pueden estimar mediante la ecuación:
$$ \ mathrm {Dopaje} \ \ mathrm {proporción} \ \ mathrm {de} \ \ upgamma - {\ mathrm {Fe}} _ 2 {\ mathrm {O}} _ 3 \ \ mathrm {nanopartículas} =\ kern0.5em \ mathrm {Mb} / \ mathrm {Ma} \ times 100 \% $$ (1)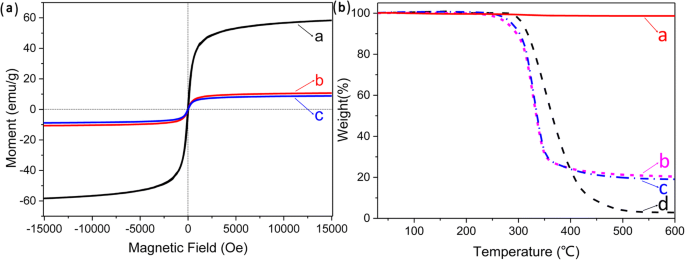
un Curvas de magnetización dependientes del campo de ( a ) γ-Fe 2 O 3 NP y γ-Fe 2 O 3 / Membranas de fibra compuesta de PU preparadas ( b ) con y ( c ) sin el uso de un electrodo auxiliar a temperatura ambiente. b Curvas termogravimétricas de ( a ) γ-Fe 2 O 3 NP, γ-Fe 2 O 3 / Membranas de fibra compuesta de PU preparadas ( b ) con y ( c ) sin el uso de un electrodo auxiliar, y ( d ) membranas de fibra pura electrohilada de PU
donde Ma, Mb son el valor de magnetización de γ-Fe 2 puro O 3 nanopartículas y membranas nanofibrosas compuestas a 15.000 Oe, respectivamente. Según Eq. (1), las relaciones de dopaje reales son aproximadamente del 18,3% y el 17,1% en las membranas compuestas preparadas con / sin el electrodo auxiliar. Además de las influencias tanto del PU como de la distribución de nanopartículas magnéticas en membranas fibrosas compuestas, la precipitación de γ-Fe 2 O 3 Los NP durante el proceso de electrohilado también juegan un papel crítico en el valor de magnetización. La medición precisa de la relación de dopaje de γ-Fe 2 O 3 Los NP se pueden realizar aún más mediante el análisis termogravimétrico (TGA).
Para confirmar la relación en peso de γ-Fe 2 O 3 NP y estabilidad térmica de las membranas fibrosas compuestas, se realizó la TGA (Fig. 6B). Como muestra la curva a en la Fig. 6B, la masa de γ-Fe 2 O 3 NPs no disminuye significativamente con el aumento de temperatura. La temperatura de descomposición térmica inicial (~ 260 ° C) de las membranas fibrosas compuestas es más baja que la de la membrana fibrosa PU pura (~ 305 ° C), lo que satisface completamente la estabilidad térmica exigida de las membranas fibrosas compuestas para el tratamiento térmico magnético. (curvas b, cyd en la Fig. 6B). Luego, en el rango de temperatura de 305 a 425 ° C, las membranas fibrosas de PU muestran una degradación constante (curva en la Fig. 6B). Cuando la temperatura alcanza hasta 500 ° C, no hay un peso residual obvio para la membrana fibrosa de PU en comparación con las membranas fibrosas compuestas. Se puede inferir de la fracción residual de las membranas fibrosas compuestas que el γ-Fe 2 O 3 Los NP dopados en las membranas compuestas son 19,1% en peso y 20,4% en peso, que corresponde a los resultados estimados de VSM. Comparando las relaciones de peso residual de las membranas fibrosas compuestas preparadas con / sin un electrodo auxiliar, es obvio que la adición del electrodo auxiliar no afecta la cantidad de dopaje de las partículas magnéticas en las membranas fibrosas compuestas. Esta pequeña desviación del γ-Fe 2 incrustado O 3 Los NP pueden atribuirse al proceso de electrohilado.
Mediciones de hipertermia in vitro
La hipertermia de nanopartículas magnéticas utiliza la capacidad del superparamagnético γ-Fe 2 O 3 NP para generar calor bajo la acción de HMA de alta frecuencia [30]. El mecanismo de pérdida del γ-Fe 2 O 3 Los NP bajo el AMF deben considerarse, respectivamente, si el γ-Fe 2 O 3 Los NP están dispersos o agregados. Aunque la generación de calor del agregado γ-Fe 2 O 3 El NP está determinado por la pérdida por histéresis y la interacción intermolecular [31], el γ-Fe 2 disperso O 3 Los NP vienen dados por la relajación de Brown y Néel [32]. Y el γ-Fe 2 O 3 Los NP se incorporan y fijan dentro de las fibras, por lo que la rotación libre de γ-Fe 2 O 3 Los NP pueden excluirse y la relajación de Brown no contribuye al calentamiento magnético que tiene lugar bajo el AMF. Para las nanopartículas magnéticas incrustadas, solo las pérdidas por histéresis y la relajación de Neel tienen un impacto crítico en el calentamiento de la pérdida por inversión magnética. La propiedad real de generación de calor dependiente de AMF del γ-Fe 2 O 3 Los NP dopados en fibras poliméricas no son fáciles de estimar debido a la compleja interacción magnética de las fases mixtas y la estructura de las membranas fibrosas compuestas, la agregación local y la dispersión parcial del γ-Fe 2 O 3 NP [33]. Por lo tanto, la propiedad real de generación de calor dependiente de AMF de la estructura mixta del γ-Fe 2 disperso y agregado O 3 Los NP en la estera de fibra se pueden evaluar adecuadamente mediante el comportamiento térmico experimental. Por lo tanto, el efecto de conversión magnética se realizó exponiendo membranas fibrosas compuestas a un AMF. La Figura 7 muestra las curvas de calentamiento dependientes del tiempo de membranas fibrosas de PU puro y diferentes fibras compuestas magnéticas. Como se muestra en la Fig. 7a, el aumento de temperatura fue de 10,5 ± 0,4, 16,2 ± 0,3, 19,1 ± 0,5 y 24,4 ± 0,3 ° C para γ-Fe 2 O 3 / PU-A5, γ-Fe 2 O 3 / PU-A10, γ-Fe 2 O 3 / PU-A15 y γ-Fe 2 O 3 / Membranas fibrosas compuestas PU-A20, respectivamente. Y en la Fig.7b, correspondiente a las membranas compuestas preparadas sin la adición de un electrodo auxiliar, el aumento de temperatura fue 4.2 ± 0.3, 5.1 ± 0.2, 6.7 ± 0.4 y 9.3 ± 0.2 ° C para γ-Fe 2 O 3 / PU-5, γ-Fe 2 O 3 / PU-10, γ-Fe 2 O 3 / PU-15 y γ-Fe 2 O 3 / Membranas compuestas PU-20, respectivamente. Se observó que la temperatura de calentamiento de todas las fibras compuestas magnéticas aumentaba rápidamente con el paso del tiempo y parecía llegar finalmente y básicamente mantener un equilibrio al final del período de examen. Además, un aumento progresivo en la velocidad de calentamiento y la temperatura de calentamiento emergió en ambas membranas fibrosas compuestas preparadas de dos formas diferentes, a medida que aumentaba el tiempo para preparar las membranas fibrosas compuestas magnéticas, y en donde la existencia de γ-Fe 2 O 3 Los NP se confirmaron mediante difracción XRD y análisis morfológico. Sin embargo, en el mismo tiempo de preparación, la velocidad de calentamiento de las membranas fibrosas compuestas preparadas con la ayuda del electrodo auxiliar fue más rápida y la temperatura estable fue más alta que la del otro. Por ejemplo, la velocidad de calentamiento de las membranas fibrosas compuestas obtenidas por electrohilado durante 15 min con la ayuda del electrodo auxiliar es de 0,42 ° C / s, y la temperatura de equilibrio es de 44,3 ° C. Moreover, if a fiber membrane having the same heating capacity is desired, a spinning time of 20 min is required with the aid of an auxiliary electrode, which means that the addition of the auxiliary electrode can remarkably improve the spinning efficiency and make full use of the spinning precursor. The results thus clearly indicate that the heating rate and the upper limit of the temperature rise are both remarkably improved compared to the composite membranes obtained without the aid of the auxiliary electrode. In contrast, the pure PU nanofibrous membranes showed slight temperature change under the identical conditions, which could be assigned to the influence of measurement error and the ambient temperature.
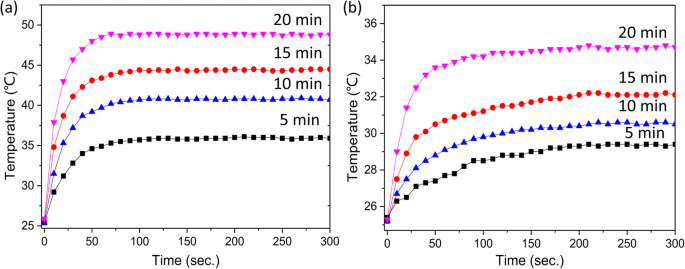
Temperature (T)-time (t) profiles for the electrospun fiber membranes prepared by in situ electrospinning a con y b without the use of an auxiliary electrode for 5, 10, 15, and 20 min upon the application of AMF
In the case of cancer therapy, the high- and low-temperature cycle of hyperthermia treatment is preferred along with other hyperthermia modes due to the chance of tumor metastasis, which means it is necessary for composite fibrous membranes to possess a uniform cyclic profile with a constant temperature rise during the heating process [34]. To test the heat stability of γ-Fe2 O 3 /PU composite fibrous membranes, γ-Fe2 O 3 /PU-A15 membranes were exposed to AMF for different cycles. As shown in Fig. 8, no obvious change in the elevated temperature profiles was observed during the three cycles of AMF effect, which indicated that the γ-Fe2 O 3 /PU composite fibrous membranes could efficiently and rapidly convert AMF energy into thermal energy. More importantly, significant superiority of the composite fibrous membranes for cancer hyperthermia treatment was their capability for repeatable heating without damaging the heating efficiency.
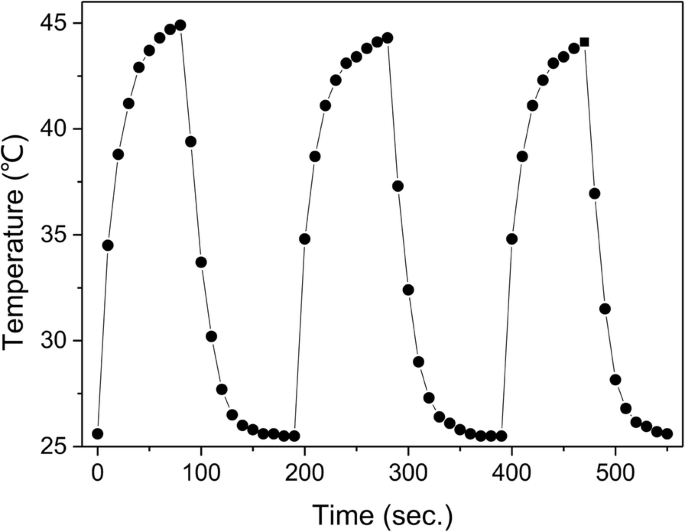
Cyclic heating profile of the electrospun fiber membranes prepared by in situ electrospinning
As mentioned above, the portable electrospinning device with the aid of an auxiliary electrode can quickly and precisely deposit the electrospun fiber membrane on the collecting pole in situ, which is in favor of the close contact between the prepared electrospun fiber membrane and the affected area, and improves the heating efficiency of the magnetocaloric therapy. Moreover, the thermotherapy fibers containing chemotherapeutic drugs can also be prepared in situ on the tumor tissue, which is beneficial to the synergistic effect of the drug and hyperthermia. As shown in Fig. 9, the electrospun fiber membrane can be prepared in situ on the surface of a hand. As can be found in Fig. 9a, a thin PU composite fibrous membrane is formed on the surface of the hand by a portable electrostatic spinner without an auxiliary electrode. Figure 9b shows that a tightly bonded, precisely deposited magnetic fibrous membrane is fabricated on the scar of the hand, which just like a second layer of skin due to the electrostatic attraction force. The mark has been completely covered by the magnetic fibrous membrane, while other skin tissue is not affected, which means a good versatility of the in situ preparation of magnetic fiber membranes under the assist of an auxiliary electrode.
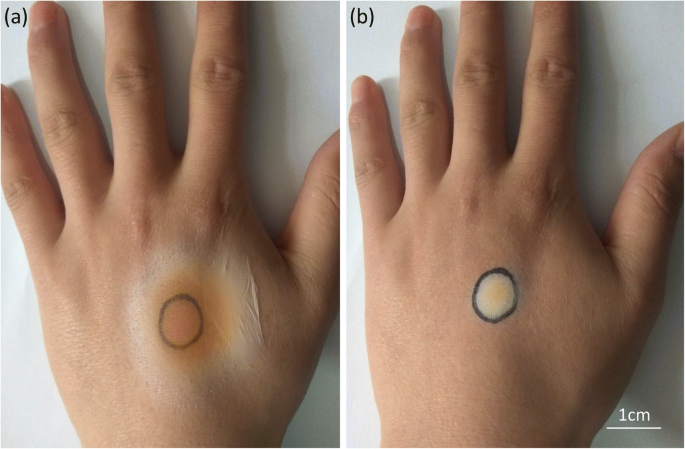
Schematic of in situ electrospun magnetic fibrous membrane on the surface of hand a without an auxiliary electrode and b with an auxiliary electrode
Conclusiones
In summary, a magnetic composite nanofiber membrane was fabricated in situ using a portable electrospinning device with the aid of an auxiliary electrode. In the electrospinning process, the addition of the auxiliary electrode prolongs the stable area of the electrospinning and reduces the fiber whipping, thereby reducing the deposition range of the fiber and accelerating the fiber deposition rate. For electrospinning techniques, the application of conical auxiliary electrodes to precisely control the deposition area is suitable for most electrospinning materials. Moreover, the microstructure (diameter, surface morphology) of the electrospinning fiber is not significantly affected. The in situ prepared magnetic composite nanofibrous membranes can convert the AMF energy to the thermal energy to elevate temperature efficiently. With the aid of the auxiliary electrode, the composite fibrous membrane prepared by in situ electrospinning showed efficient heating ability upon the application of AMF, and well-maintained cyclic heating performance under the presence of AMF. These results indicate that the magnetic composite fibrous membrane prepared in situ by the auxiliary electrode is an excellent candidate for the magnetic hyperthermia of cancer therapy.
Abreviaturas
- AMF:
-
Alternating magnetic field
- DMF:
-
N , N -Dimetilformamida
- FTIR:
-
Fourier transformer infrared spectrometer
- INOPs:
-
Iron oxide nanoparticles
- MES:
-
Magnetic electrospinning
- PU:
-
Polyurethane
- SEM:
-
Microscopía electrónica de barrido
- TEM:
-
Microscopio electrónico de transmisión
- TGA:
-
Thermogravimetric analysis
- VSM:
-
Vibration sample magnetometer
- XRD:
-
X-ray powder diffraction
Nanomateriales
- Nanofibras y filamentos para una mejor administración de fármacos
- Nanodiamantes para sensores magnéticos
- Tecnologías avanzadas de deposición de capas atómicas para micro-LED y VCSEL
- Nanofibras poliméricas electrohiladas decoradas con nanopartículas de metales nobles para detección química
- Propiedades eléctricas de materiales compuestos con alineación asistida por campo eléctrico de rellenos de nanocarbono
- Fabricación de alto rendimiento de nanofibras de calidad utilizando un electrohilado de superficie libre modificado
- Microesferas de carbono magnéticas como adsorbente reutilizable para la eliminación de sulfonamidas del agua
- Deposición de capa atómica de nanopelículas de óxido de indio para transistores de película delgada
- Un ánodo de película de Fe2O3 nanocristalino preparado por deposición de láser pulsado para baterías de iones de litio
- Síntesis sencilla de nanocompuestos magnéticos funcionalizados en superficie para una adsorción selectiva eficaz de colorantes catiónicos
- Desarrollo de biocompuesto electrohilado de quitosano-óxido de polietileno / fibrinógeno para posibles aplicaciones de cicatrización de heridas



