Ajuste de la química superficial de la polieteretercetona mediante revestimiento de oro y tratamiento con plasma
Resumen
La polieteretercetona (PEEK) tiene buenas propiedades químicas y biomecánicas que son excelentes para aplicaciones biomédicas. Sin embargo, PEEK exhibe características de superficie hidrófobas y de otro tipo que provocan una adhesión celular limitada. Hemos investigado el potencial del tratamiento con plasma de Ar para la formación de una superficie de PEEK nanoestructurada con el fin de mejorar la adhesión celular. El objetivo específico de este estudio fue revelar el efecto de la interfaz de las matrices PEEK tratadas con plasma y recubiertas de oro sobre la adhesión y la propagación de fibroblastos embrionarios de ratón. Las características de la superficie (polaridad, química de la superficie y estructura) antes y después del tratamiento se evaluaron mediante diversas técnicas experimentales (gravimetría, goniometría, espectroscopia de fotoelectrones de rayos X (XPS) y análisis electrocinético). Además, se empleó microscopía de fuerza atómica (AFM) para examinar la morfología y rugosidad de la superficie de PEEK. La respuesta biológica de las células hacia la PEEK nanoestructurada se evaluó en términos de adhesión, propagación y proliferación celular. La morfología celular detallada se evaluó mediante microscopía electrónica de barrido (SEM). En comparación con el tratamiento con plasma, el revestimiento de oro mejoró la humectabilidad del PEEK. El método XPS mostró una disminución en la concentración de carbono con el aumento del tiempo de tratamiento con plasma. La adhesión celular determinada en la interfaz entre las matrices PEEK tratadas con plasma y recubiertas de oro fue directamente proporcional al espesor de una capa de oro en una muestra. Nuestros resultados sugieren que el tratamiento con plasma en combinación con una capa de oro podría usarse en aplicaciones biomédicas que requieren una adhesión celular mejorada.
Antecedentes
Uno de los problemas del envejecimiento humano es el desgaste de las articulaciones, que se relaciona con un fuerte aumento en la abundancia de diversas afecciones del sistema esquelético y articular, incluidas fracturas, degeneraciones vertebrales, artritis y tumores óseos. Las cirugías ortopédicas con implantes artificiales son actualmente el principal método utilizado para la renovación estructural y funcional de huesos y articulaciones dañados. Los materiales que se utilizan comúnmente para los implantes ortopédicos son especialmente metales, cerámicas, polímeros y compuestos. Los implantes metálicos (p. Ej., Oro) se utilizan ampliamente en la práctica clínica, ya sea como reemplazos permanentes (p. Ej., Reemplazos de cadera, dientes artificiales) o como prótesis temporales (p. Ej., Discos, bisagras, tornillos y varillas que se utilizan para reparar fracturas). Los metales se ven favorecidos por su resistencia mecánica, resistencia al desgaste y no toxicidad [1, 2, 3]. Por otro lado, su alta resistencia mecánica y baja elasticidad son incompatibles con el tejido esquelético humano. Esto podría tener un impacto negativo en un implante óseo, lo que puede provocar la absorción de un tejido óseo adyacente y la liberación del implante. Polímeros como polietileno de peso molecular ultra alto (UHMWPE), politetrafluoretileno (PTFE), polimetilmetacrilato (PMMA), polilactida (PLA), poliglicólido (PGA) y polihidroxibutirato (PHB) se utilizan ampliamente en diversas aplicaciones biomédicas. Pero solo se ha utilizado un número limitado de polímeros como reemplazos de huesos o articulaciones, ya que tienden a ser demasiado flexibles y débiles para cumplir con las demandas impuestas a los implantes ortopédicos mecánicos [4, 5].
La polieteretercetona (PEEK) es un polímero termoplástico aromático policíclico lineal semicristalino sintetizado por primera vez en 1978 [6]. El PEEK se utiliza comúnmente como material para espaciadores intervertebrales y tornillos para huesos [7, 8]. Debido a su estructura química especial, PEEK tiene una alta resistencia a los cambios químicos y físicos [6, 9, 10]; además, es resistente al desgaste y estable a altas temperaturas [6]. Además, se demostró la biocompatibilidad de PEEK tanto in vitro como in vivo y no causa ningún efecto tóxico o mutágeno [11,12,13]. Su gran ventaja es la elasticidad similar a la de un hueso humano, que permite una distribución equilibrada del peso entre un implante y un hueso; por lo tanto, no existe un efecto de protección contra el estrés después de la implantación. Sin embargo, PEEK exhibe propiedades hidrófobas y bioinertes, que no son favorables para la adsorción de proteínas y la adhesión celular [14, 15]. Por lo tanto, para mejorar estas propiedades, es necesario modificar la superficie de PEEK.
Las características superficiales de los materiales se pueden ajustar mediante diversas técnicas [16]. Uno de estos métodos es la modificación de una superficie de biopolímero por plasma, que utiliza gas ionizado producido en un sistema de reactor cerrado que contiene gas a baja presión y un aparato para la excitación electromagnética de gas. En comparación con las técnicas húmedas, la modificación con plasma de una superficie de biopolímero es ventajosa para la flexibilidad química. Las partículas reactivas generadas electromagnéticamente interactúan con la superficie del biopolímero en un reactor provocando un cambio en sus propiedades físicas y químicas. Las propiedades mecánicas, eléctricas y ópticas del material a granel, relevantes para su aplicación, permanecen sin cambios [17], lo que es ventajoso en el diseño, desarrollo y fabricación de polímeros biocompatibles. Otro método utilizado para mejorar las propiedades de la superficie del polímero es la pulverización catódica. La integración de nanopartículas de oro en una película delgada es importante para diversas aplicaciones, por ejemplo, ingeniería de tejidos y detección biológica [18]. El tamaño de las nanopartículas influye en el comportamiento y las propiedades superficiales de la superficie del material (por ejemplo, densidad, parámetro de red, propiedades eléctricas y ópticas) [19]. Especialmente las nanopartículas de menos de 100 nm a menudo mejoran la adhesión y la proliferación celular [20].
El objetivo de este trabajo fue formar nanoestructuras en PEEK mediante tratamiento con plasma y deposición de oro para mejorar la adhesión y proliferación celular, específicamente de fibroblastos embrionarios de ratón (L929). Las características de la superficie (polaridad, química de la superficie y estructura) antes y después del tratamiento se evaluaron mediante diversas técnicas (gravimetría, goniometría, espectroscopia de fotoelectrones de rayos X y análisis electrocinético). Además, se empleó microscopía de fuerza atómica para examinar la morfología y rugosidad de la superficie de PEEK. Los resultados se discuten en el contexto de posibles aplicaciones biomédicas, principalmente para su posible utilización en la construcción de implantes espinales y otros reemplazos para ortopedia y traumatología.
Métodos
Materiales y modificaciones
Una lámina de PEEK (el grosor de 50 μm, la densidad de 1,26 g cm −3 , suministrado por Goodfellow Ltd., Reino Unido) se utilizó para todos los experimentos. Todas las muestras de PEEK (circular, ø =2 cm) se trataron con plasma, seguido de un recubrimiento de oro en la mitad de cada muestra. Las muestras de PEEK se trataron en directo (brillo, diodo) Ar + plasma utilizando un dispositivo Balzers SCD 050 (BalTec AG, Pfäffikon, CH) en las condiciones descritas en [18, 21]. Los tiempos de tratamiento fueron de 60 y 240 s, y la potencia de descarga fue de 8,3 W. El revestimiento de oro de PEEK se logró mediante el dispositivo Balzers SCD 050 a partir de un objetivo de oro (la pureza del 99,95%, suministrado por Safina Ltd., CZ). Las condiciones de deposición fueron DC Ar + plasma; pureza del gas del 99,995%; tiempos de pulverización catódica de 30, 150 y 300 s, corriente de 40 mA (potencia de descarga 15 W); y Ar total + presión. La distancia del electrodo, la densidad de potencia y la tasa de deposición promedio se ajustaron de manera similar como se describe en [18, 22]. Las muestras preparadas se almacenaron en condiciones de laboratorio (24 ° C, 40-60% de humedad) [23].
Técnicas de medición
Gravimetría
El espesor medio de las películas de oro se midió por gravimetría utilizando una microbalanza Mettler Toledo UMX2. El espesor se calculó a partir de los pesos de las muestras antes y después de la pulverización catódica utilizando la densidad aparente del oro. Se utilizaron diez muestras de cada tipo de modificación para la medición. El error de la medición gravimétrica fue inferior al 15%.
Ángulo de contacto
La humectabilidad de las muestras se determinó midiendo sus ángulos de contacto con el agua superficial (WCA). Además, la caracterización de los cambios estructurales y de composición causados por el tratamiento con plasma y la deposición de oro se determinó mediante el sistema de análisis de forma de gota DSA 100 (KRÜSS GmbH, DE) a temperatura ambiente (24 ° C, 40-60% de humedad) [23]. Se depositaron gotas de agua de 2,0 ± 0,2 μL sobre las muestras analizadas utilizando una aguja de acero inoxidable. Las imágenes de las gotas se tomaron después de un retraso de 2 s. Luego, se evaluaron los ángulos de contacto utilizando el sistema ADVANCE. Se realizaron al menos siete mediciones de diferentes posiciones en al menos tres réplicas de cada muestra y se promediaron para producir el WCA final y su desviación estándar. La medición de WCA se realizó en muestras "envejecidas" durante 14 días.
Espectroscopía fotoelectrónica de rayos X
La composición química de las muestras preparadas se determinó a partir de espectros de fotoelectrones de rayos X (XPS) medidos (tres mediciones) mediante el espectrómetro ESCAProbeP de Omicron Nanotechnology (suministrado por Omicron Nanotechnology GmbH, DE) con un error relativo del 10%. La dimensión del área expuesta y analizada fue de 2 × 3 mm 2 . Las condiciones de medición se describen en [18, 21]. El carbono característico (1 s ), oxígeno (1 s ) y oro (4 f ) se buscaron picos. La medición se realizó en un vacío ultraligero. La evaluación de los espectros adquiridos se llevó a cabo mediante el código CasaXPS [24]. Las muestras utilizadas para la medición se “envejecieron” durante 14 días. Antes de la medición, las muestras se almacenaron en condiciones estándar de laboratorio.
Potencial Zeta
El análisis electrocinético (potencial electrocinético, potencial zeta) de todas las muestras fue determinado por SurPASS Instrument (Anton Paar). Las muestras se estudiaron dentro de una celda de espacio ajustable en contacto con un electrolito (0,001 mol L −1 KCl) así como en una solución tamponada (solución salina tamponada con fosfato (PBS)). Para cada medición, se fijó un par de películas de polímero con la misma capa superior en dos portamuestras (con una sección transversal de 20 × 10 mm 2 y un espacio entre ellos de 100 μm). Todas las muestras se prepararon en dos repeticiones; todos ellos fueron medidos tres veces a pH constante de 6,8 con el error experimental del 5%. Para la determinación del potencial zeta, se utilizó el método de corriente continua y se aplicó la ecuación de Helmholtz-Smoluchowski para calcular el potencial zeta [25, 26, 27]. Las muestras envejecidas utilizadas para medir el potencial zeta se "envejecieron" durante 14 días.
Microscopía de fuerza atómica
La morfología de la superficie de las muestras se examinó mediante microscopía de fuerza atómica (AFM) utilizando el sistema VEECO CP II (Bruker Corporation, Billerica, MA, EE. UU.). La superficie se midió en un "modo de golpeteo" usando una sonda RTESPA-CP dopada con silicio P con la constante de resorte de 20-80 N m −1 (Bruker Corporation, Billerica, MA, EE. UU.). Mediante mediciones repetidas de la misma región (1 × 1 μm 2 ), verificamos que la morfología de la superficie no cambió después de tres exploraciones consecutivas. Las muestras utilizadas para la medición se envejecieron durante 14 días.
Espectroscopia de masas de plasma de acoplamiento inductivo
Se utilizó plasma acoplado inductivamente con detector de espectroscopía de masas (ICP-MS) para determinar la cantidad de iones Au liberados en PBS (pH =7,4). El análisis de elementos traza de los lixiviados de Au se realizó utilizando un espectrómetro de triple cuadrupolo Agilent 8800 (Agilent Technologies, Japón) conectado a un muestreador automático. La nebulización de la muestra se realizó utilizando un dispositivo MicroMist equipado con una bomba peristáltica. La incertidumbre de la medición (triplicados de cada muestra) fue inferior al 3%. Las lixiviaciones para ICP-MS se prepararon mediante incubación estática de las muestras en PBS en atmósfera humidificada con 5% CO 2 a 37 ° C durante 6, 24 y 72 h. Las lixiviaciones se diluyeron con agua destilada en una proporción de 1:8 y se analizaron.
Cultivo celular
De acuerdo con la norma internacional EN ISO 10993-5, las pruebas de citocompatibilidad se realizaron in vitro utilizando la línea celular L929 de fibroblastos de ratón (Sigma, EE. UU.). Las muestras de PEEK (prístinas, tratadas con plasma y recubiertas de oro) se esterilizaron en etanol al 70% en viales de contador de centelleo durante 20 min, se insertaron en placas de 12 pocillos (Jet Biofil, Ø 2,14 cm), se lavaron con PBS y se montaron en el pocillo. fondo con cilindros de plástico huecos de poli (metacrilato de metilo). Se sembraron células L929 en la parte superior de las muestras en una densidad de 30.000 células por pocillo en 1 ml de medio de Eagle modificado de Dulbecco con alto contenido de glucosa (DMEM, Sigma, EE. UU.) Que contenía suero bovino fetal al 10% (FBS, Invitrogen, EE. UU.) Y 2 mM l-glutamina estable (l-alanil-l-glutamina, Sigma, EE. UU.). Las células L929 se mantuvieron a 37 ° C en atmósfera humidificada con 5% de CO 2 .
Microscopía de fluorescencia
Después del tiempo de incubación deseado (6, 24 y 72 h), las células se fijaron y se tiñeron de manera similar como se describe en [28, 29]. Las células L929 se lavaron con PBS y se fijaron con formaldehído al 4% (Thermo Scientific, EE.UU.) en PBS (37ºC, 20 min). Después del lavado con PBS, se marcó F-actina del citoesqueleto celular con faloidina-Atto 565 (Sigma, EE.UU.) en PBS durante 20 min. Luego, los núcleos celulares se tiñeron con DAPI (dihidrocloruro de 4 ', 6-diaminido-2-fenilindol, Sigma, EE. UU.) Durante 10 min, y las células se enjuagaron con PBS, se cubrieron con medio de montaje (Vector Laboratories, EE. UU.) Y montado entre un portaobjetos de vidrio microscópico y un cubreobjetos. Todas las muestras ("envejecidas" durante 14 días) se analizaron por triplicado.
Microscopía electrónica de barrido
La morfología detallada de las células examinadas que crecen en PEEK prístino, interfaz plasma / oro y un control (cubreobjetos de vidrio) se caracterizó mediante microscopía electrónica de barrido (SEM) TESCAN LYRA3 GMU (Tescan, CZ) en un modo de electrones secundarios. Las células destinadas al análisis por SEM se lavaron con PBS, se fijaron con solución de Karnovsky [30, 31] en tampón de cacodilato 0,1 M (pH 7,2) y se deshidrataron (porcentaje creciente de etanol seguido de dos pasos finales de incubación de 10 minutos en hexametildisilazano y secar en un horno a 40 ° C durante 2 h). Las muestras deshidratadas se recubrieron con una capa de oro de 10 nm.
Resultados y discusión
Todas las mediciones se realizaron con muestras "envejecidas" 14 días después del tratamiento con plasma y la pulverización catódica de oro. Es bien sabido que los grupos funcionales formados en la superficie de un polímero tratado con plasma no son estables y cambian con el tiempo [32]. La superficie del material tiende a recuperarse a su estado sin tratar [33]. Por lo tanto, ocurre cambiar la reorientación de los grupos químicos producidos por el tratamiento con plasma en la mayor parte del material [34, 35].
La ablación de PEEK durante el tratamiento con plasma seguido de la pulverización catódica con Au se estudió por gravimetría. La pérdida de masa de un polímero causada por la ablación y el crecimiento de masa por pulverización catódica se convirtieron consecutivamente en espesor de polímero. Las pérdidas de masa determinadas después del tratamiento con plasma (60 y 240 s, la potencia de 8,3 W) se muestran en la Tabla 1. La pérdida de ablación pronunciada fue evidente al aumentar el tiempo de exposición, pero simplemente se duplicó. La leve pérdida fue causada probablemente por el carácter aromático de PEEK, que resultó en una mayor resistencia a la escisión que en el caso de, por ejemplo, cadenas alifáticas de poliolefinas (UHMWPE). Para la pulverización catódica de oro, los períodos de tiempo de 30 y 300 s se determinaron como ejemplos representativos de capas continuas y discontinuas [19, 36]. La disminución de las pérdidas por ablación ha dado como resultado un mejor anclaje del oro en la superficie de PEEK, como es obvio para las muestras con revestimiento de oro de 150 y 300 s.
Los valores del ángulo de contacto con el agua de las muestras medidas en función del tratamiento con plasma y el tiempo de pulverización de oro se muestran en la Tabla 2. Después del tratamiento con plasma, el WCA aumentó de 79,5 ± 2,4 ° (PEEK prístino sin modificar) a 94,0 ± 5,5 ° y a 95,6 ± 2,1 ° (PEEK tratado con plasma durante 60 y 240 s, respectivamente). La diferencia en los valores de WCA después del tratamiento con plasma es insignificante en comparación con las desviaciones del valor. El WCA disminuye con el recubrimiento de Au y la superficie se vuelve más hidrófila en comparación con la de las muestras tratadas con plasma.
La concentración de elementos en la superficie del polímero (la profundidad accesible de seis a ocho capas atómicas) se examinó mediante el método XPS; los resultados se resumen en la Tabla 2. Los datos de XPS se obtuvieron para PEEK prístina, una muestra tratada con plasma y una muestra tratada con plasma seguida de recubrimiento de Au. A partir de la medición de XPS, se puede ver que la concentración de oxígeno ha aumentado con el tratamiento prolongado. Esto probablemente se debió a la reorientación de los grupos que contienen oxígeno en el volumen del polímero [37,38,39]. Se comprobó que la orientación de los grupos ocurre inmediatamente después del tratamiento con plasma; así, en el “proceso de envejecimiento” de la muestra, se producen cambios en la superficie de la misma. Por esta razón, las muestras se midieron durante 14 días después del tratamiento con plasma, cuando el estado de “envejecimiento” de una muestra se estabiliza [40, 41]. La concentración de oxígeno aumentó con el tratamiento prolongado con plasma. La superficie del polímero se rompe por una descarga de plasma más fuerte con la creación de sitios de radicales en la superficie; cuanto mayor sea la potencia del plasma, más pronunciada será la modificación del polímero. Estos sitios reaccionan con el oxígeno presente en el aire y aumentan la concentración de oxígeno en la superficie tratada [42, 43]. Después de la pulverización catódica de oro, la concentración de oxígeno disminuye a expensas de la capa de oro. La concentración del oro se incrementó con un menor tiempo de pulverización, cuando la superficie no estaba tan rota.
La figura 1 muestra la morfología de la superficie de PEEK obtenida mediante AFM. El tratamiento con plasma provocó cambios detectables en la superficie de PEEK para ambos tiempos de exposición (60 y 240 s), pero como era de esperar, una exposición más prolongada al plasma dio como resultado una superficie más rugosa que provocó una diferencia en la metalización de las muestras. Las muestras tratadas con plasma durante períodos más prolongados formaron grupos de metales mejor definidos. Este efecto fue especialmente evidente en muestras con capas de oro gruesas (pulverizadas durante 300 s) y también muy delgadas (pulverizadas durante 30 s). Las muestras tratadas con plasma durante un período corto (60 s) formaron un número menor de conglomerados más grandes e irregulares. En cuanto a las capas pulverizadas solo durante 30 s, los racimos de metal eran fácilmente reconocibles solo en el sustrato tratado con plasma durante 240 s. Como era de esperar, el tamaño del racimo y la rugosidad de la superficie generalmente aumentan con el tiempo prolongado de pulverización de oro. Este comportamiento se corresponde bien con la medición XPS. Las muestras pulverizadas con metal durante 30 s ya tenían la mayor parte de su superficie cubierta por metal y la pulverización ulterior provocó un crecimiento mayoritariamente vertical de los racimos; por lo tanto, no tuvo un impacto tan significativo en la concentración de oro y aún dejó una superficie de polímero parcialmente descubierta. Además, una diferencia en la forma de los grupos en función de la duración del tratamiento con plasma se correspondía bien con los hallazgos de XPS. Grandes racimos irregulares en muestras tratadas con plasma solo durante un período corto (60 s) cubrieron una porción relativamente grande de la superficie de PEEK; por tanto, la concentración de oro determinada mediante XPS se incrementó ligeramente. Las diferencias morfológicas entre materiales prístinos pulverizados con una capa de metal de diferente espesor pueden compararse con los datos obtenidos para el ácido poli-l-láctico (PLLA) [44] y el politetrafluoretileno (PTFE) [45]. El PTFE prístino tiene una superficie muy rugosa; por lo tanto, no observamos la formación de pequeños grupos de metales sino una disminución general de la rugosidad de la superficie. Esto es causado por un fenómeno de que un metal pulverizado prefiere llenar "valles" en la superficie del polímero para permanecer en "picos". Por otro lado, la superficie PLLA muestra un aumento de granulación y formación de estructuras similares a las estructuras en PEEK, pero con menor regularidad. Estos datos sugieren que la formación de una estructura granular regular en polímeros pulverizados está fuertemente influenciada por la regularidad de la superficie del polímero; por lo tanto, PEEK (polímero con la menor rugosidad superficial entre PEEK, PLLA y PTFE) permite la formación de la mayoría de los grupos de metales regulares en la superficie.

Imágenes AFM de PEEK prístino, PEEK tratado con plasma (pl) durante 60 y 240 s, y oro (Au) pulverizado durante 30, 150 y 300 s
El análisis electrocinético mostró cambios en la química de la superficie de PEEK y la carga después de los pasos individuales de modificación de la superficie. En el primer paso, el tratamiento con plasma condujo a la creación de nuevos grupos polares en la superficie de PEEK, lo que resultó en un aumento del potencial zeta [19, 25,26,27]. En la segunda modificación, la deposición de racimos de oro en la superficie de la muestra también tuvo un impacto en la química de la superficie y el potencial zeta (Fig. 2). Debido a la presencia de un metal en la superficie del polímero, el efecto de un cambio de carga superficial juega un papel importante:la acumulación de electrones [27, 46]. También observamos diferentes potenciales zeta para muestras frescas y "envejecidas". Se detectaron cambios más dramáticos para el potencial zeta medido en PBS, que fue dado por iones de diferentes concentraciones. Mientras está en solución de KCl, la concentración de KCl es 0.001 mol L −1 ; en PBS, la concentración de iones es tres órdenes más alta. Una mayor concentración de iones en PBS provoca la presión de una doble capa eléctrica y da como resultado una disminución del potencial zeta (en valor absoluto) [27, 46]. Por lo tanto, la concentración mucho mayor de iones provocó un cambio en la carga superficial incluso de valores negativos a positivos. Por lo tanto, los cambios del potencial zeta de PEEK determinados en la solución de PBS fueron más dramáticos y los cambios en la química de la superficie y la carga fueron más pronunciados. Por lo tanto, está claro que el tratamiento con plasma y la posterior deposición de Au conducen a cambios dramáticos en la química de la superficie del polímero y la carga que dependen de la duración del tratamiento con plasma así como de la deposición de Au. Estos resultados confirmaron otros análisis realizados.
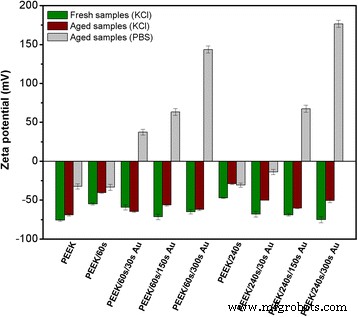
Potencial zeta de muestras PEEK tratadas con plasma (60 y 240 s) y de PEEK pulverizadas con Au (30, 150 y 300 s; corriente 40 mA) en una solución de KCl 1 mM ( columnas verdes —Muestras frescas; columnas marrones —Muestras envejecidas) y en solución PBS ( columnas grises )
Para determinar la concentración de oro liberado en un medio de cultivo durante el cultivo celular, utilizamos un sistema acuoso simple de PBS para simular estas condiciones. El oro liberado en PBS después de 6 (tiempo de adhesión celular) y 72 h (proliferación celular) de incubación estática se midió mediante ICP-MS, y los resultados se resumen en la Tabla 3. El PBS tiene el mismo pH y osmolaridad que el medio de cultivo celular.; por lo tanto, se utilizó para la medición de ICP-MS. Por un lado, PBS es un sistema simplificado; por otro lado, no hay componentes que interfieran potencialmente con la medición de ICP-MS, como es el caso de un medio de cultivo celular completo. Encontramos que la concentración de Au liberada en PBS fue mayor para las muestras de PEEK recubiertas con Au durante 30 s que durante 300 s. Esto podría deberse a un carácter discontinuo de la capa de oro que posiblemente forma pequeños grupos de oro que se disuelven más rápidamente [47]. El oro se liberó en mayor medida de la muestra PEEK / 60/300 que de PEEK / 240/300, ya que su superficie estaba menos ablacionada y el oro aparentemente estaba menos anclado.
En el siguiente paso, se examinó si la modificación de la superficie de los polímeros puede promover la adhesión de las células endoteliales. La superficie de PEEK se activó mediante tratamiento con plasma y pulverización catódica de oro. La citocompatibilidad de PEEK se determinó con base en los resultados de adhesión celular (6 h) y proliferación (24 y 72 h), como se muestra en la Fig. 3. Cada dos columnas (PEEK / plasma (ab) y PEEK / (ab) / Au (cde)) representan dos mitades de una muestra. Las diferencias en el número de células L929 que crecen en PEEK prístino y poliestireno de cultivo de tejidos de control (TCPS) están en el rango del error de medición. Se controló la adhesión celular 6 h después de la siembra de las células en la superficie de la muestra. Es obvio que el número de células de PEEK prístino aumentó en comparación con el de las muestras tratadas. Después de 24 h de crecimiento celular, observamos sólo un aumento muy leve en el número de células, que podría ser causado por una fase de retraso, cuando las células se adaptan al nuevo entorno [48]. Es evidente que 72 h después de la siembra, había un número muy pequeño de células creciendo en muestras depositadas durante 30 s (60 y 240 s tratadas con plasma) en comparación con otras muestras medidas. Estos valores se corresponden con los resultados de las mediciones de ICP-MS, en las que el oro se liberó en PBS en la mayor medida. En este caso, la capa de Au depositada sobre PEEK (durante 30 s) tenía un carácter discontinuo [36]; por tanto, los grupos de Au podrían liberarse en el medio de cultivo celular. Mediante este proceso, el medio puede volverse tóxico para las células cultivadas. El mayor número de células que crecen en una capa de oro (en comparación con la muestra tratada con plasma) se observó en la muestra PEEK / pl 60 s / 150 s, en la que la capa de oro era continua. A continuación, 72 h después de la siembra, el entorno más adecuado para el crecimiento de las células L929 fueron las muestras tratadas con plasma durante 60 o 240 sy posteriormente recubiertas con oro durante 300 s. La capa de Au en estas muestras también fue continua [36]. Según los datos de ICP-MS, solo se liberó una cantidad muy pequeña de Au en el medio de cultivo celular. Sin embargo, este oro liberado fue la causa probable del aumento de la proliferación celular en la superficie tratada con plasma.
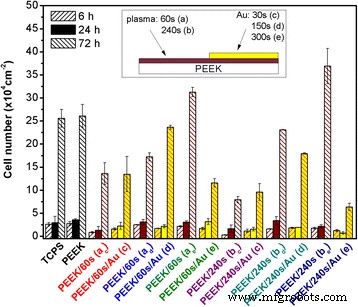
Número de células L929 después de 6, 24 y 72 h de cultivo en TCPS, PEEK prístino y PEEK con interfaces de oro de regiones tratadas con plasma (60 y 240 s) y pulverizadas con Au (30, 150 y 300 s)
Para evaluar aún más la morfología celular y las conexiones intercelulares con mayor detalle, realizamos microscopía electrónica de barrido de alta resolución de células L929 que crecían en los sustratos probados; los resultados se muestran en la Fig. 4. Las exploraciones del análisis SEM se realizaron después de 72 h de crecimiento celular en PEEK prístino y PEEK tratado con plasma y recubierto de oro, y un cubreobjetos de vidrio, que sirvió como control (se usa comúnmente para análisis SEM [49] así como para estudios de inmunofluorescencia [29]). De la Fig.4, es evidente que las células que crecen en PEEK prístino, PEEK tratadas con plasma durante 60 s (la segunda mitad es 300 s Au) y 240 s (la segunda mitad es 150 y 300 s Au), y en un cubreobjetos de vidrio tenía una forma similar después de 72 h de cultivo. Las células se extendieron por completo sobre la superficie tratada con plasma y, por encima de esta capa celular, es evidente la formación de una nueva capa de células en proliferación. Las células tenían una forma esférica en la superficie de muestras de PEEK / 60 (la segunda mitad es 150 s Au) y PEEK / 240/30 s Au, aunque el entorno no era adecuado para la proliferación celular. Las celdas más redondeadas se observaron en PEEK / 240/300 s Au, que se correlaciona completamente con los datos presentados en la Fig. 3.

Imágenes SEM de células L929 cultivadas durante 72 h en PEEK prístino, PEEK tratado con plasma (60 y 240 s), y sus partes recubiertas de oro pulverizadas durante 30 y 300 s (el cubreobjetos de vidrio microscópico sirvió como control). La barra de escala corresponde a 10 μm
Conclusiones
Comparamos dos formas diferentes de modificaciones de PEEK para crear un material con una mejor adhesión y crecimiento celular. Los resultados obtenidos confirmaron cambios variables en las propiedades de la superficie después de los pasos de modificación individuales. Ambas formas de modificación empleadas dieron como resultado cambios en la química de la superficie, morfología, humectabilidad y carga. El tratamiento con plasma durante 240 s provocó una pérdida de peso de PEEK hasta dos veces mayor que el tratamiento durante 60 s. La humectabilidad de la superficie de PEEK no cambió significativamente por el tratamiento con plasma. La medición de XPS confirmó el hecho general de que con el aumento del tiempo de tratamiento con plasma, la concentración de carbono disminuyó en la superficie de PEEK, al contrario de lo cual, la concentración de oxígeno aumentó. El espesor de una película de oro depositada fue mayor después del tratamiento con plasma durante 60 s. La pulverización de oro aumentó la humectabilidad de la superficie de PEEK. Los resultados del análisis XPS mostraron las mismas tendencias para ambas muestras tratadas con plasma (60 y 240 s), y las concentraciones de carbono y oxígeno disminuyeron con el aumento del tiempo de deposición a favor de la creciente concentración de oro. Las imágenes AFM también confirmaron las mediciones de XPS, especialmente para muestras tratadas con plasma durante 60 sy recubiertas de oro durante 300 s, en las que grandes grupos irregulares cubrían una porción relativamente grande de la superficie de PEEK; por lo tanto, la concentración de oro se incrementó ligeramente. También se descubrió que las muestras con una capa de oro delgada y también más gruesa no son adecuadas para la propagación celular.
Esta investigación muestra que el tratamiento con plasma mejora la citocompatibilidad de PEEK en comparación con el prístino. Además, el tratamiento con plasma es un método mejor para la modificación de polímeros para el crecimiento celular que la pulverización catódica de oro, cuando el oro se libera en el medio de cultivo celular.
Abreviaturas
- AFM:
-
Microscopía de fuerza atómica
- CO 2 :
-
Dióxido de carbono
- DAPI:
-
Dihidrocloruro de 4 ', 6-diaminido-2-fenilindol
- DMEM:
-
Medio Eagle modificado de Dulbecco
- FBS:
-
Suero fetal bovino
- ICP-MS:
-
Inductively coupled plasma mass spectrometry
- KCl:
-
Potassium chloride
- L929:
-
Mouse embryonic fibroblasts
- PBS:
-
Phosphate-buffered saline
- PEEK:
-
Polyetheretherketone
- PGA:
-
Polyglycolide
- PHB:
-
Polyhydroxybutyrate
- PLA:
-
Poly(l-lactide)
- PMMA:
-
Polymethylmethacrylate
- PTFE:
-
Polytetrafluorethylene
- SEM:
-
Scanning electron microscopy
- TCPS:
-
Tissue culture polystyrene
- UHMWPE:
-
Ultra-high-molecular-weight polyethylene
- WCA:
-
Water contact angle
- XPS:
-
Espectroscopia de fotoelectrones de rayos X
Nanomateriales
- Química de equipo e Industria 4.0
- Nanobiosensor de oro basado en la resonancia de plasmón superficial localizado es capaz de diagnosticar la brucelosis humana, presentando un método rápido y asequible
- Síntesis de compuesto de nanopartículas de oro / nanofibras de sílice conductoras eléctricas mediante pulsos de láser y técnica de pulverización
- Ajuste de las morfologías de la superficie y las propiedades de las películas de ZnO mediante el diseño de la capa interfacial
- Ajuste del rendimiento tribológico de nanoplaquetas de fosfato de circonio en capas en aceite mediante modificaciones de la superficie y de la capa intermedia
- Electrohilado sobre sustratos aislantes controlando la mojabilidad y la humedad de la superficie
- Influencia de la rigidez elástica y la adherencia de la superficie en el rebote de nanopartículas
- Propiedades electrónicas de la adsorción de átomos de vanadio en una superficie limpia y cubierta de grafeno de Cu (111)
- Resistencia de contacto reducida entre el metal y n-Ge mediante la inserción de ZnO con tratamiento con plasma de argón
- Tratamiento térmico de aluminio y aleaciones de aluminio
- Tratamiento térmico de cobre y aleaciones de cobre.



