Nanobiosensor de oro basado en la resonancia de plasmón superficial localizado es capaz de diagnosticar la brucelosis humana, presentando un método rápido y asequible
Resumen
La brucelosis se considera la zoonosis bacteriana más común en el mundo. Aunque los hallazgos de laboratorio son el diagnóstico más confiable en la actualidad, los métodos de laboratorio actuales tienen muchas limitaciones. Esta investigación tuvo como objetivo diseñar y evaluar el rendimiento de una técnica novedosa basada en la resonancia de plasmón superficial localizado (LSPR) para eliminar o reducir las deficiencias existentes. Para este propósito, se extrajeron lipopolisacáridos suaves de Brucella melitensis y Brucella abortus y se fija en la superficie de las nanopartículas de oro mediante interacciones covalentes. Después de algunos procesos de optimización, se utilizó la dispersión dinámica de luz para caracterizar la sonda. La detección del anticuerpo anti-Brucella capturado se realizó midiendo el corrimiento al rojo en el pico LSPR seguido de la determinación del valor de corte, que indicó una diferencia significativa entre los controles y los pacientes positivos verdaderos ( P valor <0.01). Además, se utilizaron 40 sueros de muestras verdaderas negativas y pacientes positivos para evaluar el rendimiento de este método comparando sus resultados con el estándar de oro (cultivo), la prueba de aglutinación en tubo estándar y los niveles de IgM e IgG anti-brucelosis (ELISA). La sensibilidad, especificidad, valor predictivo positivo y valor predictivo negativo mostraron un desempeño apropiado del método basado en LSPR (85%, 100%, 100% y 86%, respectivamente). Los resultados de la investigación actual proporcionan un método prometedor, rápido, conveniente y económico para detectar los anticuerpos anti-Brucella en sueros humanos, que se puede usar ampliamente en laboratorios médicos para diagnosticar la brucelosis de manera rápida y efectiva.
Introducción
Las brucelas son cocobacilos gramnegativos de crecimiento lento que pertenecen a la familia Brucellaceae [1]. Las brucelas incluyen bacterias intracelulares facultativas que infectan una variedad de animales domésticos y salvajes [2]. El descubrimiento de nuevos tipos de brucelas en los últimos años ha ampliado enormemente el género. Actualmente hay doce especies del género, cuatro de las cuales incluyen Brucella. melitensis , B. abortus , B. suis y B. canis son las principales causas de la enfermedad en humanos [3]. B. melitensis se considera que es la especie más virulenta en el ser humano [3]. Aunque la brucelosis no causa la muerte en las personas y es solo un caso excepcional de transmisión de persona a persona, la epidemia incesante de brucelosis humana en todo el mundo genera graves problemas de salud pública y daños económicos debido a la pérdida de productividad de los animales. Es importante destacar que el potencial debilitador de la brucelosis en humanos y el complicado protocolo de tratamiento de la enfermedad han convertido a estas bacterias en candidatos a agentes de guerra biológica [4, 5].
La brucelosis en humanos se etiqueta como la "enfermedad de los errores" [6] porque su presentación clínica es inespecífica y se superpone con un amplio espectro de otras enfermedades; por tanto, la corroboración de laboratorio del diagnóstico es fundamental para el correcto tratamiento de un paciente [7, 8]. Aunque el cultivo, las pruebas serológicas y las pruebas de amplificación de ácidos nucleicos pueden hacer el diagnóstico de brucelosis, estos métodos tienen muchas limitaciones. En el cultivo, como patrón oro, la principal limitación que retrasa el correcto diagnóstico y tratamiento del paciente es el largo tiempo de incubación. Los sistemas de hemocultivo automatizados avanzados (por ejemplo, los sistemas Bactec y BacTAlert) pueden detectar casos agudos de brucelosis, pero requieren de 5 a 7 días de incubación, e incluso es necesario ampliar la incubación y la realización de subcultivos ciegos para muestras prolongadas [9]. La falta de especificidad y los resultados falsos positivos, especialmente en individuos expuestos repetidamente a organismos de Brucella, son las principales limitaciones con respecto a las pruebas serológicas [9, 10]. Aunque tienen una excelente sensibilidad, especificidad, seguridad y un diagnóstico rápido de la enfermedad mediante ensayos de amplificación de ácidos nucleicos, la importancia clínica de estos métodos y sus limitadas implicaciones terapéuticas no están claras debido a la perseverancia a largo plazo de los resultados positivos de las pruebas biomoleculares en los pacientes. que se han recuperado por completo [9, 11]. Por lo tanto, es necesario diseñar un método que pueda superar todas las limitaciones de las pruebas mencionadas anteriormente y, al mismo tiempo, mejorar sus ventajas.
La mejora de los dispositivos biosensores con límites de detección bajos se ha convertido en un componente importante de las investigaciones de detección de biomarcadores porque en la última década se han dedicado un gran número de estudios a encontrar procedimientos adecuados para mejorar la sensibilidad de diferentes plataformas de detección en biosensing [12, 13]. . Los biosensores se utilizan para detectar y cuantificar un analito generando una señal a partir de interacciones que incluyen componentes biológicos. Recientemente, la mayor sensibilidad de los transductores ópticos combinada con la especificidad incomparable de las interacciones biomoleculares ha llevado al desarrollo de muchos biosensores ópticos diferentes [14]. Debido a la facilidad de aplicación, la sensibilidad a las bajas temperaturas y la generación confiable de señales, como lo demuestra un corrimiento al rojo en la banda de absorción en respuesta a interacciones biológicas, las pruebas que se basan en las propiedades ópticas únicas de las nanopartículas son rentables para detectar marcadores biológicos [ 15,16,17]. Estos métodos de detección utilizan las características biofísicas de moléculas como el peso molecular, la carga y el índice de refracción para monitorear la actividad de una molécula en particular. La resonancia de plasmón de superficie es un fenómeno causado por la oscilación colectiva de los electrones de superficie después de la exposición a la luz incidente que se ha utilizado para detectar biomoléculas unidas a la superficie de forma rápida y sencilla [18, 19]. SPR consta de dos métodos principales, localizado (LSPR) o propagación (PSPR) [20, 21]. Entre ellos, los biosensores ópticos basados en plasmones de superficie localizados se han desarrollado notablemente debido a su importante potencial de aplicación [12, 22]. Esta técnica proviene de la interacción entre los electrones de superficie de nanopartículas conductoras, que son más cortas que la longitud de onda de la luz incidente, y la onda de luz que se produce cuando en la banda de conducción la luz incidente interactúa con los electrones de superficie [23, 24]. En comparación con otras plataformas similares, los biosensores basados en resonancia de plasmón de superficie localizada tienen varias ventajas (por ejemplo, resonancia de plasmón de superficie), como tener una longitud de decaimiento de campo electromagnético más corta, ser insensibles a las alteraciones del índice de refracción masivo causadas por variaciones de temperatura o los componentes del medio circundante, y la capacidad de excitarse mediante la propagación libre de la luz [12]. Por lo tanto, en la tecnología de nanobiosensores, los nanobiosensores basados en LSPR se consideran una de las herramientas más poderosas para detectar biomoléculas.
En resumen, por un lado, las estrategias de laboratorio siguen siendo la base principal para el diagnóstico de brucelosis. Por otro lado, los métodos clínicos actuales enfrentan muchas limitaciones. Por tanto, se considera que uno de los principales componentes de los protocolos de tratamiento es proponer un nuevo método alternativo que pueda superar las deficiencias de las técnicas existentes. Por lo tanto, este estudio tuvo como objetivo introducir un nanobiosensor basado en LSPR rápido, conveniente, económico, seguro y sensible para detectar anticuerpos anti-Brucella en muestras biológicas para el diagnóstico de brucelosis. Para ello, se recubrieron los lipopolisacáridos (LPS) de B. melitensis y B. abortus sobre nanopartículas de oro (GNPs) y se evaluó la especificidad, sensibilidad, valor predictivo positivo (VPP) y valor predictivo negativo (VPN) de la técnica. comparando los resultados obtenidos con el ensayo de cultivo de suero versus el ensayo. Además, el estudio actual realizó un ensayo inmunoabsorbente ligado a enzimas para medir los anticuerpos anti-Brucellae (tanto IgM como IgG) y una prueba de aglutinación en tubo estándar para evaluar la capacidad de la tecnología actualmente diseñada para detectar la brucelosis en comparación con los métodos convencionales.
Métodos
Cultivo bacteriano y extracción de LPS
Las suaves cepas de B. melitensis y B. abortus fueron cultivados en Luria – Bertani [3] agar. En el siguiente paso, se recolectaron las bacterias y se extrajeron los LPS utilizando un método modificado de agua con fenol caliente [25]. Para confirmar la calidad del LPS extraído, se aplicó electroforesis en gel de poliacrilamida-dodecilsulfato de sodio (SDS-PAGE, Sigma-Aldrich, St. Louis, Missouri, EE. UU.) Con tinción de nitrato de plata. La cuantificación de LPS se realizó con azul de 1,9-dimetil metileno (Sigma-Aldrich, St. Louis, Missouri, EE. UU.) Con Salmonella typhimurium como estándar. Para evaluar la contaminación de proteínas y ácidos nucleicos se utilizó el método de Bradford y la absorbancia a 260 nm.
Síntesis de nanopartículas de oro esféricas
Una reducción química de la sal de oro (HAuCl 4 ) se utilizó para sintetizar las nanopartículas de oro, que es un procedimiento de síntesis rápido, económico y ecológico para nanopartículas de Au a temperatura ambiente [26]. Según el método descrito, se disolvieron 15 mg de citrato de sodio (Sigma-Aldrich, St. Louis, Missouri, EE. UU.) En 50 ml de agua destilada desionizada y se mantuvo en un baño de hielo y se mezcló en un agitador magnético (150 RPM). . Al mismo tiempo, se añadieron 600 µl de solución de sal de oro (17,3 mM). Posteriormente, se añadieron 1,2 ml de solución de borohidruro de sodio (20 mM). La solución se mezcló durante 2 h en condiciones similares y luego se mantuvo a 4 ° C para su posterior aplicación. Según estudios previos, en este tipo de síntesis, el citrato de sodio actúa simultáneamente como agente reductor (impulsando la reducción de AuIII a Au0), agente de remate (estabilizando electrostáticamente la solución coloidal de nanopartículas de oro) y mediador de pH (modificando la reactividad de Au especies involucradas en la reacción). En este ensayo, la producción de una solución de color rojo a partir de una solución de color amarillo de HAuCl4 muestra la formación de oro en un estado de oxidación cero.
Se utilizó microscopía electrónica de barrido (SEM) para estudiar la morfología de las nanopartículas de oro, y se utilizó Zetasizer NanoZS90 (Malvern Instruments Ltd, Malvern, Worcestershire, Reino Unido) para evaluar la distribución de tamaño. La dispersión dinámica de la luz (DLS), a un ángulo de dispersión de 90º, se utilizó como principio básico para medir el tamaño de las partículas. Zetasizer Nano utilizó un láser con una longitud de onda de 633 nm. Con esta técnica, la dispersión de partículas causada por el movimiento browniano se mide y se convierte en distribución de tamaño mediante la relación de Stokes-Einstein [27]. También se aplicó el potencial Zeta para determinar la carga eléctrica superficial de las nanopartículas. Los espectros de absorción de las nanopartículas se registraron con un espectrofotómetro Cary 500 UVeviseNIR (infrarrojo cercano ultravioleta visible) (Varian, Australia).
Construcción de Nanoprobe (Biosensor)
Carboxilación de nanopartículas de oro
Se recubrieron nanopartículas de oro con enlazadores de ácido tioglicólico para preparar la superficie de los GNP para cargar LPS. En resumen, se mezcló 1 ml de solución de TGA (1 mM) con 1 ml de solución de nanopartículas de oro y se mantuvo a temperatura ambiente durante 24 h. Para el aislamiento de nanopartículas de oro recubiertas, la solución se centrifugó a 12.000 g durante 15 min. Después de eso, se utilizaron dos pasos de lavado con agua desionizada bidestilada para eliminar el exceso de TGA. Finalmente, se utilizó espectrofotometría para evaluar el recubrimiento de ácido tioglicólico en la superficie de los GNP.
Optimización del recubrimiento de ácido tioglicólico en nanopartículas de oro
El recubrimiento de TGA se realizó en diferentes momentos, incluyendo 12, 18, 24, 36 y 48 h para optimizar la relación de recubrimiento de TGA en nanopartículas de oro. Posteriormente, se midió y graficó la densidad óptica para obtener el mejor tiempo de incubación.
Unión covalente de LPS a nanopartículas de oro modificadas con TGA
Para estimular la unión covalente entre el grupo carboxilo de TGA y el grupo amina de LPS, los grupos carboxilo fueron activados por EDC (el reticulante de longitud cero más popular para conjugaciones bioquímicas) y moléculas de N-hidroxisuccinimida (NHS) [28]. Las nanopartículas de oro sedimentadas se suspendieron en una solución de EDC / NHS 0,1 mM y se incubaron durante 30 min a temperatura ambiente. En el siguiente paso, se añadieron 2 ml de solución salina tamponada con fosfato (PBS) que contenía Tween-20 (PBST) al 0,05% (pH 7,4). Después de un vórtice vigoroso, las nanopartículas se centrifugaron a 12.000 RPM durante 15 min. Después de la centrifugación, se añadió la solución de LPS tras la eliminación del sobrenadante. Posteriormente, la mezcla se incubó en un baño ultrasónico durante 10 min seguido de 3 h de incubación a temperatura ambiente. Después de eso, se añadieron 2 ml de PBST y se agitó vigorosamente con un vórtex seguido de centrifugación durante 15 min a 12.000 RPM y se eliminó el sobrenadante. Finalmente, las nano-sondas se resuspendieron en 500 µl de PBS y los espectros LSPR se midieron mediante espectrofotómetro. Después de la confirmación de la unión de LPS a las nanopartículas de oro, la solución se mantuvo a 4 ° C para estudios adicionales. La Figura 1 muestra las ecuaciones de interacción química de la síntesis de nanopartículas de oro modificadas con TGA y la unión de LPS.
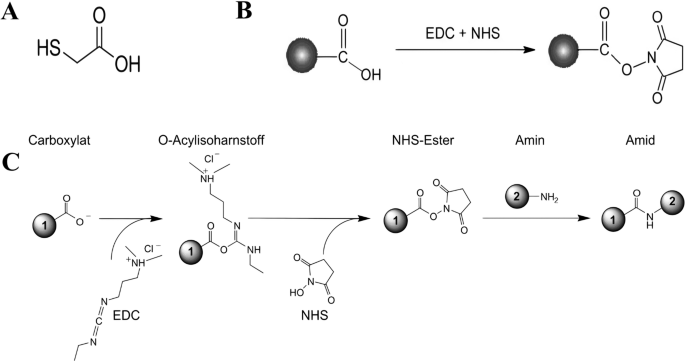
Interacciones químicas de la unión de LPS a las nanopartículas de oro. A Molécula de TGA, B Interacción EDC + NHS y C Unión covalente de LPS a nanopartículas de oro modificadas con TGA. Número 1:nanopartículas; número 2:LPS
Optimización de la concentración de LPS
Para maximizar la unión de LPS a grupos carboxilo de TGA activados, se realizó la optimización de la relación de nanopartículas de LPS a Au mediante la evaluación del cambio de pico en los espectros de LSPR en función de las concentraciones de LPS (100, 150, 200, 300 y 560 µg / ml) en una cantidad fija de nanopartículas de Au.
Detección de anticuerpos anti-LPS por nanoprobe
Se mezclaron 100 µl de las muestras diluidas (1:50 en PBS) con 200 µl del biosensor y se mezclaron pipeteando. En el siguiente paso, los biosensores se centrifugaron a 12.000 g durante 15 min después de 30 min de incubación a temperatura ambiente. Finalmente, los biosensores se suspendieron en 200 µl de PBS y se midió la absorbancia como se describió anteriormente. Para validar la función del nanobiosensor, también se proporcionaron controles positivos y negativos de un kit ELISA disponible comercialmente (Pishtazteb Zaman, Irán).
Declaración de ética
El uso de sueros humanos fue aprobado por los Comités de Ética de la Universidad de Ciencias Médicas de Fasa, Irán (IR.FUMS.1396.324). Las identidades de los donantes de sueros se codificaron y no se revelaron a nadie involucrado en este estudio. Además, todos los procedimientos se realizaron bajo pautas éticas siguiendo las regulaciones nacionales. Además, todas las muestras eran de sujetos que habían firmado el consentimiento informado por escrito.
Evaluación de la función del método diseñado
Se proporcionaron cuarenta muestras que contenían 20 casos (verdaderos positivos) y 20 controles (verdaderos negativos) para evaluar la funcionalidad del método diseñado. Por esta razón, se comparó el desempeño del método diseñado en el presente estudio con los resultados del cultivo. Además, se utilizaron kits comerciales disponibles (Pishtaz Teb, Teherán, Irán) para evaluar los niveles séricos de anticuerpos IgM e IgG. La preparación de la muestra y la evaluación de anticuerpos se realizaron de acuerdo con el protocolo del fabricante (Especificidad:99,85%, Sensibilidad:99,4%). Además, se realizó la prueba de aglutinación en tubo estándar en todas las muestras de suero para comparar y validar el rendimiento del método basado en LSPR. Para evaluar el desempeño del método diseñado, los resultados obtenidos del método basado en LSPR se compararon con las pruebas convencionales mencionadas con el cálculo de sensibilidad, especificidad, valor predictivo positivo y valor predictivo negativo basado en la fórmula común de la siguiente manera:
$$ \ begin {alineado} {\ text {Sensibilidad}} &=\ frac {{{\ text {Número}} \, {\ text {of}} \, {\ text {True}} \, {\ text {Positivos}}}} {{{\ text {Número}} \, {\ text {de}} \, {\ text {True}} \, {\ text {Positivos}} \, + \, {\ text {Número}} \, {\ text {de}} \, {\ text {False}} \, {\ text {Negativos}}}} \\ {\ text {Especificidad}} &=\ frac {{{\ text {Number}} \, {\ text {of}} \, {\ text {True}} \, {\ text {Negativos}}}} {{{\ text {Number}} \, {\ text {de }} \, {\ text {True}} \, {\ text {Negativos}} \, + {\ text {Number}} \, {\ text {of}} \, {\ text {False}} \, {\ text {Positivos}}}} \\ {\ text {PPV}} &=\ frac {{{\ text {Number}} \, {\ text {of}} \, {\ text {True}} \ , {\ text {Positivos}}}} {{{\ text {Número}} \, {\ text {de}} \, {\ text {True}} \, {\ text {Positivos}} \, + \ , {\ text {Número}} \, {\ text {de}} \, {\ text {False}} \, {\ text {Positivos}}}} \\ {\ text {NPV}} &=\ frac {{{\ text {Number}} \, {\ text {of}} \, {\ text {True}} \, {\ text {Negativos}}}} {{{\ text {Number}} \, { \ text {de}} \, {\ text {True}} \, {\ text {Negativos}} \, + \, {\ text {Número}} \, {\ text {de}} \, {\ text {Falso}} \, {\ text {Negativos}}}} \\ \ end {alineado} $$Análisis estadístico
Este estudio se analizó como un experimento de rendimiento diagnóstico clásico mediante la evaluación de la concordancia de una prueba propuesta, el nanosensor LSPR y una prueba estándar de referencia, el cultivo y algunas pruebas convencionales, incluidas ELISA y SAT, para determinar su capacidad para identificar una afección objetivo. . Los valores de corte se calcularon mediante el promedio de los sueros controles (negativos verdaderos) más los valores de desviación estándar de dos veces (2DE). Se realizó la prueba de Kolmogorov-Smirnov para determinar la normalidad y evaluar la distribución de los datos. Con base en los resultados de normalidad, que revelaron la distribución paramétrica, se utilizó la prueba ANOVA para comparar grupos. Todos los análisis estadísticos se realizaron utilizando GraphPad Prism para Windows versión 8 y SPSS para Windows versión 9.
Resultados
Análisis de extracción de lipopolisacáridos
SDS-PAGE mostró que el rendimiento de la extracción de LPS fue aproximadamente el 1 por ciento del peso húmedo de las bacterias usadas. Además, la concentración de ácido nucleico fue ≤ 0,2% de la concentración de LPS. Es importante destacar que el método Bradford demostró la ausencia de contaminación proteica.
Caracterización de nanopartículas de oro
La distribución de tamaño de las nanopartículas determina la calidad de un biosensor. Según los estudios anteriores, las nanopartículas deben poseer un tamaño específico. En este sentido, el tamaño apropiadamente pequeño de las nanopartículas da como resultado una estabilidad coloidal adecuada, altas relaciones de superficie a volumen y un movimiento rápido para altas tasas de unión que dan como resultado alta afinidad, alta sensibilidad y alta selectividad en la interacción con objetivos biológicos. Además, las nanopartículas deben ser lo más grandes posible para permitir la presencia de varios ligandos en la superficie de la partícula y obtener también interacciones multivalentes [29,30,31]. Como Gu et al. informó, la comparabilidad del tamaño de las nanopartículas con el tamaño de los objetivos biológicos es particularmente importante en la interacción de las proteínas [32]. De acuerdo con el tamaño de los anticuerpos anti-Brucella, que es de 2 a 5 nm [33], este estudio preparó nanopartículas de oro con un tamaño promedio de 10 nm y realizó la determinación de la distribución del tamaño de las nanopartículas mediante un instrumento Zetasizer NanoZS90, que utiliza un láser con una longitud de onda de 633 nm. Esta técnica se beneficia de la ecuación de Stokes-Einstein que puede convertir la difusión de partículas, causada por el movimiento browniano en una distribución de tamaño. Según la Fig. 2, los PNB se distribuyeron uniformemente a una escala de 10 nm. Los valores del potencial Zeta revelaron detalles sobre la carga superficial y la estabilidad de los PNB. Las partículas estaban cargadas negativamente y su potencial zeta era de aproximadamente -28 mV. Además, la Tabla 1 muestra la máxima longitud de onda de absorbancia de los PNB. Las longitudes de onda visual y ultravioleta se midieron con un espectrofotómetro y la absorbancia máxima fue de 530 nm. Usamos el método Turkevich para producir nanopartículas de oro. Las ventajas de este método es la producción de nanopartículas de oro, incluido un proceso de producción fácil y económico, la capacidad de controlar el tamaño de las nanopartículas y la estabilidad coloidal adecuada [34].
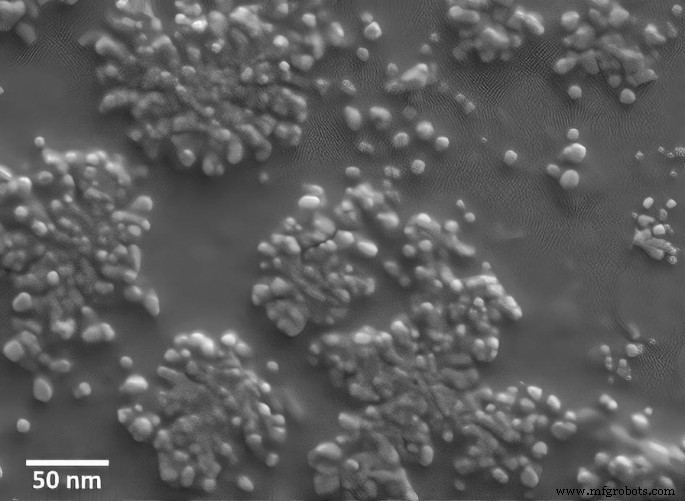
Estructura de nanopartículas de oro bajo SEM. La distribución equitativa de nanopartículas de oro se refleja bien en la figura
Caracterización de la nano-bio-sonda
Como se mencionó anteriormente, este estudio utilizó moléculas de TGA para conectar las nanopartículas de oro con LPS, lo que resultó en una ligera disminución del 4,55% en el pico de LSPR a 530 nm. Además, el presente estudio realizó varios tiempos de incubación para determinar la máxima adherencia de TGA a las nanopartículas de oro. Según los resultados que se muestran en la Fig. 3, 24 h de incubación de TGA con GNP dieron como resultado el recubrimiento máximo de TGA en la superficie de las nanopartículas de oro.
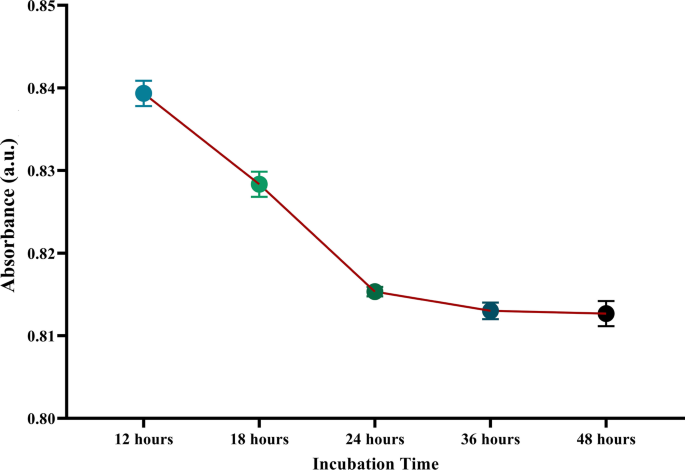
Optimización del recubrimiento de ácido tioglicólico sobre nanopartículas de oro. Como muestra la figura, no hay una alteración significativa en la absorbancia después de 24 h de incubación a pesar del alargamiento del tiempo adyacente. Por lo tanto, se seleccionó 24 h como el tiempo optimizado para el recubrimiento de ácido tioglicólico en los GNP. La Y -eje muestra la intensidad de absorbancia a 530 nm (absorbancia máxima de nanopartículas). Los experimentos se realizaron por triplicado. Los datos se presentan como media ± SEM. a.u .:Unidad de absorbancia
Con respecto a la determinación de la concentración optimizada de LPS, el presente estudio investigó concentraciones que incluían 100, 150, 200, 300 y 560 ug / ml. Como se muestra en la Fig. 4, a medida que aumenta la concentración, la absorbancia disminuye. Según los resultados, el presente estudio seleccionó una concentración de 300 ug / ml de LPS para recubrir la superficie de los GNP modificados con TGA, porque no hubo ninguna disminución notable en la intensidad del pico de absorción al aumentar la concentración de LPS.
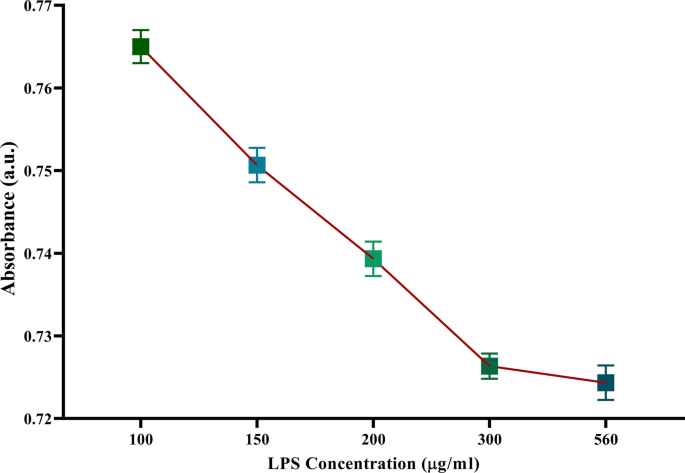
Optimización de la concentración de LPS. A medida que aumentó la concentración de LPS, la absorbancia disminuyó significativamente. Sin embargo, tras el incremento en las concentraciones de LPS de más de 300 mg / ml, no hubo una reducción significativa en la absorbancia de LSPR. Por tanto, la concentración mencionada se seleccionó como concentración optimizada. La Y -eje muestra la intensidad de absorbancia a 530 nm (absorbancia máxima de nanopartículas). Los experimentos se realizaron por triplicado. Los datos se presentan como media ± SEM. a.u .:Unidad de absorbancia
Evaluación de las funciones de la nano-bio-sonda
Como la técnica LSPR es un método óptico sensible a la superficie, puede detectar la interacción entre los anticuerpos anti-LPS y los antígenos en la superficie de las nanopartículas de oro a través de la imagen de alteraciones en el pico de absorción LSPR que es causado por la interacción electrostática entre el anticuerpo y antígeno. Para confirmar el correcto funcionamiento del biosensor, este estudio preparó un control positivo compuesto por anticuerpos anti-Brucella LPS con un título de 1:80 y control negativo, y registró el espectro LSPR del biosensor después de la incubación con los controles. Como se muestra en la Fig. 5, la incubación con control negativo no afectó la absorbancia de LSPR. Sin embargo, la incubación con control positivo provocó un cambio en la absorbancia máxima de LSPR que antes se conocía como desplazamiento al rojo. Por lo tanto, la unión de los anticuerpos anti-Brucella a los antígenos LPS limita la incidencia de incidencias de luz en la superficie de las nanoprobes.
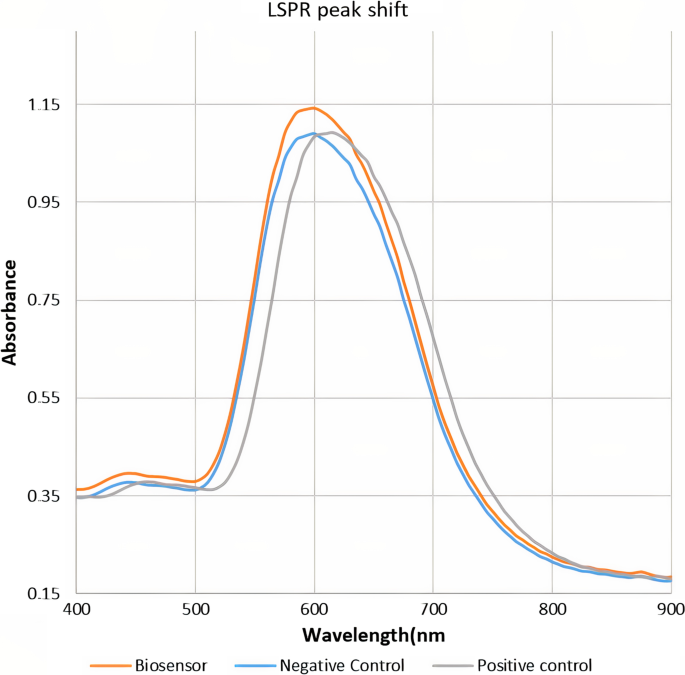
Pico de la nanoprobe LSPR en presencia de controles positivos y negativos. Los controles se proporcionaron a partir de kits de ELISA disponibles comercialmente
Determinación del valor de corte
Para este propósito, este estudio obtuvo 40 sueros de sujetos verdaderos positivos y negativos basados en el cultivo y las observaciones clínicas. Como se muestra en la Fig.6, el corrimiento al rojo promedio en las muestras verdaderas negativas (controles) fue de 1,70 nm, lo cual fue significativamente diferente de los pacientes verdaderos positivos ( P valor <0,001). Además, los resultados indicaron que el corrimiento al rojo de 4,38 nm debería utilizarse como valor de corte. Curiosamente, solo el 5% de los controles tuvo un corrimiento al rojo por encima del valor de corte, y el corrimiento al rojo en todos los pacientes estuvo por encima del valor de corte, lo que indica que el rendimiento del método es aceptable y la determinación del valor de corte es confiable.
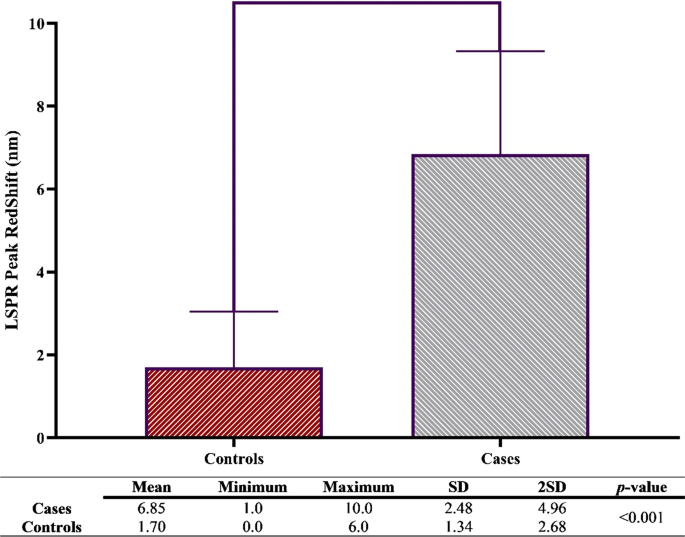
Desplazamiento al rojo máximo de LSPR en el suero de verdaderos pacientes y sujetos de control. Tras la interacción entre los anticuerpos, que se presentaron en los sueros de los individuos infectados, se produjo un corrimiento al rojo que fue significativamente diferente en comparación con los controles. Además, la figura muestra los valores SD y 2SD que son valiosos para la definición del punto de corte. Los experimentos se realizaron por triplicado para cada muestra. P valor <0.05 se consideró significativo
Validación de la función del biosensor
En los pasos anteriores, este estudio introdujo un método rápido y económico para identificar anticuerpos anti-Brucella en las muestras. Sin embargo, es necesario verificar la funcionalidad de un nuevo método. Con este fin, este estudio llevó a cabo una serie de subestudios que incluyeron la prueba de aglutinación en tubo estándar, niveles de anti-IgG y anti-IgM en los sueros de muestras negativas y positivas basadas en los resultados del cultivo. Como se muestra en la Tabla 2, la sensibilidad del método actual fue menor que la del SAT solo. Es importante destacar que la especificidad del método basado en LSPR mostró el resultado más aceptable que fue del 100%. De manera similar a la especificidad, el valor predictivo positivo del método actual fue más alto que otras pruebas convencionales (100%). En última instancia, el VPN de los métodos basados en SAT, IgG, IgM y LSPR fue del 90%, 90%, 81% y 86%, respectivamente.
Discusión
Probablemente se considere que la brucelosis es la primera infección humana después de la domesticación del ganado vacuno, ovino y caprino [35]. La brucelosis es la zoonosis bacteriana más prevalente en el mundo, con 500.000 nuevos casos humanos de la enfermedad diagnosticados a nivel mundial cada año [9, 36]. Los síntomas de la brucelosis humana no son patognomónicos porque la infección puede afectar a cualquier órgano del cuerpo [37]. Aunque los resultados de laboratorio siguen siendo un factor fiable en la detección de enfermedades, las estrategias actuales, incluidas las pruebas de cultivo, serología y amplificación de ácidos nucleicos, han mostrado graves defectos [9, 38,39,40]. Por lo tanto, este estudio intenta introducir un nuevo método de diagnóstico basado en LSPR para eliminar las limitaciones.
En los últimos años, la resonancia de plasmón de superficie localizada se ha utilizado como base para el desarrollo de biosensores. Las ventajas de la investigación actual sobre nanopartículas de oro y los avances en nanotecnología se han considerado los principales factores para mejorar el rendimiento diagnóstico. El color único y las propiedades ópticas de los GNP, debido a sus efectos plasmónicos y ajustables, son dos características sobresalientes y beneficiosas de estas partículas en comparación con otras partículas [12, 41].
En este estudio, se utilizó un corrimiento al rojo en el pico LSPR como indicador de interacción entre los antígenos LPS y los anticuerpos anti-Brucella. En otras palabras, en comparación con las muestras de control, la presencia de anticuerpos en el suero de las muestras de casos provocó un corrimiento al rojo significativo del pico de absorción LSPR, que se puede suponer que es un indicador de brucelosis. Aunque existe una diferencia significativa en el corrimiento al rojo entre las muestras de control y de casos, esta diferencia no puede cuantificar la concentración de anticuerpos en el suero, lo que puede considerarse como una de las graves limitaciones de este método. Sin embargo, debemos recordar que algunos métodos comunes, como las estrategias relacionadas con ELISA, generalmente se consideran un punto de corte [42, 43].
Es importante destacar que este estudio validó el rendimiento de la técnica basada en LSPR comparando los resultados obtenidos con otros métodos actuales mediante la evaluación de varios parámetros. El primer parámetro analizado fue la sensibilidad, que determina la probabilidad de una prueba de brucelosis positiva en un paciente [44]. Como Yagupsky et al. Habían comentado [9], la sensibilidad del hemocultivo, que se considera el estándar de oro actual, se reduce especialmente en enfermedades crónicas e infecciones focales. Además, este método también enfrentó otras limitaciones serias, como problemas de seguridad en el laboratorio, el lento crecimiento de bacterias, y un resultado positivo es una prueba indiscutible de la enfermedad [45, 46]. Esta técnica basada en LSPR representó un resultado confiable y competitivo en comparación con los métodos convencionales en sensibilidad, como los kits de cultivo, SAT y ELISA dependientes. Al mismo tiempo, se evaluó la especificidad, es decir, la probabilidad de una prueba negativa si el paciente no está infectado [45, 47]. As results showed, compared to the other diagnostic strategy, the designed LSPR-based technique had the most significant outcome in terms of specificity. It is an important characteristic of this method because the previous studies had questioned the validity and specificity of serodiagnostic methods of human brucellosis since asymptomatic and self-limiting episodes of this infection occur in zoonosis endemicity areas [48,49,50]. However, like antibody-related methods, the current method resists the possible long-term persistence of anti-Brucella antibodies within the serum, even after complete recovery from brucellosis.
Similar to previous studies, positive predictive value was defined as the ratio of the true positive results to the sum of all positive results [51]. Similarly, the NPV was described as the ratio of the true negative results to the sum of all negative results [51]. Compared to conventional diagnostic strategies, the current designed method represented the most wonderful PPV outcomes, demonstrating its ability to distinguish between infected and non-infected individuals. In addition, the evaluation of the NPV results revealed the promising potential of the LSPR-based method to exclude non-patients from real patients.
Conclusion
This study introduced a rapid, simple, low cost, reliable, and economical method for diagnosing brucellosis. Although there are some minor limitations, including the qualitative outcomes and the possibility of being positive in recovered individuals, the advantages discussed show that it has good capabilities compared to the current laboratory-based diagnostic procedures.
Disponibilidad de datos y materiales
The datasets used and/or analyzed during the current study are available from the corresponding author on reasonable request.
Abreviaturas
- LPS:
-
Lipopolysaccharides
- GNPs:
-
Gold nanoparticles
- DLS:
-
Dynamic light scattering
- LSPR:
-
Localized surface plasmon resonance
- SAT:
-
Standard tube agglutination test
- ELISA:
-
Ensayo inmunoabsorbente ligado a enzimas
- PPV:
-
Positive predictive value
- NPV:
-
Negative predictive value
- PSPR:
-
Propagating surface plasmon resonance
- SDS-PAGE:
-
Sodium dodecyl sulfate–polyacrylamide gel electrophoresis
- SEM:
-
Scanning electron microscopy
- TGA:
-
Thioglycolic acid
- NHS:
-
N-hydroxysuccinimide
- EDC:
-
N -(3-dimethylaminopropyl)-N ′-ethylcarbodiimide hydrochloride
- PBS:
-
Phosphate buffer saline
Nanomateriales
- Síntesis de compuesto de nanopartículas de oro / nanofibras de sílice conductoras eléctricas mediante pulsos de láser y técnica de pulverización
- Dependencia de la resonancia de plasmón de superficie localizada del dímero de nanoprisma Ag truncado desalineado
- Ajuste de la química superficial de la polieteretercetona mediante revestimiento de oro y tratamiento con plasma
- Efecto de la distribución de nanopartículas de oro en TiO2 sobre las características ópticas y eléctricas de las células solares sensibilizadas por colorante
- Formación y propiedades luminiscentes de Al2O3:nanocompuestos de SiOC en la base de nanopartículas de alúmina modificadas por feniltrimetoxisilano
- Ajuste de las morfologías de la superficie y las propiedades de las películas de ZnO mediante el diseño de la capa interfacial
- Los efectos de acoplamiento de los polaritones de plasma superficial y las resonancias magnéticas dipolo en metamateriales
- Modulador de electroabsorción de polarización de plasma superficial insensible a la polarización basado en óxido de estaño indio Epsilon-Near-Zero
- Saponinas Platycodon de Platycodi Radix (Platycodon grandiflorum) para la síntesis verde de nanopartículas de oro y plata
- Anticuerpo monoclonal de heparanasa marcada con nanopartículas de oro magnético y su aplicación posterior para la obtención de imágenes por resonancia magnética tumoral
- Nanorods de oro modificados con sílice conjugada con anticuerpo para el diagnóstico y la terapia fototérmica de Cryptococcus neoformans:un experimento in vitro



