Papel de la escoria en la siderurgia de convertidores
Papel de la escoria en la acería de convertidores
El proceso de conversión de oxígeno es el principal proceso de fabricación de acero para la producción de aceros al carbono y de baja aleación. El proceso es esencialmente un proceso de oxidación de refinación del metal caliente (HM) con alto contenido de carbono a acero líquido con bajo contenido de carbono. El proceso de oxidación se lleva a cabo inyectando oxígeno en el convertidor. Esto hace que el hierro líquido y otras impurezas metálicas y no metálicas presentes en el líquido fundido en el baño del convertidor formen óxidos que son más livianos que el acero líquido y flotan en la superficie del baño. El nombre genérico de estos óxidos es 'escoria'. Algunos óxidos son de naturaleza ácida y pueden reaccionar con los refractarios básicos del convertidor y, por lo tanto, normalmente se fabrica una escoria básica que utiliza cal y dolomita calcinada para proteger los refractarios del convertidor. El oxígeno también puede reaccionar con el carbono para crear un gas que genera burbujas para formar espuma en la escoria líquida y para proporcionar la energía química necesaria durante la fabricación del acero.
En el proceso de fabricación de acero, la escoria es predominantemente una mezcla de óxidos con pequeñas cantidades de sulfuros y fosfuros. Los óxidos son de naturaleza ácida o básica. La escoria se forma durante el refinado del metal caliente en el que el Si se oxida a SiO2, Mn a MnO, Fe a FeO y P a P2O5, etc., y la adición de óxidos como CaO (cal), MgO (dolomita calcinada), óxido de hierro, y otros. La adición de óxidos se realiza para obtener las propiedades fisicoquímicas deseadas de la escoria, como punto de fusión, basicidad, viscosidad, etc.
Hay cuatro fuentes primarias para la escoria durante el proceso de fabricación de acero en el convertidor. Estos son (i) la oxidación de elementos metálicos en el acero líquido (p. ej., silicio, manganeso, aluminio, titanio, cromo y vanadio, etc.), (ii) debido a la presencia de elementos no metálicos en el baño líquido (p. ej., azufre y fósforo), (iii) adiciones de fundentes (p. ej., cal, dolomita calcinada y espato flúor) y refractarios disueltos (p. ej., MgO y CaO + MgO).
Una escoria ácida erosiona el revestimiento del convertidor ya que los ladrillos de revestimiento son básicos. La escoria ácida contiene altas cantidades de SiO2, Al2O3 que pueden hacer que la escoria sea más delgada. Una escoria básica contiene óxidos como MgO y CaO, lo que hace que la escoria sea más espesa. El FeO es la parte más importante de la escoria, ya que hace que la cal se disuelva a temperaturas más bajas, lo que se denomina "fundente". La temperatura de fusión del CaO es de 2570 °C y el MgO es de 2800 °C, se puede ver que es difícil obtener cal o magnesia en solución sin que el FeO reduzca el punto de fusión donde las temperaturas de colada del acero generalmente están por debajo de los 1650 °C.
El papel que juega la escoria en el proceso siderúrgico del convertidor de oxígeno es muy importante. La cal es fundamental para la fabricación de acero. La ciencia de cómo interactúa la cal con los diversos componentes formados durante la fabricación del acero es la base para comprender la antigua frase "Haz la escoria y el acero se hará solo". La escoria es un nombre genérico y en la fabricación de acero es principalmente una solución de óxidos y sulfuros en estado líquido y las fases multicristalinas en estado sólido. La escoria es una fase separada del acero líquido ya que (i) es más liviana que el acero líquido y (ii) es inmiscible en el acero líquido. Los papeles importantes que juega la escoria durante la fabricación de acero se detallan a continuación.
- Actúa como sumidero de impurezas durante el refinado del acero.
- Controla el potencial oxidante y reductor del baño durante el refinado a través del contenido de FeO. Un contenido más alto de FeO en la escoria hace que la escoria se oxide, mientras que un contenido más bajo de FeO hace que la escoria se reduzca.
- Ayuda en la desfosforación y absorbe algo de azufre.
- Evita el paso de nitrógeno e hidrógeno de la atmósfera al acero líquido en el baño.
- Absorbe las inclusiones de óxido/sulfuro.
- Aísla el baño líquido y reduce las pérdidas térmicas. Proporciona una barrera térmica y, por lo tanto, evita la transferencia de calor del acero líquido al entorno.
- Proporciona protección al acero líquido contra la reoxidación.
- Emulsiona el metal caliente y promueve la oxidación del carbono.
Las funciones de la escoria, como se indicó anteriormente, requieren que la escoria posea ciertas propiedades químicas (basicidad, potencial de oxidación) así como propiedades físicas (densidad, punto de fusión, viscosidad). Ambas propiedades están controladas por la composición y la estructura de la escoria.
Desde el punto de vista de la formación de escoria, existen dos prácticas de soplado limitantes, a saber:(i) soplado suave con posición de lanza alta sin agitación en el fondo del gas inerte y se caracteriza por una baja intensidad de mezcla del baño de hierro, y (ii) soplado duro con posición de lanza baja y con agitación de fondo (en convertidores de soplado combinados), caracterizada por una mezcla más intensa del baño de hierro y una interacción más profunda del chorro de oxígeno con el baño líquido. En caso de soplado suave, la interacción del chorro de oxígeno con el baño de hierro es superficial, la transferencia de masa desde el interior del baño es lenta debido a la mezcla débil y el hierro se oxida primero y se convierte en escoria. En el caso de un fuerte soplado, la interacción entre el chorro de oxígeno y el baño, así como la transferencia de masa desde el interior del baño a las capas superficiales, es más intensa y las impurezas del baño se oxidan primero. Los principales efectos de la práctica de soplado suave se dan a continuación.
- Hay un aumento en la tasa de formación de escoria
- Resulta en un mayor contenido de FeO en la escoria
- Resulta en una sobresaturación de oxígeno del acero líquido
- Favorece la formación de espuma de escoria
- Promueve la desfosforación al menos a un alto nivel de carbono
- Aumenta la tasa de oxidación de Mn y otras impurezas
- Aumenta el desgaste de los refractarios
- Aumenta las probabilidades de derrame de escoria
Hay cuatro principios para controlar la escoria en la fabricación de acero. Estos son (i) el control de la basicidad de la escoria, que es la relación entre los óxidos básicos y los óxidos ácidos, (ii) la saturación de la escoria con MgO, (iii) el control de la formación de espuma de la escoria, también conocido como control de la viscosidad de la escoria, y (iv) el equilibrio de acero y escoria en el proceso de fabricación de acero para alcanzar un 'estado de equilibrio'.
El término basicidad de la escoria es un medio por el cual se determina qué tan ácida o básica es una escoria en relación con el refractario básico utilizado en el convertidor. Si la escoria es más ácida, erosionará los ladrillos, si es más básica, protegerá los ladrillos. La basicidad de la escoria normalmente se determina por la cantidad de cal y dolomita calcinada añadida, los niveles de silicio y aluminio del metal caliente y la chatarra de acero cargada, así como las ferroaleaciones. El valor más bajo de la relación indica que la escoria es ácida y, a medida que aumenta la relación, la escoria se vuelve más y más básica.
Además de la basicidad, el contenido de MgO de la escoria también es importante. La escoria contiene compuestos de calcio disueltos y compuestos ácidos que hacen que el MgO se disuelva de los ladrillos refractarios del revestimiento en la escoria. El MgO se disuelve en la escoria según las relaciones de contenido de FeO, basicidad y temperatura. Cuanto menor sea la basicidad de la escoria, mayor será el requisito de MgO para la escoria. Un aumento en el FeO y la temperatura también aumenta el requerimiento de MgO de la escoria. Los efectos sobre el MgO se pueden ver en la figura 1.
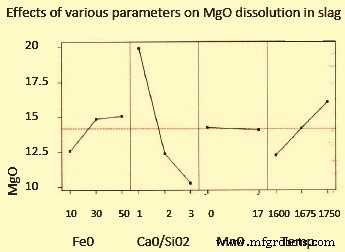
Fig. 1 Efectos de varios parámetros en la disolución de MgO en escoria
La altura de la espuma en el convertidor es una función del tiempo de soplado. La altura máxima de la espuma se alcanza cuando la masa de escoria se acerca al 70 % de la cantidad final de escoria. El polvo del convertidor reactivo es una fuente de óxidos de hierro y ayuda a la formación rápida de escoria espumosa, incluso cuando el golpe ha comenzado con una lanza baja, es decir, una práctica de golpe fuerte. La escoria espumante disminuye la relación de poscombustión y aumenta la eficiencia de transferencia de calor al baño.
Varios factores afectan la tendencia a la formación de espuma de la escoria líquida. Estos se dan a continuación
- Contenido de FeO en la escoria. La escoria debe contener FeO y debe estar en cantidad suficiente para reaccionar con el carbono y formar burbujas de CO.
- Corregir la viscosidad o la consistencia para mantener las burbujas el mayor tiempo posible.
- Suficiente MgO para minimizar el desgaste refractario y promover la formación de espuma.
El carbón de hierro líquido en el baño crea burbujas de CO para formar espuma en la escoria. La viscosidad de la escoria está determinada por la relación de los componentes de la escoria y cómo estos componentes hacen que la escoria sea delgada o espesa. Es el equilibrio de estos componentes el que hace que la escoria tenga la viscosidad correcta para mantener las burbujas por más tiempo. SiO2, FeO y Al2O3 adelgazan la escoria, mientras que CaO y MgO la espesan.
Una estimación aproximada de la densidad de la escoria del convertidor que consta de CaO, SiO2, FeO y MnO, etc. dentro de los rangos típicos de composición y temperatura del proceso del convertidor de oxígeno es de 2,8 a 3 toneladas/cum. Si la relación de masa de escoria a acero al final de un golpe de convertidor varía entre 0,08 y 0,1, la relación de volumen de escoria a acero aumenta desde casi cero al comienzo del golpe a 0,20/0,25 hacia el final del golpe.
En general, se considera que la escoria amortigua las proyecciones de metal (salpicaduras) y la formación de polvo del convertidor durante el soplado. Si se opera un convertidor con una cantidad muy baja de escoria, pueden ocurrir eyecciones de metales pesados y formación de calaveras. Las propiedades de la escoria son, sin embargo, de suma importancia. La escoria fluida y fuertemente oxidante es favorable para las reacciones de oxidación, pero puede provocar que la escoria se derrame del convertidor. El desprendimiento a menudo ocurre si la formación de escoria se retrasa, por alguna razón, y se 'carga' una gran cantidad de oxígeno en la escoria por soplado suave, adición de mineral/polvo, etc. La formación intensiva de CO de todos modos da como resultado la formación de emulsión de escoria-metal, Comienza la formación de escoria, las reacciones de oxidación secundaria y terciaria se llevan a cabo vigorosamente, y la formación de gas aumentada conduce a un fuerte derrame. El control adecuado de la formación de escoria y la formación de espuma es una medida central en la prevención de derrames.
FeO en la escoria es proporcional al oxígeno disuelto en el acero. En todas las reacciones escoria/metal existe una relación entre la cantidad de una cosa que hay en el acero y la cantidad que hay en la escoria. Esto se llama la "relación de partición". El acero y la escoria en el convertidor deben equilibrarse para que estén en estado de equilibrio. También existe una relación de contenido de carbono en el acero que controla el contenido de oxígeno del acero. El carbono influye en el nivel de oxígeno en el acero. A niveles bajos de carbono, el oxígeno reacciona con el hierro para formar FeO, lo que hace que la escoria sea más delgada e impacta en las pérdidas de rendimiento.
El contenido de SiO2 de la escoria determina cuánta cal se necesita durante la fabricación del acero. También reduce el rendimiento. Todos los materiales que ingresan al baño del convertidor en condiciones oxidantes influyen en los requisitos que necesita la escoria y el costo de estas adiciones, así como las pérdidas de rendimiento. El metal caliente y la chatarra juntos influyen en el contenido de SiO2 de la escoria. Cada kilogramo de silicio que reacciona con el oxígeno crea 2,17 kilogramos de SiO2. Este SiO2 debe neutralizarse con cal y dolomita calcinada para formar una escoria básica. Esta escoria básica provoca una pérdida de 5 kilogramos de hierro en la escoria como FeO. La razón es que hay un aumento en el volumen de la escoria al aumentar la cantidad de material ácido que debe equilibrarse con un material básico como la cal.
El desgaste químico del revestimiento refractario depende, entre otros, de su interacción con la escoria/emulsión, el metal líquido y la fase gaseosa, incluido el golpe de O2. El mecanismo más importante es la disolución del revestimiento en la escoria. La formación rápida de escoria para unir y neutralizar la formación de SiO2 ácido al comienzo del soplado es un punto clave. La escoria caliente altamente oxidante disuelve fácilmente el revestimiento de magnesia o dolomita. El uso de dolomita calcinada puede mejorar en gran medida la vida útil del revestimiento. Recientemente, la salpicadura de escoria se ha convertido en una práctica establecida para prolongar la vida útil del convertidor. La escoria residual en el convertidor se acondiciona para la composición química y la temperatura después del golpeteo y es salpicada por un violento flujo de nitrógeno alrededor de la pared del convertidor. El procedimiento en sí, así como las consecuencias para el proceso de conversión, son bastante complejos y la escoria debe ajustarse estrictamente para el tratamiento.
La escoria debe realizar varias tareas durante el proceso de fabricación de acero en el convertidor de oxígeno. Principalmente, se forma espontáneamente por los óxidos no volátiles que resultan en la oxidación del hierro y los componentes menores del metal caliente (SiO2, MnO, P2O5 y FeO). Para fundir los óxidos de impureza y formar una escoria fluida de bajo punto de fusión, se cargan en el convertidor cal y dolomita calcinada (una mezcla de CaO y MgO) y, si es necesario, espato flúor (CaF2). En segundo lugar, la escoria líquida proporciona un entorno de reacción para la eliminación de azufre y fósforo a través de los procesos de desulfuración y desfosforación, aunque con el desarrollo de la metalurgia secundaria la importancia de estas reacciones en el convertidor de oxígeno ha desaparecido. La escoria, cuando forma una emulsión con monóxido de carbono (CO) y gotitas de acero líquido (espuma de escoria), obviamente juega algún papel en la post-combustión de CO a dióxido de carbono (CO2), y afecta la transferencia de calor por radiación desde el 'punto caliente' formado. en la cavidad de impacto del chorro de oxígeno-hierro líquido, nivelando la distribución de temperatura en el convertidor. La escoria espumosa también disminuye claramente la tasa de generación de polvo al absorber una fracción de polvo.
La formación de escoria comienza con la disolución del oxígeno en el hierro líquido y la oxidación simultánea del hierro y otros componentes del baño en la zona de impacto del chorro de oxígeno. Como la temperatura del baño líquido en la zona de impacto del chorro de oxígeno es muy alta (más de 2000 °C), el hierro puede disolver una gran cantidad de oxígeno (hasta un 1 %). En esta zona de oxidación primaria, se forma óxido de hierro y el hierro líquido con alto contenido de oxígeno penetra en el baño y entra en contacto con el hierro líquido del baño fresco que tiene un mayor contenido de carbono y otros componentes que los oxidan. Parte de los productos de reacción primarios se salpican en la escoria y la atmósfera del horno.
El óxido de hierro y otros productos de oxidación no volátiles como SiO2, MnO y P2O5, etc. se mezclan con la escoria existente y se disuelve más cal y dolomita calcinada en la escoria líquida. La escoria se forma, por tanto, por una compleja cadena de reacciones. Las reacciones de formación de escoria se dan a continuación.
[Si] + 2[O] =SiO2 |
[Mn] + [O] =MnO |
[Fe] + [O] =FeO |
[P] + 5[O] =P2O5 | + CaO + (CaO + MgO) => Escoria
Estas reacciones son seguidas por reacciones secundarias de oxidación-reducción, especialmente por la descarburación que tiene lugar en la superficie de las gotas de hierro líquido que circulan en la escoria.
[FexOy] + y C =x Fe + y CO (g)
En el período de arranque de un soplado de convertidor, cuando la temperatura del baño es baja, la escoria suele estar saturada de silicato dicálcico (2CaO.SiO2), pero con el progreso de la oxidación del metal caliente, la composición de la escoria se aparta del silicato dicálcico. la 'nariz' de silicato regresa en la etapa posterior del golpe y la pasa al rango de saturación de silicato tricálcico (3CaO.SiO2) o incluso de saturación de cal. La evaluación de la ruta de la escoria que pasa por las superficies liquidus de alta temperatura, como la nariz de 2CaO.SiO2 o las superficies liquidus del 3CaO.SiO2 o la cal y la precipitación correspondiente de las fases sólidas del baño líquido, está algo oscurecida por el hecho de que las escorias son de varios componentes. Se ha informado que las fases y las temperaturas de la escoria superan, incluso en varios cientos de grados, la temperatura promedio del baño de hierro líquido.
Las afinidades locales en los límites de fase (escoria/baño, escoria/gota, baño/escoria de gas/gas, etc.) controlan el progreso de reacciones similares de los componentes en la misma fase de solución (fundición de hierro o escoria). La magnitud de la afinidad de la reacción depende de la afinidad estándar y de las actividades (potenciales químicos) de los componentes de la reacción en las fases de solución. Las afinidades de reacción locales que controlan la distribución de oxígeno entre la reacción de oxidación de elementos menores en el baño de hierro y el hierro, es decir, el progreso mutuo de las reacciones de oxidación, cambian con la evolución del tiempo y la temperatura del proceso. De la misma manera, las afinidades locales de las reacciones de oxidación secundaria por el hierro (y otros óxidos en la escoria, como el óxido de manganeso) controlan el progreso de la descarburación frente a la oxidación de otros constituyentes menores de las gotas de hierro en el ambiente de la escoria. Este control termodinámico de la reacción de oxidación explica por qué el hierro se oxida y se escoria en el golpe suave. Una mezcla débil en un baño de hierro da como resultado un transporte lento de los componentes menores del baño (Si, Mn, C, etc.) desde el interior del baño hasta las capas superficiales donde tiene lugar la oxidación y desde las cuales las gotas de hierro se salpican o estallan en la escoria. Estas capas son la desaparición de elementos menores, sus actividades en la fase metálica y, en consecuencia, las afinidades de reacción disminuyen en relación con el hierro. La oxidación del hierro se vuelve así termodinámicamente favorable.
Para la escoria de desfosforación juega un papel importante en la fabricación de acero del convertidor de oxígeno. El equilibrio de la actividad del oxígeno en el acero y la escoria se puede relacionar con la fase de oxidación, así como con los materiales que se utilizan para la desfosforación. La ecuación para eliminar el fósforo del acero es, en términos simples, la siguiente.
2P + CaO + 5FeO => P2O5.CaO + 5 Fe Temperatura <1640 °C
2P + CaO + 5FeO <=P2O5.CaO + 5 Fe Temperatura> 1640 °C
Todo esto muestra que para eliminar el fósforo del acero se necesita cal (CaO) y oxígeno (FeO) para producir el producto de P2O5.CaO para atrapar en la escoria. Sin embargo, si la temperatura supera los 1640 grados C, la reacción se invierte y se produce la refosforización. Por lo tanto, para la eliminación de fósforo, la escoria que contiene P2O5.CaO debe eliminarse mediante el desescoriado del convertidor en medio del soplado o es necesario agregar más cal, soplar más el calor (actividad de oxígeno) o mantenerlo enfriador.
Proceso de manufactura
- Pantalla de cristal líquido (LCD)
- La escoria de alto horno y su papel en la operación del horno
- Inclusiones en siderurgia y siderurgia secundaria
- Fabricación de acero verde
- Horno de inducción y siderurgia
- Proceso de soplado combinado en siderurgia de convertidores
- Proceso CAS-OB de siderurgia secundaria
- Papel del molde en la colada continua de acero
- El papel de la tubería de precisión en los sistemas de dosificación de líquidos:Parte 3 de 3
- El papel de la tubería de precisión en los sistemas de dosificación de líquidos:Parte 2 de 3
- El papel de la tubería de precisión en los sistemas de dosificación de líquidos:Parte 1



