Preparación de nanoplacas de oro utilizando compuestos ortocarbonilo como agentes de protección para la detección electroquímica de iones de plomo
Resumen
En este estudio, se sintetizaron nanoplacas de oro utilizando moléculas vegetales (ácido gálico) siguiendo un modo de control cinético. El crecimiento de nanoplacas se debe principalmente a la adsorción específica de agentes de recubrimiento en ciertas facetas de los cristales. A través de caracterizaciones sistemáticas, se encuentra que la distancia entre dos átomos de oxígeno en compuestos ortocarbonílicos coincide exactamente con el espaciado reticular de las facetas del oro (111), lo cual es beneficioso para la formación de semillas gemelas y favorece el crecimiento de oro en forma de placa. nanopartículas. Las nanoplacas de oro sobre el electrodo de carbono vítreo muestran una actividad de detección electroquímica notablemente mejorada de los iones de plomo en comparación con el electrodo de carbono vítreo desnudo o el electrodo esférico modificado con nanopartículas de oro. Se espera que el electrodo modificado se utilice en la detección de la concentración de iones de plomo en aguas residuales de metales pesados.
Introducción
Gracias a la propiedad de resonancia de plasmón de superficie localizada (LSPR) [1,2,3,4], las nanopartículas de oro (GNP) han encontrado muchas aplicaciones ópticas y electroquímicas, que incluyen detección, espectroscopia Raman, imágenes biológicas, catálisis, biomedicina, etc. [5,6,7,8,9,10]. Las propiedades plasmáticas de los PNB dependen de su forma, tamaño, composición y entorno dieléctrico; especialmente, la mejora de campo cercano de los PNB anisotrópicos suele estar muy amplificada debido a sus características estructurales nítidas [11, 12]. En diversas morfologías, las nanoplacas de oro bidimensionales han atraído mucha atención debido a sus propiedades ópticas únicas, alta conductividad, estabilidad térmica y actividad catalítica [13, 14, 15]. En las últimas décadas, se han desarrollado una serie de métodos de preparación para sintetizar nanoplacas de oro bidimensionales, incluido el método de reacción fotoquímica, el método de descomposición térmica, el método mediado por semillas, el método asistido por microondas y el método asistido por ultrasonidos [16,17, 18,19,20]. Sin embargo, la mayoría de estos métodos de síntesis no son respetuosos con el medio ambiente, ya que a menudo implican el uso de muchos tensioactivos o agentes de protección (bromuro de cetiltrimetilamonio, dodecil sulfato de sodio), agentes químicos reductores (NaBH 4 ), etc. [21, 22, 23].
En los últimos años, el vigoroso desarrollo de la química verde ha promovido la preparación de nanoplacas de oro por métodos biológicos [24]. Biomasa como limoncillo, aloe vera , algas, alfalfa, E. coli y Platycladus orientalis El extracto se ha utilizado como agentes reductores y protectores para sintetizar nanoplacas de oro [25, 26]. Por ejemplo, Shankar et al. [27] desarrolló un método biológico para producir hasta un 45% de nanoplacas de oro mediante extracto de hoja de citronela. Montes et al. [28] prepararon con éxito nanoplacas de oro anisotrópicas con un tamaño de 500 a 4000 nm y un grosor de 15 a 30 nm mediante la reducción de HAuCl 4 solución con el extracto acuoso de alfalfa. Zhan y col. [29] informó sobre un nuevo método para la síntesis de nanoplacas de oro, es decir, la reducción biológica de HAuCl 4 mediante el uso de Platycladus orientalis extraer con un instrumento de control cinético. Vale la pena mencionar que el rendimiento de las nanoplacas de oro se puede ajustar ajustando los parámetros experimentales, como la forma / velocidad de alimentación del reactivo, o la temperatura y el pH de la solución de alimentación. Por ejemplo, cuando el pH era 2,81 y la temperatura era de 60 ° C, el rendimiento de las nanoplacas de oro podría ser de hasta un 39% inyectando Platycladus orientalis extraer en el precursor de oro a una velocidad de 60 mL · h −1 .
Es difícil dar el mecanismo exacto de nucleación y crecimiento de los GNP en la biosíntesis porque las moléculas activas reales en los extractos de plantas son difíciles de distinguir [30]. En estudios anteriores, se encontró que los polifenoles juegan un papel importante en la formación de nanoplacas de oro [31]. En este estudio, se utilizó ácido gálico como representante de polifenoles para estudiar el mecanismo de crecimiento de los PNB. A través de un amplio espectro de caracterizaciones estructurales, se identificó el papel de los compuestos ortocarbonílicos en el crecimiento de nanoclusters de oro en semillas gemelas y luego en nanopartículas en forma de placas, y estas nanoplacas de oro preparadas se utilizaron posteriormente en la detección electroquímica de iones de plomo.
Material y método
Material
El ácido cloroáurico, el ácido gálico, el oxalato de sodio, el ácido ascórbico, el ferricianuro de potasio, el dicloruro de cadmio y el sulfato de plomo son todos analíticamente puros y se compran de Aladdin Chemical Reagent Co., Ltd.
Preparación de nanoplacas de oro
En una síntesis típica de nanoplacas de oro, se precalentó un matraz de dos bocas (50 ml) que contenía 10 ml de ácido cloroáurico (1,0 mM) en un baño de aceite (equipado con agitación magnética) a 30 ° C durante 5 min. Las soluciones de alimentación (ácido gálico, 0,6 mM, 10 ml) se inyectaron simultáneamente en el matraz a través de una bomba de jeringa (Shenzhen Medical Equipment Technology Development Co., Ltd., SK-500, China) a una tasa de adición de 0,5, 1,0, 1,5, 2,0 y 2,5 ml · min −1 , respectivamente. La mezcla de reacción se mantuvo en agitación durante 30 minutos más después de completar la alimentación.
Caracterización
El espectro UV-Vis de los PNB se midió con un espectrofotómetro UV-Vis (TU-1900, Beijing Purkinje General Instrument Co., Ltd., China) con agua como referencia, el rango de longitud de onda de exploración fue de 330 a 1100 nm y el paso de exploración la longitud fue de 1,0 nm. Se realizaron microscopía electrónica de transmisión (TEM), microscopía electrónica de transmisión de alta resolución (HRTEM), difracción electrónica de área seleccionada (SAED) y espectroscopía de dispersión de energía (EDS) en un microscopio electrónico Phillips Analytical FEI Tecnai 30 (300 kV). El análisis del espectrómetro de infrarrojos por transformada de Fourier (FTIR) se llevó a cabo con un espectrómetro de infrarrojos (Nicolet iS50, empresa Nicolet, EE. UU.), Y el rango del número de onda de exploración fue de 400 a 4000 cm −1 . El análisis de termogravimetría (TG) se realizó en el analizador de termogravimetría (TG209F1, Netzsch, Alemania). El rango de temperatura era de 30 a 800 ° C, la velocidad de calentamiento era de 10 ° C · min −1 , y la tasa de flujo de aire fue de 20 mL · min −1 . Las mediciones de XRD para las nanoplacas de oro se realizaron en un difractómetro de rayos X (Bruker D8 Advance, Alemania) equipado con radiación Cu Ka (40 kV, 30 mA). El análisis XPS se realizó en un espectrómetro Quantum 2000 utilizando la línea Al-Ka como fuente de excitación. La separación cromatográfica se realizó mediante un sistema LC Agilent 1290 equipado con una columna Waters Cortecs C18 y una fase móvil compuesta por una solución de ácido fórmico (mezclada con agua al 10%) y metanol a un caudal de 0,2 mL / min. El volumen de extracto inyectado fue de 20 μL. El gradiente de metanol utilizado fue el siguiente:10% en el momento ( t ) =0 min, 10% en t =1 min, 90% en t =8 min, 100% en t =12 min y mantenido hasta t =13 min. La detección de EM se llevó a cabo usando un espectrómetro de masas Agilent 6550 equipado con una fuente de ionización por electropulverización calentada, y todos los compuestos se determinaron en modo negativo. El rendimiento de las nanoplacas de oro se calculó dividiendo el número de nanoplacas de oro por el número total de PNB. Para garantizar la precisión de los datos, la cantidad de nanopartículas analizadas fue más de 1000.
Detección electroquímica de iones de plomo
El electrodo de carbono vítreo (GCE, 3 mm de diámetro) se pulió con alúmina de 0,3 y 0,05 µm y luego se lavó por ultrasonidos durante 15 min en etanol y agua ultrapura, respectivamente. El sol de GNPs preparado (100 µl) se vertió por goteo sobre el electrodo de carbono vítreo y se secó al aire. El casting de PNB se repitió tres veces. La prueba de voltamperometría de barrido lineal se realizó con un electrodo de carbono vítreo (modificado con GNP) como electrodo de trabajo, un alambre de platino como contraelectrodo y un electrodo de Ag-AgCl como electrodo de referencia. Las condiciones de la prueba voltamperométrica fueron:voltaje mínimo - 2.0 V, voltaje máximo 2.0 V y velocidad de exploración 1 mV · S −1 .La concentración de iones de plomo en la prueba voltamétrica varía de 1000 a 1 mg · L −1 , y esta concentración de iones de plomo suele aparecer en muestras de agua contaminante [32, 33].
Resultados y discusión
Efecto de la tasa de alimentación
Para evitar la nucleación violenta y el crecimiento de los PNB, la tasa de alimentación de ácido gálico se controló mediante una bomba de inyección, que en consecuencia regula la tasa de liberación de átomos de oro durante el proceso de reducción. Se investigó el efecto de la velocidad de alimentación sobre el rendimiento de nanoplacas de oro. Como se muestra en la Fig. 1, a medida que disminuye la velocidad de alimentación, el pico de resonancia del plasmón superficial de los GNP esféricos disminuye gradualmente, mientras que aparece un nuevo pico de absorción en la región de longitud de onda larga (como la línea roja en la Fig. 1).
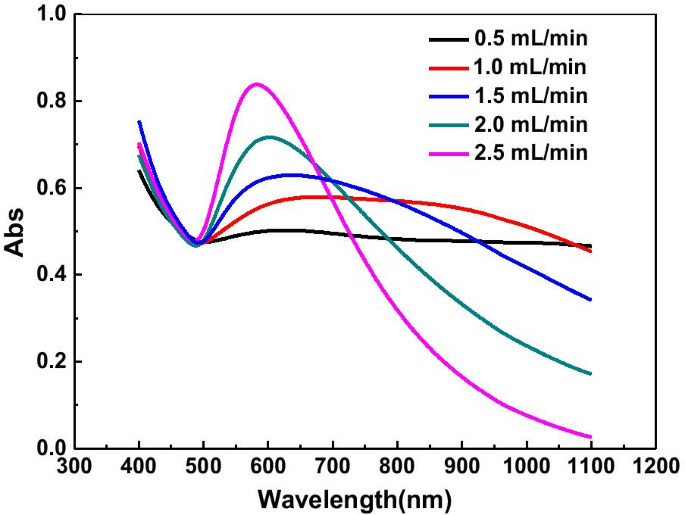
Espectros UV-Vis de GNP preparados con una velocidad de alimentación de 0.5, 1.0, 1.5, 2.0 y 2.5 mL · min −1
La Figura 2 muestra las imágenes del microscopio electrónico de transmisión (TEM) de los GNP sintetizados en diferentes condiciones. A medida que disminuye la velocidad de alimentación, el rendimiento de las nanoplacas aumenta de 0 a casi el 53%, y la longitud lateral de las nanoplacas es de aproximadamente 500 nm. Este resultado muestra que una liberación rápida de átomos no conduce a una nucleación heterogénea, que requiere semillas gemelas y una tasa de crecimiento adecuada.

Caracterizaciones TEM de GNP preparadas con la tasa de alimentación de 0.5, 1.0, 1.5, 2.0 y 2.5 mL · min −1 ( a - e ) y patrón SAED de nanoplacas de oro ( f )
Mecanismo de formación de nanoplacas de oro
Los espectros FTIR de ácido gálico, GNP esféricos y en forma de placa se muestran en la Fig. 3. Los picos en 3496 y 1538 cm −1 en el espectro del ácido gálico corresponden al hidroxilo fenólico y al anillo de benceno, que desaparecen en los espectros de los GNP esféricos y en forma de placa. Esto significa que el ácido gálico no se absorbería en las nanopartículas. Los picos a 1722 y 1618 cm −1 pertenecen al grupo carbonilo, y se observan dobles enlaces carbono-carbono tanto en los GNP esféricos como en placas. La diferencia es que la absorción del grupo carbonilo es mucho más fuerte en las nanopartículas en forma de placa. Este resultado indica que el hidroxilo fenólico se oxidó a la estructura del enol (absorbido en nanopartículas esféricas) y luego al compuesto ortocarbonílico (absorbido en nanopartículas en forma de placa).
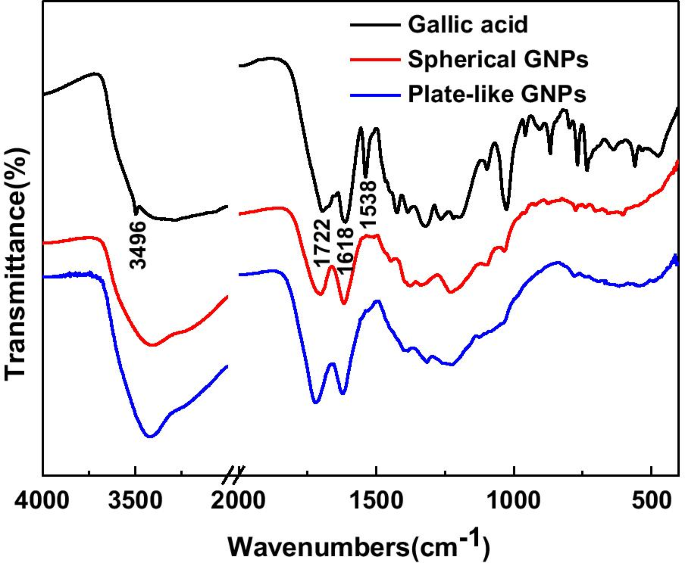
Espectros FTIR de ácido gálico, GNP esféricos y en forma de placa
El sobrenadante del producto de reacción (5 ml / min y 0,5 ml / min, respectivamente) se analizó por CL-EM. Como se muestra en la Fig. 4, para el sobrenadante obtenido de la reacción rápida, todas las moléculas se eluyen en aproximadamente 0,7 min de la columna. En este momento, las principales sustancias detectadas por espectrometría de masas son moléculas con peso molecular de 169; mientras que cuando el caudal es lento, los productos de reacción del ácido gálico son relativamente complejos y el tiempo de elución es de 0,5 a 1,1 min. En este momento, el m / z de la molécula detectada por espectrometría de masas es 167, 169, 203, etc. El ácido gálico podría oxidarse a compuestos de ortocarbono, e incluso los compuestos de ortocarbono podrían oxidarse adicionalmente para formar ácidos carboxílicos. Los resultados del análisis LC-MS mostraron que las nanopartículas en forma de placa se formaron en un entorno más compuesto de carbonilo.
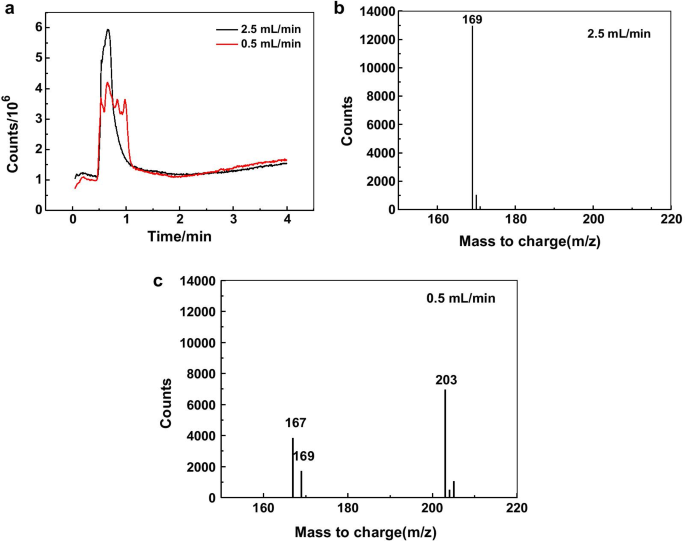
Análisis LC – MS del producto de reacción del ácido gálico
Como solo había ácido gálico y ácido cloroáurico en el sistema de reacción, sus productos de oxidación primario, secundario y adicional (como se muestra en el Esquema 1) podrían servir como reactivos de protección e inducir la formación de PNB. Al comienzo de la reacción (con una velocidad de alimentación de 0.5 mL · min −1 ), el ácido cloroáurico era excesivo, el ácido gálico se oxidaría completamente a compuestos ortocarbonílicos, mientras que a una velocidad de alimentación alta (es decir, 2,5 ml · min −1 ), el ácido gálico podría oxidarse a compuestos enólicos.
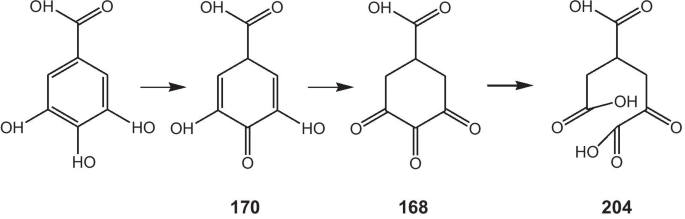
Oxidación del ácido gálico a compuestos enol y ortocarbonilo
Para aclarar la adsorción específica de ortocarbonilo en las nanoplacas de oro, las moléculas adsorbidas en las nanoplacas de oro fueron estudiadas por EDS (Fig. 5a). A excepción del elemento Au, solo C y O se encuentran en la superficie de las nanoplacas de oro. La proporción de C a O en la superficie de las nanoplacas de oro medida por EDS es 6.8:5 (815:599), cercana a la del ácido gálico (C 7 H 6 O 5 ) es 7:5. Esto indica que las moléculas en la superficie de las nanoplacas de oro provienen principalmente de los productos de oxidación del ácido gálico. Se realizó un análisis de TG para examinar las moléculas residuales en las nanoplacas de oro. Evidentemente, la Fig. 5b muestra que la biomasa representa el 5,6% del peso total de las nanoplacas de oro. La temperatura de descomposición de la biomasa está en el rango de 400-700 K, de acuerdo con la de la materia orgánica [34]. Este resultado sugiere que la biomasa se adhiere a los PNB como una capa delgada y actúa como agentes protectores que evitan la agregación de los PNB, lo que concuerda con un informe anterior [35].
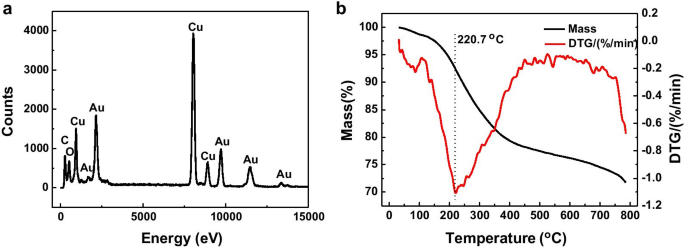
Espectro EDS ( a ) y TG ( b ) perfiles de nanoplacas de oro
Como todos sabemos, el espaciado de celosía de diferentes planos de cristal es diferente. Por ejemplo, el espaciado reticular del plano de Au (111) es 0.2355 nm y el del plano (100) es 0.408 nm, y el espaciado reticular del plano (110) es 0.288 nm. Debido a los diferentes ángulos de disposición entre los átomos, las longitudes de los enlaces formados por los átomos en diferentes planos cristalinos también son diferentes. El plano Au (111) es el que está más cerca, lo que resulta en la menor cantidad de defectos electrónicos, por lo que la energía del plano cristalino es la más baja. En este estudio, la distancia calculada entre dos filas de átomos de oro es 0.234 nm (Fig. 6a). Los patrones XRD de nanoplacas de oro (Fig.6b) muestran cuatro picos intensos a 38.30 °, 44.58 °, 64.71 ° y 77.72 °, respectivamente, que representan las facetas (111), (200), (220) y (311) de la estructura cristalina cúbica centrada en la cara.
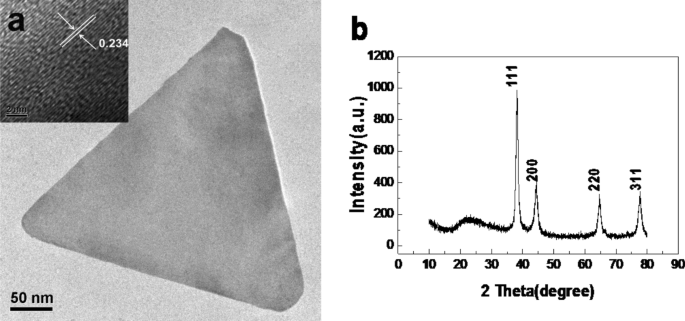
HRTEM ( a ) y XRD ( b ) caracterización de nanoplacas de oro
El análisis XPS mostró que los picos de Au y O eran similares a los informados en la mayoría de los estudios [36] (Fig. 7), pero los espectros de C eran más complejos. Hubo grandes picos de absorción a 284,5 keV, 286 keV y 288,3 keV, que podrían atribuirse a enlaces C – C, C – O y C =O, respectivamente. El espectro XPS también mostró que había muchos compuestos de carbonilo anclados en la superficie de las nanoplacas de oro.
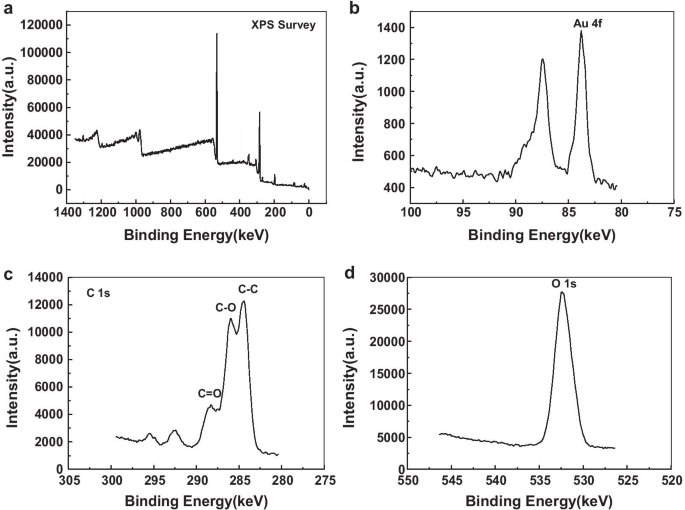
Caracterización XPS de nanoplacas de oro
Los productos de oxidación primaria y secundaria del ácido gálico tienen grupos carboxilo y carbonilo, y la diferencia es que estos últimos tienen grupos ortocarbonilo. La longitud del enlace del enlace simple C – C y del enlace doble C =O son 0,15 y 0,12 nm, respectivamente, mientras que los cuatro átomos del grupo ortocarbonilo forman un trapezoide isósceles con un ángulo de base de 60 ° (esquema 2). Por lo tanto, la distancia entre los dos átomos de oxígeno se puede calcular en 0,27 nm, lo que coincide con la distancia atómica de los planos de Au (111). Este resultado confirma que el grupo ortocarbonilo se adsorbería preferentemente en los planos de la superficie Au (111) para formar semillas gemelas.
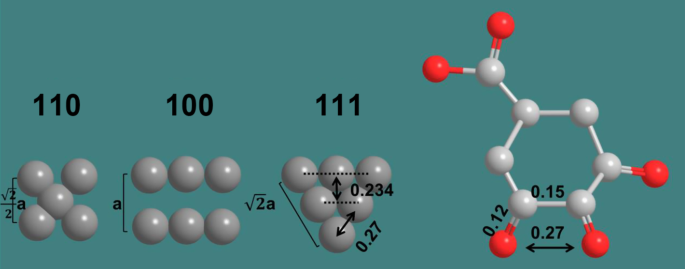
Diagrama esquemático de la adsorción preferencial de reactivos de protección en la faceta Au (111)
Preparación de nanoplacas de oro con compuestos de ortocarbonilo como agentes de remate
Para investigar más a fondo el efecto de los compuestos ortocarbonílicos en la formación de nanoplacas de oro, se utilizó oxalato de sodio con estructura similar como agente protector y ácido ascórbico como agente reductor para preparar GNP. Cuando la concentración de ácido ascórbico fue de 0,4 mM y la concentración de precursor de oro fue de 1,0 mM. Las nanopartículas preparadas se caracterizaron por espectroscopia UV-Vis (Fig. 8a). A medida que la concentración de oxalato de sodio aumenta de 0,1 a 0,6 mM, el pico de absorción de las nanopartículas esféricas disminuye gradualmente, mientras que la absorción en la región de longitud de onda larga aumenta gradualmente. A través de la caracterización TEM, se puede encontrar que cuando la concentración de oxalato de sodio era de 0,6 mM, la mayoría de las nanopartículas obtenidas poseían una morfología en forma de placa (Fig. 8b).
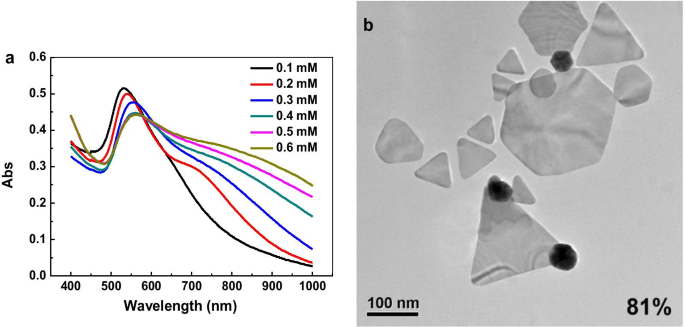
Preparación de PNB con oxalato de sodio como agente protector: a Espectros UV-Vis; b Imagen TEM
Detección electroquímica de iones de plomo
La respuesta electroquímica de nanopartículas en forma de placa, nanopartículas esféricas y el GCE desnudo a los iones de plomo se muestra en la Fig. 9. Se puede encontrar que la respuesta actual de las nanopartículas en forma de placa a la concentración de iones de plomo muestra una alta linealidad ( R 2 =0.9979, Fig.9a, b), mientras que para los PNB esféricos, la linealidad entre la concentración y el valor actual es menor ( R 2 =0,9884, figura 9c, d). El GCE desnudo muestra una linealidad aún menor ( R 2 =0.9719, Fig. 9e, f) entre la concentración y la corriente en el rango de concentración de 1000-10 mg · L −1 . Es más, la respuesta actual del GCE desnudo es mucho más débil que la de los electrodos cargados con GNP. Los GNP en forma de placa tienen bordes activos y, por lo tanto, muestran señales amplificadas en la solución de iones de plomo [37, 38]. La durabilidad de la GCE modificada con nanoplacas de oro se evaluó adicionalmente en la prueba electroquímica de iones de plomo después de haber sido colocada en atmósfera ambiente durante 3 semanas. Como se muestra en la Fig. 10g, h, la relación entre la concentración y la corriente sigue siendo de alta linealidad ( R 2 =0,9950), y se espera que este electrodo modificado se utilice en la detección de la concentración de iones de plomo en aguas residuales de metales pesados.
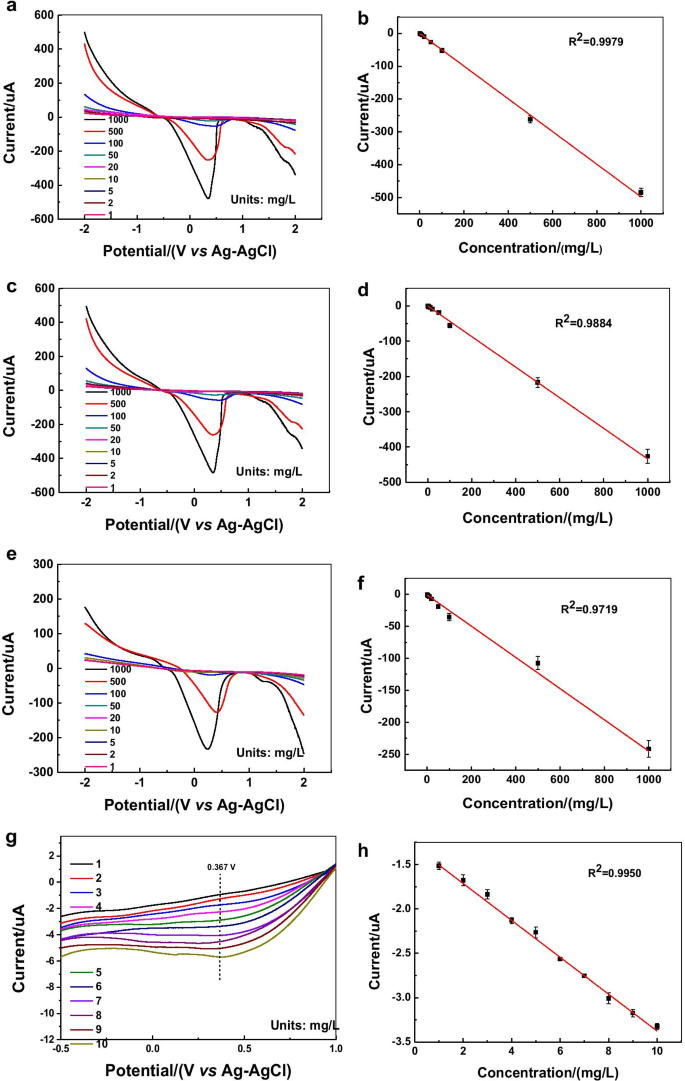
La aplicación de PNB en la detección de iones de plomo mediante el método de voltamperometría de barrido lineal
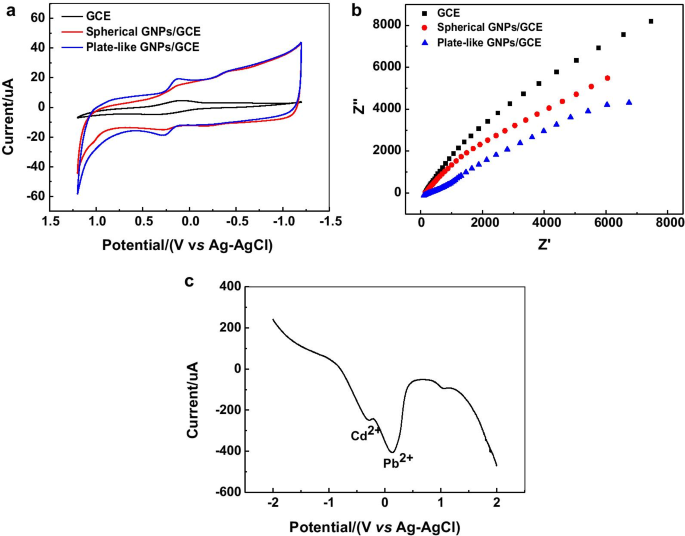
CV ( a ) y EIS ( b ) caracterización de los electrodos preparados. c Rendimiento antiinterferente del electrodo GNP / GCE en forma de placa
Para investigar las características de la superficie de los electrodos modificados, los electrodos preparados se caracterizaron por CV en 1,0 mM K 3 [Fe (CN) 6 ] solución con KCl 0,5 M como electrolito de soporte. El escaneo potencial osciló entre - 1.2 y 1.2 V, y la velocidad de escaneo fue de 0.05 V · s −1 . Según la Fig. 10a, se detectó un pico redox distinto en el caso de GCE desnudo. Cuando la superficie de la GCE se modificó con GNP, la respuesta actual fue más alta que la de la GCE desnuda. Este aumento se atribuye al hecho de que los GNP pueden promover la transferencia de electrones y mejorar la conductividad del electrodo. Cabe mencionar que el aumento de la respuesta actual sería mayor cuando la GCE fuera modificada por nanoplacas de oro. Además, la propiedad de la interfaz del electrodo también se investiga mediante espectroscopia de impedancia electroquímica (EIS), y los resultados se presentan en la Fig. 10b. Los radios del semicírculo en el gráfico de Nyquist representan la resistencia de transferencia de carga ( R ct ). La R ct de electrodos modificados con GNP, tanto esféricos como en forma de placa, es mucho más baja que la del GCE desnudo, debido a la alta conductividad de los GNP. Otro problema importante que dificulta la detección e identificación precisas de iones de plomo es la interferencia de otros iones de metales pesados. El rendimiento antiinterferente del electrodo GNP / GCE en forma de placa se probó en una solución mixta que contenía 1,0 g · L −1 ion de plomo y 1,0 g · L −1 ion cadmio. Como se muestra en la Fig.10c, no hay un cambio obvio en el potencial y la intensidad de respuesta de corriente del pico característico del ión de plomo, mientras que la diferencia entre las posiciones de los picos del ión de cadmio y el ión de plomo es de 433 mV, lo que indica que el pico en forma de placa El electrodo GNP / GCE tiene buena selectividad y capacidad antiinterferente.
En la voltamperometría de barrido lineal, el potencial máximo está relacionado con la naturaleza de la sustancia y el electrolito de soporte, mientras que la corriente máxima está relacionada linealmente con la concentración de la sustancia. En este experimento, un GCE desnudo podría detectar la concentración de iones de plomo, pero la precisión de detección es baja debido a la pasivación de la superficie y otros factores de influencia. Los GNP tienen buena conductividad y propiedades superficiales especiales, que pueden reducir la impedancia del electrodo, amplificando así la señal de corriente y obteniendo una mejor precisión en la detección de iones de plomo (Esquema 3). Debido a la interacción única entre los iones de plomo y los compuestos de orto carbonilo, que se anclaron en las nanoplacas de oro, muestra una buena selectividad con los iones de plomo.
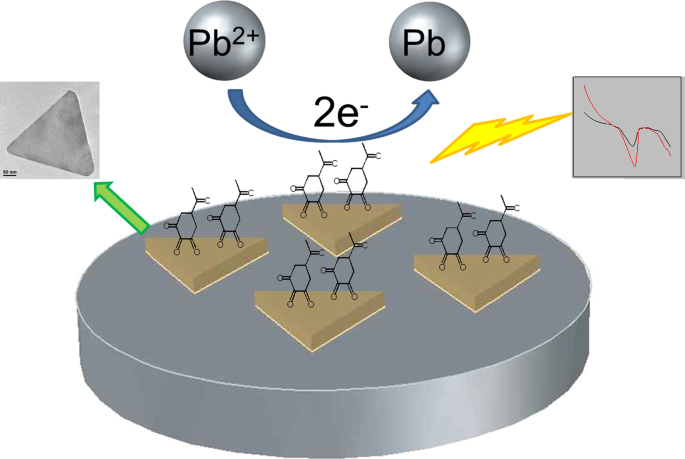
Ilustración esquemática de la detección de iones de plomo por el GCE modificado con nanoplacas de oro
Conclusiones
En conclusión, las nanoplacas de oro han sido sintetizadas por moléculas vegetales. La formación de nanoplacas se debe principalmente a la adsorción específica de compuestos ortocarbonílicos en las facetas del oro (111). La distancia entre dos átomos de oxígeno coincide bien con el espaciado de la faceta del oro (111), lo que es beneficioso para la formación de semillas gemelas y favorece el crecimiento de los PNB en forma de placa. Debido al "efecto de borde" distintivo de las nanoplacas de oro, la señal de los iones de plomo en la prueba de voltamperometría de barrido lineal es mucho más fuerte que la del electrodo desnudo o el electrodo esférico modificado con nanopartículas de oro. Se espera que las nanoplacas de oro desarrolladas se utilicen en la detección de la concentración de iones de plomo en aguas residuales de metales pesados.
Disponibilidad de datos y materiales
Los conjuntos de datos utilizados y / o analizados durante el estudio actual están disponibles del autor que respondió a una solicitud razonable.
Abreviaturas
- LSPR:
-
Resonancia de plasmón de superficie localizada
- PNB:
-
Nanopartículas de oro
- TEM:
-
Microscopía electrónica de transmisión
- HRTEM:
-
Microscopía electrónica de transmisión de alta resolución
- SAED:
-
Difracción de electrones de área seleccionada
- EDS:
-
Espectroscopía de dispersión de energía
- FTIR:
-
Espectrómetro de infrarrojos por transformada de Fourier
- TG:
-
Termogravimetría
- XRD:
-
Difractómero de rayos X
- XPS:
-
Espectroscopia de fotoelectrones de rayos X
- LC:
-
Cromatógrafo de líquidos
- MS:
-
Espectrómetro de masas
- LC – MS:
-
Cromatógrafo de líquidos-espectrómetro de masas
- GCE:
-
Electrodo de carbono vítreo
- CV:
-
Voltamperometría cíclica
- EIS:
-
Espectroscopia de impedancia electroquímica
- R ct :
-
Resistencia a la transferencia de carga
Nanomateriales
- Nanopartículas de oro para sensores de quimioterapia
- Nanorods de oro recubiertos con BSA para la terapia fototérmica NIR-II
- Nanofibras poliméricas electrohiladas decoradas con nanopartículas de metales nobles para detección química
- Nanopétalos mesoporosos de óxido de níquel (NiO) para detección de glucosa ultrasensible
- Estudio de los comportamientos de fricción a nanoescala del grafeno en sustratos de oro utilizando dinámica molecular
- Diseño de un absorbente de metamaterial de terahercios de cuatro bandas utilizando un resonador rectangular perforado para aplicaciones de detección
- Un método sencillo para la preparación de heterounión Cu2O-TiO2 NTA con actividad fotocatalítica visible
- Nanoestructuras de oro en crecimiento para la absorción celular selectiva por formas
- Síntesis mediada por semillas de nanobarras de oro con relación de aspecto sintonizable para imágenes fotoacústicas en el infrarrojo cercano
- Aplicaciones biomédicas para nanoclusters de oro:desarrollos recientes y perspectivas futuras
- Plataforma para tecnologías cuánticas usando oro



