Puntos de carbono como materiales de nueva generación para nanotermómetros:revise
Resumen
La detección de temperatura en modo sin contacto de alta sensibilidad es fundamental para estudiar reacciones químicas fundamentales, procesos biológicos y aplicaciones en el diagnóstico médico. Los termómetros basados en nanoescala garantizan sondas no invasivas para la detección de temperatura sensible y precisa con resolución subcelular. Los sensores de temperatura basados en fluorescencia han demostrado una gran capacidad ya que operan como modo "sin contacto" y ofrecen las funciones duales de imágenes celulares y detección de temperatura a nivel molecular. Los avances en nanomateriales y nanotecnología han llevado al desarrollo de sensores novedosos, como los nanotermómetros (materiales novedosos que detectan la temperatura con una alta resolución espacial a nanoescala). Estos nanotermómetros se han desarrollado utilizando diferentes plataformas, como proteínas fluorescentes, compuestos orgánicos, nanopartículas metálicas, nanopartículas dopadas con tierras raras y puntos cuánticos semiconductores. Los puntos de carbono (CD) han atraído el interés en muchos campos de investigación debido a propiedades sobresalientes tales como fuerte fluorescencia, resistencia al fotoblanqueo, estabilidad química, precursores de bajo costo, baja toxicidad y biocompatibilidad. Informes recientes mostraron el comportamiento de detección térmica de algunos CD que los convierte en una alternativa a otros termómetros basados en nanomateriales. Este tipo de termómetro de base luminiscente es prometedor para la detección de temperatura en nanocavidades y el mapeo térmico para comprender mejor los procesos biológicos. Con los CD aún en sus primeras etapas como material a nanoescala para la detección térmica, en esta revisión, proporcionamos una comprensión integral de este novedoso nanotermómetro, los métodos de funcionalización para mejorar la sensibilidad y resolución térmica y el mecanismo del comportamiento de la detección térmica.
Introducción
La temperatura es una variable termodinámica fundamental que tiene una influencia notable en los sistemas biológicos y químicos. Debido a su amplia gama de aplicaciones, casi en todos los campos de las ciencias naturales, la ingeniería, las ciencias agrícolas y médicas, la determinación precisa de la temperatura es de gran importancia [1, 2]. En aplicaciones médicas, la termometría se utiliza para la detección precoz de diversas enfermedades, como ictus, cáncer o inflamaciones, uno de cuyos síntomas incipientes es la aparición de peculiaridades de temperatura localizadas.
En la historia, la estimación más temprana de la temperatura se basó en la sensación o la observación. En la antigüedad, 200-10 aC, los experimentos neumáticos (expansión del aire por calor) se asignan como las referencias reconocidas más antiguas de aparatos utilizados para mediciones cuantitativas de calor. Entre los escritos más primitivos relacionados con el aire expandido por calor se atribuyen las obras de Filón de Bizancio y Hero (o Garza) de Alejandría sobre experimentos neumáticos [3]. Más tarde, entre los años 1592 y 1603, Galileo Galilei inventó un termoscopio estableciendo experimentos con la expansión del aire por calor mediante la construcción de un aparato simple utilizando un tubo que abarca el aire atrapado sobre una columna de agua. Después de Galileo, el italiano Santorio es el primero en ser acreditado por integrar este sencillo aparato en los exámenes médicos de fiebre. El primer termómetro de líquido en vidrio completamente sellado, tubo de vidrio lleno de alcohol, fue ensamblado por Fernando II en el año 1641. Pudo medir la temperatura sin ayuda de presión barométrica, a diferencia del termoscopio abierto de Galileo y Santorio. El trabajo práctico de Fahrenheit en termometría surgió en 1706; Comenzó con el alcohol, pero posteriormente se convirtió en una leyenda por sus termómetros de mercurio. El reconocimiento de la escala de temperatura centesimal se le otorgó a Anders Celsius, quien en 1742 proyectó una escala con cero a la temperatura del agua hirviendo y 100 a la temperatura del agua helada. Experimentaciones electrónicas realizadas en el siglo XIX cuando Thomas Johann Seebeck consideró el concepto de termoelectricidad. En una sucesión de experimentos realizados entre los años 1820 y 1823, verificó el potencial eléctrico en los puntos de unión de dos metales diferentes cuando hay una diferencia de calor entre las uniones. Esto se conoció más tarde como el efecto Seebeck y sirve como el origen del termopar, que se considera la medida más precisa de temperatura [3, 4, 5, 6, 7]. La línea de tiempo esquemática del termómetro se muestra en la Fig. 1.
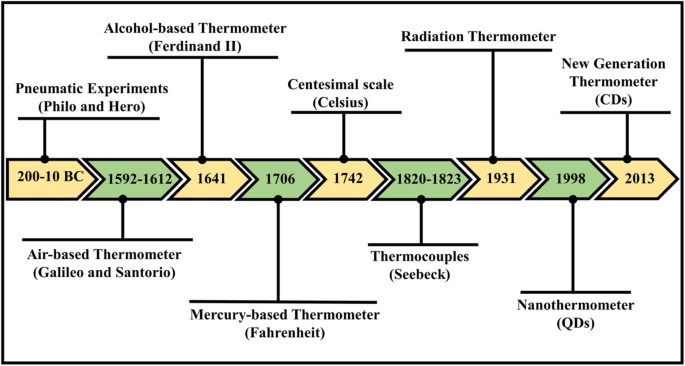
Esquema de la línea de tiempo para la evolución de los termómetros
Los termómetros convencionales se pueden clasificar en:
- 1.
Termómetros de vidrio llenos de líquido basados en la expansión térmica de materiales
- 2.
Termopares basados en el efecto Seebeck
- 3.
Sensores ópticos [8]
Además, se pueden clasificar como termómetros de contacto o sin contacto. El modo de contacto, incluido el vidrio clásico relleno de líquido, los termopares, los termistores y los detectores de temperatura de resistencia (RTD), requieren cableado eléctrico y un contacto directo entre el termómetro y el sustrato. Este modo no es apropiado para aplicaciones en las que el ruido electromagnético es fuerte, las chispas pueden ser peligrosas, el entorno es destructivo o las piezas se mueven rápidamente. Además, los termómetros tradicionales no son capaces de medir cuando la resolución espacial desciende a la escala submicrométrica, por ejemplo, en las variaciones de temperatura intracelular y en el mapeo de la temperatura de microcircuitos y microfluidos [9]. De la misma manera, las aplicaciones de ingeniería requieren estrategias termosensibles avanzadas para regiones en miniatura y entornos difíciles [10]. Por lo tanto, para los dominios de nanoescala, uno debería pensar en otros enfoques y materiales.
La nueva termometría sin contacto puede superar los problemas mencionados anteriormente. Por ejemplo, los termosensores ópticos (termómetros moleculares) son una generación más reciente de herramientas analíticas que consta de clases moleculares que utilizan la medición de la luz emitida para extraer la temperatura [11, 12]. Las sondas fluorescentes sensibles a la temperatura ofrecen un área prometedora para la termometría en aplicaciones de nano-sistemas. La información de temperatura se puede extraer en función de su intensidad de fluorescencia, la forma de la banda, el desplazamiento de Stokes o la vida útil de la descomposición puede relacionar la temperatura si se calibra correctamente [13, 14].
Los termómetros moleculares tienen un gran potencial para diagnosticar células enfermas o cancerígenas, que tienen temperaturas fisiológicas diferentes a las de las células ordinarias. En las aplicaciones médicas, las posibilidades van desde el control inducido por la temperatura de la expresión génica [15] y el metabolismo celular [16] hasta la penetración selectiva de células y el tratamiento de enfermedades [17] y la mejora de la disipación de calor de las fuentes de calor integradas [18]. . Recientemente, nanomateriales como semiconductores [19], nanopartículas poliméricas [10] y metálicas [20] se han utilizado como sensores térmicos (nanotermómetros) que mostraron una resolución térmica submicrométrica.
Los termómetros que pueden resolver subgrados de temperatura en una amplia gama de temperaturas que también pueden integrarse dentro de los sistemas vivos podrían ofrecer una nueva herramienta influyente en innumerables áreas de investigación biológica, física y química. Por lo tanto, en esta revisión, nos enfocamos en una “nueva generación” o una “nueva clase” de nanotermómetro que se basa en nanomateriales de carbono (materiales carbonosos). Hasta donde sabemos, no existe ningún artículo de revisión sobre los puntos de carbono como nanotermómetro. Recientemente, los puntos de carbono (puntos cuánticos de carbono, puntos cuánticos de grafeno) junto con sus características únicas mostraron propiedades térmicas sensibles que los hacen excelentes candidatos para el comportamiento termométrico en el dominio de nanoescala. Aquí, se revisan las definiciones, ventajas y mecanismos del comportamiento de detección térmica de los puntos de carbono. Finalmente, se presentan las perspectivas futuras de esta nueva clase de termomateriales.
Nanotermometría
Lo que se entiende por "nanotermometría" es el uso de materiales termosensibles a nanoescala para proporcionar información sobre la temperatura sobre el entorno local de la región a nanoescala o microescala [21, 22]. Las sondas térmicas basadas en nanopartículas tienen una gran capacidad en un amplio espectro de aplicaciones de detección, y últimamente se han reportado numerosos denominados “nanotermómetros” progresivos. Además, se ha informado que diferentes tipos de nanomateriales convencionales tienen propiedades luminiscentes termosensibles, como polímeros [23, 24], nanocristales [25], nanopartículas dopadas con tierras raras [26, 27] y nanopartículas metálicas [28].
Por lo tanto, los nanotermosensores son termómetros precisos no invasivos, sin contacto y que funcionan a nanoescala con una resolución de alta sensibilidad [9]. La detección térmica que utiliza nanomateriales se puede lograr manipulando sus propiedades ópticas. La nanotermometría de fluorescencia se puede clasificar en bastantes clases dependiendo del parámetro preciso del cual se deriva la medición térmica que involucra la intensidad de la señal, la forma de la banda, la vida útil de la fluorescencia, el cambio de banda, la polarización de la longitud de onda de excitación y el cambio espectral. En el primer caso, la fluorescencia cambia con diferentes temperaturas y puede detectarse como un aumento (o disminución) absoluto de la señal [9, 29, 30, 31].
La nanotermometría de luminiscencia sin contacto, que utiliza nanomateriales luminiscentes con emisiones dependientes de la temperatura, es predominantemente apropiada para aplicaciones biológicas [32, 33]. Estos nanomateriales luminiscentes incluyen polímeros fluorescentes [24], nanopartículas metálicas [34], nanopartículas dopadas con tierras raras [35] y nanodiamantes [36] que tienen una propiedad termosensible en el rango fisiológico. Estos trabajos pioneros fueron capaces de entregar la temperatura promedio para celdas individuales. Sondas luminiscentes dependientes de la temperatura basadas en tintes orgánicos (p. Ej., Rodamina 6G) y polímeros (p. Ej., Poli ( N -isopropil acrilamida)) generalmente presentan una fotoestabilidad deficiente y una sensibilidad cruzada pronunciada al oxígeno, lo que no es deseable para el trabajo con células vivas [8]. Además, existe una fuerte dependencia del pH de la vida útil del fluoróforo, lo que dificulta su uso sin el control preciso del pH del entorno que se está midiendo [37].
Se ha informado de otra clase de nanotermómetros basados en nanocristales semiconductores puros y dopados, con los candidatos más destacados como CdSe, ZnS, InP o PbSe [19, 38,39,40]. Los puntos cuánticos semiconductores (SQD) son candidatos para termómetros a nanoescala, considerando que tienen un alto rendimiento cuántico, una larga vida útil antes del fotoblanqueo y una biocompatibilidad adecuada después de la modificación adecuada de la superficie. Además, se pueden conjugar fácilmente con proteínas y ADN para la detección y la obtención de imágenes [41]. El desafío excepcional al que se enfrenta este tipo de termómetros luminiscentes es el reconocimiento asociado de brillo, fotoestabilidad, sensibilidad y precisión en T =20–40 ° C al sondear microambientes subcelulares. Los SQD se han revisado exhaustivamente en términos de síntesis, propiedades fisicoquímicas, luminiscencia y sus posibles aplicaciones. Aquí, dirigimos la atención del lector a estas numerosas reseñas notables [42,43,44,45,46]. En comparación con los tintes orgánicos, los SQD exhiben un brillo superior para la detección, un perfil de excitación más amplio para la multiplexación y una mejor fotoestabilidad para estudios a largo plazo. Además, los SQD como sensores de temperatura son resistentes al pH y otras variaciones ambientales que se espera que prevalezcan dentro de una celda [47].
Generalmente, en las SQD debido a una combinación de diferentes procesos, un aumento de temperatura produce una disminución en la intensidad de fluorescencia (extinción), que se acompaña de un cambio espectral. Se puede suponer que este cambio es lineal en el rango biofísico. La magnitud de ambos efectos (extinción de la luminiscencia y desplazamiento espectral) depende en gran medida del material que constituye los QD y de su tamaño [48].
Cada grupo de nanomateriales luminiscentes tiene limitaciones de uso junto con sus ventajas. Como se describió anteriormente, los SQD se favorecen más que los polímeros fluorescentes y los tintes orgánicos. Las SQD son buenas en términos de fotoestabilidad, eficiencia cuántica y fluorescencia sintonizable, pero las QD no se pueden utilizar para rastrear una sola molécula para la monitorización a largo plazo debido a su parpadeo intrínseco [49]. Además, el principal escollo de los QD es su toxicidad, que se debe a su contenido de metales pesados, incluidos metales como el cadmio; esto limita sus aplicaciones biológicas y ambientales. Además, la disponibilidad de elementos precursores en la naturaleza es relativamente baja y, por lo tanto, los SQD se consideran costosos [50].
Puntos de carbono como nanotermómetros
Para superar los problemas que surgieron con los nanotermómetros no basados en carbono (como explicamos en la sección anterior), se han preparado nanomateriales basados en carbono que muestran propiedades únicas, como baja toxicidad, fácil preparación, precursor de bajo costo, fotoestabilidad. y biocompatibilidad. Estos nanomateriales a base de carbono mostraron propiedades sensibles de detección térmica. Además, la mejora de las nanopartículas libres de metales es importante y urgente debido al peligro medioambiental de las aplicaciones biológicas de dichos materiales tóxicos [51, 52]. Entre la familia de nanomateriales basados en carbono, los nanodiamantes fluorescentes se han descrito por primera vez como nanotermómetros [53]. Los nanodiamantes fluorescentes poseen biocompatibilidad intrínseca como resultado de su superficie químicamente robusta e inerte [54]. Recientemente se han utilizado otros nanodiamantes para la detección térmica intracelular con un grado de precisión inferior [55, 56]. La sensibilidad térmica de estos nanodiamantes se basa en los llamados centros de color vacantes de nitrógeno, que son defectos puntuales que consisten en un átomo de nitrógeno que reemplaza un átomo de carbono reticular y un sitio reticular vacío cercano [48, 57]. El centro de vacantes de nitrógeno de los nanodiamantes fluorescentes se ha estudiado extensamente y se ha caracterizado bien por su fotofísica, así como por su uso en aplicaciones biológicas [58]. El principio de funcionamiento de la termometría basada en vacantes de nitrógeno depende de la medición precisa de este centro de color, que puede detectarse ópticamente con una alta resolución espacial [30, 59]. Sin embargo, la baja eficiencia de fluorescencia y la escasa capacidad de control impiden enormemente la aplicación de nanodiamantes fluorescentes [36].
Una de las clases más nuevas de la familia de nanomateriales basados en carbono son los puntos de carbono (CD) altamente luminiscentes, que tienen una fotoluminiscencia brillante excepcional, estabilidad fotoquímica, solubilidad en agua, gran biocompatibilidad y no toxicidad [60,61,62]. Los CD son nanopartículas de dimensión cero y con forma de esfera que poseen diámetros inferiores a 10 nm [63, 64]. Se han aplicado varios enfoques para preparar diversos tipos de CD, por ejemplo, ablación con láser [65], solvotermal [66], síntesis hidrotermal [67], asistida por microondas [68], descarga de arco [69], oxidación ácida [70], y más enfoques químicos y físicos [71, 72]. Además, los CD presentan una perspectiva deseable para diversas aplicaciones, como imágenes biológicas [73], biodetección y química [74,75,76,77], administración de fármacos dirigida [78], análisis farmacéutico [79] y catálisis [80, 81]. Los puntos de carbono se han revisado ampliamente en términos de síntesis, propiedades fisicoquímicas y sus aplicaciones potenciales. Aquí, remitimos al lector a las numerosas buenas críticas sobre puntos de carbono [72, 82,83,84,85,86,87,88].
En los últimos años, los CD fluorescentes como sensores de temperatura han atraído mucha atención por parte de los investigadores. En principio, se necesita algún requisito para la medición eficaz de la temperatura, como los nanodots de carbono deberían exhibir una variación apreciable en su fotoluminiscencia en el rango de temperaturas relevantes [89]. La fotoestabilidad, la estabilidad del pH y la vida útil son otros requisitos que deben tenerse en cuenta para la aplicación práctica.
Los CD son alternativas prometedoras para los puntos cuánticos semiconductores convencionales (SQD). En comparación con los QD, los CD muestran muchas ventajas sobresalientes, como el bajo costo, la baja toxicidad y sus propiedades ópticas / químicas únicas y robustas [90]. Además, los CD muestran muy menos fotoblanqueo. En comparación con otras materias primas fluorescentes, los CD se producen a partir de fuentes de carbono económicas que abundan en la naturaleza [91]. Además, existen varios métodos sencillos para modificar y funcionalizar el estado de la superficie de los CD, que permiten adaptar la solubilidad, la estabilidad, las propiedades fisicoquímicas y los rendimientos cuánticos de los CD de acuerdo con sus requisitos experimentales [49, 92, 93].
En la literatura, hay un número escaso de artículos reportados de puntos de carbono con fluorescencia dependiente de la temperatura y se muestran en la Tabla 1.
Yu y col. [51] en 2012 fueron los primeros en investigar la fluorescencia dependiente de la temperatura en nanodots de carbono y los compararon con semiconductores y nanopartículas a base de metales. Dependían de la medición de la vida útil de la fotoluminiscencia dependiente de la temperatura a través de la técnica de conteo de fotones individuales correlacionados en el tiempo (TCSPC). La dinámica de relajación de la fotoluminiscencia se vuelve más rápida a temperaturas más altas (Fig. 2a), lo que puede atribuirse a los procesos de desintegración no radiativa. Se realizó la medición de los espectros de fluorescencia de la película de CD en función de la temperatura desde la temperatura criogénica hasta la temperatura ambiente (Fig. 2b). Con un aumento de temperatura, la intensidad de la fluorescencia muestra una disminución repetitiva.
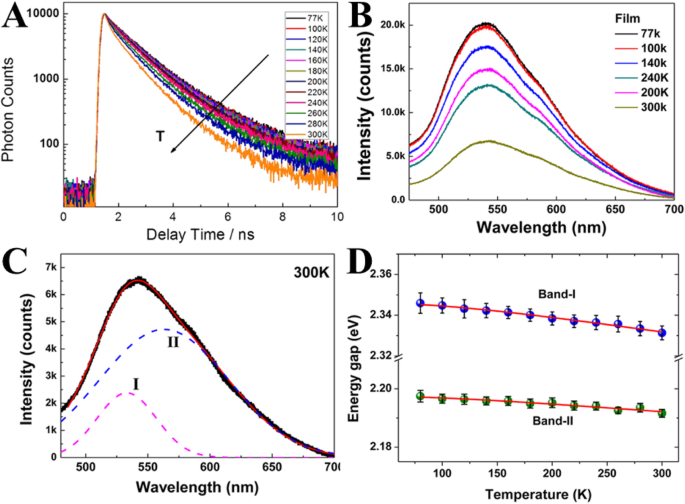
un Medidas de fotoluminiscencia resueltas en el tiempo en función de la temperatura. b Espectros de fluorescencia de la película de CD en función de la temperatura. c Espectros de fluorescencia a 300 K ajustados por una función de dos gaussianos. d El ancho de banda de la fluorescencia en función de la temperatura. (Reproducido con permiso de la referencia [51])
El espectro PL exhibe picos asimétricos, por lo tanto, los espectros PL a cada temperatura podrían ajustarse bien mediante una función de dos gaussianos mostrada en la Fig. 2c. La banda de alta energía, banda I; la banda de baja energía, banda II (Fig. 2d).
Además, se inspeccionó la brecha de energía (ancho de banda) de la fluorescencia en función de la temperatura (Fig. 2d). El ancho de banda total se pronuncia independientemente de la temperatura (dispersión de electrón-electrón) y dependiente de la temperatura (electrón-fonón y dispersión de superficie / defecto). El ancho de banda de la banda I y la banda II es independiente de la temperatura, lo que especifica que la dispersión electrón-electrón domina en los CD.
Por lo tanto, el efecto débil de la temperatura en los CD está de acuerdo con el hecho de que el principal mecanismo de interacción implica interacciones electrón-electrón en lugar del acoplamiento electrón-fonón. Además, una banda PL ancha (> 100 nm) generalmente observada incluso a muy baja temperatura (77 K) se refiere a una fuerte interacción electrón-electrón (Fig. 2c). Este resultado es similar a los nanoclusters metálicos y diferente de los QD de semiconductores. Por lo tanto, Yu y sus colaboradores especularon que los electrones π en los CD pueden actuar de manera similar como electrones libres en los nanoclusters metálicos.
Kalytchuk y col. [89] sintetizó N, S-CD altamente luminiscentes solubles en agua mediante un tratamiento hidrotermal de un solo paso de ácido cítrico y l-cisteína. Recolectaron espectros de absorción en estado estacionario en un amplio rango de temperaturas para caracterizar las propiedades PL de dependencia de la temperatura de los CD. Los espectros de absorción de N, S-CD dispersos en agua a temperaturas entre 10 y 70 ° C (aumentando en 5 ° C por paso) se muestran en la Fig. 3a. A diferencia de los nanocristales semiconductores, la posición y la intensidad de la banda de absorción no cambiaron con la temperatura. Anteriormente se informaron resultados similares para las CD sintetizadas mediante el tratamiento hidrotermal de la glucosa en presencia de glutatión [1].
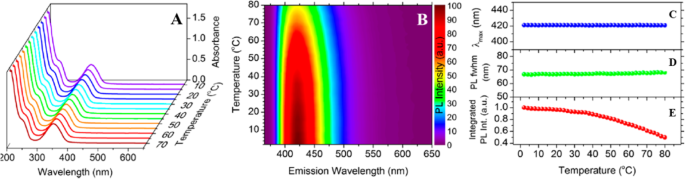
un Absorción dependiente de la temperatura tomada en el rango de temperatura de 10 a 70 ° C. b Gráfico de color normalizado de la emisión de PL dependiente de la temperatura a temperaturas entre 2 y 80 ° C con un tamaño de paso de 2 ° C y excitación a 355 nm. Cambios correspondientes dependientes de la temperatura en el pico máximo de PL λmax ( c ), PL fwhm ( d ) e intensidad PL integrada ( e ). (Reproducido de la referencia [89])
En su trabajo, mostraron un diagrama de color de los espectros PL de N, S-CD adquiridos a temperaturas que van de 2 a 80 ° C con un paso de 2 ° C (Fig. 3b). El aumento de la temperatura redujo la intensidad de las emisiones de PL en aproximadamente un factor de 2 sin ningún cambio detectable de las emisiones de PL [89]. La posición del máximo de emisión de PL, el ancho completo de PL a la mitad del máximo (fwhm) y la intensidad de PL integrada se determinaron cuantitativamente a la temperatura estudiada, condensando los resultados en la Fig. 3c-e, respectivamente.
La posición del pico PL de N, S-CD muestra una dependencia débil de la temperatura, a diferencia de la mayoría de los nanocristales semiconductores, cuya banda prohibida cambia con la temperatura, lo que induce el cambio de emisión de PL. Además, su PL fwhm exhibe sólo un ensanchamiento insignificante (1,4 ± 1 nm) en el mismo rango de temperatura (Fig. 3d), lo que indica que el pico PL de los N, S-CD muestra un ensanchamiento térmico insignificante. Para caracterizar los procesos de relajación no radiativa que ocurren en los CD, analizaron la extinción de la intensidad de PL integrada en función de la temperatura. En la figura 3e se muestra un gráfico de la intensidad PL integrada dependiente de la temperatura para N, S-CD, con los valores normalizados a la intensidad a 2 ° C, lo que revela que la intensidad disminuye monótonamente en el rango de temperatura estudiado, con eso en 80 ° C es aproximadamente la mitad que a 2 ° C. Con base en estos resultados, la energía de activación de la extinción térmica para los CD a temperaturas entre 2 y 80 ° C se estimó en 17.0 ± 0.7 meV utilizando la fórmula de Arrhenius para N, S-CD, que está cerca del valor informado por Yu et al. [51].
Además, Kalytchuk et al. [89] examinó la dinámica de emisión de CD a diferentes temperaturas. La Figura 4a-c muestra la fuerte dependencia de la temperatura de su emisión PL resuelta en el tiempo, mostrando datos de espectroscopía de emisión resuelta en el tiempo para tres temperaturas diferentes. Se adquirieron mapas de emisión de PL transitorios de CD en la región espectral entre 375 y 650 nm a 2, 50 y 80 ° C, como se muestra en la Fig. 4a-c. Hay una clara disminución en la desintegración de PL a medida que aumenta la temperatura, lo que sugiere que los CD tienen propiedades satisfactorias para la detección de temperatura basada en la vida útil de PL. Es importante señalar que se observó una desintegración exponencial simple espectralmente uniforme en los perfiles de emisión de los puntos a todas las temperaturas estudiadas, lo que indica que la recombinación se produce a través de canales muy similares y altamente emisores en todo el conjunto de CD. La dinámica PL de los CD es posiblemente su cualidad más prometedora en relación con las aplicaciones de detección de temperatura. Específicamente, la sensibilidad a la temperatura de los CD los convierte en nanotermómetros de vida útil PL.
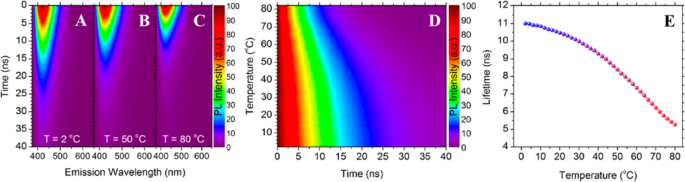
Emisión PL de CD dependiente de la temperatura resuelta en el tiempo. Gráficos de color normalizados que muestran mapas de emisión PL resueltos en el tiempo para CD en a 2 ° C, b 50 ° C y c 80 ° C. d El gráfico de color normalizado de la intensidad de PL resuelto en el tiempo en el máximo de emisión de PL (λem =421 nm) a temperaturas entre 2 y 80 ° C. e La vida útil de los PL extraídos se representa como una función de la temperatura en el rango de 2 a 80 ° C. (Reproducido de la referencia [89])
La variación de la vida útil del PL de los CD a temperaturas entre 2 y 80 ° C se ha investigado a fondo; La Fig. 4d, e muestra datos de PL resueltos en el tiempo recopilados en el máximo de emisión de PL de los puntos en función de la temperatura. En la Fig. 4d se presenta una gráfica de color de PL transitoria a lo largo del rango de temperatura estudiado, que muestra que el aumento de la temperatura conduce a un acortamiento monótono de la desintegración aparente de PL. Todas las curvas de desintegración registradas se ajustaron utilizando una función exponencial simple. Los datos sobre las vidas útiles extraídas se presentan en la Fig. 4e. A medida que la temperatura aumenta de 2 a 80 ° C, la vida útil del PL disminuye monótonamente de 11,0 a 5,3 ns. El rango de temperatura sobre el que se ha demostrado esta sensibilidad de vida útil PL (2–80 ° C) cubre tanto el rango de temperatura fisiológicamente relevante como las temperaturas de funcionamiento típicas de muchos dispositivos electrónicos. La sensibilidad pseudo-lineal absoluta de esta sonda térmica basada en CD de vida útil PL es 0.08 ns K −1 y su sensibilidad relativa máxima es 1,79% K −1 a 62 ° C. El ajuste exponencial simple de la desintegración PL de la nanoprobe luminiscente basada en CD en el rango de temperatura estudiado produce un solo parámetro, la vida útil PL (τ), que se puede convertir directamente en unidades de temperatura mediante una curva de calibración. Esta es una ventaja importante sobre los puntos cuánticos semiconductores típicos, que exhiben un decaimiento multi-exponencial que limita su utilidad en aplicaciones que involucran mediciones de vida útil PL.
También estudiaron la dependencia de la temperatura de la vida útil de los CD PL en solución salina tamponada con fosfato (PBS) y el medio de Eagle modificado de Dulbecco (DMEM) y mostraron un comportamiento similar.
Para demostrar la reutilización de los termómetros de luminiscencia basados en CD, se midieron las curvas de desintegración de PL de muestras seleccionadas durante siete ciclos sucesivos de calentamiento y enfriamiento a temperaturas entre 15 y 45 ° C (Fig. 5a).
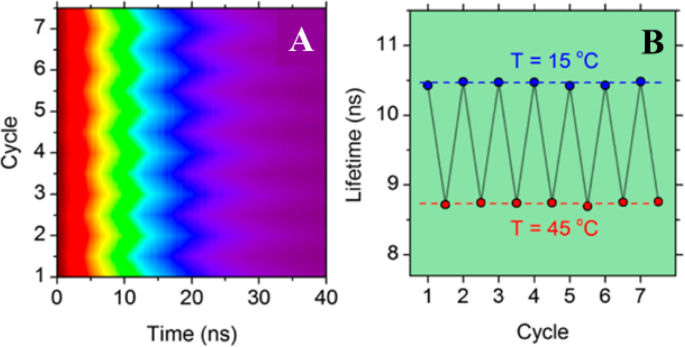
un Gráfico de color normalizado de la reversibilidad de la caída de PL durante siete ciclos secuenciales de calentamiento y enfriamiento. b Estabilidad térmica correspondiente de la vida útil de PL durante siete ciclos de calentamiento y enfriamiento entre 15 y 40 ° C. (Reproducido de la referencia [89])
En cada ciclo de medición, la caída de PL se midió después de un equilibrio térmico de 5 minutos. No se observó histéresis térmica durante los ciclos de calentamiento y enfriamiento, y la variación de la vida útil del PL resultante se grafica como una función del tiempo en (Fig. 5b), lo que demuestra que la vida útil PL de los CD exhibe una excelente estabilidad térmica.
Posteriormente, se prepararon varios CD con emisión dependiente de la temperatura utilizando una variedad de métodos de síntesis, como tratamiento hidrotermal y solvotermal [2, 77, 92, 95, 97,98,99,100,101,102,103], reflujo de calor [94, 96] y láser ablación [14] como se muestra en la Tabla 1. Los CD preparados mostraron fluorescencia lineal dependiente de la temperatura en los rangos fisiológicos (mostrados en la Tabla 1). La intensidad de fluorescencia de los CD disminuyó al aumentar la temperatura. Además, en todos los artículos se ha estudiado la reversibilidad y restaurabilidad de la intensidad de la fluorescencia. La Figura 6 muestra algunas propiedades comunes de los CD estudiados en varios artículos.
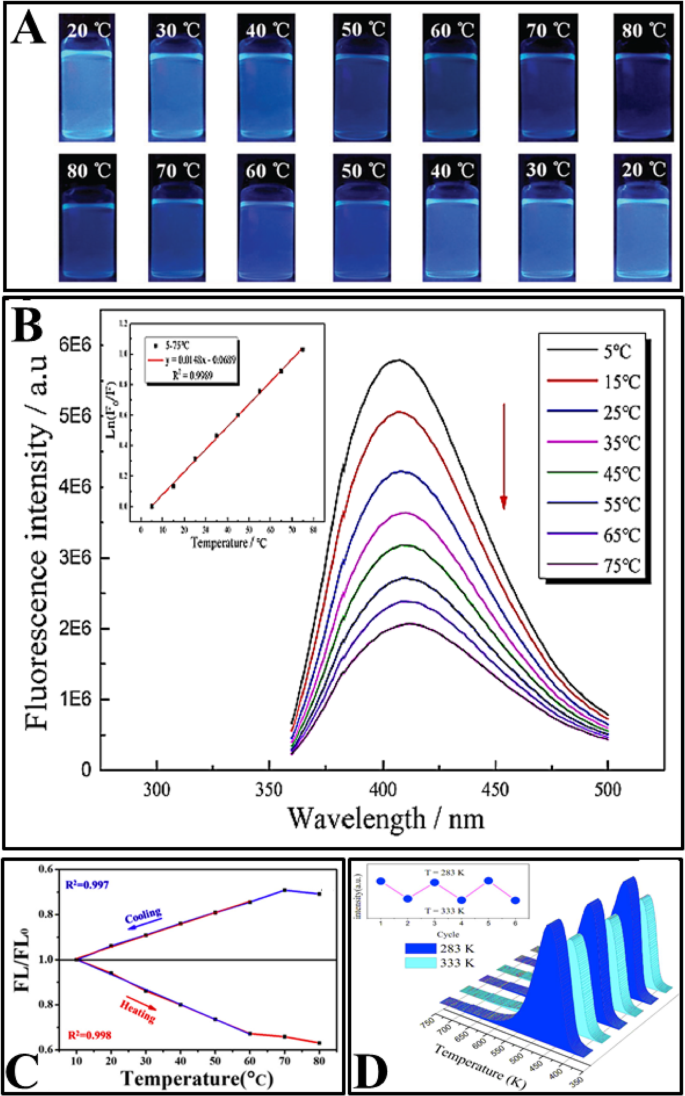
un Fotografías digitales de N, S-CD bajo excitación de luz UV (365 nm) a diferentes temperaturas durante los procesos de calentamiento (superior) y enfriamiento (inferior). (Reproducido de la referencia [96]). b Espectros de emisión de fluorescencia de CD codopados con N, S medidos en el rango de 5-75 ° C (de arriba a abajo) cuando se excitan a 340 nm, recuadro:la regresión lineal correspondiente de la temperatura frente a Ln ( F / F 0 ). (Reproducido de la referencia [97]). c FL / FL 0 - Gráficos de temperatura de MnOx-CD durante los procesos de enfriamiento y calentamiento. (Reproducido de la referencia [103]). d Dependencia reversible de la temperatura del PL de la solución de CD. (Reproducido de la referencia [102])
Nguyen y col. [14] puntos de carbono sintetizados (CD) mediante ablación con láser de femtosegundo de polvo de grafito en etilendiamina. Se formaron abundantes grupos funcionales en la superficie, lo que forma múltiples estados de superficie en el sitio de la superficie y da como resultado la emisión múltiple de CD. Investigaron la sensibilidad a la temperatura dependiente de la fluorescencia de los CD utilizando espectros de fluorescencia de estado estacionario. Los espectros de emisión dependientes de la temperatura de los CD a una excitación de 320 nm se muestran en la Fig. 7a. Ambas intensidades de fluorescencia de picos de 400 y 465 nm disminuyen gradualmente con el aumento de temperatura debido a la activación térmica de las vías de desintegración no radiativa. Las intensidades máximas cambian linealmente con temperaturas que oscilan entre 5 y 85 ° C (Fig. 7b). Los CD sensibles a la temperatura mostraron un cambio de intensidad de fluorescencia de 3.3 y 2.1% por ° C para picos de 400 y 465 nm, respectivamente. Esto indica que los CD se pueden utilizar como un sensor de temperatura convencional basado en la intensidad con alta sensibilidad.
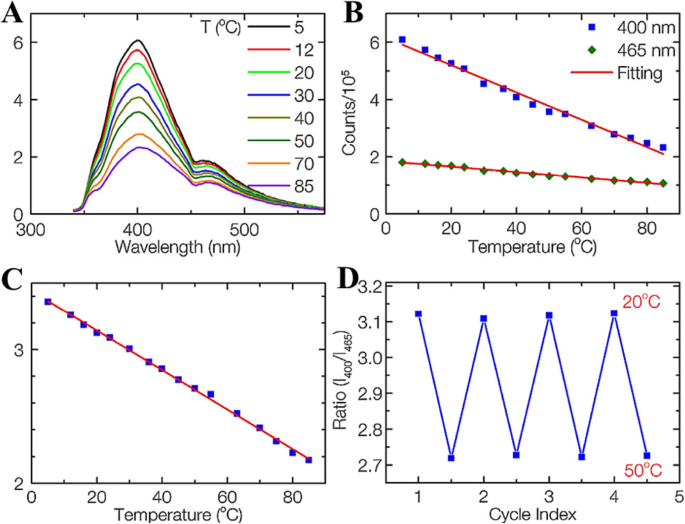
un Espectros de emisión de CD registrados de 5 a 85 ° C, excitados a 320 nm. b Intensidades de fluorescencia de los picos de 400 y 465 nm frente a la temperatura. c La relación de los 400 nm sobre los picos de 465 nm en función de la temperatura. d Estudio de reversibilidad de temperatura de CDs entre 20 y 50 ° C. (Reproducido de la referencia [14])
Sorprendentemente, la propiedad única de múltiples emisiones hace que los CD prometan fluoróforos para sensores de temperatura fluorescentes radiométricos. La relación de las dos intensidades de fluorescencia a 400 y 465 nm (excitación de 320 nm) frente a la temperatura se muestra en la Fig. 5c. There is a very good linear relationship between the intensity ratio and temperature in a wide temperature range from 5 to 85 °C (R 2 =0.998). Thermal linearity is advantageous since it makes the correlation between the peak-intensity ratio and temperature straightforward and meanwhile provides a constant thermal sensitivity along with the entire dynamic range. The temperature-sensitivity of CDs is determined to be 1.48% °C −1 , which is comparable with that of other materials. It should be noted that the temperature response range of CDs is much wider than those of other reports on dual-emission temperature sensors and covers both the physiological temperature for biology studies and the working temperature for many electronic devices. Besides 320 nm excitation, the CDs also work at other excitation wavelengths, such as 340 and 365 nm, with the same sensitivity. Thus, the CDs can be utilized for temperature sensing in many practical applications by selected different working wavelengths.
They have shown that the ratiometric temperature sensor was reversible between 20 and 50 °C, four cycles and photostable (when the intensity of the power source changed) as shown in Fig. 7d. This result suggests that the CDs sensing system is stable and robust with any changes in sample concentration, excitation, or detection efficiency.
Increasing temperature is not always accompanied by PL quenching; however, it could show enhancement of the PL as well. Macairan et al. [29] showed the PL enhancement of dual-fluorescent carbon dots with increasing temperature. They prepared biocompatible dual-fluorescing carbon dots CDs in a one-step microwave assisted-reaction using formamide and glutathione. They found that following excitation at 640 nm, the fluorescence intensity and PL integrated area increase over the range of 5–60 C by a factor of 3.5 observed over the entire analysis range and the temperature (Fig. 8a). As shown in Fig. 8b, a linear response (R 2 =0.999) is observed over the entire analysis range and the temperature sensitivity was determined to be as high as 3.71% C −1 .
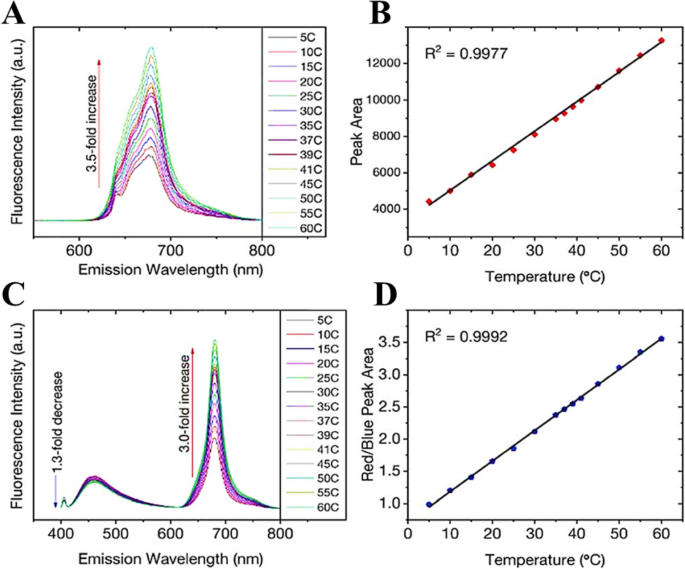
un Excitation at 640 nm yields a 3.5-fold increase in fluorescence intensity and the corresponding integrated area is plotted in b showing a linear response over the range of 5–60 °C. c Changes in the fluorescence spectra of the CDs (λex =405 nm) as a function of temperature over the entire range. A 1.3-fold decrease is noted for the blue fluorescence in contrast to the 3-fold increase for the red counterpart. d The ratio of the integrated areas of the red and blue fluorescence components are plotted as a function of temperature showing a linear increase over the entire temperature range. (Reproduced from reference [29])
The temperature-dependent fluorescence was also studied following excitation at 405 nm. Interestingly, the blue and red fluorescence bands are not equally sensitive to the change in temperature. With increasing temperature, the fluorescence intensity (and the corresponding integrated area under the curve) of the blue component shows a very slight decrease in contrast to the red component, which significantly increases (Fig. 8c). These observations are noted over the range of 5–60 °C where the blue emission decreases by a factor of 1.3 in contrast to the red emission, which increases by a factor of 3.0.
As shown in Fig. 8d, the ratio of red to blue fluorescence increases with temperature, and a highly linear response is triplicate on 3 unique samples and the linear plot reflects the observed with an R 2 =0.998. These analyses were repeated in an average of these measurements, which have small deviations at each temperature. The thermal sensitivity of the CDs, over the entire temperature range, varied from 1.33 to 4.81% °C −1 , which is an improvement over previously reported carbon dot nano-thermometry systems and other dual-emitting nanomaterials such as quantum dots and metal-organic frameworks-dye composites. The thermal resolution of the CDs was calculated to be 0.048 K −1 indicating that it is indeed possible to measure small thermal changes.
Zhang y col. [98] synthesized CDs that have temperature-responsive characteristics in the range of 25–95 °C, and they have excellent sensitivity and remarkable reversibility/recoverability (Fig. 9a). CD/epoxy composites were further prepared by uniformly doping CDs into an epoxy resin. First, 5 μg of the CDs were dissolved in 50 μL of triethylenetetramine (TETA). Then, 350 μL epoxy resin was added to the mixed solution and fully mixed by high-speed stirring. The resulting composite showed significantly enhanced temperature response.
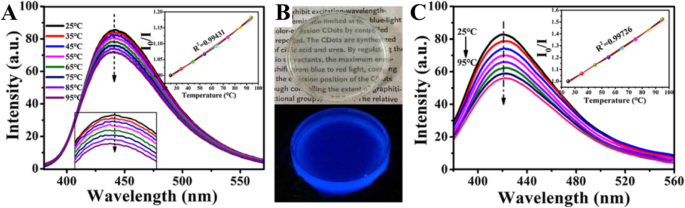
un Temperature dependence of the CD emission. b CD/epoxy composites. c Temperature dependence of the emission of the CD/epoxy composites. (Reproduced from reference [98])
Epoxy resin is a common thermosetting resin and is widely used to package LED chips. Figure 9b shows optical micrographs of CD/epoxy composite discs of approximately 2 cm in diameter and 8–10 mm in thickness. The cured CD/epoxy composites are transparent, and their fluorescence emission spectra are shown in Fig. 9c. The emission peak of the CD/epoxy composite is blue-shifted by approximately 10 nm compared to that of the CDs’ solution. Notably, the temperature response of the composite is significantly improved. In the temperature range of 25–95 °C, the fluorescence intensity decreases by 35% with increasing temperature, which is more than twice that of the solution state, and the linear results are more stable. The linear equation satisfies I 0 / Yo =0.0074 [°C] + 0.80454 (R 2 =0.99724), where I 0 y yo are the fluorescence intensity of the CD/epoxy composite before and after the temperature rise, and the excitation wavelength is 360 nm. The blue shift of the emission peak and the enhancement of the temperature response characteristics may be due to changes in the dielectric constant of the environment in which the CDs are located. The composite has a wide temperature detection range, and its excellent sensitivity and stability make it suitable for use as a temperature sensor based on a fluorescent nanomaterial in a variety of environments.
Mechanism of Thermo-sensing
Up to now, there is no well-established mechanism for explaining the thermo-sensing behavior of carbon dots. Some reports attribute the mechanism to the thermal activation of non-radiative channels of surface (trap/defect) states. The general picture is that the non-radiative channels were not activated at low temperatures, so the excited electrons could emit photons radiatively. On the contrary, as the temperature increases, more non-radiative channels became activated, and excited electrons got back to the ground state by non-radiative processes, leading to the decreasing fluorescence intensity [2, 95, 99, 100, 103]. The mechanism of CDs emissions with heating/cooling is shown in Fig. 10.
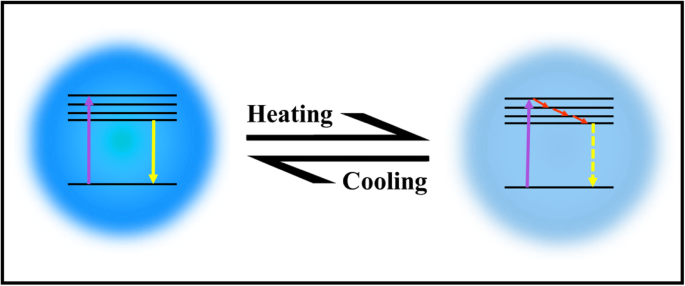
Schematic illustration of CDs responding to temperature changes
To better understand the thermodynamics of the CD emission processes, Kalytchuk et al. [89] correlated the radiative (\( {\tau}_r^{-1} \)) and nonradiative ( \( {\tau}_{nr}^{-1} \)) recombination rates of a CD sample with its PL quantum yield. The radiative rate is determined from the PL quantum yield (QY) and the measured recombination rate τ −1 as \( {\tau}_r^{-1} \) =QY × τ −1 . The nonradiative relaxation rate \( {\tau}_{nr}^{-1} \) is expressed as \( {\tau}_{nr}^{-1} \) =τ −1 - \( {\tau}_r^{-1} \). The PL QY of CDs at various temperatures was calculated from their temperature-dependent absorption and integrated PL intensity together with the PL QY determined at room temperature. Both radiative and nonradiative recombination rates derived from time-resolved PL measurement data are plotted as functions of temperature in Fig. 11. The radiative recombination rate is greater than the correspondent nonradiative rate up to 70 °C and does not vary appreciably at temperatures between 2 and 80 °C, remaining in the range of (0.74–0.82) × 10 6 s −1 . In contrast, there is a pronounced (almost 7-fold, from 0.16 × 10 6 to 1.12 × 10 6 s −1 ) monotonic increase in the rate of nonradiative recombination by increasing the temperature from 2 to 80 °C. Temperature-dependent crossover of the radiative and nonradiative rates occurs at 70 °C, at which temperature the PL QY is 50%. These results suggest that the temperature activation of PL quenching in their CDs is primarily caused by the activation of nonradiative relaxation channels [89].
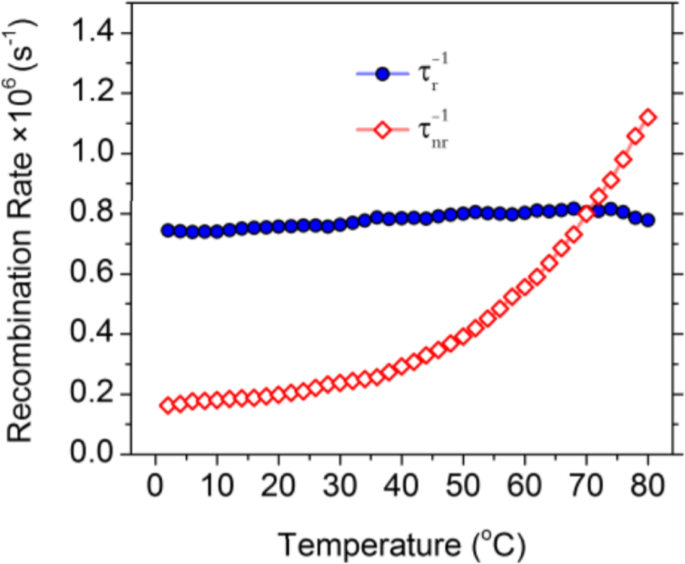
Radiative (solid symbols, blue color) and nonradiative (hollow symbols, red color) recombination rates for CDs plotted against the temperature for temperatures of 2–80 °C. (Reproduced from supporting information of reference [89])
Guo y col. [102] ascribed the thermal-quenching of their prepared carbon dots not just to activation of the nonradiative decay process, but also to the occurrence of nonradiative trapping with increasing temperature. They measured the temperature-dependent decay lifetimes of the CDs and shown in Fig. 12a. The data were collected by monitoring emission maximum as a function of the temperature under the 320 nm laser excitation. The result shows that the PL lifetime drops from 15.03 to 11.70 ns with the temperature increasing from 283 to 343 K, which could be ascribed to the occurrence of nonradiative decay processes. Besides, the PL relaxation dynamics of the CDs reveal multi-exponential decay with temperature increasing, which suggests the photoexcited carriers following the complicated relaxation processes. The occurrence of non-radiative trapping will be increased with rising temperature, and this could be quantitatively analyzed by the Arrhenius plot of the integrated PL intensities as:
$$ I={I}_0/\left[1+\mathrm{a}\ \exp\ \left(\hbox{-} {\mathrm{E}}_a/\mathrm{kT}\right)\right] $$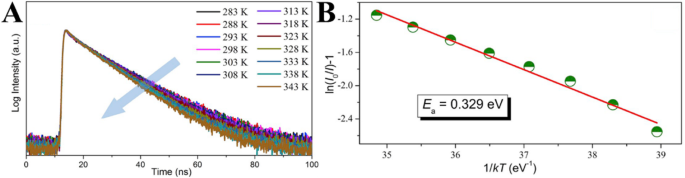
Temperature-dependent decay curves of CDs solution (a , λex =350 nm, λem =450 nm); the dependence of ln[(I 0 / Yo T )-1] on 1/kT CDs solution (b ). (Reproduced from reference [102])
donde E a is the activation energy, k is the Boltzmann constant, and a es una constante. Figure 12a displays the plotting of the emission intensity with respect to 1/T , where the value of activation energy (E a ) is calculated to be 0.329 ± 0.02 eV. In order to probe the reason for thermal quenching of CDs emission process, the radiative (V r ) and nonradiative (V nr ) recombination rates of CDs were determined from the lifetime (τ*) and quantum yield (QY) as:
$$ {\tau}^{\ast }=\frac{1}{V\mathrm{r}+V\mathrm{nr}};\mathrm{QY}=\frac{V\mathrm{r}}{V\mathrm{r}+V\mathrm{nr}} $$The QY of CDs at various temperatures was calculated from their temperature-dependent absorption and integrated PL intensity with the QY determined at room temperature. They have noticed that the radiative rates have a slight decline when the temperature rises from 283 to 343 K; at the same time, the nonradiative recombination rates have gradually increased by about 2-fold. These results further indicate that the temperature-activated PL quenching in CDs is mainly due to the activation of nonradiative relaxation channels [102].
Other groups used microscopic and spectroscopic techniques to understand the mechanism of thermos-sensing of carbon dots.
Wang at el. used TEM and UV–Vis spectra to study the temperature-responsive PL behavior of prepared CDs. As shown in Fig. 13a, the CDs display no change in the UV–Vis spectra upon increasing the temperature from 20 to 80 °C. However, it was found that the average diameter of CDs increased from 2.6 ± 0.2 nm at room temperature to 4.4 ± 0.2 nm at 80 °C (Fig. 13b). Thus, increasing the temperature, the aggregation of as-prepared CDs occurred which caused the obvious fluorescence quenching [1].
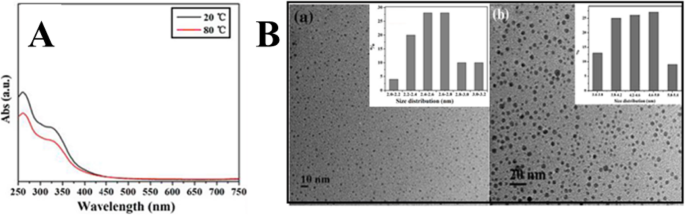
un UV–Vis absorption spectra of CDs in aqueous solution under 20 and 80 °C. b the TEM image of CDs in aqueous solution (a ) at room temperature, the average size was 2.6 ± 0.2 nm (b ) at 80 °C, and the size increased up to 4.4 ± 0.2 nm. (Reproduced from reference [1])
He et al. [101] reported that the hydration particle size of their CDs emerges as larger with the increase in the temperature (Fig. 14a), which indicates that the temperature rise gives rise to the aggregation of the CDs, eventually results in the fluorescence quenching. Nonetheless, with the decline in the temperature, the hydration particle size of CDs starts declining (Fig. 14b), which indicates that the cooling has the potential of causing CDs to depolymerize [101].
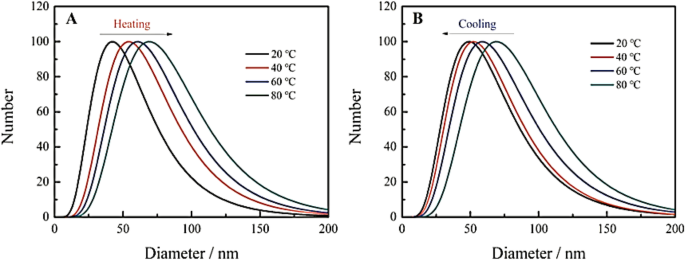
Change of hydrated particle size of carbon dots during heating (a ) and cooling (b ). (Reproduced from reference [101])
Another group such as Cui et al. also attributed the fluorescence quenching to the aggregation of CDs. They also tried to apply the undoped CDs synthesized using only acrylic acid as a precursor in temperature sensors. Unfortunately, undoped CDs possessed weaker quenching effects under the same temperature elevation than doped CDs [92].
Yang y col. [94] in their work proposed two key factors concerning the temperature-dependent PL property of the N-CDs, including (i) surface functional groups and (ii) hydrogen-bonding interaction. To examine the effect of the first factor, the surface O-containing groups, another control experiment was conducted by treating N-CDs (4.0 mL) with a strong reducing agent NaBH4 (1.0 mL, 0.1 mol L −1 ) to remove C=O species on carbon dots surface. The obtained reduced N-CDs are denoted as r-N-CDs for brevity. Compared with N-CDs, the r-N-CDs exhibit weaker fluorescence intensity (Fig. 15a). Besides, the fluorescence intensity of r-N-CDs only decreases by 13% with temperature increasing from 20 to 80 °C (the inset in Fig. 15a) that gives a much lower temperature sensitivity, which is ascribed to the decreased O-containing groups [94].
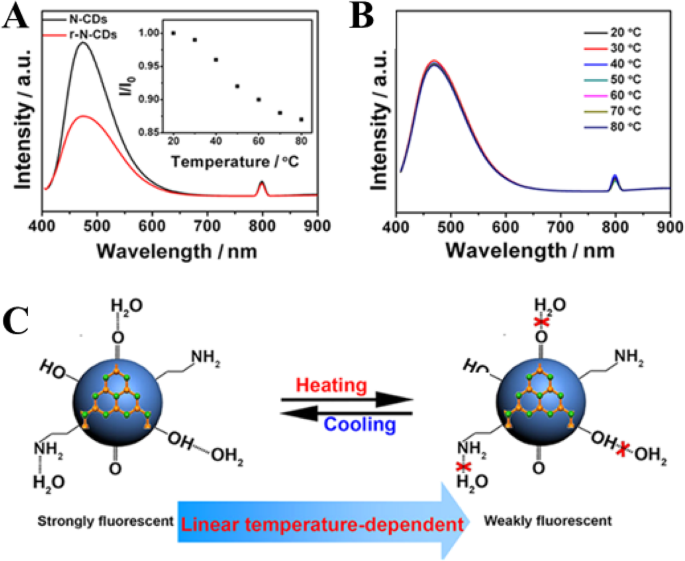
un PL spectra (excitation wavelength, 400 nm) of N-CDs (black trace) and r-N-CDs (red trace). The inset shows I / Yo 0 −T of reduced N-CDs. b PL spectra (excitation wavelength, 400 nm) of N-CDs dispersed in C2 H 5 OH at various temperatures. c A schematic mechanism for the temperature-dependent fluorescence intensity of N-CDs. (Reproduced from reference [94])
The second factor, the effect of hydrogen bonding with the solvent on fluorescent behavior of N-CDs was explored. N-CDs solution (1.0 mL) was dropped on a filter paper and left to dry in the air to obtain a solid sample, which still emits bright fluorescence. However, no obvious change of fluorescence intensity of the solid N-CDs with temperature increase was observed. They also measured the fluorescence of N-CDs dispersed in ethanol. The fluorescence intensity of N-CDs in C2 H 5 OH is lower than that in water and little variation of the PL intensity is observed with temperature increasing from 20 to 80 °C (Fig. 15b). Hence, the strong hydrogen bonds play a key role in the temperature-dependent PL property of the N-CDs. Figure 15c is a schematic mechanism for the temperature-dependent fluorescence intensity of N-CDs [94].
However, our group used the same experimental strategy as Yang group; in both cases, the r-CDs and e-CDs emissions were quenched linearly with increasing temperature, in the same way as the original results of their CDs (Fig. 16). Thus, our results ruled out the synergistic effects of abundant oxygen-containing functional groups and hydrogen bonds [77].
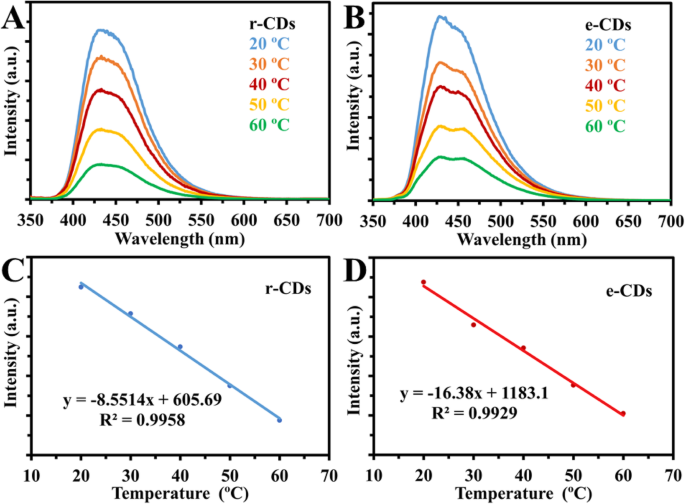
un , b Fluorescence spectra of reduced CDs (r-CDs) and CDs in ethanol (e-CDs) at temperatures (20 to 60 °C). c , d Linear correlation between fluorescence intensity and temperature (°C) for r-CDs and e-CDs respectively. (Reproduced from the supplementary information of reference [77])
Bioimaging in Living Cells (Thermal Imaging)
In literature, only a few articles explored the temperature-responsive fluorescent properties of CDs in biological imaging. Prior to such experimentations, in vitro cytotoxicity analysis is crucial for CDs because they make it possible to estimate the CD’s toxicity in living subjects. In vitro cytotoxicity analysis evaluates the effect or influence of the nanomaterial on cultured cells [89].
Yang y col. [94] verified that the CDs could be used as an effective thermometer in living cells; HeLa cells were washed with PBS after treatment with CDs for 6 h. Bright-blue fluorescence of the CDs in HeLa cells is observed when the temperature is 25 °C as shown in Fig. 17a. With the temperature increasing to 37 °C, the blue fluorescence becomes weaker (Fig. 17b), the fluorescence of N-CDs is recovered when the temperature was decreased to 25 °C (Fig. 17c). As a thermos-imaging in vivo, the fluorescent images of mice were collected immediately after being injected with N-CDs at different temperatures. By setting the fluorescence intensity at 28 °C as the reference (I o ), yo / Yo o of the area where CDs were injected varies from 1.0 to 0.87 with the increase of temperature from 28 to 34 °C (Fig. 17d, e). With temperature further increasing to 43 °C, I / Yo o declines to 0.52 and the fluorescence becomes nearly undetectable (Fig. 17f). And I / Yo o can be reversibly enhanced back from 0.66 to 1.0 with the temperature decreases from 39 to 28 °C (Fig. 17g–i). All of these results indicated that N-CD could be used as an effective in vitro and in vivo nanothermometer [94].
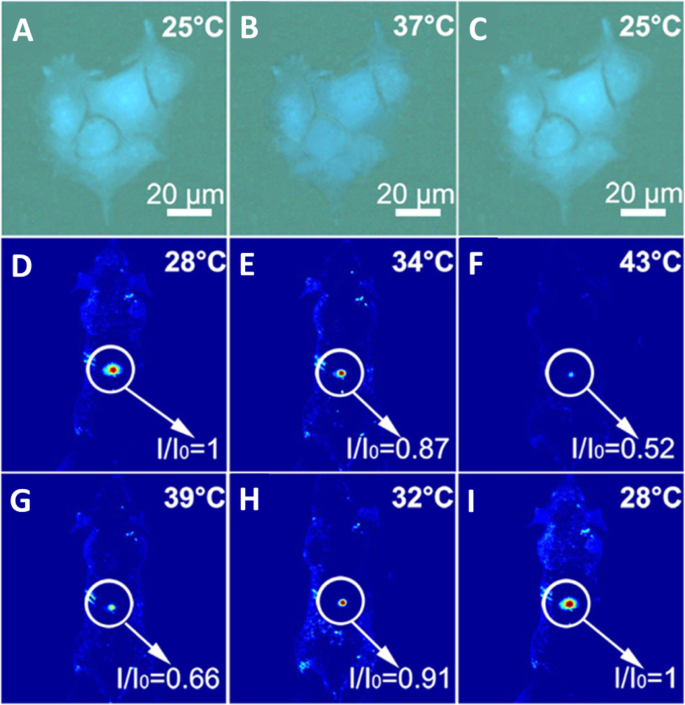
a–c Fluorescent images of a single Hela cell at 25, 37, and 25 °C after treatment with N-CDs, respectively. d - f Fluorescent photographs of a mouse given an injection of N-CDs at increasing temperatures. g - yo Fluorescent photographs of a mouse given an injection of N-CDs at decreasing temperatures. ( Reproduced from reference [94])
In an exploratory experiment, Kalytchuk et al. tested the capacity of CDs for intracellular temperature monitoring in human cervical cancer HeLa cells. Figure 18 shows the measured intracellular temperatures of HeLa cells incubated with CDs (500 μg/mL). The CDs’ PL decay curves at each temperature were highly reproducible and could be fitted with a single-exponential function at all recorded temperatures. In Fig. 18a, the recorded PL decay curves for temperatures between 25 and 50 °C (with a step size of 5 °C) are indicated by symbols, while the corresponding single-exponential fits are represented by solid lines. They were able to confirm that the PL signal in these PL lifetime measurements was derived exclusively from the CDs for the CD concentration of ≥ 100 μg/mL. The intracellular temperature in each measurement was determined from the calibration curve between PL lifetimes as the temperature increases from 2 to 80 °C. The temperatures determined in this way (T meas ) are plotted as functions of the PL lifetime in Fig. 18b. Independently, the temperature of the cell solution was determined using a calibrated reference thermometer (shown in Fig. 18b as Tset ). The temperatures reported by the luminescent CD probe and the reference detector are in good agreement. These results show that the PL lifetime of nanoprobes based on CDs can be reliably used to measure intracellular temperatures [89].
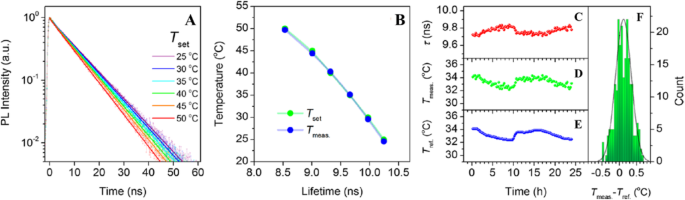
In vitro intracellular PL lifetime thermal sensing using CDs. un PL emission decays of HeLa cells incubated with CDs (500 μg/mL) at different temperatures (T establecer ). b Temperatures determined using the calibration (T meas ) and set temperatures (T establecer ) plotted against the PL lifetime. c - f Applicability of CDs for long-term remote intracellular temperature monitoring. c PL lifetimes extracted from PL transients recorded every 15 min for 24 h of HeLa cells incubated with CDs (500 μg/mL). d Temperatures determined using the calibration curve. e Temperatures measured with a reference thermometer (T ref ). f Histogram showing the distribution of temperature differences between the obtained and reference temperatures; the solid line is the distribution curve. (Reproduced from reference [89])
To further evaluate the potential of luminescent CD nanoprobes for long-term real-time temperature monitoring, PL decay profiles of HeLa cells incubated with CDs (500 μg/mL) every 15 min for 24 h were recorded. The PL lifetimes extracted from the measured PL decay values during this period were then plotted as functions of time, as shown in Fig. 18c. Using these results, the temperature variation over time was calculated using the calibration curve, as shown in Fig. 18d. In addition, the sample’s temperature at each measurement point was determined using a reference thermometer with a temperature reproducibility of 60 mK. The temperature determined with the reference thermometer is plotted in Fig. 18e, which shows that there was excellent agreement between the measured and reference temperatures. The high accuracy of the PL-based temperature measurements is further demonstrated by statistical analysis of the differences between the measured and real (reference) temperatures (Fig. 18f). Using these data, the absolute average accuracy of temperature detection by the presented method was calculated to be 0.27 °C. This experiment confirms the potential of CD-based thermal probes in biological systems [89].
Macairan et al. [29] displayed that the prepared CDs can be used for thermal sensing inside cells using intensity and ratiometric approaches. HeLa cells treated with CDs were allowed to equilibrate at 32, 37, and 42 °C (Fig. 19). Excitation at 640 nm was used to selectively monitor the red fluorescence of the CDs in the cells. The thermal changes could be due to changes in intracellular concentration or not correlate with a change in intensity (λex + 640 nm). This could be due to changes in intracellular concentration or localization of the CDs at higher temperatures. Thus, simply relying on changes in fluorescence intensity leads to accurate intracellular thermal sensing.
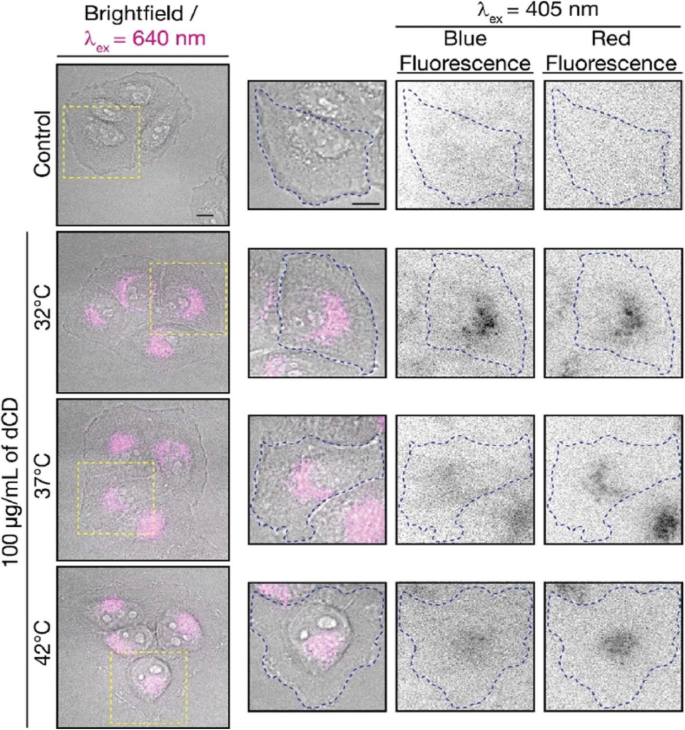
Fluorescence microscopy images of CD-treated HeLa cells. Fluorescence signals from the CDs (λex =640 nm; left and 405 nm; right) fluorescence ratios are 1.8 at 32 °C, 2.0 at 37 °C, and 2.3 at 42 °C. The control shows untreated HeLa cells at 42 °C with no fluorescence signal as expected. (Reproduced from reference [29])
In contrast, these limitations are excluded using the ratiometric approach. The CDs maintain dual blue and red fluorescence in cells following excitation at 405 nm, as previously observed for the colloidal dispersions (Fig. 19). The red-to-blue ratio increases with increasing temperature, with values of 1.8 at 32 °C, 2.0 at 37 °C, and 2.3 at 42 °C. The ratiometric relationship of the red-to-blue fluorescence of the CDs highlights the advantage of ratiometric temperature sensing in the development of fluorescent nano-thermometry probes. The relative red-to-blue emission ratio remains unaffected, regardless of the amount of CDs taken up by the cells, which can be affected by various factors such as confluency and is not concentration-dependent. Lastly, the CDs have shown fluorescence reversibility with respect to changes in intracellular temperature. Following incubation in HeLa cells, they were subjected to a heating/cooling cycle from 32/42/32 °C. This emphasizes the robustness of the proposed CD-nanothermometer and these findings further demonstrate the fluorescence reversibility [29].
Confocal laser scanning microscopy was used to thermal image colon cancer cell HT-29 using N, S, and I-doped CDs, as shown in Fig. 20 [100]. The fluorescent spots were temperature-dependent as shown in Fig. 20g–i, as the most intense is at 15 °C, while the weakest point was at 35 °C. Interestingly, the fluorescence spots were reversible, and the spots were very photostable after 20 min of continuous excitation [100]. Shin et al. [96] also used confocal laser scanning microscopy for Hela cells, shown in Fig. 20e–g.
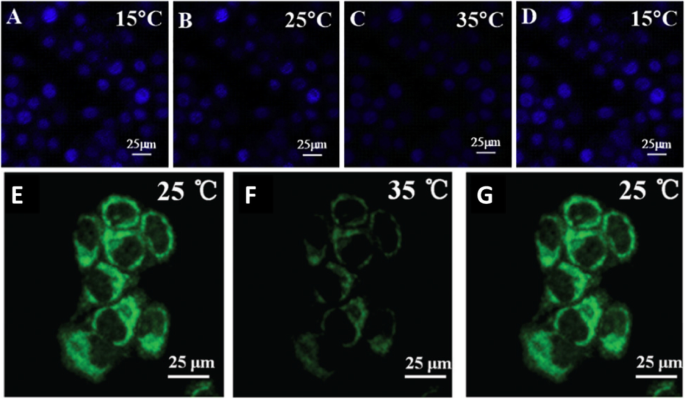
a–d Are confocal microscopy images of N, S, I-CDs-colon cancer cell HT-29 with corresponding fluorescence field at 15, 25, 35, and 15 °C, respectively. (Reproduced from reference [100]). e - g Confocal microscopy images of N, S-CDs-stained cells with corresponding fluorescence field at 25, 35, and 25 1C, respectively. (Reproduced from reference [96])
Li y col. 103 prepared a nanocomposite composed of MnOx-CDs to be used as a nano thermos responsive fluorophore for biological environments. HepG2 cells were incubated with MnOx-CDs at different culture temperatures. As illustrated by confocal laser scanning microscopy (excited at 405 nm), the blue luminescence of the MnOx-CDs in the HepG2 cells is weak when the environmental temperature was 40 °C (Fig. 21a), and the blue luminescence of the MnOx-CDs in HepG2 cells enhances as the temperature decreased to 30 °C (Fig. 21b) even to 20 °C (Fig. 21c). Due to the temperature-responsive properties, the as-synthesized MnOx-CDs can be readily applied in the biomedical fields like bioimaging and photothermal therapy in cancer treatment [103].
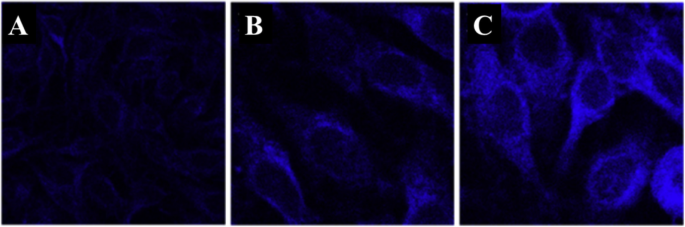
Confocal laser scanning microscopy images (excited at 405 nm) of MnOx-CDs in HepG2 cells at 40 °C (a ), at 30 °C (b ), and 20 °C (c ). (Reproduced from reference [103])
Conclusions and Future Perspective
Carbon nanodots exhibit unique properties to be exploited for nanothermometry, such as thermal-sensitivity, low-cost, and photostability. Flexible surface modification and facile preparation will pave the way to establish an enormous number of thermal sensitive nanomaterials for a variety of applications. The overall trends in thermo-sensing nanomaterials are aimed at enhancing photostability and thermal-resolution with using low-cost and safe materials. CDs can be classified as a new generation of thermometer that can fulfill these requirements and can be used for biomedical thermometry applications, such as temperature monitoring during hyperthermia treatment. Facile-preparation protocols, biocompatibility, and easy functionalization of CDs are promising criteria which make the CDs alternative next-generation nanothermometer materials. More efforts are required to promote basic research in this field. Limitations should be overcome to produce carbon dot-based nanothermometers comprising enhancing thermal sensitivity, and working in a broader range of temperature. A better understanding of the fluorescence thermal-sensing mechanism is another key issue to be able to design and manipulate the structure of CDs and enhance thermal resolution. More experiments and theoretical modeling are necessary to understand the correlation between the methods of fabrication of CDs with their thermal behavior.
Nanomateriales
- Novedades en materiales para impresión 3D:seguimiento del progreso reciente
- Investigación del MIT para establecer un nuevo estándar para la evaluación del ciclo de vida
- Nueva gama de tecnologías antivirales para una variedad de materiales
- Materiales:Nuevo LSR autoadhesivo para sobremoldeo en PC, PBT
- Materiales:Consejos de recocido para polímeros amorfos, Parte 2
- Parte 3 Materiales:puntas de recocido para polímeros semicristalinos
- Materiales:PP reforzado con fibra de carbono y vidrio para automoción
- DARPA está trabajando en materiales de próxima generación para vehículos hipersónicos
- Nuevos cristales para tecnologías de visualización de próxima generación
- Trelleborg anuncia nuevo distribuidor para materiales de herramientas
- Nuevos materiales Solvay, procesos diseñados para la industrialización



