Verde sintetizado fitoquímicamente (Zingiber officinale y Allium sativum) Nanopartículas de óxido de níquel reducidas Potencial catalítico y bactericida confirmado
Resumen
Las nanopartículas fito-sintetizadas (NP) que tienen una toxicidad química reducida se han enfocado a nivel mundial y se han convertido recientemente en un componente esencial de la nanotecnología. Preparamos fitoquímicamente verdes (jengibre y ajo) NP-NiO reducidos para reemplazar al agente catalítico y bactericida sintético en la industria textil. Las NP se caracterizaron mediante espectroscopia visible ultravioleta (UV-Vis), difracción de rayos X (XRD), espectroscopia de fotoelectrones de rayos X (XPS), espectroscopia de infrarrojos por transformada de Fourier (FTIR), espectroscopia de rayos X de dispersión de energía (EDS). ), microscopía electrónica de barrido (SEM) y microscopía electrónica de transmisión (TEM). La síntesis de NP fue confirmada por XRD y UV-Vis que tienen una fuerte absorción a 350 nm con un tamaño que varía entre 16 y 52 nm para el jengibre y entre 11 y 59 nm para el ajo. La microscopía electrónica de barrido y transmisión confirmó el pleomorfismo con NP de forma cúbica y más esférica. Además, las cantidades exactas de extractos de ajo y jengibre (1:3,6 ml) incorporadas para sintetizar NiO-NP han sido confirmadas con éxito por FTIR. Los NP reducidos fitoquímicamente por el ajo presentaron una actividad bactericida mejorada contra el Staphylococcus aureus resistente a múltiples fármacos. a concentraciones crecientes (0,5, 1,0 mg / 50 μl) y también degradó el colorante azul de metileno (MB) de manera eficiente. En conclusión, los NiO-NP sintetizados en verde son activistas inminentes para resolver la resistencia a los medicamentos, así como un agente catalítico respetuoso con el medio ambiente que puede optarse a escala industrial.
Introducción
Influencia de la materia de la nanotecnología con al menos un tamaño de dimensión de 1 a 100 nm que proporciona la capacidad de diseñar material controlando su tamaño [17]. Las NP, debido a sus propiedades químicas, físicas y biológicas únicas en diversos campos, incluida la medicina, han recibido una gran atención. Sus propiedades se pueden alterar fácilmente cambiando el tamaño a escala nanométrica [47].
Los NP de níquel (Ni) y óxido de níquel (NiO) tienen gran importancia debido a sus propiedades magnéticas, catalíticas y electrónicas particulares en tecnología energética, magnetismo, biomedicina y electrónica [9, 26, 35]. NiO con una banda prohibida amplia de 3.6 a 4.0 eV y una estructura de celosía cúbica tiene potencial debido al semiconductor tipo p. Estos NP que tienen alta estabilidad química, propiedades de supercapacidad, capacidad de transferencia de electrones y electrocatálisis se utilizan en biomedicinas y actividades fotocatalíticas, antiinflamatorias y antibacterianas [8, 10, 11, 45]. La aparición de enfermedades infecciosas, especialmente resistentes a los antibióticos (MDR), ha devastado la salud pública en todo el mundo. En general, las cepas bacterianas patógenas Gram-positivas (G + ve) y Gram-negativas (G −ve) se encuentran entre las principales amenazas para la salud pública.
En la industria láctea, la mastitis bovina es una enfermedad problemática importante que tiene un gran impacto económico y se caracteriza por cambios químicos, microbiológicos y físicos en la leche, mientras que cambios patológicos en los tejidos glandulares de la ubre [6, 19]. La etiología de la mastitis incluye agentes infecciosos, es decir, bacterias, virus y hongos, y las más importantes son las bacterias, divididas en dos grupos:principales ( Streptococci, Staphylococcus aureus , Corynebacterium pyogenes y coliformes ) y patógenos menores ( Corynebacterium bovis y estafilococos coagulasa negativos ) [25]. La aparición de múltiples cepas bacterianas Gram-positivas y Gram-negativas resistentes a los medicamentos representa una amenaza significativa para la salud pública [23, 32].
Zingiber officinale (jengibre) es un ingrediente importante en Ayurvedia y Unani, y la medicina herbal china se trata para diversas dolencias como las náuseas, la ayuda digestiva, el reumatismo y los trastornos hemorrágicos debido a la amplia diversidad de aceites volátiles como zingiberol, monoterpeno, sesquiterpeno y hidrocarburos sesquiterpénicos [12, 13, 43]. Sin embargo, Allium sativum (ajo) contienen componentes organosulfurados, es decir, grupos alil sulfuro, aliína, ajoeno, alil cisteína y alicina, y otros como vitaminas, fosfolípidos, flavonoides, aminoácidos y ácidos grasos que orientan sus propiedades médicas [14, 24] . Nuestro objetivo fue evaluar la acción bactericida de las NP de óxido metálico de Ni reducidas fitoquímicamente contra MDR ( S. aureus ), un aislado de mastitis bovina, y este será el primer informe de Pakistán en el área de investigación veterinaria sobre el agente antes mencionado.
Métodos
El presente estudio tuvo como objetivo investigar la acción bactericida de los NiO-NP reducidos fitoquímicamente contra MDR ( S. aureus ), un aislado de mastitis bovina.
Materiales
Nitrato de níquel [Ni (NO 3 ) 2 ], hidróxido de sodio (NaOH), azul de metileno (MB) y borohidruro de sodio (NaBH 4 ) de grado analítico se compraron a Sigma-Aldrich®, y se recolectaron raíces frescas de jengibre y ajo del mercado local. Las raíces se secaron a la sombra para lograr un peso constante para su posterior procesamiento. Los discos de antibióticos se adquirieron de Bioanalyse® (Turquía). Los medios de crecimiento bacteriano utilizados fueron de calidad analítica por TM Media, (Titan Biotech Ltd, India).
Preparación de extractos acuosos
Las raíces de jengibre y ajo se pulverizaron hasta obtener un polvo fino utilizando un molinillo eléctrico y se conservaron en recipientes de plástico. El polvo de la raíz triturada se mezcló con una cantidad controlada de agua destilada-DIW (1:10) con agitación vigorosa a 70 ° C durante 30 min. Los extractos se enfriaron, se filtraron con papel de filtro Whatman No.1 y se almacenaron a 4 ° C (Fig. 1) hasta su uso posterior.
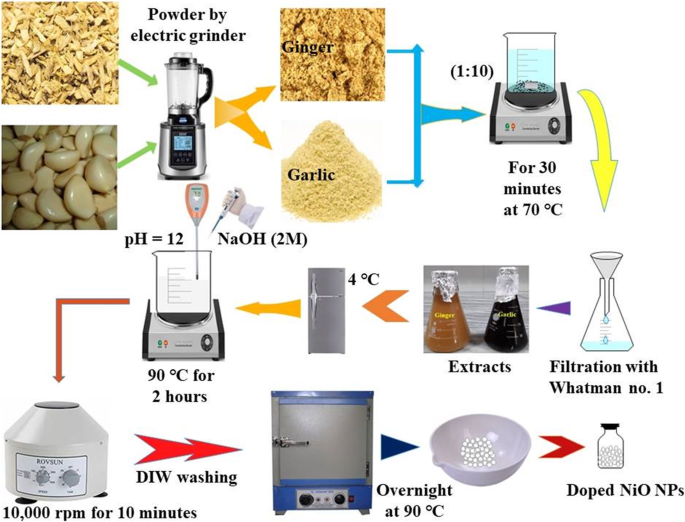
Esquema de síntesis de extracción de jengibre y ajo y NP-NiO reducidas fitoquímicamente
Síntesis verde de NiO-NP
Se añadieron extractos acuosos de jengibre y ajo de diversas proporciones (1,2, 1,8, 2,4, 3,0, 3,6 y 4,2 ml) a nitrato de níquel (0,1 M) con agitación continua. La solución agitada a pH 12 se mantuvo usando NaOH (2 M) a 90ºC durante 2 h. Los precipitados formados se centrifugaron a 10.000 rpm durante 10 min, se lavaron con DIW y se secaron durante la noche en un horno de aire caliente a 90 ° C como se ilustra en la Fig. 1.
Caracterización
Máximos de absorción ( ƛ máx ) de NP sintetizadas se escanearon con un espectrofotómetro UV-Visible (Genesys 10 S) de longitudes de onda de 200 a 800 nm. La composición de fases y la información estructural se analizaron mediante difracción de rayos X (XRD) BUNKER D2 phaser que tiene un rango de 2θ de (10–80 °) equipado con radiaciones de Cu Kα1 de λ =1,540 Å. Los grupos funcionales NiO-NP sintetizados en verde se registraron utilizando espectroscopia infrarroja por transformada de Fourier (ATR-FTIR). El tamaño, la forma y el análisis elemental de las NP se analizaron mediante microscopio electrónico de emisión de campo (FESEM) y microscopía electrónica de transmisión Hitachi H7100FA (TEM). La composición de la muestra con los correspondientes huecos de banda se investigó mediante espectroscopía de fotoelectrones de rayos X (XPS).
Aislamiento e identificación de MDR S. aureus
Aislamiento de S. aureus
Se cultivaron muestras de leche bovina clínicamente positivas recogidas en granjas y hospitales veterinarios del sector público y privado en Punjab, Pakistán, en agar sangre de oveja al 5% y se incubaron a 37 ° C durante 24 a 48 h. Las colonias características obtenidas se sembraron más en estrías en agar con sal de manitol (MSA) TM Media (Titan Biotech Ltd, India) en tripletes para aislar S. aureus .
Identificación de MDR S. aureus
La identificación de colonias bacterianas se realizó mediante características morfológicas, tinción de Gram y procedimientos bioquímicos (prueba de coagulasa y catalasa) según la descripción del manual de bacteriología determinante de Burgey.
La susceptibilidad a los antibióticos de las colonias características se evaluó mediante una prueba de difusión en disco basada en las pautas del Comité Nacional de Estándares de Laboratorio Clínico (NCCLS) para el aislamiento de MDR S. aureus . Discos de antibióticos que contienen oxitetraciclina (30 μg), tilosina (30 μg), gentamicina (10 μg), ciprofloxacina (5 μg) y trimetoprim + sulfametoxazol (1,25 μg + 23,75 μg) aplicados asépticamente en medios de agar Mueller-Hinton (MHA) TM (Titan Biotech Ltd, India) 1 × 10 8 Las UFC / ml se mantuvieron a 37 ° C durante 24 h [7]. La bacteria que se encontró resistente a un mínimo de tres antibióticos fue declarada MDR [28].
Actividad antimicrobiana
El potencial de acción antimicrobiana in vitro de las NiO-NP fitoquímicamente reducidas se evaluó mediante el método de difusión de pozos de agar sobre diez aislamientos representativos de MDR S. aureus extraído de la leche mastitic. Las placas de Petri se frotaron con 1,5 × 10 8 UFC / ml (estándar 0,5 McFarland) MDR S. aureus en MSA. Se formaron pocillos de 6 mm de diámetro utilizando un taladro de corcho estéril. Se aplicaron diversas concentraciones de extractos acuosos individuales de jengibre, ajo y NiO-NP sintetizados en verde (reducidos fitoquímicamente). Se utilizaron extractos acuosos a concentraciones de (10 mg / 100 μl) y (50 mg / 100 μl) y NiO (0,5 mg / 50 μl) y (1,0 mg / 50 μl). Se utilizó ciprofloxacina (0,005 mg / 50 μl) como control positivo y DIW como control negativo (50 μl).
Análisis estadístico
La eficacia antimicrobiana se calculó en términos de tamaño de la zona de inhibición (mm) y los diámetros de la zona de inhibición se analizaron estadísticamente mediante análisis de varianza unidireccional (ANOVA) utilizando SPSS 20.
Catálisis
Para la evaluación catalítica del extracto sintetizado de NiO, se mezcló borohidruro de sodio acuoso recién preparado (300 μl) con 3 ml de azul de metileno (0 . 03 × 10 −3 M) solución. Posteriormente, se añadieron a las soluciones 300 µl de muestra coloidal de la concentración deseada. El color azul claro del tinte azul de metileno (MB) desapareció, lo que representa la degradación del tinte a azul de leucometileno como se muestra en la Fig. 2. La absorción se observó entre 200 y 800 nm utilizando un espectrofotómetro UV-Vis.
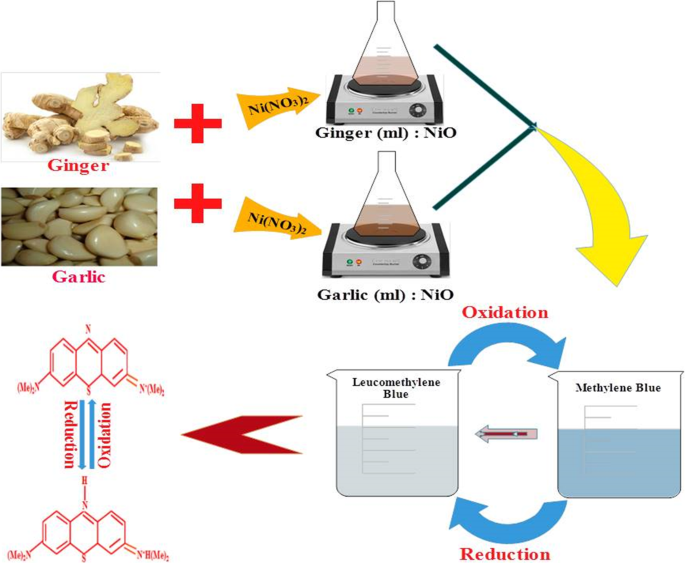
Diagrama esquemático para la reducción catalítica de MB a LMB mediante NP sintetizadas en verde
Resultados y discusión
Las propiedades ópticas del NiO reducido fitoquímicamente por extractos acuosos de jengibre y ajo entre 200 y 600 nm se presentan en la Fig. 3a, b. La absorbancia máxima ( λ máx ) en NiO-NPs se observó alrededor de 350 nm (1:3,6 ml) que aumentó con la concentración de extractos acompañada de desplazamiento azul. Los picos de absorción de extractos de jengibre y ajo aparecieron alrededor de 275 y 280 nm, respectivamente. Se observó un cambio de color abrupto en las mezclas de reacción de rojo vino a verde claro después de la incorporación de extractos de raíces. La amplitud máxima indicó la aglomeración de partículas y la transición electrónica de la valencia a las bandas de conducción con concentración de extracto en NiO, como lo revelan las bandas de absorción fuertes [20]. Por tanto, en la Fig. 3a, los resultados b mostraron una disminución en la absorción de NP sintetizadas al aumentar o disminuir el volumen del extracto más allá del valor optimizado (1:3,6 ml). La banda prohibida se calculó utilizando la gráfica de Tauc (Ec. 1).
$$ \ left (\ alpha hv \ right) =B {\ left (hv- {E} _g \ right)} ^ {\ raisebox {1ex} {$ 1 $} \! \ left / \! \ raisebox {-1ex } {$ 2 $} \ right.} $$ (1)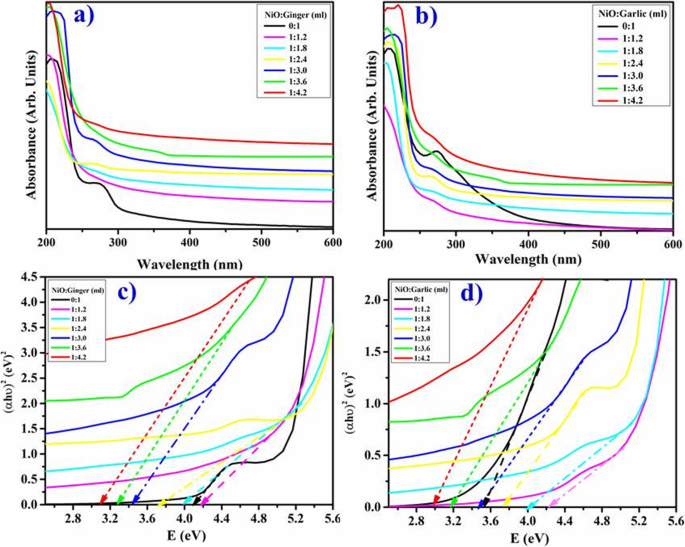
un - d Espectros de absorción de NiO-NP sintetizados en verde con jengibre ( a ) y extracto de ajo ( b ). Band gap de NiO reducido fitoquímicamente por jengibre ( c ) y ajo ( d ) respectivamente
Donde α es el coeficiente de absorción, h es la constante de Planck, B es una constante, υ se conoce como frecuencia de fotones y E g es la banda prohibida de energía. La banda prohibida estimada de NiO reducido fitoquímicamente por el jengibre y el ajo de una parcela de ( αhʋ ) 1/2 contra la energía de los fotones ( hʋ ). La intersección de una tangente a x -eje se registró, que proporciona energías de banda prohibida de muestras como se muestra en la Fig. 3c, d. Las variaciones en las energías de la banda prohibida se determinaron al dopar jengibre en NiO de 4,15 a 3,1 eV y con ajo de 3,5 a 3,0 eV respectivamente (Fig. 3c, d).
La cristalinidad, el tamaño y la composición de fases de NiO-NP se confirmaron mediante XRD como se muestra en la Fig. 4 a, b. Los picos en los valores 2θ 37.10 °, 43.32 °, 62.81 ° y 76.51 ° corresponden a (111), (200), (220) y (311) (tarjeta JCPDS no:00-047-1049) (Fig. 4a , b) referenciado por [30]. La intensidad máxima indica NiO cúbico (fcc) hexagonal y centrado en las caras con un tamaño medio de 32,9 nm calculado por D =0.9λ / βcosθ para jengibre y 29.92 nm para NiO-NPs fitoquímicamente reducidos de ajo. Los picos anchos indican la presencia de espacios de oxígeno y un trastorno de la red local en la muestra [38]. Varios fitoquímicos de jengibre (flavonoides, alcaloides, taninos y saponinas) y extractos acuosos de ajo (alicina, sulfuro de alilo, aliina, ácidos grasos, glicolípidos, fenólicos, aminoácidos y flavonoides) que actúan como agentes de cobertura son responsables del tamaño medio de cristalito de NP de óxido metálico [14, 46].
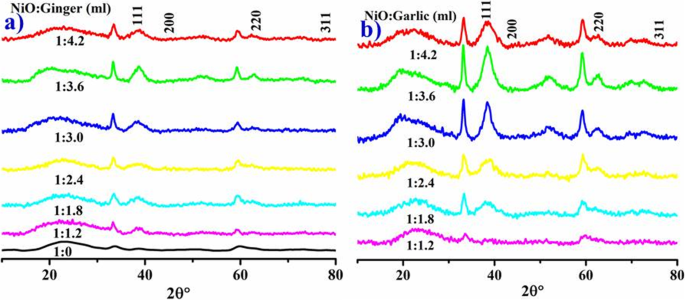
Patrón de XRD de diferentes concentraciones de NiO reducido fitoquímicamente por el jengibre ( a ) y ajo ( b ) y NiO estándar ( c )
Los espectros FTIR registrados de NiO biosintetizados a partir de raíces de jengibre y ajo se muestran en la Fig. 5 a, b. Absorción amplia elaborada a 3380 cm −1 corresponden a OH y la amplitud del pico indica un grupo carbonilo con frecuencia de estiramiento de amina (N-H) [50]. La fuerte absorción a 2313 cm −1 indica vibraciones de estiramiento de CO 2 ya sea aéreo o CO 2 dentro de los granos NP. Absorción rápida de CO 2 atmosférico indica una mayor superficie de material [18]. La amplia absorción a 1629 cm −1 corresponden al estiramiento del anillo aromático C =C y picos agudos a 1392 y 1064 cm −1 corresponden a las vibraciones de estiramiento de las aminas alifáticas C – N [48]. Los picos intensos a 978 cm −1 frecuencia de estiramiento de oxígeno metálico confirmado de NiO [44].
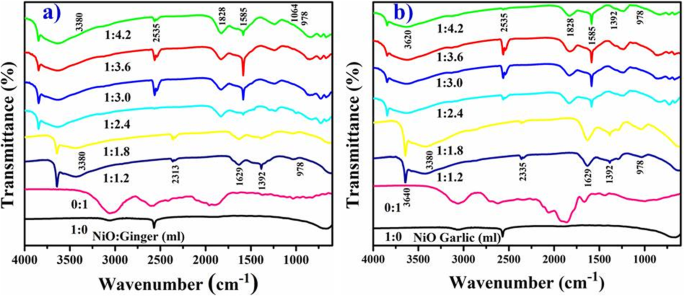
Espectros FTIR con extracto de jengibre a NiO ( a ) y ajo ( b )
Los cambios máximos observados después de la bio-reducción de NiO como 2535–2313, 1828–1629 y 1585–1392 cm −1 indican fitoquímicos, terpenoides, flavonoides, polioles y proteínas que tienen grupos funcionales cetonas, alcoholes, ácido carboxílico y aminas responsables de la quelación y la protección de la biorreducción [42].
La morfología de la superficie y el tamaño de las NiO-NP fitoquímicamente reducidas se determinaron mediante microscopía electrónica de transmisión y exploración de emisión de campo, como se presenta en la Fig. 6a-f. Los NiO-NPs mostraron pleomorfismo con forma cúbica y más esférica (<50 nm) con ligera aglomeración [40]. La aglomeración de NP podría ser evidente por la adherencia del polímero y la interacción magnética entre las partículas [49].
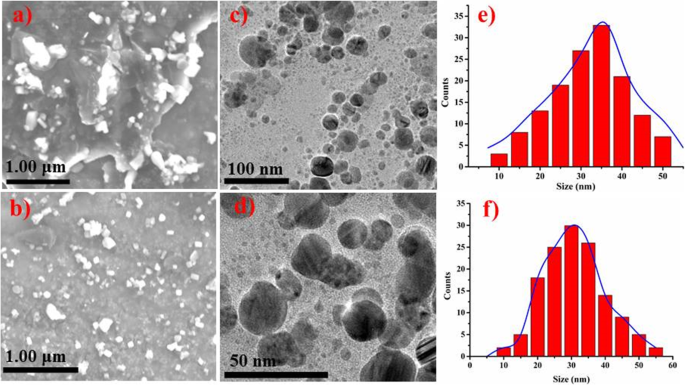
un - f Imagen SEM de NiO reducido fitoquímicamente por jengibre ( a ) y ajo ( b ). Imagen TEM de NiO reducido fitoquímicamente con jengibre ( c ) y ajo ( d ) y distribución del tamaño del NiO reducido fitoquímicamente por el jengibre ( e ) y ajo ( f )
El análisis elemental y otras características de las NiO-NP sintetizadas se describieron mediante espectroscopía de rayos X de dispersión de energía (EDS) que confirmó las fases de NiO puro como se muestra en la Fig. 7a, b. Los espectros de EDS confirmaron tres picos directamente relacionados con la alta pureza del Ni presente en las muestras analizadas entre 1 y 10 kV. Los porcentajes de peso atómico observados a través de los espectros de Ni, O, C y Zn son 54,69, 27,81, 18,06 y - 0,55, respectivamente.
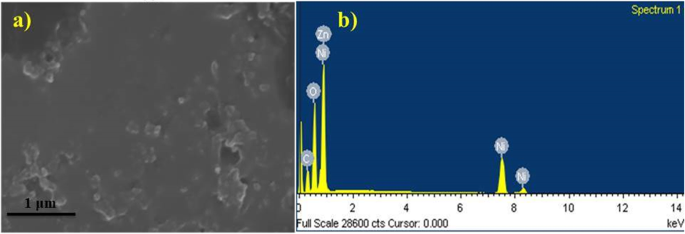
un , b Espectro EDS de NiO-NP sintetizados en verde
XPS muestra C1 s , O1 s y Ni2 p espectros de NiO-NP fitoquímicamente reducidos en la Fig. 8a-d que sugiere la naturaleza química y los estados de enlace de las muestras sintetizadas. Los picos más intensos a 284,8 y 286,2 eV demuestran C1 s espectro (Fig. 8b) correspondiente a C – C y C – OH / C – O – C [21]. Los O1 s El pico a 530,8 eV (Fig. 8c) podría asignarse a grupos hidroxilo de átomos de oxígeno, átomos de oxígeno adyacentes a las vacantes de níquel o átomos de carbono unidos por oxígeno C =O [1, 15, 37]. La contribución ubicada en 532,2 eV se atribuye a los átomos de oxígeno en las moléculas de agua absorbidas (NiOH) [31, 41]. El Ni2 p espectro que contiene Ni2 p 3/2 y Ni2 p 1/2 picos se pueden separar usando la función gaussiana-lorentziana en cinco componentes (Fig. 8d). Los picos más intensos a 872,72 y 855,82 eV pertenecen a Ni2 p 1/2 y Ni2 p 3/2 con picos de satélite correspondientes 879,36 y 861,57 eV, respectivamente [16]. El giro-órbita que se divide entre el Ni (2 p 1/2) y Ni (2 p 3/2) y el nivel básico de NiO-NP es 17.28 eV, lo que se corresponde bien con informes anteriores [33, 34].
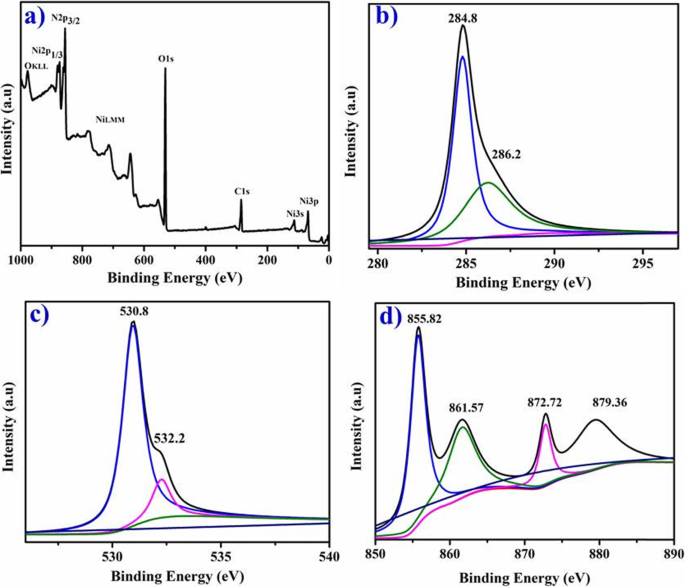
un - d Estudio XPS de partículas reducidas fitoquímicamente ( a ), C1 s orbitales ( b ), O1 s espectros de NiO ( c ) y Ni2 p ( d )
La acción antimicrobiana / bactericida de los extractos de raíz de jengibre y ajo y los NiO-NP verdes / reducidos fitoquímicamente se evaluó utilizando un ensayo de difusión en pozos de agar mediante la medición de la zona de inhibición (mm) como se muestra en la Fig. 9a-dy la Tabla 1. Los resultados muestran una fuerte relación entre la concentración de NP y las zonas de inhibición (mm). Zonas de inhibición significativas (mm) ( P <0.05) se registraron para la muestra 1 (1.2 ml:1), 2 (1.8 ml:1), 3 (2.4 ml:1), 4 (3 ml:1), 5 (3.6 ml:1) y 6 ( 4,2 ml:1) que varían (3–4,9 mm) y (3,05–5,2 mm) a concentraciones bajas y altas NP-NiO reducidas fitoquímicamente por el jengibre (Fig. 9c, d), mientras que (3,15–5,3 mm) y (3,75– 5,9 mm) NP reducidas fitoquímicamente con ajo contra MDR S. aureus (Fig. 9e, f) . Los extractos acuosos de raíz de jengibre mostraron una eficacia cero (Fig. 9a), y las raíces de ajo mostraron zonas de inhibición de 2,65 y 5 mm a concentraciones bajas y altas, respectivamente (Fig. 9b). Todos los resultados se compararon con el control negativo DIW (0 mm) y el control positivo con ciprofloxacina (12,55 mm). En general, los NiO-NP fitoquímicamente reducidos con ajo mostraron una ( P <0.05) acción bactericida mejorada contra MDR S. aureus.
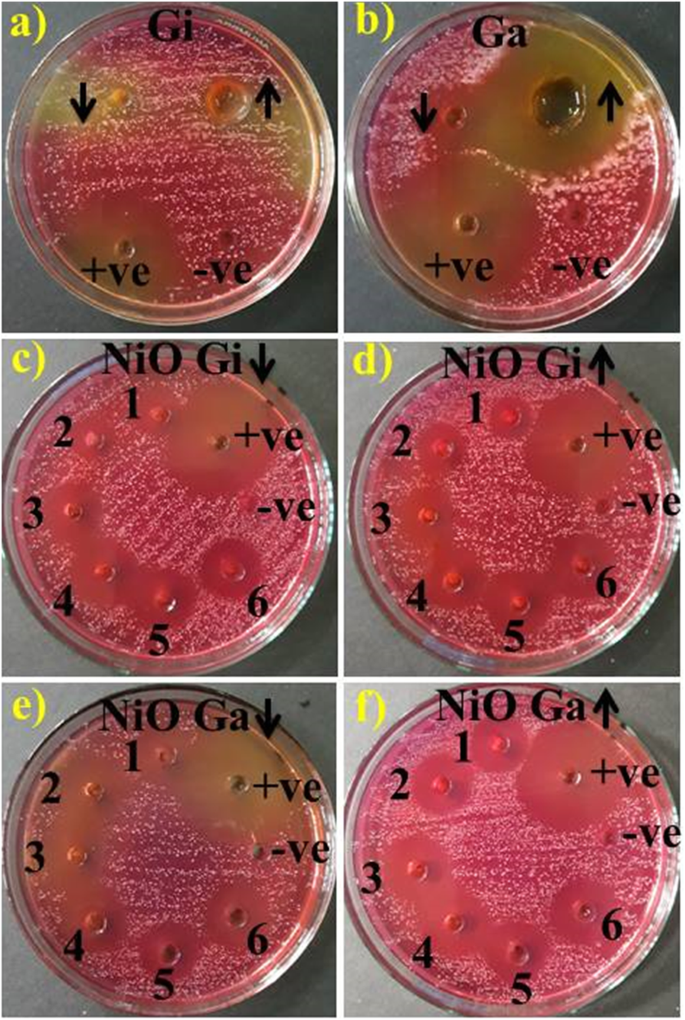
un - f Actividad antimicrobiana in vitro del extracto acuoso de jengibre ( a ), ajo ( b ) y NiO-NPs sintetizados fitoquímicamente por extracto de jengibre en dosis bajas y altas ( c , d ) y ajo ( e , f )
La diferencia en la tolerancia al estrés oxidativo depende de varios factores como el área de superficie, la morfología y el tamaño de partícula del nanomaterial sintetizado que desempeña un papel inferencial en el potencial de acción antibacteriano [29, 36]. Una interacción electrostática entre cepas bacterianas y materiales a nanoescala da como resultado la generación de especies reactivas de oxígeno que se encuentran responsables de la muerte celular bacteriana [2, 3, 4, 5, 22]. Se encontraron dos reacciones posibles para la reacción de nanomateriales con cepas bacterianas, incluida una fuerte interacción de los cationes Ni 2+ con partes cargadas negativamente de la célula bacteriana que dan como resultado el colapso, mientras que la segunda reacción da como resultado la excitación electrónica de la cenefa a la banda de conducción tras la irradiación de la superficie de NiO con luz. Más reacción electrónica con O 2 genera O - 2 radicales que dan como resultado H 2 O 2 producción. La producción de · OH se produjo tras la reacción de h + con agua. Por lo tanto, O - resultante 2 Las especies · y · OH desempeñaron un papel importante en la degradación de la molécula de lípidos o proteínas presentes en la superficie externa de las células bacterianas [39].
Actividad catalítica
Figura 10 a – e que demuestra la reducción catalítica de MB en presencia de extractos de raíces y NiO-NP verdes / reducidas fitoquímicamente a temperatura ambiente. La Figura 10a muestra el potencial catalítico de NiO-NP sintetizadas por la ruta convencional, mientras que (Fig. 10b, c) representa el potencial catalítico de extractos acuosos de jengibre y raíz de ajo. La capacidad catalítica de las NiO-NP fitoquímicamente reducidas se representa en la Fig. 10d, e. Es obvio que el NiO y los extractos de raíces de plantas no son un nanocatalizador eficiente, ya que consumían 15, 21 y 38 minutos para la reducción del azul de metileno (Fig. 10a-c). Los NP reducidos fitoquímicamente con jengibre mostraron una rápida degradación ( λ máx =8 min) con conversión eficiente de MB a azul de leucometileno (Fig. 10d). Los NiO-NP mediados por ajo mostraron un patrón similar de reducción del tinte del 100% en 5 minutos (Fig. 10e).
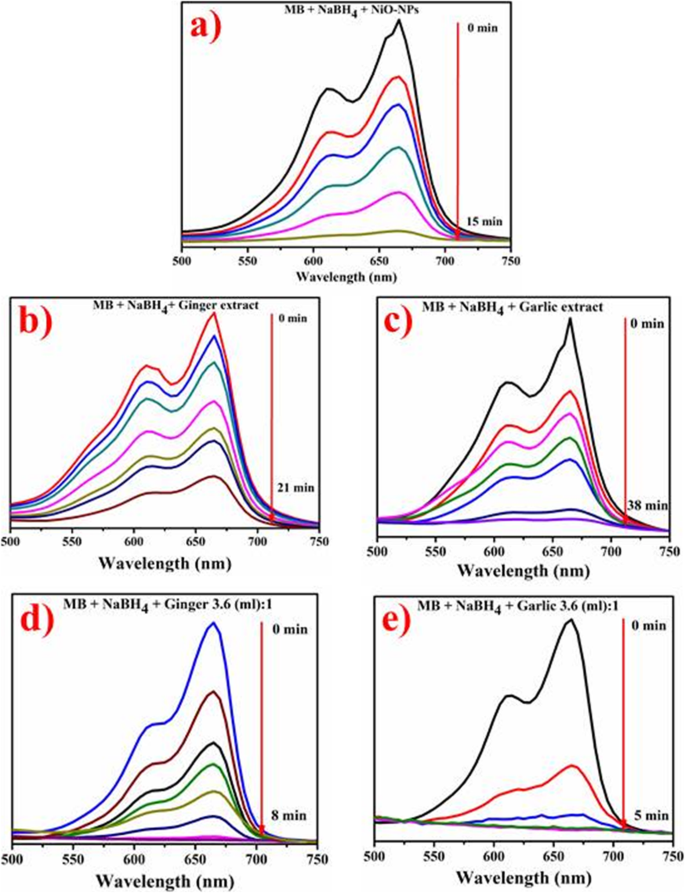
un - e Actividad catalítica de NiO ( a ), extracto de jengibre ( b ), extracto de ajo ( c ), NiO reducido fitoquímicamente por jengibre ( d ) y NPs reducidos en ajo ( e )
Los NP verdes / fitoquímicamente reducidos realizan una degradación catalítica significativa del colorante mediante la transferencia de electrones de especies donantes (BH 4 ) al aceptor (MB) y estabilizar el sistema reduciendo la energía de activación [27]. Los datos revelaron que las NP verdes son un nanocatalizador eficiente en comparación con las NP convencionales y el extracto individual.
Conclusión
Los NP-NiO con extractos de raíz de jengibre y ajo sirvieron como un excelente agente bactericida y catalítico. La incorporación de extracto de raíz que tiene grupos fitoquímicos dio como resultado una síntesis exitosa de NiO-NP revelada por FTIR. Los picos XRD confirmaron una red hexagonal de NiO y cúbica centrada en la cara (fcc) y la SEM confirmó el pleomorfismo con morfología cúbica y más esférica de NP que tenían un tamaño medio de 16–52 (dopaje con jengibre) y 11–59 nm (dopaje con ajo). Sin embargo, el análisis elemental reveló la naturaleza química y los estados de unión analizados por EDS y XPS y presentó el porcentaje real de níquel y oxígeno, mientras que el análisis UV verificó la diferencia de picos de absorción en el rango de 350 nm e introdujo un desplazamiento azul en una mayor cantidad de dopantes. Se encontró que el NiO reducido fitoquímicamente con ajo a alta concentración era más potente en comparación con los NP reducidos en jengibre contra MDR S. aureus así como MB reducido de manera eficiente. Por lo tanto, el NiO verde / reducido fitoquímicamente de los extractos de raíz de ajo puede adoptarse en la medicina avanzada como sustituto de la resistencia a los antibióticos y en las industrias textiles como agente catalítico sin peligro para el medio ambiente.
Disponibilidad de datos y materiales
Todos los datos están completamente disponibles sin restricciones.
Abreviaturas
- EDS:
-
Espectroscopia de rayos X de dispersión de energía
- fcc:
-
Cúbico centrado en la cara
- FTIR:
-
Espectroscopía infrarroja por transformada de Fourier
- G + ve:
-
Gram positivo
- G –ve:
-
Gram negativo
- JCPDS:
-
Comité conjunto sobre estándares de difracción de polvo
- MB:
-
Azul de metileno
- Ni:
-
Níquel
- NiO:
-
Óxido de níquel
- nm:
-
Nanómetro
- NP:
-
Nanopartículas
- SEM:
-
Microscopía electrónica de barrido
- TEM:
-
Microscopía electrónica de transmisión
- UV-Vis:
-
Espectroscopia visible ultravioleta
- XPS:
-
Espectroscopia de fotoelectrones de rayos X
- XRD:
-
Difracción de rayos X
Nanomateriales
- Nanopartículas de FePO4 biocompatibles:administración de fármacos, estabilización de ARN y actividad funcional
- Síntesis biogénica, caracterización y evaluación del potencial antibacteriano de nanopartículas de óxido de cobre contra Escherichia coli
- Preparación y actividad de hidrogenación catalítica mejorada de nanopartículas de Sb / Palygorskita (PAL)
- Nanopartículas como bomba de eflujo e inhibidor de biopelícula para rejuvenecer el efecto bactericida de los antibióticos convencionales
- Síntesis verde en un recipiente de microesferas de SnO2 decoradas con Ag:un catalizador eficiente y reutilizable para la reducción de 4-nitrofenol
- La posible toxicidad hepática, cerebral y embrionaria de las nanopartículas de dióxido de titanio en ratones
- Poliglicerol hiperramificado modificado como dispersante para el control del tamaño y la estabilización de nanopartículas de oro en hidrocarburos
- Determinación de la actividad catalítica de nanopartículas de TiO2 dopado con metal de transición mediante análisis espectroscópico de superficie
- Síntesis y rendimiento in vitro de nanopartículas de hierro-platino recubiertas de polipirrol para terapia fototérmica e imágenes fotoacústicas
- Aptitud ecológica en la síntesis y estabilización de nanopartículas de cobre:actividades catalíticas, antibacterianas, citotóxicas y antioxidantes
- Un escrutinio comparativo in vivo de nanopartículas de óxido de zinc y cobre biosintetizadas por vías de administración intraperitoneal e intravenosa en ratas



