Caracterización estructural de una cadena autoensamblada como la nanoestructura de capa de Fe-FeOx Core
Resumen
Uno de los grandes desafíos de estudiar las nanoestructuras de hierro núcleo-capa es conocer la naturaleza de la capa de óxido, es decir, si es γ-Fe 2 O 3 (Maghemita), Fe 3 O 4 (Magnetita), α -Fe 2 O 3 (Hematita) o FeO (wustita). Al conocer la naturaleza de la capa de óxido de hierro con núcleo de hierro de valencia cero, se puede determinar el comportamiento químico o físico de las nanoestructuras núcleo-capa. Se prepararon nanocadenas núcleo-capa de Fe (NC) mediante la reducción de Fe 3+ iones mediante borohidruro de sodio en solución acuosa en atmósfera ambiente, y los Fe NC se envejecieron adicionalmente en agua hasta 240 min. Se utilizó XRD para estudiar la estructura de Fe NC. TEM realizó un análisis adicional de la naturaleza núcleo-capa de Fe NC, los resultados mostraron un aumento en el espesor de la capa de óxido (de 2.5, 4, 6 a 10 nm) a medida que aumenta el tiempo de envejecimiento del agua (de 0 min, 120 min, 240 min a 360 min). Se empleó la espectroscopía Raman para estudiar la naturaleza de óxido de Fe NC. Para confirmar aún más la fase de magnetita en Fe NC, la espectroscopia de Mössbauer se realizó en Fe NCs-0 y Fe NCs-6. El resultado muestra la presencia de magnetita en la muestra antes del envejecimiento en agua, y la muestra después del envejecimiento prolongado contiene la fase de hematita pura . Muestra que la oxidación prolongada del agua transforma la estructura de la capa de Fe NC de una mezcla de hematita y magnetita en una capa de hematita pura. Las propiedades magnéticas de los Fe NC se midieron mediante VSM a 320 K. Debido a los valores de magnetización de alta saturación (Ms), los Fe NC podrían usarse como r 2 contrasta agentes para imágenes de resonancia magnética (MRI) en un futuro próximo.
Introducción
Los nanocables magnéticos (NW), ya sea sintetizados a través de plantillas o métodos de ensamblaje, tienen grandes momentos magnéticos y anisotropía de forma, como se muestra en la Fig. 1. Trabajos anteriores afirman que las estructuras en forma de cadena con relaciones de aspecto altas son más eficientes en aplicaciones biomédicas, especialmente para la separación magnética. hipertermia magnética (HM) y resonancia magnética que las nanopartículas [1, 2]. Para MH 1-D, los NW magnéticos pueden proporcionar áreas reactivas de fricción más grandes que las nanopartículas de dimensión cero (0-D). Esto permite que los NW magnéticos unidimensionales (1-D) tengan una mejor eficiencia de calentamiento, lo que reduce el tiempo de tratamiento de los pacientes con cáncer. Park y col. [3] informó que los nano gusanos 1-D muestran una capacidad superior de direccionamiento tumoral in vivo que las nanoesferas con un diámetro similar. Jeotikanta y col. preparado [4] Fe 3 O 4 nanovarillas (NR) por hidrólisis de FeCl 3 solución acuosa y funcionalizado con polietilenimina como medio de contraste para resonancia magnética. Descubrieron que el r 2 La relajación de los NR es mayor que la de las nanopartículas que utilizan el mismo volumen de material. Los NW de óxidos de hierro superan a los NP similares en las pruebas de R 2 relajaciones [5]. El R calculado 2 el valor para NW es 116 mM −1 s −1 que es más alto que los NP (70 mM −1 s −1 ). El autor concluye que la naturaleza alargada y la magnetización de saturación más alta de los NW dan como resultado un mejor contraste de RM [5].
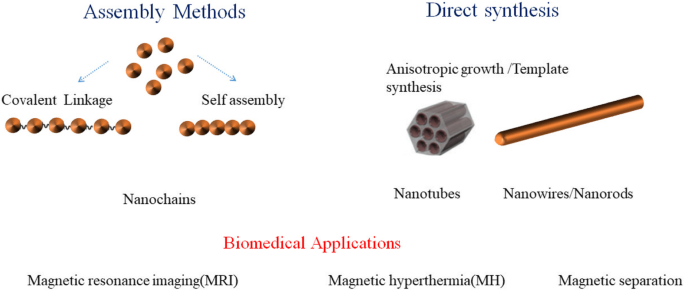
Nanocables magnéticos anisotrópicos de gran forma preparados mediante métodos de síntesis o ensamblaje directos y sus aplicaciones biomédicas
A pesar del hecho de que las propiedades estructurales generales de las nanoestructuras de hierro núcleo-caparazón están bien estudiadas, la estructura exacta y la fase de las capas de óxido son difíciles de determinar. La composición y fase de la capa de óxido formada en un núcleo de hierro depende de la distancia desde el núcleo interno de Fe a las capas externas de óxido, es decir, generalmente una progresión desde cero valencia Fe → FeO → Fe 3 O 4 → Fe 2 O 3 ocurre [6]. Aunque, para la oxidación a temperatura ambiente, se formó una capa de óxido muy fina que era difícil de diferenciar la variación espacial de las cáscaras de óxido. Para la oxidación a temperatura ambiente usando EELS en caracterizaciones TEM, algunos autores afirman que la capa de óxido de hierro está hecha de γ -Fe 2 O 3 o Fe 3 O 4 [7, 8] o que FeO se formó inicialmente y después de calentar la capa de FeO se transformó en γ -Fe 2 O 3 o Fe 3 O 4 concha [9]. Sin embargo γ -Fe 2 O 3 y Fe 3 O 4 son fases metaestables de hierro y podrían transformarse en α -Fe 2 O 3 después de oxidación a alta temperatura hasta 500 ° C [10]. Además, el procedimiento de oxidación del núcleo de hierro de valencia cero está fuertemente influenciado por la solución acuosa oxigenada y la oxidación ocurre en un H 2 Interfaz de O y óxido [11]. A medida que se produce la transferencia de iones de hierro desde el núcleo de hierro de valencia cero a la capa de óxido, se produce la formación de una nueva fase de óxido. También se encontró una oxidación similar en [12] con la presencia de oxígeno.
El propósito de esta investigación fue estudiar la estructura de Fe NC recién preparados sintetizados por la reducción de la solución de cloruro de hierro (III) mediante la adición de una solución de borohidruro de sodio. El estudio muestra que el grosor de la cáscara y el diámetro del núcleo magnético de Fe NC son sintonizables. Se utilizaron XRD, FE-SEM y TEM para estudiar la estructura y la naturaleza núcleo-capa de Fe-NC. Además, se empleó espectroscopia Raman con láser verde (longitud de onda de excitación 532 nm) y láser He-Ne (longitud de onda de excitación 633 nm) para estudiar la naturaleza de óxido de Fe-NC. Los resultados fueron confirmados por espectroscopía de Mössbauer en FeNCs-0 y FeNCs-6 a 320 K. Con el fin de estudiar el efecto de magnetización en Fe-NC, para futuras posibles aplicaciones biomédicas , Las propiedades magnéticas de Fe NCs-0, Fe NCs-2, Fe NCs-4 y Fe NCs-6 se midieron mediante VSM a temperatura ambiente. Después de examinar los valores de magnetización de saturación de Fe NC, posiblemente pueda sugerir que Fe NC podría usarse como r 2 agentes de contraste para imágenes por resonancia magnética (MRI) en un futuro próximo.
Métodos
Productos químicos
Hexahidrato de cloruro férrico (FeCl 3 .6H 2 O) (99% de pureza) y borohidruro de sodio (NaBH 4 ) (98% puro) se adquirieron de National Medicines Corporation Ltd. (China). Se compró gas argón de alta pureza (99,9%) a la empresa de gas Hubei Minghui (China).
Síntesis de NC de Fe Core-Shell
Para la síntesis de CN de Fe de núcleo-capa, 3 g de cloruro férrico hexahidratado (FeCl 3 .6H 2 O) se disolvió en 1000 ml de agua desionizada (DI) para formar una solución de cloruro de hierro (III). Borohidruro de sodio (NaBH 4 ) se formó la solución agregando 6 g de NaBH 4 añadido a 400 ml de agua desionizada [13]. La adición de NaBH 4 La solución se hizo a razón de 1,5 mL / s en solución férrica sin agitar y se dejó la solución durante 0 min, 120 min, 240 min y 360 min. Se formaron precipitados negros, se recogieron de la solución y se lavaron con agua desionizada y etanol y se secaron bajo gas argón (Ar) para caracterizaciones. Los Fe NC se formaron mediante la reducción de la solución de cloruro de hierro (III) mediante la adición de una solución de borohidruro de sodio, que se realiza mediante la siguiente reacción [13],
$$ 3B {H} _4 ^ {-} + 3 {H} _2O + Fe {\ left ({H} _2O \ right)} _ 6 ^ 3 =Fe + 3B {(OH)} _ 3 + 1/2 {H} _2 $$Mediante la adición de NaBH 4 solución en la solución férrica se forman núcleos de hierro bajo H 2 proteccion. Mediante el autoensamblaje de núcleos de hierro debido a la alta interacción magnética entre ellos, se formaron nanoestructuras en forma de cadena. La Figura 2 muestra la síntesis y formación de NC de Fe de núcleo-capa preparadas mediante reacción de reducción.
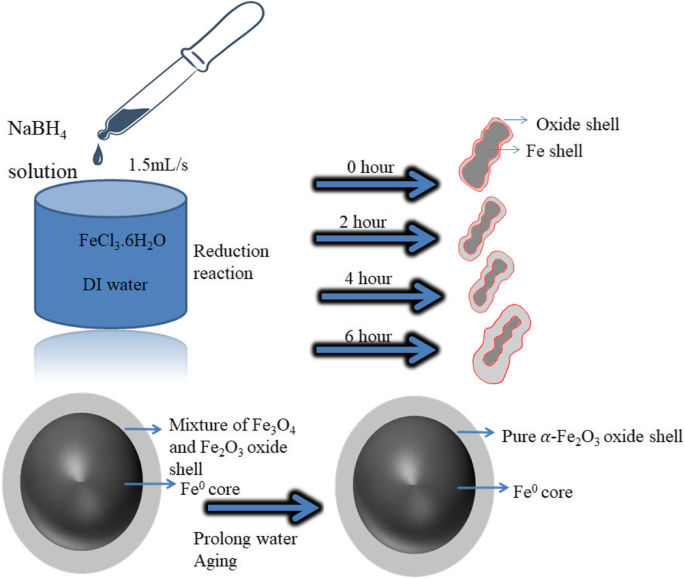
Ilustración esquemática de síntesis y formación de NC de Fe de núcleo-capa
Caracterizaciones
Los NW de Fe núcleo-capa se examinaron mediante microscopía electrónica de barrido por emisión de campo (FE-SEM, NOVA 400 Nano) con espectroscopia de rayos X de dispersión de energía (EDX, Le350 PentaFETx-3). Para las observaciones de FE-SEM, los Fe NW se pulverizaron con una fina capa de oro durante 100 segundos. La difracción de rayos X (XRD, X’Pert PRO MRD, PANalytical, Países Bajos) se realizó con Cu-K α radiación, espectrómetro Raman (laboratorio RAM HR JY-Evaluation) con una longitud de onda de excitación de 532 nm (con potencia de 60 mW y potencia de láser de 6 mW) y con láser He-Ne (con láser de 0,1, 0,6, 1 y 3 mW energía). La microscopía electrónica de transmisión (TEM) se llevó a cabo en un microscopio electrónico Tecnai G2 F30 S-TWIN que funcionaba a 300 kV. Para las observaciones de TEM, las muestras se prepararon dispersando los polvos en etanol absoluto por ultrasonidos. Las mediciones magnéticas se realizaron utilizando un magnetómetro de muestra vibrante (VSM, Lake Shore 7307). Las curvas de magnetización M / Ms Vs H (KOe) se midieron bajo un campo magnético de hasta 20 KOe. La espectroscopia de Mössbauer se realizó utilizando una fuente de rayos de 57Co /:Rhc (14,4 KeV) montada en un impulsor electromagnético con señales de velocidad triangular a 320 K. Los espectros eran mínimos cuadrados ajustados para obtener los parámetros hiperfinos.
Resultados y discusión
FE-SEM
La Figura 3a-d muestra imágenes FESEM de Fe NCs-0, Fe NCs-2, Fe NCs-4 y Fe NCs-6 de núcleo-capa recién preparadas, a través de la reacción de reducción de tricloruro de hierro por borohidruro de sodio a 0, 120 , 240 y 360 min. Se puede ver en la Fig. 3a-d que la nanoestructura de Fe obtenida aparece como una cadena de nanopartículas de Fe unidas entre sí. Además, cada una de las nanopartículas de Fe está separada de la otra por una fina interfaz de óxido, que es una característica específica del método de síntesis aplicado utilizado en este estudio. La Figura 3e muestra la composición de Fe NCs-2 medida usando EDX. El pico de hierro (Fe) con pico de oxígeno (O) aparece como hombro al pico de Fe que se observa, además del pico de carbono (C) se observó debido a la cinta de carbono que se utilizó como sustrato durante la caracterización de FESEM y aparecen picos de oro (Au) de la pulverización catódica de la muestra con oro para fines de conducción. El recuadro de la Fig. 3e muestra el porcentaje atómico de Fe y O en Fe NCs-2 (At% =O, 22,35%; Fe, 77,65%).

un - e Imagen FE-SEM de ( a ) FeNCs – 0, ( b ) FeNCs – 2, ( c ) FeNCs – 4, ( d ) FeNCs – 6, ( e ) Patrón EDX de Fe NCs – 2, la tabla insertada muestra el porcentaje atómico y en peso del elemento hierro y oxígeno
XRD
Las figuras 4a-d muestran patrones de rayos X de Fe NCs-0, Fe NCs-2, Fe NCs-4 y Fe NCs-6. El pico dominante se encuentra en 2 θ =44,9 ° se puede atribuir inequívocamente a bcc Fe según el archivo JCDP n. ° 6-696 con a =0.2866A ° . La DRX es la técnica más utilizada para la confirmación de la naturaleza amorfa del óxido de hierro [14, 15]. Una línea plana muestra la falta de periodicidad en la red cristalina. Por tanto, la ausencia de picos de difracción de Braggs podría ser el marcador de identificación de la naturaleza amorfa del Fe 2 O 3 [15] y su distinción de los polimorfos (hametita y maghemita) Fe 2 O 3 . Además, a partir de la figura XRD se vio que el pico característico de bcc Fe a 44,9 ° tiene un cambio muy leve hacia un ángulo más bajo con el aumento del contenido de oxígeno en Fe NC. Este fenómeno podría observarse debido a la diferencia en los radios iónicos entre el elemento principal (Fe) y el ion dopante (O) [16], lo que indica que los átomos de O se han producido con éxito en la superficie de Fe NC. Como el pico de óxido no aparece en la difracción de rayos X, los resultados fueron confirmados por TEM, espectroscopía Raman y espectroscopía Mössbauer.
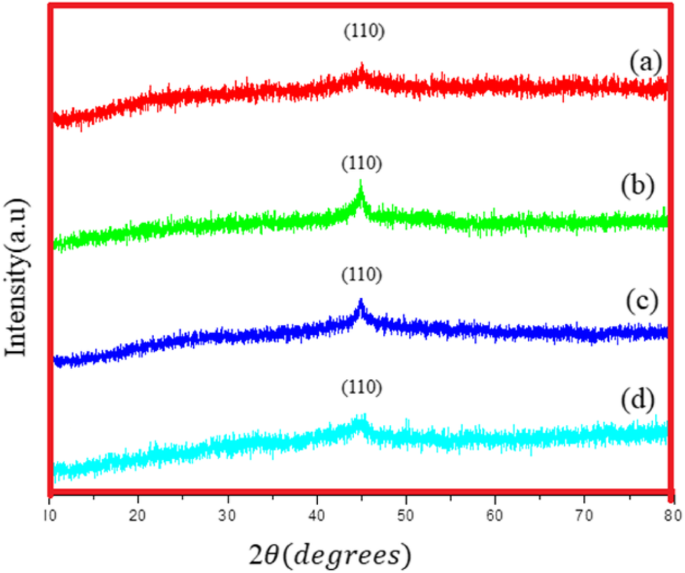
Patrón XRD de (a) Fe NCs-0, (b) Fe NCs-2, (c) Fe NCs-4 y (d) Fe NCs-6
TEM
El resultado fue confirmado adicionalmente por TEM. La Figura 5a-d muestra el TEM de Fe NCs-0, Fe NCs-2, Fe NCs-4, Fe NCs-6. Sorprendentemente, se vio claramente el contraste entre el centro oscuro y el borde gris, lo que sugiere la estructura núcleo-caparazón de los NC. Como está claro en la Fig.5a, la capa de Fe NCs-0 era de aproximadamente 2,5 nm, a medida que la oxidación en agua aumenta de 0 a 120 min, la capa aumentaba de espesor a 4 nm (Fig. 5b), lo que aumentaba aún más el tiempo de reacción. hasta 240 min el espesor de óxido de la capa se incrementó a 6 nm (Fig. 5c), finalmente el envejecimiento en agua durante 360 min la capa de óxido se incrementó hasta 10 nm (Fig. 5 d). Como se desprende de la observación de TEM, hay un aumento gradual en el grosor de la capa de 2,5, 4, 6 a 10 nm. Se podría concluir que un mayor tiempo de envejecimiento con agua da como resultado una capa de óxido más gruesa debido a la reacción del hierro de valencia cero con O 2 / H 2 O en la solución. El aumento en el espesor de la cáscara también fue observado por Xue et al. mediante la preparación del nanocompuesto núcleo-capa, sintetizado mediante el método de reflujo fácil [17, 18].
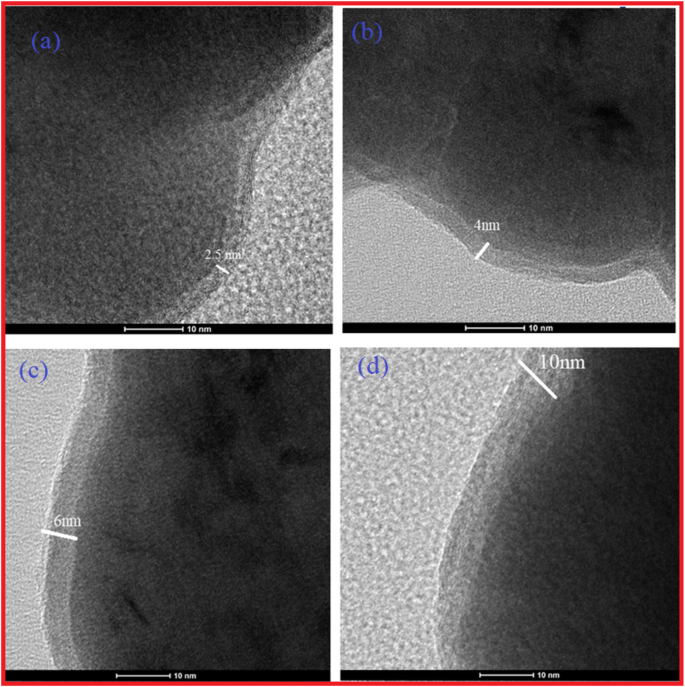
Imagen TEM de a Fe NCs-0, b Fe NCs-2, c Fe NCs-4 y d Fe NCs- (6) que muestra la naturaleza núcleo-capa de Fe NC con un aumento en el espesor del óxido de 2,5 nm, 4 nm, 6 nm y 10 nm
Espectroscopia Raman
La espectroscopia Raman es una técnica analítica que se ha utilizado para estudiar la estructura de los óxidos de hierro durante muchos años [19,20,21,22,23]. Proporciona una evaluación clara de la fase de óxido y puede medir la cristalinidad de la muestra en estudio observando los modos de fonón. La espectroscopía vibracional Raman es una gran herramienta para caracterizar los polvos o películas de óxido, ya que estudios previos muestran que los polimorfos de óxido de hierro (hematita, maghemita y magnetita) muestran distintas señales Raman [20, 24, 25]. La Figura 6 muestra los espectros Raman recogidos de Fe NC a una potencia de láser de 60 mW, medidos con láser verde (532 nm). Los picos aparecieron a 217 cm −1 (A 1g ), 275 cm −1 (E g ) y 386 cm −1 (E g ), y se observó una amplia joroba entre 1200 y 1300 cm −1 , corresponde a la fase de hematites con picos desplazados hacia números de onda más bajos (como los datos anteriores recogidos en la Tabla 1). Este cambio de pico podría corresponder a la oxidación por láser; la alta temperatura inducida por la potencia del láser enfocado podría resultar en un cambio de fase del material que también es observado por el grupo de estudios de Mendili et al. [29,30,31]. Para confirmar aún más la naturaleza de óxido de Fe NC, los espectros Raman se realizaron a potencias de láser más bajas (6 mW) utilizando láser verde (532 nm) y láser He-Ne (633 nm). La Figura 7 a muestra picos (láser verde) a una longitud de onda de 214 cm −1 (A 1g ), 278 cm −1 (E g ), 394 cm −1 (E g ), 490 cm −1 (A 1g ), 597 cm −1 (E g ) y 1290 cm −1 . Como se desprende de los datos de Raman recopilados en la Tabla 1, estos picos podrían corresponder a picos de hematita con el número de onda desplazado hacia los números de onda inferiores. Por tanto, se utilizó el láser He-Ne (Fig. 7b) con una potencia de láser de 6 mW. Los picos en el número de onda 224 cm −1 (A 1g ), 287 cm −1 (E g ) y 484 cm −1 (A 1g ) y 1306 cm −1 corresponde a la fase de hematita pura [10, 24, 32]. Al conocer la relación \ ({P} _ {\ mathrm {disperso}} \ propto \ frac {I_0} {\ lambda ^ 4} \) (donde P dispersos es el tiempo de dispersión Raman y λ es la longitud de onda del láser), el tiempo de exploración del láser He-Ne es más largo que el del láser verde, lo que da mejores resultados para los NC de Fe de núcleo y capa sintetizados mediante la reacción de reducción. Como se ve claramente en la Fig. 7b, apareció un pico débil a 660 cm −1 para Fe NCs-0 y Fe NCs-2. Este pico fue visto por otros grupos en los espectros Raman de hematita y podría ser la presencia de contaminación de magnetita [24, 33]. Para confirmar aún más la fase de magnetita en Fe NC, los espectros Raman se recogieron con potencias de láser más bajas (0,1 mW, 0,6 mW, 1 mW y 2 mW) utilizando láser He-Ne (los resultados se dan en el archivo adicional 1). No se observaron señales Raman, solo se observó una línea plana con potencias láser bajas. Los espectros Raman se recogieron a 3 mW usando láser He-Ne como se muestra en la Fig. 8. Un pico de magnetita fuerte aparece claramente a 670 cm −1 (A 1g ) para Fe NCs-0 con picos de hematita a 224 cm −1 (A 1g ), 287 cm −1 (E g ) 406 cm −1 (E g ), 500 cm −1 (A 1g ) y 1310 cm −1 (E g ) números de onda. El pico de magnetita se desplaza hacia un número de onda más bajo con intensidades más bajas para Fe NCs-2 y desaparece para Fe NCs-4 y Fe NCs-6. A partir de la espectroscopia Raman, se podría suponer que la capa de Fe NCs-4 y Fe NCs-6 corresponden a la fase de hematita pura.
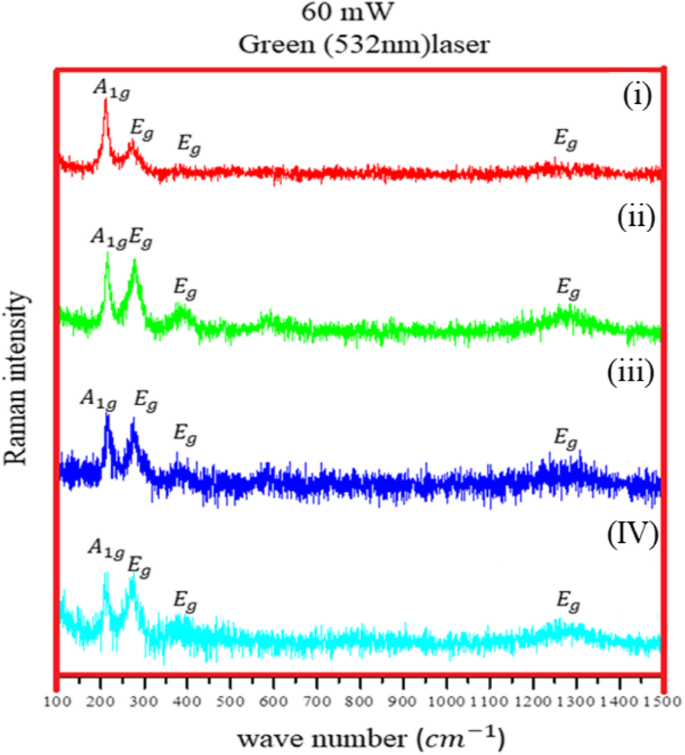
Espectros Raman de (i) FeNCs-0, (ii) FeNCs-2, (iii) FeNCs-4, (IV) FeNCs-6 a una potencia de láser de 60 mW con láser verde
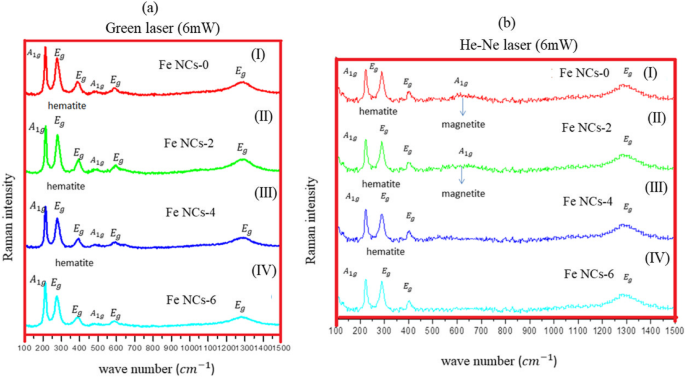
Espectros Raman de a Fe NCs-0 (I), Fe NCs-2 (II), Fe NCs-4 (III) y Fe NCs-6 (IV) recogidos a una potencia de láser de 6 mW con láser verde y b Fe NCs-0 (I), Fe NCs-2 (II), Fe NCs-4 (III) y Fe NCs-6 (IV) recogidos a una potencia de láser de 6 mW con láser He-Ne
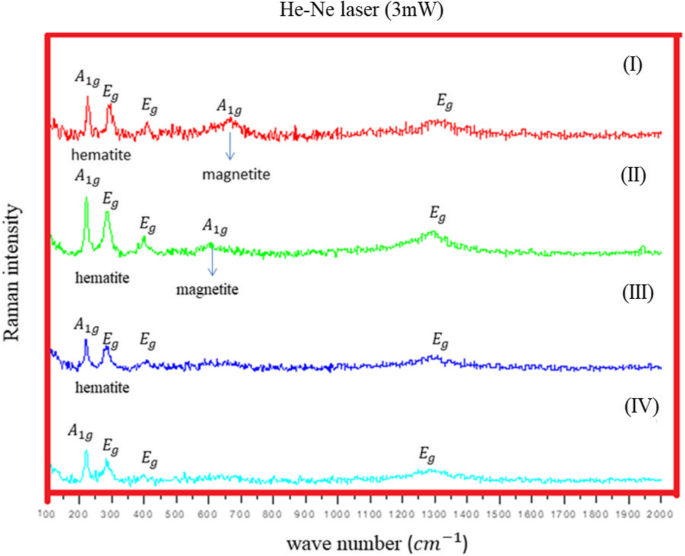
Espectros Raman de Fe NCs-0 (I), Fe NCs-2 (II), Fe NCs-4 (III), Fe NCs-6 (IV) a una potencia de láser de 3 mW con láser He-Ne
Mössbauer Spectra
Para confirmar la fase de magnetita en Fe NC, se realizó la espectroscopia de Mössbauer en Fe NCs-0 y Fe NCs-6. Los espectros de Mössbauer para Fe NCs-0 se obtienen a 320 K y se muestran en la Fig. 9. Los espectros de Mössbauer para Fe NCs-6 se obtienen a 320 K y se muestran en la Fig. 10. Se observan espectros de seis líneas bien resueltos en ambos espectros. Los valores de los cambios de isómeros ( δ ), división de cuadrupolo ( Q ), campo hiperfino ( H ), los anchos de línea y la población del sitio se deducen de los datos de Mössbauer. Los mejores ajustes a los datos experimentales se obtuvieron con un doblete cuadrupolo y cuatro sextetos Zeeman. El cambio de isómero proporciona información sobre la distribución de carga de electrones. Un doblete con cambios de isómeros ( δ ) 0,24 mm / sy división de cuadrupolo ( Q ) 0,94 mm / s, en Fe NCs-0 y en Fe NCs-6 con δ 0,21 mm / sy Q 1,11 mm / s atribuido a Fe superparamgnético +3 estado, también visto por otros investigadores mientras estudiaban Fe 2 O 3 nanopartículas [34,35,36,37]. Los sextetos especifican estados de espín magnético en Fe NC. El δ los valores de 0,7 a 1,4 mm / s se atribuyen a Fe +2 y valores de 0,1 a 0,6 mm / s que indican hierro en Fe +3 estado [38,39,40,41]. δ Los valores dados en la Tabla 2 para el sexteto 2 son 0.10 mm / sy para Q es - 0.04 mm / s, lo que muestra que el estado de valencia del hierro es +3. También se observan valores similares por Joos et al. [42] para Fe 3 O 4 nanopartículas; atribuyeron estos valores a Fe tetraédrico +3 . δ los valores de Fe NCs-6 dados en la Tabla 3 para los sextetos 3 y 4 son 0.15 mm / sy 0.20 mm / s muestran Fe +3 en Fe 2 O 3 . Xie y col. [43] asignó valores similares para Fe 2 más grande O 3 nanopartículas. Se podría deducir de los datos de Mössbauer que existe una pequeña contaminación de magnetita que está presente en Fe NCs-0 y Fe NCs-6 y corresponde a la capa de hematita pura. Korecki y Gradmann [44] hicieron espectroscopía de Mössbauer en películas de Fe (110), los valores de desplazamiento de isómero obtenidos son 0.02 mm / s, 0.04 mm / sy 0.07 mm / s. Estos valores concordaron bien con los valores de bcc Fe dados en la Tabla 2 y la Tabla 3 para Fe NCs-0 y Fe NCs-6. Se espera que la concentración de Fe en las NC de Fe disminuya a medida que la capa de óxido aumenta de 2,5 a 10 nm. La población de sitios de Fe disminuye y la población de sitios de hematites aumenta significativamente en Fe NCs-6. La división del cuadrupolo y los anchos de línea también cambian con el aumento en el grosor de la capa de Fe NCs-0 a Fe NCs-6.
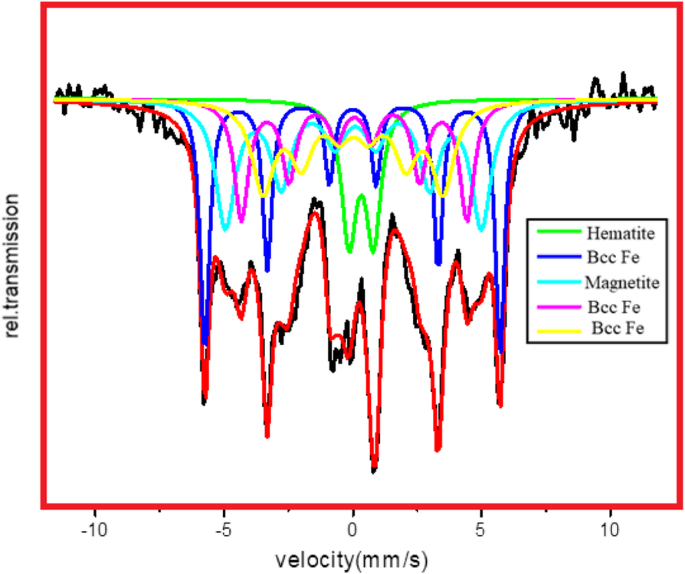
Espectros de Mössbauer de Fe NCs-0 a 320 K
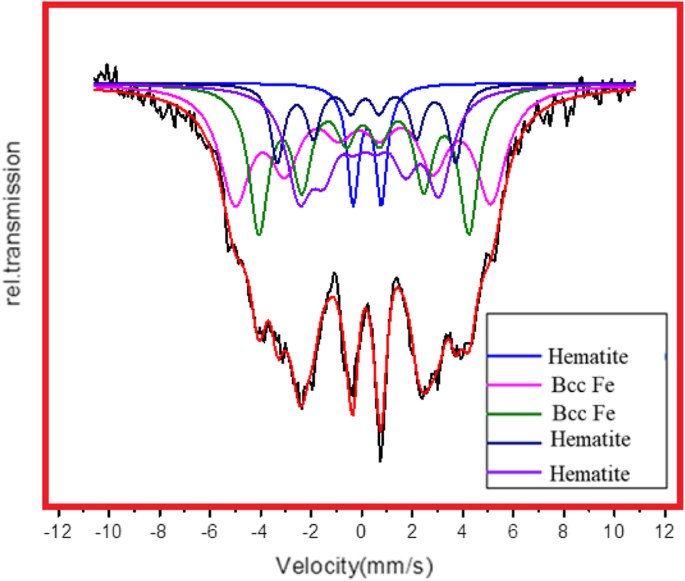
Espectros de Mössbauer de Fe NCs-6 a 320 K
La ilustración esquemática (Esquema 1) muestra el mecanismo para la formación de NC de Fe de núcleo-capa explicado por O 2 vía de activación por oxidación de Fe NC en agua. El esquema 1a muestra que cuando se expuso Fe de valencia cero a H 2 O y O 2 la capa de óxido de hierro se produjo en la superficie de Fe NC. A medida que aumenta el tiempo de reacción en agua de 0 a 360 min, aumenta el crecimiento de la capa de óxido y disminuye el núcleo de Fe. La oxidación del núcleo de Fe ocurre debido a la transferencia de electrones desde el núcleo de Fe a la capa de óxido de hierro a través de la banda de conducción. La transferencia de electrones se produce debido al efecto de la función de trabajo. Como la función de trabajo del Fe (4,5 eV) es menor que la magnetita (5,52 eV) y la hematita (5,6 eV), la transferencia de electrones se produce para reducir las energías, por lo que se ajustó la posición del nivel de Fermi [45, 46]. La oxidación de Fe cero valente a Fe +2 iones (iones ferrosos) se siguió con la transferencia de 2 electrones desde el núcleo de Fe NC al gas oxígeno en la solución para producir peróxido de hidrógeno (Esquema 1b) [47].
$$ {Fe} ^ 0 + {O} _2 + 2 {H} ^ {+} \ to {Fe} ^ {2 +} + {H} _2 {O} _2 $$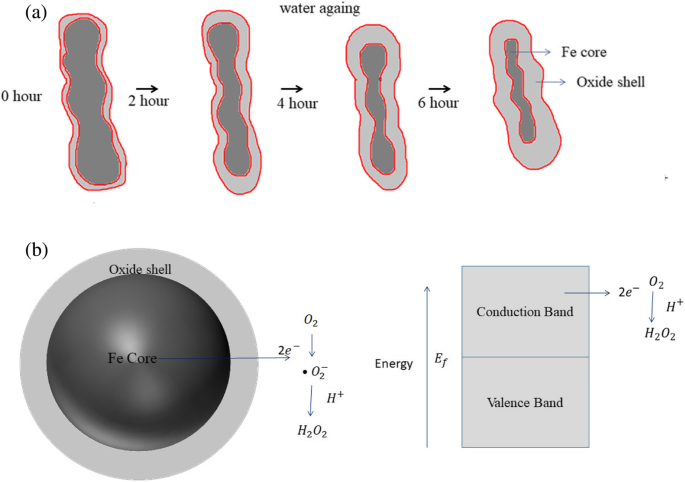
un Formación de Fe NC preparadas mediante 120, 240 y 360 min de envejecimiento en agua, b mecanismo de O 2 ruta de activación sobre los NC de Fe de núcleo-shell
Además, H 2 O 2 reacciona con iones ferrosos para producir radicales hidroxilo e iones férricos [47].
$$ {Fe} ^ {2 +} + {H} _2 {O} _2 \ to {Fe} ^ {3 +} + {OH} ^ {-} + \ bullet \ kern0.5em OH $$La tasa de transferencia de electrones podría verse afectada por el aumento del espesor de la capa de óxido. El análisis TEM muestra que a medida que aumenta el tiempo de reacción en el agua, aumenta el grosor de la capa de óxido, lo que podría detener aún más la tasa de transferencia de electrones. A una temperatura por debajo de 150 ° C, la transferencia de electrones se produce principalmente por efecto de túnel de electrones en la formación de la capa de óxido de hasta unos pocos nanómetros [48]. Entonces, después de una oxidación prolongada del agua, se formó una capa de óxido estable en la superficie del núcleo de Fe, porque durante la síntesis, los precipitados de Fe NC obtenidos se secaron bajo la atmósfera inerte (en nuestro caso, Argón) para reducir el riesgo de oxidación adicional. . Estos Fe NC pueden ser estables hasta 6 meses sin oxidación adicional, lo que los convierte en candidatos biocompatibles y adecuados para aplicaciones biomédicas.
VSM
Las propiedades magnéticas de los Fe NC se midieron a 320 K como se muestra en la Fig. 11. Se desprende de la Fig. 11 que el Fe NCs-0 y Fe NCs-2 poseen el valor de magnetización de saturación (Ms) de 1400 emu / gy 1420 emu / g, que es superior a Fe NCs-4 y Fe NCs-6 con valores de Ms de 1200 emu / gy 910 emu / g. En la etapa inicial de oxidación (durante 0 min y 120 min), la capa de Fe NCs-0 y Fe NCs-2 estaba hecha de una mezcla de magnetita y hematita que causa una reducción en la contribución del núcleo de Fe de valencia cero, pero debido a presencia de magnetita en ambas muestras poseen un alto momento magnético, por lo que el valor de saturación de magnetización de Fe NCs-0 es más cercano al Fe NCs-2. Pero un mayor aumento en el envejecimiento del agua (de 120, 240 a 360 min), la magnetita se convierte gradualmente en hematita , y también el núcleo de Fe disminuye, por lo que la magnetización de saturación de las muestras Fe NCs-2, FeNCs-4 y Fe NCs-6 también disminuye (es decir, 1420 emu /, 1200 emu / g, 910 emu / g). La Figura 12 muestra la dependencia de los valores de Ms (emu / g) del aumento del espesor de la capa oxidada para Fe NCs-0, Fe NCs-2, Fe NCs-4 y Fe NCs-6 con un diámetro similar promedio de 96 nm y diferentes R core / R shell ratio (Tabla 4).
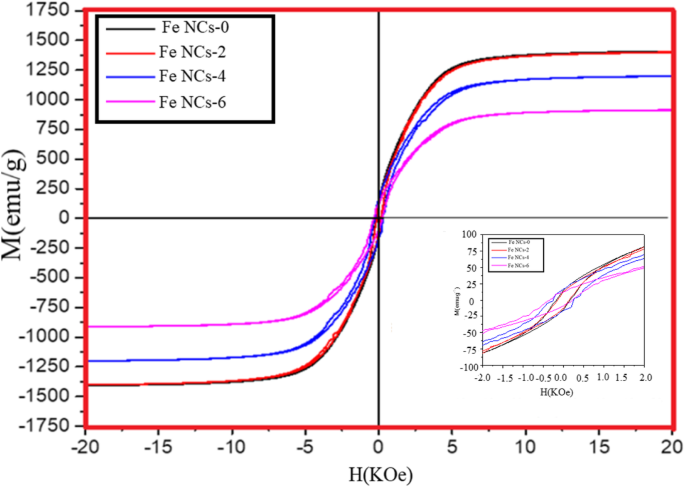
Histéresis magnética medida a temperatura ambiente, el recuadro muestra la curva ampliada entre - 2,0 y 2,0 kOe
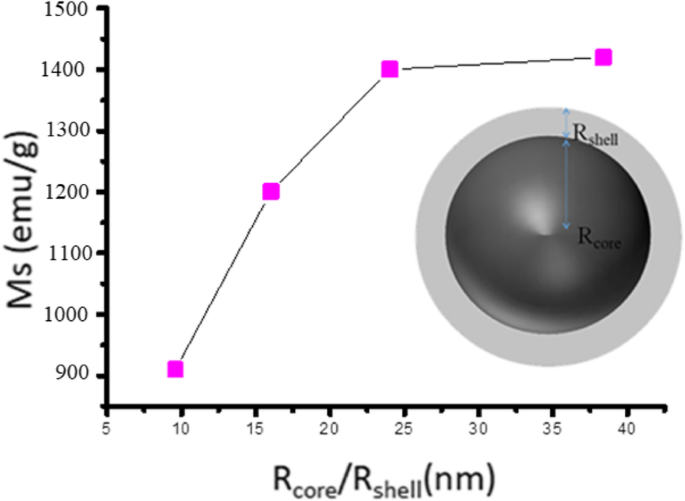
Sra. Vs R núcleo / R shell curva, tomando el diámetro promedio de Fe NCs 96 nm
Para explicar los fenómenos de inversión de magnetización en una cadena compuesta por partículas esféricas de dominio único, Jacobs y Beans [49] introdujeron el "modelo de cadena de esferas". El modelo de cadena de esferas podría aplicarse para Fe NC, considerando el ensamblaje en cadena de nanopartículas de Fe [49]. Aunque el módulo sólo es aplicable a las partículas de dominio único con interacciones dipolares de largo alcance entre, en este caso, los valores de Hc para Fe NC se consideran muy bajos en comparación con los valores predichos en [49]. Los dos mecanismos importantes, el mecanismo de abanico y el mecanismo de rizado, están relacionados con dos estados propios de magnetización. En nuestro caso, ambos mecanismos no son aplicables. Recientemente, Krajewski et al. [50] han estudiado las propiedades estructurales y magnéticas de Fe NC y NP y predijeron que las Fe NC siguen el mecanismo de abanico. Aunque (1) a diferencia de los resultados de Zhang y Manthirama [51], su estudio no proporcionó la prueba de que los Fe NC se encuentran en la región de dominio único (es decir, los resultados de Zhang y Manthirama muestran que los valores de Hc de Fe NC aumentan con el aumento del diámetro de partícula , y en el rango de diámetro de 28 a 35 nm, el valor de Hc permanece casi máximo (≈ 1250 Oe), esta es la región que corresponde a un solo dominio de Fe NC). (2) En segundo lugar, el valor de Hc en su estudio [50] resultó muy bajo (es decir, 300 Oe) que los estudios teóricos anteriores que explican el mecanismo de abanico (es decir, Hc ≥ 900 Oe para n =2 – ∞, donde n es el número de partículas en la cadena) [49]. (3) Finalmente, no hay explicación sobre el comportamiento de inversión de magnetización de Fe NC.
Trabajos anteriores muestran que para las aplicaciones de resonancia magnética, la morfología de las nanopartículas (valor de Ms, tamaño y material dopante) se consideró fuertemente para mejorar la r 2 valores [52,53,54]. La teoría de la esfera exterior de la mecánica cuántica explica que la r 2 la relaxividad depende tanto del radio efectivo como del valor de Ms del núcleo superparamagnético [55, 56]. La relaxividad r 2 de NPs de Fe superparamagnéticos puede explicarse por [57,58,59,60]
$$ {r} _2 =\ frac {\ left (256 {\ pi} ^ 2 {\ gamma} ^ 2 \ right) {kM} _s ^ 2 {r} ^ 2} {D \ left (1+ \ frac {L} {r} \ right)} $$ (1)donde γ y Ms son magnetización de saturación, r es el radio del núcleo magnético, L es el grosor, D es la difusividad de las moléculas de agua y k es el factor de conversión. Esta ecuación muestra que r 2 los valores dependen directamente de los valores de Ms y del radio del material magnético. Teniendo esto en cuenta, Fe NCs-0 podría ser un candidato potencial para r 2 agentes de contraste para resonancia magnética en un futuro próximo.
Conclusión
El análisis estructural de Fe NC se realizó mediante XRD, TEM, espectroscopía Raman y espectroscopía Mössbauer. El análisis XRD muestra que el núcleo de Fe NC fue elaborado por bcc Fe, pero no se observó ningún pico de óxido de hierro. Los resultados de TEM muestran que se formó una fina capa de óxido en Fe NC, lo que confirma la naturaleza núcleo-capa de Fe NC. Con el aumento del tiempo de reacción en agua de 0 a 360 min, el espesor de la capa de óxido aumenta de 2,5 a 10 nm. Los estudios Raman muestran que la capa de Fe NCs-0 y Fe NCs-2 era una mezcla de fase de hematita y magnetita. El pico de magnetita parece desaparecer para Fe NCs-4 y Fe NCs-6. Al analizar la espectroscopia de Mössbauer en Fe NCs-0 y Fe NCs-6, se observó que el núcleo de Fe NCs-0 y Fe NCs-6 estaba hecho de bcc Fe. La capa de Fe NCs-0 estaba hecha de magnetita, y la fase de hematita y la capa de Fe NCs-6 muestran una fase de hematita pura. El posible mecanismo para la formación de NC de Fe núcleo-capa, como se deduce de la espectroscopía de Mössbauer y la espectroscopía Raman, es el tiempo inicial de oxidación; el núcleo de Fe de valencia cero se cubrió inmediatamente con una capa de magnetita y una cubierta de hematita, pero debido al tiempo prolongado de oxidación del agua, la magnetita se convirtió gradualmente en hematita. Las propiedades magnéticas de los Fe NC se midieron mediante VSM a temperatura ambiente. Los valores de Ms disminuyen con el aumento de la capa de óxido, debido a un aumento en la contribución de la fase de hematites de menor momento magnético.
Disponibilidad de datos y materiales
Los conjuntos de datos que respaldan las conclusiones de este artículo se incluyen dentro del artículo.
Abreviaturas
- 0-D:
-
Cero dimensional
- 1-D:
-
One dimensional
- DI:
-
Desionizado
- EDX:
-
Espectroscopia de rayos X de dispersión de energía
- FE-SEM:
-
Field emission scanning electron miscroscopy
- H:
-
Hyperfine field
- Hc:
-
Coercivity
- MH:
-
Magnetic hyperthermia
- Mr:
-
Remanent magnetization
- IRM:
-
Imágenes por resonancia magnética
- Ms:
-
Saturation magnetization
- NC:
-
Nanochains
- NW:
-
Nanocables
- P:
-
Quadrupole splitting
- TEM:
-
Microscopía electrónica de transmisión
- VSM:
-
Magnetómetro de muestra vibrante
- XRD:
-
Difracción de rayos X
- δ :
-
Isomer shifts
Nanomateriales
- Inductores
- Concha de metralla
- Nanocups pueden doblar la luz
- Tratamiento de campo electromagnético de RF de absorbentes de luz CZTSSe de kesterita tetragonal
- Síntesis de puntos cuánticos de tipo II / tipo I de ZnSe / CdS / ZnS con supresión de reabsorción y su aplicación para el ensayo inmunoabsorbente
- Síntesis ecológica de puntos cuánticos de núcleo / carcasa de InP / ZnS para su aplicación en diodos emisores de luz sin metales pesados
- Fabricación, caracterización y citotoxicidad de nanopartículas de carbonato de calcio derivadas de concha de oro-berberecho conjugado de forma esférica para aplicaciones biomédicas
- Control electroquímico reversible sobre la luminiscencia fotoexcitada de la película de puntos cuánticos de núcleo / carcasa CdSe / ZnS
- Prueba de las propiedades estructurales, electrónicas y magnéticas de Ag n V (n =1–12) Clusters
- Profundos efectos interfaciales en CoFe2O4 / Fe3O4 y Fe3O4 / CoFe2O4 Core / Shell Nanoparticles
- Fabricación y caracterización de nanoclips de ZnO mediante el proceso mediado por poliol



