Fabricación de nanoestructuras híbridas basadas en nanoclusters de Fe3O4 como agentes teranósticos para la obtención de imágenes por resonancia magnética y la administración de fármacos
Resumen
La combinación de medicamentos contra el cáncer con nanocristales inorgánicos para construir nanoestructuras híbridas multifuncionales se ha convertido en una poderosa herramienta para el tratamiento del cáncer y la supresión de tumores. Sin embargo, sigue siendo un desafío crítico sintetizar nanoestructuras compactas y multifuncionales con funcionalidad y reproducibilidad mejoradas. En este estudio, informamos sobre la fabricación de nanoestructuras híbridas de magnetita que emplean Fe 3 O 4 nanopartículas (NP) para formar nanoclusters de magnetita (NC) multifuncionales mediante la combinación de un conjunto de microemulsión de aceite en agua y un método capa por capa (LBL). El Fe 3 O 4 Los NC se prepararon en primer lugar mediante una técnica de autoensamblaje en microemulsión. Luego, capas de polielectrolito compuestas de poli (clorhidrato de alilamina) (PAH) y poli (4-estirenosulfonato de sodio) (PSS) y clorhidrato de doxorrubicina (DOX) se taparon con Fe 3 O 4 NC para construir el Fe 3 O 4 Nanoestructuras híbridas NC / PAH / PSS / DOX mediante el método LBL. Las nanoestructuras híbridas preparadas cargadas con DOX demostraron la liberación del fármaco sensible al pH y una mayor citotoxicidad hacia las células de cáncer de pulmón humano (A549) in vitro y pueden servir como T 2 agentes de contraste de resonancia magnética (IRM) ponderados, que pueden mejorar significativamente T 2 relajación y conducen a un mejor efecto de contraste de resonancia magnética celular. Los DOX cargados que emiten señales rojas bajo excitación con 490 nm son adecuados para aplicaciones de bioimagen. Este trabajo proporciona una estrategia novedosa para construir un Fe 3 O 4 nanoplataforma teranóstica multifuncional basada en T 2 resonancia magnética ponderada, imágenes de fluorescencia y administración de fármacos.
Introducción
En los últimos años, se han desarrollado varios sistemas de administración de fármacos multifuncionales para el diagnóstico y la terapia futuros en aplicaciones biomédicas [1, 2, 3, 4]. Las nanoestructuras híbridas multifuncionales que tienen propiedades favorables integradas poseerán aplicaciones importantes como la obtención de imágenes multimodales y el diagnóstico y la terapia simultáneos [5,6,7,8,9,10,11]. Además, estas nanoestructuras son sistemas de administración de fármacos que responden a estímulos para mejorar la acumulación de fármacos, mejorar la eficacia terapéutica y / o reducir los efectos secundarios. Especialmente, estos sistemas de administración de fármacos sensibles al pH han atraído un gran interés en la investigación. Esto se debe a que la mayoría de los tumores humanos tienen un valor de pH más ácido, lo que proporciona una forma posible de diseñar la liberación controlada de moléculas de fármaco [12,13,14,15,16].
En las últimas décadas, se han desarrollado varias nanoestructuras híbridas combinando nanomateriales inorgánicos con polímeros orgánicos [17,18,19,20], incluidas partículas magnéticas [21,22,23], nanopartículas de conversión ascendente (NP) [17, 24] y partículas de sílice mesoporosas [25]. Entre ellos, las nanoestructuras híbridas magnéticas basadas en óxidos de hierro con magnetización relativamente grande a temperatura ambiente se han utilizado ampliamente en los campos biomédicos [26, 27, 28, 29]. La funcionalización de nanomateriales inorgánicos recubiertos con capas de polielectrolito puede realizar una encapsulación sensible al pH y la liberación de moléculas de fármaco [12, 17, 30]. Más recientemente, las capas de polielectrolito compuestas de poli (estireno sulfonato) (PSS) y el policatión poli (clorhidrato de alilamina) (PAH) se han estudiado ampliamente [31,32,33,34,35,36]. También se han informado recientemente capas de polielectrolitos combinadas con NP magnéticas y luminiscentes o moléculas de fármaco para sistemas de administración de fármacos multifuncionales [37,38,39]. Óxido de hierro (Fe 3 O 4 ) Los NP están recibiendo cada vez más atención en el campo de la resonancia magnética (MRI) y la administración de fármacos debido a sus propiedades superparamagnéticas únicas, biocompatibilidad, baja citotoxicidad y flexibilidad [9, 11, 28, 29, 40,41,42 ]. En general, existen dos métodos para mejorar la capacidad de respuesta magnética del Fe 3 O 4 NP. El primero es sintetizar las partículas de magnetita del tamaño de un micrómetro. Sin embargo, debido a su gran tamaño, tienden a agregarse en solución acuosa, lo que no es beneficioso para las aplicaciones biomédicas. El otro enfoque es ensamblar Fe 3 O 4 NP en nanoclusters (NC). Estos Fe 3 O 4 Los NC mejoraron enormemente la capacidad de respuesta magnética en comparación con el Fe 3 individual O 4 NP [22, 43]. Por lo tanto, si el Fe 3 autoensamblado O 4 Los NC se adoptan como el núcleo para fabricar nanoestructuras híbridas multifuncionales, el rendimiento de la resonancia magnética se mejorará por el efecto colectivo de Fe 3 O 4 NP [43, 44, 45]. Hasta donde sabemos, el Fe 3 autoensamblado O 4 Rara vez se han informado NC funcionalizados con multicapas PAH / PSS para la liberación de fármacos que responden al pH.
En este trabajo, una nanoplataforma teranóstica versátil basada en Fe 3 O 4 Se preparó NP para MRI y administración de fármacos. En nuestro enfoque, Fe 3 O 4 Se obtuvieron nanoestructuras híbridas NC / PAH / PSS / DOX combinando un método de microemulsión de aceite en agua y un método de adsorción electrostática capa por capa (LBL). Se espera que el Fe 3 empaquetado O 4 El sistema NC puede conducir a una T mejorada 2 relajación y contraste de imagen, y la gran superficie específica de Fe 3 O 4 Las nanoestructuras híbridas NC / PAH / PSS permiten una alta carga de medicamentos contra el cáncer. Además, el experimento in vitro muestra que el contraste de resonancia magnética celular de células de cáncer de pulmón humano (A549) incubadas con Fe 3 O 4 NC / PAH / PSS / DOX se ha mejorado significativamente.
Materiales y métodos
Materiales
FeCl 3 · 6H 2 O (99,99%), FeCl 2 · 4H 2 Se adquirieron O (99,99%), ácido oleico (OA, 90%) y 1-octadeceno (ODE, 90%) de Alfa Aeasar. Oleato de sodio (NaOA), etanol, hexano, ciclohexano, isopropanol, dodecilbencenosulfonato de sodio (SDBS), fluoruro de amonio (NH 4 F), hidróxido de sodio (NaOH), dimetilsulfóxido (DMSO) y amoniaco se adquirieron de Sinopharm Chemical Reagent Co., Ltd (China). Se adquirieron poli (clorhidrato de alilamina) (PAH), poli (estireno sulfonato) (PSS) y bromuro de 3- (4,5-dimetiltiazol-2-il) -2,5-difeniltetrazolio de Sigma-Aldrich. El fármaco anticáncer hidrocloruro de doxorrubicina (DOX,> 98%) se adquirió de Shanghai Sangon Biotech Company (Shanghai, China). El medio de crecimiento APMI 1640 y el suero fetal bovino (FBS) se adquirieron de Hyclone. Todos los reactivos se utilizaron tal como se recibieron sin purificación adicional.
Preparación de oleato férrico
La síntesis de NP magnéticas partió de la síntesis de oleato férrico. FeCl 3 · 6H 2 O (2,59 g), NaOA (14,6 g), C 2 H 5 OH (32 ml), H 2 Se mezclaron O (24 mL) y hexano (56 mL) en un matraz de tres bocas de 150 mL y se calentaron a 70 ° C a reflujo durante 4 h para formar una solución de complejos de oleato férrico transparente. Después de eso, el líquido se separó mediante un embudo de separación y se conservó la capa superior de aceite. El hexano en el líquido se evaporó a 70 ° C mediante evaporación rotatoria y se secó durante 48 h al vacío. Las muestras preparadas se almacenaron en una caja de guantes al vacío para su uso posterior.
Síntesis de Fe 3 O 4 NP
Sintetizamos Fe 3 O 4 NP siguiendo procedimientos previamente informados con ligeras modificaciones [46]. Se mezclaron oleato férrico (7,2 g), OA (1,28 ml) y ODE (50 ml) en un matraz de tres bocas de 100 ml y se calentaron a 300ºC durante 40 min bajo protección de argón; después de eso, la mezcla se enfrió a temperatura ambiente y se oxidó al aire durante más de 12 h. Los nanocristales resultantes se precipitaron mediante la adición de isopropanol, se centrifugaron y se lavaron dos veces con una mezcla de etanol y agua (1:1 v / v ). El Fe 3 protegido con ácido oleico O 4 Finalmente, las NP se dispersaron en 200 ml de ciclohexano y el sobrenadante se selló y se almacenó para los experimentos posteriores.
Preparación de Fe 3 O 4 NC
Fe 3 O 4 Los NC se prepararon mediante una técnica de autoensamblaje de microemulsión sencilla y sencilla, como se describió anteriormente con modificaciones [47]. Brevemente, una solución de 200 μL de Fe 3 O 4 Se vertieron nanocristales en ciclohexano en 4 ml de solución acuosa que contenía 14 mg de SDBS. La solución mezclada se sometió a un tratamiento ultrasónico durante 5 min durante 4 veces. La emulsión de sólido en aceite en agua (S / O / W) formada se agitó a temperatura ambiente durante 6 h para evaporar el disolvente orgánico seguido del autoensamblaje de Fe 3 O 4 NP para formar NC 3D. Los productos finales se lavaron con agua desionizada 3 veces para eliminar el exceso de SDBS, los nanocristales no incorporados y algunos posibles contaminantes más grandes.
Preparación de Fe 3 O 4 Nanoestructuras híbridas NC / PAH / PSS / DOX
El Fe 3 O 4 Se prepararon nanoestructuras híbridas NC / PAH / PSS / DOX mediante interacciones atractivas electrostáticas. El Fe 3 preparado O 4 Los NC están cargados negativamente debido a la encapsulación de los tensioactivos aniónicos. Primero se volvieron a cargar positivamente por adsorción de una capa de polielectrolito cargado positivamente, poli (clorhidrato de alilamina) (PAH, MW 15 000). Específicamente, un Fe 3 de 300 μL O 4 La muestra NC se diluyó en primer lugar 10 veces a 3 ml con agua desionizada. El Fe 3 O 4 Posteriormente, la mezcla NC se añadió gota a gota a una solución acuosa de PAH (1 ml, 10 g / L, NaCl 4 mM) con agitación vigorosa. Después de que la solución se agitó durante 24 h, el exceso de PAH se eliminó mediante centrifugación y el Fe 3 recubierto con PAH resultante O 4 NC (Fe 3 O 4 NC / PAH) se redispersaron en agua (3 ml).
El Fe 3 O 4 Luego, los NC / PAH se volvieron cargados negativamente por adsorción de una capa de polielectrolito cargado negativamente, poli (4-estirenosulfonato de sodio) (PSS, PM 70 000). Específicamente, un Fe 3 de 3 ml O 4 Se añadió gota a gota solución de muestra de NC / PAH a una solución acuosa de PSS (1 ml, 10 g / L, NaCl 4 mM) con agitación vigorosa. Después de que la solución se agitó durante 24 h, el exceso de PSS se eliminó mediante centrifugación y el Fe 3 recubierto con PSS resultante O 4 NC / PAH (Fe 3 O 4 NC / PAH / PSS) se redispersaron en agua (3 ml).
En primer lugar, se preparó la solución madre acuosa de DOX [17]. La concentración fue de 5,0 mg / ml. La solución de nanoestructura híbrida se obtuvo mezclando el Fe 3 O 4 Solución NC / PAH / PSS (3 mL, 32 mg / mL) y la solución stock DOX (60 μL) en un pequeño tubo de plástico con agitación durante 24 h en el cuarto oscuro. Después de la centrifugación, el Fe 3 O 4 Finalmente se obtuvieron nanoestructuras híbridas NC / PAH / PSS / DOX.
Mediciones de resonancia magnética
Las mediciones de resonancia magnética se realizaron en un sistema de micro imágenes de 11,7 T micro 2,5 (Bruker, Alemania). La diferente cantidad de Fe 3 O 4 Se dispersaron nanoestructuras híbridas NC / PAH / PSS / DOX en 1,2 ml de solución acuosa de agarosa y luego se cargaron en los microtubos para las mediciones de resonancia magnética. La concentración final de iones Fe fue 0 mM, 0,013 mM, 0,026 mM, 0,032 mM, 0,041 mM, 0,052 mM y 0,065 mM, respectivamente. Los parámetros de medición son los siguientes:tiempo de repetición (TR) =300 ms, tiempo de eco (TE) =4,5 ms, matriz de imagen =128 × 128, grosor de corte =1,2 mm, campo de visión (FOV) =2,0 × 2,0 cm, y número de promedios (NA) =2.
Captación celular e imágenes por resonancia magnética
Para demostrar una absorción celular eficiente, las células A549 se sembraron en el cubreobjetos en el plato confocal y se incubaron en un 5% CO 2 humidificado atmósfera durante 4 ha 37 ° C. Luego, el Fe 3 O 4 Se añadieron nanoestructuras híbridas NC / PAH / PSS / DOX al medio de incubación a diferentes concentraciones y se incubaron durante 2 h. Las concentraciones finales de iones Fe se obtuvieron como 0, 2,2, 4,5, 9,0 y 13,5 µM, respectivamente. Una vez que se retiró el medio, las células se lavaron dos veces con PBS (pH =7,4, 20 mM) y se usaron directamente para la obtención de imágenes por RM.
Curva estándar de DOX
Se disolvió una cantidad adecuada de DOX en agua por oscilación. Luego, se prepararon una serie de diferentes concentraciones de solución acuosa de DOX (0-0.03 mg / mL). Se midió la intensidad de fluorescencia de diferentes concentraciones de solución de DOX ( λ ex =490 nm). Finalmente, la curva estándar de DOX se determinó mediante el ajuste de la curva de la intensidad de fluorescencia vs la concentración de DOX.
La curva estándar de área: Y =447.4423 + 69745.08457X.
Tasa de precisión de la curva estándar: R 2 =0,9992.
Carga y liberación de DOX
Para medir las capacidades de carga del Fe 3 O 4 Nanoestructuras híbridas NC / PAH / PSS / DOX, la solución sobrenadante se recogió después de la centrifugación de las nanoestructuras híbridas preparadas. Se examinó el espectro de fluorescencia de las moléculas de DOX en la solución sobrenadante y se calculó la concentración de DOX en el sobrenadante comparando la curva estándar de DOX. Los porcentajes de DOX que quedan en el Fe 3 O 4 Las nanoestructuras híbridas NC / PAH / PSS / DOX se calcularon de acuerdo con la siguiente ecuación:
$$ \ mathrm {Cargando} \ \ mathrm {eficiencia} \ \ left (\% \ right) =\ left ({\ mathrm {W}} _ 0 \ hbox {-} {\ mathrm {W}} _ {\ mathrm {s}} \ right) / {\ mathrm {W}} _ 0 \ times 100 \% $$donde W 0 y W s representan la masa DOX inicial y la masa DOX en los sobrenadantes, respectivamente.
Para los estudios de liberación acumulativa de DOX en soluciones tampón de PBS (pH 5,0 y 7,4) con la misma concentración de NaCl de 0,15 M, el Fe 3 O 4 Se dispersaron nanoestructuras híbridas NC / PAH / PSS / DOX en 1,0 ml de solución tampón y luego se transfirieron a una bolsa de diálisis. Luego, se mantuvo en solución tampón y se agitó suavemente a 37 ° C en el cuarto oscuro. A intervalos de tiempo seleccionados, se extrajeron 100 μL de solución y se analizaron mediante el espectro de fluorescencia, y luego se devolvieron a la solución original.
Citotoxicidad in vitro de Fe 3 O 4 Nanoestructuras híbridas NC / PAH / PSS / DOX
Citotoxicidad in vitro del Fe 3 O 4 Se evaluaron nanoestructuras híbridas NC / PAH / PSS / DOX frente a células A549 basándose en el ensayo estándar de metil tiazoliltetrazolio (MTT). Las células A549 se cultivaron en medio de crecimiento APMI 1640 complementado con suero bovino fetal (FBS) al 10%, estreptomicina a 100 µg / ml y penicilina a 100 µg / ml. Las células se mantuvieron a 37 ° C en una atmósfera humidificada de 5% de CO 2 en aire. El ensayo se realizó por triplicado de la misma manera. Brevemente, se sembraron células A549 en placas de 96 pocillos a una densidad de 8 × 10 3 células por pocillo en 100 μL de medio. Después del crecimiento durante la noche, las células se incubaron a varias concentraciones de DOX libre, Fe 3 O 4 NC / PAH / PSS y Fe 3 O 4 Nanoestructuras híbridas NC / PAH / PSS / DOX (0,1, 0,2, 0,4, 0,8, 1,2, 1,6, 2,0 μM) durante 24 h. Después de incubarse durante 24 h, se agregaron 10 μL de solución de bromuro de 3- (4, 5-dimetiltiazol-2-il) -2,5-difeniltetrazolio (5 mg / ml) a cada pocillo y las células se incubaron durante 4 ha 37ºC. Después de eliminar la solución de bromuro de 3- (4, 5-dimetiltiazol-2-il) -2,5-difeniltetrazolio, se agregaron 150 μL de dimetilsulfóxido (DMSO) a cada pocillo y la placa se agitó suavemente durante 10 minutos para disolverla. los cristales violetas precipitados. La densidad óptica (DO) se midió a 490 nm usando un lector de microplacas (Perkin Elmer, Victor X4). La viabilidad celular se evaluó como un porcentaje en comparación con las células de control.
Caracterización
Los tamaños y morfologías de Fe 3 O 4 NP y Fe 3 O 4 Las nanoestructuras híbridas NC / PAH / PSS / DOX fueron examinadas por un microscopio electrónico de transmisión FEI Tecnai G2-F20 (TEM) a un voltaje de aceleración de 200 kV. Se realizaron mediciones de dispersión dinámica de luz (DLS) en un analizador de tamaño de partícula y potencial zeta de Malvern (Zetasizer Nano ZS90). Los espectros de absorción UV-vis fueron adquiridos por un espectrómetro Perkin Elmer Lambda-25 UV-vis. Los espectros de fluorescencia se registraron usando un espectrofotómetro de fluorescencia Hitachi F-4600. Se utilizó espectroscopia de emisión atómica de plasma acoplado inductivamente (ICP-AES) (Agilent 5100) para analizar las concentraciones del elemento Fe en el Fe 3 O 4 Nanoestructuras híbridas NC / PAH / PSS / DOX.
Resultados y discusión
El Fe 3 O 4 Las nanoestructuras híbridas NC / PAH / PSS / DOX se preparan por autoensamblaje de óxido de hierro primario (Fe 3 O 4 ) NP que resultan en agregados esféricos densamente empaquetados a través de una técnica de autoensamblaje en microemulsión como se describió anteriormente con la modificación [17, 47], seguida de un método de adsorción electrostática LBL. La Figura 1 ilustra la ilustración esquemática de la síntesis de Fe 3 O 4 Nanoestructuras híbridas NC / PAH / PSS / DOX. Magnetita Fe 3 recubierta con ácido oleico hidrófobo O 4 Las NP se produjeron inicialmente mediante el proceso de descomposición térmica en un disolvente orgánico [46]. Fe 3 O 4 Los NP son esféricos y de tamaño uniforme con un tamaño de partícula promedio de aproximadamente 15 nm (archivo adicional 1:Figura S1). Para el montaje de NC magnéticos, el Fe 3 recubierto de OA O 4 Las NP se dispersaron en ciclohexano y luego se añadieron gota a gota a una solución acuosa que contenía SDBS. La solución compleja se trató ultrasónicamente para formar una emulsión estable de aceite en agua. Después de la evaporación del solvente orgánico en la emulsión, Fe 3 O 4 Las NP se autoensamblaron para formar nanoclusters esféricos mediante interacción hidrofóbica. A continuación, el Fe 3 O 4 Se prepararon nanoestructuras híbridas NC / PAH / PSS / DOX mediante un método LBL mediante interacciones atractivas electrostáticas, que se ilustra esquemáticamente en la Fig. 1.
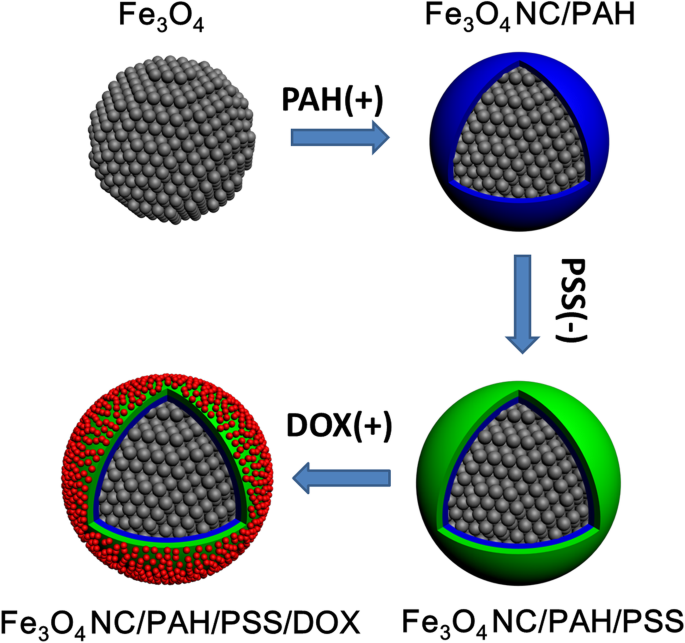
Ilustración esquemática de la síntesis de Fe 3 O 4 Nanoestructuras híbridas NC / PAH / PSS / DOX como agentes teranósticos para IRM y administración de fármacos
Las morfologías y tamaños del Fe 3 O 4 NC y Fe 3 O 4 Se examinaron nanoestructuras híbridas NC / PAH / PSS con TEM y DLS, respectivamente. Como se muestra en la Fig. 2a yb, el Fe 3 O 4 Los NC demuestran los cúmulos cuasi esféricos. El tamaño de partícula promedio medido por DLS es de aproximadamente 57 nm (Fig. 2e). En informes anteriores, HAP con carga positiva o PSS con carga negativa se deposita alternativamente en la superficie de la plantilla debido a sus excelentes propiedades electrostáticas [48,49,50,51]. Estudiar la formación de cada capa de polielectrolito depositada sobre el Fe 3 O 4 NC, se realizaron los experimentos de potencial zeta. La variación del potencial zeta con la capa de polielectrolito para revestimientos de PSS / PAH y DOX se muestran en el archivo adicional 1:Figura S2. El inmaculado Fe 3 O 4 Los NC tienen un potencial zeta negativo de - 19,7 mV debido a la existencia de SDBS. La absorción de una sola capa de PAH cargada positivamente en Fe 3 O 4 NC invierte el potencial de superficie de - 19,7 a + 32 mV. Posteriormente, la deposición de la capa de PSS cargada negativamente provoca otra reversión del potencial superficial de + 32 a - 34 mV. Esto indica un crecimiento gradual de la capa durante la fabricación de nanoestructuras híbridas magnéticas NC. Estos resultados muestran que las capas de PAH y PSS se recubrieron con éxito sobre el Fe 3 O 4 NC. Finalmente, DOX fue adsorbido con éxito en la superficie del Fe 3 O 4 Nanoestructuras híbridas NC / PAH / PSS / DOX, que fue confirmado por el potencial zeta positivo (+ 1,91 mV) (archivo adicional 1:Figura S2). Las imágenes TEM con un aumento diferente del Fe 3 O 4 Las nanoestructuras híbridas NC / PAH / PSS se muestran en la Fig. 2c y d. No se observa ninguna diferencia estructural y morfológica significativa después de los revestimientos de polielectrolitos. En comparación con la Fig. 2a yb, se puede observar el contraste brillante y el tamaño del Fe 3 O 4 Las nanoestructuras híbridas NC / PAH / PSS aumentan ligeramente debido al recubrimiento de las capas de PAH y PSS. Las nanoestructuras híbridas magnéticas sintetizadas muestran una forma cuasi esférica casi mono-dispersa con un tamaño promedio de aproximadamente 84 nm según los resultados de la medición DLS (Fig. 2f).
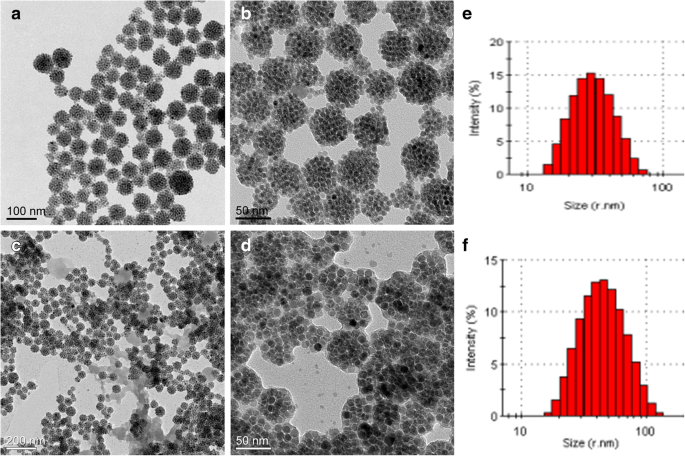
Imágenes TEM de Fe 3 O 4 NC ( a , b ) y Fe 3 O 4 NC / PAH / PSS ( c , d ) a menor y mayor aumento, respectivamente. Distribución de tamaño de Fe 3 O 4 NC ( e ) y Fe 3 O 4 Nanoestructuras híbridas NC / PAH / PSS ( f )
Evaluar la posible aplicación de Fe 3 O 4 Nanoestructuras híbridas NC / PAH / PSS en MRI, las tasas de relajación transversal de protones (1 / T 2 ) en función de la concentración de iones Fe se determinaron usando un espectrómetro Bruker AVANCE 500WB a 11,7 T. Se observó una relación lineal entre las velocidades de relajación y la concentración de iones Fe, como se muestra en la Fig. 3b. Además, las tasas de relajación transversal (1 / T 2 ) aumentó al aumentar la concentración de Fe 3 O 4 NC debido al alto grado de agregación del Fe 3 O 4 Núcleo magnético de NP, lo que demuestra que las nanoestructuras híbridas magnéticas podrían ser una T eficaz 2 medio de contraste ponderado para resonancia magnética (Fig. 3a). Basado en la pendiente del gráfico en la Fig. 3b, el valor de la relaxividad transversal ( r 2 ) se determinó en 651,38 mM −1 S −1 , que es superior al del trabajo informado [22]. En comparación con T comercial 2 medios de contraste, los nanoclusters pueden mejorar significativamente la capacidad de contraste del Fe después de que los NP magnéticos se autoensamblen sobre la base del efecto colectivo, mejorando así en gran medida el efecto angiográfico. En el trabajo anterior, los nanocristales de magnetita ensamblados exhibieron un nivel más alto de magnetización de saturación que los nanocristales individuales debido al efecto colectivo de los nanocristales magnéticos [43, 52].
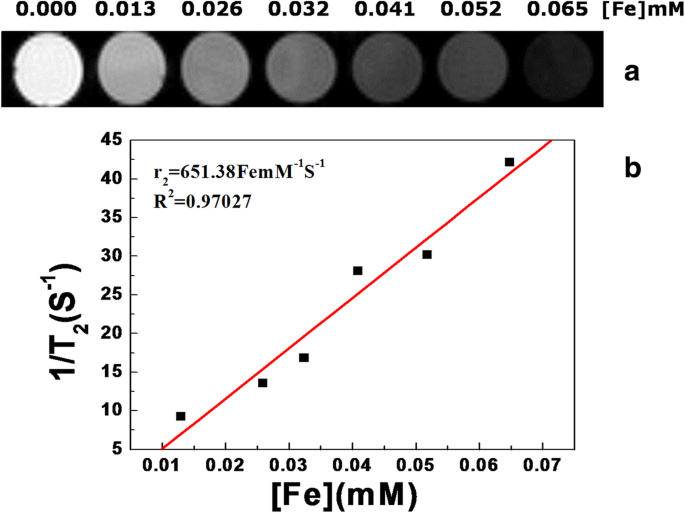
un T 2 imágenes de resonancia magnética ponderadas del Fe 3 O 4 Nanoestructuras híbridas NC / PAH / PSS a diferentes concentraciones en agua. b Gráfico de la tasa de relajación r 2 versus Concentración de Fe en Fe 3 O 4 Nanoestructuras híbridas NC / PAH / PSS. El valor de la relajación r 2 se obtuvo a partir de la pendiente del ajuste lineal de los datos experimentales
Evaluar la capacidad de carga de fármaco de Fe 3 O 4 Nanoestructuras híbridas NC / PAH / PSS / DOX como portadores de administración de fármacos, se eligió un fármaco anticáncer soluble en agua (DOX) como fármaco modelo. El almacenamiento de DOX en las nanoestructuras híbridas con una alta eficiencia fue revelado por primera vez por el cambio de color de la solución. El color de la solución de Fe 3 O 4 NC / PAH / PSS y la solución de DOX pura eran amarillentas y rojas, respectivamente (Fig. 4a y b). Después de la formación del Fe 3 O 4 Nanoestructuras híbridas NC / PAH / PSS / DOX, el color de la solución se volvió naranja (Fig. 4c). Debido a la presencia de Fe 3 O 4 NP, las nanoestructuras cargadas con DOX en la suspensión podrían separarse mediante un imán externo, lo que sugiere que el gran potencial de las nanoestructuras híbridas obtenidas para la administración de fármacos dirigidos magnéticamente (Fig. 4d). Se utilizó espectroscopia de absorción UV-vis para determinar la capacidad efectiva de almacenamiento de DOX. La Figura 4e muestra los espectros de absorción UV-vis de la solución acuosa de DOX antes y después de la interacción con Fe 3 O 4 Nanoestructuras híbridas NC / PAH / PSS. En comparación con el DOX libre, se observaron características de pico de absorción similares en el Fe 3 O 4 Nanoestructuras híbridas NC / PAH / PSS / DOX, que es el pico de absorción de recombinación de Fe 3 O 4 NC y DOX. La muestra sin DOX solo muestra el pico de absorción de Fe 3 O 4 NC. Estos datos indican que el DOX como fármaco se puede absorber con éxito en la superficie de las nanoestructuras híbridas. También se encuentra que existe un límite superior de concentración de adsorción de DOX cargado en la superficie de las nanoestructuras híbridas. La Figura 4f muestra el espectro PL del Fe 3 O 4 Nanoestructuras híbridas NC / PAH / PSS / DOX después de la centrifugación cuando se agregaron diferentes concentraciones de DOX al Fe 3 O 4 Solución NC / PAH / PSS. La intensidad de luminiscencia de DOX aumenta a medida que aumenta la DOX añadida hasta alcanzar un techo (8 mg / mL) con la concentración de Fe 3 O 4 NC / PAH / PSS (1,30 × 10 −2 mg / mL) sin cambios. Posteriormente, la cantidad de atrapamiento disminuye debido al exceso de DOX, que no puede adsorberse en la superficie del Fe 3 O 4 Nanoestructuras híbridas NC / PAH / PSS / DOX. La intensidad de fluorescencia más fuerte de DOX corresponde a la concentración a 8 mg / mL, y la muestra correspondiente se usaría para estudios adicionales para realizar experimentos biomédicos. La eficacia asegurada de la carga de fármacos de las nanoestructuras híbridas es crucial para la aplicación clínica. La eficiencia de carga se calculó mediante el área integral de la intensidad de fluorescencia de DOX utilizando el método de curva estándar de DOX [53, 54]. La eficiencia de carga se calculó hasta un 24,39% para el Fe 3 O 4 Nanoestructuras híbridas NC / PAH / PSS / DOX. Por tanto, se ha construido una plataforma teranóstica basada en el Fe 3 O 4 Nanoestructuras híbridas NC / PAH / PSS / DOX debido a la absorción eficaz del fármaco antitumoral DOX.
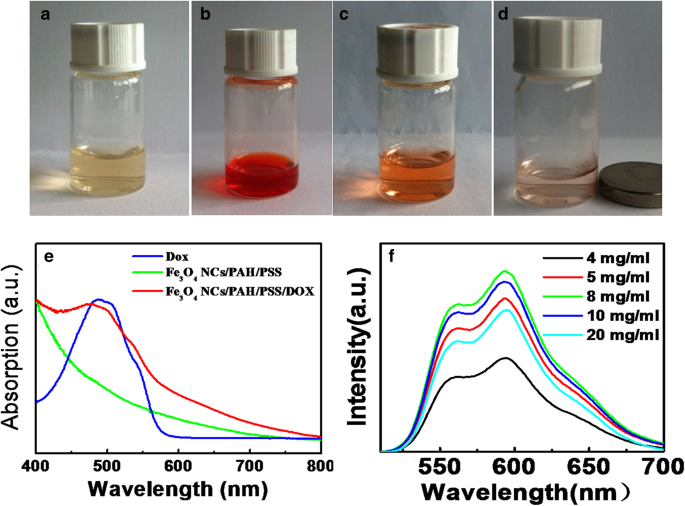
Fotografías ( a - d ) de las diferentes etapas absorbidas de DOX en el Fe 3 O 4 Nanoestructuras híbridas NC / PAH / PSS. Los espectros de absorción UV-vis ( e ) de DOX, Fe 3 O 4 NC / PAH / PSS y Fe 3 O 4 Nanoestructuras híbridas NC / PAH / PSS / DOX. Los espectros de luminiscencia ( f ) de Fe 3 O 4 Nanoestructuras híbridas NC / PAH / PSS / DOX cuando se agregó la diferente concentración de DOX al Fe 3 O 4 Solución de nanoestructura híbrida NC / PAH / PSS
Los perfiles de liberación de fármacos in vitro de Fe 3 O 4 Las nanoestructuras híbridas NC / PAH / PSS / DOX bajo varios valores de pH ambiental se muestran en la Fig. 5. El Fe 3 O 4 Se dializaron nanoestructuras híbridas NC / PAH / PSS / DOX a través de una membrana de diálisis en tampones de fosfato a 37 ° C. Se recogió el DOX liberado de las nanoestructuras híbridas y luego se calculó la cantidad liberada de DOX mediante la intensidad de fluorescencia del sobrenadante. A pH fisiológico de 7,4, la liberación de fármaco observada es un proceso de liberación lenta. Aproximadamente el 20% en peso de DOX se liberó en las 5 h iniciales y luego entró en la etapa estable de liberación lenta. A pH 5,0, aproximadamente el 80% en peso de DOX se liberó de las nanoestructuras híbridas en las primeras 15 h antes de que se alcanzara una meseta de liberación. Los porcentajes de meseta de liberación de DOX observados durante un período de 30 h fueron 80 ± 3% en peso y 20 ± 3% en peso a pH 5,0 y 7,4, respectivamente. Puede verse que el Fe 3 O 4 Las nanoestructuras híbridas NC / PAH / PSS / DOX han revelado un perfil de liberación sostenida y una tasa de liberación de DOX más alta a pH 5,0 que a pH 7,4. El pH ambiental bajo acelera la liberación de DOX del Fe 3 O 4 Nanoestructuras híbridas NC / PAH / PSS / DOX. Eso se debe a la protonación del –NH 2 grupo de DOX en condiciones ácidas, que reduce la interacción electrostática entre los polímeros DOX y PSS a valores de pH bajos [55]. Los estudios de liberación de fármacos indican la buena estabilidad de las moléculas de fármaco unidas electrostáticamente en pH fisiológico y la liberación desencadenada en condiciones ácidas, similar a los trabajos publicados [56,57,58]. Por lo tanto, el Fe 3 obtenido O 4 Las nanoestructuras híbridas NC / PAH / PSS / DOX son los sistemas sensibles al pH para la administración de fármacos DOX y adecuados para el tratamiento específico de tumores sólidos [59].
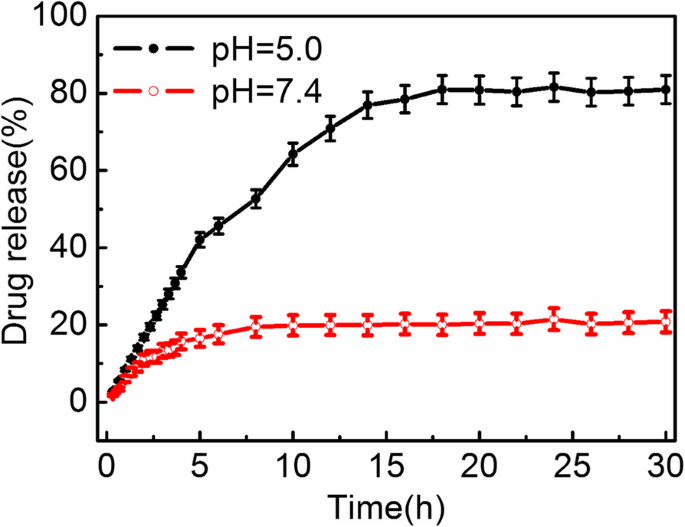
Gráfico de la liberación de DOX del Fe 3 O 4 Nanoestructuras híbridas NC / PAH / PSS / DOX en tampón PBS a pH 7,4 y 5,0, respectivamente
La captación celular y la citotoxicidad son factores clave para evaluar el potencial de un nuevo sistema de administración de fármacos. La captación celular y la citotoxicidad de Fe 3 O 4 Se estudiaron nanoestructuras híbridas NC / PAH / PSS / DOX en líneas celulares A549. La captación intercelular de Fe 3 O 4 Se investigaron nanoestructuras híbridas NC / PAH / PSS / DOX utilizando microscopía óptica y de fluorescencia, que se realizó principalmente mediante el seguimiento de la fluorescencia de DOX. El Fe 3 O 4 Se ha demostrado que las nanoestructuras híbridas NC / PAH / PSS / DOX son eficaces para administrar DOX a las células cancerosas. Como se muestra en la Fig. 6, se observó una fuerte fluorescencia roja de DOX en las células cancerosas después de la incubación durante 24 h. Las nanoestructuras híbridas se internalizaron principalmente mediante endocitosis [60]. Después de la absorción celular, las nanoestructuras híbridas liberaron DOX en el entorno ácido alrededor del endosoma / lisosomas, en el que un pH suficientemente bajo (4,3) podría desencadenar una liberación efectiva de DOX (pH 5,0, Fig. 5). El Fe 3 O 4 Las nanoestructuras híbridas NC / PAH / PSS / DOX exhibieron una captación dependiente del tiempo en las células cancerosas A549, como se muestra en la Fig. 6. A las 0,5 h después de la incubación, la fluorescencia roja era visible alrededor de las células. Los resultados muestran que las nanoestructuras híbridas que contienen DOX permanecieron principalmente alrededor de las células A549. Sin embargo, cuando el tiempo de incubación aumentó a 24 h, la señal de fluorescencia intercelular aumentó de las células A549. Obviamente, muchas nanoestructuras híbridas pueden ingresar a las células cancerosas con el tiempo. Estos resultados confirman que el Fe 3 O 4 Las nanoestructuras híbridas NC / PAH / PSS / DOX pueden transferir DOX de manera eficiente a las células A549. El DOX liberado de las nanoestructuras híbridas en el citoplasma pasa a través de la membrana nuclear y finalmente se acumula en el núcleo, matando las células al causar cambios en la conformación del ADN [61].
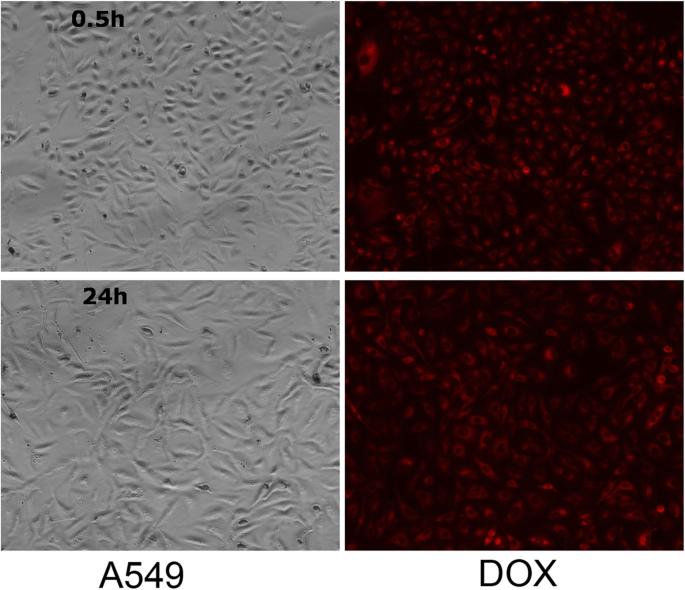
Imágenes microscópicas de fluorescencia confocal de células A549 incubadas con Fe 3 O 4 NC/PAH/PSS/DOX hybrid nanostructures at 37 °C for a 0.5 h and b 24 h. Scale bar, 20 μm
In order to evaluate the pharmacological activity of the Fe3 O 4 NC/PAH/PSS/DOX hybrid nanostructures, the cytotoxicity to A549 cells in vitro was determined by MTT method. Figure 7 shows the cell activity of free DOX, Fe3 O 4 NC/PAH/PSS, and Fe3 O 4 NC/PAH/PSS/DOX hybrid nanostructures with different concentrations after incubation with A549 cells for 24 h. The material amounts were calculated according to the concentration of DOX. The free DOX concentration was the same as the DOX concentration in Fe3 O 4 NC/PAH/PSS/DOX hybrid nanostructures, and the concentration of Fe3 O 4 NC/PAH/PSS hybrid nanostructure was the same as the Fe3 O 4 NC/PAH/PSS concentration in the Fe3 O 4 NC/PAH/PSS/DOX hybrid nanostructures. Each sample was cultured with A549 cells for 24 h. The concentration of Fe3 O 4 NC/PAH/PSS ranged from 0.1 to 2.0 μΜ, and the cell survival rate exceeded 85%. This indicated that Fe3 O 4 NC/PAH/PSS hybrid nanostructures had no obvious cytotoxicity to cancer cells and had good biocompatibility. After incubating with cancer cells for 24 h, however, the free DOX and Fe3 O 4 NC/PAH/PSS/DOX hybrid nanostructures showed obvious cytotoxicity. The cellular viability progressively decreased with increasing effective DOX concentration. As shown in Fig. 7, when the effective DOX concentration was increased from 0.1 up to 2.0 μM, the relative cell viability decreased from about 92% to about 50% for free DOX, and from about 89% to about 40 % for Fe3 O 4 NC/PAH/PSS/DOX hybrid nanostructures, respectively.
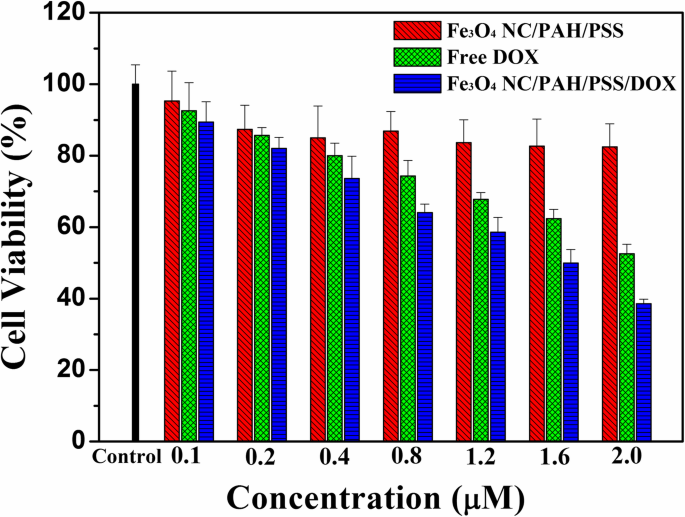
Relative viability of A549 cells incubated with free DOX, Fe3 O 4 NC/PAH/PSS, and Fe3 O 4 NC/PAH/PSS/DOX hybrid nanostructures at different concentrations for 24 h. Error bars were based on triplicate samples
These results indicate that both free DOX and Fe3 O 4 NC/PAH/PSS/DOX hybrid nanostructures have dose-dependent cytotoxicity to cancer cells. The cytotoxicity originates from the loaded DOX rather than Fe3 O 4 NC/PAH/PSS hybrid nanostructures. Cell uptake of free DOX is faster than that of DOX-loaded hybrid nanostructures. This reason is that small DOX molecules can quickly spread into cells, while Fe3 O 4 NC/PAH/PSS/DOX hybrid nanostructures must be endocytosis in order to enter cancer cells. Because of the hypoxia-induced coordinated upregulation of glycolysis, the acidic extracellular environment of solid tumors is stronger than that of normal tissues [62]. At the cellular level, the internalization of most of the hybrid nanostructures will take place through endocytosis. With the increase of DOX concentration, more and more hybrid nanostructures loaded with DOX are endocytosed into cancer cells. After cellular endocytosis, the DOX-loaded hybrid nanostructures usually enter the early endosomes, then enter the late endosomes/lysosomes, and finally fused with lysosomes. Furthermore, both endosomes (pH 5.0–6.0) and lysosomes (pH 4.5–5.0) have an acidic microenvironment. In our study, the pH-responsive Fe3 O 4 NC/PAH/PSS/DOX hybrid nanostructures were more likely to decompose and release drugs in acidic environments, thus effectively reducing side effects, prolonging half-life of drugs, and providing more effective and lasting treatment. Due to the main target of DOX being cell nucleus, DOX can bind to double-stranded DNA to form DNA adducts, inhibit the activity of topoisomerase and induce cell death (apoptosis) [63]. As a result, the released DOX molecules were located in the cell nucleus. Therefore, the obtained Fe3 O 4 NC/PAH/PSS/DOX hybrid nanostructures may have good potential for cancer chemotherapy.
As discussed above, the Fe3 O 4 NC/PAH/PSS/DOX hybrid nanostructures exhibit high relaxivity in aqueous solution and can be uptaken efficiently by A549 cells. The intracellular MRI of the Fe3 O 4 NC/PAH/PSS/DOX hybrid nanostructures were then investigated by incubation of A549 cells with the hybrid nanostructures with different Fe3 O 4 concentrations. Figure 8 presents the T 2 -weighted MRI of A549 cells. With the increase of Fe3 O 4 concentration in Fe3 O 4 NC/PAH/PSS/DOX hybrid nanostructures, the cellular MRI signal increased gradually (Fig. 8). Currently, cell labeling is mainly accomplished by the endocytosis of Fe3 O 4 NC/PAH/PSS/DOX hybrid nanostructures as T 2 -negative contrast agents. These results demonstrate that the Fe3 O 4 NC/PAH/PSS/DOX hybrid nanostructures can be internalized into cells and exhibit good T 2 -weighted MRI contrast for cellular imaging. Our current research is limited to the cellular level. Future in vivo studies would be necessary for the practical application of the Fe3 O 4 NC/PAH/PSS/DOX hybrid nanostructures. To specially target a specific site in animal studies, small ligands such as lactic acid and folic acid (both containing carboxyl groups) would require to be used to conjugate amino-terminated Fe3 O 4 NC/PAH/PSS/DOX hybrid nanostructures.

T 2 -weighted cellular MR images of A549 cells incubated with the Fe3 O 4 NC/PAH/PSS/DOX hybrid nanostructures at a Fe concentration of 2.2, 4.5, 9.0, and 13.5 μM, respectively
Conclusion
The multifunctional Fe3 O 4 NC/PAH/PSS/DOX hybrid nanostructures were developed as the pH-triggered drug delivery system for effective cancer chemotherapy and MRI. The quasi-spherical Fe3 O 4 NCs can significantly improve the contrast ability of MRI compared with Fe3 O 4 NPs. The Fe3 O 4 NC/PAH/PSS/DOX hybrid nanostructures can act as contrast agents to enhance MRI and as a fluorescence probe for cell imaging. The DOX can be released from the Fe3 O 4 NC/PAH/PSS/DOX hybrid nanostructures at acidic environment and exhibit an excellent cellular cytotoxic effect on A549 cells. The Fe3 O 4 NC/PAH/PSS/DOX hybrid nanostructures as multifunctional theranostic platform have great potential for biomedical application, including MRI, fluorescence imaging, and stimuli-responsive drug delivery nanocarriers.
Availability of Data and Materials
Data sharing is not applicable to this article as no datasets were generated or analyzed during the current study. Please contact the author for data requests.
Abreviaturas
- 1/T 2 :
-
The proton transverse relaxation rates
- A549:
-
Human lung cancer
- DLS:
-
Dynamic light scattering
- DMSO:
-
Dimethyl sulfoxide
- DOX:
-
Doxorubicin hydrochloride
- FBS:
-
Fetal bovine serum
- Fe3 O 4 :
-
Iron oxide
- FOV:
-
Field of view
- LBL:
-
Layer-by-layer
- MRI:
-
Magnetic resonance imaging
- MTT:
-
Methyl thiazolyltetrazolium
- NA:
-
Number of averages
- NaOA:
-
Sodium oleate
- NaOH:
-
Sodium hydroxide
- NC:
-
Nanocluster
- NCs:
-
Nanoclusters
- NH4 F:
-
Ammonium fluoride
- NPs:
-
Nanoparticles
- OA:
-
Oleic acid
- OD:
-
Optical density
- ODE:
-
1-Octadecene
- PAH:
-
Poly(allylamine hydrochloride)
- PSS:
-
Poly(sodium 4-styrenesulfonate)
- S/O/W:
-
Solid-in-oil-in-water
- SDBS:
-
Sodium dodecyl benzene sulfonate
- TE:
-
Echo time
- TEM:
-
Microscopio electrónico de transmisión
- TR:
-
Repetition time
Nanomateriales
- Imágenes por resonancia magnética (IRM)
- Nanofibras y filamentos para una mejor administración de fármacos
- Administración de medicamentos basados en células para aplicaciones de cáncer
- Progreso en nanoestructuras basadas en óxidos de hierro para aplicaciones en almacenamiento de energía
- Nanotecnología:del sistema de imágenes in vivo a la administración controlada de fármacos
- Profundos efectos interfaciales en CoFe2O4 / Fe3O4 y Fe3O4 / CoFe2O4 Core / Shell Nanoparticles
- Comparación entre el ácido fólico y la funcionalización basada en péptidos gH625 de nanopartículas magnéticas de Fe3O4 para una internalización celular mejorada
- Agentes teranósticos de próxima generación basados en microcápsulas de polielectrolito codificadas con nanocristales semiconductores:desarrollo y caracterización funcional
- Anticuerpo monoclonal de heparanasa marcada con nanopartículas de oro magnético y su aplicación posterior para la obtención de imágenes por resonancia magnética tumoral
- La liberación de CpG con nanopartículas magnéticas de Fe3O4 modificadas inhibe el crecimiento tumoral y las metástasis pulmonares espontáneas para mejorar la inmunoterapia
- Los microrobots impresos en 3D son prometedores para la administración de medicamentos



