Administración de medicamentos basados en células para aplicaciones de cáncer
Resumen
La aplicación de células como portadores para encapsular fármacos de quimioterapia es de gran importancia en la terapia antitumoral. Las ventajas de reducir la toxicidad sistémica, mejorar la focalización y mejorar la penetrabilidad de los fármacos en las células tumorales hacen que tenga un gran potencial para su aplicación clínica en el futuro. Se han realizado muchos estudios y avances en la encapsulación de fármacos mediante el uso de eritrocitos, glóbulos blancos, plaquetas, células inmunes e incluso células tumorales. Los resultados mostraron que el efecto antitumoral de los fármacos de quimioterapia de encapsulación celular fue mejor que el de los fármacos de quimioterapia individuales. En los últimos años, la aplicación de vectores celulares en el cáncer se ha diversificado. Tanto los fármacos quimioterapéuticos como los fotosensibilizadores pueden encapsularse, para lograr múltiples efectos antitumorales de la quimioterapia, la terapia fototérmica y la terapia fotodinámica. Varias formas de tratamiento coordinado pueden producir resultados ideales incluso frente a tumores metastásicos y resistentes a múltiples fármacos. Sin embargo, es lamentable que esta tecnología solo se utilice in vitro por el momento. Aún no se han obtenido respuestas estándar para la preservación de células cargadas de fármaco y la forma segura de infusión en el cuerpo humano. Por lo tanto, la aplicación exitosa de la tecnología de administración de fármacos en la clínica aún enfrenta muchos desafíos en el futuro. En este artículo, discutimos el último desarrollo de diferentes sistemas de administración de fármacos derivados de células y los desafíos que enfrentará en el futuro.
Introducción
El cáncer sigue siendo una enfermedad insuperable en el campo de la medicina. La quimioterapia es el principal tratamiento para el cáncer. Sin embargo, la toxicidad sistémica y la resistencia a los fármacos que aportan los fármacos de quimioterapia provocan un aumento de la tasa de fracaso [1]. En los últimos años, los investigadores se han centrado en el estudio de la encapsulación de fármacos por células o nanopartículas (NP). La administración intravenosa de fármacos quimioterapéuticos tendrá grandes efectos secundarios en el cuerpo humano. Al mismo tiempo, muchos fármacos tienen poca penetración y dirección a las células tumorales. La escasa solubilidad en agua de los fármacos quimioterapéuticos también es un problema clínico común. Afortunadamente, la aparición de una nueva tecnología de carga de fármacos puede resolver estos problemas [2]. Los fármacos suelen infiltrarse en las células mediante el método hipotónico cuando se utilizan células para cargar fármacos. Sin embargo, el cambio de permeabilidad conducirá a la deformación de las células y reducirá la estabilidad de la membrana celular. La combinación de NP y células puede mejorar la encapsulación y liberación de fármacos, que se ha convertido en un tema de investigación candente en los últimos años [3, 4]. El aumento de la biocompatibilidad de las NP, la mejora de la capacidad de focalización del tumor y la prolongación de la circulación son las principales ventajas del vector derivado de células. Entre ellos, la mejora de la administración de fármacos dirigida se ha convertido en una preocupación importante [5]. Para resolver este problema, los investigadores modifican la superficie celular para mejorar la dirección de DDS al tejido tumoral, mejorar la concentración del fármaco en el tejido tumoral y finalmente lograr un efecto de inhibición tumoral eficaz [6]. Esta revisión presenta el desarrollo de la encapsulación de fármacos o NP con eritrocitos, plaquetas, células inmunes, células tumorales y células madre (Tabla 1) [7,8,9,10,11,12,13,14,15,16,17 , 18,19,20,21,22,23,24,25,26,27,28,29,30,31,32,33,34,35].
Eritrocito
Los eritrocitos se consideran una plataforma prometedora de administración de fármacos mediada por células debido a las ventajas inherentes de la biocompatibilidad, la larga vida útil y el fácil acceso [7, 36]. Inicialmente, los eritrocitos a menudo encapsulan fármacos directamente. Con el desarrollo de la investigación, aparecieron eritrocitos combinados con NP funcionales. Se ha logrado la transformación de la quimioterapia con un solo fármaco en terapia dirigida, inmunoterapia, terapia fototérmica (PTT), etc. La membrana de eritrocitos puede combinarse con NP de muchas formas. Sun y col. resumió varias tecnologías de portadores de membranas de eritrocitos construidas por métodos de unión covalente y no covalente que incluyen inserción de lípidos, puente biotina-avidina, acoplamiento EDC / NHS, conjugación anticuerpo / ligando-receptor y adsorción pasiva (Fig. 1) [36]. Wang y col. estudiaron la membrana híbrida de células cancerosas y eritrocitos para lograr la administración del fármaco. La membrana híbrida no solo tiene la capacidad de camuflarse inmunológicamente, sino que también tiene la capacidad de dirigirse al tumor [4]. La eficacia de administración de los NP terapéuticos basados en el direccionamiento pasivo del tumor depende en gran medida de la regulación adecuada del tiempo de circulación sanguínea o del microambiente del tumor. Con base en esta teoría, Sousa Junior et al. propuso un nuevo esquema de nanoportador magnetofluorescente camuflado (MMFn) por membrana de eritrocitos. El tiempo de circulación sanguínea del MMFn es de hasta 92 h, y tiene una alta eficiencia de transferencia, lo que se ha verificado en el modelo de tumor de ratón [8]. El desarrollo clínico objetivo de la vacuna contra el cáncer es limitado. Esto está relacionado con el alto nivel de expresión del ligando 1 de muerte programada (PD-L1) en las células tumorales, lo que conduce a las características inmunosupresoras del microambiente tumoral. La expresión de PD-L1 en células presentadoras de antígenos (APC) puede inducir células T reguladoras [37]. Por tanto, la combinación de anti-PD-L1 (aPD-L1) y vacuna contra el cáncer puede resultar beneficiosa. Los eritrocitos envejecidos tienen una capacidad única para atacar las células presentadoras de antígenos del bazo. Por tanto, la combinación del bloqueo de aPD-L1 con nano-eritrocitos puede provocar una reacción antigénica in vivo, que puede inhibir de forma válida el crecimiento tumoral y reducir la metástasis tumoral [9]. PTT es un nuevo método para el tratamiento de tumores, que tiene un gran potencial de desarrollo y se convertirá en un método importante para el tratamiento de tumores. Los NP de azul de Prusia (PB) con alta conversión fototérmica, azul fuerte, magnéticos, buena biocompatibilidad y estabilidad se consideran adecuados para el cáncer PTT. Sin embargo, el tiempo de retención en sangre de los PB NP es corto, lo que hace que su efecto antitumoral se reduzca considerablemente. El CD47 en la superficie de los eritrocitos es la proteína de autorreconocimiento del sistema reticuloendotelial in vivo, por lo que los nanomateriales recubiertos con eritrocitos pueden mejorar la capacidad de escape inmunológico y prolongar la vida media en la circulación. La membrana de eritrocitos se utilizó para mejorar la acumulación de fármaco de PB en el sitio del tumor [10]. Como nuevo sistema de administración de fármacos (DDS), el portador de vesículas extracelulares (EV) tiene las ventajas de seguridad, alta eficiencia y circulación prolongada. Sin embargo, las desventajas del bajo rendimiento, el alto costo y la heterogeneidad limitan la aplicación de EV [38]. La preparación de vesículas artificiales derivadas de membranas mediante fractura y autoensamblaje se ha convertido en una estrategia eficaz para superar el problema. El tamaño y la uniformidad de las vesículas mímicas multifuncionales derivadas de los glóbulos rojos pueden controlarse bien. Los investigadores utilizaron vesículas mímicas derivadas de eritrocitos (MV) cargadas con ARNip de glicoproteína P (P-gp) y doxorrubicina (DOX) para el tratamiento dirigido de tumores resistentes a múltiples fármacos. Este DDS basado en MV proporciona una nueva dirección para la terapia dirigida colaborativa del tumor [11]. La plataforma de transporte derivada de eritrocitos puede diseñarse mediante operación mecánica, lo que puede hacer que el diámetro sea de micrómetro a nano. Los resultados de la investigación indican que la dinámica de circulación en tiempo real del vector de eritrocitos está relacionada con su diámetro. Los investigadores diseñaron un portador óptico de micro y nanoeritrocitos basado en imágenes de fluorescencia en tiempo real de partículas en el sistema vascular subcutáneo de ratones sanos y estudiaron la dinámica de la circulación. El resultado sugiere que la vida media de emisión promedio de los micro y nanoportadores en los vasos sanguíneos fue de ~ 49 min y 15 min, respectivamente. Después de 7 días, la segunda inyección de partículas aumentó la vida media de emisión promedio del portador de tamaño micro a 1 h, y la vida media variable de los nanoportadores osciló entre 25 y 60 min [39]. La fosfatidilserina expuesta en la superficie del portador es un mecanismo importante para su eliminación de la circulación [40]. La vida media de emisión de los NP en sangre es más corta después de la primera inyección, lo que indica que los macrófagos pueden ser más efectivos para eliminar estas partículas cuando están mediados por el mecanismo de exposición de la superficie a la fosfatidilserina. Las características de forma y deformación de los portadores de tamaño micro contribuyen al tiempo de ciclo de estas partículas. Estas características bioquímicas y biomecánicas son factores importantes para la traducción segura y eficaz de la plataforma derivada de glóbulos rojos [39]. Por tanto, esta serie de resultados de investigación muestran que es necesario realizar una investigación más detallada sobre vectores derivados de eritrocitos. Solo de esta manera, podemos comprender el mecanismo del portador que actúa sobre la enfermedad y utilizar estos mecanismos para diseñar un mejor portador derivado de eritrocitos.
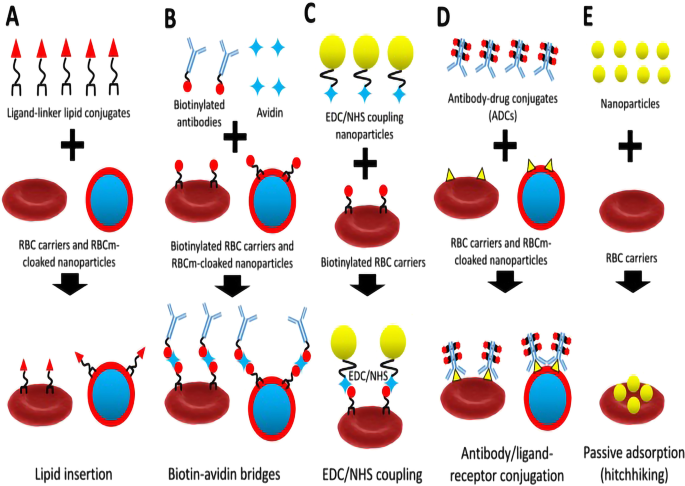
Reproducido con permiso de Ref. [30]. Copyright © 2019, Teranósticos
Diagrama esquemático del método de unión entre la membrana de eritrocitos y las NP ( A ), puentes biotina-avidina ( B ), Acoplamiento EDC / NHS ( C ), conjugación anticuerpo / ligando-receptor ( D ) y adsorción pasiva (autostop) ( E ) métodos para la refuncionalización de la nanomedicina basada en eritrocitos.
Plaqueta
Las plaquetas son un tipo de glóbulo sin núcleo. La vida útil de las plaquetas es de unos 8 a 10 días. En comparación con el tiempo de circulación prolongado de los eritrocitos durante cuatro meses, el tiempo de circulación adecuado de las plaquetas puede evitar la acumulación innecesaria in vivo [41]. La proteína de membrana CD47 de las plaquetas puede enviar una señal de "no me comas" a los macrófagos para evitar la fagocitosis por los macrófagos. Por lo tanto, se espera que el DDS biomimético de plaquetas mejore el escape de macrófagos in vivo y mejore la retención en el tejido tumoral [17]. Los estudios han indicado que las plaquetas desempeñan un papel importante en la promoción de la proliferación de células tumorales, la integridad vascular del tumor y la invasión de las células tumorales debido a sus múltiples reguladores angiogénicos. Las micropartículas derivadas de plaquetas (P-MP), como el factor de crecimiento endotelial vascular (VEGF), la metaloproteinasa de matriz (MMP), el factor de crecimiento epidérmico (EGF) y el factor de crecimiento derivado de plaquetas (PDGF), pueden inducir la activación de MAPK y AKT vías de señalización en las células tumorales, a fin de estimular la sobreexpresión de las proteínas necesarias para la proliferación de las células tumorales [42]. La agregación plaquetaria está relacionada con las células tumorales circulantes (CTC). Además, las plaquetas pueden prevenir la extravasación vascular de CTC mejorando la adhesión entre las plaquetas y las células endoteliales. Más importante aún, las plaquetas pueden proteger a la CTC de la vigilancia inmunológica de las células asesinas naturales. Por lo tanto, es prometedor establecer DDS basado en la membrana plaquetaria utilizando la ventaja de dirigir las plaquetas a las células tumorales. El método habitual de preparación de la membrana plaquetaria es la ecografía y la congelación-descongelación repetida [41]. En un estudio anterior sobre NP encapsuladas en plaquetas, Hu et al. demostró que las plaquetas pueden encapsular NP cargadas de forma eficaz. El vector derivado de plaquetas tiene una gran capacidad para dirigirse a los vasos sanguíneos lesionados y los tumores y desempeña un buen papel terapéutico en la enfermedad [43]. Liu y col. desarrolló un portador de fármaco híbrido de lípidos y membrana plaquetaria sensible al pH para la administración dirigida a tumores. El sistema de plataforma de carga de fármacos mostró una vida media en plasma más prolongada y una mayor acumulación de tumores cuando la doxorrubicina se activa y se libera en modelos de tumores de ratón. Este resultado es superior al del liposoma tradicional sensible al pH (Fig. 2) [18]. El DDS plaquetario combina fármacos inmunoterapéuticos con agentes fototérmicos. En la última investigación, el DDS plaquetario combina fármacos inmunoterapéuticos con fármacos fototérmicos. Las plaquetas modificadas con fármacos se reclutan en el sitio del tumor para activar aún más la respuesta inmune anticancerosa, inhibir el crecimiento del tumor residual y mejorar la tasa de supervivencia. Esto se debe a inflamación y lesión en el sitio del tumor después de la ablación térmica [19]. Las investigaciones existentes sobre nanoportadores derivados de plaquetas muestran que el DDS mediado por plaquetas tiene amplias perspectivas.
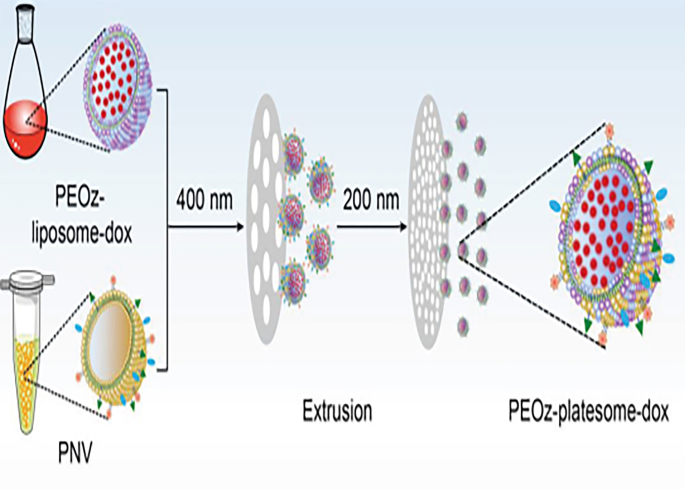
Reproducido con permiso de Ref. [14]. Derechos de autor © 2019, Wiley
Ilustración esquemática de la preparación de PEOz-plateome-dox. PEOz-plateome-dox se generó por coextrusión de PEOz-liposome-dox y PNV.
Célula inmunológica
En la actualidad, muchas personas se centran en la modificación de la superficie de los portadores de NP para adaptarse al entorno biológico y la complejidad. Sin embargo, el sistema de fagos mononucleares tiene la capacidad de reconocer y aislar sustancias extrañas, lo que conduce a la disminución de la concentración del fármaco en el sitio del tumor [25]. Los NP también pueden administrar fármacos a áreas tumorales de acuerdo con una mayor permeabilidad y retención, pero la permeabilidad de los vasos tumorales a menudo se ve afectada por anomalías estructurales vasculares y heterogeneidad del suministro de sangre. Otra razón que debemos considerar es que el tamaño y la carga de los NP también afectan la cantidad de ellos que ingresan al tumor. Por ejemplo, los NP de más de 100 nm de diámetro pueden ser fagocitados por macrófagos o filtrados por el hígado [22]. Por lo tanto, la existencia de estos factores a menudo conduce a que los NP no puedan ingresar al sitio del tumor de manera eficiente. Las células inmunes desempeñan un papel importante en el direccionamiento tumoral y la prevención de la difusión del fármaco a los tejidos normales. Los macrófagos se convierten en uno de los portadores de fármacos ideales para el DDS debido a su capacidad fagocítica natural, barrera sanguínea y quimiotaxis para tumores sólidos. Las NP encapsuladas por macrófagos mejorarán la permeabilidad de las NP al tejido tumoral. Y el efecto antitumoral aumentará aún más cuando los fármacos antitumorales se combinen con terapia fototérmica, lo que se ha confirmado en una determinada investigación (fig. 3) [23]. Se considera que los monocitos son precursores de los macrófagos, con capacidad de fagocitosis, eliminación de células lesionadas y participación en la respuesta inmunitaria. Además, los monocitos son las células más grandes de la sangre, lo que facilita la carga de NP terapéuticas. Se diferenciarán en macrófagos cuando se recluten monocitos en el sitio del tumor. Las NP encapsuladas por macrófagos luego migrarán y serán quimiotácticas al área anóxica del tumor [24, 44].
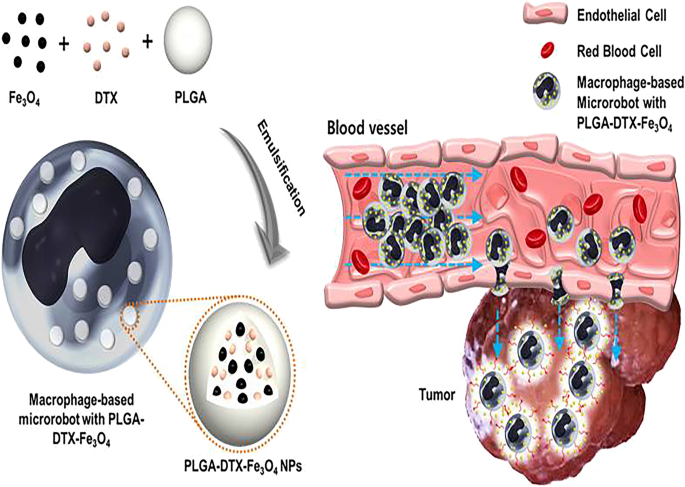
Reproducido con permiso de Ref. [20]. Derechos de autor © 2016, Sci Rep
Diagrama esquemático del microrobot basado en macrófagos con PLGA-DTX-Fe 3 O 4 (izquierda). Describa la orientación y el tratamiento de los tumores en el entorno in vivo (derecha).
Los linfocitos T citotóxicos (CTL), una subdivisión de los glóbulos blancos, son células T específicas que secretan varias citocinas para participar en la función inmunológica. Tiene un efecto letal sobre virus y células tumorales y forma una importante línea de defensa contra virus y tumores junto con las células asesinas naturales. CTL, también conocido como linfocito T asesino, es una parte importante del cuerpo antitumoral y una de las células de efecto principal de la inmunoterapia tumoral. Tiene un tiempo de circulación sanguíneo prolongado y una alta expresión de moléculas de adhesión. Por lo tanto, CTL tiene la capacidad de reclutar y localizar los sitios del tumor. Todas estas ventajas sientan las bases para el tratamiento de tumores con NP derivadas de CTL [26].
Los leucocitos son un tipo de células sanguíneas incoloras, esféricas y nucleadas. El número total de leucocitos en adultos normales fue (4.0-10.0) × 10 9 / L [45]. Cuando ocurre la inflamación, los leucocitos se activan para combatir bacterias o virus, lo cual es una manifestación de su importante papel en el sistema inmunológico. Los leucocitos participan en diversas reacciones inmunes, interacciones celulares y tienen la capacidad de migrar [46]. Son portadores ideales de fármacos quimioterapéuticos y factores reguladores del microambiente tumoral (TEM), que se deben principalmente a las características de localización de los leucocitos en sitios inflamatorios y tumorales. Roberto Molinaro y col. utilizó las características de orientación de los leucocitos a los vasos sanguíneos relacionados con tumores con inflamación para administrar DOX a modelos de ratón con cáncer de mama y melanoma de manera efectiva. Los resultados mostraron que los leucocitos cargados con DOX mostraron una actividad antitumoral más fuerte para reducir el volumen del tumor y prolongar el tiempo de supervivencia [27, 47]. Los neutrófilos son el tipo más abundante de leucocitos, y representan 40 a 75% del número total de leucocitos. Además, los neutrófilos son el primer tipo de células que llegan al lugar de la inflamación. La acumulación de DDS mediada por neutrófilos en el sitio del tumor aumenta aún más cuando la terapia fototérmica desencadena la inflamación del sitio del tumor [48]. En las enfermedades no cancerosas, las características de migración de los neutrófilos también proporcionan una nueva idea para el tratamiento de la enfermedad. Las investigaciones muestran que los neutrófilos pueden transportar selectivamente liposomas cRGD como portadores de células, cuando ocurre isquemia cerebral. Por tanto, los neutrófilos penetran en la barrera hematoencefálica y penetran en el parénquima cerebral y, finalmente, administran el fármaco en el lugar que necesita tratamiento [49]. Las CTC en la sangre proliferan fácilmente y forman metástasis en órganos anatómicamente distantes. Sin embargo, es difícil ser una terapia dirigida debido al estado circulatorio y la baja concentración de CTC. Afortunadamente, son fáciles de recolectar cerca de las células endoteliales, lo que es similar a las características de migración de los glóbulos blancos. La razón principal es que la CTC es similar a los leucocitos en volumen y forma, por lo que también está rodeada por la pared celular endotelial cuando fluye la sangre. Este tipo de fenómeno de borde puede rodear al CTC en los glóbulos blancos de manera efectiva. En otras palabras, los leucocitos también son vectores terapéuticos potenciales para la CTC [50].
La célula asesina natural (NK) es una célula inmunitaria importante en el cuerpo, que no solo está relacionada con la infección antitumoral, antivirus y la regulación inmunológica, sino que también está involucrada en reacciones de hipersensibilidad y enfermedades autoinmunes en algunos casos. NK puede reconocer células diana y medios de destrucción. A diferencia de las células T y B, es un tipo de linfocito que puede destruir células tumorales y células infectadas por virus sin sensibilización previa [51]. Deng y col. encontraron que las NP derivadas de NK tienen un efecto dirigido sobre el tumor según el análisis proteómico de la membrana de las células NK. Es más satisfactorio que las células NK también puedan inducir o potenciar la polarización de macrófagos M1 proinflamatorios, produciendo así inmunidad antitumoral. Apoyado por esta teoría, Deng y otros investigadores encapsularon agentes fotodinámicos en células NK. El resultado mostró que el DDS de células NK mostró un fuerte efecto inmunoterapéutico en el proceso antitumoral. No solo puede inhibir eficazmente el crecimiento del tumor primario, sino que también tiene un efecto inhibidor obvio sobre el tumor distante [28].
Célula cancerosa
La capacidad infinita de las células cancerosas para replicarse es una molestia, pero la capacidad de las células cancerosas para resistir la muerte celular les permite superar el aclaramiento inmunológico [30]. Las células cancerosas que expresan moléculas de adhesión a la superficie, como moléculas de adhesión de células epiteliales, n-cadherina y galectina-3, tienen dominios de adhesión homólogos, que pueden promover la aparición de agregación multicelular. La capacidad de unirse de forma homóloga a proteínas de membrana conduce al uso de células cancerosas para la funcionalización de la superficie de las NP. Chen y col. usó la membrana de la célula cancerosa para encapsular el núcleo de ICG (verde de indocianina) / poli (ácido láctico coglicólico) (PLGA) y la capa de la membrana de la célula cancerosa para lograr la focalización sincrónica y el tratamiento del tumor. Los resultados mostraron que este método no solo tenía un alto efecto de direccionamiento homólogo a nivel celular, sino que también tenía una resolución espacial superior y una penetración profunda a nivel animal (Fig. 4) [29]. Los estudios han demostrado que las mitocondrias juegan un papel importante en la regulación de la proliferación de células cancerosas. El inicio de la apoptosis en las mitocondrias conduce a la liberación de citocinas como el citocromo c, que conduce a una cascada de actividad citosólica y muerte celular [52]. La mitocondria también está estrechamente relacionada con la resistencia a múltiples fármacos (MDR) del cáncer [53]. La intervención dirigida a las mitocondrias se convertirá en una estrategia prometedora para el tratamiento del cáncer. La acumulación de fármacos dirigidos a las mitocondrias puede desencadenar la vía de la apoptosis mitocondrial, que conduce a la muerte celular programada y al suicidio de las células cancerosas. Los estudios han demostrado que los óxidos metálicos como el zinc, el cobre y la ceria pueden inhibir la proliferación de células cancerosas en una variedad de líneas de células cancerosas a través de este mecanismo. Por tanto, algunos investigadores han desarrollado nanopartículas dirigidas a las mitocondrias. Por ejemplo, NP de CuO dopado con Zn (TPP-ZC-IR-PNP) y cocargado con el sistema de docetaxel y lonidamina (cl-M / DL) estudiado por Ruttala et al. Todos ellos tienen una gran capacidad de focalización y un efecto terapéutico en la terapia tumoral [52, 54].
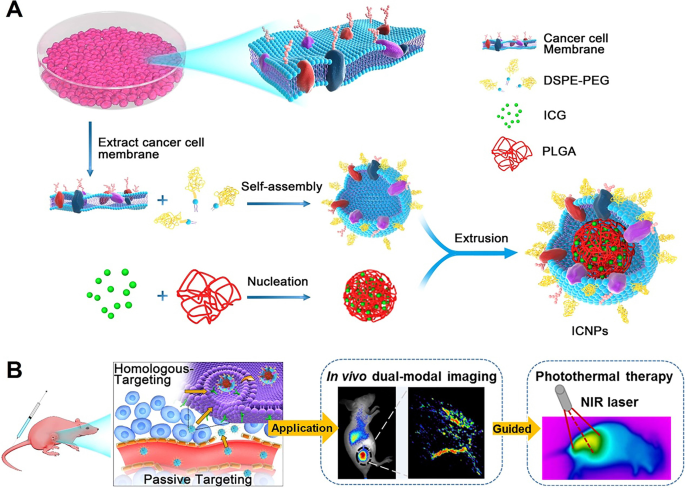
Reproducido con permiso de Ref. [24]. Copyright © 2016, Publicación ACS
Ilustración de los NP biomiméticos de la membrana de la célula cancerosa para el reconocimiento de objetivos de la célula cancerosa de origen, la obtención de imágenes de modalidad dual y la terapia fototérmica. ( A ) Procedimiento de preparación de las ICNP. Extracción de la membrana celular MCF-7 del cáncer hibridada con fosfolípidos PEGilados (DSPE-PEG) y luego recubierta sobre núcleos poliméricos cargados con ICG por extrusión. ( B ) Esquema de las ICNP dirigidas homólogas para la terapia fototérmica guiada por imágenes de modalidad dual. A través de la focalización homóloga específica y el efecto EPR (focalización pasiva), las ICNP lograron una acumulación de tumores perfecta, imágenes de FL / PA de dos modos y una terapia fototérmica eficaz después de la inyección intravenosa.
Célula madre
El tumor puede emitir quimiocinas para reclutar células madre mesenquimales (MSC) para formar una matriz de soporte para el crecimiento tumoral [55]. MSC es un tipo de célula madre pluripotente, que tiene la capacidad de autorrenovación, diferenciación multidireccional y regulación de la respuesta inmunitaria. Se aisló con éxito del cerebro, pulmón, hígado, riñón, sangre del cordón umbilical, placenta y otros tejidos. Se especula que las CMM pueden migrar al sitio de la lesión o inflamación y reparar la lesión produciendo células específicas de tejido y / o liberando factores paracrinos. Las MSC también pueden secretar moléculas solubles inmunomoduladoras para regular la inmunidad y se utilizan principalmente en el tratamiento de la enfermedad de Crohn, insuficiencia hepática, fibrosis y otras enfermedades. La presencia de CMM en el microambiente de los tumores malignos es útil para el crecimiento tumoral y la metástasis [56]. Sin embargo, algunos estudios han demostrado que las CMM derivadas del cordón umbilical pueden inhibir el crecimiento de células cancerosas de páncreas en ratones [57, 58]. Las MSC pueden transducir eficazmente adenovirus, lentivirus, retrovirus de ratón y otros vectores virales importantes. Las CMM transformadas y modificadas genéticamente pueden expandirse ampliamente in vitro, lo que las convierte en el vector ideal de transferencia génica [59]. La formación de un tumor requiere nuevas células para sustentarlo, al igual que el tejido en desarrollo o dañado. La migración de las CMM al tejido tumoral hace que sea ampliamente utilizado como portador de fármacos antitumorales. Stefania Lenna y col. han logrado logros en la inhibición del crecimiento del osteosarcoma basados en la tecnología fotodinámica de las CMM cargadas con NP. Prepararon NP de polidopamina acopladas con cloro e6 (Ce6) (PDA-Ce6) y se cargaron en MSC. Las MSC cargadas con PDA-Ce6 (MSC-PDA-Ce6) pueden apuntar y penetrar en el tumor. Vale la pena mencionar que la tasa de liberación efectiva es de hasta el 60% en 72 h. MSC-PDA-Ce6 es un transporte similar a un "caballo de Troya" a través del proceso de endocitosis-exocitosis-endocitosis entre las CMM y las células cancerosas. Lo que es más gratificante es que puede haber un cierto grado de esperanza incluso frente a pequeños tumores inoperables o pacientes resistentes a los fármacos [33]. Asimismo, tiene un buen efecto en el tratamiento del melanoma [34].
Desarrollo
Las proteínas en la superficie de la membrana retienen la función biológica de la tecnología de administración de fármacos mediada por células en células. Como se mencionó anteriormente, muchos estudios han demostrado que la administración de fármacos a base de células mejora la biocompatibilidad, la capacidad de focalización y la capacidad de escape inmunológico, reduce los efectos secundarios tóxicos y previene la formación de corona proteica. Todas estas ventajas evitan y reducen la complejidad en la preparación de NP [55]. La nanotecnología se ha estudiado ampliamente en el campo de la medicina debido a sus ventajas de fácil funcionalización de la superficie, diseño controlable y reducción de los efectos secundarios de los medicamentos. El diámetro de las NP utilizadas en los estudios es similar al de las bacterias, virus y otros patógenos, generalmente alrededor de 100 nm, por lo que el mecanismo de depuración del sistema reticuloendotelial in vivo es fácil de activar. Las NP derivadas de células reducen en gran medida la estimulación de los macrófagos para liberar citocinas [60]. Un problema grave de los NP es que entrarán en contacto con las proteínas plasmáticas cuando ingresen al sistema sanguíneo. Las proteínas plasmáticas adsorbidas en la superficie de las NP forman una corona proteica que afecta la interacción entre las NP y los componentes sanguíneos, conduce además a un aumento de la activación celular y puede conducir a la coagulación o incluso a la trombosis eventualmente [61]. Por lo tanto, la combinación de NP y células ofrece una nueva perspectiva para la aplicación clínica de DDS. El progreso del DDS también se refleja en la combinación de tratamiento y diagnóstico. La adición de ICG y otros tintes fluorescentes con efecto fototérmico facilita el seguimiento de los rastros de fármacos en el proceso de las células antitumorales. Al mismo tiempo, también es conveniente para la formación de imágenes de tumores y fácil de evaluar el efecto terapéutico [62]. Desafortunadamente, la tecnología actual de administración de fármacos celulares solo se utiliza para la investigación preclínica in vitro. No se prevé si los cambios en la composición de la membrana celular y la modificación de la superficie conducirán a una respuesta inmune cuando se utilice la tecnología de administración de fármacos en el cuerpo humano. No está claro si el fármaco puede liberarse en el cuerpo a tiempo para producir citotoxicidad y si la degradación de los NP en el cuerpo afectará la salud humana. Estos problemas conducirán a un mayor estudio de los DDS basados en células [63].
Conclusiones
En comparación con la quimioterapia sola, el DDS basado en células tiene las ventajas de mejorar la biocompatibilidad, mejorar el escape inmunológico, la circulación prolongada y mejorar la focalización. Al mismo tiempo, la encapsulación de fotosensibilizadores, fármacos de quimioterapia y otros reactivos en el portador puede promover el tratamiento cooperativo del tumor. Los eritrocitos, plaquetas, leucocitos y otras células del DDS se han estudiado ampliamente y se han obtenido muchos resultados. En la actualidad, la investigación sobre la combinación de células sanguíneas y NP es la más. Los NP tienen las ventajas de una permeabilidad mejorada y un efecto de retención (EPR), una alta eficiencia de carga de fármacos y cierta capacidad de focalización, que tienen claros beneficios para la terapia tumoral.
Disponibilidad de datos y materiales
No aplica.
Abreviaturas
- NP:
-
Nanopartículas
- PTT:
-
Terapia fototérmica
- MMFn:
-
Nanoportador magnetofluorescente
- PD-L1:
-
Ligando-1 de muerte programada
- APC:
-
Célula presentadora de antígenos
- PB:
-
Azul de Prusia
- DDS:
-
Sistema de administración de fármacos
- EV:
-
Vesícula extracelular
- MV:
-
Vesículas mímicas
- P-gp:
-
Glicoproteína P
- DOX:
-
Doxorrubicina
- P-MPs:
-
Micropartículas derivadas de plaquetas
- VEGF:
-
Factor de crecimiento endotelial vascular
- MMP:
-
Metaloproteinasa de matriz
- EGF:
-
Factor de crecimiento epidérmico
- PDGF:
-
Factor de crecimiento derivado de plaquetas
- CTC:
-
Células tumorales circulantes
- CTL:
-
Linfocitos T citotóxicos
- TEM:
-
Microambiente tumoral
- NK:
-
Célula asesina natural
- MDR:
-
Resistencia a múltiples fármacos
- TPP-ZC-IR-PNP:
-
NP de CuO dopadas con Zn
- cl-M / DL:
-
Cocargado con docetaxel y lonidamina
- MSC:
-
Células madre mesenquimales
- Ce6:
-
Cloro e6
- PDA:
-
Polidopamina
- ICG:
-
Verde de indocianina
- EPR:
-
Efecto de retención y permeabilidad mejorada
Nanomateriales
- Nanofibras y filamentos para una mejor administración de fármacos
- Nanoárboles para células solares sensibilizadas con colorante
- Nanoheterouniones para células solares
- Demostración de un biosensor flexible basado en grafeno para la detección rápida y sensible de células de cáncer de ovario
- Marcos metal-orgánicos sensibles al medio ambiente como sistema de administración de fármacos para la terapia tumoral
- Pez cebra:un sistema modelo en tiempo real prometedor para la administración de fármacos neuroespecíficos mediada por nanotecnología
- Las nanotecnologías desactivan las células madre cancerosas
- Nanopartículas de lípidos de PLGA trazadas con 131I como portadores de administración de fármacos para el tratamiento quimioterapéutico dirigido del melanoma
- La administración de ADN tetraedro mejora la apoptosis inducida por doxorrubicina de las células de cáncer de colon HT-29
- Nanoportadores basados en lípidos y nucleósidos para la administración de sorafenib
- Los microrobots impresos en 3D son prometedores para la administración de medicamentos



