Progreso en nanoestructuras basadas en óxidos de hierro para aplicaciones en almacenamiento de energía
Resumen
La demanda de dispositivos de almacenamiento de energía ecológicos y eficientes en la vida diaria aumenta constantemente, lo que es causado por el medio ambiente mundial y los problemas energéticos. Las baterías de iones de litio (LIB), un tipo importante de dispositivos de almacenamiento de energía, están atrayendo mucha atención. El grafito se utiliza como ánodo LIBs, sin embargo, su capacidad teórica es baja, por lo que es necesario desarrollar ánodo LIBs con mayor capacidad. En esta revisión se resumen las estrategias de aplicación y los avances de la investigación de los óxidos de hierro novedosos y sus compuestos como ánodo LIB en los últimos años. Aquí enumeramos varios métodos de síntesis típicos para obtener una variedad de nanoestructuras basadas en óxidos de hierro, tales como deposición en fase gaseosa, coprecipitación, método electroquímico, etc. Para la caracterización de nanoestructuras basadas en óxidos de hierro, especialmente la difracción de rayos X in-situ. y 57 Se elaboran espectroscopía de Fe Mössbauer. Además, se discuten y resumen las aplicaciones electroquímicas de nanoestructuras basadas en óxidos de hierro y sus compuestos.
Resumen gráfico
Introducción
Los problemas mundiales de energía y medio ambiente conducen a una creciente demanda de energía verde altamente eficiente, por ejemplo, energía solar, pilas de combustible, baterías de iones de litio (LIB) y módulos termoeléctricos, etc. [1,2,3,4,5,6, 7,8,9,10,11]. La investigación y el desarrollo de un sistema de almacenamiento de energía de alto rendimiento y bajo costo es una solución importante para estos problemas. Entre los dispositivos de almacenamiento de energía con amplias aplicaciones, los LIB son candidatos importantes para un sistema de almacenamiento de energía altamente eficaz [12,13,14,15,16,17,18,19,20,21,22,23,24]. Sin embargo, el ánodo de grafito comercial actual tiene las limitaciones, por ejemplo, una capacidad teórica relativamente baja (372 mA h g −1 ), y se propone aplicar algunos materiales electroquímicamente activos en LIB [25,26,27,28,29]. En 2000, Poizot et al. [30] informó que los óxidos de metales de transición (TMO) se consideran un tipo de ánodos importantes en los LIB debido a sus altas capacidades teóricas de 2 a 3 veces la del grafito. Por lo tanto, los TMO y los compuestos relacionados están atrayendo mucha atención como ánodo LIB. Durante el proceso de inserción / extracción de litio, los TMO tienen la siguiente reacción [31].
$$ {\ text {M}} _ {x} {\ text {O}} _ {y} + 2y {\ text {e}} ^ {-} + 2y {\ text {Li}} ^ {+} \ leftrightarrow x {\ text {M}} ^ {0} + y {\ text {Li}} _ {2} {\ text {O}} $$ (1)donde, M representan Ni, Cu, Fe, Co, etc. Durante el proceso de inserción de litio, estos óxidos son reducidos por litio, y el compuesto que consiste en racimos metálicos dispersos en una matriz de Li 2 amorfo O se forma [30, 31].
Entre los TMO, los ánodos basados en óxidos de hierro son un tipo de candidatos excelentes con un gran potencial en los LIB ya que poseen tales ventajas, por ejemplo, abundancia, bajo costo y no toxicidad [32, 33]. Sin embargo, al igual que otros TMO, los óxidos de hierro que sirven como ánodo LIB tienen dos problemas críticos. Uno es la gran capacidad irreversible, causada por la descomposición del electrolito y la formación de una capa de interfaz de electrolito sólido (SEI) en el primer proceso de descarga. Además, la formación de Fe y Li 2 O es termodinámicamente factible y la extracción de iones de litio (Li + ) de Li 2 O es termodinámicamente inestable [34], ya que una parte de Li + no se puede extraer de Li 2 O formado en el primer proceso de descarga. Esto también da como resultado una capacidad irreversible parcial. Otro problema es su baja estabilidad cíclica como resultado principalmente de una gran variación de volumen y una agregación severa de Fe en la inserción / desinserción de Li + , lo que conduce a la pulverización de los electrodos y al rápido deterioro de la capacidad [3]. Para solucionar estos problemas, se está centrando un gran esfuerzo en superar estos problemas y se proponen algunos enfoques muy eficaces. Hasta donde sabemos, una estrategia muy eficaz es la nanoestructuración de óxidos de hierro [3, 35]. Para algunas nanoestructuras únicas, la variación de tensión y volumen resultó de la inserción / desinserción de Li + se inhibirá en gran medida, también el Li + se puede difundir fácilmente en los electrodos, lo que mejora significativamente el rendimiento electroquímico del ánodo [11]. Además, se introducen materiales carbonosos, por ejemplo, fibras de carbono (CF), nanotubos de carbono (CNT), grafeno y carbono pirolizado, etc., para su composición con óxidos de hierro [36,37,38]. La variación de volumen de los electrodos compuestos en carga / descarga puede ser amortiguada por estos materiales carbonosos con estructuras únicas, por lo tanto, el contacto electrónico y la estabilidad cíclica de las nanoestructuras de óxidos de hierro aumentan.
En esta revisión, las estrategias desarrolladas recientemente y las actualizaciones importantes de la investigación sobre los óxidos de hierro (Fe 1− x O, Fe 2 O 3 , Fe 3 O 4 ) se elaboran y resumen nanoestructuras basadas en aplicaciones en LIB y supercondensadores. Específicamente, nos concentramos en la síntesis y el diseño de la nanoestructura basada en óxidos de hierro, así como en su desempeño electroquímico.
Wustite (Fe 1− x O)
Wustita (Fe 1− x O) es un compuesto no estequiométrico con 0 < x <0,0464 [11]. Tiene la estructura cúbica de sal de roca y su constante de celosía es ~ 4.330 Å [11]. Fe 1− x O, en comparación con Fe 2 O 3 y Fe 3 O 4 , tiene menos aplicaciones en almacenamiento de energía ya que su capacidad específica relativamente baja y su fase metaestable por debajo de 843.15 K tiende a descomponerse en Fe y Fe 3 O 4 . Sin embargo, Fe 1− x O, un ánodo muy prometedor para LIB, tiene una conductividad eléctrica más alta que los de Fe 2 O 3 y Fe 3 O 4 .
Síntesis y caracterización
Hasta donde sabemos, la composición de TMO con cobertura de alto rendimiento tiene un gran potencial para el ánodo LIB de alto rendimiento [7]. En LIB, el mecanismo electroquímico del ánodo de wustita se describe como la siguiente ecuación [8].
$$ {\ text {FeO}} + 2 {\ text {Li}} ^ {+} + 2 {\ text {e}} ^ {-} \ leftrightarrow {\ text {Fe}} + {\ text {Li }} _ {2} {\ text {O}} $$ (2)Los compuestos de FeO / C se sintetizaron utilizando un método sencillo de Gao et al. [31]. En su síntesis, α-Fe 2 O 3 Se mezclaron partículas con un tamaño de 30-120 nm con negro de acetileno (AB) de diferentes porcentajes y se obtuvo una mezcla uniforme mediante molienda de bolas. Luego, la mezcla de α-Fe 2 O 3 y AB se redujo térmicamente con carbón a 800 ° C durante 10 h en N 2 atmósfera para obtener compuestos de FeO / C uniformes. El compuesto FeO / C posee una estabilidad cíclica mucho mayor que la del Fe 2 O 3 / AB mezcla. Cuando el contenido de AB es 50% en peso, la capacidad del compuesto FeO / C es 511 mA h g −1 , superior a 396 mA h g −1 de Fe 2 O 3 / AB. Además, la capacidad de retención después de 50 ciclos es> 96%, obviamente un 70-80% más alta que la del Fe 2 O 3 / AB. Es creíble que el rendimiento electroquímico superior del compuesto FeO / C sea el resultado de su conductividad eléctrica más alta, resultado de la conexión reforzada de las partículas de FeO y AB después de la reducción carbono-térmica.
Posteriormente, en 2016, Jung et al. [11] preparó un compuesto de potasio (K) -FeO / grafeno como ánodo LIBs basado en nanopartículas de FeO dopadas con K mediante difusión térmica de K en Fe 2 O 3 / grafeno mediante reducción de poliol. Fe romboédrico 2 O 3 Los cristales se transformaron en cristales de FeO (cúbicos centrados en las caras, FCC), que muestran un amplio espaciado d (5,2 Å) de (111) planos cristalinos, mediante la calcinación de Fe 2 dopado con K O 3 / grafeno. Comparando con Fe 2 previamente estudiado O 3 / compuesto de grafeno [11], el K-FeO / grafeno mostró una capacidad de descarga de 1776 mA h g −1 con alta estabilidad cíclica durante 50 ciclos a una densidad de corriente de 100 mA g −1 , mientras que Fe 2 O 3 / grafeno entregó una capacidad de descarga de 1569 mA h g −1 . Incluso a una alta densidad de corriente de 18,56 A g −1 , la capacidad de K-FeO / grafeno se mantuvo en 851 mA h g −1 después de 800 ciclos. Esta diferencia es mucho mayor después de que los electrodos se ciclan durante más tiempo a una alta densidad de corriente de 18,56 A g −1 . Como se muestra en la Fig.1, en comparación con el Fe 2 O 3 / grafeno, el ánodo de K-FeO / grafeno tiene una estructura cristalina y un mecanismo de reacción únicos. La alta capacidad de descarga de K-FeO / grafeno indica esa capacidad específica mediante el almacenamiento de Li + adicional debe aportarse desde las vacantes y el amplio espaciado d dentro de las celosías de Wustite a través de la difusión de potasio en Fe 2 O 3 celosías.
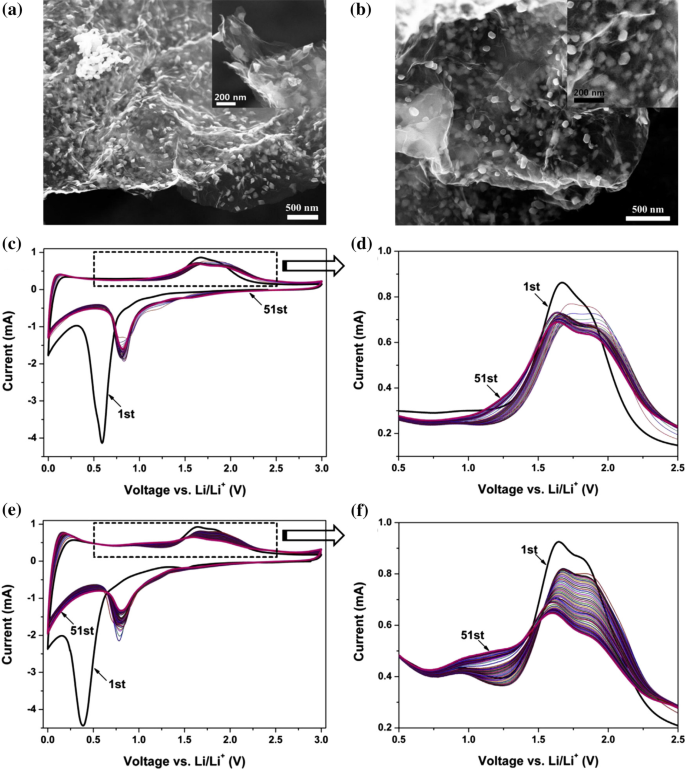
Reproducido con permiso de [11]. Derechos de autor, Elsevier B.V
Imágenes SEM de a Fe 2 O 3 / grafeno y b K-FeO / grafeno y el recuadro en ( a , b ) son sus imágenes ampliadas, respectivamente. Voltamogramas cíclicos repetidos de c , d el Fe 2 O 3 / electrodo de grafeno y e , f el electrodo de K-FeO / grafeno. Se escanearon continuamente dos electrodos para los ciclos 51 con una tasa de barrido potencial de 0,5 mV s −1 .
Difracción de rayos X in situ
Mediante difracción de rayos X in situ (XRD), la información del cambio estructural en tiempo real durante el proceso de reacción de la muestra y una gran cantidad de información comparable se puede obtener en un período corto. No solo puede observar el cambio estructural de la muestra durante el proceso de síntesis, también se puede utilizar para detectar el cambio estructural correspondiente de la muestra a diferentes temperaturas bajo carga / descarga a un cierto potencial, lo cual es muy útil para monitorear el mecanismo de reacción real. de ánodo / cátodo en batería. Además, nuestro grupo estudió el conocimiento preciso de la constante de celosía de la wustita que se requiere para la investigación de sus propiedades físicas y químicas a alta temperatura. El Fe 1− x O fue sintetizado y caracterizado por difractómetro de rayos X de alta temperatura (RINT2000-TTR, Rigaku Denki Co., Ltd.) con haces paralelos (Fig.2a) para medir los picos de difracción específicos, y la relación entre la composición y la constante de celosía de También se investiga la wustita a alta temperatura. El proceso de síntesis de wustita con α-Fe (95% en peso) y Fe 3 O 4 (99% en peso) de polvos como materiales iniciales es una reacción eutectoide (Fig. 2b). Esta reacción se puede producir entre 843.15 y 1673.15 K en ciertos Pco / Pco 2 ya que la wustita es inestable por debajo de 843,15 K, y los reactivos son 19% Fe (% en peso) y 81% Fe 3 O 4 (% en peso). La Figura 2c muestra el patrón XRD de los reactivos iniciales (magnetita y hierro). La condición del experimento se describe en la Tabla 1. Después de purgar gas helio (He) (25 ml min −1 ) en el horno del sistema XRD durante 60 min, los reactivos se calentaron a una velocidad constante de 10 ° C min −1 hasta que la temperatura de las muestras alcanzó los 843,15 K, que también se encontraban en atmósfera de He con un caudal de 25 ml min −1 . Luego, se agotó el gas He y CO / CO 2 Se purgó gas con cierta proporción (por ejemplo, 1:1 y 1:2) en el horno. Después de la calibración de alta temperatura mediante la fusión de escamas de Au, se pudo obtener la temperatura real del portamuestras. De 843,15 K a la temperatura deseada (1265,28 y 1365,28 K), la velocidad de calentamiento fue de 2 ° C min −1 y se empleó el XRD para medir la muestra para confirmar la fase wustita. Cuando la muestra se reservó a la temperatura deseada y la mayor parte de la cual era fase de wustita, se midieron los ángulos de difracción de los planos cristalinos de wustita durante un período de 240 a 420 min, luego la temperatura de la muestra se elevó a 50 ° C y permaneció a esta temperatura. durante 60 min. Después de estos procedimientos, la temperatura de la muestra disminuyó a la temperatura deseada anterior y la medición de XRD para los ángulos de difracción de los planos cristalinos de wustita se llevó a cabo nuevamente en un período de 180 a 240 min.
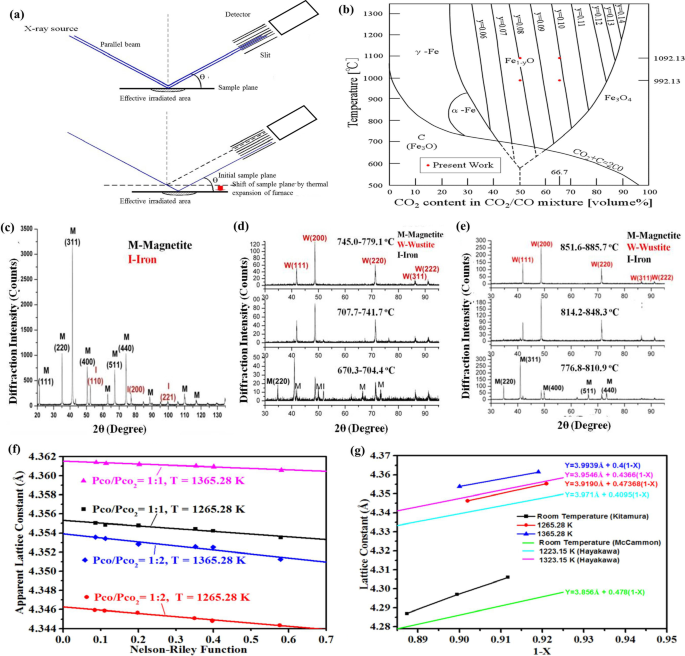
un Diagrama esquemático de XRD in situ. b Equilibrio entre Fe, Fe 1− y O, Fe 3 O 4 , CO, CO 2 y carbono. c Patrón XRD de los reactivos iniciales. d Patrón XRD de la muestra sintetizada en Pco / Pco 2 =1:1. e Patrón XRD de la muestra sintetizada en Pco / Pco 2 =1:2. f Las diferentes constantes de celosía aparente de función NR de wustita sintetizadas a diferentes temperaturas y Pco / Pco 2 . g Los resultados de la constante de celosía de wustita
La constante de celosía se puede obtener de una extrapolación lineal de las constantes de celosía aparentes a cero de esta función, es decir, 2 Theta =180 °. Los picos de difracción de (111), (200), (220), (311) y (222) planos cristalinos de wustita están indexados en la Fig.2d, e, y el patrón XRD de la muestra se obtiene en Pco / Pco. 2 de 1:1 y 1:2, respectivamente. La relación entre la constante de celosía aparente y la función de Nelson-Riley bajo diferentes Pco / Pco 2 y se obtienen las temperaturas, como se muestra en la Fig. 2f. Las líneas rectas representan los cuadrados que se ajustan a los datos. Mediante estas líneas rectas, las constantes de celosía aparente se extrapolaron al cero de la función de Nelson-Riley. Por lo tanto, como se muestra en la Fig.2f:los resultados de las verdaderas constantes de celosía obtenidas a diferentes temperaturas y Pco / Pco 2 son 4,355 Å (1265,28 K, Pco / Pco 2 =1:1), 4,346 Å (1265,28 K, Pco / Pco 2 =1:2), 4,362 Å (1365,28 K, Pco / Pco 2 =1:1) y 4,354 Å (1365,28 K, Pco / Pco 2 =1:2), respectivamente. Como se muestra en la Fig. 2g, la constante de la red aumenta con el aumento de x de Fe 1− x O, y cuanto mayor sea la temperatura, mayor será la constante de celosía. La relación entre la composición y la constante de celosía de la wustita a alta temperatura se puede obtener como las siguientes Ecs. (3) y (4).
$$ {\ text {a}} \, \ left ({{\ AA}} \ right) =3.919 + 0.474 \ left ({1 - x} \ right) {} \ left ({1265.28 \, {\ text {K}}} \ right) $$ (3) $$ {\ text {a}} \, \ left ({{\ AA}} \ right) =3.994 + 0.400 \ left ({1 - x} \ right ) {} \ left ({1365.28 \, {\ text {K}}} \ right) $$ (4)57 Espectroscopia Fe Mössbauer
El 57 La espectroscopía de Fe Mössbauer involucra propiedades del núcleo, incluida la estructura del nivel de energía del núcleo y el entorno químico en el que se encuentra el núcleo. Por lo tanto, se puede aplicar en consecuencia para estudiar la valencia de los átomos, la ionicidad de los enlaces químicos, el número de coordinación, la estructura cristalina, la densidad de electrones y las propiedades magnéticas de la muestra. El 57 La espectroscopia de Fe Mössbauer se utiliza ampliamente en los campos de la química y los materiales. Aquí, elaboramos el 57 Espectroscopía de Fe Mössbauer para la caracterización de óxidos de hierro. El 57 La espectroscopia de Fe Mössbauer se utiliza para distinguir y caracterizar varias fases de óxido de hierro y para controlar el entorno local de átomos de Fe en la red cristalina [39, 40].
Los parámetros hiperfinos, como desplazamiento de isómero (IS), división de cuadrupolo (QS), desplazamiento de cuadrupolo ( ɛ Q ) y campo magnético hiperfino ( B hf ) se puede obtener analizando la posición de las líneas espectrales en el espectro de Mössbauer [41, 42]. Las características de la muestra se pueden inferir del ancho y asimetría de las líneas espectrales. La dependencia de la temperatura y el campo de los parámetros hiperfinos también permite deducir parámetros valiosos.
Aldon y col. [42] estudiaron la reacción de conversión inducida por litio de Fe 1− x O usando 57 Espectroscopía de Fe Mössbauer. Los parámetros hiperfinos (IS y QS) son bastante característicos de las especies FeII en antiferromagnético (TN =198 K [43]) Fe 1− x O, que muestra una absorción paramagnética típica a temperatura ambiente (RT). Como se indica en el 57 Espectro de Fe Mössbauer (Fig. 3a), hay tres dobletes ampliados con un IS ~ 1 mm s −1 y QS que van desde ~ 0,50 a 1,50 mm s −1 , y sus áreas relativas se corrigen a partir de la contribución magnética de α-Fe. Las intensidades de absorción son 42, 26 y 15%. Un cuarto doblete centrado en IS ~ 0.55 mm s −1 , QS ~ 0,90 mm s −1 con un área relativa del 11% es común para FeII I especie, como se esperaba en Fe no estequiométrica 1− x O. Del FeII / FeII I relación, la cantidad de vacantes se estima en ~ 0.057 ± 0.008, cerrado a 0.050 por caracterización XRD. Finalmente, el doblete ubicado en QS ~ 1.68 mm s −1 e IS ~ 0 mm s −1 , correspondiente a α-Fe, hace una contribución de ~ 6%.
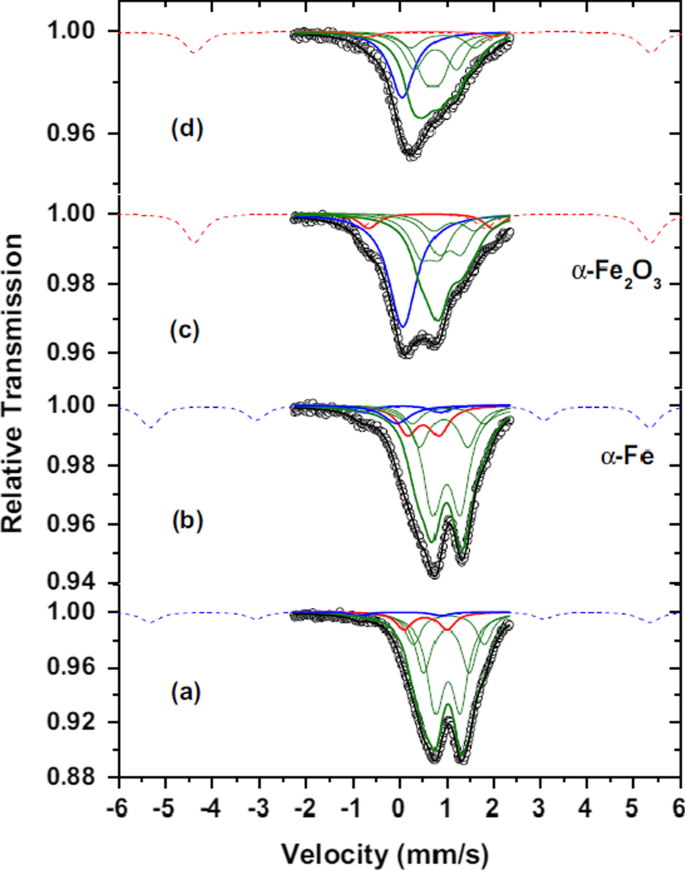
Reproducido con permiso de [42]. Derechos de autor, Elsevier Masson SAS
Comparación de 57 Espectros de Fe Mössbauer a 300 K del prístino Fe 1− x O material ( a ), después de una absorción de 1 Li ( b ) y el final de la descarga a 2,16 Li ( c ). Las contribuciones verdes se atribuyen a FeII. La línea verde más gruesa es la suma de la más fina correspondiente al Fe sin reaccionar 1− x O. La línea azul discontinua corresponde a la contribución creciente esperada de α-Fe de ( a ) a ( c ). En el caso de ( c ), el sexteto magnético se ha desplazado ligeramente como guía del ojo. Espectro ( d ) corresponde al final de la primera carga a 0,94 Li sin contribución de α-Fe, pero el ε-Fe metálico nanométrico singlete azul 0 todavía está presente.
Comparando con Fe 2 O 3 y Fe 3 O 4 , la capacidad específica de Fe 1− x O es el más bajo. Además, su método de síntesis es más complicado. En la mayoría de los casos, la reacción de reducción a alta temperatura es inevitable [3, 4, 5, 6, 9, 11]. Como resultado, Fe 1− x O no es un ánodo LIB ideal en comparación con Fe 2 O 3 o Fe 3 O 4 .
Fe 2 O 3 Nanoestructuras basadas
Entre estos óxidos de hierro, especialmente Fe 2 O 3 , está atrayendo la atención de muchos investigadores debido a la alta capacidad teórica, que puede alcanzar los 1000 mA h g −1 [44]. Además, Fe 2 O 3 tiene ventajas distintivas, como alta resistencia a la corrosión, bajo costo de producción, respeto al medio ambiente, no inflamabilidad, no toxicidad y alta disponibilidad natural [45]. Debido a estas excelentes propiedades, Fe 2 O 3 es muy prometedor para aplicaciones en ánodo LIB [46,47,48,49,50]. Aquí, una descripción concisa del desarrollo reciente sobre la síntesis, caracterización y desempeño electroquímico de Fe 2 O 3 se proporcionan nanoestructuras basadas.
Síntesis y caracterización
En la última década, se han realizado enormes esfuerzos para explorar métodos sintéticos de Fe 2 O 3 nanoestructuras basadas. En esta sección, elaboramos y resumimos métodos sintéticos de Fe 2 O 3 nanoestructuras basadas, incluida la deposición en fase gaseosa [51], el método basado en solución [52], el método electroquímico [53], el tratamiento térmico [54] y otros métodos [55, 56]. Además, comparamos diferentes métodos de síntesis.
Además, el 57 Caracterización por espectroscopía de Fe Mössbauer de Fe 2 O 3 nanoestructuras se describen en detalle. Dado que solo ciertos núcleos tienen absorción de resonancia, el 57 La espectroscopia de Fe Mössbauer no se ve interferida por otros elementos. El rango de 57 La espectroscopia de Fe Mössbauer afectada por un entorno extranuclear se encuentra generalmente dentro de varios nanómetros, por lo que es muy adecuada para caracterizar nanoestructuras.
Deposición en fase gaseosa
La deposición en fase gaseosa se aplica ampliamente en la síntesis de muchas películas delgadas y otras nanoestructuras, como Fe 2 O 3 y otras nanoestructuras basadas en óxidos de hierro. La deposición química de vapor (CVD), la deposición de capa atómica (ALD), la deposición física de vapor (PVD), la deposición electrolítica y la pulverización catódica reactiva son métodos típicos de deposición en fase gaseosa [57,58,59,60].
ALD es una forma única de sintetizar películas delgadas de alta cristalinidad y una ruta más barata que la deposición en fase líquida. En el proceso ALD, la reacción química de cada capa se acompaña directamente con la capa anterior. De esta forma, solo se deposita una capa por ciclo de reacción. Por ejemplo, Lin et al. [51] utilizó ALD para depositar una α-Fe 2 ultrafina de alta calidad O 3 película en TiSi 2 nanorredes. Las películas delgadas nanoporosas autoorganizadas en 3D fueron fabricadas por Yang et al. [61] a través de CVD e integrado en un Fe 2 heterogéneo O 3 / Fe 3 C-grafeno. Como ánodo LIB, su capacidad de velocidad y ciclabilidad pueden mejorarse en gran medida mediante la deposición de esta película delgada. Cesar y col. [62] depositaron películas delgadas de Fe 2 dopado con silicio O 3 nanoestructuras dendríticas por CVD a presión atmosférica (APCVD), que produjeron Fe 2 O 3 fotoanodos que oxidan el agua bajo luz visible con una eficiencia sin precedentes. El α-Fe 2 dendrítico O 3 nanoestructuras mostraron una superficie macroscópica de 0,5 cm 2 [62]. El α-Fe 2 alineado verticalmente O 3 La matriz de nanorods se cultiva en un sustrato de silicio a través de CVD metal-orgánico (MOCVD) por Wu et al. [63]. Además, Jia et al. [64] utilizó una deposición de pulverización catódica de radiofrecuencia para fabricar α-Fe 2 O 3 películas ultrafinas.
Aunque la deposición en fase gaseosa es capaz de preparar Fe 2 de alta calidad O 3 nanoestructuras basadas, también tiene desventajas. Por ejemplo, APCVD y MOCVD tienen alta toxicidad e inflamabilidad en el proceso de precursores.
Método sintético basado en soluciones
El método sintético basado en soluciones es común y fácil de fabricar Fe 2 O 3 y otros óxidos de hierro. Fe 2 O 3 con diversas morfologías, como nanoflores [65], nanoesferas [66], nanopartículas [67], nanobarras [68], nanotubos [14], nanorings [69], nanocinturones [70], nanoflakes [71], nanocables [72] , nanofibras [73] y microcajas [54], se sintetizaron mediante un método basado en solución, por ejemplo, enfoques hidrotermal, solvotermal y sol-gel. Estos métodos son muy fáciles y están disponibles. Zhong y col. [65] utilizó un método solvotermal para fabricar Fe 2 O 3 nanoflores (Fig. 4) mediante un proceso de autoensamblaje mediado por etilenglicol. Vayssieres y col. [52] informó el crecimiento de Fe 2 poroso O 3 Matriz de nanobarras sobre vidrio conductor de óxido de estaño dopado con flúor (FTO) mediante un proceso hidrotermal. Por crecimiento hidrotermal de α-Fe 2 O 3 precursor de SnO 2 tallos de nanocables, una nueva α-Fe 2 ramificada con simetría de seis veces O 3 / SnO 2 Se sintetizó la heteroestructura (Fig. 5) [74]. Existe otra técnica fácil y económica, el método sol-gel, para sintetizar Fe 2 O 3 nanoestructuras. Woo y col. [68] utilizó un método sol-gel para obtener α-Fe 2 O 3 nanovarillas por reacción del omnipresente Fe 3+ en micelas inversas. Las nanovarillas obtenidas por este mecanismo tienen baja dimensionalidad y alta superficie, que se puede extender a magnetita y wustita.

Reproducido con permiso de [65]. Derechos de autor, Wiley-VCH
un SEM y b Imágenes TEM de la α-Fe 2 obtenida O 3 . c Imagen TEM de gran aumento del pétalo de la estructura similar a una flor de la α-Fe 2 obtenida O 3 . d Patrón SAED del α-Fe 2 obtenido O 3 .

Reproducido con permiso de [74]. Derechos de autor, Wiley-VCH
un - f Imágenes SEM de los productos (después del recocido) en varias etapas de reacción estableciendo el tiempo de reacción. Los recuadros son las correspondientes imágenes SEM ampliadas. Las barras de escala en las figuras y los recuadros son de 2 μm y 500 nm, respectivamente. g Esquema del proceso de formación del α-Fe 2 ensamblado jerárquicamente O 3 / SnO 2 nanocompuesto.
Método electroquímico
Se utiliza un método electroquímico para sintetizar Fe 2 O 3 nanoestructuras, por ejemplo, la deposición electroquímica se aplica en la fabricación de Fe 2 O 3 nanopartículas [53]. Mediante la anodización de una lámina de hierro en una solución de electrolito de etilenglicol que contiene agua desionizada (DI) y NH 4 F a un voltaje de 30 a 60 V, α-Fe 2 O 3 Se obtuvo una matriz de nanotubos [75]. Además, la anodización electroquímica se emplea para sintetizar Fe 2 O 3 matriz de nanotubos [76]. Mao y col. [77] informó la síntesis de Fe 2 O 3 matriz mediante deposición electroquímica. En su trabajo de investigación, el hierro se depositó en canales de plantilla de AAO mediante deposición electroquímica, luego la plantilla de AAO se eliminó mediante una solución de NaOH y, finalmente, la matriz de nanovarillas de hierro se convirtió en Fe 2 O 3 formación. La característica de esta investigación es que, al cambiar la duración de la deposición, la longitud del Fe 2 O 3 las nanovarillas se pueden controlar con precisión.
Tratamiento térmico
El tratamiento térmico para la síntesis de Fe 2 O 3 implica dos enfoques importantes, la oxidación térmica y la pirólisis térmica. Por ejemplo, Zhang et al. [54] preparó Fe 2 O 3 microcajas (Fig. 6) a través de la descomposición oxidativa inducida térmicamente de microcubos de azul de Prusia (PB) a 350–650 ° C. El enfoque de estado sólido proporcionará una forma más fácil de síntesis a gran escala de estructuras huecas anisotrópicas uniformes en comparación con el método basado en solución ampliamente utilizado. Fe 2 O 3 con diferentes morfologías se prepararon mediante el comando de parámetros de oxidación térmica. α-Fe 2 O 3 Se proponen nanoestructuras por fácil tratamiento térmico de precursores a base de hierro. Por ejemplo, Rao y Zheng [71] utilizaron tratamiento térmico para preparar α-Fe 2 densamente alineados O 3 matriz de nanoflakes.
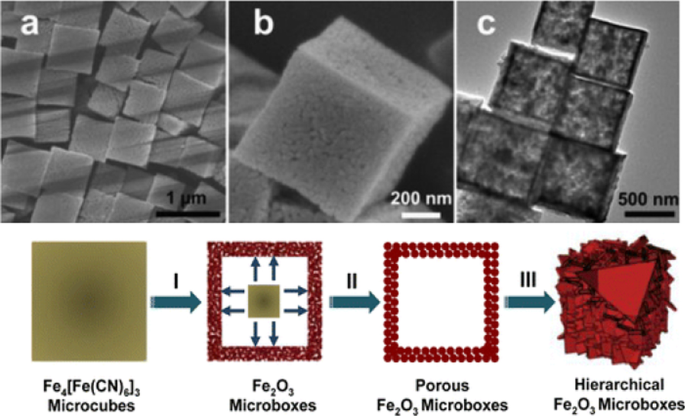
Reproducido con permiso de [54]. Copyright, Sociedad Química Estadounidense
un , b FESEM y c Imágenes TEM de Fe 2 hueca O 3 microcajas obtenidas a 350 ° C. d Ilustración esquemática de la formación de Fe 2 hueco O 3 microcajas y la evolución de la estructura de la cáscara con el aumento de la temperatura de calcinación.
La pirólisis térmica es otro método común para depositar Fe 2 O 3 Peliculas delgadas. Duret y col. [78] aplicó este método para obtener α-Fe 2 mesoscópica O 3 películas de folletos mediante pirólisis por pulverización ultrasónica, mientras que las películas fabricadas tienen una fotoactividad más alta que las fabricadas mediante técnicas convencionales de pirólisis por pulverización. Además, la síntesis de α-Fe 2 O 3 Se informa de nanoflakes, nanoflores, nanoalambres y nanobarras mediante deposición en fase de vapor, deposición en fase líquida y tratamiento térmico [63, 71, 72, 79].
Otros métodos
En 2016, Guivar et al. [55] maghemita ordenada por vacante compuesta (γ-Fe 2 O 3 ) nanopartículas funcionalizadas con nanohidroxiapatita (nanoHAp), utilizando una ruta química típica de coprecipitación. Sorprendentemente, el γ-Fe 2 O 3 funcionalizado con nanoHAp etiquetado como γ-Fe 2 O 3 @HAp se forma sin ningún proceso térmico como calcinación.
Hay muchas formas de sintetizar Fe 2 O 3 , pero la mayoría de ellos no son amigables con el medio ambiente. En 2019, Bashir et al. [56] desarrolló un método ecológico para obtener α-Fe 2 O 3 nanopartículas, utilizando extracto de semillas de Persea Americana. Utilizaron dos precursores diferentes para preparar dos muestras de α-Fe 2 O 3 , una muestra (A) preparada a partir de Fe (NO 3 ) 3 · 9H 2 O, y otra muestra (B) preparó FeCl 3 · 9H 2 O.
El 57 Los espectros de Fe Mössbauer de las muestras A y B registrados a 300 K (temperatura ambiente (RT)) se presentan en la Fig. 7. El 57 La espectroscopía de Fe Mössbauer es una técnica muy valiosa para explorar el comportamiento magnético local y el estado de oxidación de los átomos de hierro en una matriz particular [80]. Both samples revealed magnetic ordering, and displayed only single sextet indicating magnetically ordered state. Table 2 shows 57 Fe extracted Mössbauer parameters at RT, which lists IS, ɛ Q and B hf . Both samples’ B hf above 51 T are related to α-Fe2 O 3 [81]. Furthermore, the values of ɛ Q is also consistent with α-Fe2 O 3 . Both quadrupole interactions indicate Fe as Fe 3+ since the observed IS of 0.3653 mm/s and 0.3754 mm/s for the samples A and B, respectively, are typical for Fe 3+ [82]. Therefore, the negative values of quadrupole splitting indicate the weak ferromagnetic property of the samples A and B, the characteristic of pure α-Fe2 O 3 phase.
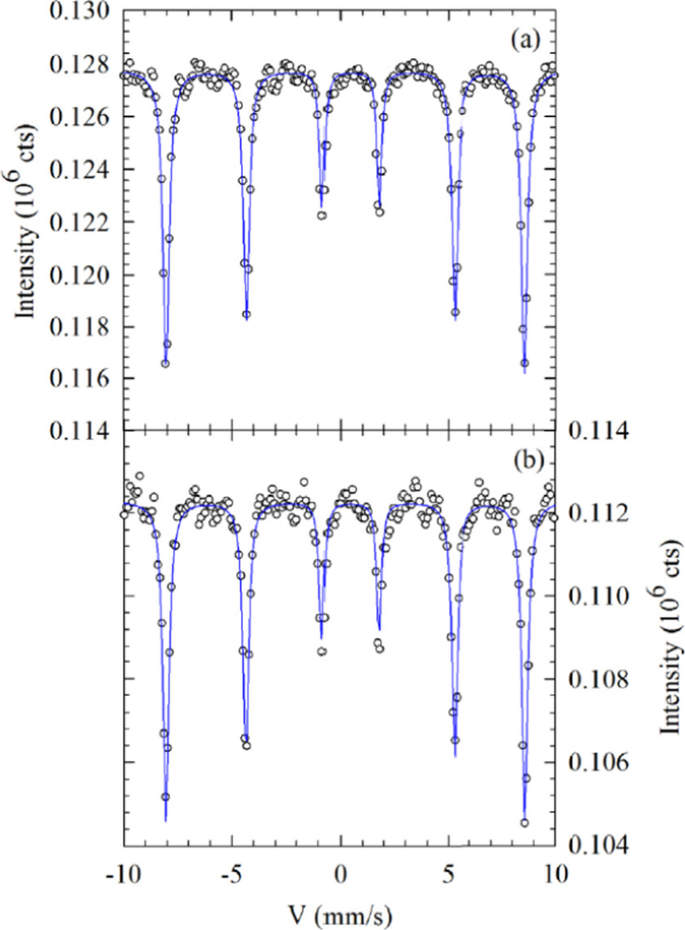
Reprinted with Permission from [56]. Copyright, American Chemical Society
57 Fe Mössbauer spectra recorded at room temperature for α-Fe2 O 3 nanoparticles. un sample A (ferric nitrate as a precursor) and b sample B (ferric chloride as a precursor).
Electrochemical Performance
The charge/discharge cycling at the voltage window of 0.005–3.0 V (vs. Li + ) under a current density of 200 mA g −1 at RT is shown in Fig. 8a. During the initial discharge process, there is an obvious voltage platform of ~ 0.75 V, and it gradually moved to a voltage plateau of ~ 1.0 V, and remain stable in the second and fifth cycles. Meanwhile, an ambiguous plateau was observed at ~ 1.8 V in the charge process. The first discharge profile qualitatively resembles the results by Larcher et al. [83] and Morales et al. [84] on nanoparticle Fe2 O 3 , and Wang et al. [14] on Fe2 O 3 nanotubes. The cycling performance of three samples (hierarchical Fe2 O 3 microboxes, Fe2 O 3 microboxes and porous Fe2 O 3 microboxes) is discribed in Fig. 8b. After 30 cycles, hierarchical Fe2 O 3 microboxes exhibit the highest reversible capacity of 945 mA h g −1 , follow by 872 mA h g −1 for porous Fe2 O 3 microboxes, and finally 802 mA h g −1 for Fe2 O 3 microboxes. The results demonstrated that three samples display excellent cycling stability, and the morphology of nanostructured Fe2 O 3 plays a significant role in determining the discharge characteristics.
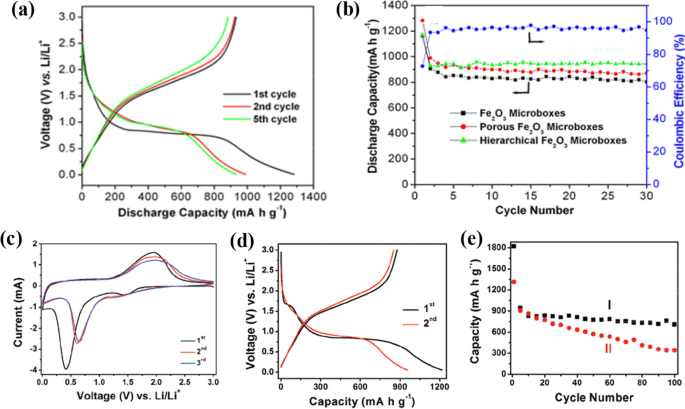
c –e Reprinted with Permission from [85]. Copyright, American Chemical Society
un Discharge − charge voltage profiles of porous Fe2 O 3 microboxes obtained at 550 °C. b Cycling performance of Fe2 O 3 microboxes (350 °C), porous Fe2 O 3 microboxes (550 °C), and hierarchical Fe2 O 3 microboxes (650 °C) and Coulombic efficiency of porous Fe2 O 3 microboxes (550 °C) over the voltage range 0.01 − 3.0 V vs. Li/Li + at the same current density of 200 mA g -1 . (a , b Reprinted with Permission from [54]. Copyright, American Chemical Society). Electrochemical measurements of the sample. c CVs between 5 mV and 3 V at a scan rate of 0.5 mV s −1 . d Charge–discharge voltage profiles. e Comparative cycling performance of (I) the as-prepared α-Fe2 O 3 hollow spheres and (II) α-Fe2 O 3 microparticles. All the galvanostatic tests are performed at a constant current rate of 200 mA g −1 between 0.05 and 3 V.
Cyclic voltammogram (CV) is used to characterize the cells with α-Fe2 O 3 nanoflakes anode in the 0.005–3.0 V under a slow scan rate (at RT). Li metal is used as the counter and reference electrodes [20], consistent with previously reported results [85]. CV curves of α-Fe2 O 3 hollow spheres between 5 mV and 3 V at a scan rate of 5 mV s −1 are presented in Fig. 8c. There are apparent redox current peaks, and demonstrate good reversibility of electrochemical reaction. As shown in Fig. 8d, a distinct voltage plateau can be discovered at ~ 0.75 V, consistent with CV curves. The charge–discharge voltage profiles reflect the lithium storage capacity of α-Fe2 O 3 . The first cyclic discharge capacity and the charge capacity is 1219 mA h g −1 and 877 mA h g −1 respectively, which lead to a relatively low irreversible capacity loss of 28%. In the second cycle, the Coulombic efficiency increased quickly to 89%. Cycling performance of two samples are demonstrated in Fig. 8e. The sample (I) exhibits excellent cyclic capacity retention from the second cycle onward. After 100 cycles of charge/discharge, the reversible capacity is still as high as 710 mA h g −1 . Compared with α-Fe2 O 3 microparticles, the unique hierarchical α-Fe2 O 3 hollow spheres apparently have enhanced Li storage performance, and a more stable cycling capacity retention and a higher reversible capacity are realized. This superior performance can be attributed to the thin nanosheet subunits that provide rapid and efficient transport of Li + , as well as the unique hollow interior that allows the material to effectively buffer the stress generated during charge/discharge process.
Iron oxides are cheap, abundant and environmentally compatible, and Fe2 O 3 has excellent electrochemical performance. Some of the above studies have shown that Fe2 O 3 based nanostructures can be an alternative anode to replace the presently used graphite in LIBs. The nanostructured Fe2 O 3 has great potential in LIBs anode [86,87,88,89,90,91,92,93,94,95]. Recently, several studies about Fe2 O 3 anode in asymmetric supercapacitors are reported [96,97,98,99,100]. However, low surface area and poor electrical conductivity are still two critical issues limiting the specific capacitance and power density of Fe2 O 3 . For solutions of these problems, CNTs and CNFs are regarded as conductive matrices to load Fe2 O 3 nanoparticles for realizing improved performance [101]. Table 3 summarizes some typical Fe2 O 3 based nanostructures with their synthesis and electrochemical performance.
Fe3 O4 Based Nanostructures
Magnetite (Fe3 O4 ) and Fe3 O4 based nanostructure composites with pseudocapacitance, high theoretical capacity, environmental friendliness and low cost, are extensively applied to electromagnetic wave absorption [106], LIBs [3, 12, 15], biotechnological devices [107, 108], and supercapacitor [4, 109]. Fe3 O4 nanoparticles is one of the high-performance anodes in electrochemical devices. Unfortunately, Fe3 O4 nanostructures still face some problems, such as a severe volume variation (~ 200%) during the insertion and extraction of Li + and relatively low electrical conductivity, posing negative influence on the cycling stability [19, 110, 111]. From research results, we found that the structure and morphology of Fe3 O4 have a high influence on the electrochemical performance of Fe3 O4 and Fe3 O4 based composites.
Synthesis and Characterization
Recently, nanostructure engineering is demonstrated as a highly-effective approach to obtain improved electrochemical performance of Fe3 O4 and Fe3 O4 based composites. Therefore, various nanostructures including 0D nanoparticles [112], 1D nanorods/wires [113, 114], 2D nanoflakes/sheets [115, 116], 3D hierarchical/porous architectures [117, 118], and hybrid nanostructures of iron oxides [16] are proposed. The electrochemical performance of Fe3 O4 nanostructures can be optimized by rational design of their morphology, composition, porosity and surface characteristics.
Solution phase synthetic method is a facile and rapid way to obtain Fe3 O4 based nanostructures, because of the associative advantages, such as low synthesis temperature (always below 250 °C), easy control of morphology via adjusting hydrothermal conditions (e.g., PH, density of reactant and dosage of active agent, etc.). Solution phase synthetic method includes solvothermal synthesis [119], thermolysis [120], co-precipitation [121], sol–gel process [122, 123], micro-emulsion [124], etc. Simultaneously we compare the pros and cons of these methods.
Solvothermal Synthesis
Solvothermal synthesis, which reacts in a special closed reaction vessel, is one commonly used methods for synthesizing Fe3 O4 . In a hermetic environment, it is a facile method using aqueous solution as reaction medium at high temperature and high-pressure hermetic environment. Fe3 O4 nanostructures with various morphologies (0D, 1D, 2D and 3D) were synthesized applying this approach.
An et al. [119] obtained the Fe3 O4 /graphene nanowires by solvothermal synthesis and calcination with FeCl3 , NH4 VO3 and graphene as precursors. Phase transition of Fe3 O4 /VOx (FVO) after annealing was confirmed by XRD. For the XRD pattern of sample without annealing, all diffraction peaks of FVO and graphene decorated FVO correspond to FeVO4 ·1.1H2 O. For the XRD pattern of sample after annealing, there are no peaks of any vanadium oxides. And the inductive coupled high frequency plasma (ICP) result indicated that the molarity ratio of Fe and V is ~ 0.94:1, confirming the existence of amorphous vanadium oxide.
Mu et al. [125] reported dispersed Fe3 O4 nanosheets on carbon nanofiber by combing the electrospinning and solvothermal process. In this work, Fe3 O4 nanosheets are uniformly attached on the surface of carbon nanofiber with the diameter of about 500 nm.
Fe3 O4 nanoparticle with high specific surface area via FeCl3 and organic solvent ethanolamine (ETA) as precursors is reported by Wang et al. [126]. In this preparation, ETA is critical factor for compounding Fe3 O4 nanoparticles with high specific surface area, and Fe 3+ is gradually reduced to Fe 2+ by ETA during dissolution process, demonstrating that Fe 2+ increased as the increase of ultrasonication time. The ratio of ETA and FeCl3 has a large impact on the nanoscale grain size and specific surface area of Fe3 O4 . And the results showed that the grain size of 20–40 nm is achieved with 60 mL ETA and 6 mmol FeCl3 . When the amount of ETA is 80 mL, smaller nanoparticles (5–10 nm) are obtained.
Another representative work is reported by Chen et al. [127], in which graphene nanosheets decorated with Fe3 O4 nanoparticles (USIO/G) were synthesized using a facile solvothermal process. For the synthesis of USIO composite decorated with reduced graphene oxide (RGO), is used FeCl3 ·H2 O as precursor, then NaHCO3 and L-ascorbic acid were added to form USIO/G. In this process, L-ascorbic acid was oxidized to dehydroascorbic acid (DHAA) by some of Fe 3+ , which were reduced to Fe 2+ . Formation process of USIO/G is schematically shown in Fig. 9. The Fe3 O4 nanoparticles with uniform distribution, which are beneficial for electrical conductivity of graphene, mitigation of volume expansion of Fe3 O4 , and facilitating Fe3 O4 particles into the electrolyte.
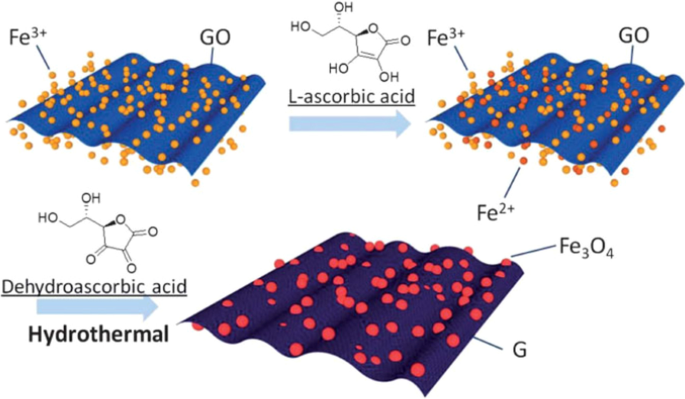
Reprinted with Permission from [127]. Copyright, Royal Society of Chemistry
Schematic illustration of the formation process of USIO/G.
Xiong et al. [128] a kind of hierarchical hollow Fe3 O4 (H-Fe3 O4 ) microspheres prepared by controlled thermal decomposition of iron alkoxide precursor. In a classical reaction, ethylene glycol (EG) serves as reduction reagent that partly reduces Fe 3+ to Fe 2+ with sodium acetate (NaAc), and polyvinylpyrrolidone (PVP) [128]. For this synthesis, PVP served as a surface stabilizer, which has important role in the formation and transformation of hollow interiors.
With the development of solvothermal synthesis, it emerging as an efficient method with the advantages of low energy consumption, little reunion and easy to control shape, etc. Chen et al. [129] synthesized poly (acrylic acid) (PAA)-entangled Fe3 O4 nanospheres by a facile solvothermal method. In their synthesis, the ethylenediamine is crucial to the controlling of the uniformity of nanospheres, and the PAA molecules served as carbon source that transforms into the carbon matrix by heating treatment in inert atmosphere. As shown in SEM image of the prepared C-Fe3 O4 nanospheres, very uniform spherical particles with a diameter of 150–200 nm are synthesized. Observed from SEM images in Fig. 10a, the nanospheres contain small irregular particles, and have a relatively rough surface. In the control experiment without ethylenediamine (EDA), the synthesized particles are much less uniform with a wider size distribution of 100–500 nm, allowing the formation of nanospheres with smaller size.

Reprinted with Permission from [130]. Copyright, Wiley–VCH
un SEM images of the Fe3 O4 nanospheres synthesized with ethylenediamine (EDA). The inset of (a ) shows a SEM image with higher magnification. (Reprinted with Permission from [129]. Copyright, American Chemical Society.). Physicochemical characterization of the octahedral Fe3 O4 nanoparticles. b SEM image showing the octahedral geometry of the iron oxide nanoparticles.
Co-precipitation
Due to its high cost-effectiveness, environmental friendliness, and facile synthesizing protocol, co-precipitation is a general approach for Fe3 O4 nanoparticles. Thus, in iron based rechargeable battery systems, Fe3 O4 nanomaterials are especially suitable for large-scale electrochemical applications to solve the energy requirement of the modern society.
Li et al. [121] proposed Fe3 O4 polyhedron as LIBs anode for alkaline secondary batteries by a co-precipitation. Annealing temperature makes a high effect on the physical and electrochemical performance of Fe3 O4 nanomaterials. The 700 °C-annealed Fe3 O4 exhibited a higher electrochemical performance, such as a higher specific discharge capacity of 604.2 mA h g −1 with a charging efficiency of 83.9% at 120 mA g −1 . Ooi et al. [130] demonstrated octahedral Fe3 O4 nanoparticles using a facile solvothermal route. Scanning electron microscope (SEM) image of Fe3 O4 nanoparticles is shown in Fig. 10b, which depicts that octahedral Fe3 O4 nanoparticles with an average length of 93 ± 18 nm were prepared by the hydrothermal method, showing a roughly Gaussian size distribution. Then, the crystal structure of octahedral nanoparticles can be further evaluated by HRTEM, and the composition of the bulk sample was further characterized by XRD and X-ray photo electron spectroscopy (XPS).
Thermolysis
The thermolysis is small monodisperse magnetic nanocrystals synthesized by organic metal compounds in high boiling point solvents containing stabilizing agent. Previous Organic metal bodies include metal acetylacetone compounds, metal cupferron, or metal Carbonyl compounds, and usually choose fatty acids, oleic acid, or hexadecyl amine as a surfactant. Zhang y col. [120] reported ultrafine Fe3 O4 nanocrystals uniformly encapsulated in two-dimensional (2D) carbon nanonetworks through thermolysis of Fe(C5 H7 O 2 )3 precursor at 350 °C under vacuum, which named as 2D Fe3 O4 /C nanonetworks. This facile process using low-cost precursor proposed a green approach for preparing Fe3 O4 /carbon composite. Additionally, compared with the reported Fe3 O4 /carbon composites, the particle size of Fe3 O4 is controllable and a size of ∼ 3 nm can be obtained.
Benefitting from synergistic effects of carbon nanonetworks with excellent electrical conductivity and ultrafine Fe3 O4 particles with uniform distribution, high reversible capacity, excellent rate capability and superior cyclability at the voltage of 0.01–3.0 V (vs. Li/Li + ) are obtained. Nanoparticles with unique iron oxide (Fe3 O4 ) cores and zinc oxide (ZnO) shells were prepared by Jaramillo et al. [131]. Fe3 O4 nanoparticle synthesized through a thermolysis method using Fe(C5 H7 O 2 )3 as organic metal body presoma, triethylene glycol as surface active agent, and core–shell Fe3 O4 @ZnO nanoparticles were successfully synthesized using straightforward methodologies. The structural and optical properties of the materials were characterized using a combination of X-ray diffraction, electron microscopy, and light spectroscopy. Importantly, the purity of the core and shell phases in the Fe3 O4 @ZnO nanoparticles was confirmed by both XRD and TEM, and the ZnO shell was shown to increase the transparency of the core–shell nanoparticles relative to the single-component Fe3 O4 nanoparticles. Zhang y col. [132] demonstrated a high crystalline Fe3 O4 -graphene composite by one-step reaction of thermolysis. And they demonstrated that the attachment of iron-organic complex with graphene oxide (GO) sheets can facilely result in magnetic graphene composites via a time-dependent calcination process.
Sol–Gel Process
The specific method is using the metal alkoxide, metal mineral compound or a mixture of the above two substances to hydrolysis and polymerization, uniform gel gradually, then condense into a transparent gel, however, after drying and heating, finally the oxide ultrafine powders was received. Tang et al. [122] prepared nanostructured magnetite thin film by sol–gel method using inexpensive iron (II) chloride precursor. Fe3 O4 nanoparticles were prepared at 300 °C, however, α-Fe2 O 3 is generated when temperature increased to 350 °C, and this result restricts its applications. Xu et al. [123] proposed magnetite nanoparticles by virtue of sol–gel process combined with annealing in vacuum at 200–400 °C using nontoxic and low-cost ferric nitrate. In their study, Fe3 O4 nanoparticles with various sizes can be synthesized facilely through varying the annealing temperature.
Micro-emulsion Method
Micro-emulsion is composed of two mutual miscibility of liquid mixture of thermodynamic stability and isotropy dispersion, one of these or two kinds of liquid called micro area, and fixed by interface layer of the surfactant molecules. The key factors controlling the reaction solution contain concentration, pH value, reaction time and temperature. Micro-emulsion as a rapid expansion of new technology possesses many advantages. For example, high purity and uniform particle size distribution molecular dopant was synthesized at low temperature and simple reaction process. But there are also some shortcomings, for instance, the reaction system mostly contains organic solvents, which leads to high cost, pollution of environmental health and long reaction time. The prepared Fe3 O4 nanoparticles have excellent catalytic performance for the synthesis of quinoxaline in different solvents. Novel core–shell magnetic Fe3 O4 /silica nanocomposites with triblock-copolymer grafted on their surface (Fe3 O4 @SiO2 @MDN) were successfully synthesized by combining sol–gel process with seeded aqueous-phase radical copolymerization approach [133]. The Fe3 O4 @SiO2 @MDN microspheres were synthesized in following three steps. Firstly, the initial magnetic Fe3 O4 microspheres were synthesized by a solvothermal reaction. Then a sol–gel process was utilized to prepare silica coated Fe3 O4 microspheres (Fe3 O4 @SiO2 ), and a thin amorphous silica layer was formed on Fe3 O4 microspheres. Afterward, the Fe3 O4 @SiO2 microspheres were modified by 3-(methacryloxypropyl) trimethoxysilane (MPS). Finally, the triblock copolymer was fabricated by aqueous phase radical copolymerization reaction among MPS, divinylbenzene (DVB) and N-Vinyl-2-pyrrolidone (NVP) on the surface of Fe3 O4 @SiO2 . The magnetic Fe3 O4 particles with narrow size distribution have nearly spherical shape and smooth surface. Li et al. [124] reported hexagonal and triangular monodisperse Fe3 O4 nanosheets by a two-step microemulsion solvothermal approach, in which the uniform Fe3 O4 nanoparticles are prepared and then these hydrophobic nanocrystals are dispersed in a uniform microemulsion environment as “seeds” for further re-growth through a secondary solvothermal process. In the first step, near-spherical monodisperse 7–8 nm Fe3 O4 nanoparticles were formed through a kinetically controlled process. In the second step, the formation of anisotropic Fe3 O4 nanosheets is a thermodynamically controlled process and all the exposed surfaces of the triangular and hexagonal nanosheets are (111) crystal planes, which have the lowest surface energy for FCC Fe3 O4 .
Other Methods
Physical methods are also significant ways to prepared Fe3 O4 nanostructure for anode of LIBs. Several advantages, such as good crystallization, fine-tuned particle size, and high purity of products are highlighted in recent literatures. But these methods usually demand advanced and expensive equipment, result in a higher cost, poor dispensability of particles dispersion, and agglomeration of nanostructures. For instance, Du et al. [109] fabricated activated carbon (AC)-Fe3 O4 nanoparticles asymmetric supercapacitor, and Fe3 O4 nanostructure was prepared by microwave method. The precursor, FeSO4 ·7H2 O and NH3 ·H2 O mixed solution, was heated in microwave oven. The black precipitate was separated by magnet and washed repeatedly with DI water. The resulted microstructural properties of prepared nanoparticle were characterized by nitrogen adsorption (Quantachrome NOVA 2000), XRD and SEM [109]. Chen et al. [127] synthesized graphene nanosheets decorated with ultra-small Fe3 O4 nanoparticles (USIO/G). Seo et al. [134] reported an integrated usage of magnetic particles in microalgal downstream processes, specifically microalgal harvesting and lipid extraction through one-step aerosol spray pyrolysis and applied in microalgal harvesting and serial microalgal lipid entrapment. TEM/EDS, XPS, and FT-IR analysis suggested that the cationic and lipophilic functionalities arose from not fully decomposed PVP, due to the short residence time in the reactor. Kang et al. [135] proposed Fe3 O4 nanocrystals confined in mesocellular carbon foam (MSU-F–C) by a “host–guest” approach and applied it as LIBs anode. In this study, a precursor of Fe(NO3 )3 ·9H2 O is impregnated in MSU-F–C having uniform cellular pores with a diamter of ~ 30 nm, followed by heating treatment at 400 °C for 4 h in argon (Ar) atmosphere. Fe3 O4 nanocrystals with size of 13–27 nm were fabricated inside the pores of MSU-F–C. The existance of the carbon most likely allows the reduction of some Fe 3+ to Fe 2+ ions by a carbothermoreduction process. The physical performance and pore structure of MSU-F–C and Fe3 O4 -loaded composites were characterized with nitrogen sorption, and the composites have high capacities of ∼800–1000 mA h g −1 at 0.1 A g −1 (∼0.1 C rate), high rate capability and good cycling performance.
Application
Fe3 O4 possesses lots of unique properties, and is highly promising for applications in LIBs and supercapacitors [136,137,138,139,140,141,142]. Table 4 summarizes some applications.
Li-Ion Batteries
Due to conversion reaction of Fe3 O4 during charge/discharge process and other advantages, the Fe3 O4 is usually studied and applied as LIBs anode [143,144,145,146,147]. For TMOs, they have higher theoretical capacity (~ 500–1000 mA h g −1 ) than conventional graphite (about 372 mA h g −1 ). Furthermore, Fe3 O4 has superior conductivity compared with other transition metal oxides. Thus, it is well-focused by recent studies. It has been reported that composite electrodes with graphene have high performance due to their large surface area, high electrical conductivity and adaptive or flexible structure for high reliability. Qiu et al. [3] reported a kind of composite anode composed of ultra-dispersed Fe3 O4 nanoparticles (3–8 nm) and RGO sheet. It has excellent cyclic performance (624 mA h g −1 for up to 50 charge/discharge cycles at a current density of 0.1 A g −1 ), and good specific capability (624 and 415 mAh g −1 at 0.1 and 2.4 A g −1 , respectively) for LIBs. The obtained Fe3 O4 /RGO exhibited high and ultrastable Photo-Fenton activity (Fig. 11).
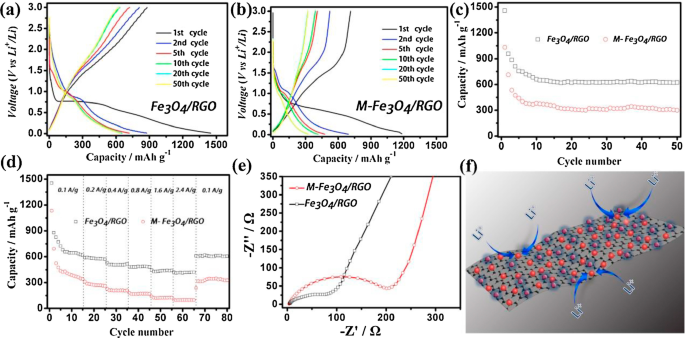
Reprinted with Permission from [3]. Copyright, Elsevier B.V
The charge/discharge curve of Fe3 O4 /RGO composites (a ) and mechanically mixed Fe3 O4 /RGO composites (M-Fe3 O4 /RGO) (b ) electrodes at constant current densities of 0.1 A g −1 . Cycling performance of Fe3 O4 /RGO composites and M-Fe3 O4 /RGO composites electrode at constant current densities of 0.1 A g −1 (c ). Rate capability of Fe3 O4/ RGO composites and physically mixed Fe3 O4 /RGO composites at the current densities between 0.1 A g −1 and 2.4 A g −1 (d ). Nyquist plots of the electrodes of Fe3 O4 /RGO sheet and mechanically mixed Fe3 O4 /RGO composites. All of the measurements were conducted using a voltage window of 0.01–3.0 V (e ). Schematic representation of the electrochemical reaction path on the Fe3 O4 /RGO composites (f ).
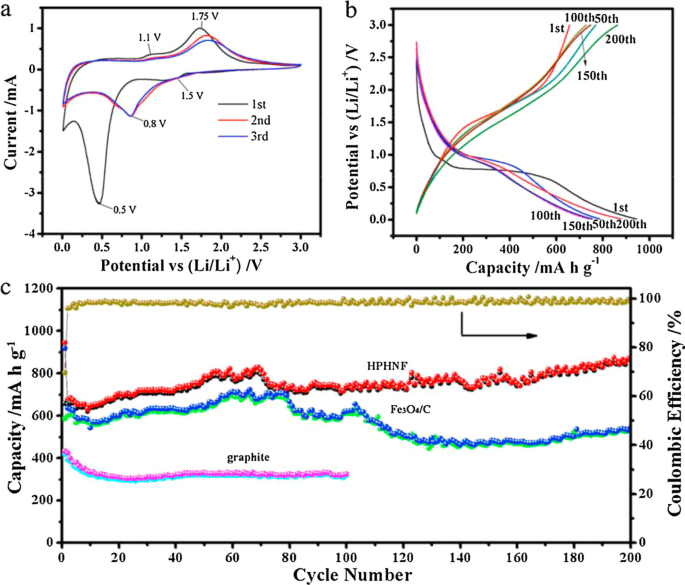
Pyrolyzed carbon is also a good “companion” for Fe3 O4 anodes. Apart from the facile protocol, porous structure formed by pyrolysis always exhibits high specific capacity of Fe3 O4 composite anode. Wang et al. [12] reported hollow N-doped Fe3 O4 /C nanocages with hierarchical porosities by carbonizing polydopamine-coated PB nanocrystals as LIBs anode (Fig. 12). The specific capacity of N-doped Fe3 O4 /C nanocages is ~ 878.7 mA h g −1 after 200 cycles at a current density of 200 mA g −1 , much higher than that of N-doped Fe3 O4 /C derived from pure PB (merely 547 mA h g −1 ). It is also desirable to design anisotropic structure of Fe3 O4 nanoparticles with carbon coated layer. Zhang y col. [19] reported a kind of carbon-coated Fe3 O4 nanospindles derived from α-Fe2 O 3 nanospindles with length of about 500 nm and an axis ratio of ~ 4. Following by a hydrothermal synthesis method with glucose, the obtained LIBs anode delivered a high reversible capacity of ~ 745 mA h g −1 at C/5 and ~ 600 mA h g −1 at C/2.
Reprinted with Permission from [12], Copyright, Elsevier Ltd
un CVs of the HPHNF during the first three cycles at 0.2 mV s −1 , b Galvanostatic charge/discharge profiles of the HPHNF electrodes for the 1st, 50th, 100th, 150th and 200th cycle at a specific current of 200 mA g −1 . c Cycling performance of the HPHNF nanocomposites, N-doped Fe3 O4 /C nanocomposites and graphite at a specific current of 200 mA g −1 . d Coulombic efficiency of HPHNF.
The most impressive work towards this field is probably the mesoporous iron oxide nanoparticle clusters with carbon coating reported by Lee et al. [148]. After a few cycles, the formation of SEI greatly enhanced the stability of interface between electrode and electrolyte. Electrochemical test exhibited a high specific capacity of 970 mA h g −1 for LIBs.
Supercapacitors
Fe3 O4 is a highly promising candidate for supercapacitor electrode because of its relatively high electrical conductivity, fast reversible redox reaction, low cost and eco-friendly nature [149,150,151,152]. Similar to batteries, high performance supercapacitors also require two factors:large specific surface area and long-term stability. Those two features usually were achieved by building some porous structures and carbon coated layers. Fe3 O4 nanoparticle with a high specific surface area was synthesized by Wang et al. [126] using a bottom up approach. Ferric chloride was firstly sonicated with ethanolamine and then processed through a solvothermal reaction. The obtained active nanomaterials showed a specific surface area of 165.05 m 2 g −1 and a specific capacitance of 207.7 F g −1 at 0.4 A g −1 .
Also, highly dispersed Fe3 O4 nanosheets on 1D CNFs is reported by Mu et al. [125]. The Fe3 O4 /CNFs composites showed a higher specific capacitance than pure Fe3 O4 in 1 M Na2 SO3 . To further enlarge the specific capacitance and cycle stability, hierarchically porous carbon spheres with Fe3 O4 using as supercapacitors exhibited high capacitivity of 1153 F g −1 at 2 A g −1 and high specific capacitance of 514 F g −1 at 100 A g −1 . In addition, the assembled asymmetric supercapacitor with double-shelled hollow carbon spheres and Fe3 O4 , has excellent cycling stability (96.7% retention after 8000 cycles) and high energy density (17–45 Wh kg −1 ) at a power density of 400–8000 W kg −1 [4].
Conclusion
Iron oxides (Fe1−x O, Fe2 O 3 , Fe3 O4 ) based nanostructures have much higher specific capacities than those of commercial carbon based anodes. They are considered as highly promising candidates for LIBs anode. However, large irreversible capacity and low cycle stability are two serious problems that obstruct the application of iron oxides based nanostructures. In this review, we summarized the recent progress on novel iron oxides and their composites as LIBs anode and supercapacitor electrode. Several typical synthetic methods of various novel iron oxides based nanostructures are listed. By comparing the electrochemical performance of these various iron oxides based nanostructures, some strategies are expected to solve the problems of iron oxides based nanostructures.
Disponibilidad de datos y materiales
Not applicable.
Nanomateriales
- Cervoz:elegir el almacenamiento flash adecuado para aplicaciones industriales
- Optimización de la IA para aplicaciones integradas
- PPA para aplicaciones de movilidad eléctrica
- Tres grandes preguntas para cualquiera que ingrese al campo del almacenamiento de energía
- Nanopartículas para la terapia del cáncer:avances y desafíos actuales
- Administración de medicamentos basados en células para aplicaciones de cáncer
- Progreso en nanoestructuras basadas en óxidos de hierro para aplicaciones en almacenamiento de energía
- Estimación del almacenamiento de energía del supercondensador basada en ecuaciones diferenciales fraccionales
- Evaluación de estructuras de grafeno / WO3 y grafeno / ceO x como electrodos para aplicaciones de supercondensadores
- Nanoestructuras de superficie formadas por separación de fases de película de nanocompuesto de polímero y sal metálica para aplicaciones antirreflectantes y superhidrofóbicas
- Preguntas y respuestas:pozos de petróleo y gas para almacenamiento de energía



