Evaluación de la toxicidad de las nanopartículas de PEG-PCCL e investigación preliminar sobre su efecto antitumoral de la carga de paclitaxel
Resumen
La eficacia del tratamiento único de los fármacos de quimioterapia convencionales se ve reducida de forma desagradable por las barreras fisiológicas de los tumores. En este sentido, las nanopartículas se han vuelto atractivas para lograr el propósito médico de la terapia dirigida contra el cáncer mediante la administración de agentes antitumorales al área necesaria. Se ha informado que un nuevo liberador de fármacos, el poli (etilenglicol) carboxil-poli (ε-caprolactona) (PEG-PCCL), es altamente hidrófilo y estable, aunque se sabe poco acerca de su toxicidad orgánica. Este estudio se centró en las evaluaciones de la toxicidad sistémica de PEG-PCCL. Se investigó preliminarmente la farmacocinética de PEG-PCCL (PEG-PCCL / PTX) cargado con PTX y su efecto antitumoral. En el presente trabajo, PEG-PCCL se caracterizó por un analizador de tamaño de partículas láser y microscopía electrónica de transmisión. La citotoxicidad se investigó mediante prueba MTT, ensayo de fuga de LDH, inmunofluorescencia y microscopía electrónica de transmisión. Se realizaron pruebas de hemólisis, flebitis y toxicidad orgánica para demostrar la biocompatibilidad y biotoxicidad aguda. Se utilizaron ratones portadores de tumor H22 para evaluar la farmacocinética de las micelas de PEG-PCCL / PTX y su efecto antitumoral. Los resultados mostraron que el tamaño de las nanoesferas de PEG-PCCL era 97 ± 2,6 nm. El tratamiento con PEG-PCCL mostró poca citotoxicidad y buena biocompatibilidad, y no mostró toxicidad orgánica. La eficiencia de carga de PTX fue del 49,98%. El estudio farmacocinético en ratones portadores de tumores H22 reveló que PEG-PCCL / PTX tiene una mayor estabilidad y una liberación más lenta que la PTX sola. Juntos, estos resultados sugieren que la nanoesfera de PEG-PCCL tiene poca toxicidad para los organismos y es un candidato potencial de vehículo de fármaco biocompatible para fármacos hidrófobos.
Introducción
La tendencia creciente de la incidencia del cáncer continúa junto con el aumento del envejecimiento de la población en las últimas décadas [1]. La eficacia de la quimioterapia convencional de los cánceres ha sido limitada, ya que sólo una pequeña parte de la dosis total llega al sitio del tumor, el resto de la cual se distribuye por los tejidos sanos, lo que produce efectos negativos, especialmente neutropenia y miocardiopatía [2]. Las nanopartículas representan una plataforma potencial para la administración de fármacos quimioterapéuticos debido a sus características físicas y químicas únicas [3]. Como resultado, se pueden lograr efectos secundarios reducidos y eficacia terapéutica mejorada. Se supone que los copolímeros basados en poli (etilenglicol) (PEG) y metoxi poli (etilenglicol) (MePEG) / poli (ɛ-caprolactona) (PCL) son nanopartículas orgánicas prometedoras utilizadas en sistemas de administración de fármacos (DDS), y ya se han utilizado aprobado por la FDA. Estas nanopartículas poseen características fáciles de controlar como biocompatibilidad, biodegradabilidad y termosensibilidad [4]. Algunos polímeros dibloque y tribloque se han investigado en aplicaciones biomédicas, como la nanoesfera PCL [5], PEG-PCL-PEG [6,7,8] y el hidrogel PCL-PEG-PCL [9]. Los bloques de PCL componen un núcleo hidrófobo que encapsula fármacos hidrófobos, mientras que los bloques de PEG forman una capa hidrófila, que produce nanoestructuras micelares núcleo-capa. Estos polímeros dibloques y tribloques atraen una atención considerable debido a características tales como estructura estable, duración prolongada en la circulación sanguínea y selección de objetivos pasivos por medio de un efecto mejorado de permeación y retención [10]. Sin embargo, todavía existen desafíos controvertidos de los polímeros orgánicos, incluida la toxicidad, la baja carga útil del fármaco, la fuga no deseada del fármaco y la eliminación por el sistema reticuloendotelial [11,12,13].
En comparación con los polímeros antes mencionados, el PEG-PCCL, uno que además es carboxilo modificado covalentemente en la caprolactona y ha sido preparado y caracterizado en nuestros estudios previos [14, 15], muestra una mayor hidrofilicidad y una mejor estabilidad a través del efecto del enlace de hidrógeno. . Aparte de los resultados de las características fisicoquímicas, se informaron pocos datos relacionados con el estudio de toxicidad in vivo e in vitro de vehículos poliméricos. No obstante, los modelos predictivos y los métodos estándar validados requieren un conjunto de reglas de diseño que involucran el ensayo de toxicidad de nanopartículas.
Dado eso, nos centramos aquí en la evaluación de la toxicidad aguda in vivo e in vitro de PEG-PCCL cualitativa y cuantitativamente a pesar de sus atributos favorables de alta tolerancia y biodegradabilidad in vivo. Una nanopartícula ampliamente utilizada en la investigación biomédica, la polieterimida (PEI), fue elegida como control positivo. El paclitaxel (PTX) es un fármaco anticanceroso de primera línea [16], especialmente un quimioterapéutico optimizado para el cáncer de ovario y el cáncer de pulmón de células no pequeñas, y se ha incluido en la Lista de medicamentos esenciales de la Organización Mundial de la Salud . Con el desarrollo de la nanotecnología, la carga de PTX en nanopartículas se considera una solución potencial para la administración de fármacos en un lugar específico en el marco de un tratamiento de cooperación multidisciplinar [17, 18]. En este estudio, se utilizó PEG-PCCL cargado con PTX para examinar la farmacocinética y su efecto antitumoral in vivo en un modelo de ratones con tumor hepático H22.
Métodos
Materiales, células y animales
ε-caprolactona (ε-CL, Alfa Aesar, EE. UU.), poli (etilenglicol) (PEG, Mn =1000, Fluka, EE. UU.), diisocianato de hexametileno (HMDI, Aldrich, EE. UU.), Palladium sur charbon (pd / c, Sigma , EE. UU.), Medio de Eagle modificado de Dulbecco (DMEM, Hyclone, EE. UU.), Bromuro de 3- (4,5-dimetiltiazol-2-il) -2,5-difenil tetrazolio (MTT, Sigma, EE. UU.), Albúmina de suero bovino (BSA , BR, BoAo Co. Ltd., China) sin purificación adicional. Todos los materiales eran de grado reactivo analítico.
Se compraron ratones macho Balb / C (de 7 a 8 semanas de edad, de 20 a 25 g de peso) y conejo de Nueva Zelanda (de 2,5 a 3,0 kg de peso) a las empresas de biotecnología de Chengdu DaShuo (Sichuan, China) con el certificado de calidad n.º SCXK2013– 24. Los animales se mantuvieron en un entorno libre de patógenos específicos estándar con suficiente comida y agua del grifo. Los experimentos se realizaron de acuerdo con la Guía para el cuidado y uso de animales de laboratorio (Ministerio de Ciencia y Tecnología de China, 2006). Todos los procedimientos experimentales con animales fueron aprobados por el Comité de Ética para Animales de Laboratorio del Centro Médico de China Occidental de la Universidad de Sichuan.
Se obtuvieron células de hepatocarcinoma de ratón H22 (H22), células de riñón embrionario humano (HEK293T) y células de carcinoma de hepatoma (Hep G2) del Departamento de Inmunología de la Facultad de Ciencias Médicas Básicas y Medicina Forense de China Occidental, Universidad de Sichuan. HEK293T y Hep G2 se cultivaron en medio Eagle modificado de Dulbecco (DMEM) (Hyclone, UT, EE. UU.), Complementado con suero de ternero fetal al 10% (FCS) (Hyclone, UT, EE. UU.) Y antibióticos (penicilina 100 U / ml y estreptomicina 100 U / mL) a 37 ° C en CO2 al 5%.
Preparación de micelios PEG-PCCL y PEG-PCCL cargados con PTX
Los PEG-PCCL y PTX-NP fueron suministrados por nuestro colaborador, el profesor Liu de la Escuela de Microelectrónica y Electrónica de Estado Sólido de la Universidad de Ciencia y Tecnología Electrónica de China. Los copolímeros dibloque de PEG-PCCL se sintetizaron mediante la polimerización por apertura de anillo de ɛ-CL en presencia de homopolímero de PEG con los catalizadores de paladio sur charbon como el diagrama de flujo siguiente (Fig. 1). Los copolímeros de PEG-PCCL obtenidos se purificaron y se guardaron en bolsas herméticas hasta su uso.
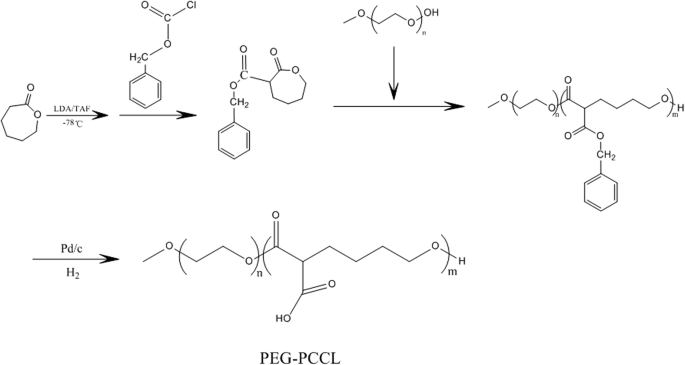
El diagrama de flujo de la síntesis del dipolímero PEG-PCCL
Para cargar PTX en nanopartículas de PEG-PCCL, se realizó una dispersión sólida, una técnica simple y valiosa sin solvente orgánico venenoso [19], después de que se preparó PEG-PCCL. Luego, la solución se evaporó a 60 ° C bajo presión reducida. Después de la evaporación del alcohol, se obtuvieron copolímeros homogéneos. La PTX se encapsuló mediante vehículos poliméricos en forma amorfa. La coevaporación se disolvió en agua a 65 ° C para producir una solución de PTX-NP, que se filtró con un filtro de 0,22 nm para obtener una solución clarificada y estéril. El polvo de PTX-NP se obtuvo de la solución liofilizada de un sistema de secado por congelación. La eficiencia de atrapamiento (EE) de PTX se determinó con el método de centrifugación en minicolumna [20]. Las concentraciones de PTX incorporadas en PEG-PCCL (C I ) o el fármaco total en dispersiones de PEG-PCCL (C T ) fueron analizados por HPLC. EE (%) =(C I / C T ) × 100%.
Caracterización
El tamaño de partícula y el potencial zeta de PEG-PCCL se midieron con un analizador de tamaño de partícula láser (Malvern Nano-ZS 90). Se utilizó microscopía electrónica de transmisión (TEM, H-6009IV, Hitachi, Japón) para evaluar la morfología de PEG-PCCL. Específicamente, la solución de nanopartículas se colocó sobre una rejilla de cobre cubierta con nitrocelulosa, y luego las muestras se tiñeron con ácido fosfotúngstico y se secaron a temperatura ambiente.
Ensayos de citotoxicidad
La citotoxicidad se evaluó mediante un ensayo de fuga de MTT y LDH en Hep-G2 y HEK293T. La metabolización de MTS se cuantificó en células intactas de acuerdo con el procedimiento de MTT [21]. Las suspensiones celulares se prepararon con tripsina / EDTA (HyClone, UT, EE. UU.). Un total de 0,4 × 10 4 las células se sembraron en una placa de 96 pocillos (Corning, MA, EE. UU.). Las placas se incubaron durante 12 h para permitir que las células se adhirieran a la superficie de plástico de las placas de cultivo. Luego, se retiró el medio y se agregaron a los pocillos 200 μl de medio de cultivo fresco o medio que contenía diferentes concentraciones de PEG-PCCL (de 0 a 1 mg / mL). No se añadió FCS al medio durante el período de exposición de 24 h. La tasa de supervivencia se determinó mediante parámetros de citotoxicidad y se presentó mediante la ecuación:Tasa de supervivencia (%) =(OD T / OD C ) × 100. Aquí, OD T y OD C se refieren al valor de absorbancia (medido con el lector de espectrofotómetro a 570 nm) de las células tratadas con nanopartículas de PEG-PCCL o PEI y de las células no tratadas, respectivamente.
La fuga de LDH en el medio de cultivo se examinó utilizando el kit de ensayo de LDH (Biotech, China). Todas las mediciones espectrométricas de los grupos tratados con nanopartículas se corrigieron mediante un control sin células. Para el estudio morfológico, las células HepG2 se sembraron y expusieron de la misma forma que en los ensayos de citotoxicidad. Las células se fijaron en paraformaldehído al 4% y se observaron bajo el microscopio electrónico de transmisión (TEM).
Ensayos de apoptosis
La apoptosis se determinó mediante tinción doble con Anexina V-FITC y PI [22]. Brevemente, las células HepG2 se sembraron en placas de 12 pocillos a una densidad de 4 × 10 4 células / pocillo y se trató con PEG-PCCL (0,5 mg / ml) y PEI (0,5 mg / ml) durante 48 h. Luego, las células se lavaron con solución salina tamponada con fosfato (PBS) fría tres veces seguido de incubación con Anexina V-FITC durante 15 minutos y tinción con PI durante otros 15 minutos a 4 ° C en la oscuridad. Las células teñidas se observaron con un microscopio de fluorescencia (Olympus Co. Ltd., Tokio, Japón) en 30 minutos.
Ensayo de hemocompatibilidad
La hemocompatibilidad de PEG / PCCL se evaluó de acuerdo con la prueba de hemólisis in vitro de glóbulos rojos (RBC) informada anteriormente [23]. Se recogieron las muestras de sangre de los ratones y se disolvieron los eritrocitos en PBS (solución de RBC al 2%). Se mezclaron solución salina fisiológica, PEI o PEG-PCCL de 0,5 mg / ml con la solución de RBC al 2%. Se preparó un control de hemólisis positivo agregando un volumen igual de suspensión de eritrocitos y agua destilada. Después de que la mezcla se mantuvo durante 1 y 3 ha 37 ° C y luego se centrifugó a 2000 r / min durante 5 min, los sobrenadantes se detectaron con un lector de microplacas (Bio-Rad, CA, EE. UU.) A 570 nm. El porcentaje de hemólisis se calculó mediante la ecuación:hemólisis% =(OD T –OD NC ) / (OD PC –OD NC ) × 100. Aquí, OD T , OD NC y OD PC se refieren a los valores de absorbancia de la muestra, el control negativo y el control positivo, respectivamente. Además, la hemólisis in vivo se analizó contando el número de glóbulos rojos de la muestra de sangre recolectada a través de la vena caudal de los ratones tratados con solución salina normal, PEI (20 mg / kg) o PEG-PCCL (20 mg / kg) durante 3 h.
Flebitis de conejo
Se emplearon venas en ambas orejas de conejos para comparar la infiltración de células inflamatorias y la degeneración epidérmica [24, 25]. Los conejos se dividieron aleatoriamente en dos grupos; a cada uno se le administró 1 ml de solución salina fisiológica o 0,5 mg / ml de PEG-PCCL a través de la vena auricular. Los conejos fueron sacrificados por una sobredosis de hidrato de cloral (4%, Sigma, EE. UU.) A las 24 h después de la infusión de nanopartículas. Se obtuvieron dos muestras de la vena de la oreja, incluida la región a 10-15 mm de la punta del catéter, tanto en sentido proximal como distal. Estas venas se fijaron en una solución de paraformaldehído al 4%. Luego se prepararon cortes transversales de parafina y se tiñeron con hematoxilina y eosina (HE). El examen histopatológico se realizó a ciegas. Los hallazgos se clasificaron de acuerdo con los criterios que se muestran en la tabla, que se basaron en los de Kuwahara [17] con la adición de la degeneración epidérmica.
Pruebas de función hepatorrenal
Después de 7 días de administración de PEG-PCCL (0.5 mL, 20 mg / kg) en ratones, las muestras de sangre se extrajeron del plexo venoso orbital (2 mL) y se centrifugaron inmediatamente a 1300 g, 4 ° C. Se extrajo el sobrenadante. Luego, los parámetros de bioquímica sérica [26], incluida la aspartato aminotransferasa (AST), la alanina aminotransferasa (ALT), la fosfatasa alcalina (ALP), la bilirrubi, la creatinina, el ácido úrico y la albúmina, se evaluaron utilizando un analizador bioquímico automático de animales (Dri-Chem 3000 , Fuji Photo, Tokio, Japón), que son indicadores indirectos de la función hepática y renal.
Examen histopatológico
Los cambios histopatológicos del pulmón, hígado y riñón se examinaron con tinción H&E a las 24 h, 48 h y 7 días después de la inyección de PEG-PCCL, solución de PEI o solución salina normal (0,5 ml, 20 mg / kg) a través de ratones. vena de la cola. Estos órganos se obtuvieron después del sacrificio de animales. La sección de histopatología y la tinción H&E se realizaron como se describe en otra parte [26]. Los cambios histopatológicos se observaron al microscopio óptico y se registraron con una cámara variada (Leica, Co. Ltd., Alemania).
Concentración en sangre
La concentración sanguínea de PTX se calculó usando un espectrofotómetro (LAMBDA 950, PerkinElmer, China). Se extrajeron muestras de sangre de la órbita de los ratones a las 0,08, 0,25, 0,5, 0,75, 1, 2, 6, 12, 24 h después del tratamiento. Se recogió el sobrenadante (100 μL) después de centrifugar a 1300 g durante 10 min. La concentración de PTX en cada muestra de sangre se determinó con un espectrofotómetro a 760 nm.
Modelos y tratamiento de tumores de ratón
Suspensión de células H22 (0,25 ml, 4 × 10 6 células / ratón) se inyectó intraperitonealmente en ratones Balb / C el día 0. Cuando se formó la ascitis (en el día 3 ~ 5), los ratones portadores de tumores se dividieron aleatoriamente en tres grupos ( n =5) y se inició el tratamiento. Los ratones se inyectaron con solución salina normal, PEG-PCCL / PTX (20 mg / kg) o PTX (10 mg / kg) por vía intraperitoneal a un volumen de 0,5 ml en los días 3 y 10 para evaluar la eficacia antitumoral. El perímetro abdominal (AP) se midió todos los días para calcular el porcentaje aumentado de AP (IPAP) como la siguiente formulación:IPAP =( P n - P 0 ) / P n . El día 10, los ratones supervivientes se sacrificaron mediante dislocación cervical, y se recogió y pesó la ascitis. Se observó el tiempo de supervivencia de los ratones hasta el día 20. Los ratones portadores de tumores se ejecutaron en el punto final con signos de angustia, que incluían una frecuencia respiratoria alta, alboroto, postura encorvada, actividad reducida y formación progresiva de ascitis [27]. La actividad antitumoral se evaluó de forma exhaustiva mediante los días de supervivencia, el perímetro abdominal y el volumen de ascitis. Los ratones se alimentaron en condiciones estándar de laboratorio.
Análisis estadístico
El análisis estadístico se realizó con SPSS 19.0 (IBM, NY, EE. UU.). Cada tratamiento experimental se repitió de forma independiente durante al menos tres veces. Los datos se presentaron como media ± desviación estándar (DE). Se utilizó el análisis de varianza (ANOVA) para el análisis estadístico. El grado de cada hallazgo de flebitis se analizó mediante la prueba de suma de rangos de Wilcoxon. Se utilizó la prueba de Dunnett para comparar las intervenciones individuales. La significancia estadística se indicó en P <0.05.
Resultados
Morfología, diámetro y potencial zeta de PEG-PCCL
Los resultados del analizador de tamaño de partículas por láser mostraron que el diámetro medio de PEG-PCCL era 97 ± 2,6 nm. Los resultados de TEM de PEG-PCCL (Fig. 2) revelaron que PEG-PCCL tenía formas esféricas y uniformes en la solución. El potencial zeta medio de PEG-PCCL fue - 18,4 mV. El método de centrifugación en minicolumna mostró que el% de EE fue del 55,98%.

La característica de la imagen PEG-PCCL:TEM. Las barras de escala eran de 100 nm
Citotoxicidad
La citotoxicidad de PEG-PCCL se evaluó comparándola con PEI, un vehículo típico a nanoescala, en líneas celulares HEK293T y Hep-G2. Dentro del rango de concentración (de 0 a 1 mg / mL) de PEG-PCCL o PEI, la viabilidad de las células HEK293T (Fig. 3a) y las células tumorales (Hep-G2) (Fig. 3b) descendió en una concentración dependiente manera. Las células embrionarias parecían más sensibles a la concentración de 0,25 mg / mL, mientras que las células tumorales sobre 1 mg / mL. En comparación con PEI, PEG-PCCL mostró menos citotoxicidad, especialmente a concentraciones más altas, es decir, 0,75 y 1 mg / ml ( P =0,023). El ensayo de LDH mostró que la tasa de muerte tanto en células embrionarias como en células tumorales aumentó con el tiempo de exposición; (i) fue 19 y 42% a las 24 y 48 h, respectivamente, a 0,5 mg / ml de PEG-PCCL (Fig. 3c) menos que la de PEI. (ii) Las células tumorales mostraron una tasa de muerte ligeramente menor (32%) en el momento de 48 h cuando las células se expusieron a PEG-PCCL en comparación con PEI ( P =0.037) (Fig. 3d).
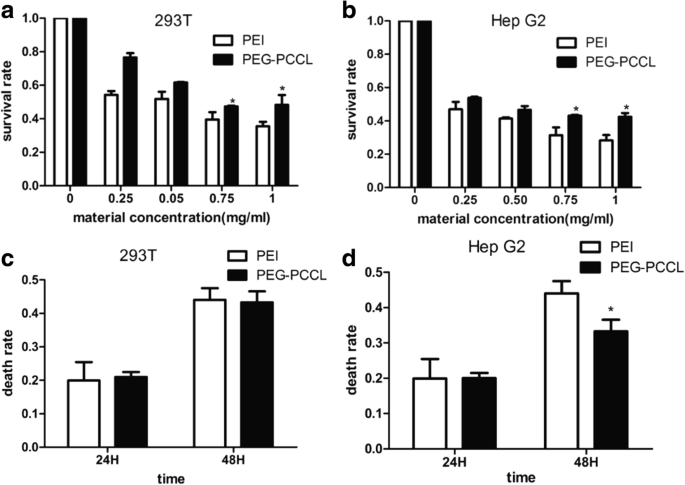
La citotoxicidad de PEG-PCCL en comparación con PEI. un , b El ensayo MTT mostró la tasa de supervivencia de 293 T y la concentración de HepG2 de forma dependiente en comparación con el grupo controlado negativo (PEI). c , d Ensayo de fuga de LDH de 293 T y HepG2 que se exponen a PEG-PCCL y PEI después de 48 h. * P <0,05 frente al grupo de PEI
SEM
Las imágenes de microscopía electrónica de células Hep-G2 intactas y células tratadas con nanopartículas de PEG-PCCL se muestran en la Fig. 4. En las células Hep-G2 intactas, había abundantes microvellosidades (Mv) en cada superficie, y el núcleo (N) estaba ubicado más hacia las bases que hacia la porción apical. Numerosas mitocondrias (Mt), complejo de Golgi (Go) y retículo endoplásmico rugoso (RER) se distribuyeron en el citoplasma. En las células tratadas con PEG-PCCL, las vesículas pinocitóticas aumentaron definitivamente. No se observaron cambios histopatológicos significativos y los organelos redondos N y citoplasmáticos, incluidos Mt, RER y Go, estaban intactos.
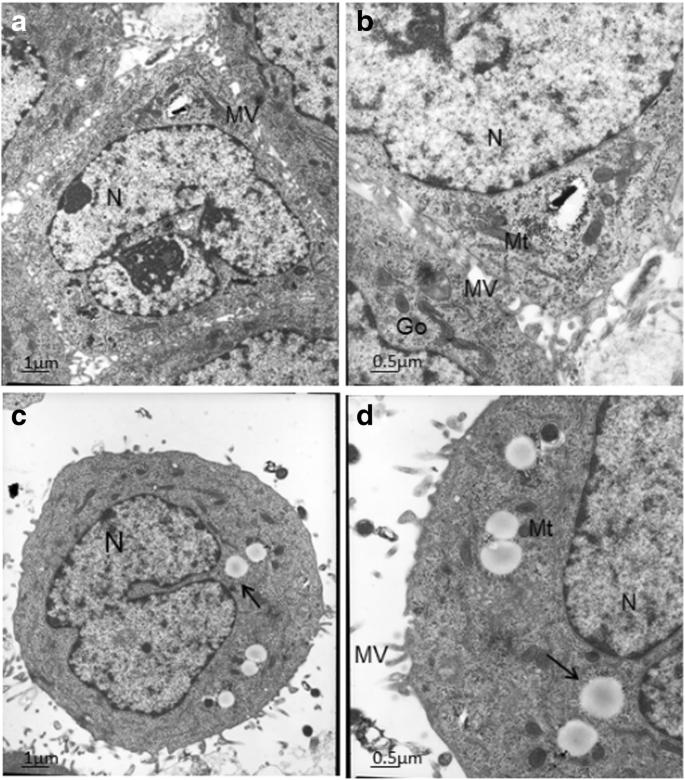
Micrografías de electrones. un , b Células HepG2 normales. c , d Células tratadas con nanopartículas de PEG-PCCL mediante SEM (microscopio electrónico de barrido). La flecha oscura apunta a las vesículas pinocitóticas
Apoptosis
La disminución significativa de la viabilidad celular puede estar correlacionada con las características del tamaño de partícula, la química de la superficie y la concentración [28], lo que motivó nuestro interés en los mecanismos subyacentes a la muerte celular observada en las células HepG2. Para determinar si la muerte celular se atribuyó a apoptosis o necrosis, las células HepG2 se trataron con PEI o PEG-PCCL para la tinción conjunta de Anexina V y PI. Como se observó bajo el microscopio de fluorescencia (Fig.5), las células tratadas con PEI o PEG-PCCL mostraron una apoptosis más temprana en comparación con el grupo de control en blanco, como lo indica la fluorescencia verde teñida con anexina V.Las células tratadas con PEI exhibieron una apoptosis más potente que las de PEG-PCCL, que estaba en línea con el resultado anterior del ensayo MTT.
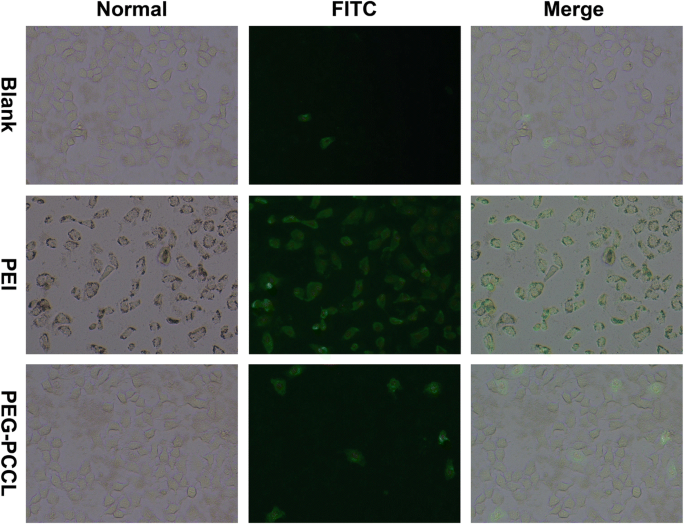
La tinción de FITC-anexina V representó la apoptosis celular. Se obtuvieron imágenes de células HepG2 incubadas con nanopartículas a una concentración de 0,5 mg / ml durante 48 hy luego teñidas conjuntamente con yoduro de propidio (rojo) y anexina V (verde) a × 40
Biocompatibilidad
Hemólisis
Dado que las nanopartículas biocompatibles están diseñadas para aplicaciones endovasculares, se requieren investigaciones de hemocompatibilidad y citotoxicidad endotelial. La prueba in vitro mostró que, durante las 3 h de observación, la hemólisis aumentó con el tiempo, en el que PEG-PCCL exhibió una relación de hemólisis más baja que la solución salina normal (Fig. 6a). La prueba in vivo reveló una tendencia similar. Por el contrario, PEI causó hemólisis severa tanto in vitro como in vivo (Fig. 6b).
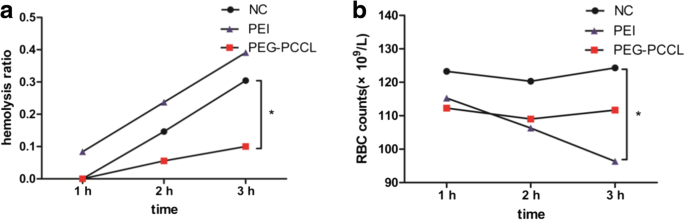
Relación de hemólisis y recuento de células (× 10 9 / L) de muestra de sangre en 3 h. In vitro ( a ) in vivo ( b ) * P <0,05 frente al grupo de control negativo
Flebitis de conejo
El examen histopatológico (Fig. 7) mostró un endotelio vascular intacto sin necrosis de cronocitos en el cartílago auricular. Se observó poco edema de la parte proximal de la vena. Con respecto a la pérdida de células endoteliales venosas y la infiltración de células inflamatorias, la co-infusión (Tabla 1) de los grupos tratados con PEG-PCCL después de 12 y 24 h tendió a aumentar, pero la mejora no fue estadísticamente significativa ( P > 0,05).
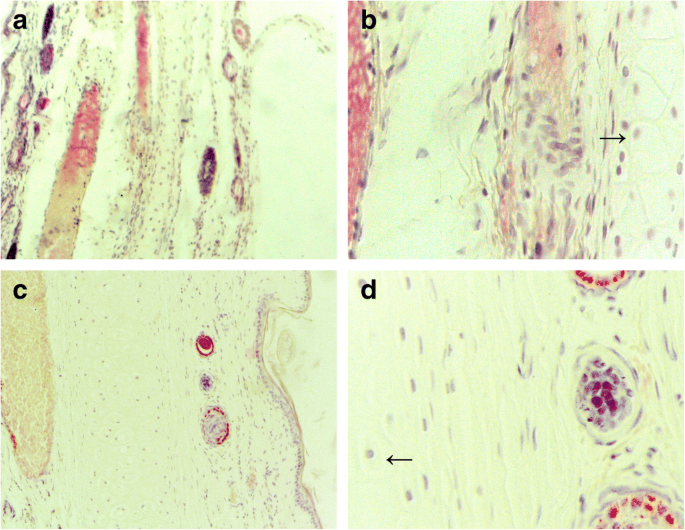
Microfotografías de la vena de la oreja después de la infusión de 24 h teñidas con H&E. un , b Grupo de infusión con suero fisiológico. c , d Grupo de infusión con PEG-PCCL. Las agujas representan el cartílago auricular. (Imagen izquierda × 10, imagen derecha × 40)
Toxicidad en órganos
Para evaluar la toxicidad aguda de PEG-PCCL en los órganos principales, se realizó un examen histopatológico en el pulmón, el hígado y el riñón después de la administración intravenosa de PEG-PCCL a 0,5 mg / ml durante 3 días en ratones ( n =5). Se utilizaron como controles solución salina normal y PEI. Los resultados mostraron que la PEI provocó una ligera inflamación y un espesor del intersticio lobulillar y cariopyknosis de los hepatocitos (Fig. 8). Aunque, en comparación con el grupo de solución salina normal, no se observaron cambios histopatológicos aparentes en todos los órganos examinados en el grupo tratado con PEG-PCCL (Fig. 7); Se examinó la función hepatorrenal para confirmar más su no toxicidad (Tabla 2).
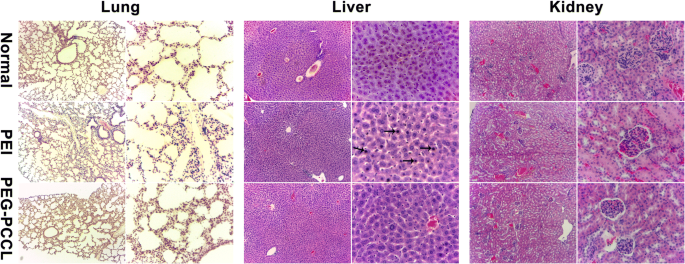
Las imágenes microscópicas de luz de teñido H&E del pulmón, el hígado y el riñón. Las imágenes se recogen de ratones a los que se les administró por vía intravenosa NS, PEI y PEG-PCCL. Las agujas representan la cariopyknosis de los hepatocitos. (Imágenes de las columnas de la izquierda, × 10; imágenes de las columnas de la derecha × 40)
Estudio farmacocinético
El estudio farmacocinético se realizó después de la inyección intravenosa de 10 mg / kg de PTX de Taxol® o 20 mg / kg de PEG-PCCL / PTX (PP + PTX) (relación de carga del 50%). El pico de concentración plasmática (Cmax) fue 312 ± 2,59 μg / mL (PTX) y 283 ± 2,79 μg / Ml (PP + PTX). El tiempo de concentración máxima (Tmax) y el área bajo la curva concentración plasmática-tiempo fueron 0.54 ± 0.20 h, 52.00 ± 4.30 μg h / mL y 4 ± 1.22 h, 282.21 ± 21.08 μg h / mL para PTX y PTX-NPs , respectivamente. La curva de concentración en sangre-tiempo se muestra en la Fig. 9.
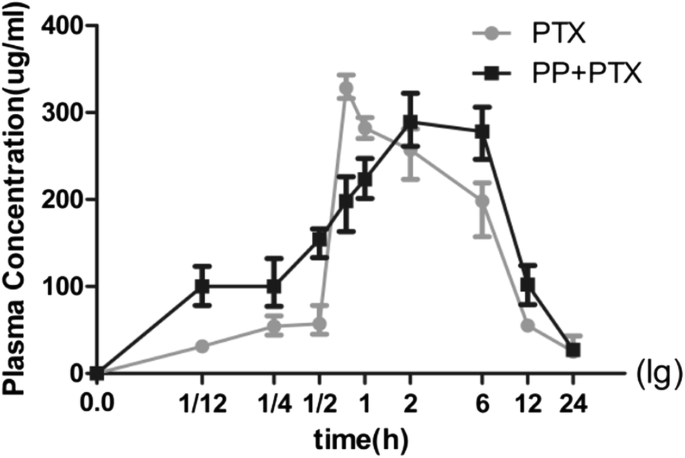
La curva de concentración en sangre-tiempo. En ratones después de la administración intravenosa de PTX o PP + PTX. ( n =6)
Efecto de PEG-PCCL / PTX en ratones portadores de tumores
Para investigar el efecto antitumoral de PEG-PCCL / PTX in vivo, (i) se calculó diariamente el porcentaje aumentado de perímetro abdominal (IPAP) de ratones portadores de tumor H22 (Fig. 10a). En el día 3, la ascitis comenzó a formarse y la IPAP de cada grupo aumentó drásticamente, en el que el grupo PP / PTX y el grupo PTX, en comparación con el grupo NS, mostraron un aumento más lento con el tiempo. (ii) Se recogió ascitis el día 10 y se midió el volumen (Fig. 10b). En comparación con el grupo NS, el volumen de ascitis tanto del grupo PTX como del grupo PP / PTX se redujo significativamente ( P =0.0005 y P =0.0052), donde el grupo PP / PTX exhibió un volumen más bajo que el grupo PTX ( P =0,0138). (iii) la supervivencia de cada grupo se observó durante 20 días a partir del día 0. El grupo PP / PTX y el grupo PTX tuvieron una vida útil más larga y una tasa de supervivencia más alta que el grupo NS.
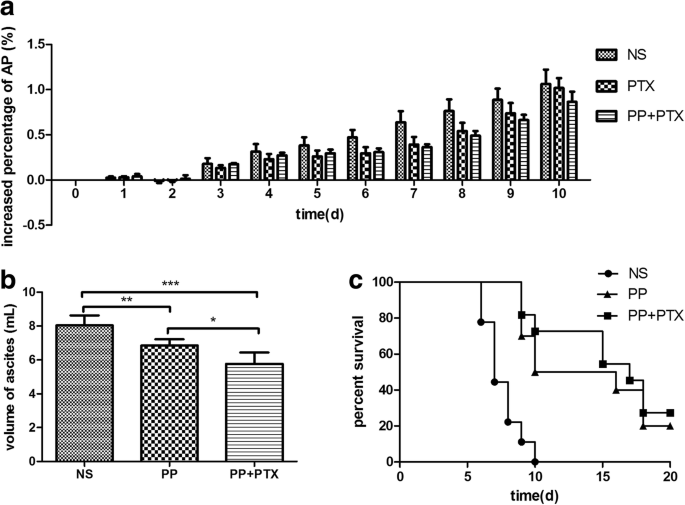
El efecto antitumoral de PP / PTX en ratones portadores de tumores H22. un Ratones Balb / C ( n =5) se inyectaron intraperitonealmente con PP / PTX o PTX el día 3. b Ascitis de cada grupo ( n =5) se recogieron el día 10. c La supervivencia de cada grupo ( n =10) se observó diariamente. * P <0.05, ** P <0.01, *** P <0,001
Discusión
Se ha sugerido que muchos polímeros, incluido el PEI, son portadores de fármacos químicos y biofarmacéuticos para una conjugación adecuada. PEI es un polímero catiónico ampliamente investigado y se ha considerado el estándar de oro en ensayos con respecto a la eficacia de la transfección [29]. Sin embargo, los efectos secundarios (p. Ej., Citotoxicidad) impiden que se aplique PEI en uso médico. Para buscar un material basado en nanopartículas más seguro y eficaz, hemos preparado con éxito un nuevo candidato para la administración de fármacos; El PEG-PCCL se caracteriza por una alta hidrofilia y una estabilidad favorable debido al efecto del enlace de hidrógeno. El objetivo principal del estudio fue evaluar la toxicidad in vivo e in vitro de PEG-PCCL, que abre una ventana potencialmente terapéutica para el tratamiento del cáncer.
Dado que la permeabilidad mejorada y el efecto de retención se consideran mecanismos de administración selectivos de tumores, se ha prestado considerable atención a los fármacos de tamaño nanométrico [30, 31]. Las nanopartículas de menor diámetro tienen mejor inmunocompatibilidad [32] y menor absorción por el hígado, mayor tiempo de circulación sanguínea y mayor biodisponibilidad [33]. Nuestros dipolímeros son de tamaños apropiados (97 ± 2,6 nm) (Fig. 2) para penetrar en y fuera del vaso sanguíneo del tumor, así como evadir el sistema inmunológico del huésped, mientras que se informó que los polímeros catiónicos con el potencial zeta positivo eran tóxicos [34]. Esta toxicidad de PEG-PCCL con potencial zeta negativo se suponía que debía evitarse idealmente. De hecho, en las evaluaciones de toxicidad del presente estudio, hubo pocas preocupaciones sobre la toxicidad con PEG-PCCL. Otro laboratorio también informó resultados similares [35,36,37].
Los experimentos in vitro revelaron una propiedad libre de toxicidad para PEG-PCCL. Como se observa en SEM (Fig. 4), (i) las vesículas pinocitóticas reconocidas por la flecha oscura indicaron una endocitosis susceptible [38]. (ii) El núcleo completo y los orgánulos intactos (Mt, RER y Go) mostraron poca citotoxicidad y buena biocompatibilidad de PEG-PCCL a nivel celular. En el ensayo de MTT y el ensayo de fuga de LDH (Fig.3), PEI y PEG-PCCL condujeron a una tendencia similar de viabilidad celular de una manera dependiente de la dosis y el tiempo tanto en las células T 293 como en las células HepG2, aunque el PEG-PCCL mostró una menor citotoxicidad, especialmente a concentraciones más altas ( P <0,05). Estos resultados sugirieron que la unión covalente del carboxilo no aumenta la toxicidad adicional. La hemólisis in vitro está ampliamente aceptada como un método útil y confiable para evaluar la compatibilidad sanguínea de NP. En la prueba de hemólisis in vitro, el PEG-PCCL mostró una relación de hemólisis más baja que la solución salina normal (Fig. 6a). Esto puede deberse al potencial negativo de PEG-PCCL que protege las células sanguíneas. La prueba de hemólisis in vivo reveló una tendencia similar. En contraste, PEI exhibió hemólisis severa. Collectively, PEG-PCCL nanoparticles are hemocompatible as they did not exhibit any hemolytic effect neither in vitro nor in vivo model (Fig. 6b).
The innoxious nature of PEG-PCCL was further proved by in vivo experiments. Since phlebitis induced by intravenously administered antineoplastic agents [24] is frequently seen in clinical practice, we tested the inflammatory reaction after PEG-PCCL injection. In the rabbit phlebitis study (Fig. 7), little inflammatory infiltration or tissue edema was observed, indicating that the new formulation of chemotherapeutic drugs captured by PEG-PCCL is biocompatible, and that co-infusion of PEG-PCCL could be a favorable candidate as intravenous drug deliverer. Meanwhile, in the H&E staining assay (Fig. 8), no obvious histopathological changes of organs were observed in PEG-PCCL nanoparticles treatment group compared to normal group. Further hepatorenal function was investigated for safety evaluation (Table 2), in which no significant differences were shown between normal saline group and PEG-PCCL group. Consequently, it is evident that PEG-PCCL is a kind of safe and non-toxic nanoparticles with potentiality to be applied in targeting intervention.
Furthermore, preliminary evaluation of drug-loaded effect in regard of pharmacokinetics and anti-tumor was carried out in H22 tumor-bearing mice. In the pharmacokinetic study (Fig. 9), Tmax of PP + PTX was 4 ± 1.22 h, which exhibited better persistence than that of PTX (0.54 ± 0.20 h). PP + PTX also performed larger area under the plasma concentration-time curve than PTX. These results showed that PEG-PCCL/PTX lasted longer than PTX alone in blood, which indicated higher stability and more delayed release of PEG-PCCL/PTX. However, the EE% of PEG-PCCL was dissatisfactory (55.98%) and sustained drug release was less than ideal (4 ± 1.22 h). Therefore, more research is needed to modify the nanoparticle to achieve a higher EE and longer drug release. For example, adjusting the proportion of PEG and PCCL can be considered [39]. Although no metastasis was seen in abdominal organs in our model, tissue distribution and concentration of PTX-NPs should be investigated in further study to find out the possible side effects. Moreover, the combination of PEG-PCCL and PTX made an improvement in life expectancy and a reduction in tumor ascites formation (Fig. 10). Notably, the anti-tumor effect was enhanced when PTX was loaded with PEG-PCCL, suggesting a possibility of a promising drug carrier. Besides, nanoparticles may be beneficial to confront anti-tumor drug resistance. Modification with folate [40] has been reported to overcome TLR4 driven chemotherapy resistance, and its co-encapsulation of anti-tumor agents [41] could be a promising option. Nanoparticle modified by additional Fe3 O 4 [42] may be more easily guided to its targets under the applied magnetic field, which would lower chemotherapeutic drugs-induced systemic toxicity [43].
Conclusions
PEG-PCCL nanospheres showed less cytotoxicity and better biocompatibility than mature medical nanoparticles (PEI) at the therapeutical concentration. PEG-PCCL-loaded PTX revealed higher stability and slower release in tumor mice. These results suggest that PEG-PCCL is a potential candidate of biocompatible drug vehicle for hydrophobic drugs.
Nanomateriales
- La interacción giro-órbita de Coin Paradox mejora el efecto magnetoóptico y su aplicación en el aislador óptico integrado en el chip
- Nanopartículas para la terapia del cáncer:avances y desafíos actuales
- Preparación y propiedades magnéticas de nanopartículas de espinela de FeMn2O4 dopadas con cobalto
- Nanopartículas como bomba de eflujo e inhibidor de biopelícula para rejuvenecer el efecto bactericida de los antibióticos convencionales
- La posible toxicidad hepática, cerebral y embrionaria de las nanopartículas de dióxido de titanio en ratones
- La preparación de la nanoestructura yema-cáscara de Au @ TiO2 y sus aplicaciones para la degradación y detección del azul de metileno
- Influencia de la rigidez elástica y la adherencia de la superficie en el rebote de nanopartículas
- Avances recientes en métodos sintéticos y aplicaciones de nanoestructuras de plata
- Toxicidad de nanopartículas de CoFe2O4 recubiertas de PEG con efecto de tratamiento de curcumina
- Efecto del agente peptizante ácido sobre la relación anatasa-rutilo y el rendimiento fotocatalítico de nanopartículas de TiO2
- Nanopartículas de oro de forma redonda:efecto del tamaño de partícula y la concentración sobre el crecimiento de la raíz de Arabidopsis thaliana



