Preparación y caracterización de nanopartículas de hemina en forma de renacuajo y esfera para mejorar la solubilidad
Resumen
Hemin es un potente suplemento de hierro. Una limitación importante de la aplicabilidad de la hemina es su solubilidad y biodisponibilidad en agua extremadamente bajas. El objetivo de este trabajo es preparar nanopartículas de hemina con mejor solubilidad. Imágenes de microscopio electrónico de emisión de emisión mostraron que nanopartículas de hemina con diferentes concentraciones iniciales de hemina (0,1 y 0,5 mg / ml) tenían forma de renacuajo (cabeza de aproximadamente 200 nm y cola de 100 nm) y forma de esfera (50-100 nm), respectivamente. Además, las nanopartículas de hemina mostraron una mayor solubilidad que la hemina libre. La solubilidad de las nanopartículas en forma de esfera fue 308,2 veces mayor que la de la hemina pura a 25 ° C. Las nanopartículas de hemina eran estables en condiciones ácidas y mostraban una excelente estabilidad térmica. Estos resultados sugirieron que las nanopartículas de hemina podrían servir como un posible suplemento de hierro con aplicaciones potenciales en los campos de la terapia alimentaria, biomédica y fotodinámica-fototérmica.
Introducción
El hierro es un elemento esencial en los procesos metabólicos del cuerpo, como la transferencia, el almacenamiento y el transporte de oxígeno de electrones [1]. La deficiencia de hierro es una de las deficiencias nutricionales más comunes y afecta aproximadamente al 20% de la población mundial [2]. La consecuencia más negativa de la deficiencia de hierro es la anemia sideropénica. Se debe principalmente a una ingesta dietética insuficiente de hierro, a menudo cuando la demanda es alta. En los seres humanos, el hierro de la dieta puede ingresar al cuerpo en dos formas principales:una es hierro inorgánico (hierro no hemo), liberado principalmente de vegetales y alimentos de origen vegetal, y la otra es hierro hemo, adquirido a partir de la descomposición de la hemoglobina o mioglobina presente en animales. La hemina se ha encontrado en la sangre y los productos cárnicos, es un componente de muchas hemoproteínas (incluidas la mioglobina, la hemoglobina y los citocromos byc) y se absorbe dos o tres veces más fácilmente (50-87%) que el hierro no hemo [3]. . Recientemente, los investigadores han sido testigos de importantes avances en nuestra comprensión del papel fisiológico de la hemina. Desafortunadamente, la hemina es hidrófoba debido a la presencia de un gran macrociclo tetrapirrólico [4]. Debido a la alta hidrofobicidad y la escasa solubilidad de la hemina en solución acuosa neutra, su aplicación en diversos campos ha sido limitada. Por lo tanto, existe una necesidad urgente de aumentar la solubilidad de la hemina.
Para abordar este desafío, se han dedicado muchos esfuerzos a mejorar la solubilidad de la hemina. Berner [5] descubrió que la proteína en solución enzimática parcial (aislado de soja, harina de soja o concentrado de soja) podía unirse con el hierro hemo para mejorar la absorción de hierro, lo que mejoraba la biodisponibilidad del hierro. Wang y col. [6] indicó que la hemina cristalina y el L-arginato podrían preparar la coacervación de hemina-arginato soluble en agua, que podría usarse como un nuevo suplemento de hierro hemo en aditivos alimentarios, alimentos funcionales y productos farmacéuticos. Zhang y col. [7] informó que la hemina podría combinarse con la β-ciclodextrina mediante un oligosacárido cíclico de siete unidades de glucosa ligadas a α [1, 4], lo que conduce a una mejora significativa en la solubilidad de la hemina. Aunque hubo algunos avances en la mejora de la solubilidad del hierro hemo, la industrialización no fue fácil debido al complicado proceso de preparación. Por lo tanto, desarrollar un método simple para mejorar la solubilidad de la hemina sigue siendo un gran desafío.
La nanociencia y la nanotecnología tienen el potencial de proporcionar nuevas soluciones en el desarrollo de sustancias funcionales, en particular la inclusión de compuestos bioactivos sin afectar la percepción sensorial de los consumidores y mejorando la absorción de ciertos componentes [8]. Las nanopartículas tienen varias ventajas [9], incluida la promoción de la solubilidad de sustancias hidrófobas [10]. Duhem y col. [11] desarrolló nanomedicinas novedosas basadas en vitamina E a través de nanotecnologías, que ofrecían múltiples ventajas en la administración de fármacos como biocompatibilidad, mejor solubilidad del fármaco y actividad anticancerígena. Chang y col. [12] informó que las nanopartículas preparadas por cadenas cortas de glucano modificadas con anhídrido succínico podrían cargar luteína hidrofóbica, lo que podría mejorar la solubilidad en agua de la luteína. A pesar del enorme potencial de las nanopartículas, aún no se ha informado de la hemina a nanoescala. Postulamos que la solubilidad de las nanopartículas de hemina podría aumentar en comparación con la hemina libre, que podría tener aplicaciones valiosas.
El objetivo principal del presente trabajo es desarrollar nanopartículas de hemina de diferentes formas utilizando una técnica de diálisis fácil y mejorar su solubilidad. Se evaluaron los parámetros de preparación de la concentración inicial de hemina y las condiciones de diálisis. Además, se evaluó la solubilidad y estabilidad frente al pH, el tratamiento térmico y la sal de las nanopartículas de hemina formadas. En general, las mejoras en la solubilidad de la hemina tienen una variedad de campos de aplicación potenciales.
Materiales y métodos
Materiales
Se adquirieron hemina y membranas de diálisis con un límite de peso molecular de 8-12 kDa de Beijing Solarbio Science &Technology Co., Ltd. (Beijing, China). Acetona (CH 3 COCH 3 , ≥ 99,5%) se adquirió de Kant Chemical Co., Ltd. (Laiyang, China). Todos los demás reactivos utilizados fueron de calidad analítica.
Preparación de nanopartículas de hemín
Las nanopartículas de hemina se prepararon utilizando un método de diálisis:0,1 mg / ml (o 0,5 mg / ml) de hemina disueltos en acetona acidificada con 0,1 ml de ácido clorhídrico concentrado. La solución de hemina se dializó por diferentes días, el agua se cambió todos los días y se liofilizó para obtener nanopartículas de hemina. Para determinar el efecto de los parámetros variables en la preparación de nanopartículas de hemina, las relaciones de volumen de hemina / agua se establecieron en 1:3, 1:5, 1:10 y 1:50; las temperaturas de cultivo se fijaron entre 4 y 25 ° C; y los tiempos de incubación se establecieron en 1, 3 y 5 días.
Microscopía electrónica de transmisión (TEM)
Las imágenes TEM de nanopartículas se tomaron con un microscopio electrónico de transmisión 7700 (Hitachi, Tokio, Japón) con un voltaje de aceleración de 80 kV. Se depositó una pequeña gota de muestra sobre una rejilla de cobre recubierta de carbono y luego se liofilizó para su observación.
Mediciones de tamaño medio y potencial zeta
El tamaño medio, el potencial zeta (potencial ζ) y el índice de polidispersidad (PDI) de las partículas se midieron mediante dispersión de luz dinámica (DLS), utilizando un Malvern Zetasizer Nano (Malvern Instruments Ltd., Reino Unido). Las muestras se diluyeron en agua MilliQ y se analizaron a 25 ° C. La concentración de muestras diluidas fue 0.05%.
Espectro de absorción UV-Vis
Las mediciones de espectroscopía UV-Vis de las nanopartículas de hemina libre y hemina disueltas en acetona acuosa acidificada se llevaron a cabo en un espectrofotómetro UV-Vis (TU-1810, Beijing, China). La absorción molecular se escaneó a una longitud de onda de 200 a 800 nm a intervalos de 1 nm para obtener un espectro.
Ensayo de solubilidad
La solubilidad acuosa cuantitativa de hemina pura y nanopartículas se investigó de acuerdo con el método informado por Gidwani et al. [13]. Brevemente, se añadieron por separado soluciones sobresaturadas de hemina pura y nanopartículas a 5 ml de agua desionizada en tubos de ensayo, respectivamente. Los tubos de ensayo se agitaron constantemente (500 rpm) a diferentes temperaturas (25, 37, 60 y 80 ° C) durante 30 min. Luego, la solución se centrifugó a 3500 g y el sobrenadante se diluyó adecuadamente con acetona acuosa acidificada. La concentración de las muestras se determinó a 640 nm mediante un espectrofotómetro UV-Vis. Para cada medición, la línea de base se estableció utilizando acetona acuosa acidificada en blanco como referencia.
pH, temperatura y estabilidad de la sal
Se midieron el tamaño, el potencial ζ, el PDI y la turbidez de las nanopartículas (0,5 mg / mL) y se compararon con los valores iniciales para evaluar la estabilidad de las nanopartículas. Las suspensiones de partículas se dividieron en diez grupos:seis grupos se ajustaron a los valores de pH deseados [2, 3, 5, 7, 9, 11], y utilizando ácido clorhídrico (0,1 M) o solución de hidróxido de sodio (0,1 M); tres grupos se calentaron a 25, 60 y 80 ° C y luego se enfriaron a temperatura ambiente; otro se realizó con diferentes concentraciones de cloruro de sodio (NaCl, 0, 10, 50, 100, 250 y 500 mM), respectivamente. Las soluciones mezcladas se dejaron reposar durante la noche a 25 ° C.
Espectroscopia infrarroja por transformada de Fourier (FTIR)
Las estructuras químicas de las nanopartículas de hemina se confirmaron usando espectros FTIR (Tensor 27, Jasco Inc., Easton, MD, EE. UU.). Un total de 32 escaneos con una resolución de 4 cm - 1 se acumularon utilizando el software de escaneo rápido en OMNIC 8.0 para obtener un solo espectro. El rango espectral fue de 400 a 4000 cm - 1 .
Espectroscopia de fluorescencia
Las mediciones de fluorescencia de hemina libre y nanopartículas se realizaron utilizando un espectrofotómetro de fluorescencia (F-7000, Hitachi, Japón). Los espectros de fluorescencia de las muestras se obtuvieron a longitudes de onda entre 300 y 600 nm con excitación a 402 nm.
Difractograma de rayos X (XRD)
La XRD de hemina libre y nanopartículas se obtuvo utilizando un difractómetro de rayos X (AXS D8 ADVANCE; Bruker, Karlsruhe, Alemania), y las muestras se investigaron en el 2 θ rango de 4–40 °. La cristalinidad relativa de la hemina libre y las nanopartículas se determinó trazando la línea base de los picos en el difractograma y calculando el área usando el visor de espectro de software basado en el método informado por Jivan et al. [14]. El área por encima y por debajo de la curva correspondía a dominios cristalinos y regiones amorfas, respectivamente. La relación entre el área superior y el área total se tomó como la cristalinidad relativa:
Cristalinidad relativa (%) =Área bajo los picos / Área total de la curva × 100.
Análisis estadístico
Se obtuvieron muestras por triplicado de todos los resultados cuantitativos. Los resultados se informaron como valores medios y desviaciones estándar. El análisis estadístico se realizó mediante pruebas de rango múltiple de Duncan utilizando el paquete de software estadístico SPSS V.17 (SPSS Inc., Chicago, IL, EE. UU.).
Resultados y discusión
Formación y caracterización de nanopartículas de hemin
TEM examinó la morfología y el tamaño de las nanopartículas de hemina fabricadas mediante el método de diálisis. Cuando la concentración de hemina fue de 0,5 mg / ml, se formaron nanoestructuras de hemina con diferentes tamaños en varias proporciones de volumen de hemina / agua y para diferentes días de diálisis (Fig. 1, archivo adicional 1:Figura S1-S3). Las nanopartículas tenían formas esféricas bien definidas y tenían diámetros de 50-100 nm cuando la relación de volumen de hemina / agua era 1:10 después de 3 días de diálisis. Con un aumento en la relación de volumen de hemina / agua (1:50), las nanopartículas se reunieron en partículas en forma de varilla (Fig. 1). En particular, encontramos que a medida que el tiempo de diálisis aumentó de 1 a 3 días, las nanopartículas de hemina se dispersaron uniformemente (archivo adicional 1:Figura S1-S3). La temperatura (4 y 25 ° C) de la diálisis tuvo poca influencia en el tamaño de las partículas y la dispersión de las nanopartículas de hemina (Archivo adicional 1:Figura S4).

Imágenes TEM de nanopartículas de hemina preparadas mediante diálisis durante 3 días con varias proporciones de volumen de hemina / agua, incluido 1:3 ( a ), 1:5 ( b ), 1:10 ( c ) y 1:50 ( d ) a 25 ° C. La concentración de hemina fue de 0,5 mg / ml
La Figura 2 muestra las imágenes TEM típicas de nanopartículas de hemina preparadas para diferentes días de diálisis con la concentración de hemina de 0.1 mg / mL. Los productos eran principalmente nanopartículas bien definidas, dispersas individualmente, estructuralmente inusuales y con forma de renacuajo. Las nanopartículas en forma de renacuajo se distribuyeron preferiblemente con 3 días de diálisis. El renacuajo mostró una disparidad significativa en tamaño desde el ancho máximo de la cabeza (200 nm) hasta la cola (100 nm). Nuestros resultados mostraron que se podrían formar nanopartículas uniformemente dispersas en la relación de volumen de hemina / agua de 1:10 y después de dializar durante 3 días a 25 ° C para nanopartículas en forma de esfera y renacuajo. Por lo tanto, elegimos estos dos tipos de nanopartículas de hemina para la siguiente investigación.

Imágenes TEM de nanopartículas de hemina preparadas con una relación de volumen de hemina / agua de 1:10 en varios días de diálisis, incluido 1 día ( a ), 3 días ( b ) y 5 días ( c ) a 25 ° C. La concentración de hemina fue de 0,1 mg / ml
Para examinar más a fondo el tamaño de las nanopartículas de hemina, se utilizó la determinación de DLS para confirmar la formación de nanoestructuras. Los diámetros de las nanopartículas en forma de esfera y renacuajo fueron de aproximadamente 218,2 ± 6,2 y 299,8 ± 7,6 nm, respectivamente (Fig. 3a). El tamaño de las nanopartículas medidas por DLS fue algo mayor que los resultados medidos por TEM; esta diferencia se atribuyó al hinchamiento de las nanopartículas en solución acuosa. Se sabía que la medición DLS indicaba los diámetros hidrodinámicos de las nanopartículas en una solución [15]. El potencial ζ de las nanopartículas en forma de esfera (- 21,4 mV) era aproximadamente el doble que el de las nanopartículas en forma de renacuajo (- 10,8 mV) (Fig. 3b). También se determinó el PDI de las nanopartículas de hemina para analizar la distribución del tamaño de partícula. Los resultados mostraron que el PDI de las nanopartículas en forma de esfera y en forma de renacuajo fue de 0,348 y 0,402, respectivamente (Fig. 3c). Este hallazgo indicó que las nanopartículas de hemina obtenidas tenían una buena polidispersidad.
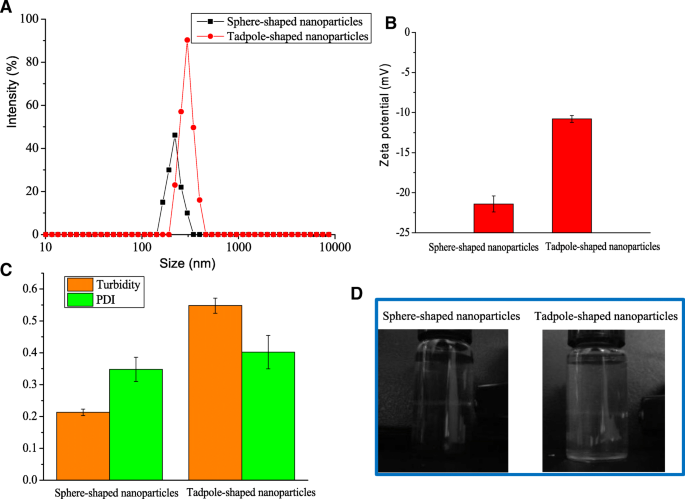
El tamaño medio ( a ), potencial ζ ( b ), PDI y turbidez ( c ) y el efecto Tyndall ( d ) de nanopartículas de hemina de diferentes formas
Cuando un haz de luz atraviesa una dispersión coloidal, las partículas coloidales presentes en la solución dispersan una parte de la luz, lo que provoca una divergencia del haz de luz. Este comportamiento se denomina efecto Faraday-Tyndall [16]. En este caso, la solución de hemina libre no presentó efecto Tyndall (Archivo adicional 1:Figura S5). Sin embargo, el efecto Tyndall se observó en la suspensión de nanopartículas en forma de esfera y renacuajo (Fig. 3d), verificando la formación de coloides o nanopartículas en la suspensión fina. El mecanismo de formación de nanopartículas de hemina por el método de diálisis puede deberse a la difusión del disolvente a través de la interfaz entre la fase acuosa en el exterior y la fase de disolvente orgánico en el interior, lo que resultó en una disminución de la solubilidad de la hemina y la formación de un núcleo cristalino. Posteriormente, se formaron nanopartículas de hemina de diferentes formas debido al crecimiento y autoensamblaje del núcleo de cristal único de diferentes maneras.
Análisis de absorción UV-Vis
De acuerdo con los resultados anteriores, investigamos si había diferencias entre las dos formas de nanopartículas de hemina en su generación de cromóforos. El espectro UV-Vis de las nanopartículas en forma de esfera y renacuajo mostró las mismas bandas de absorción a 265 nm (Fig. 4a). Las nanopartículas en forma de esfera presentaron una banda de absorción estrecha a 667 nm y 775 nm. En comparación, la solución de nanopartículas en forma de renacuajo mostró un pico ancho a 658 nm sin un pico de 775 nm. Además, la intensidad de absorción de las nanopartículas en forma de esfera era más alta que la de las nanopartículas en forma de renacuajo. Una diferencia tan grande no podría explicarse considerando al renacuajo como la suma de una esfera y una varilla cónica ni por una configuración de esfera algo imperfecta. La oscilación de electrones correspondiente a una absorción de plasmón a lo largo del eje largo está retardada y / o en una trayectoria reflectante. Por tanto, las propiedades ópticas de las nanopartículas de hemina dependían de la forma, similar al informe de Hu et al. [17], quien descubrió que las nanopartículas de oro con forma de renacuajo y esfera tenían diferentes propiedades ópticas.
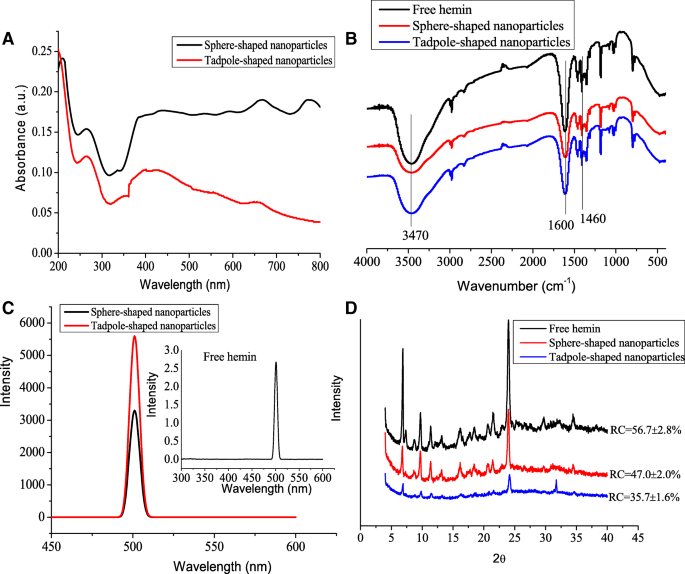
un Espectro UV-Vis, b Espectros FTIR, c espectros de emisión de fluorescencia y d Patrones XRD de hemina libre, nanopartículas en forma de esfera y nanopartículas en forma de renacuajo. Las nanopartículas se dispersaron en agua desionizada. RC, cristalinidad relativa
La solución de hemina libre mostró una absorción máxima a 344 nm, y esto se atribuyó a la banda de Soret comúnmente asociada con las porfirinas (archivo adicional 1:Figura S5). La banda de absorción de las nanopartículas de hemina cambió de 344 a 265 nm, lo que sugirió que se mejoró el efecto conjugativo π-π de las nanopartículas de hemina. Sorprendentemente, en comparación con la hemina libre, ambos tipos de nanopartículas exhibieron una alta y fuerte absorción en el infrarrojo cercano, que es muy apropiada para aplicaciones basadas en la absorción, como la terapia fototérmica y la formación de imágenes fotoacústicas [18]. Magno y col. [19] también informó que las nanopartículas de porfirina con absorción en el infrarrojo cercano han recibido un interés considerable para aplicaciones en fototerapias y fotodiagnósticos, incluso como nanopartículas magnéticas para la terapia de hipertermia magnética y sistemas de administración de fármacos.
Solubilidad
La solubilidad de la hemina es un factor importante que puede afectar directamente la eficacia de absorción en el cuerpo. Se ensayó la solubilidad acuosa cuantitativa de hemina pura y nanopartículas de hemina a diferentes temperaturas (Tabla 1). A medida que aumentaba la temperatura, aumentaba la solubilidad acuosa de todas las muestras. Por ejemplo, la solubilidad de la hemina libre a 25, 37, 60 y 80 ° C fue 0.009 ± 0.000, 0.060 ± 0.002, 0.144 ± 0.004 y 0.245 ± 0.008 mg / mL, respectivamente (Tabla 1).
La cantidad de nanopartículas en forma de esfera disueltas a 25, 37, 60 y 80 ° C fue de 1.333 ± 0.023, 1.499 ± 0.072, 1.889 ± 0.081 y 3.853 ± 0.124 mg / mL, respectivamente, y la de las nanopartículas en forma de renacuajo fueron 0,997 ± 0,045, 1,231 ± 0,035, 1,521 ± 0,058 y 1,795 ± 0,050 mg / ml, respectivamente. Los resultados del estudio de solubilidad acuosa de nanopartículas mostraron un aumento significativo en comparación con la hemina pura. Las nanopartículas en forma de esfera exhibieron una mayor solubilidad a temperaturas de 25, 37, 60 y 80 ° C que las de las nanopartículas en forma de renacuajo. Este hallazgo sugiere que la solubilidad de las nanopartículas en forma de esfera podría ser 308,2 veces mayor en comparación con la hemina libre a 25 ° C. Este aumento en la solubilidad se debió principalmente al tamaño de partícula único a nanoescala. Este resultado concuerda con otros estudios informados por Gidwani y Vyas [13].
Análisis de espectros FTIR
Los espectros FTIR se pueden utilizar para identificar tipos de grupos funcionales. La banda a 3470 cm - 1 se atribuye principalmente a la vibración de estiramiento de N – H y los grupos hidroxilo de la hemina (Fig. 4b). Una banda a 1460 cm - 1 se atribuye a la vibración en el plano N – H debido a la vibración de flexión fuera del plano de –CH 3 del anillo pirrol aromático de hemina. El pico a 1600 cm - 1 es el pico característico del enlace amida debido a la vibración de estiramiento de C =O del grupo carboxilo unido a la superficie de la hemina, lo que revela que el enlace amida secundario existe en la hemina. Estos resultados son consistentes con los de Xi et al. [20]. Sin embargo, el pico a 3470 cm - 1 de nanopartículas de hemina era más amplio que el de hemina libre, lo que indica claramente la interacción mejorada de puentes de hidrógeno entre las nanopartículas.
Espectros de fluorescencia
Las propiedades de fluorescencia de hemina libre y nanopartículas de hemina también se controlaron mediante espectroscopia de fluorescencia. Las señales de fluorescencia de las nanopartículas en forma de esfera y renacuajo aumentaron en el máximo de emisión aparente a 500 nm en comparación con la hemina libre (Fig. 4c). Esto podría deberse a la mayor solubilidad de la hemina después de la formación de nanopartículas [21].
Análisis XRD
La naturaleza cristalina de hemina libre y nanopartículas de hemina fue confirmada por XRD. Como se ilustra en la Fig. 4d, los patrones XRD de hemina libre mostraron varios picos de reflexión relativamente fuertes a 2 θ =6,8, 9,6, 11,5, 16,2, 21,5 y 23,9 °. Los picos característicos de las nanopartículas en forma de esfera eran los mismos que los de la hemina libre, lo que indica que la estructura cristalina de las nanopartículas en forma de esfera no cambió en las formulaciones de las nanopartículas. Sin embargo, para las nanopartículas en forma de renacuajo, los picos más característicos desaparecieron. Además, la cristalinidad relativa de las nanopartículas en forma de esfera y renacuajo se redujo significativamente al 47,0% y el 35,7%, respectivamente, en comparación con el 56,7% de la hemina libre. Estos resultados indicaron que las formulaciones de nanopartículas podrían destruir las regiones cristalinas parciales de la hemina.
Efectos del pH, la temperatura y la concentración de sal en la estabilidad
Se midieron las variaciones en el tamaño, PDI, potencial ζ y turbidez de las nanopartículas de hemina después de la incubación a diferentes niveles de pH [2, 3, 4, 5, 6, 7, 8, 9, 10, 11] (Fig. 5a , B). El tamaño de las nanopartículas de hemina permaneció casi sin cambios con diámetros promedio de aproximadamente 200 nm en condiciones ácidas (Fig. 5a). A valores de pH bajos de 2, el tamaño de las nanopartículas de hemina se redujo a aproximadamente 122,4 nm. A un pH de 7, el tamaño de las nanopartículas aumentó a 293,6 nm y aumentó significativamente ( P <0,05) en condiciones alcalinas (un pH de 9 y 11,0) con diámetros medios superiores a 400 nm. El PDI de las nanopartículas fue inferior a 0,5 en condiciones ácidas, lo que demuestra que no hay agregación aparente de nanopartículas [22]. El potencial ζ de las nanopartículas disminuyó al aumentar los valores de pH (Fig. 5b). La turbidez de las nanopartículas mostró la misma tendencia en tamaño. Estos resultados indicaron que las nanopartículas eran estables en condiciones ácidas e inestables en condiciones alcalinas.
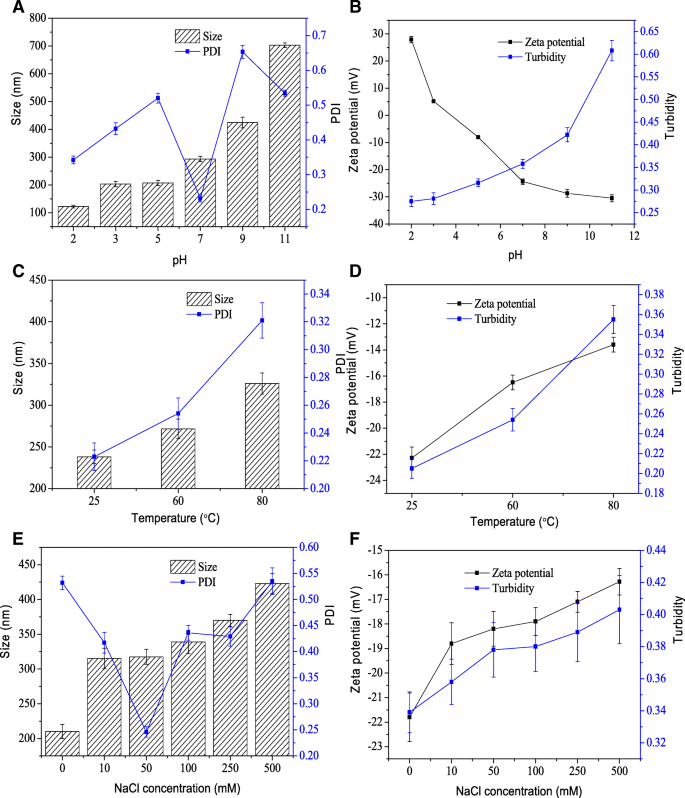
Estabilidad de las nanopartículas de hemina. El efecto de varios niveles de pH ( a ), temperaturas ( c ) y concentraciones de sal ( e ) sobre el tamaño de partícula y PDI de nanopartículas. El efecto de varios niveles de pH ( b ), temperaturas ( d ) y concentraciones de sal ( f ) sobre el potencial ζ y la turbidez
Se determinaron los efectos del tratamiento térmico (25, 60 y 80 ° C) durante 30 min sobre el tamaño, el PDI, el potencial ζ y la turbidez de las nanopartículas de hemina (Fig. 5c, d). Cuando se aumentó la temperatura, el tamaño de partícula, el PDI, el potencial ζ y la turbidez de las nanopartículas aumentaron ligeramente. Los resultados sugieren que las nanopartículas de hemina tenían una excelente estabilidad térmica. De manera similar, a medida que se incrementó la fuerza iónica, también aumentaron el tamaño, el potencial ζ y la turbidez de las nanopartículas, lo que provocó la disociación de las nanopartículas (Fig. 5e, f).
Conclusiones
En este trabajo, primero desarrollamos nanopartículas de hemina en forma de renacuajo y esfera utilizando una técnica de diálisis fácil, que podría mejorar significativamente la solubilidad en 308,2 veces a 25 ° C. Además, las nanopartículas de hemina eran estables en condiciones ácidas y mostraban una excelente estabilidad térmica. Además, ambas nanopartículas exhibieron una fuerte absorción en el infrarrojo cercano. El trabajo futuro se centrará en el estudio en profundidad del diseño de un sistema nanoportador de hemina de respuesta optotérmica para la carga de ingredientes activos. Las nanopartículas de hemina con solubilidad mejorada podrían tener aplicaciones potenciales en los campos de la terapia biomédica, alimentaria, fotodinámica y fotodinámica-fototérmica.
Abreviaturas
- DLS:
-
Dispersión de luz dinámica
- FTIR:
-
Infrarrojos por transformada de Fourier
- TEM:
-
Microscopía electrónica de transmisión
- XRD:
-
Difractograma de rayos X
Nanomateriales
- Nanofibras y filamentos para una mejor administración de fármacos
- Nanopartículas de oro multifuncionales para aplicaciones terapéuticas y diagnósticas mejoradas:una revisión
- Nanopartículas para la terapia del cáncer:avances y desafíos actuales
- Preparación y propiedades magnéticas de nanopartículas de espinela de FeMn2O4 dopadas con cobalto
- Preparación y actividad de hidrogenación catalítica mejorada de nanopartículas de Sb / Palygorskita (PAL)
- Nanopartículas de quitosano cargadas con genisteína y bioflavonoides dirigidas al receptor de folato para un efecto anticancerígeno mejorado en los cánceres de cuello uterino
- Síntesis hidrotermal de nanopartículas de In2O3, gemelos híbridos, discos hexagonales, heteroestructuras de ZnO para mejorar las actividades fotocatalíticas y la estabilidad
- Nuevas nanopartículas de Au Nanostars @ PEG biocompatibles para la obtención de imágenes de TC in vivo y las propiedades de depuración renal
- Método de postratamiento para la síntesis de nanopartículas de FePt-Fe3O4 binarias monodispersas
- La preparación de la nanoestructura yema-cáscara de Au @ TiO2 y sus aplicaciones para la degradación y detección del azul de metileno
- Tornos mejorados para pulido y desbarbado



