Soporte de catalizador anódico novedoso para pila de combustible de metanol directo:caracterizaciones y rendimiento de una sola pila
Resumen
Este estudio presenta una nueva nanofibra de carbono de dióxido de titanio (TiO 2 -CNF) soporte para catalizador anódico en pila de combustible de metanol directo. El proceso de síntesis catalítica implica varios métodos, a saber, los métodos de sol-gel, electrohilado y deposición. El electrocatalizador sintetizado se compara con otros tres electrocatalizadores con diferentes tipos de soporte. Todos estos electrocatalizadores se diferencian en función de una serie de características físicas y electroquímicas. Los resultados experimentales muestran que el TiO 2 -El soporte de CNF proporcionó la densidad de corriente más alta a 345,64 mA mg de catalizador −1 , que equivale a 5,54 veces la del soporte de carbono, mientras que la densidad de potencia es casi el doble que la del electrocatalizador comercial.
Antecedentes
Una celda de combustible de metanol directo (DMFC) es uno de los candidatos más prometedores para una fuente de energía renovable. Es un sistema de generación de energía que produce energía eléctrica al convertir la energía de un combustible químico líquido (metanol) directamente, sin dispositivos auxiliares. Los DMFC funcionan con sus interesantes posibilidades en el transporte y la aplicación estacionaria. Además, los investigadores también creen que este sistema es una de las fuentes de energía más prometedoras para muchas aplicaciones móviles y portátiles, así como una nueva alternativa a la tecnología de baterías recargables. Los DMFC ofrecen muchas ventajas, incluido un tamaño y un peso de sistema más pequeños. También son portadores de energía limpia y reducen la contaminación. Sin embargo, a pesar de estas ventajas, también enfrentan problemas que dificultan su comercialización. Los problemas más desafiantes son la mala cinética de electrooxidación del metanol y el bajo rendimiento del sistema. Es necesario reducir el costo general y es necesario mejorar problemas como el cruce de metanol, la durabilidad, la estabilidad, el calor y la gestión del agua para que el DMFC tenga éxito [1,2,3].
El desarrollo del DMFC comenzó hace una década con la creación de muchas soluciones que utilizaban catalizadores. Uno de los estudios sobre la mejora del rendimiento de DMFC analizó diferentes estructuras de soporte de catalizador, incluidas nanofibras de carbono (CNF), nanotubos de carbono (CNT), nanocables de carbono (CNW) y otras capas de estructura. La adición de nuevo material al catalizador, incluida la creación de un nuevo catalizador híbrido, también se ha convertido en una tendencia en la evolución de DMFC [4, 5, 6]. A pesar de esta investigación, aún existen problemas, especialmente aquellos relacionados con la baja actividad catalítica, estabilidad y conductividad tanto para el funcionamiento electrónico como protónico.
El platino (Pt) es el mejor catalizador tanto para la reacción de oxidación de hidrógeno (HOR) como para la reacción de reducción de oxígeno (ORR). A pesar de ser eficaz en aplicaciones de electrocatalizador [7,8,9,10], el Pt es caro, lo que requiere más investigación para encontrar un nuevo catalizador. Actualmente, el platino-rutenio bimetálico (PtRu) es el mejor catalizador para DMFC. El uso de este catalizador redujo la carga de Pt, lo que redujo el costo del electrocatalizador de DMFC con una relación estándar de 1:1. El papel del Ru en este catalizador bimetálico es eliminar el monóxido de carbono (CO) de los sitios activos para el HOR, lo que conduce a superar el envenenamiento por CO del catalizador [11, 12]. Según un estudio de Bock et al., PtRu mostró una actividad catalítica superior en la DMFC, y estaba claro que el rendimiento catalítico dependía en gran medida de la distribución de los sitios de Pt y Ru a nivel atómico [13]. Sin embargo, el problema de la baja oxidación del metanol no se puede resolver utilizando el catalizador PtRu, por lo que se debe realizar una alteración adicional del catalizador para ayudar a la industria de las pilas de combustible.
Los óxidos metálicos son los materiales más destacados utilizados para mejorar la electrocatálisis de DMFC. Dióxido de titanio (TiO 2 ), también conocida como titania, es una sustancia inorgánica que es naturalmente estable, no inflamable y muy resistente a la corrosión. Titania tampoco está clasificada como sustancia peligrosa por el Sistema Globalmente Armonizado (GHS) de Clasificación y Etiquetado de Productos Químicos de las Naciones Unidas (ONU). Además, las estructuras cristalinas de TiO 2 son termodinámicamente estables y ayudan a crear un material compuesto con buena estabilidad electroquímica y térmica [14]. Los portadores de carga de la forma anatasa se excitan más profundamente en el material a granel, crean más reacciones superficiales y mejoran gradualmente la actividad catalítica [15]. El comportamiento electrónico del material se mejora cuando la interacción entre el TiO 2 se produce óxido de metal y el otro material. Esta mejora también puede mejorar la actividad de oxidación al reducir los potenciales de oxidación del CO [6]. El uso de TiO 2 como soporte del catalizador metálico afecta la cinética de reacción y el mecanismo de reacción [16]. TiO 2 tiene todos los beneficios enumerados anteriormente para muchas aplicaciones en diversas industrias. A pesar de estos beneficios, el principal problema que impide su uso generalizado para aplicaciones de pilas de combustible es su baja conductividad. Sin embargo, para superar este problema, las altas cargas de un catalizador de Pt sobre TiO 2 compuesto con un material conductor eléctrico, como carbono dopado con N, y el empleo de TiO 2 subestequiométrico son obligatorios [5].
Este estudio informó la síntesis y caracterización de nanofibras de carbono-dióxido de titanio (TiO 2 -CNF) depositado sobre un catalizador de platino-rutenio (PtRu) para la aplicación de DMFC. El objetivo del estudio fue sintetizar el electrocatalizador compuesto con TiO 2 en una estructura de nanofibras que puede reducir el efecto de envenenamiento del catalizador mientras mejora la actividad catalítica para mejorar el rendimiento de DMFC más que el electrocatalizador comercial PtRu / C. TiO 2 -CNF se preparó mediante electrohilado, seguido de carbonización; finalmente, PtRu se depositó con una anotación de PtRu / TiO 2 -CNF. Para caracterizar el PtRu / TiO 2 preparado -Se utilizó electrocatalizador compuesto CNF con diferentes soportes, difracción de rayos X (XRD), Brunauer-Emmett-Teller (BET), microscopio electrónico de barrido (SEM) y microscopio electrónico de transmisión (TEM). El rendimiento del electrocatalizador se evaluó mediante voltamperometría cíclica (CV), área de superficie electroquímica (ECSA), análisis de Tafel, cronoamperometría (CA) y celda única de DMFC. Toda la información de rendimiento se comparó con varios otros soportes, incluidos C, CNF y TiO 2 . Con base en los resultados experimentales, se discutió el efecto de usar el óxido metálico como soporte para mejorar la actividad catalítica en el DMFC.
Métodos
Materiales
Se obtuvo isopropóxido de titanio (TiPP, 97%) de Sigma-Aldrich Co., Ltd. Se recibieron poli (acetato de vinilo) (PVAc (Mw 500.000)), dimetilformamida (DMF (99,8%)) y ácido acético (99,7%) de Sigma-Aldrich Co., Ltd. Se adquirió etanol (99,8%) de R&M Chemical Reagents. Estos reactivos químicos se utilizaron para la preparación de nanofibras. La deposición incluyó un precursor de Pt, H 2 PtCl 6 (40% de contenido), de Merck, Alemania, y un precursor de Ru, RuCl 3 (45-55% de contenido) y agente reductor, borohidruro de sodio (NaBH 4 , 96%), de Sigma-Aldrich Co., Ltd. El soporte catalizador comercial para C, CNF y TiO 2 Los nanopolvos se obtuvieron de Cabot Corporation, Cheap Tubes Inc. y Sigma-Aldrich Co., Ltd., respectivamente. Las propiedades detalladas del soporte del catalizador se tabulan en la Tabla 1. Todos los reactivos químicos se usaron sin purificación adicional.
Preparación del TiO 2 -CNF
TiO 2 -CNF se sintetizó mediante el método sol-gel y la técnica de electrohilado. La solución de PVAc (11,5% en peso) se preparó disolviendo el polímero con DMF durante 1 ha una temperatura de 60ºC y se agitó continuamente durante la noche. Se mezclaron 50% en peso de TiPP y unas pocas gotas de etanol y ácido acético en la solución de PVAc y se agitó con un homogeneizador hasta que la mezcla fue homogénea. La solución mezclada se alimentó con una jeringa con una aguja de acero inoxidable para la técnica de electrohilado a una velocidad constante de 0.1 mL h −1 , una tensión aplicada de 16 kV, y una distancia de 18 cm entre la punta y el colector. La nanofibra electrohilada se secó durante 5 ha temperatura ambiente y continuó estabilizándose a 130 ° C durante 8 h. La fibra se carbonizó usando un horno tubular a 600 ° C durante 2 h en una atmósfera de nitrógeno. Luego, la fibra calcinada se sometió a un proceso de control de tamaño utilizando un mortero antes de su uso posterior en este estudio.
Preparación del electrocatalizador compuesto
Todos los electrocatalizadores se sintetizaron mediante el método de deposición por reducción química de NaBH 4 . El 20% en peso de PtRu con la relación atómica 1:1 se carga en diferentes soportes de catalizador, que son soporte sintetizado, TiO 2 -CNF, y otros tres soportes comerciales, C, CNF y TiO 2 . Se añadió una mezcla de agua desionizada (agua desionizada) y alcohol isopropílico (IPA) al material de soporte y se sonicó durante 30 min. Los precursores se mezclaron con la mezcla de soporte y se agitaron continuamente durante otros 30 min hasta que la solución se mezcló bien. El valor de pH de la solución se ajustó a 8 usando una solución de NaOH 1 M. Luego, se aumentó la temperatura de la solución a 80 ° C. Un volumen de 25 ml de una solución 0,2 M de NaBH 4 se añadió gota a gota a la solución y se agitó durante una hora más. La mezcla se enfrió, se filtró y se lavó repetidamente con agua desionizada. El polvo de electrocatalizador se secó durante 3 ha 120 ° C al vacío y se trituró con un mortero y un mortero para obtener un polvo fino.
Caracterización del electrocatalizador
El patrón de difracción de rayos X (XRD) y la estructura cristalina de todos los electrocatalizadores se investigaron con un difractómetro de rayos X (D8 Advance / Bruker AXS Alemania) usando muestras en polvo y operadas a 40 kV y 20 mA. Micromeritics ASAP 2020 realizó el análisis de área de superficie y tamaño de poro usando BET en la condición de isoterma de adsorción / desorción de nitrógeno a 77 K. microscopía (FESEM (SUPRA 55 VP)). Se realizó un análisis de mapeo para observar la distribución de los elementos en un área seleccionada en el electrocatalizador compuesto. La estructura detallada del soporte y electrocatalizador compuesto se analizó con imágenes de alta resolución obtenidas mediante microscopía electrónica de transmisión (TEM (Tecnai G2 F20 X-Twin)).
Evaluación de la medición electroquímica
Las mediciones electroquímicas fueron evaluadas por la estación de trabajo electroquímica Autolab. La actividad de la reacción de oxidación de metanol (MOR) para el electrocatalizador se midió usando la voltamperometría cíclica (CV) de un sistema de celda de tres electrodos. Este sistema utilizó un electrodo de carbono vítreo (GCE, 3 mm de diámetro) como electrodo de trabajo y electrodos de Pt y plata / cloruro de plata (Ag / AgCl) como electrodos de referencia y contador, respectivamente, operados a temperatura ambiente. El electrodo de trabajo debe limpiarse con papel de pulir y alúmina antes de su uso. La preparación de la tinta del electrocatalizador para el electrodo de trabajo se dispersó ultrasónicamente con 15 mg del electrocatalizador en una mezcla de 400 μL de agua DI, 400 μL de IPA y 125 μL de solución de Nafion (5% en peso) durante 30 min. Se utilizó una micropipeta para transferir 2,5 μl de tinta electrocatalizadora a un GCE. El electrodo de trabajo se secó al aire durante 1 ha temperatura ambiente y luego se calentó en un horno durante 30 min a 80 ° C. El electrodo de trabajo estaba entonces listo para la medición de CV. Una solución de 0,5 M H 2 SO 4 en metanol 2 M se preparó como electrolito. Esta solución de electrolito se burbujeó con gas nitrógeno (N 2 ) durante 20 min para lograr el contenido libre de oxígeno. La medición de CV se realizó a una velocidad de exploración de 20 mV s −1 , y el rango de potenciales fue de 0 a 1,1 V frente a Ag / AgCl. El rendimiento a largo plazo de todos los electrocatalizadores se evaluó mediante cronoamperometría (CA) en la solución de electrolitos a un potencial de 0,5 V durante 3600 s.
Fabricación de MEA
El conjunto de electrodos de membrana (MEA) consta de tres partes principales:membrana, ánodo y cátodo. Se selecciona Nafion 117 como membrana, y la membrana se trata para eliminar las impurezas con peróxido de hidrógeno (H 2 O 2 ) y agua desionizada aplicada en el estudio de Hasran et al. [17]. La membrana tratada se almacena en el vaso de precipitados lleno de agua desionizada hasta que esté lista para ser utilizada. La tela de carbono se utiliza como capa de respaldo del ánodo y del cátodo. Esta tela de carbón se trata con un 5% en peso de politetrafluoroetileno (PTFE) para que sea impermeable. La tela de carbón se sumerge en la solución de PTFE y se seca en el horno durante 30 min a 380 ° C. La capa de respaldo está recubierta con una capa de difusión de gas de carbono, donde la carga es de 2 mg cm −2 . El carbón se mezcla con la dispersión D520 de IPA y Nafion (Dupont). La suspensión de carbón se vierte sobre la tela de carbón y se seca en el horno a 100 ° C durante 1 h. Luego, la capa de electrocatalizador está lista para ser recubierta y sintetizada por PtRu / TiO 2 -CNF y electrocatalizador comercial PtRu / C, utilizado para la parte del ánodo, y Pt / C para la parte del cátodo. 2 mg cm −2 La carga de electrocatalizador se agrega con IPA (1100 μL), agua DI (300 μL) y dispersión de Nafion (24 mg). La solución se dispersa en el homogeneizador durante 1 min y se vierte sobre la tela de carbón. El ánodo y el cátodo se secan en el horno durante 1 ha 100 ° C. El ánodo y el cátodo se sujetan con una membrana en el medio usando una prensa en caliente en la condición de 135 ° C y 50 kPa durante 3 min. El MEA está listo para usarse en pruebas de rendimiento de una sola celda.
Prueba de rendimiento de celda única
Las pruebas de rendimiento de una sola celda de DMFC se llevaron a cabo en condiciones pasivas y a temperatura ambiente. El MEA con un 2 de 4 cm El área activa se indica en la celda única, donde la parte del ánodo se fija en el tanque de metanol. Se introducen diez mililitros de metanol 3 M en el tanque y se prueban usando potenciostato / galvanostato (WonATech, Corea). La curva de polarización celular se obtiene para diferentes electrocatalizadores.
Resultados y discusión
Caracterización estructural
El patrón y la estructura cristalina del soporte de catalizador fabricado, TiO 2 -CNF, electrocatalizador sintetizado, PtRu / TiO 2 -CNF y otros electrocatalizadores (PtRu / C, PtRu / CNF y PtRu / TiO 2 ) fueron investigados mediante análisis XRD. Este análisis se completó utilizando un difractómetro de rayos X en el rango de 5 ° -90 ° con 2 θ , como se muestra en la Fig. 1. El resultado para TiO 2 sintetizado -CNF muestra la existencia de todos los materiales, TiO 2 y C. El pico de difracción de 25 ° (1 0 1) representa el TiO 2 estructura anatasa, mientras que el pico a 27 ° (1 1 0) es el TiO 2 estructura de rutilo. Estas estructuras existentes se forman en una estructura tetragonal (estructura cristalográfica para anatasa y rutilo) [18]. Sin embargo, esta muestra tenía la estructura anatasa porque el TiO 2 La estructura cambió de anatasa a rutilo mientras la muestra estuvo expuesta a temperaturas superiores a 700 ° C [19], mientras que la temperatura utilizada en esta investigación fue de solo 600 ° C.
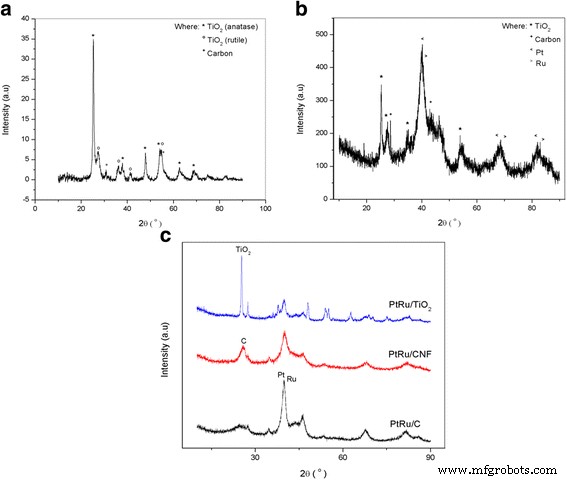
Patrones de difracción de rayos X. un TiO 2 -CNF, b PtRu / TiO 2 -CNF y c electrocatalizadores comparados
El TiO 2 -CNF muestra más picos de difracción para TiO 2 anatasa a 38 ° (1 1 2), 48 ° (2 0 0), 55 ° (2 1 1), 63 ° (2 0 4), 69 ° (1 1 6) y 75 ° (2 1 5) , mientras que los de TiO 2 rutilo son 36 ° (1 0 1), 41 ° (1 1 1) y 54 ° (2 1 1). El carbono se muestra en los picos de difracción de 31 ° (1 1 0) y 55 ° (2 1 1) en estructura cúbica. El patrón XRD para PtRu / TiO 2 -El electrocatalizador CNF muestra el pico de difracción para todos los electrocatalizadores involucrados, Pt, Ru, TiO 2 y C. El pico de TiO 2 y C es casi igual con el TiO 2 -Muestra CNF, y el Pt y Ru se destacan con otros cuatro picos para cada material, que es Pt a 39,7 ° (1 1 1), 46,2 ° (2 0 0), 67,5 ° (2 2 0) y 81,3 ° (3 1 1). Los picos de difracción para Ru son 40,7 ° (1 1 1), 47 ° (2 0 0), 69 ° (2 2 0) y 83,7 ° (3 1 1). Ambos metales vienen en estructura cúbica. El electrocatalizador sintetizado se compara con algunos electrocatalizadores soportados con diferentes soportes de catalizador, a saber, negro de humo (PtRu / C), nanofibras de carbono (PtRu / CNF) y nanopartículas de dióxido de titanio (PtRu / TiO 2 ), y el patrón de difracción se calcula en la Fig. 1c.
Los ángulos de Bragg altos eran claramente visibles, especialmente en el rango de 25 ° a 60 ° para toda la muestra de electrocatalizador. Esto mostró que había una interacción bimetálica o de aleación que se producía en el catalizador [20]. Se observó una intensidad débil y amplia para todas las muestras de electrocatalizador, lo que ilustra altas dispersiones en la muestra preparada. El tamaño de los cristalitos se midió utilizando la ecuación de Debye-Scherrer [8]; tamaño de cristalita =0,98 α / β porque θ . Donde α es la longitud de onda de la radiografía, θ es el ángulo en el pico y β es el ancho del pico a media altura. El valor del tamaño de cristalito estaba disponible a través del software Eva para analizar los resultados de XRD, y se calculó usando la ecuación de Debye-Scherrer. El tamaño de cristalito para todas las muestras se tabula en la Tabla 2. El tamaño de cristalito para PtRu se calculó como 4,64 a 9,84 nm, TiO 2 osciló entre 19 y 38,4 nm y C entre 10,7 y 19,2 nm.
Se analizaron el área de superficie y el análisis de porosidad de todas las muestras de electrocatalizador mediante análisis BET. La isoterma de absorción / desorción de nitrógeno se lleva a cabo a 77 K. El área de superficie, el volumen de poro total y el diámetro de poro promedio de PtRu / TiO 2 -CNF, PtRu / C, PtRu / CNF y PtRu / TiO 2 Los electrocatalizadores se enumeran en la Tabla 3. El área de superficie BET para la estructura de nanofibras del compuesto de óxido metálico, PtRu / TiO 2 -Electrocatalizador CNF, muestra el valor más bajo con 50,59 m 2 / g, seguido de PtRu / CNF, PtRu / TiO 2 y electrocatalizadores PtRu / C en orden ascendente. Los resultados obtenidos en este estudio están cerca de los resultados del área de superficie BET realizados por otro estudio [6], donde el electrocatalizador PtRu / C muestra un área de superficie mucho mayor en comparación con el electrocatalizador compuesto de óxido metálico.
El volumen total de poros, V Poro total , muestra los resultados en orden ascendente iniciados por PtRu / TiO 2 -CNF
Los gráficos de isotermas de adsorción / desorción de nitrógeno a 77 K para todos los electrocatalizadores se resumen en la figura 2. Los resultados muestran que los poros de todas las muestras de electrocatalizador resaltan las propiedades mesoporosas, que tienen un diámetro promedio dentro del rango de 2 a 50 nm, que puede En gran parte se atribuye a la gran brecha que se encuentra en la red del electrocatalizador. Este tipo de electrocatalizador tiene la capacidad de aumentar el nivel de distribución y homogeneidad del catalizador inmovilizado, lo que mejora la estabilidad y la actividad catalítica [22].
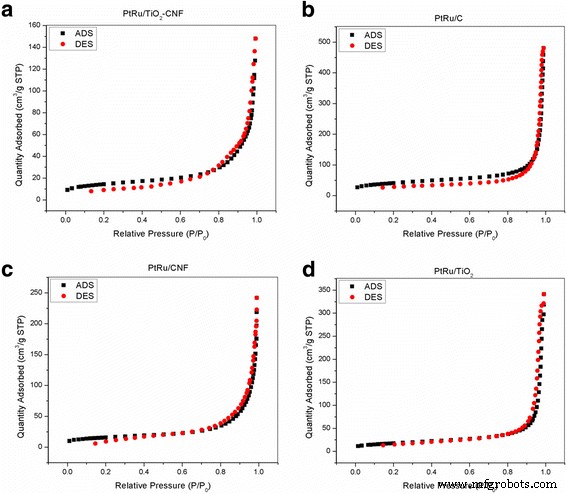
Isoterma de adsorción de nitrógeno (ADS) y desorción (DES) a 77 K. a PtRu / TiO 2 -CNF, b PtRu / C, c PtRu / CNF y d PtRu / TiO 2
El diámetro de poro promedio de las cuatro muestras de electrocatalizador probadas fue de entre 22 y 33 nm, y el diámetro de poro de PtRu / TiO 2 -CNF mostró el diámetro más bajo en comparación con otros electrocatalizadores. El tamaño de diámetro pequeño ilustra el tamaño de la partícula en su conjunto. El tamaño de partícula pequeño tiene una alta relación superficie-volumen y potencialmente da como resultado un aumento de la reactividad y solubilidad de la superficie y puede alterar el perfil de toxicidad de la sustancia. Además, la observación en el gráfico de isoterma de adsorción / desorción de nitrógeno parece plana a una presión relativamente baja ( P / P o ≤ 0,6), lo que puede deberse a la absorción de microporos en la muestra. En un área de presión relativamente alta (0,6 < P / P o <1.0), hay un incremento en la capacidad de adsorción de la muestra debido a la adsorción de moléculas de nitrógeno monocapa y / o multicapa en la mesoestructura.
La Figura 9 muestra las imágenes SEM para el soporte de nanofibras, TiO 2 -CNF. La imagen ilustra que la nanofibra se produce sin problemas sin aglomerados, perlas o nanofibras conectadas, lo que ocurre debido a parámetros de electrohilado equivalentes [23]. La distribución del tamaño del diámetro de TiO 2 -CNF se investiga mediante la recopilación de 100 medidas de diámetro para este soporte de catalizador y se analiza con el "Software de origen", y el tamaño del diámetro de distribución es 136,73 ± 39,56 nm en el rango de 90-170 nm.
El electrocatalizador preparado, PtRu / TiO 2 -CNF, también se sometió a análisis SEM, y la imagen se muestra en la Fig. 10. La Figura 10a es el catalizador depositado sobre el soporte, PtRu / TiO 2 -CNF, después del proceso de fresado. La imagen SEM detectada que la fibra larga está cubierta con nanopartículas de Pt y Ru. Sin embargo, la imagen muestra cierta aglomeración de nanopartículas de Pt y Ru. Para ver la distribución de Pt y Ru, el mapeo se muestra en la Fig. 10b para Pt y la Fig. 10c para Ru. Los resultados del mapeo ilustraron que ambos metales estaban uniformemente dispersos en la nanofibra; sin embargo, se produjo cierta aglomeración de Pt debido a un error durante el proceso de deposición. La aglomeración de nanopartículas fue el resultado de una reacción debido al uso excesivo de la solución de NaOH durante el ajuste del pH para el proceso de deposición [24].
Las imágenes TEM para el soporte del catalizador preparado, TiO 2 -CNF y electrocatalizador, PtRu / TiO 2 -CNF, se muestran en la Fig. 11. Las imágenes TEM del soporte del catalizador de la Fig. 11a muestran que el TiO 2 se dispersó homogéneamente en una nanofibra de carbono de 136 nm de diámetro, debido a la dispersión homogénea de la solución de polímero y TiO 2 precursor durante el método sol-gel. La Figura 11b muestra la imagen del catalizador depositado en TiO 2 -CNF, donde se depositaron partículas de PtRu con un diámetro de aproximadamente 7 nm sobre el TiO 2 -CNF y expuesto al TiO 2 superficie. Esta conexión y la exposición a TiO 2 puede producir un punto de reacción más activo durante la actuación. Sin embargo, las partículas de PtRu se aglomeraron y no se distribuyeron de manera homogénea en la superficie de la nanofibra.
Caracterización electroquímica
La caracterización electroquímica se aplica a todos los catalizadores, para ver su potencial y desempeño como catalizador anódico en DMFC. Hay dos mediciones principales en esta sección, que es la voltamperometría cíclica (CV), para medir el rendimiento electrocatalítico, y la cronoamperometría (CA), para probar la estabilidad y durabilidad a largo plazo de las muestras. La Figura 3 muestra los perfiles CV de todos los catalizadores en 0.5 M H 2 SO 4 solución en el rango de potencial entre - 0,2 y 1,2 V. La región de adsorción / desorción de hidrógeno, en el rango de - 0,2 a 0,1 V, también se indica como el área de superficie activa electroquímica (ECSA). El ECSA es la estimación del área de superficie de las nanopartículas de PtRu en el electrocatalizador [25]. El procedimiento involucró un ciclo de corriente de electrodo en el rango de voltaje, donde las reacciones de transferencia de carga están limitadas por adsorción en los sitios de activación. La carga total requerida para la adsorción / desorción de monocapa se utiliza como sitios de superficie reactiva para ECSA [26]. El resultado de ECSA evaluado se informa en la Tabla 4. La ECSA para la medición de CV se determinó utilizando la siguiente ecuación:
$$ \ mathrm {ECSA} \ \ left ({\ mathrm {m}} ^ 2 {\ mathrm {g}} _ {\ mathrm {Pt}} ^ {- 1} \ right) =\ frac {Q} { \ varGamma. {W} _ {Pt}} $$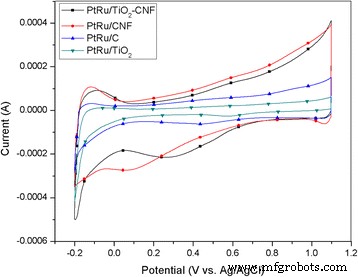
Perfiles de voltamperometría cíclica de los diferentes soportes del catalizador, PtRu / TiO 2 -CNF, PtRu / CNF, PtRu / C y PtRu / TiO 2 en 0,5 M H 2 SO 4 solución a una velocidad de escaneo de 20 mV s −1
donde Q es la densidad de carga o el área debajo del gráfico ((C) del experimento CV), Γ (2,1 Cm Pt −2 ) es la constante de la carga requerida para reducir la monocapa de protones en el Pt, y W Pt es la carga de Pt (g Pt ) en el electrodo. Los resultados del cálculo de ECSA muestran que el electrocatalizador sintetizado, PtRu / TiO 2 -CNF, tiene el valor más alto de 10,4 m 2 g PtRu −1 , seguido de PtRu / CNF (8,4 m 2 / g PtRu ), PtRu / C (0,94 m 2 g PtRu −1 ) y PtRu / TiO 2 (0,76 m 2 g PtRu −1 ). Esto sucedió debido a varios factores clave. Uno de ellos es el tamaño de cristalito de PtRu, como se menciona en la Tabla 2 del análisis XRD; el tamaño de cristalita de PtRu para PtRu / TiO 2 -CNF es el más pequeño y muestra un valor ECSA alto. El tamaño de cristalito más pequeño puede provocar un aumento en el catalizador y en el área de la superficie de reacción. La tendencia del tamaño de los cristalitos se sigue con la tendencia del valor ECSA para PtRu / CNF y PtRu / C. Sin embargo, PtRu / TiO 2 La muestra supuestamente puede producir un valor ECSA más alto que PtRu / C, ya que el tamaño del cristalito es menor, pero la ECSA obtenida es menor. Esto puede suceder debido a la aglomeración de partículas de PtRu en la muestra. Esta aglomeración puede reducir el área de superficie potencial para reaccionar y disminuir la ECSA.
El rendimiento electrocatalítico del electrocatalizador sintetizado y otro electrocatalizador se analizó con CV como se ilustra en la Fig. 4. La curva CV para los electrocatalizadores, incluido PtRu / TiO 2 -CNF, PtRu / C, PtRu / CNF y PtRu / TiO 2 , se mide en metanol 2 M con 0,5 M H 2 SO 4 con N 2 saturado gas a temperatura ambiente. Las múltiples curvas se miden dentro del rango de potencial de - 0,1 a 1,1 V frente a Ag / AgCl. La Figura 4 muestra que la densidad de corriente máxima en orden decreciente fue PtRu / TiO 2 -CNF> PtRu / CNF> PtRu / C> PtRu / TiO 2 . La densidad de corriente máxima de PtRu / TiO 2 -CNF para el MOR pareció ser aproximadamente 0,639 V frente a Ag / AgCl. La densidad de corriente máxima y otros valores de CV para todas las muestras se informan en la Tabla 4. El valor de densidad de corriente para PtRu / TiO 2 -El catalizador CNF es 345,64 mA (mg PtRu ) −1 , que son 1,85 y 5,54 veces más altos que PtRu / CNF y el electrocatalizador comercial, PtRu / C. Esto muestra que el TiO 2 -El soporte del catalizador CNF fue un mejor sustituto del soporte del catalizador de negro de humo. Esto se debe a que la mezcla de nanofibras, a través del proceso de carbonización, puede aumentar la conductividad eléctrica y térmica del catalizador [27].
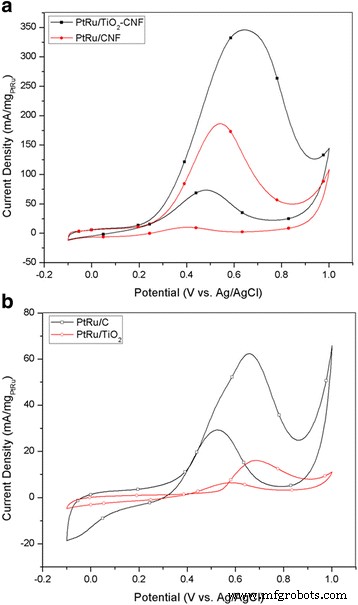
CV en metanol 2 M y H 2 0,5 M SO 4 a la velocidad de exploración de 20 mV s −1 . un PtRu / TiO 2 -CNF y PtRu / CNF. b PtRu / C y PtRu / TiO 2
La estructura de nanofibras en el electrocatalizador compuesto puede aumentar el área de superficie total y el sitio de reacción activo en el área de superficie del electrocatalizador. Otra ventaja fue la presencia de TiO 2 de alta anatasa composición como resultado del análisis XRD. La anatasa adquiere una mayor actividad electrocatalítica que el rutilo TiO 2 . La interacción metal-soporte también muestra un efecto positivo con una mayor densidad de corriente máxima, donde la combinación de materiales entre PtRu y TiO 2 -CNF exhibe una combinación exitosa de electrocatalizador en DMFC. El segundo pico más alto de densidad de corriente con el valor de 186,29 mA / mg PtRu pertenece a PtRu / CNF que es 2,99 veces más alto que el electrocatalizador comercial, PtRu / C. Este resultado se corresponde con el estudio de Zainoodin et al. [28] e Ito et al. [29]. La similitud de PtRu / TiO 2 -CNF y PtRu / CNF es la estructura de soporte del catalizador de nanofibras. La alta densidad de corriente máxima para ambas muestras demuestra que la nanofibra puede proporcionar un rendimiento sobresaliente de oxidación del metanol debido a la capacidad de la nanofibra para aumentar el área de superficie del electrocatalizador y mejorar la actividad catalítica. El rendimiento de PtRu / C es mucho menor que el resultado de la aglomeración de PtRu, donde se muestran el valor ECSA y el tamaño de cristalito de XRD. Esta situación reduce el potencial de la superficie del electrocatalizador para ser un sitio activo y reduce el rendimiento del electrocatalizador. La muy baja actividad de PtRu / TiO 2 se debió a la naturaleza del TiO 2 soporte de catalizador con baja conductividad eléctrica [4]. Estos resultados muestran claramente que el medio electroconductor era esencial para los sistemas catalíticos de una reacción electroquímica [30].
Las múltiples curvas de CV de la Fig. 4a, b muestran la exploración inversa y el pequeño pico de oxidación aparece entre 0,4 y 0,57 V frente a Ag / AgCl. La formación de especies carbonáceas oxidadas incompletas durante el primer pico de oxidación dio como resultado una pequeña oxidación en el barrido inverso, también conocida como pico de oxidación inverso [31]. This oxidation peak shows the tolerance of electrocatalyst towards the carbonaceous species by calculating the ratio of forward (I f ) and reversed (I b ) oxidation peak. The oxidation peak ratio called as CO tolerance is tabulated in Table 4. The result shows that both samples using nanofiber support, PtRu/TiO2 -CNF, and PtRu/CNF have the highest electrocatalyst tolerance against carbonaceous species, which means these can lower the catalyst poisoning potential, with the ratio exceeding 4.7 respectively. This result shows that nanofiber structure and the combination of metal oxide in electrocatalyst can reduce the main problem faced by DMFC technology and have high potential to replace the commercial support used in this technology.
The synthesis electrocatalyst, PtRu/TiO2 -CNF, is compared with other PtRu-based electrocatalyst, nanostructured catalyst support, and combination of metal oxide in electrocatalyst for DMFC technology and shown in Table 5. The result shows that the peak current density for PtRu/TiO2 -CNF is the highest among other electrocatalysts. However, the high value of current density is obtained by using the nanostructure catalyst support and TiO2 as one of the side material in the composite electrocatalyst. Even though there are several different types of metal oxide used in the other study, the performance shows a gap with the TiO2 -utilized electrocatalyst.
Other than CV, linear sweep voltammetry (LSV) is one of the important electrochemical studies of electroactive substance. LSV is quite similar to CV, which measures the current response as a voltage function. Figure 5 shows the LSV plot for all the electrocatalysts that were measured in 2 M methanol and 0.5 M H2 SO 4 at the scan rate of 20 mVs −1 in the N2 gas environment. The result shows that the synthesized electrocatalyst, PtRu/TiO2 -CNF, shows the highest current density that was calculated over the electrode surface area. The trend of the current density for LSV and CV is equalized. The LSV point shows the rising region between 0.5 and 0.7 V vs Ag/AgCl, and this region is known as a Tafel region that appeared when the electron transfer kinetics occur in the electrocatalyst surface [32]. The LSV data is extracted to present Tafel plot, where it relates the electrochemical reaction rate to the overpotential.
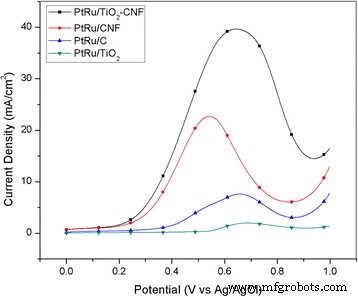
LSV in 2 M methanol and 0.5 M H2 SO 4 at the scan rate of 20 mV s −1 for all samples
The Tafel plot of overpotential, E , against log I is presented in Fig. 6, and data extraction of the plot is tabulated in Table 6. This plot can provide and calculate the slope of anodic Tafel plot (b a ) and ionic exchanging current density (j ) from the slope and interception of the Tafel plot. Anodic Tafel slope, b a , for all the electrocatalyst has not much difference in value, while the ionic exchange current density gives a big gap between each electrocatalyst. The ionic exchange current density is also known as a catalytic activity explainer [33]. The j for all electrocatalysts shows the difference, where the highest value belongs to PtRu/TiO2 -CNF with the value of 0.5012 mA cm −2 . This result demonstrates that the synthesized electrocatalyst can produce the highest catalytic activity of bimetallic PtRu compared with other electrocatalyst. Even though the bimetallic composition for all the electrocatalysts is same, the synthesized electrocatalyst gets a greater help from the metal oxide in producing the highest active area for catalytic activity. PtRu/CNF and PtRu/C electrocatalysts have the same value, while PtRu/TiO2 has the lowest of ionic exchange current density with 0.112 and 0.046 mA cm −2 , respectivamente.
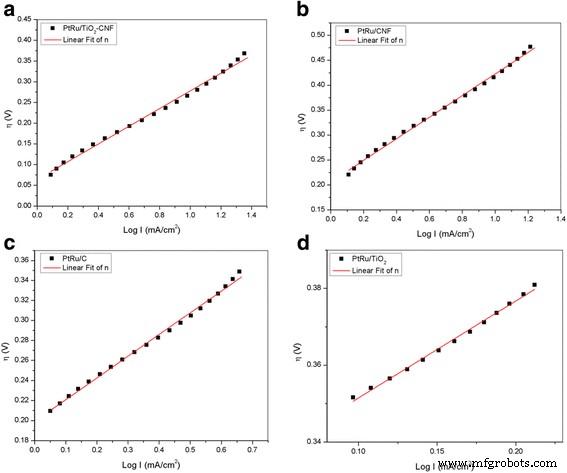
Tafel plot of the electrocatalyst a PtRu/TiO2 -CNF, b PtRu/CNF, c PtRu/C, and d PtRu/TiO2
The CA experiments were conducted to determine the stability and durability of the electrocatalyst for the long-term performance of MOR in a 2-M solution of methanol containing 0.5 M H2 SO 4 for 3600 s. Figure 7 shows the CA curve for the PtRu/TiO2 -CNF, PtRu/C, PtRu/CNF, and PtRu/TiO2 electrocatalysts at a constant potential, 0.5 V. The current density of PtRu/TiO2 electrocatalysts shows the effect of a sharp drop at the start of the experiment, possibly due to the effect of poisoning by methanol oxidation mediation. The PtRu/TiO2 -CNF, PtRu/CNF, and PtRu/C electrocatalysts showed a slight decline of approximately 5 and 3% in current density, respectively. After 3600 s, all of the electrocatalysts were stable, and the reducing current density ratios in increasing order are as follows:PtRu/CNF (6.16) < PtRu/TiO2 -CNF (6.54) < PtRu/C (11.66) < PtRu/TiO2 (14.82). The PtRu/TiO2 -CNF electrocatalyst showed the reducing current density ratio is slightly higher than PtRu/CNF, but this electrocatalyst reached the highest current density of all the electrocatalysts. This was due to good dispersion of the catalyst support and also to increased use of catalysis [6].
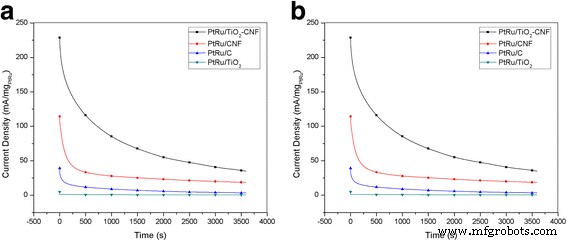
CA curve at potential of 0.5 V vs Ag/AgCl for PtRu/TiO2 -CNF, PtRu/C, PtRu/CNF, and PtRu/TiO2 catalizadores
DMFC Single-Cell Performance
The synthesized electrocatalyst, PtRu/TiO2 -CNF, with the highest electrochemical/half-cell performance was tested with single-cell performance. The performance is compared with commercial electrocatalyst, PtRu/C, using same composition, 20 wt% of PtRu. The 4-cm 2 anode electrocatalyst layer clamped with cathode and membrane to be MEA, ready for single-cell performance using 3 M methanol of passive system. Figure 8 shows the current–voltage curve for PtRu/TiO2 -CNF and PtRu/C. The PtRu/TiO2 -CNF showed the highest performance compared to the commercial electrocatalyst, which is 1.66 times higher. The maximum power density for synthesized electrocatalyst was 3.8 mW cm −2 , while PtRu/C was 2.2 mW cm −2 .
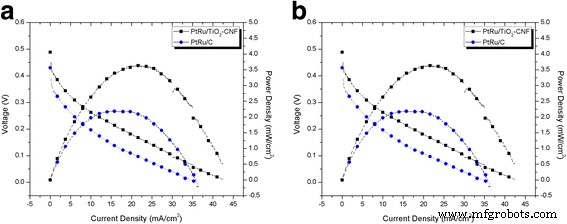
Current–voltage curve for PtRu/TiO2 -CNF and PtRu/C in 3 M methanol with 2 mg cm −2 catalyst loading at room temperature
The best PtRu/TiO2 -CNF performance is confirmed by comparing this result with the previous study of commercial PtRu/C electrocatalyst, using the same catalyst loading in passive mode system that is tabulated in Table 7. The overall electrochemical and single-cell performance conclude that the combination of bimetallic catalyst, PtRu, and introduction of metal oxide nanofiber with carbon nanofiber have high potential to be replaced with PtRu/C in DMFC technology (Figs. 9, 10, and 11). By using the low composition of bimetallic catalyst and electrocatalyst loading, the synthesized electrocatalyst reveals the superior DMFC performance.
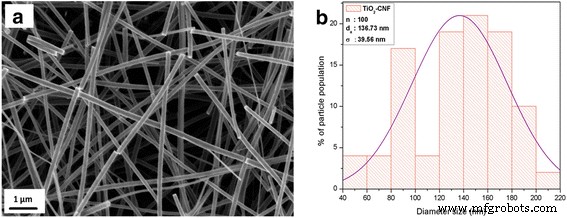
SEM images. un TiO 2 -CNF image (magnification × 10,000). b Distribution of diameter size for TiO2 -CNF

PtRu/TiO2 -CNF catalyst after deposition and milling. un SEM images (magnification × 30,000), b mapping of Pt nanoparticles, and c mapping of Ru nanoparticles

TEM images for prepared a TiO 2 -CNF catalyst support and b PtRu/TiO2 -CNF electrocatalyst
Conclusiones
El TiO 2 -CNF was synthesized using an electrospinning method and applied in the DMFC as a catalyst support for an anodic catalyst. The catalytic activity for the electrocatalyst was prepared for different catalyst supports including PtRu/TiO2 -CNF, PtRu/C, PtRu/CNF, and PtRu/TiO2 , which were compared with one another. The results showed that the prepared electrocatalyst, PtRu/TiO2 -CNF, had the highest current density, which was 5.54 times higher than that of the commercial electrocatalyst, PtRu/C. The DMFC single-cell performance of PtRu/TiO2 -CNF reveals the superior performance almost twice higher than that of PtRu/C. The highest catalytic activity was due to the nanofiber catalyst structure and the introduction of TiO2 as the catalyst support. The reaction with the metal support interface between the PtRu and TiO2 -CNF catalysts helped to improve the properties of the catalyst layer. PtRu/TiO2 -CNF is a promising candidate for support of the anode catalyst in DMFCs.
Abreviaturas
- BET:
-
Brunauer-Emmett-Teller
- CA:
-
Chronoamperometry
- CNF:
-
Carbon nanofiber
- CNT:
-
Carbon nanotube
- CNW:
-
Carbon nanowire
- CV:
-
Voltamperometría cíclica
- DI:
-
Desionizado
- DMF:
-
Dimetilformamida
- DMFC:
-
Direct methanol fuel cell
- ECSA:
-
Electrochemical surface area
- GCE:
-
Electrodo de carbono vítreo
- GHS:
-
Globally Harmonized System
- HOR:
-
Hydrogen oxidation reaction
- IPA:
-
Isopropyl alcohol
- LSV:
-
Linear sweep voltammetry
- MEA:
-
Membrane electrode assembly
- MOR:
-
Methanol oxidation reaction
- ORR:
-
Oxygen reduction reaction
- PTFE:
-
Polytetrafluoroethylene
- SEM:
-
Microscopio electrónico de barrido
- TEM:
-
Microscopio electrónico de transmisión
- UN:
-
United Nations
- XRD:
-
Difracción de rayos X
Nanomateriales
- Pinzas de inyección de combustible personalizadas con impresión 3D para un robot Pick and Place
- Nanofibras y filamentos para una mejor administración de fármacos
- Técnicas para la fabricación aditiva y la creación de prototipos
- Nuevo nailon 6 termoestabilizado para trenes de potencia híbridos y eléctricos
- Síntesis verde en un recipiente de microesferas de SnO2 decoradas con Ag:un catalizador eficiente y reutilizable para la reducción de 4-nitrofenol
- Nuevas nanopartículas de Au Nanostars @ PEG biocompatibles para la obtención de imágenes de TC in vivo y las propiedades de depuración renal
- Fabricación y caracterización de un nuevo catalizador anódico compuesto de nanofibras de carbono Tio2 para celdas de combustible de metanol directo mediante el método de electrohilado
- Rendimiento mejorado de un nuevo catalizador anódico de PdAu / VGCNF para la electrooxidación en una pila de combustible de glicerol
- Comparación entre el ácido fólico y la funcionalización basada en péptidos gH625 de nanopartículas magnéticas de Fe3O4 para una internalización celular mejorada
- Cómo maximizar la eficiencia del combustible para equipos pesados de construcción y agrícolas
- Fabricación y Matricería de Piezas Metálicas para Sistemas de Inyección de Combustible



