Electrodeposición de SnO2 en FTO y su aplicación en células solares de perovskita de heterounión plana como capa de transporte de electrones
Resumen
Divulgamos el rendimiento de las células solares de perovskita (PSC) con una capa de transporte de electrones (ETL) que consiste en un SnO 2 película fina obtenida por deposición electroquímica. La morfología de la superficie y el espesor del SnO 2 electrodepositado Las películas estaban estrechamente relacionadas con las condiciones del proceso electroquímico, es decir, el voltaje aplicado, la temperatura del baño y el tiempo de deposición. Investigamos el rendimiento de los PSC según el SnO 2 Película (s. Sorprendentemente, los factores experimentales que están estrechamente asociados con el rendimiento fotovoltaico se vieron fuertemente afectados por el SnO 2 ETL. Finalmente, para mejorar el rendimiento fotovoltaico, las superficies del SnO 2 Las películas fueron modificadas ligeramente por TiCl 4 hidrólisis. Este proceso mejora la extracción de carga y suprime la recombinación de carga.
Antecedentes
Los dispositivos de células solares basados en materiales de perovskita de haluro organometálico han mostrado un rendimiento sin precedentes en el breve lapso de 6 años, y las células solares de perovskita de haluro organometálico (PSC) se muestran prometedoras como células solares alternativas asequibles con alta eficiencia de conversión de energía (PCE) [1,2, 3]. El gran interés en esta nueva clase de células solares se debe a su alto coeficiente de absorción, transporte de carga ambipolar, pequeña energía de enlace de excitones y gran longitud de difusión [4, 5, 6]. A pesar de estas excelentes propiedades, las PSC presentan varios inconvenientes. Los más importantes son la sensibilidad de los materiales de perovskita a la humedad, el calor y la radiación ultravioleta. Para abordar estos inconvenientes, se ha descubierto que la adición de formamidinio y / o un catión inorgánico (Cs o Rb) a un catión de metilamonio mejora la estabilidad frente a estos factores ambientales [3], por lo que la durabilidad de los PSC depende tanto de la configuración del dispositivo (nip, pin) y los semiconductores de óxido metálico [7]. Generalmente, TiO 2 Los materiales se utilizan ampliamente en las PSC como capas de transporte de electrones (ETL) en la configuración del dispositivo n-i-p debido a su gran banda prohibida y alineación de banda, y las PSC altamente eficientes se realizan utilizando TiO 2 ETL [8]. Aunque los PSC con TiO 2 Los ETL exhiben una eficiencia notable, la sensibilidad a los rayos UV y las propiedades electrónicas del TiO 2 se han sugerido como objetivos de mejora para reducir la histéresis y obtener PSC duraderos [9]. Específicamente, Heo et al. informó que el dopaje con Li puede mejorar la movilidad del portador y la conductividad del TiO 2 y así producir PSC sin histéresis significativa [10]. Ito y col. informó que cuando TiO 2 en un PSC se expone a irradiación UV, los electrones se extraen en el TiO 2 / interfaz de perovskita, degradando el material de perovskita [11].
Óxido estánnico (SnO 2 ) ha sido ampliamente estudiado para diversas aplicaciones como baterías, sensores de gas [12], células solares [13] y catalizadores. Se considera un candidato prometedor para su uso como material conductor transparente y fotoelectrodo en dispositivos fotovoltaicos. Recientemente se ha prestado mucha atención a su aplicación en PSC como ETL alternativo con el objetivo de mejorar el rendimiento del dispositivo y la estabilidad a la luz, ya que tiene una banda prohibida más grande (~ 3.6 eV a 300 K), mayor conductividad eléctrica y mayor estabilidad química. que TiO 2 semiconductores [2]. Varias rutas sintéticas a SnO 2 , incluidos los métodos sol-gel [14], síntesis de sales fundidas [15], técnicas de microondas [16], deposición de capa atómica (ALD) y deposición electroquímica (ED) [17,18,19,20]. Los procesos de solución de revestimiento por rotación y ALD son los métodos dominantes para fabricar SnO 2 ETL en PSC [21,22,23]. La fabricación de ETL en dispositivos fotovoltaicos es fundamental para limitar los costos de producción debido a los requisitos para su producción, como el tratamiento térmico, múltiples pasos de procesamiento, control de operación y procesamiento escalable.
Aquí, informamos sobre la síntesis y la aplicación ETL de SnO 2 películas delgadas sobre óxido de estaño dopado con flúor (FTO) por ED. Entre los métodos disponibles, la electrodeposición tiene las ventajas de un coste de producción reducido y una fabricación a gran escala porque no requiere un entorno de vacío o un control operativo complejo. Teniendo en cuenta que los materiales de perovskita son adecuados para la fabricación de rollo a rollo, la aplicación de electrodeposición para obtener SnO 2 Los ETL demostrarán no solo una estrategia simple, rentable y escalable para ETL alternativos, sino que también facilitarán el desarrollo de un proceso continuo de rollo a rollo para la aplicación industrial de los PSC.
Métodos
Preparación de SnO 2 Película
Se utilizó una técnica de cronovoltamperometría (VSP 200, Biologic) para la DE de las nanoesferas de Sn en un sustrato de FTO utilizando un sistema estándar de tres electrodos en una solución de agua desionizada (50 ml) que contenía 0.05 M de SnCl 2 ∙ 2H 2 O [cloruro de estaño (Π), Sigma Aldrich] y 1 mL de ácido nítrico (HNO 3 , Samchun Chemical). A continuación, las nanoesferas se trataron térmicamente en aire a 400 ° C durante 30 min para obtener SnO 2 . La solución acuosa se agitó durante 1 ha 60ºC en una placa calefactora. Después de N 2 purgando durante 10 min, la solución se utilizó para electrodeposición. En el sistema estándar de tres electrodos, se usó FTO como electrodo de trabajo y se usó una placa de platino como contraelectrodo. El electrodo de referencia fue un electrodo de Ag / AgCl (CHI111) en una solución de KCl 1 M.
Fabricación de dispositivos
El SnO 2 preparado Se utilizaron películas delgadas sobre FTO (TEC 8) en la fabricación de PSC. La capa de perovskita se procesó en dos pasos. Una mezcla de PbI 2 (99,999%, Aldrich) y PbCl 2 (99,999%, Aldrich) se disolvió en N , N -dimetilformamida y se agitó a 60 ° C. La relación molar de la solución precursora (PbI 2 :PbCl 2 ) fue 1:1 (1 M). El PbI 2 / PbCl 2 La solución se revistió por centrifugación en el SnO 2 -recubierto con FTO a 5000 rpm durante 30 s en una guantera y secado en una placa calefactora a 70 ° C. Para convertirlo en un material de perovskita, se cargaron 120 μL de solución de yoduro de metilamonio (40 mg / mL) a 0 rpm durante 35 sy luego se revistió por rotación a 3500 rpm durante 20 s; A continuación, la muestra se recoció isotérmicamente a 105 ° C durante 75 min en el medio ambiente. Después del recocido, las películas se trasladaron a la guantera en N 2 atmósfera, y un material transportador de agujeros (HTM) se revistió por centrifugación en el MAPbI 3-x Cl x / SnO 2 / Película FTO a 3000 rpm durante 30 s. Se utilizó una solución de poli [bis (4-fenil) (2,4,6-trimetilfenil) amina] (índice EM) (20 mg / 1 ml) como HTM con 15 μl de Li-bis (trifluorometanosulfonil) imida) / acetonitrilo. (170 mg / 1 mL) y 15 μL de terc-butilpiridina. Finalmente, se depositó Au mediante evaporación térmica. TiCl 4 El tratamiento de hidrólisis se aplicó sumergiendo el SnO 2 electrodepositado películas en un TiCl 4 de 40 mM solución a 70 ° C durante 30 min y secarlos a 150 ° C al aire.
Caracterización
Se realizaron mediciones de voltamperometría cíclica (CV, frecuencia de exploración de 50 mV / s) para confirmar el comportamiento electroquímico del SnCl 2 ∙ 2H 2 Solución de O de -1,5 a 2 V.La estructura cristalina de las muestras se caracterizó por difracción de rayos X (XRD, Rigaku, Dmax 2200, Cu Kα) y espectroscopia de fotoelectrones de rayos X (XPS, ULVAC-PHI 5000, VersaProbe II) . Las morfologías de las muestras se observaron mediante microscopía electrónica de barrido de emisión de campo (SEM, Hitachi S4800). El J - V Las curvas de las PSC se obtuvieron utilizando una estación electroquímica (VSP200, Bio-Logic) por debajo de 100 mW / cm 2 Luz AM 1,5G (Sun 3000 clase AAA, tecnología ABET) con una máscara de metal de 0,098 cm 2 en la zona. Los dispositivos se escanearon a una velocidad de escaneo de 20 mV / s. Las mediciones de CV del efecto de la capa de bloqueo se realizaron usando una configuración de tres electrodos después de purgar con nitrógeno durante 10 min. El electrolito acuoso contenía KCl 0,5 M y el par de electrones redox K 4 [Fe (II) (CN) 6 ] / K 3 [Fe (III) (CN) 6 ] a una concentración de 5 mM. Se usó un electrodo de Ag / AgCl para el electrodo de referencia y un alambre de Pt para el contraelectrodo; la velocidad de exploración fue de 50 mV / s. Se utilizó una celda solar de Si calibrada con Oriel (SRC-1000-TC-KG5-N) para ajustar la intensidad de la luz a la iluminación de un sol. La eficiencia cuántica externa (EQE) se midió usando un potenciostato de Ivium y un monocromador (DongWoo Optron Co., Ltd.) bajo un soporte de luz (lámpara de xenón ABET 150 W, Tecnología ABET). Los datos de EQE se adquirieron en modo DC. Los espectros de fotoluminiscencia (PL) se midieron usando un espectrómetro de luminiscencia (LS 55, PerkinElmer) con excitación a 530 nm. La fotocorriente y el fotovoltaje de intensidad modulada se midieron con un potenciostato Ivium con un LED Modulight (Ivium).
Resultados y discusión
Realizamos mediciones de CV del SnCl 2 ∙ 2H 2 O solución para identificar valores potenciales adecuados. La Figura 1a muestra la curva CV, que se escaneó de 2,0 a -1,2 V. Todos los valores de potencial se registraron con respecto al electrodo de referencia (Ag / AgCl). Como se muestra en la Fig. 1a, se observó un aumento en la corriente catódica de −0.5 a −1.2 V. Generalmente, cuando el voltaje se barre en un experimento de CV de voltaje positivo a negativo, la corriente primero aumenta debido a una reacción electroquímica en la superficie del electrodo de trabajo y luego disminuye debido al agotamiento local de las especies químicas cercanas al electrodo de trabajo.
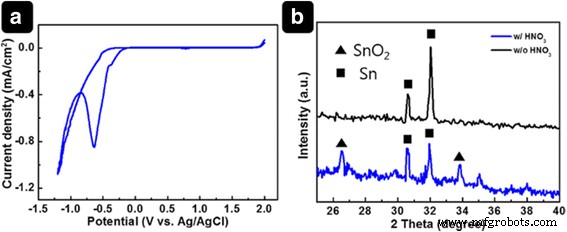
( a ) Curva CV medida a una velocidad de exploración de 50 mV / sy ( b ) Patrones XRD de SnO 2 electrodepositado
Sobre la base del resultado CV, realizamos la DE mediante una técnica de cronovoltamperometría. Tenga en cuenta que la fase de los depósitos depende de la relación de concentración de [HNO 3 ] a [Sn 2+ ] porque el ácido nítrico actúa como fuente de oxígeno en la fase [24]. La presencia de HNO 3 (como se identifica en el patrón XRD, Fig. 1b) facilitó la generación de un SnO 2 –Sn co-fase. Esto se denominará SnO 2 –Nanoesferas SN para distinguirlo del SnO 2 puro . La Figura 2 muestra imágenes SEM del SnO 2 –Nanoesferas Sn depositadas sobre sustratos FTO a diferentes valores de potencial (−0,5, −0,6, −0,7, −0,8, −0,9 y −1 V). Descubrimos que el voltaje aplicado es un parámetro muy importante en el proceso de electrodeposición, ya que las morfologías de los depósitos eran dramáticamente diferentes. Para potenciales absolutos relativamente bajos (−0,5 y −0,6 V), pocos SnO 2 –Nanoesferas de SN formadas. Por otro lado, el FTO se superpuso con Sn que tiene formas irregulares en −0,9 y −1 V. A pesar de que SnO 2 comparable –La formación de nanoesferas SN ocurrió a –0,7 y –0,8 V, la uniformidad fue mejor a –0,7 V. Como resultado de estas observaciones, se eligió –0,7 V como potencial adecuado para la electrodeposición de SnO 2 –Nanoesferas SN.

Imágenes SEM de vista superior de SnO 2 películas electrodepositadas a varios voltajes aplicados. ( a ) - 0,5 V, ( b ) −0,6 V, ( c ) −0,7 V, ( d ) −0,8 V, ( e ) −0,9 V y ( f ) -1,0 V frente a Ag / AgCl. Barra de escala es de 1 μm
También se utilizó un potencial de −0,7 V para optimizar el tiempo de deposición en el rango de 150 a 210 s. La Figura 3 muestra imágenes SEM de muestras obtenidas en varios tiempos de deposición y el rendimiento del dispositivo correspondiente. Se formaron menos partículas a 150 s que a 180 s. Para un tiempo de deposición más largo (210 s), agregación de SnO 2 –Se confirmó nanoesferas SN. Evaluar el rendimiento fotovoltaico de las PSC con el SnO 2 electrodepositado películas, el SnO 2 –Las películas de nanoesferas de SN se trataron térmicamente en aire a 450 ° C durante 30 minutos para obtener SnO 2 completamente convertido Película (s. A CH 3 NH 3 PbI 3-x Cl x La capa de perovskita se fabricó mediante un proceso de interdifusión asistido por capa de semilla de PbICl. Los detalles se proporcionan en la sección experimental. Como se muestra en la Fig. 3e, f, para un tiempo de deposición de 150 s, la densidad de corriente de cortocircuito ( J sc ), voltaje de circuito abierto ( V oc ), factor de llenado (FF) y PCE (%) fueron 17,84 mA / cm 2 , 1.03, 0.496 y 9.11%, respectivamente. A medida que el tiempo de deposición aumentó de 150 a 180 s, J sc mejoró y se obtuvo un PCE superior de 10,0. El uso de un tiempo de deposición de 210 s afectó principalmente al J sc y valor de FF, lo que lleva a un PCE más bajo de 8,22. Para obtener más información sobre las resistencias parasitarias, calculamos la resistencia en serie ( R s ) y resistencia de derivación ( R sh ) de J – V curvas. R s los valores son 10,4, 5,2 y 12,5 (ohmios cm 2 ); R sh los valores son 194,9, 558,5 y 167,1 (ohmios cm 2 ) durante el tiempo de 150, 180 y 210 s, respectivamente. Las resistencias parásitas calculadas explican el rendimiento del dispositivo en funcionamiento obtenido de diferentes condiciones de deposición electroquímica. Como se muestra en la imagen SEM en la Fig. 3d, la mala morfología del SnO 2 Se espera que la película en un tiempo de deposición de 210 s impida la transferencia de carga entre CH 3 NH 3 PbI 3-x Cl x y FTO, lo que resulta en una reducción de J sc .
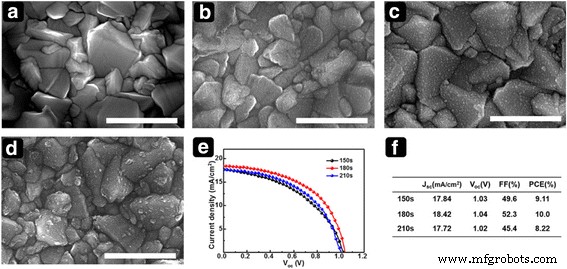
Imágenes SEM de vista superior de sustratos para diferentes tiempos de deposición. ( a ) FTO desnudo y SnO 2 películas depositadas para ( b ) 150 s, ( c ) 180 s, y ( d ) 210 s. Rendimiento fotovoltaico correspondiente:( e ) J - V curvas y ( f ) parámetros fotovoltaicos de PSC con SnO 2 electrodepositado ETL. Barra de escala es de 1 μm
Teniendo en cuenta que el proceso de electrodeposición depende de la movilidad de los iones en una solución de electrolito, también exploramos el efecto de la temperatura en la morfología de las películas. La Figura 4 muestra imágenes SEM de vista superior de películas depositadas a diferentes temperaturas del baño con −0,7 V durante 180 s. Como era de esperar, la morfología de la superficie del SnO 2 –Las nanoesferas de SN preparadas a diferentes temperaturas del baño varían. El tamaño, la rugosidad y el grosor de la nanoesfera parecen verse afectados, ya que la migración de Sn 2+ los iones se potenciaron a mayor temperatura. La eficiencia fotovoltaica de las PSC fabricadas con estas películas se compara en la Fig. 4e, f. Un SnO 2 más fino la película produce un mejor rendimiento y se obtuvo la eficiencia óptima para la película depositada a 60 ° C. El SnO 2 Se espera que la morfología de la película afecte significativamente el rendimiento de la PSC porque las PSC planas tienen una interfaz directa entre el ETL y la capa de perovskita. La conformalidad mejorada podría resultar en un buen contacto que proporciona un transporte de electrones mejorado [25]. Las imágenes SEM de la capa de perovskita fabricadas a partir de ETL variadas se proporcionaron en la información de apoyo (SI) Archivo adicional 1:Figura S1.
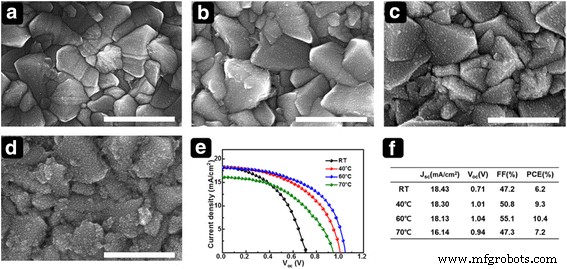
Imágenes SEM de vista superior de SnO 2 películas electrodepositadas a diversas temperaturas del baño. ( a ) RT, ( b ) 40 ° C, e ( c ) 60 ° C y ( d ) 70 ° C. Rendimiento fotovoltaico correspondiente:( e ) J - V curvas y ( f ) parámetros fotovoltaicos de PSC con SnO 2 electrodepositado ETL. Barra de escala es de 1 μm
Para examinar más a fondo el efecto de la temperatura sobre la morfología con respecto al efecto de bloqueo del SnO 2 electrodepositado películas, realizamos mediciones de CV en un electrolito acuoso que contiene [Fe (CN) 6 ] 3− / [Fe (CN) 6 ] 4− porque la reacción redox depende de la transferencia de carga entre el FTO y el electrolito [26]. La cinética de transferencia de electrones se puede interpretar extrayendo la separación de los picos de potencial y pico de corriente de un sistema redox de las curvas CV. Si la reacción redox entre [Fe (CN) 6 ] 3− / [Fe (CN) 6 ] 4− iones se ve obstaculizado por el SnO 2 capa, las formas oxidadas y reducidas del par redox exhiben picos de potencial que se alejan del control en el FTO desnudo y se vuelven semireversibles; en consecuencia, la densidad de corriente máxima se reducirá [27]. La Figura 5a muestra las curvas CV de FTO desnudo y SnO 2 Película (s. La curva CV del FTO desnudo muestra claramente una reacción redox reversible, lo que indica una barrera más baja para la transferencia de electrones. Por el contrario, el FTO con SnO 2 electrodepositado exhibe una mayor separación pico a pico (Δ E p ) de los potenciales pico catódico y anódico en comparación con el de FTO desnudo. El Δ E p los valores de las películas depositadas a temperatura ambiente (TA), 40, 60 y 70 ° C son 125, 175, 207 y 230 mV, respectivamente. Esto indica que la cinética de la reacción redox cambia por el efecto de bloqueo del SnO 2 Película (s. Por el contrario, la transferencia de carga en el FTO está altamente suprimida por la película depositada a 70 ° C, lo que implica que el SnO 2 se deposita densamente en el FTO. El SnO grueso 2 La película podría resultar en un transporte de electrones menos efectivo y más lento, lo que afectaría negativamente al rendimiento fotovoltaico. La corriente pico catódica ( I p ) de las películas disminuyó al aumentar la temperatura del baño, lo que indica que se mejoró la cobertura de FTO.
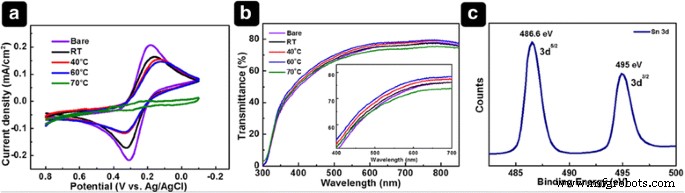
Varios análisis para las películas. ( a ) Curvas CV en el sistema de solución redox y ( b ) espectros de transmisión de FTO y SnO desnudos 2 películas electrodepositadas a diferentes temperaturas de baño en sistema de solución redox. ( c ) Espectro XPS Sn 3d de SnO 2 tratado térmicamente película
Sobre la base de los resultados de CV y las imágenes SEM, podríamos especular que el electrodo FTO a baja temperatura está cubierto con menos nanopartículas; por lo tanto, concluimos que el SnO 2 La película fabricada a 60 ° C tiene un espesor y una morfología adecuados para su uso en PSC y tiene un efecto dominante en el rendimiento del dispositivo. La transmisión óptica del SnO 2 También se comparan las películas (Fig. 5b). A medida que la temperatura del baño aumenta de RT a 60 ° C, la transmitancia del SnO 2 Las películas se mejoran en comparación con las de FTO. A una temperatura alta del baño de 70 ° C, la transmitancia es inferior a la del FTO, lo que se atribuye al aumento del espesor de la película, como lo demuestra la imagen SEM.
Se realizó XPS para medir la composición de las películas electrodepositadas. El espectro XPS del SnO 2 tratado térmicamente La película se muestra en la Fig. 5c. Sn 3d 5/2 y Sn 3d 3/2 Se observaron picos a energías de unión de 486,6 y 495 eV, respectivamente, mientras que la película sin tratamiento térmico mostró Sn 3d 5/2 y Sn 3d 3/2 picos a 484,8 y 493,2 eV, respectivamente (SI, archivo adicional 1:Figura S2) [21]. El SnO 2 la película se obtiene claramente mediante tratamiento térmico.
Por otro lado, aunque SnO 2 La electrodeposición proporciona una ruta versátil y de bajo costo hacia sistemas de fabricación escalables [28], el rendimiento fotovoltaico demostrado del SnO 2 electrodepositado películas no es impresionante. Para mejorar el rendimiento del dispositivo, TiCl 4 se utilizó el tratamiento para modificar el SnO 2 superficie. Como se muestra en la Fig. 6a, el dispositivo basado en SnO 2 sin TiCl 4 el tratamiento muestra una J sc valor de 18,12 mA / cm 2 , a V oc valor de 1,04 V, un FF de 57,3% y un PCE de 10,83%. En comparación, el dispositivo basado en SnO 2 con TiCl 4 tratamiento (SnO 2 –TiCl 4 ) exhibe una J sc valor de 18,65 mA / cm 2 , a V oc valor de 1,02 V, un FF del 79,1% y un PCE del 14,97% (una mejora del 38%). La mejora de la eficiencia se atribuye principalmente a la mejora de J sc y FF.
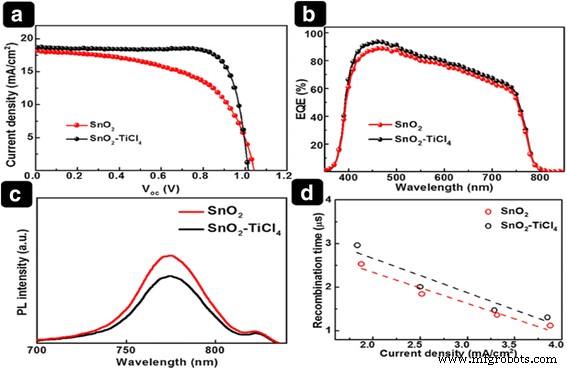
Rendimiento celular con datos IPCE y PL. ( a ) J - V curvas y ( b ) Espectros EQE de dispositivos PSC basados en SnO 2 y SnO 2 –TiCl 4 . ( c ) Espectros PL en estado estacionario de FTO / SnO 2 / perovskita y FTO / SnO 2 -TiCl 4 / muestras de perovskita. ( d ) Tiempo de recombinación versus densidad de corriente
Comprender el mecanismo por el cual TiCl 4 el tratamiento mejora la J sc valor, medimos el EQE (Fig. 6b). El EQE del SnO 2 –TiCl 4 el dispositivo muestra un aumento de 17,8 a 18,6 mA / cm 2 en toda la región espectral de longitud de onda. La mejora en el EQE después de TiCl 4 el tratamiento está de acuerdo con la J mejorada sc en el J - V curvas, lo que implica una recaudación de carga eficiente. Se espera que la mejora de EQE se origine a partir de una mejor inyección de electrones en la interfaz ETL / perovskita [29, 30]. Para investigar más a fondo la inyección de electrones, se midió el PL en estado estable para sustratos con ambos ETL. La Figura 6c muestra los espectros PL de FTO / SnO 2 / perovskita y FTO / SnO 2 –TiCl 4 / muestras de perovskita. Comparado con SnO 2 película basada en SnO 2 –TiCl 4 -la película basada en PL mostró una intensidad PL reducida, lo que indica que la transferencia de electrones de la perovskita al ETL fue mejorada por TiCl 4 tratamiento ya que la emisión de PL de la capa de perovskita se apaga por contacto. Posiblemente, la inyección mejorada de electrones en ETL con TiCl 4 El tratamiento mejoró el EQE. Para examinar más a fondo el rendimiento mejorado del SnO 2 –TiCl 4 -dispositivo basado en espectroscopia de fotovoltaje de intensidad modulada (IMVS, archivo adicional 1:Figura S3) se realizó para caracterizar el tiempo de recombinación ( τ r ) (Figura 6d). La vida útil de la recombinación depende de la concentración de portadores de carga en la célula solar. Por tanto, el tiempo de recombinación está influenciado por la densidad de corriente, que se modula variando la intensidad de la luz. El tiempo de recombinación del portador para el SnO 2 –TiCl 4 -basado en el dispositivo era 1,17 veces más largo que el del SnO 2 -dispositivos basados en. Se espera que la constante de tiempo más larga para la recombinación produzca un aumento en J sc , FF y un mejor rendimiento del dispositivo [31, 32]. Las estadísticas del dispositivo (30 muestras para cada uno) se proporcionaron en el archivo adicional 1:Figura S4.
Conclusiones
En resumen, demostramos una técnica de electrodeposición versátil y escalable para obtener un SnO 2 ETL para PSC de heterounión plana. Las propiedades del SnO 2 electrodepositado dependía en gran medida del tiempo de deposición, la temperatura del baño de electrolito y el voltaje aplicado. Además, los dispositivos basados en SnO 2 tratado con TiCl 4 mostró una V significativamente mejorada oc y J sc , lo que lleva a una mejora de la PCE del 42%.
Abreviaturas
- ALD:
-
Deposición de la capa atómica
- CV:
-
Voltamperometría cíclica
- ED:
-
Deposición electroquímica
- EQE:
-
Eficiencia cuántica externa
- ETL:
-
Capa de transporte de electrones
- FF:
-
Factor de relleno
- FTO:
-
Óxido de estaño dopado con flúor
- HTM:
-
Material de transporte de agujeros
- IMVS:
-
Espectroscopia de fotovoltaje de intensidad modulada
- PCE:
-
Eficiencia de conversión de energía
- PL:
-
Fotoluminiscencia
- PSC:
-
Célula solar de perovskita
- RT:
-
Temperatura ambiente
- SEM:
-
Microscopía electrónica de barrido
- XPS:
-
Espectroscopia de fotoelectrones de rayos X
- XRD:
-
Difracción de rayos X
Nanomateriales
- Un breve informe de progreso sobre las células solares de perovskita de alta eficiencia
- Síntesis de nanocristales de ZnO y aplicación en células solares de polímero invertido
- Células solares de perovskita invertida altamente eficientes con capa de transporte de electrones CdSe QD / LiF
- Perovskita híbrida de vaporización secuencial para células solares de heterounión plana
- El precursor de titanio óptimo para la fabricación de una capa compacta de TiO2 para células solares de perovskita
- RGO-PEDOT híbrido tratado con ozono UV:PSS como material de transporte de orificios eficiente en células solares planas invertidas de perovskita
- Efecto de diferentes morfologías de CH3NH3PbI3 en las propiedades fotovoltaicas de las células solares de perovskita
- Tratamiento UV de capas de transporte de electrones de SnO2 procesado a baja temperatura para células solares planas de perovskita
- Influencia de nanopartículas de agricultura con diferentes tamaños y concentraciones incrustadas en una capa compacta de TiO2 en la eficiencia de conversión de las células solares de perovskita
- Un nuevo material de conversión ascendente de Ho3 + -Yb3 + -Mg2 + TiO2 tri-dopado y sus aplicaciones a las células solares de perovskita
- Fabricación de células solares de perovskita orgánico-inorgánica eficientes en aire ambiental



