Dopaje sustitutivo para aluminosilicato mineral y rendimiento superior de separación de agua
Resumen
El dopaje sustitutivo es una estrategia en la que se añaden opcionalmente impurezas atómicas a un material huésped para promover sus propiedades, mientras que la evolución de la estructura geométrica y electrónica del mineral de nanoarcilla natural tras el dopaje metálico sustitutivo sigue siendo ambigua. Este artículo diseñó primero una estrategia de dopaje eficiente con lantano (La) para arcilla nanotubular (nanotubo halloysita, HNT) a través del equilibrio dinámico de un átomo de sustitución en presencia de AlCl 3 saturado solución y caracterización sistemática de las muestras. Se llevaron a cabo cálculos adicionales de la teoría funcional de la densidad (DFT) para revelar la evolución de la estructura geométrica y electrónica sobre el dopaje metálico, así como para verificar el efecto del dopaje La a nivel de átomo. La carga de CdS y su correspondiente comportamiento de división del agua podrían demostrar el efecto del dopaje La. Las nanopartículas de CdS (11% en peso) se depositaron uniformemente sobre la superficie del nanotubo de halloysita dopado con La (La-HNT) con un tamaño promedio de 5 nm, y la notable tasa de evolución de hidrógeno fotocatalítico de CdS / La-HNT alcanzó hasta 47,5 μmol / h. Los resultados podrían proporcionar una nueva estrategia para el dopaje con iones metálicos y una visión constructiva del mecanismo de dopaje sustitutivo.
Antecedentes
Los minerales de aluminosilicato (p. Ej., Caolinita [1,2,3], zeolita [4, 5] montmorillonita [6, 7] y halloysita [8,9,10,11,12,13]) se han investigado ampliamente como soporte del catalizador. materiales porque no son tóxicos para el medio ambiente y están disponibles en abundancia y a bajo costo a partir de depósitos naturales. Se han utilizado varias técnicas para mejorar las funcionalidades de los materiales de soporte, como el revestimiento de polímero [14, 15], el revestimiento de carbono [8] y el dopaje atómico [16,17,18,19]. Los minerales de aluminosilicato dopados pueden formarse en la naturaleza, pero su síntesis en un laboratorio permite varias propiedades con los dopantes especificados [20, 21, 22, 23]. La incorporación de iones metálicos en la estructura de la capa de aluminosilicato hace que el nanomaterial correspondiente sea atractivo para diversas aplicaciones, incluida la catálisis [24, 25, 26], la liberación controlada de productos farmacéuticos [27, 28] y las baterías de iones de litio [29, 30]. Recientemente, sobre la base de cálculos de la teoría funcional de la densidad (DFT), se han revelado la estabilidad, las propiedades electrónicas y mecánicas de los aluminosilicatos nanoestructurados, como la imogolita, la halloisita y el crisotilo [31]. Sin embargo, el mecanismo de dopaje sustitutivo y la evolución de la estructura electrónica de un metal en los aluminosilicatos siguen siendo ambiguos [32, 33].
Con el objetivo de mejorar nuestra comprensión de este mecanismo, diseñamos una estrategia de dopaje eficiente para uno de los minerales de aluminosilicato representativos (nanotubo de halloysita [34,35,36], HNT) a través del equilibrio dinámico de un átomo de sustitución en presencia de saturados AlCl 3 solución, que contenía sal de lantano. Luego, se presenta una estrategia de dopaje atómico sustitutivo basada en el dopaje La en la estructura HNT y la parte reemplazada del átomo de Al de la hoja Al – O. Halloysita (HNT, Al 2 Si 2 O 5 (OH) 4 ∙ nH 2 O), como un mineral de arcilla natural, contiene gibbsita octahsedral Al (OH) 3 y SiO 4 tetraédrico hojas, y también consta de cilindros huecos formados por múltiples capas laminadas. El CdS es un material semiconductor atractivo que puede convertir la energía solar en energía química bajo irradiación de luz visible. La incorporación de nanopartículas de CdS en La-HNT y su correspondiente rendimiento de división del agua podría demostrar los efectos del dopaje La. El proceso de difusión de Al 3+ solución saturada y las láminas de alúmina de halloysita, el cambio de formas cristalinas y estructuras superficiales, y la posibilidad de actividad catalítica mejorada se investigaron en detalle. Se caracterizaron las microestructuras y morfologías de las muestras y se investigó la estructura interfacial entre CdS y La-HNT. Se evaluó la actividad fotocatalítica del hidrógeno y también se investigó el papel de La-HNT para mejorar la actividad catalítica de CdS / La-HNT.
Métodos
Sección experimental
Preparación de materiales
Los nanotubos de haloisita (HNT) se obtuvieron de Hunan, China. Todos los productos químicos eran de calidad analítica y se utilizaron sin purificación adicional. Los HNT se pretrataron mediante dispersión en emulsión, se filtraron, se lavaron con agua destilada y se secaron durante 8 ha 313 K. La-HNT se sintetizaron mediante una ruta hidrotermal modificada. Una cantidad de 34,3 g de AlCl 3 se disolvió en 60 ml de agua desionizada para formar AlCl 3 solución sobresaturada, mientras que 3 mmol de HNT y 6 mmol de La (NO 3 ) 3 · 6H 2 O se disolvieron en agua desionizada (5 ml), respectivamente. Entonces La (NO 3 ) 3 · 6H 2 La solución de O y la suspensión de HNT se agregaron a AlCl 3 solución sobresaturada para formar una suspensión. La suspensión resultante se agitó durante 10 min en un vaso de precipitados de polipropileno y se sonicó durante 10 min para romper las agregaciones de material de partida. El volumen se limitó a 70 ml (L / S =70–80). La mezcla se transfirió a una botella de teflón (100 ml) y se trató bajo presión autogenerada sin agitar a 373 K durante 48 h. El autoclave se enfrió naturalmente a temperatura ambiente y los precipitados obtenidos se filtraron y lavaron varias veces con agua desionizada y finalmente se secaron a 353 K en vacío (indicado como La-HNT). Para la comparación, se disolvió HNT tratado con ácido sintetizado por 1,00 g de HNT en 250 ml de solución de HCl 6 M a 373 K en un baño de agua. La reacción se llevó a cabo en un matraz cónico durante 4 h con agitación constante. El matraz cónico se enfrió naturalmente a temperatura ambiente, y los precipitados obtenidos se filtraron y lavaron varias veces con agua desionizada, y finalmente se secaron a 353 K en vacío (indicado como HNT tratado con ácido).
Se sintetizaron CdS / La-HNT mediante el método de adsorción y reacción de capas iónicas sucesivas (SILAR), se disolvieron 3 mmol de La-HNT en 50 ml de Cd 0,5 M (NO 3 ) 2 solución de etanol durante 5 min, se enjuaga con etanol y luego se disuelve durante otros 5 min en 50 ml de Na 2 0,5 M S solución de metanol y se enjuaga nuevamente con metanol. Dicho ciclo de inmersión se repitió varias veces hasta que se logró la deposición deseada de nanopartículas de CdS. Luego, los precipitados obtenidos se filtraron y lavaron varias veces con agua desionizada, y finalmente se secaron a 353 K en vacío (denotado como CdS / D-Lax-HNT).
Caracterización
El análisis de espectroscopía de fotoelectrones de rayos X (XPS) se realizó usando un espectrómetro Thermo Fisher Scientific K-Alpha 1063 equipado con una fuente de rayos X monocromática Al Ka. La presión de la cámara de prueba se mantuvo por debajo de 10 −9 mbar durante la adquisición espectral. La energía de enlace XPS (BE) se referencia internamente a los C 1 s pico (BE =284,1 eV). Las fases cristalinas se identificaron mediante análisis XRD utilizando un difractómetro de polvo RIGAKU D / max-2550VB1 de 18 kW con radiación Cu Ka ( λ =1,5418 Å). Los datos se recopilaron en el rango de exploración 2θ =10–80 °, con una velocidad de exploración de 2 ° / min. Los espectros FTIR se registraron usando un espectrofotómetro Nicolet 5700. El área de superficie específica se calculó a partir de las isotermas de adsorción de nitrógeno utilizando la ecuación de Brunauer-Emmet-Teller (BET). Las imágenes de microscopía electrónica de transmisión (TEM) se obtuvieron utilizando un instrumento JEOL JEM-200CX equipado con una espectroscopía de rayos X de dispersión de energía (EDS) a un voltaje de aceleración de 200 kV. El espectro (PL) de la muestra se detectó en un espectrómetro de fluorescencia Hitachi H-4500 usando una lámpara Xe como fuente de luz. Los espectros UV-vis de muestras en solución acuosa se obtuvieron utilizando un espectrómetro UV-2400 (Shimadzu Corp., Japón). Estado sólido 29 Si y 27 Los espectros de RMN Al MAS se registraron usando un espectrómetro Bruker AMX400 en un campo magnético estático de 9,4 T a una frecuencia de resonancia de 79,49 MHz. El análisis electroquímico se llevó a cabo en una celda convencional de tres electrodos utilizando un alambre negro platino y un electrodo de calomelanos saturado (SCE) como contraelectrodo y electrodo de referencia, respectivamente. El electrodo de trabajo se preparó sobre vidrio conductor FTO (óxido de flúor y estaño). En detalle, se añadieron 20 mg de muestra a 10 ml de etanol y se formó una suspensión uniforme. Como en un proceso estándar de recubrimiento por centrifugación, la suspensión de etanol se extendió sobre vidrio FTO, cuya parte lateral se protegió previamente con cinta adhesiva. El centrifugado se realizó a una velocidad alta de 150 rps y luego se secó en un horno a 70 ° C durante 1 h. Las respuestas de fotocorriente transitoria de diferentes muestras se midieron en 0,1 M Na 2 S + 0,02 M Na 2 SO 3 solución acuosa bajo irradiación de luz visible (≥420 nm) a 0 V frente a SCE. El área iluminada del electrodo de trabajo es de 2 cm 2 . El experimento fotoelectroquímico se realizó utilizando una estación de trabajo electroquímica CHI-660A (ChenHua Instruments Co. Ltd., Shanghai, China). La espectroscopia de impedancia electroquímica (EIS) se midió con una estación de trabajo electroquímica CHI-660A (ChenHua Instruments Co. Ltd., Shanghai, China), y el electrolito consistió en hexacianoferrato de potasio (III) 0,01 mol / L, hexacianoferrato de potasio 0,01 mol / L (II) y 0,5 mol / L de KCl. El potencial aplicado fue potencial de circuito abierto (OCP).
Reacción fotocatalítica
Las reacciones de separación del agua se llevaron a cabo en una circulación cerrada por gas dentro de un vacío. Se dispersó una muestra de 100 mg de fotocatalizador en polvo en una solución acuosa de 300 ml de Na 2 0,1 M S y 0,1 M Na 2 SO 3 . La fuente de luz era una lámpara Xe de 300 W y la intensidad de la luz que llegaba a la superficie de la solución de reacción era de 135 mW / cm 2 . La cantidad de H 2 la evolución se determinó mediante un cromatógrafo de gases (Agilent Technologies:6890 N).
Detalles computacionales
Todos los cálculos se realizaron con el código CASTEP, basado en la teoría funcional de densidad de primer principio (DFT). Para los cálculos se utilizó el potencial de aproximación de densidad local (LDA). Se utilizó el formalismo de onda plana de pseudopotencial ultra suave y un corte de energía de 400 eV. La cuadrícula Monkhorst-Pack con 3 × 3 × 1 k Se utilizó una malla de puntos para el cálculo preciso de los resultados de DOS, mientras que el punto Gamma se utilizó durante la relajación de la geometría. La energía total autoconsistente en el estado fundamental se obtuvo de manera efectiva mediante el esquema de mezcla de densidad. Para las optimizaciones de geometría, el umbral de convergencia para la tolerancia de campo autoconsistente (SCF) se estableció en 1.0 × 10 −6 eV / átomo, todas las fuerzas sobre los átomos convergieron a menos de 0,03 eV / Å, el tensor de tensión total se redujo al orden de 0,05 GPa y el desplazamiento iónico máximo estaba dentro de 0,001 Å. Los parámetros celulares y la coordinación atómica de las estructuras se optimizaron utilizando un algoritmo de minimización de Broyden-Fletcher-Goldfarb-Shanno (BFGS).
Resultados y discusión
La integridad de la morfología es importante para asegurar el éxito del dopaje porque el ácido puede dañar la estructura de la halloysita mientras se satura el AlCl 3 la solución no lo hará. Las imágenes TEM de HNT y La-HNT se muestran en la Fig. 1. HNT muestra una estructura tubular multicapa de 0,7 a 1,5 μm de longitud, con un diámetro exterior de 50 a 75 nm y un diámetro interior de 10 a 30 nm (Fig. 1a). Después del dopaje con La, la morfología tubular típica se ha mantenido con un contenido de La del 4,2% (Fig. 1b). Para el HNT tratado con ácido, también se mantuvo la morfología tubular típica (archivo adicional 1:Figura S1a), pero amorfa.
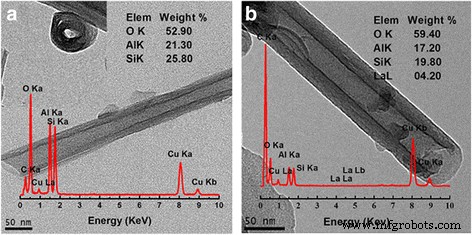
Imágenes TEM de a HNT y b Muestras de La-HNT
La estructura de HNT puede verse influenciada por el dopaje debido al mayor tamaño del átomo de La utilizado para reemplazar el átomo de Al. Para La-HNT, los datos característicos de la halloysita (tarjeta JCPDS No. 29-1487) se pueden observar en la Fig. 2a y el archivo adicional 1:Tabla S1, que indican que la fase cristalina de La-HNT se ha mantenido. El ligero cambio del primer pico en La-HNT se atribuye a la sustitución de los átomos de Al por átomos de La de mayor tamaño, lo que imparte la ampliación del espaciado interlaminar (001). Sin embargo, solo hay un pico amplio centrado en 22 ° para HNT tratado con ácido (archivo adicional 1:Figura S1b), lo que indica que hay sílice amorfa. Los espectros FTIR de HNT y La-HNT se muestran en la Fig. 2b, y la asignación relativa de cada pico vibratorio se enumeran en el archivo adicional 1:Tabla S2. Para HNT, estas asignaciones se basan en la literatura anterior [37,38,39,40]. Para La-HNT, la vibración de deformación O – H de los grupos internos Al – OH a 909 cm −1 y la vibración de deformación Al – OSi de láminas tetraédricas Al – O a 553 cm −1 cambiar a 915 y 544 cm −1 , respectivamente. Sin embargo, la hoja octaédrica de gibbsita de halloysita se destruye por completo y las bandas de estiramiento de Al – O desaparecen para el HNT tratado con ácido (archivo adicional 1:Figura S1c). Todas estas observaciones prueban el éxito del dopaje de La en la estructura de HNT y el cambio de la estructura de HNT influenciado por el dopaje de La. El 27 Los espectros de Al CP / MAS NMR de muestras de HNT y La-HNT se presentan en la Fig. 2c. La señal de resonancia a -3 ppm se asigna a Al coordinado con 6. La señal de resonancia a 64 ppm se atribuye al cambio de Al 4 coordinado a 58 ppm después del dopaje La, lo que indica que el entorno del átomo de Al fue influenciado por el dopaje La. Sin embargo, hay tres picos en −111,32, −101,70 y −91,71 ppm en el HNT tratado con ácido, identificado como Si (OSi) 4 , Si (OSi) 3 OH y Si (OSi) 2 (OH) 2 (Archivo adicional 1:Figura S1d), respectivamente. Las isotermas de sorción de nitrógeno de HNT y La-HNT se muestran en la Fig. 2d, y los datos relativos se resumen en el archivo adicional 1:Tabla S3. La S APUESTA , el volumen de poro y el diámetro de poro promedio de La-HNT son 59 m 2 / g, 0,37 cm 3 / gy 25 nm, respectivamente. La S APUESTA y los valores del volumen de poros de La-HNT son más bajos que los de HNT (82 m 2 / g, 0,41 cm 3 / g), mientras que su diámetro medio de poro (25 nm) es superior al del HNT (20 nm). Sin embargo, la S APUESTA El valor y el volumen de poros para el HNT tratado con ácido son tres veces más altos que el de HNT (archivo adicional 1:Figura S1e). Todos estos resultados demuestran que el dopaje La influye en la estructura de HNT, dado que la S BET para La-HNT es menor que la de HNT, y hay una disminución en el volumen total de poros. La S APUESTA disminuida y el volumen de los poros podría asignarse a la parte de las capas de halloysita colapsadas, y el aumento del tamaño de los poros podría estar asociado con el reemplazo del átomo de Al por el átomo de La, de acuerdo con los análisis XRD y FTIR [18]. Por lo tanto, se especula que La-HNT puede servir como un soporte excelente al cambiar el rendimiento químico y estructural de la halloysita y, por lo tanto, podría contribuir a la actividad de catálisis mejorada para materiales nanocompuestos catalíticos basados en HNT.
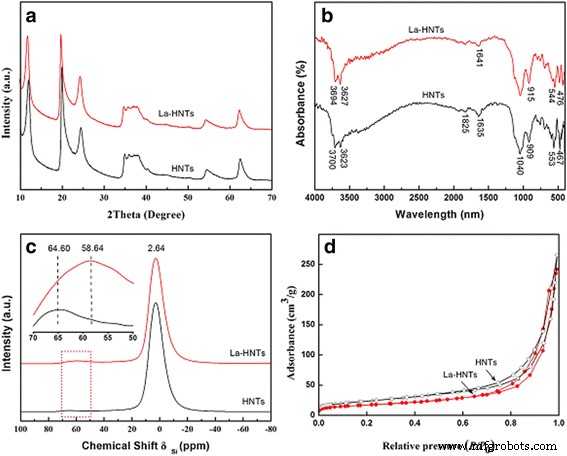
un Patrones XRD, b Espectros FTIR, c 27 Espectros de RMN Al y d isotermas de adsorción-desorción de nitrógeno de muestras de HNT y La-HNT
Para confirmar los efectos del dopaje La, se depositaron nanopartículas de CdS en la superficie de La-HNT y HNT. La Figura 3a-c, e muestra claramente que la superficie de HNT y La-HNT están bien cubiertas con una capa de nanopartículas de CdS continua, densa y uniforme con un grosor de aproximadamente 5 nm. Sin embargo, el elemento La no se ha detectado en la muestra CdS / La-HNT (recuadro en la Fig. 3e). La desaparición del elemento La en los CdS / La-HNTs puede atribuirse al refugio de la capa de nanopartículas de CdS, más el elemento La bajo relevante. La relación de CdS en CdS / HNT a CdS / La-HNT es 11% en peso. La figura 3d, f muestra una imagen típica de HRTEM de la capa de recubrimiento de nanopartículas de CdS en la superficie del host con un diámetro de 5 nm, correspondiente al tamaño de partícula de 5 nm calculado por la ecuación de Scherrer (archivo adicional 1:figura S2).
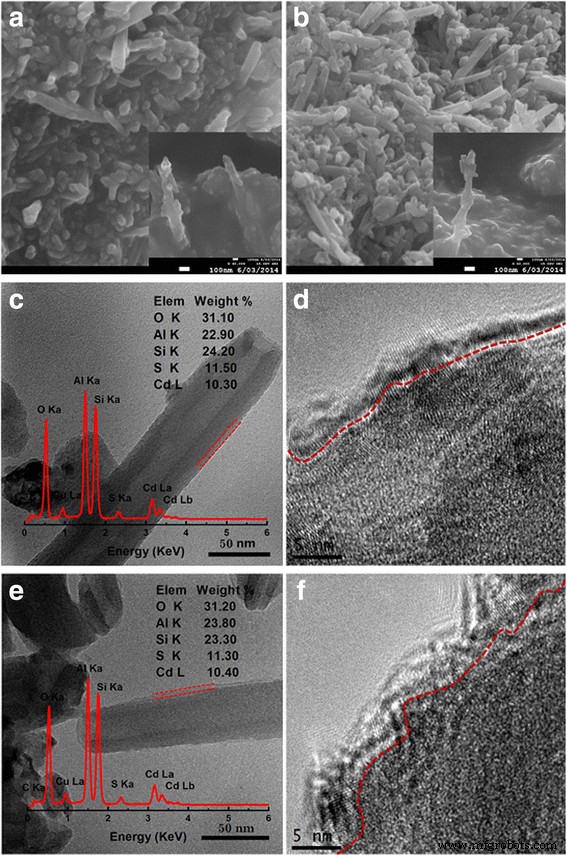
Imágenes SEM y TEM de a , c , d CdS / HNT y b , e , f Muestras de CdS / La-HNT
Las propiedades ópticas de los compuestos HNT, La-HNT, CdS / HNT y CdS / La-HNT se caracterizan por la espectroscopia de reflectancia difusa UV-vis (Fig. 4a). Los bordes de absorción de CdS / HNT y CdS / La-HNT están a 554 y 562 nm, respectivamente, y CdS / La-HNT muestra una intensidad de absorción más fuerte que CdS / HNT en la región de luz visible. Los compuestos de La-HNT no presentan absorción en la región UV y las características de absorción son similares a las de HNT en el aspecto de una amplia absorción en la región de la luz visible. El E obtenido g los valores son 2,31 y 2,25 eV para CdS / HNT y CdS / La-HNT, respectivamente. Se evaluó el rendimiento catalítico de La-HNT para la división del agua para revelar cómo el proceso de dopaje y el cambio de microestructura correspondiente afectan las propiedades macroscópicas. Fotocatalítico H 2 La evolución de CdS / HNT y CdS / La-HNT (Fig. 4b) se llevó a cabo en una solución acuosa que contenía SO 3 2− y S 2− iones como reactivos de sacrificio bajo irradiación de luz solar simulada [41,42,43]. Los resultados muestran que el fotocatalítico H 2 La tasa de CdS / La-HNT (47.5 μmol / h) es mayor que la de CdS / HNT (26.0 μmol / h) en las mismas condiciones de reacción (archivo adicional 1:Tabla S4), y CdS / La-HNT y CdS / Los HNT muestran una tasa de hidrogenación más alta que la mayoría de los fotocatalizadores basados en CdS publicados anteriormente en la literatura [43-45]. Para averiguar si el fotocatalítico superior H 2 derivada del dopaje La, las respuestas de fotocorriente transitoria de CdS / HNT y CdS / La-HNT se midieron en la Fig. 4c. Se puede ver claramente que la fotocorriente aumenta rápidamente a un valor alto bajo iluminación, y la fotocorriente disminuye a casi cero cuando la luz está apagada. Los resultados muestran que la intensidad de la fotocorriente de CdS / La-HNT es más alta que la de CdS / HNT, lo que indica que el dopaje La influyó en una separación más eficiente de los portadores de carga.
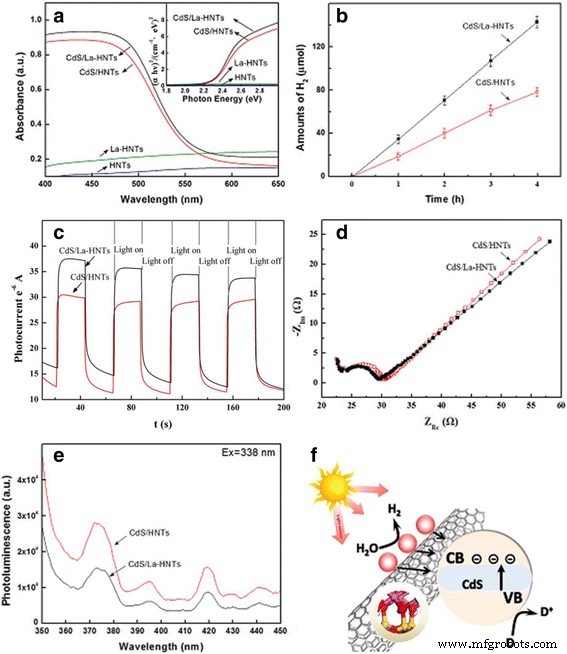
un Espectros UV-vis, b curva de hidrógeno fotocatalítico, c las respuestas de fotocorriente transitoria, d Gráficos de impedancia de Nyquist, e Espectros PL y f correspondiente esquema catalítico de muestras de CdS / HNT y CdS / La-HNT
Para examinar la transferencia de carga y el transporte de iones, se empleó la espectroscopia de impedancia electroquímica (EIS) [2], y en la figura 4d se midió el comportamiento de impedancia de CdS / HNT y CdS / La-HNT. Las gráficas de Nyquist mostraron un semicírculo, que ocurrió debido al proceso electroquímico a un nivel de alta frecuencia, seguido de una línea que indica la resistencia a la difusión del electrolito y los materiales activos. La resistencia de transferencia de carga confinada en semicírculo, que está estrechamente relacionada con la reversibilidad de las reacciones electroquímicas. CdS / La-HNT muestra un arco más pequeño que el de CdS / HNT, lo que indica que el dopaje La llevó a una transferencia de carga más eficiente sobre CdS / La-HNT.
El radio de semicírculo más pequeño de CdS / La-HNT en comparación con CdS / HNT reveló que el nanocompuesto de CdS / La-HNT tiene una menor resistencia a la transferencia de carga y una buena resistencia electroquímica. Los efectos del dopaje La también se confirman por los espectros de emisión de fotoluminiscencia (PL) (Fig. 4e), cuanto menor es la intensidad de PL, mayor es la eficiencia en la separación de electrones y huecos fotogenerados.
Aquí, investigamos la estructura de la superficie de HNT para confirmar aún más el entorno del átomo de Al influenciado por el dopaje de La. La gama completa de espectros XPS de HNT y La-HNT se muestran en la Fig. 5a, y la concentración atómica relativa se muestra en el archivo adicional 1:Tabla S5. Los elementos Si y Al se detectan en HNT y La-HNT, mientras que el elemento La se detecta solo en La-HNT. La relación de concentración de Al / Si es 0,62 en La-HNT, menor que la de HNT (0,88), lo que puede deberse a que el átomo de Al está siendo reemplazado por el átomo de La. Para el HNT tratado con ácido, solo Si 2 p y O 1 s se detectan debido a la eliminación de la hoja de alúmina (Archivo adicional 1:Figura S1f). La Figura 5b muestra La 3 d espectros, y sus posiciones de los picos se observan a 835,7 eV (La 3 d 5/2 ), 839,0 eV (La 3 d 5/2 ), 852,3 eV (La 3 d 3/2 ) y 855,9 eV (La 3 d 3/2 ), respectivamente. La figura 5c, d muestra el Al 2 p y Si 2 p espectros y sus posiciones máximas se observan a 74,8 eV (Al – OH), 74,3 eV (Al – O), 103,3 eV (Si – OH) y 102,7 eV (Si – O), respectivamente. Sorprendentemente, los valores de energía de enlace (BE) del átomo de Al en Al – OH y Al – OSi se desplazaron a 75,1 y 74,6 eV, respectivamente, mientras que la posición del valor BE de los átomos de Si no ha cambiado. Por lo tanto, todos los resultados anteriores confirman que el átomo de La reemplazó parte del átomo de Al de la hoja de Al – O y que el entorno de los átomos de Al ha sido influenciado.
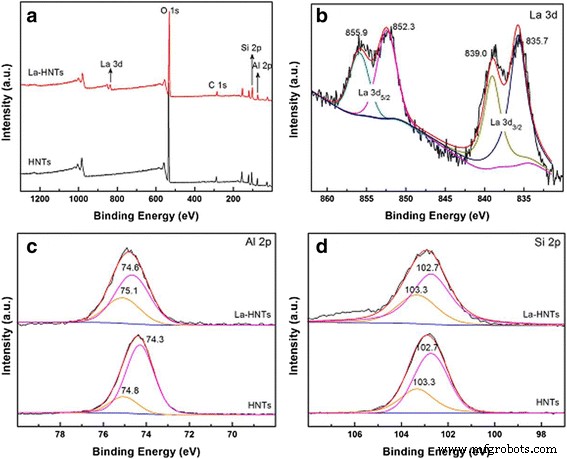
un rango completo, b La3d, c Al2p y d Espectros Si2p XPS de muestras HNT y La-HNT
Basado en la caracterización del dopaje La en la estructura HNT y la parte reemplazada del átomo de Al de la hoja Al – O, se propuso un modelo de dopaje atómico sustitutivo como sigue (Fig. 6). Cada capa de HNT consta de una hoja tetraédrica de Si y una hoja octaédrica de Al. La distancia entre las celdas unitarias es difícil de cambiar debido a la fuerte fuerza de acoplamiento, por lo que las moléculas de agua no pueden entrar. Por tanto, la halloysita ha sido identificada como el mineral aluminosilicato de baja actividad. En la etapa inicial, el típico AlCl saturado 3 se ha elegido la solución porque el AlCl 3 anhidro es un ácido de Lewis fuerte, capaz de formar aductos a base de ácido de Lewis con agua, como AlO 2 2− , HCl y H 3 O + . El grabado comienza por los aductos a base de ácido de Lewis que interactúan con la alúmina en la estructura de la halloysita, y el grado de reacción aumenta con la concentración de Al 3+ creciente. Como la concentración de Al 3+ ya está sobre saturado, se formará una capa de inhibición, cerca de la superficie de la halloysita. En esta situación, la sustitución de cationes podría ocurrir en la capa de inhibición. La 3+ iones siguiendo Al 3+ La solución saturada se sustituye con los átomos de aluminio solubles de halloysita en la capa de inhibición de acuerdo con el principio de la concentración de conservación de la solución saturada de iones. Luego, se logra el equilibrio dinámico del dopaje atómico sustitutivo formado y los compuestos de halloysita dopados con La. El uso de un autoclave en el proceso fue para forzar el proceso de dopaje porque el radio de La 3+ el ion es más grande que el de Al 3+ . Las formas de los cristales y las estructuras de la superficie se pueden cambiar obviamente mediante el dopaje, y se mejoraría el rendimiento químico y estructural del soporte, lo que aporta una uniformidad continua a la carga de nanopartículas y mejora la actividad de catálisis de los materiales nanocompuestos catalíticos.
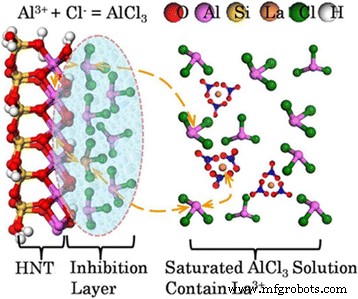
Mecanismo propuesto de dopaje de La en HNT
Los cálculos de la teoría funcional de la densidad del primer principio (DFT) se realizaron para investigar más a fondo la racionalidad del mecanismo de dopaje y el efecto del dopaje La. El modelo de estructura de HNT se simula usando aproximaciones cristalinas, y el La-HNT se construye reemplazando el átomo de Al de halloysita con el átomo de La. Se simula la estructura de HNT mediante el uso de la estructura de caolinita (Fig. 7a, b), y las estructuras de la superficie se construyen escindiendo una estructura de capa 2 × 1 de dos capas de Al-O-Si de espesor de la haloisita a granel. Se utiliza un espacio de vacío de 15 Å. El La-HNT se construye reemplazando un Al en la hoja de Al de halloysita con un átomo de La o agregando La (OH) 3 sobre la superficie de halloysita (Fig. 7c, d). Se encontró que los enlaces Al – O (Al s –O) y Si – O se unen perpendicularmente a la capa de cepillado (Si ps –O) en la superficie HNT aumentan ligeramente en comparación con la de la estructura a granel HNT (archivo adicional 1:Figura S3), es decir, 0.05-0.10 y 0.02-0.03 Å, respectivamente. Al mismo tiempo, los enlaces Si – O en la capa de cepillado (Si es –O) disminuyó. Además, la distribución de enlaces O – H en la superficie HNT se amplía debido al efecto de superficie. Para el caso de dopado con La, una contracción de los Al s –O y Si ps –O enlaces, así como una expansión del Si es –O enlace, se produce en cambio después de la relajación de la estructura atómica de la superficie La-HNT (archivo adicional 1:Figura S3). La estructura local alrededor de La muestra que los seis enlaces La – O poseen una longitud de enlace (alrededor de 2,3-2,5 Å) mucho más larga que los enlaces Al – O, lo que aumenta el espacio alrededor del sitio de dopaje La (Archivo adicional 1:Figura S4a). En particular, el alargamiento de tres enlaces OH de la superficie con H dirigiéndose directamente hacia los átomos de O de La (OH) 3 (H La ) induce tres grupos OH de superficie reactiva alrededor del átomo de La en la superficie de La-HNT.
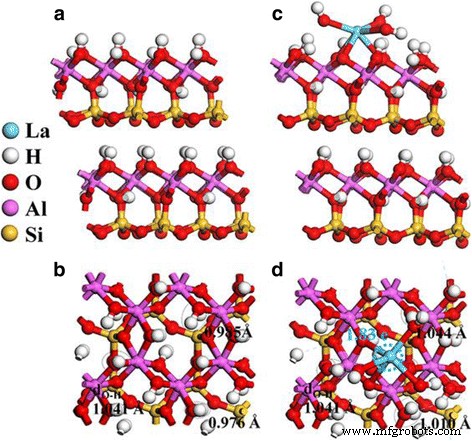
Estructura geométrica de a vista lateral y b vista superior de HNT y c vista lateral y d vista superior de La-HNT
La carga de Mulliken calculada para el átomo de La en La-HNT es 1.83 e (Fig. 7d), que corresponde a los estados de cenefa +3. El resultado de PDOS muestra una banda prohibida de 5,2 eV para HNT prístino, y la banda de cenefa cerca del nivel de fermi está compuesta principalmente por O 2 p estado mientras que el mínimo de banda de conducción (CBM) se mezcla principalmente con H 1 s , Si 3 s 3 p y parcialmente O 2 p , Al 3 s Estados 3p (archivo adicional 1:Figura S4b). El apoyo de La en la superficie HNT introduce La 5 d estados en el CBM (Fig. 8a, púrpura), y el dopante La reactivo con 5 d z 2 Los orbitales se confirman como una impureza de tipo donante. Mientras tanto, los tres grupos OH alrededor de La han suministrado algunos pares de electrones solitarios (Fig. 8a, amarillo y verde) al máximo de la banda de cenefa (VBM), lo que mejorará la capacidad de absorción de la superficie. La diferencia de densidad de carga alrededor de la interfaz La-HNT muestra que hay una transferencia de carga desde los átomos de Al circundantes de la superficie HNT a los dopantes La después del dopaje La (Fig. 8b). Se supone que los dopantes La podrían servir como un puente de transferencia de carga entre la superficie del HNT y las nanopartículas funcionales como CdS y, por lo tanto, se mejoraría la tasa de evolución de hidrógeno fotocatalítico. Por lo tanto, la conformidad de la experimentación y la simulación ha verificado la racionalidad del modelo de simulación y el modelo de dopaje atómico sustitutivo.
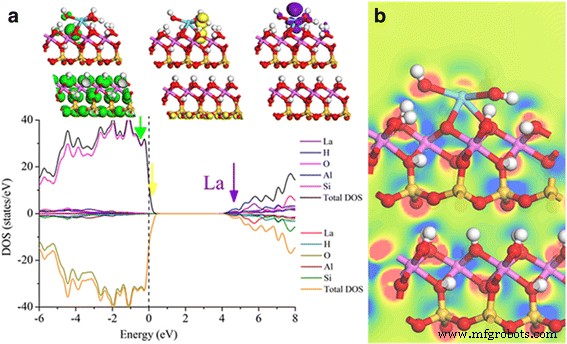
un Los resultados de PDOS de la superficie La-HNT. b Diferencia de densidad de carga de la interfaz La-HNT trazada a lo largo del plano designado por las líneas de puntos mostrado en el panel inferior de la Fig. 7c. Azul corresponde al agotamiento de la carga y rojo cobrar ganancia. Las isosuperficies se muestran en el rango [−0,08, 0,08] (e / Å 3 ). Los contornos de densidad de carga constante están separados por 0,005 eV / Å 3
Conclusiones
En resumen, el átomo de La ha dopado con éxito nanotubos de halloysita naturales. El dopaje La en la estructura de HNT conduce a formas de cristal y cambios obvios en la estructura de la superficie, lo que brinda uniformidad continua para la carga de CdS y cambia la actividad de catálisis para materiales compuestos nanocatalíticos, lo que resulta en una tasa de evolución de hidrógeno fotocatalítico mejorada. El contraste del desprendimiento de hidrógeno fotocatalítico de CdS / La-HNT y CdS / HNT confirma la alta eficiencia del dopaje La. Este resultado es muy alentador y debería ser muy aplicable para extender la técnica de dopaje a otros minerales de aluminosilicato y el correspondiente diseño de materiales funcionales.
Nanomateriales
- Supervisión del rendimiento que funciona tanto para operaciones de TI como para propietarios de aplicaciones
- Mejorar el rendimiento de las aplicaciones para los usuarios y clientes en CyrusOne
- Requisitos para un buen rendimiento del enlace de comunicaciones:modulación y demodulación de IQ
- Nanofibras y filamentos para una mejor administración de fármacos
- El HDPE representa un cambio radical en el rendimiento de las botellas y recipientes moldeados por soplado
- Nanopartículas para la terapia del cáncer:avances y desafíos actuales
- Ingeniería del proceso de recubrimiento por inmersión y optimización del rendimiento para dispositivos electrocrómicos de tres estados
- Síntesis y propiedades electroquímicas de materiales de cátodo LiNi0.5Mn1.5O4 con dopaje compuesto Cr3 + y F− para baterías de iones de litio
- Preparación de micromateriales híbridos de MnO2 recubiertos de PPy y su rendimiento cíclico mejorado como ánodo para baterías de iones de litio
- Síntesis y rendimiento in vitro de nanopartículas de hierro-platino recubiertas de polipirrol para terapia fototérmica e imágenes fotoacústicas
- El caso de la división del inventario, por marcas grandes y pequeñas



