Efecto de los álcalis en el proceso de fabricación de hierro en un alto horno
Efecto de los álcalis en el proceso de fabricación de hierro en un alto horno
Uno de los principales objetivos durante la operación de un alto horno (BF) es maximizar la producción de metal caliente (HM) de la composición química deseada al mínimo costo. Esto requiere una base de materia prima de alta calidad y un funcionamiento regular y fluido del alto horno. La calidad de los materiales de carga es muy importante para evitar problemas en el proceso causados por elementos no deseados que ingresan al horno. En esta área, también se debe prestar atención al contenido de elementos no deseados en el cargo de entrada. Estos elementos no deseados provocan una serie de problemas tecnológicos en el BF. Además, afectan significativamente el costo de producción del HM. Los principales elementos no deseados presentes en la carga que pueden ser problemáticos con respecto a la remoción y el desempeño del BF son los compuestos alcalinos de los metales potasio (K) y sodio (Na).
En el proceso BF, se sabe que la presencia de álcalis tiene influencias negativas en el proceso. Los álcalis causan una mayor reactividad del coque, ablandamiento prematuro de la carga de mineral, descomposición del sinterizado, hinchamiento de los gránulos y están involucrados en la formación de depósitos en el revestimiento refractario del BF que aceleran el desgaste del revestimiento. Los efectos negativos de los álcalis se deben al efecto catalítico sobre la gasificación del coque, la destrucción de la estructura del carbono (C) debido a la inserción de álcali, la formación de andamios y el ataque refractario. Los álcalis se introducen con las materias primas y, debido a la circulación de álcalis (Fig. 1), los álcalis se recogen en el camino hacia la zona de mayor temperatura en el BF.
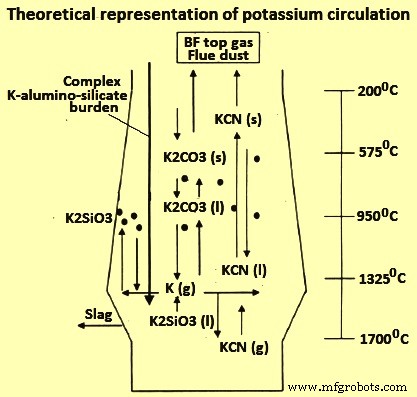
Fig1 Representación teórica de la circulación de K
La presencia de álcali provoca una menor producción y un mayor consumo de coque en el BF, en torno al 4,5 % y 2,3 % respectivamente por cada kg/tHM de álcali añadido con la carga superior de materia prima. El álcali disminuye la producción debido a la reducción del umbral para la reacción reversible de Boudouard, C (s) + CO2 (g) =2CO (g), aumento del gas de coque y reducción de la fuerza del coque. La permeabilidad al gas se reduce debido a la degradación del coque y puede ocurrir un andamiaje en las paredes, lo que reduce el volumen del BF.
Reacciones alcalinas en el BF
En todas las reacciones alcalinas dadas en este artículo, el K puede ser sustituido por Na. La reducción de silicatos alcalinos por C puede tener lugar según las reacciones reversibles K2SiO3 (escoria) + C (s) =2K (g) + SiO2 (escoria) + CO (g), y K2SiO3 (escoria) + 3C (s) =2K (g) + Si (HM) + 3CO (g). El alcance de estas reacciones depende de la temperatura y la presión parcial de CO (monóxido de carbono). Los óxidos alcalinos se pueden reducir con C en el coque o con CO según las reacciones reversibles K2O + C (s) =2 K (g) + CO (g), y K2O + CO (g) =2 K (g ) + CO2 (g).
Los álcalis se volatilizan como elementos o reaccionan con C y N2 (nitrógeno) en la región bosh del BF formando vapores de cianuro de potasio (KCN) o cianuro de sodio (NaCN) según la reacción reversible 2K (g) + N2 (g) =2KCN (gramo). Los vapores se transportan junto con el gas del horno y no se disuelven en el HM ni en la escoria. El punto de fusión y el punto de ebullición del K son 63,4 ºC y 759 ºC respectivamente, mientras que las temperaturas de fusión y ebullición correspondientes del Na son 97,7 ºC y 883 ºC respectivamente. Los puntos de fusión de KCN y NaCN son 622 °C y 562 °C respectivamente, y los puntos de ebullición son 1625 °C y 1530 °C respectivamente. El estado de estos compuestos es líquido en el eje inferior y gaseoso en la zona de rodadura y solera, dependiendo de la temperatura. El gas es transportado por los gases que se mueven rápidamente en el BF.
En el eje donde aumenta el potencial de oxígeno (O2) (alrededor de 1100 grados C), K y KCN ya no son estables y son oxidados por el dióxido de carbono (CO2) a carbonatos alcalinos (K2CO3, Na2CO3) según las reacciones 2K ( g) + 2CO2 (g) =K2CO3 + CO (g), y 2KCN (g) + 4CO2 (g) =K2CO3 (s) + N2 (g) + 5CO (g) respectivamente y óxidos alcalinos por el CO según el reacción reversible 2KCN (g) + CO (g) =K2O + 3C + N2 (g). Los carbonatos alcalinos generados salen en forma de finos blancos, que se distribuyen en la superficie del material de carga o se ubican en el revestimiento de ladrillo.
Los componentes alcalinos adsorbidos en el material de carga y el coque forman nuevos compuestos de acuerdo con su estabilidad relativa. El carbonato de potasio (K2CO3) y el carbonato de sodio (Na2CO3) son sólidos a temperaturas por debajo de 891 °C y por debajo de 851 °C, respectivamente. Los compuestos alcalinos descienden con los materiales de carga y se reducen y vaporizan nuevamente alcanzando la zona de alta temperatura, según la reacción reversible K2CO3(l) + 2C =2K (g) =3CO (g).
La mayor parte del álcali se drena del BF con la escoria. Sin embargo, una parte del álcali de la escoria se reduce generando vapor de álcali que asciende con el gas circundante. El vapor alcalino se condensa en la parte superior del BF donde una parte sale con el gas superior, mientras que el resto se condensa en las paredes internas o en el material de alimentación. Debido a la volatilización y condensación del álcali en las diferentes zonas térmicas, el álcali tiende a circular dentro del BF, lo que lleva a una acumulación e interacciones con otros materiales de alimentación. Esto puede tener un impacto significativo en el proceso, incluso cuando el álcali se carga en pequeñas cantidades, generalmente menos de 5 kilogramos por tonelada de metal caliente (kg/tHM). En la Fig. 2 se muestra una vista simplificada de la circulación de álcali en el BF. Los estudios de BF excavados han demostrado que el nivel de álcali es más alto donde la temperatura está por encima de los 1000 °C, lo que significa que hay una mayor concentración de álcali en la parte inferior del BF. el BF.
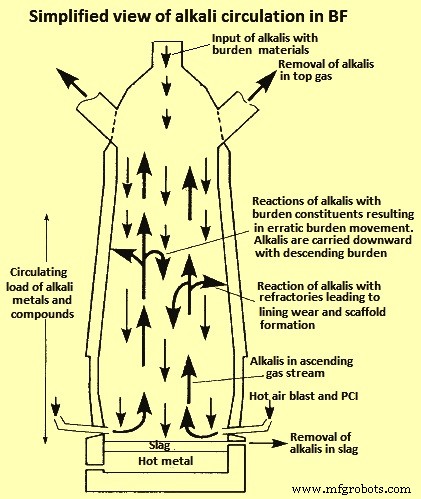
Fig. 2 Una vista simplificada de la circulación de álcalis en el BF
Ciclo alcalino en el BF
Los álcalis normalmente ingresan al BF con el material de hierro y con el coque en forma de silicatos. Para una operación BF suave y eficiente, es deseable limitar la cantidad de álcali a alrededor de 1,5 kg/tHM a 5 kg/tHM, pero normalmente oscila entre 2,5 kg/tHM y 7,5 kg/tHM en diferentes plantas. De las dos sustancias alcalinas Na y K, el K es normalmente el compuesto principal que ingresa al BF. La mayoría de los álcalis se van con la escoria, mientras que algunos se convierten en parte del gas superior y salen del horno con el gas superior. El álcali recirculante puede ser eliminado por la escoria o por el gas. El K pasa al gas superior en mayor grado ya que es más volátil en comparación con el Na, que sale más con la escoria.
Los álcalis ingresan al BF en forma de silicatos (K2SiO3). Los estudios del ciclo alcalino han demostrado que los silicatos descienden con la carga y el ciclo comienza cuando el silicato alcalino se reduce por el C del coque en la zona de fusión según la ecuación K2SiO3 + C (s) =2K (g) + SiO2 + CO (g). Las reacciones tienen lugar alrededor de 1550 grados C según los datos termodinámicos de las reacciones. Los óxidos alcalinos que entran o se forman en el BF reaccionan más arriba en el BF a temperaturas más bajas de acuerdo con la ecuación K2O + CO (g) =2K (g) + CO2 (g) ya que no son estables. K2O también puede disolverse en la escoria primaria.
Además, los vapores de K producidos al nivel del hogar en el BF reaccionan con el carbón pulverizado inyectado y el N2 del chorro de aire caliente según la ecuación 2K (g) + 2C (s) + N2 (g) =2KCN (g , l). El punto de ebullición del KCN es de 1625 grados C, por lo que a medida que el cianuro de potasio (KCN) se eleva y se aleja del chorro de aire caliente de las toberas, se transforma en una fase líquida cuando baja la temperatura. El tiempo en la zona de la tobera es muy corto debido al alto flujo de gas, por lo que los cianuros alcalinos tienen tiempo de subir por el BF antes de transformarse en la fase líquida. Más arriba en el BF, los cianuros alcalinos reaccionan con el CO2 (dióxido de carbono) para formar carbonatos más estables a temperaturas inferiores a 1100 °C según la ecuación 2KCN (l) + 4CO2 (g) =K2CO3 + N2 (g) + 5CO ( gramo). Los carbonatos siguen el gas superior como gas o se depositan en la carga a medida que comienzan a condensarse por debajo de los 900 °C.
En comparación con los silicatos alcalinos, los cianuros alcalinos son inestables, por lo que cualquier SiO2 presente en la parte del hogar del BF puede reaccionar con los cianuros alcalinos para formar nuevamente silicatos alcalinos. El proceso en el que los silicatos alcalinos se reducen a vapor alcalino, que ascienden en el BF, salen con el gas superior o reaccionan con el CO2 para formar carbonatos, se conoce como ciclo alcalino. Hay algunos puntos de vista diferentes que tienen un resumen ligeramente diferente del proceso al diferir exactamente sobre qué reacciones tienen lugar. Hay dudas sobre si los carbonatos se forman realmente en la parte superior de la BF ya que no se encuentran carbonatos durante la excavación de las BF. Sin embargo, el proceso principal en el que se forman los cianuros alcalinos y que el álcali circula en el BF está de acuerdo en todas las vistas.
La figura 3 muestra la circulación de álcalis en el BF. El material cargado desciende a la zona de alta temperatura antes de que los silicatos alcalinos se descompongan en vapores alcalinos o sean absorbidos por la fase de escoria primaria en forma de K2O o Na2O. El ciclo también indica cuándo el vapor alcalino reacciona con los silicatos para volver a formar silicatos. La distribución de los vapores alcalinos a través del BF depende de las rutas del flujo de gas y de la extensión del flujo de gas central. Los flujos de gas tienen un gran efecto sobre cómo se distribuye el calor en un BF. Más flujo central significa más fusión en el medio y menos en la periferia del BF.
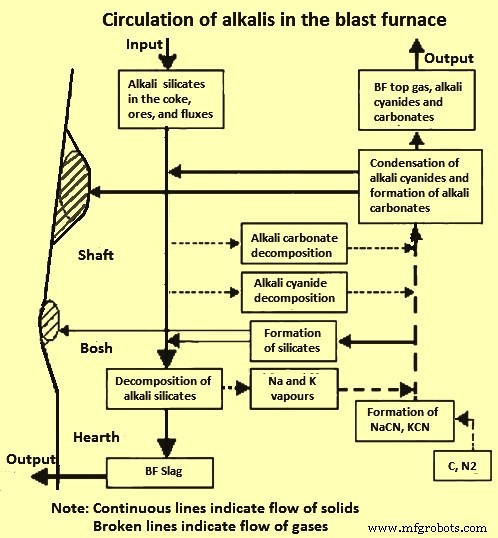
Fig. 3 Circulación de álcalis en el BF
Formación de amoníaco y cianuro de hidrógeno en el BF
Se cree que el amoníaco (NH3) se forma en el BF. Las reacciones básicas detrás de la formación de NH3 y cianuro de hidrógeno (HCN) en el BF son 2KCN + 3H2O =K2CO3 + 2NH3 + C, y NH3 + CO =HCN + H2O. La relación entre estas reacciones depende de varios parámetros como (i) la cantidad de humedad disponible, (ii) la cantidad de KCN disponible en la parte superior y (ii) la temperatura durante las reacciones. El umbral de temperatura para el NH3 es de alrededor de 600 °C y la formación de NH3 disminuye exponencialmente hasta los 500 °C y luego no se detecta. El NH3 adicional que se forma es oxidado por Fe2O3 o CO2 y la cantidad de NH3 formado disminuye. La oxidación de NH3 por Fe2O3 o MnO2 depende de la temperatura. A temperaturas más bajas, el MnO2 es un oxidante más fuerte y, a temperaturas más altas, el Fe2O3 es el oxidante más fuerte.
Como se pueden encontrar HCN y NH3 en el gas superior, la cinética de oxidación del NH3 no es lo suficientemente rápida como para eliminarlo por completo. La mayor cantidad de agua que se encuentra en el gas superior significa que hay más formación de NH3 que puede tener lugar de acuerdo con la reacción anterior. La formación de NH3 en el BF es compleja ya que varios parámetros, como se indica a continuación, afectan su formación.
Temperatura del gas superior – La temperatura del gas superior depende de la relación entre reacciones endotérmicas/exotérmicas en el BF. La temperatura afecta el contenido de humedad. Una temperatura más baja también puede conducir a una mayor solubilidad del NH3 en agua y el HCN es miscible en agua, por lo que la presencia de agua puede disminuir su presencia en el gas superior.
Temperatura de llama – La temperatura de la llama tiene un efecto menor sobre la cantidad de vapor alcalino producido y la carga total de álcali. Se necesita una temperatura alta para reducir los silicatos alcalinos a gas alcalino que inicia la circulación alcalina. Por lo tanto, una temperatura de llama más baja conduce a que más álcali salga del BF a través de la escoria.
Básica – Una basicidad más baja conduce a una mayor absorción de álcali en la escoria, por lo que hay menos álcali circulante en el BF y se produce menos NH3.
Contenido de humedad – Menos humedad introducida con la carga o por otras vías en el BF da menos agua para que ocurra la reacción de formación de NH3.
Efecto del álcali y eliminación
La concentración de álcali en la materia prima ha aumentado en los últimos años debido a la menor disponibilidad de carbón coquizable de alta calidad. El álcali es perjudicial para la operación BF ya que provoca un aumento de la reactividad del coque debido al efecto catalítico en la reacción de pérdida de solución (reacción de Boudouard).
Uno de los principales efectos negativos del álcali es que cataliza la reacción reversible de Boudouard, bajando la temperatura de la reacción de 900 °C a 950 °C hasta alrededor de 750 °C a 850 °C y aumentando la reactividad del coque dependiendo de la calidad de la coca. También afecta negativamente a la estructura del coque. El umbral más bajo para la reacción de Boudouard significa que se consume más C en el BF en una reacción fuertemente endotérmica. Por lo tanto, se necesita aumentar la adición de coque en el BF para mantener una operación estable con 2 kg a 10 kg de coque por kg de álcali o con 6 kg a 11 kg de coque dependiendo de las fuentes utilizadas.
El álcali que ha entrado en la estructura del coque disminuye la fuerza del coque en la parte inferior del BF debido al aumento de la reactividad del coque y, por lo tanto, al aumento de la degradación. Se ha demostrado que la velocidad de reacción aparente del coque al nivel de la tobera es diez veces la velocidad de reacción del coque de alimentación, que está relacionada con la cantidad total de presencia de K. Se sabe que K aumenta la reactividad del coque con CO2 y puede resultar en la fractura del coque debido al hinchamiento de los granos de coque por inserción de K. Un aumento de la reactividad puede ser ventajoso ya que reduce la temperatura de operación del BF, la temperatura en la zona de reserva térmica y, por lo tanto, reduce la temperatura para la reducción del óxido de hierro. Sin embargo, el propósito del coque también es actuar como soporte de carga dentro del horno y, por lo tanto, es necesario minimizar la fractura del coque.
Los estudios sobre la penetración del vapor de K en el coque han confirmado que la estructura de los minerales de coque puede romperse debido a la expansión del volumen de los minerales alcalinizados, especialmente la calsilita. El área superficial entre los minerales y la matriz C aumenta debido a la rotura de los minerales en el coque. Esto facilita la interacción de la materia mineral con los gases C y BF acelerando la gasificación del coque. También puede ocurrir una expansión en el coque cuando los vapores alcalinos penetran en las capas cristalinas del coque para formar compuestos entre capas. La fuerza del coque y el soporte de la carga durante la operación BF son críticos, ya que el colapso de la carga reduce la permeabilidad de gases y líquidos, lo que reduce la eficiencia tanto en la producción de HM como en el aumento de las emisiones de CO2.
Pequeñas partículas de coque de diferentes tamaños reducen los vacíos en el lecho de coque en la zona húmeda y aumenta el área superficial del coque. La rotura del coque también promueve la inundación, la obstrucción del hogar y el aumento de la quema de toberas y muescas de escoria, todo lo cual limita la producción del horno. La tendencia de que el gas ascendente sea transportado cerca de las paredes aumenta cuando se reduce la permeabilidad, lo que disminuye la utilización del gas y, por lo tanto, aumenta la tasa de coque.
Otro efecto del álcali es la mayor posibilidad de formación de andamios en el eje, ya que el álcali se condensa en el revestimiento y puede unir el material fino a él. Los andamios son una acumulación de material sólido en la pared del horno y se proyectan hacia el centro del horno. Los andamios pueden ocurrir en cualquier lugar desde la mitad hasta la parte superior del eje. El efecto de la formación de andamios es que el descenso de la carga se ralentiza o se interrumpe y, en casos extremos, provoca que se cuelgue, resbale y se cargue sin control. Los andamios también reducen el volumen de trabajo del BF. La velocidad del gas aumenta en las partes no afectadas del eje, lo que da como resultado una mayor temperatura del gas superior y una menor utilización del CO. Cuando los andamios se separan de la pared del horno, a menudo resulta en un hogar frío. Los andamios se pueden quitar aumentando temporalmente la temperatura del horno o se quitan cuando un flujo de gas de alta temperatura llega al área.
El material de carga también se puede unir mediante cianuros y carbonatos líquidos condensados, lo que reduce la permeabilidad del lecho. Además, el álcali puede atacar el material refractario, especialmente los refractarios a base de C que normalmente se usan en la parte inferior del horno. Los compuestos alcalinos penetran en los bloques C que se consumen formando vapor alcalino. Esto da como resultado una vida más corta del revestimiento refractario y la necesidad de un revestimiento más frecuente.
La eliminación de álcali se realiza principalmente con la escoria y se realiza mejor con valores de basicidad más bajos. Del álcali eliminado, más del 90 % se elimina a través de la escoria. Aquí la basicidad se considera como CaO/SiO2. Los resultados de varios estudios han demostrado que la basicidad más baja de la escoria aumenta la cantidad de álcali en la escoria. Sin embargo, el problema con una basicidad demasiado baja es que queda un nivel más alto de azufre (S) en el HM, ya que el S puede ser contrarrestado por el CaO presente en la escoria BF y el CaO es más bajo cuando la basicidad es más baja. El límite inferior de la basicidad para mantener la calidad de HM bajo control difiere de una planta a otra. El límite depende de los parámetros BF y la calidad de la materia prima utilizada. Un valor de basicidad justo por encima o alrededor de 1 puede verse como el límite si se va a eliminar el álcali y se va a mantener la calidad HM.
Para impedir la gasificación de los silicatos alcalinos, es necesario mantener alta la presión parcial de CO. La alta temperatura de la reacción a 1550 °C significa que también se puede usar una temperatura de llama más baja para ralentizar la reducción y la gasificación y, por lo tanto, reducir la circulación del álcali. La eliminación de álcali necesita una menor recirculación de materiales que contienen álcali al BF ya que, de lo contrario, el álcali se reintroduce en el BF.
La reducción del efecto catalizador del álcali en la gasificación del coque puede lograrse mediante la adición de cenizas de coque que pueden unir el álcali existente en formas más estables. Se ha probado con cierta adición de minerales antes. A medida que el álcali se difunde a través del coque, una capa de la adición de minerales puede estabilizar el álcali en la superficie del coque evitando que degrade las partes internas del coque.
Control de carga alcalina
Para controlar la carga de álcali en el BF, la entrada de álcali debe mantenerse lo más baja posible. Si hay una variación en el material entrante, la mezcla de minerales debe mezclarse bien para minimizar el riesgo de secciones con alto contenido de álcali en el BF. Otra precaución es evitar la recirculación de polvo de combustión con altos niveles de álcali. Una forma de minimizar el riesgo de formación de andamios es aumentar la resistencia de la carga ferrosa y del coque para evitar la formación de finos.
El BF se puede operar con un flujo de gas central. Debido a esto, la temperatura del gas superior en el centro aumenta a tal nivel que parte del álcali sale del horno como vapor con el gas superior. Sin embargo, las temperaturas más altas del gas superior dan como resultado mayores pérdidas de calor.
El álcali recirculado se puede disminuir y, en su lugar, dejar el BF a través de la escoria haciendo funcionar el BF con una escoria ácida. Cuanto menor es la basicidad de la escoria, más fácilmente se absorben el K y el Na básicos en la escoria, ya que la cal (CaO) y la magnesia (MgO) ocupan los mismos sitios en la red de sílice que los óxidos alcalinos. Se puede lograr una basicidad disminuida disminuyendo la basicidad en las adiciones de carga y fundente ferroso. Sin embargo, una basicidad más baja también da como resultado un mayor contenido de S (azufre) en el HM, ya que el S se une al Ca en la escoria.
Otra posibilidad de disminuir la carga de álcali es aumentar el volumen de escoria, lo que disminuye la actividad de los óxidos alcalinos en la escoria y, por lo tanto, aumenta la absorción de álcali y la salida a través de la escoria, pero un mayor volumen de escoria también aumenta la tasa de coque.
Una temperatura más baja en el BF da como resultado una menor reducción y vaporización del álcali. Operar el BF con una temperatura de llama más baja da como resultado una menor carga de álcali, pero también una menor productividad y una mayor tasa de coque. La carga de álcali también se puede disminuir haciendo funcionar el BF con alta presión parcial de CO, ya que se opone a la reacción de gasificación de álcali. Esto se puede lograr mediante el enriquecimiento de O2 de la explosión o alta presión superior.
Proceso de manufactura
- Sistema de control, medición y automatización de procesos de alto horno
- Uso de coque de nuez en un alto horno
- Proceso HIsmelt de fabricación de hierro
- Proceso HIsarna para la fabricación de hierro
- Irregularidades del alto horno durante la operación
- Sistema de enfriamiento de alto horno
- Química del Proceso de Fabricación de Hierro por Alto Horno
- Revestimiento refractario de alto horno
- Alto Horno y su Diseño
- Métodos para apagar un alto horno
- Fabricación de hierro por alto horno y emisiones de dióxido de carbono



