Síntesis en un recipiente de efecto confinado al espacio de heteroestructuras de γ-AlO (OH) / MgAl-LDH con excelente rendimiento de adsorción
Resumen
Aquí, γ-AlO (OH) como inorgánico se insertó con éxito en la capa de MgAl-LDH mediante una síntesis en un solo recipiente, el compuesto como adsorbente para eliminar el naranja de metilo (MO) de las aguas residuales. Se caracterizaron la estructura y el rendimiento de adsorción de γ-AlO (OH) / MgAl-LDH. La investigación muestra que el plano de expansión (003) y el sitio activo de hidroxilo de γ-AlO (OH) / MgAl-LDH pueden promover la capacidad de adsorción y la cinética de adsorción, respectivamente. Por lo tanto, γ-AlO (OH) / MgAl-LDH exhibe un rendimiento de súper adsorción, que adsorbe completamente MO a la concentración de 1000 mg g −1 . Además, la capacidad máxima de adsorción de MO fue de 4681,40 mg g −1 según el modelo de Langmuir. Estos resultados indican que γ-AlO (OH) / MgAl-LDH es un adsorbente potencial para la eliminación de colorantes orgánicos en el agua.
Introducción
Los tintes orgánicos se utilizan ampliamente en muchos productos como textiles, cuero, pintura y caucho [1, 2, 3]. Estos colorantes se descargan fácilmente en el agua [4], lo que provoca serios problemas ambientales, como dañar los organismos acuáticos, consumir oxígeno disuelto y manchar el agua [3, 5]. Además, la mayoría de los tintes orgánicos son altamente polares, no volátiles y difíciles de biodegradar. Se observa que las aguas residuales con tintes son muy perjudiciales para la salud humana. Por tanto, el tratamiento de las aguas residuales con tintes es una tarea urgente. En la actualidad, la mayoría de los tratamientos para las aguas residuales de colorantes utilizan adsorción física, fotocatálisis, oxidación biológica y química, floculación y separación por membranas [4, 6]. Entre ellos, el método de adsorción física tiene una posición especial en el campo del tratamiento de aguas residuales debido a su capacidad para enriquecer selectivamente ciertos compuestos. Además, el método de adsorción tiene las características de un buen efecto de adsorción, operación simple y amplio rango de aplicación y ha sido ampliamente utilizado en el campo del tratamiento de aguas residuales con tintes [7, 8].
Los hidróxidos dobles en capas (LDH), una arcilla aniónica común, están formados por capas similares a la brucita [9]. Su fórmula general se puede expresar como [ M 2+ 1 - x M 3+ x (OH) 2 ] [( A n - ) x / n ] · YH 2 O, donde M 2+ , M 3+ y A n - representan los cationes bivalentes, cationes trivalentes y n -aniones valentes, respectivamente [10]. LDH tiene excelentes propiedades de adsorción para tintes debido a su alta capacidad de intercambio aniónico y gran área de superficie. Por ejemplo, Lafi et al. preparó MgAl-LDH mediante un método de coprecipitación; la capacidad de adsorción del adsorbente en rojo Congo alcanzó 111.111 mg g −1 [11]. Zheng y col. preparó Zn-Mg-Al LDH también mediante el método de coprecipitación, que tiene una excelente capacidad de adsorción de hasta 883,24 mg g −1 para naranja de metilo en la condición de pH =3 [12]. Claramente, para los adsorbentes de LDH, la mayoría de los investigadores se enfocan en la búsqueda de una alta capacidad de intercambio iónico y una gran superficie específica. Desafortunadamente, la nanocristalización de LDH no está exenta de límites. En los últimos años, los investigadores han descubierto que el inserto orgánico o inorgánico en las capas de LDH puede aumentar la capacidad de adsorción de LDH. Por ejemplo, Mandal et al. insertó alginato de sodio entre las capas de LDH para formar un adsorbente compuesto. El alginato de sodio ayuda a ampliar el espacio entre capas de la LDH y aumenta la capacidad de adsorción del adsorbente para el tinte naranja II [13]. Bruna y col. sintetizado orgánico / LDH (inserto de dodecilsulfato de anión orgánico (DDS) para MgAl-LDH) como adsorbente de hidrocarburos aromáticos policíclicos en sistemas de agua y suelo-agua [14]. Por lo tanto, es una buena idea diseñar el adsorbente insertando un compuesto entre las capas de LDH. El hidróxido de óxido de aluminio (γ-AlO (OH)) es un buen adsorbente para el tratamiento de aguas residuales, debido a su alta superficie específica y a la gran cantidad de grupos hidroxilo en la superficie [15, 16]. Por lo tanto, γ-AlO (OH) es un material de intercalación inorgánico potencial para MgAl-LDH.
En este artículo, γ-AlO (OH) se insertó con éxito en MgAl-LDH mediante un método hidrotermal. Este compuesto exhibe excelentes propiedades de adsorción de naranja de metilo (MO). Las características estructurales de los compuestos γ-AlO (OH) / MgAl-LDH se evaluaron mediante difracción de rayos X en polvo (XRD), espectroscopía infrarroja por transformada de Fourier (FTIR), microscopía electrónica de barrido por emisión de campo (FESEM), microscopía electrónica de transmisión ( TEM) y microscopía electrónica de transmisión de alta resolución (HRTEM). Las propiedades de adsorción de los compuestos se evaluaron mediante la adsorción de MO y se realizó una investigación en profundidad sobre el mecanismo sinérgico de γ-AlO (OH) y MgAl-LDH.
Métodos
Preparación de γ-AlO (OH) / MgAl-LDH
Todos los reactivos químicos eran de calidad analítica y se utilizaron sin purificación adicional. El compuesto γ-AlO (OH) / MgAl-LDH se preparó utilizando el método hidrotermal. En una síntesis típica, Mg (NO 3 ) 2 · 6H 2 O (4,615 g) y Al (NO 3 ) 3 · 9H 2 Se disolvieron O (3.376 g) en 50 mL de agua desionizada (DI) (Mili-Q, 18.2 MΩ) para formar la solución 1. Se disolvió NaOH (2.516 g) en 25 mL de agua desionizada desgasificada, de modo que se produjo la solución 2 . Las soluciones 1 y 2 se añadieron gota a gota a un recipiente de reacción que contenía 25 ml de agua desionizada y se agitó vigorosamente a un valor de pH constante de 10 y una temperatura de 60ºC. Luego, la suspensión resultante se trató adicionalmente en condiciones hidrotermales a 140 ° C durante 10 h y se enfrió a temperatura ambiente. γ-AlO (OH) / MgAl-LDH se lavó varias veces con agua desionizada y se liofilizó en un liofilizador al vacío. A modo de comparación, se prepararon MgAl-LDH y γ-AlO (OH) puros mediante el mismo tratamiento hidrotermal (140 ° C, 10 h).
Caracterización
La estructura de fase se caracterizó por difracción de rayos X en polvo (XRD; X’Pert PRO PANalytical) en el 2 θ rango de 5-80 ° con radiación Cu Kα a una longitud de onda de 0.15406 nm. Se obtuvieron imágenes de la morfología de la superficie de la muestra mediante FESEM (S4800) a 5 kV. La microestructura de las muestras se analizó mediante HRTEM (JEM-2100F) a 200 kV. Los espectros de infrarrojos se registraron en el rango de 4000 a 400 cm −1 utilizando un espectrómetro FTIR (NEXUS 470, Nicolet instruments) con una resolución óptica de 4 cm −1 y un tamaño de apertura de 100 im. Los experimentos de adsorción-desorción de nitrógeno para la cuantificación de la superficie y la porosidad se realizaron a - 196 ° C con un instrumento NOVA-1200e. Antes del análisis, las muestras se pretrataron a 80 ° C durante 12 h al vacío. Se realizaron mediciones de espectroscopía de fotoelectrones de rayos X (XPS; ESCALAB 250Xi) utilizando radiación Al Kα. La energía de la exploración del espectro de levantamiento fue de 100 eV por el tamaño de paso de 1 eV. La energía del escaneo de alta resolución fue de 20 eV por el tamaño de paso de 0,1 eV. El vacío de la prueba es 10 −10 mbar. Los espectros de absorción UV-Vis de las diferentes muestras se obtuvieron mediante un espectrofotómetro UV-3600 equipado con una esfera integradora. Los espectros de fotoluminiscencia de los materiales se obtuvieron mediante un espectrofotómetro de fluorescencia (VARIAN).
Experimentos de adsorción
Se probó el rendimiento de adsorción de las muestras para la adsorción de naranja de metilo (MO) en solución acuosa. Se colocó una muestra de 50 mg en 50 ml de 1000 mg L −1 Solución de MO bajo agitación magnética. El valor de pH de la solución se ajustó usando 0.1 M HNO 3 ácido o solución de NaOH 1 M. Después de un tiempo apropiado, se tomó la muestra de agua (3 mL) de la suspensión. El sobrenadante se obtuvo por centrifugación y la concentración de la solución se midió con un espectrofotómetro UV-Vis (UV-3600). La cantidad de equilibrio de adsorción ( q e (mg g −1 )) y la cantidad instantánea de adsorción ( q t (mg g −1 )) se calcularon mediante las siguientes ecuaciones:
$$ {q} _t =\ frac {\ left ({C} _0- {C} _t \ right) V} {m} \ kern35em (1) $$$$ {q} _e =\ frac {\ left ( {C} _0- {C} _e \ derecha) V} {m} \ kern35.25em (2) $$donde C 0 (mg L −1 ) es la concentración inicial de MO; C e (mg L −1 ) y C t (mg L −1 ) son la concentración de MO en equilibrio y en el tiempo t (min), respectivamente; V (L) es el volumen de la solución; y m (g) es la masa del adsorbente.
Experimentos de desorción
El experimento de desorción de MO se realizó utilizando agua desionizada como agente perturbador. Una porción de 50 mg de las muestras usadas se lavó suavemente con agua para eliminar cualquier MO no perturbado. Además, las muestras de MO cargadas se agitaron vigorosamente con una solución de etanol y se centrifugaron. Después de la centrifugación, las muestras obtenidas se liofilizaron. Luego, las muestras de polvo resultantes se sometieron a sucesivos ciclos de adsorción-desorción.
Resultados y discusión
Caracterización de muestras como sintetizadas
Los patrones XRD de las muestras tal como se sintetizaron se muestran en la Fig. 1a. Para γ-AlO (OH) / MgAl-LDH, se observa que los picos de difracción mayores se encuentran en 10.09 °, 19.95 °, 34.40 °, 60.56 ° y 61.48 °, que corresponden a (003), (006), (012), (110) y (113) planos de MgAl-LDH (JPCDS No. 89-0460), respectivamente. Además, los picos a 14,1 °, 27,9 °, 38,1 ° y 48,9 ° se pueden atribuir a los planos de difracción (020), (120), (031) y (051) de γ-AlO (OH) (JPCDS No. 21-1307), respectivamente. Este resultado indica que el compuesto γ-AlO (OH) / MgAl-LDH tiene fases MgAl-LDH y γ-AlO (OH). Además, a modo de comparación, el plano (003) de MgAl-LDH se encuentra en 2 θ =11,63 °, lo que indica que cuando se insertó γ-AlO (OH) en MgAl-LDH, el espaciado del plano (003) aumentó de 7,6 Å (2 θ =11,63 °) a 8,77 Å (2 θ =10,09 °). Los parámetros de la celda unitaria se muestran en la Tabla 1. Se observa que los ejes "a" de MgAl-LDH y γ-AlO (OH) / MgAl-LDH no han cambiado.
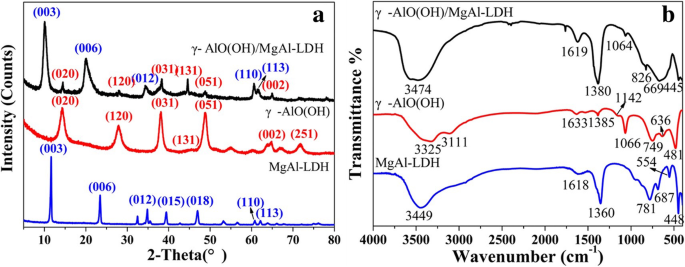
Patrones XRD de muestras sintetizadas ( a ). Los espectros FTIR de muestras sintetizadas a 400–4000 cm −1 ( b )
Los espectros FTIR de las muestras tal como se sintetizaron se muestran en la Fig. 1b. En el espectro FTIR de MgAl-LDH, la banda a 3449 cm −1 puede atribuirse a la vibración de estiramiento O – H [17]. Las bandas de 400 a 900 cm −1 se deben a M – O, O – M – O y M – O – M (M =Mg 2+ y Al 3+ ) estirando las vibraciones [18], y la banda a 781 cm −1 se debe a una vibración Al-OH [19]. Para γ-AlO (OH), las bandas en 3111 y 3325 cm −1 pertenecen a las vibraciones de estiramiento υas (Al) O – H y υs (Al) O – H, respectivamente [20]. Las vibraciones de los enlaces de hidrógeno se observaron a 1142 y 1066 cm −1 [21]. Además, los picos a 481, 636 y 749 cm −1 puede asignarse a enlaces Al – O [22]. Para γ-AlO (OH) / MgAl-LDH, la mayoría de las bandas se pueden asignar fácilmente basándose en la comparación con γ-AlO (OH) y MgAl-LDH. La banda fuerte a 3474 cm −1 puede atribuirse a la vibración de estiramiento de los grupos –OH en γ-AlO (OH) y MgAl-LDH. Las bandas a 826, 669 y 445 cm −1 corresponden a vibraciones de estiramiento metal-oxígeno, metal-oxígeno-metal y oxígeno-metal-oxígeno en MgAl-LDH, respectivamente [18]. En comparación con MgAl-LDH, la banda de Al-OH se desplaza de 781 a 826 cm −1 . Además, la banda a 1064 cm −1 puede asignarse a la vibración del enlace de hidrógeno en γ-AlO (OH). Las bandas a 1618, 1633 y 1619 cm −1 en MgAl-LDH, γ-AlO (OH) y γ-AlO (OH) / MgAl-LDH, respectivamente, se pueden asignar a la vibración de flexión de las moléculas de agua. Además, las bandas a 1360, 1385 y 1380 cm −1 en MgAl-LDH, γ-AlO (OH) y γ-AlO (OH) / MgAl-LDH, respectivamente, están relacionados con CO 3 2− [23]. La banda de CO 3 2− en γ-AlO (OH) indica que algunos residuos a base de carbonato permanecen atrapados dentro del monolito celular altamente poroso incluso después de lavados repetidos [24].
La morfología y la microestructura de las muestras se investigaron mediante microscopía electrónica de barrido de emisión de campo (FESEM) y microscopía electrónica de transmisión (TEM). Como se muestra en la Fig. 2a, se observa que la muestra de MgAl-LDH consta de nanohojas. Se estima que el grosor medio de las nanoláminas se sitúa entre 140 y 150 nm. La imagen de FESEM en la Fig. 2b muestra que γ-AlO (OH) consta de nanoagujas. La muestra de γ-AlO (OH) / MgAl-LDH que se muestra en la Fig. 2c tiene una morfología que consiste en aglomerados escamosos en lugar de la morfología de γ-AlO (OH). En el caso de la Fig. 2d, e, las imágenes TEM de MgAl-LDH y γ-AlO (OH), respectivamente, también muestran una fuerte evidencia de la morfología en forma de nanohoja de MgAl-LDH y la morfología en forma de nanoaguja de γ- AlO (OH). Curiosamente, se observa claramente que la muestra de γ-AlO (OH) / MgAl-LDH consta de nanohojas y nanoagujas (Fig. 2f). Además, en la imagen HRTEM de γ-AlO (OH) / MgAl-LDH (Fig.2g), el espaciado de la red de 0.235 nm y 0.152 nm correspondió al plano (031) de γ-AlO (OH) y (110) plano de MgAl-LDH. Además, el mapeo EDX de la Fig. 2h demostró la distribución uniforme de los elementos C, O, Mg y Al en los compuestos, lo que indica que el compuesto γ-AlO (OH) / MgAl-LDH se mezcló de manera homogénea.

Imágenes FESEM de MgAl-LDH ( a ), γ-AlO (OH) ( b ) y γ-AlO (OH) / MgAl-LDH ( c ). Imágenes TEM de MgAl-LDH ( d ), γ-AlO (OH) ( e ) y γ-AlO (OH) / MgAl-LDH ( f ). Imagen HRTEM ( g ) y mapeo EDX ( h , yo ) de γ-AlO (OH) / MgAl-LDH
Los análisis XRD, FTIR, FESEM y HRTEM muestran que la nanoaguja γ-AlO (OH) se preparó con éxito en las capas de MgAl-LDH mediante el método hidrotermal, que aprovecha el efecto de "espacio confinado" del MgAl-LDH.
Efecto del pH de la solución inicial
El pH de la solución juega un papel importante en el proceso de adsorción debido a la carga superficial del adsorbente [25]. La Figura 3 muestra el rendimiento de adsorción de la muestra de γ-AlO (OH) / MgAl-LDH en MO bajo diferentes valores de pH, con la concentración inicial de MO en 1000 mg L −1 . Se observa que la mayor adsorción ocurre cuando el pH inicial =3, y la capacidad de adsorción disminuye al aumentar el pH, lo que indica que la muestra sintetizada es más efectiva para adsorber MO en solución ácida. Además, las estructuras de los materiales estratificados con láminas de hidróxido desaparecen cuando el pH es inferior a 3 [26]. Por lo tanto, se sugiere que el pH de la solución inicial usado en este estudio sea 3. Fotografías de la muestra de γ-AlO (OH) / MgAl-LDH que adsorbe MO a diferentes valores de pH también se muestran en la Fig. 3 (recuadro). Se observa que a pH =3, después de que el MO se adsorbió durante 210 min, el color de la solución era claro, lo que indica que el MO se adsorbió por completo. A medida que aumentaba el pH, el color de la solución se oscurecía.
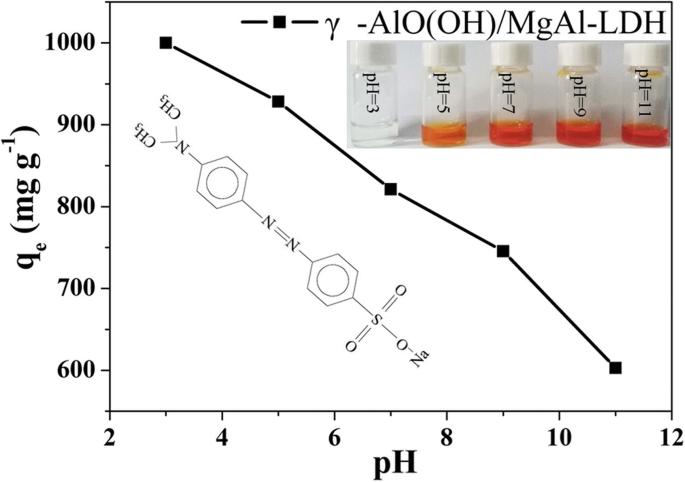
Efecto de los valores de pH de la solución inicial sobre la adsorción de MO de γ-AlO (OH) / MgAl-LDH (concentración inicial de MO:1000 mg L −1 , dosis de adsorbente:1 g L −1 , tiempo de contacto:210 min), recuadro:las fotografías ópticas de la solución de MO después de adsorbida a diferentes pH
Efecto del tiempo de contacto y la cinética de la adsorción
El efecto del tiempo de contacto sobre la adsorción de MO por las muestras se muestra en la Fig. 4. Para todos los adsorbentes, las velocidades iniciales de adsorción son muy rápidas. En comparación con γ-AlO (OH) y MgAl-LDH puros, γ-AlO (OH) / MgAl-LDH muestra un rendimiento de adsorción mejorado en términos de velocidad y capacidad de adsorción. Cuando la concentración inicial de MO fue de 1000 mg L −1 para γ-AlO (OH) / MgAl-LDH y 200 mg L −1 para γ-AlO (OH) y MgAl-LDH, la capacidad máxima de adsorción en equilibrio experimental de 1000 mg g −1 se obtuvo utilizando γ-AlO (OH) / MgAl-LDH, que fue superior al de γ-AlO (OH) (183,3 mg g −1 ) y MgAl-LDH (155,5 mg g −1 ). Como se muestra en la Fig. 4 (recuadro), se observa que la solución de γ-AlO (OH) / MgAl-LDH es completamente incolora después del equilibrio. Sin embargo, los colores de las soluciones puras de γ-AlO (OH) y MgAl-LDH permanecen muy profundos.
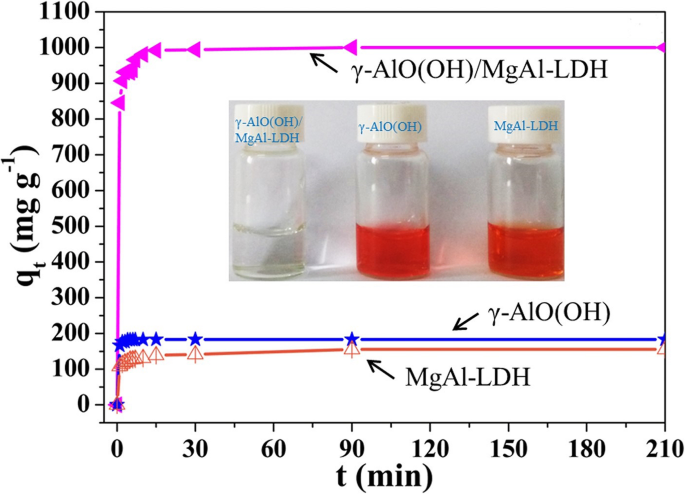
Efecto del tiempo de contacto sobre la adsorción de MO, recuadro:fotografías ópticas de equilibrio de la solución de MO después de la adsorción
Para comprender los mecanismos de adsorción de las muestras, se utilizaron modelos cinéticos de pseudo-primer orden y pseudo-segundo orden para ajustar los datos experimentales. Las leyes de tasa de pseudo-primer orden y pseudo-segundo orden se calculan a partir de las Ecs. (3) y (4) [27], respectivamente:
$$ \ ln \ left ({q} _e- {q} _t \ right) =\ ln {q} _e- {k} _1t \ kern30.25em (3) $$$$ \ frac {t} {q_t} =\ frac {1} {k_2 {q} _e ^ 2} + \ frac {t} {q_e} \ kern37.25em (4) $$donde q t (mg g −1 ) y q e (mg g −1 ) son la cantidad de MO adsorbido en el momento t (min) y en equilibrio, respectivamente, y k 1 (mínimo −1 ) y k 2 (g mg −1 min −1 ) son las constantes de velocidad de adsorción de los modelos cinéticos de pseudo primer orden y pseudo segundo orden [28], respectivamente.
La Tabla 2 muestra los dos modelos cinéticos de adsorción y los coeficientes de correlación. Del coeficiente de correlación R 2 En la Tabla 2, se observa que la adsorción de muestras fue ajustada mejor por el modelo de pseudo-segundo orden que por el modelo de pseudo-primer orden. Además, los valores teóricos calculados ( q e, cal ) del modelo de pseudo-segundo orden están más cerca de los valores experimentales ( q e, exp ) que los del modelo de pseudoprimer orden. Por lo tanto, basándose en el supuesto de una cinética de pseudo-segundo orden, las tasas de adsorción de MgAl-LDH, γ-AlO (OH) y γ-AlO (OH) / MgAl-LDH están controladas por interacciones químicas [29].
Isotermas de adsorción
La Figura 5 muestra las isotermas de adsorción de las muestras sintetizadas. Entre las tres muestras, el q e El valor de γ-AlO (OH) / MgAl-LDH exhibió el aumento más rápido con C e . Además, los datos del experimento de adsorción se analizaron mediante los modelos de Langmuir y Freundlich para evaluar la relación entre el MO y los adsorbentes en equilibrio [30]. Las ecuaciones son las siguientes:
$$ \ mathrm {Idioma}:\ frac {C_e} {q_e} =\ frac {1} {q_m {K} _L} + \ frac {C_e} {q_m} \ kern29em (5) $$$$ \ mathrm { Francés}:\ ln {q} _e =\ ln {K} _F + \ frac {1} {n} \ ln {C} _e \ kern27.25em (6) $$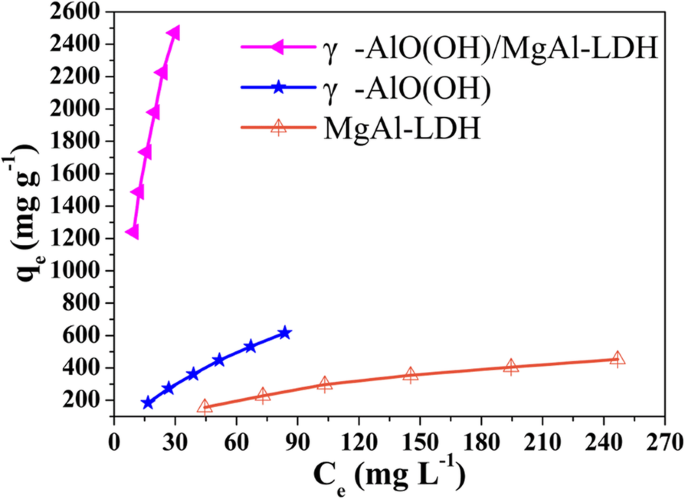
Las isotermas de adsorción de equilibrio de las muestras
donde C e (mg L −1 ) es la concentración de equilibrio del MO, q e (mg g −1 ) es la cantidad de MO adsorbido por unidad de masa de los adsorbentes, y q m (mg g −1 ) es la capacidad de adsorción de una monocapa. K L (L mg −1 ) es la constante de Langmuir relacionada con la tasa de adsorción. K F [(mg g −1 ) (L mg −1 ) 1 / n ] y n −1 (adimensionales) son constantes de Freundlich relacionadas con la capacidad de adsorción y la fuerza de adsorción, respectivamente.
Los parámetros correspondientes de las isotermas de adsorción simuladas de las muestras se enumeran en la Tabla 3. Se observa que la capacidad máxima de adsorción de MO en γ-AlO (OH) / MgAl-LDH fue significativamente mayor que en γ-AlO (OH) y MgAl-LDH. Además, en comparación con el modelo de Freundlich, el modelo de Langmuir se ajusta mejor a los datos experimentales y tiene una R más alta 2 . El q m de γ-AlO (OH) / MgAl-LDH (4681,40 mg g −1 ) de la ecuación de Langmuir es mucho más alta que la de γ-AlO (OH) (1492,5 mg g −1 ) y MgAl-LDH (769,2 mg g −1 ). Además, el K más grande F de la ecuación de Freundlich también indica que γ-AlO (OH) / MgAl-LDH tiene una mayor afinidad por MO. Sorprendentemente, la capacidad de adsorción de γ-AlO (OH) / MgAl-LDH fue mucho mayor que la mayoría de los reportados (como se muestra en la Tabla 4).
El mecanismo de adsorción de γ-AlO (OH) / MgAl-LDH para MO
La Figura 6a, b muestra el N 2 isotermas de adsorción-desorción y distribución del tamaño de poro BJH de las muestras. Según la clasificación IUPAC, las isotermas se pueden clasificar como curvas IV con bucles de histéresis H3 a alta presión relativa. Está comprobado que los adsorbentes tienen propiedades de material mesoporoso. La distribución del tamaño de los poros calculada por el método BJH se muestra en la Fig. 6b. En comparación con MgAl-LDH, γ-AlO (OH) y γ-AlO (OH) / MgAl-LDH tienen curvas de distribución de tamaño de poro más amplias. Como se muestra en la Tabla 1, los resultados del análisis BET de MgAl-LDH, γ-AlO (OH) y γ-AlO (OH) / MgAl-LDH fueron 14,1 m
2
g
−1
, 95,9 m
2
g
−1
y 34,1 m
2
g
−1
, respectivamente. Los resultados demostraron que el excelente rendimiento de adsorción de γ-AlO (OH) / MgAl-LDH no depende de la gran superficie específica. Las fotografías ópticas de las muestras antes y después de la adsorción de MO se muestran en la Fig. 6c (antes de la centrifugación). Según las fotografías ópticas antes de la adsorción, el volumen original de la muestra era γ-AlO (OH) / MgAl-LDH <γ-AlO (OH)
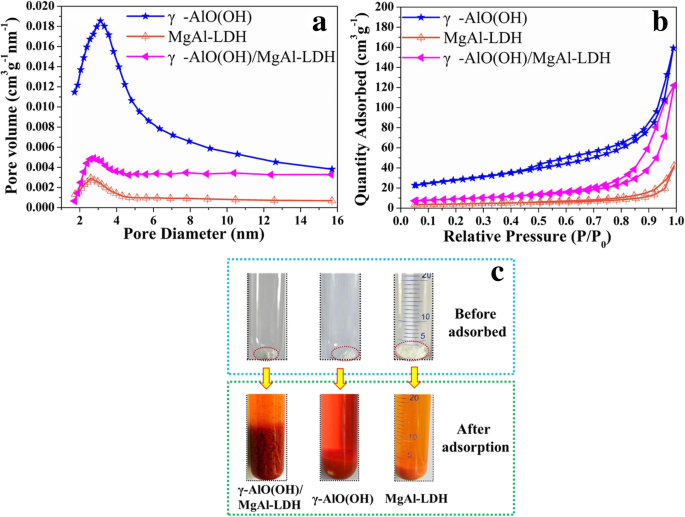
N 2 curvas de isotermas de adsorción-desorción ( a ) y curvas de distribución del tamaño de los poros ( b ) de muestras. Las fotografías ópticas de muestras antes y después de la adsorción ( c )
La Figura 7a muestra los patrones XRD de γ-AlO (OH) / MgAl-LDH antes y después de la adsorción de MO. En comparación con γ-AlO (OH) / MgAl-LDH, aparecieron muchos picos nuevos en los espectros de γ-AlO (OH) / MgAl-LDH después de la adsorción de MO. Además, a excepción de los planos (003) y (006) de MgAl-LDH, los otros planos no se desplazaron a un ángulo bajo. Los nuevos picos indican que los aniones MO entran en la capa intermedia de γ-AlO (OH) / MgAl-LDH a través del intercambio aniónico y conducen a un desplazamiento del plano (003) al plano del ángulo menor [8]. Más importante aún, el plano (003) de γ-AlO (OH) / MgAl-LDH aumentó en 3,22 Å de 8,77 a 11,99 Å después de la adsorción de MO. Curiosamente, como se muestra en la Fig. 7b, el grado correspondiente al plano (003) de MgAl-LDH no cambió después de adsorber MO, lo que indica que MO no puede adsorberse en las capas de MgAl-LDH. Se observa que γ-AlO (OH) juega un papel importante en la capa de LDH, y el efecto de adsorción sobre el MO se muestra en el Esquema 1. Por un lado, por el efecto de “espacio confinado”, la nanoaguja γ-AlO (OH ) se puede cultivar entre las capas de MgAl-LDH para expandir el espaciado del plano (003), lo que ayuda a que MO entre en la capa intermedia de MgAl-LDH por atracción electrostática. Por otro lado, MgAl-LDH tiene más espacio para almacenar MO, debido a la expansión entre las capas LDH.
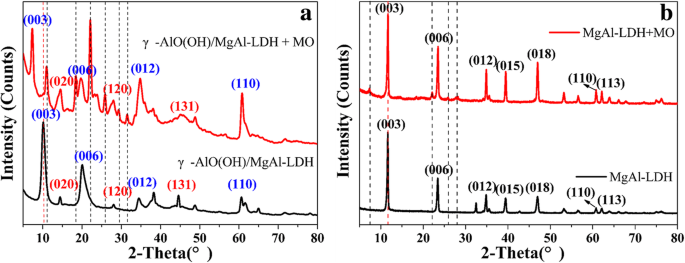
Los patrones de XRD de γ-AlO (OH) / MgAl-LDH ( a ) y MgAl-LDH ( b ) antes y después del MO adsorbido, respectivamente
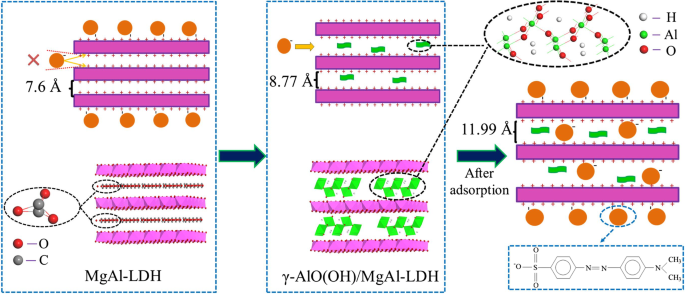
El mecanismo de γ-AlO (OH) / MgAl-LDH para mejorar la adsorción de MO
A partir de la discusión anterior, se sabe que γ-AlO (OH) / MgAl-LDH tiene una cinética de adsorción y un rendimiento de adsorción más altos que γ-AlO (OH) y MgAl-LDH. Para estudiar mejor el mecanismo de mejora del rendimiento, las muestras se sometieron a una prueba de potencial zeta. Como se muestra en la Fig.8a, la suspensión de las muestras a pH =3 mostró una superficie cargada positivamente y el valor de potencial ζ de γ-AlO (OH) / MgAl-LDH (43.03 mV) fue mucho mayor que el de MgAl- LDH (13,88 mV) y γ-AlO (OH) (4,32 mV). Este resultado indica que el efecto sinérgico se puede producir debido a que γ-AlO (OH) ingresa a la capa de MgAl-LDH, lo que mejora el potencial zeta de la muestra de γ-AlO (OH) / MgAl-LDH. Como se muestra en el esquema 1, la molécula de MO se puede formar en C 14 H 14 N 3 SO 3 - y Na + en agua. Porque C 14 H 14 N 3 SO 3 - El anión está cargado negativamente, es fácilmente adsorbido por γ-AlO (OH) / MgAl-LDH. Se podría inferir que LDH presenta una buena capacidad de adsorción de colorantes aniónicos.
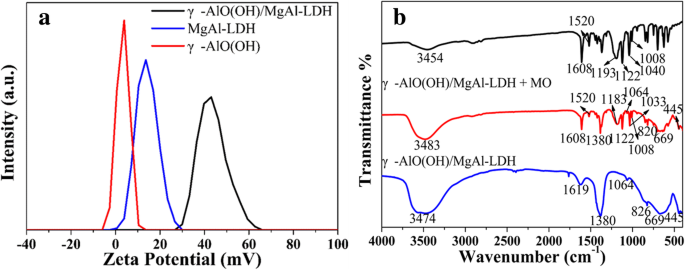
ζ-potenciales de muestras (0,2 mg mL −1 ) en solución acuosa a pH =3 ( a ). Espectros FTIR de MO, γ-AlO (OH) / MgAl-LDH antes y después de MO adsorbido ( b )
Los espectros FTIR de γ-AlO (OH) / MgAl-LDH después de adsorber MO se muestran en la Fig. 8b. En comparación con el γ-AlO (OH) / MgAl-LDH original, los espectros FTIR de γ-AlO (OH) / MgAl-LDH mostraron cambios obvios después de absorber MO. Las bandas a 1608 y 1520 cm −1 se debieron a la vibración de estiramiento N =N y la vibración de flexión N – H. Además, las bandas a 1183 y 1033 cm −1 se debieron a las vibraciones de estiramiento asimétricas y simétricas del grupo del ácido sulfónico (–SO 3 - ), respectivamente. La banda a 1122 cm −1 se debió a la vibración de estiramiento simétrico de O =S =O [36]. La banda a 1008 cm −1 se relacionó con la vibración de flexión aromática en el plano C – H [1]. Obviamente, el pico O – H de γ-AlO (OH) / MgAl-LDH se desplazó de 3474 a 3843 cm −1 cuando se absorbió el MO, lo que indica que el enlace de hidrógeno participa en el proceso de adsorción.
Además, se utilizó XPS para caracterizar el adsorbente antes y después de adsorber el MO. Como se muestra en la Fig. 9, el elemento S apareció en el espectro de γ-AlO (OH) / MgAl-LDH después de adsorber MO. El espectro de alta resolución de S 2p ubicado en 167 eV, que se muestra en la Fig. 9b, indica la presencia de MO en el adsorbente. La Figura 9c, d muestra el espectro de O 1s de γ-AlO (OH) / MgAl-LDH antes y después de la adsorción de MO, respectivamente. En la Fig. 9c, d se muestran tres picos ubicados en 530.5, 531 y 531.8 eV, y se pueden asignar al O en forma de óxido metálico (M – O), el carbonato (CO 3 2− ) y metal-hidroxilo (M – OH) de la capa intermedia de MgAl-LDH [1]. En particular, hay cambios significativos en la intensidad y composición de los O 1 del adsorbente después de la adsorción de MO. El pico de aparición reciente ubicado a 531,6 eV en la Fig. 9d podría asignarse al O en el grupo sulfato (S – O). Además, como se muestra en la Tabla 5, el CO 3 2− disminuyó de 27,2 a 18,1%, debido al intercambio iónico. La proporción relativa de M – O después de adsorber MO aumenta de 9 a 26,4%, y la proporción relativa de M – OH disminuyó de 63,8 a 25,7%. Los resultados muestran que el sitio activo de hidroxilo de γ-AlO (OH) / MgAl-LDH juega un papel importante en la adsorción de naranja de metilo, lo que indica que la adsorción de MO está controlada por interacciones químicas; esto es consistente con el modelo cinético de pseudo-segundo orden.
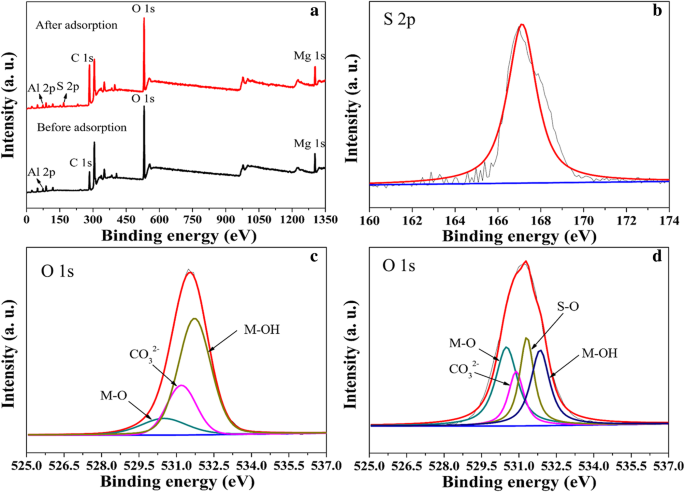
Amplios espectros XPS de γ-AlO (OH) / MgAl-LDH antes y después de la adsorción de MO ( a ), S 2p XPS estrecho de γ-AlO (OH) / MgAl-LDH después de MO adsorbido ( b ), Espectro de O 1s de γ-AlO (OH) / MgAl-LDH ( c ), Espectro de O 1s de γ-AlO (OH) / MgAl-LDH después de MO adsorbido ( d )
Reciclaje de adsorbentes
Se estudió el rendimiento de regeneración del adsorbente γ-AlO (OH) / MgAl-LDH mediante ciclos de adsorción-desorción. Como se muestra en la Fig.10, la capacidad de adsorción de γ-AlO (OH) / MgAl-LDH se mantuvo en 762 mg g −1 después de 4 ciclos, y la eficiencia de eliminación se mantuvo por encima del 76%. La disminución de la capacidad se debe a la desorción incompleta de MO y la pérdida del adsorbente durante la adsorción y el lavado de las moléculas de tinte. Estos resultados indican que γ-AlO (OH) / MgAl-LDH puede considerarse un adsorbente eficiente y reciclable para la eliminación de MO del agua.
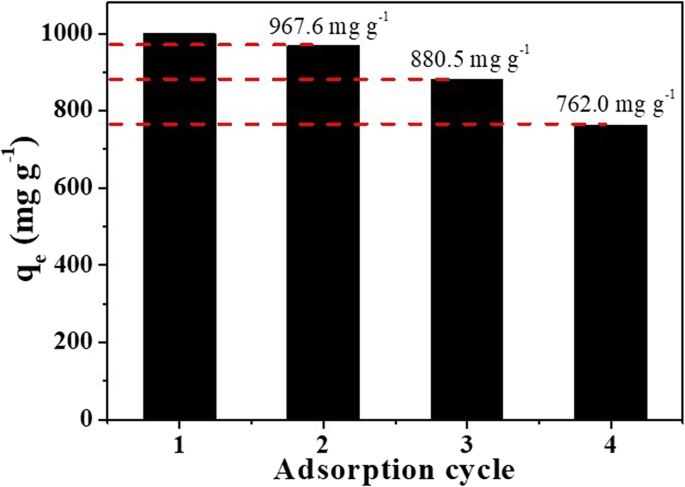
Rendimiento del ciclo de adsorción de γ-AlO (OH) / MgAl-LDH. Concentración inicial de MO:1000 mg L −1
Conclusión
El compuesto de γ-AlO (OH) / MgAl-LDH se sintetizó mediante el método de un solo recipiente. Como adsorbente, el compuesto exhibe un excelente rendimiento de adsorción de MO. Por un lado, basándose en el efecto de “espacio confinado”, se preparó nanoaguja de γ-AlO (OH) entre las capas de MgAl-LDH. La expansión entre las capas de LDH conduce a más espacio para almacenar MO. Por otro lado, el sitio activo de hidroxilo da como resultado una interacción química entre γ-AlO (OH) / MgAl-LDH y MO, lo que promueve la cinética de adsorción. Por lo tanto, la γ-AlO (OH) / MgAl-LDH exhibe un excelente rendimiento de adsorción de MO, que puede adsorberse completamente en 210 min a la concentración inicial de 1000 mg L −1 . Después de 4 ciclos, el adsorbente regenerado puede mantener una capacidad de adsorción inicial de más del 76%. Además, la capacidad máxima de adsorción de γ-AlO (OH) / MgAl-LDH alcanza los 4681,40 mg g −1 según el modelo de adsorción de Langmuir. Basado en el potencial zeta positivo de γ-AlO (OH) / MgAl-LDH, el compuesto tiene una cinética de adsorción más fuerte y propiedades de adsorción para tintes aniónicos como MO, Rojo Congo y Naranja Ácido 7. Estos tintes adsorbidos se pueden desorber y reutilizar. , o incinerado directamente. Además, el material compuesto también es un portador de fotocatalizador potencial. Cuando el fotocatalizador se carga en γ-AlO (OH) / MgAl-LDH, los colorantes se absorberán rápidamente alrededor del catalizador, lo que mejora la cinética de la reacción fotocatalítica. Por lo tanto, γ-AlO (OH) / MgAl-LDH tiene un gran potencial en el tratamiento de la contaminación del agua.
Disponibilidad de datos y materiales
Los conjuntos de datos generados durante y / o analizados durante el estudio actual están disponibles del autor correspondiente a solicitud razonable.
Abreviaturas
- DDS:
-
Dodecilsulfato de aniones orgánicos
- DI:
-
Desionizado
- FESEM:
-
Microscopía electrónica de barrido por emisión de campo
- FTIR:
-
Espectroscopía infrarroja por transformada de Fourier
- HRTEM:
-
Microscopía electrónica de transmisión de alta resolución
- LDH:
-
Hidróxidos dobles en capas
- MO:
-
Naranja de metilo
- TEM:
-
Microscopía electrónica de transmisión
- XPS:
-
Espectroscopia de fotoelectrones de rayos X
- XRD:
-
Difracción de rayos X en polvo
- γ-AlO (OH):
-
Hidróxido de óxido de aluminio
Nanomateriales
- Un nuevo fotocatalizador de heterounión Bi4Ti3O12 / Ag3PO4 con rendimiento fotocatalítico mejorado
- Efecto del método de síntesis de nanopartículas de manganita La1 - xSr x MnO3 en sus propiedades
- Síntesis en un solo recipiente de nanoplacas de Cu2ZnSnSe4 y su actividad fotocatalítica impulsada por la luz visible
- Toxicidad de nanopartículas de CoFe2O4 recubiertas de PEG con efecto de tratamiento de curcumina
- Síntesis en un solo recipiente de nanopartículas de núcleo-capa de CoFe2O4 @ Ag monodispersas y su caracterización
- Síntesis controlada y propiedades de adsorción selectiva de las nanohojas de Pr2CuO4:una discusión del mecanismo
- Fabricación de heteroestructuras jerárquicas de núcleo-capa de ZnO @ NiO para un rendimiento fotocatalítico mejorado
- Síntesis sencilla en un solo recipiente de puntos de carbono de polidopamina para terapia fototérmica
- Síntesis y caracterización de zeolitas jerárquicas ZSM-5 con mesoporosidad excepcional y excelentes propiedades catalíticas
- Adsorción de tetraciclina con óxido de grafeno reducido decorado con nanopartículas de MnFe2O4
- Fabricación de hidrogeles compuestos de poli (ácido acrílico) / nitruro de boro con excelentes propiedades mecánicas y rápida autocuración a través de interacciones jerárquicamente físicas



