Síntesis en solución fácil de nanopartículas de fósforo rojo para ánodos de baterías de iones de litio
Resumen
El fósforo rojo (RP) ha atraído una gran atención como material anódico para baterías de iones de litio (LIB) debido a su alta capacidad específica teórica de 2596 mA h g - 1 y abundancia de la tierra. Sin embargo, la preparación fácil y a gran escala de los nanomateriales de fósforo rojo a través de una síntesis en solución sigue siendo un desafío. En este documento, desarrollamos un método de solución simple y fácil para preparar nanopartículas de fósforo rojo (RP NP). PCl 3 reacciona fácilmente con HSiCl 3 en presencia de aminas a temperatura ambiente para producir RP NP amorfas con tamaños de entre 100 y 200 nm con altos rendimientos. Cuando se utiliza como ánodo para una batería de iones de litio recargable, el electrodo RP NP presenta un buen rendimiento electroquímico con una capacidad reversible de 1380 mA h g - 1 después de 100 ciclos a una densidad de corriente de 100 mA g - 1 y eficiencias de Coulombic que alcanzan casi el 100% para cada ciclo. El estudio muestra que la síntesis de esta solución es un enfoque fácil y conveniente para la producción a gran escala de materiales RP NP para su uso en baterías de iones de litio de alto rendimiento.
Introducción
Se ha sabido durante mucho tiempo que los combustibles fósiles no son renovables, finitos y dañinos para el medio ambiente. Las baterías recargables de iones de litio (LIB) con alta densidad energética y ciclo de vida prolongado han despertado un gran interés en la investigación debido a su potencial como sistemas de almacenamiento de energía eficientes y baratos [1, 2, 3]. La creciente demanda de baterías de iones de litio (LIB) de bajo costo con alta densidad de energía y ciclo de vida prolongado requiere el desarrollo de nuevos materiales para electrodos [4, 5, 6, 7]. El ánodo de grafito tradicional, comúnmente utilizado en baterías de iones de litio, está limitado con respecto a sus bajas capacidades (372 mA h g - 1 ) [8, 9]. Para abordar este problema o cuestión, se han dedicado una gran cantidad de esfuerzos a explorar y desarrollar materiales de ánodos alternativos con una capacidad y eficiencias de Coulombic sustancialmente mejoradas [10,11,12,13,14,15,16,17]. Entre una amplia gama de materiales de ánodos de alta capacidad, el fósforo y sus compuestos muestran aplicaciones potenciales debido a su bajo costo, abundancia y alta capacidad específica teórica (≈ 2600 mA h g - 1 ) [18,19,20,21,22].
El fósforo tiene tres alótropos, P blanco, P negro y P rojo [23]. White P es tóxico y químicamente inestable, y no es adecuado para la aplicación en LIB. Black P tiene buena estabilidad termodinámica y conductividad, pero el complejo proceso de preparación limita sus aplicaciones a gran escala [24, 25, 26]. Entre estos tres alótropos diferentes, el rojo P es el candidato más prometedor [27] para los materiales anódicos de alta energía de próxima generación debido a su estabilidad y abundancia. Sin embargo, el rojo P está afectado por su baja conductividad electrónica (10 - 12 S m - 1 ) y un cambio drástico de volumen (300%) durante el proceso de litiación-desitiación cuando se utilizan como ánodos para LIB recargables [28, 29].
Para sortear estos impedimentos, el P rojo se ha encapsulado en diferentes tipos de materiales hospedantes de carbono [30, 31, 32, 33, 34, 35, 36] para mejorar sustancialmente el rendimiento electroquímico de los ánodos de P rojo para los LIB. Por ejemplo, Li et al. mejoró significativamente tanto el almacenamiento de litio como el rendimiento del almacenamiento de sodio del P rojo al confinar el P rojo amorfo de tamaño nanométrico en una matriz de carbono mesoporoso (P @ CMK-3) a través del proceso de vaporización-condensación-conversión [37]. Ruan y col. diseñó una nueva estrategia para incrustar partículas rojas de P en una película de carbono estructural de enlace cruzado (película P-C) para su uso como ánodo flexible libre de aglutinantes en LIB, con el fin de mejorar la conductividad electrónica y adaptarse a la expansión de volumen [38]. Sin embargo, la relación de carga de P rojo en los materiales compuestos preparados por el método de vaporización-condensación es típicamente baja, lo que es desfavorable para la aplicación práctica [39, 40]. Con este fin, el uso de nanopartículas o nanoestructuras huecas de P rojo preparadas mediante control de tamaño e ingeniería morfológica [41, 42] se han considerado estrategias efectivas para adaptarse a la gran deformación inducida por la expansión de volumen y evitar la pulverización del material. Por ejemplo, Chang et al. desarrolló una síntesis a gran escala de nanopartículas de fósforo rojo (RPNP) mediante la reducción de PI 3 en yodobenceno por etilenglicol en presencia de CTAB. Los electrodos de RPNP obtenidos exhibieron una alta capacidad específica, una larga vida útil y una excelente capacidad de velocidad como ánodos para LIB [43]. Además, Zhou et al. informó de un método solvotermal húmedo para sintetizar nanoesferas huecas de fósforo rojo con capas porosas. Los electrodos de nanoesferas de P huecos obtenidos demostraron altas capacidades y un excelente rendimiento de ciclos largos debido a los méritos de las estructuras porosas y huecas [44]. Aunque varias publicaciones han informado de los métodos para la síntesis a gran escala de fósforo rojo, sigue siendo muy deseable desarrollar un método fácil de alto rendimiento y bajo costo para preparar el fósforo rojo. En particular, la preparación del nanomaterial de fósforo rojo a través de una síntesis en solución sigue siendo un desafío.
En este documento, informamos sobre un enfoque sencillo, rápido y novedoso basado en soluciones para sintetizar RP NP, empleando la reacción a temperatura ambiente de PCl 3 con HSiCl 3 en CH 2 Cl 2 en presencia de aminas. Esta nueva solución proporciona un enfoque rentable para la producción masiva de nanopartículas de fósforo rojo para su uso en baterías de iones de litio.
Métodos
Materiales
Triclorosilano (HSiCl 3 ) se compró a TCI. n-tripropilamina (Pr 3 N) se obtuvo de Aladdin. Tricloruro de fósforo (PCl 3 ) se adquirió de Sinopharm Chemical Reagent Co. Ltd. Diclorometano (CH 2 Cl 2 ) se secó sobre CaH 2 antes de usar. Todos los demás reactivos químicos se utilizaron tal como se recibieron sin purificación adicional.
Síntesis de nanopartículas de fósforo rojo
En una preparación típica, 0,55 mL de Pr 3 N y 0,5 mL de HSiCl 3 se agregaron a 20 ml de CH 2 anhidro Cl 2 . La solución incolora formada se agitó magnéticamente durante la noche a temperatura ambiente, durante la cual el color se volvió amarillo claro. Y luego 0.5 mL de PCl 3 se agregaron a la solución. Se obtuvieron nanopartículas de fósforo rojo (RP NP) en varios segundos. Los productos se centrifugaron, separaron y lavaron con CH 2 anhidro. Cl 2 , HF 1 M y agua destilada para eliminar el PCl 3 sin reaccionar y sílice.
Mediciones electroquímicas
Las propiedades electroquímicas de las nanopartículas de fósforo rojo como materiales de ánodo en LIB se estudiaron utilizando un conjunto de celda de moneda 2032 con láminas de metal de litio que sirvieron como contraelectrodos. Las celdas CR2032 se ensamblaron en una caja de guantes llena de argón (tanto H 2 O y O 2 <0,1 ppm). El electrodo de trabajo se preparó mezclando material activo (RP NPs), grafito conductor y carboximetilcelulosa de sodio (CMC) en una proporción en peso de 5:3:2 en agua desionizada para formar una suspensión homogénea, que luego se depositó con la cuchilla en un Lámina de Cu. Después de secar a 80 ° C durante 12 h al vacío, la hoja se cortó en discos de 14 mm de diámetro. La carga de masa total de materiales activos en el electrodo fue de ~ 0,5 mg cm - 2 . El electrolito era LiPF 6 1,0 M en una mezcla de 1:1 ( v / v ) carbonato de etileno / carbonato de dietilo (Shenzhen Kejingstar Technology Ltd., China). Los perfiles de carga-descarga de las medias celdas se registraron utilizando un dispositivo de prueba de batería Neware (Shenzhen, China) en un modo de corriente constante.
Caracterización
La difracción de rayos X en polvo (PXRD) se llevó a cabo en un difractómetro de rayos X Bruker D8 con radiación de Cu Kα (λ =1,5418 Å). Se obtuvieron imágenes de microscopía electrónica de barrido (SEM) y espectros de espectroscopia de dispersión de energía (EDS) (obleas de silicio como sustrato) en un microscopio electrónico de barrido de emisión de campo Hitachi (S-4800). La microscopía electrónica de transmisión (TEM) y la TEM de alta resolución (HR) se realizaron con un equipo JEM-2100 (Japón). N 2 Las isotermas de adsorción se recogieron a 77 K (analizador Micromeritics ASAP 2020) después de desgasificar al vacío la muestra a 100 ° C durante 10 h. Se utilizó espectroscopía Raman (LabRAM Aramis, Horiba, equipada con láser de 633 nm) para investigar la estructura de RP NP. Las mediciones de espectroscopía de fotoelectrones de rayos X (XPS) se registraron con una PHI 5000 VersaProbe. Los análisis termogravimétricos (TG) se realizaron en un analizador térmico STA449F3 (Netzche) simultáneo con N 2 que fluye . Las curvas I-V de RP NP se midieron utilizando el instrumento Biologic VMP3 de la estación de sonda criogénica (CRX-4K, Lake Shore, EE. UU.). Las pruebas de voltametría cíclica (CV) se realizaron en una estación electroquímica CHI650d (Shanghai Chenhua Instruments Inc., China).
Resultados y discusión
Síntesis y caracterización de RPNP
Las nanopartículas de fósforo rojo (denominadas RP NP) se sintetizaron mediante un método de solución fácil, que se muestra en el Esquema 1. Encontramos que el tricloruro de fósforo (PCl 3 ) reaccionó fácilmente con HSiCl 3 premezclado y tripropilamina (Pr 3 N) en CH 2 Cl 2 a temperatura ambiente para producir polvos de naranja en varios segundos. El color de la solución cambió a naranja muy rápidamente al mezclar una solución de HSiCl 3 –Pr 3 N – CH 2 Cl 2 con PCl 3 , lo que indica la formación de RP NP (archivo adicional 1:Figura S1). Postulamos que PCl 3 se redujeron mediante cloruros de oligosilano subvalentes para formar las nanopartículas de fósforo. Los cloruros de oligosilano se formaron mediante la reacción de HSiCl 3 con tripropilamina (Pr 3 N) en CH 2 Cl 2 como resultado de la reacción de desproporción de HSiCl 3 en presencia de catalizadores de amina [45,46,47]. Se observa que los intermedios de oligosilano preformados eran esenciales para que ocurriera la reacción. Sin aminas (Pr 3 N), la reacción de HSiCl 3 con PCl 3 no pudo tener lugar a temperatura ambiente. Del mismo modo, el Pr 3 N no pudo reaccionar con PCl 3 para producir RP NP a temperatura ambiente. El rendimiento de RP NP, basado en la cantidad de átomos de P en PCl 3 , fue aproximadamente del 38%, que es mucho más alto que la literatura publicada [43]. Además, este enfoque de fase de solución utiliza PCl 3 de costo relativamente bajo en lugar de PI 3 en yodobenceno, que podría ampliarse de manera más económica y fácil para obtener grandes cantidades de RP NP. El color de los RPNP era naranja claro, a diferencia del color rojo intenso del RP comercial (Archivo adicional 1:Figura S2).
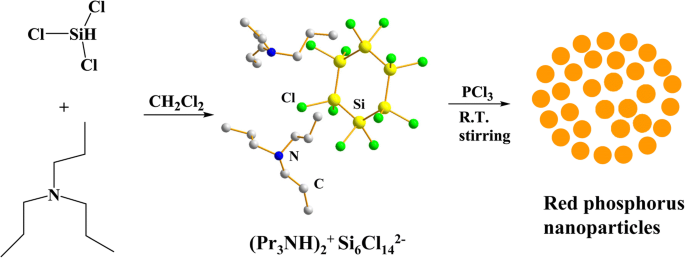
Ilustración esquemática del proceso de síntesis de RP NP
El análisis PXRD mostró que el producto era fósforo rojo. Como se muestra en la Fig. 1a, los tres picos de difracción ensanchados a 13-16 °, 25-38 ° y 47-65 °, de acuerdo con el patrón XRD de RP comercial informado en la literatura [21, 36]. Las imágenes SEM muestran que la mayoría de los NP de RP sintetizados exhibieron una forma esférica irregular con tamaños de entre 100 y 200 nm de diámetro. El patrón SAED correspondiente de RP NP (imagen insertada de la Fig. 2b) reveló que RP NP eran estructura amorfa. Los espectros Raman de RP NP presentaron tres picos fruncidos entre 300 y 500 cm - 1 , que es consistente con el espectro Raman de RP comercial informado en la literatura [36]. Los tres picos se pueden asignar bien a los modos de flexión de enlace (modo fundamental B1), vibraciones de flexión de enlace (movimiento de estiramiento simétrico A1) y vibraciones de estiramiento (modo degenerado E1) del rojo amorfo P (Fig. 1b). El análisis termogravimétrico (TGA) de los RPNP en la Fig. 3a muestra una fuerte pérdida de peso entre 380 y 430 ° C bajo una atmósfera de nitrógeno debido a la sublimación, mientras que la RP comercial muestra una fuerte pérdida de peso entre 450 y 500 ° C. La depresión observada de la temperatura de sublimación de RP NP puede resultar de altas relaciones de superficie a volumen de nanopartículas [43, 48]. Para obtener cuantitativamente la información de la superficie, N 2 Se llevaron a cabo medidas de sorción (Fig. 3b). Los resultados revelaron que el área de superficie Brunauer-Emmett-Teller (BET) de RP NP era de aproximadamente 37 m 2 g - 1 , que es mucho más grande que el del RP comercial.
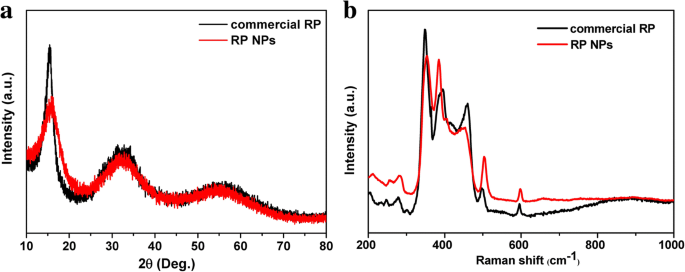
Caracterización de RPNP. un Patrones XRD de RPNP y RP comercial. b Espectros Raman de RPNP y RP comercial

Morfología de NP RP. un Imágenes SEM de RP NP. b Imágenes TEM de RP NP. La imagen insertada es el patrón SAED
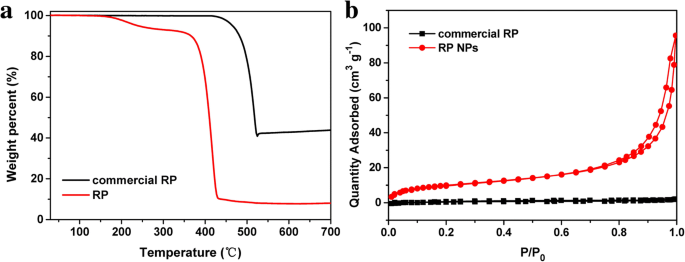
un TGA de RP NP y RP comercial. b N 2 isotermas de adsorción de RP NP y RP comercial
Para caracterizar aún más las estructuras, composiciones y estados químicos de los RP NP preparados, se llevaron a cabo mediciones de espectroscopía de rayos X de dispersión de energía (EDS) y espectroscopía de fotoelectrones de rayos X (XPS) (Fig. 4). Los espectros de EDS muestran que los RP NP están compuestos casi por completo de fósforo elemental. El espectro de levantamiento XPS (Fig. 4b) confirma además que P es el elemento dominante. El pico principal en el espectro P 2p de XPS podría descomponerse en dos picos a 129,74 y 130,74 eV, que corresponden al 2p 3/2 y 2p 1/2 de P en el enlace P – P, respectivamente, de acuerdo con la literatura anterior [49, 50]. Además, se podría asignar un pico débil a 133,50 eV al enlace P – O que posiblemente se formó a través de la oxidación de la superficie durante la exposición al aire. Por lo tanto, los resultados anteriores indican que las nanopartículas preparadas son P roja amorfa. Además, se han medido las curvas de corriente-voltaje (I-V) de RP NP, como se muestra en el archivo adicional 1:Figura S3. La conductividad de los RPNP es de aproximadamente 1,7 × 10 - 7 S m - 1 (0–2 V), que es 10 5 veces más alto que el RP comercial (10 - 12 S m - 1 ).
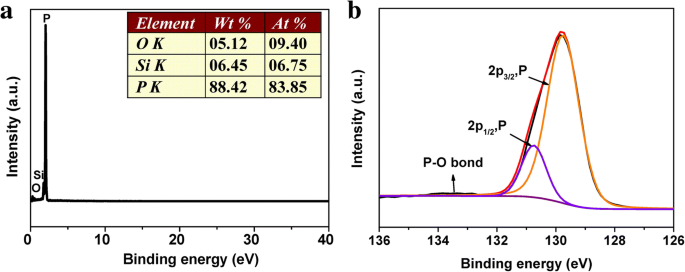
un Espectros EDS de RP NP. b Espectro P 2p XPS de RP NP
El rendimiento electroquímico de los RP NP como materiales de ánodo en LIB se probó en pilas de botón CR2032 utilizando una lámina de metal de litio como contraelectrodo dentro de los voltajes de funcionamiento de 0,01 a 2,5 V. La figura 5a muestra las curvas CV típicas de los RP NP en un escaneo velocidad de 0,1 mV s - 1 . Hay un pico amplio en el primer ciclo de litiación, que se atribuye al proceso de activación de la inserción de iones de Li en el fósforo. Un par de picos redox ubicados a 0.5–0.75 V y 1.0–1.25 V se atribuyen a la litiación de P y la des-litiación de las aleaciones P – Li [32, 51, 52] respectivamente. La desviación entre la primera y la siguiente curva catódica implica una pérdida de capacidad irreversible, que podría atribuirse a la formación de la interfaz de electrolitos sólidos (SEI), así como a la aparición de reacciones secundarias en las superficies de los electrodos, como reacciones secundarias de defecto. sitios, oxígeno de la superficie e impurezas del agua [36, 37, 53], un comportamiento comúnmente observado para los ánodos LIB. La figura 5b muestra los perfiles típicos de voltaje de descarga-carga del electrodo RP NP durante los primeros 3 ciclos a una densidad de corriente de 0,1 A g - 1 . Las aparentes mesetas de voltaje de carga y descarga cortas en alrededor de 0,7 V y 1,1 V se deben a la litiación y deslitiación de los componentes de RP NP, respectivamente, que concuerdan bien con los resultados de CV. El electrodo entregó una descarga específica y capacidades de carga de 2818 y 1641 mA h g - 1 , respectivamente, para el primer ciclo, dando una primera eficiencia Coulombic del 58,2%. La capacidad de carga disminuida podría atribuirse a la formación irreversible de la membrana SEI. Se observa que la eficiencia Coulombic de los RP NP aumentó rápidamente al 100% después del segundo ciclo. Los RP NP exhibieron un evidente deterioro de la capacidad en los primeros 3 ciclos. La capacidad irreversible en los primeros pasos de descarga-carga resultó de la descomposición del electrolito, lo que provocó la formación de SEI en la superficie del electrodo y el consumo de Li-ion. Además, las nanopartículas poseen una gran superficie en contacto con la solución de electrolito, lo que daría lugar a más reacciones secundarias, reduciendo la eficiencia Coulombic inicial en el primer ciclo [54].
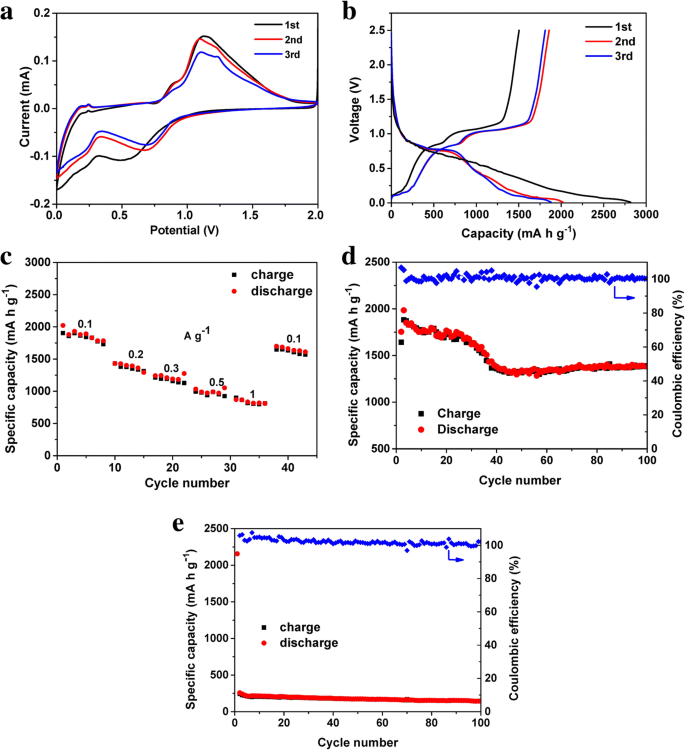
Rendimiento electroquímico de los RPNP. un Curvas CV de los RPNP. b Perfiles de tensión de los RPNP. c Tasa de rendimiento de los RPNP ciclados a diferentes densidades de corriente. d Rendimiento cíclico de los RPNP a una velocidad de 0,1 A g - 1 . e Rendimiento cíclico de RP comercial a una velocidad de 0,1 A g - 1
La velocidad típica y el rendimiento de estabilidad cíclica a largo plazo del electrodo RP NP se muestran en las Fig. 5c, d, respectivamente. Los RPNP entregaron las capacidades de carga específicas de 1801, 1430, 1245, 1227, 1184 y 871 mA h g - 1 a tasas de 0,1, 0,2, 0,3, 0,5 y 1 A g - 1 , respectivamente. El electrodo mostró una buena reversibilidad de la velocidad, con la capacidad de descarga específica recuperada al valor inicial cuando la densidad de corriente volvió a 0,1 A g - 1 después de pedalear a altas densidades de corriente. Los RP NP finalmente mantuvieron una alta capacidad de descarga reversible de 1380 mA h g - 1 , es decir, la retención del 89,1%, después de 100 ciclos con eficiencias de Coulombic cercanas al 100% en todas las mediciones. En comparación con los RP comerciales (Fig. 5e), los RP NP mostraron una estabilidad cíclica a largo plazo mucho mejor.
Conclusiones
En resumen, desarrollamos un nuevo enfoque de fase de solución fácil para la síntesis de nanopartículas de fósforo rojo a través de la reacción de PCl 3 y HSiCl 3 en presencia de aminas en el medio ambiente. Los RP NP exhibieron un rendimiento electroquímico mucho mejor con alta capacidad reversible y estabilidad cíclica a largo plazo que los RP comerciales cuando se utilizaron como ánodos para baterías de iones de litio recargables. Los electrodos RP NP mantuvieron una alta capacidad de descarga reversible de 1380 mA h g - 1 (retención del 89,1%) después de 100 ciclos, con una eficiencia Coulombic cercana al 100% para cada ciclo. Este sencillo método de preparación allana el camino para la producción rentable de RP NP como ánodos de alto rendimiento para la industria de baterías de iones de litio.
Abreviaturas
- CH 2 Cl 2 :
-
Diclorometano
- CV:
-
Voltamperometría cíclica
- EDS:
-
Espectroscopía de energía dispersiva
- HSiCl 3 :
-
Triclorosilano
- PCl 3 :
-
Tricloruro de fósforo
- Pr 3 N:
-
n-tripropilamina
- PXRD:
-
Difracción de rayos X en polvo
- RP NP:
-
Nanopartículas de fósforo rojo
- SEM:
-
Microscopía electrónica de barrido
- TEM:
-
Microscopía electrónica de transmisión
- TG:
-
Termogravimétrico
- XPS:
-
Espectroscopia de fotoelectrones de rayos X
Nanomateriales
- Nanocristales de estaño para futuras baterías
- Nano y ánodo de batería:una revisión
- Síntesis fácil y propiedades ópticas de nanocristales y nanovarillas de selenio pequeños
- Síntesis fácil de nanopartículas de SiO2 @ C ancladas en MWNT como materiales de ánodo de alto rendimiento para baterías de iones de litio
- Membranas compuestas que contienen nanopartículas de intercambiadores de iones inorgánicos para la desalación electrodialítica de glicerol
- Síntesis fácil de compuesto de CuSCN coloreado y conductor recubierto con nanopartículas de CuS
- Crecimiento directo de estructuras de ZnO similares a plumas mediante una técnica de solución fácil para la aplicación de fotodetección
- Nanopartículas de sílice para la administración intracelular de proteínas:un nuevo enfoque de síntesis que utiliza proteína verde fluorescente
- Método de postratamiento para la síntesis de nanopartículas de FePt-Fe3O4 binarias monodispersas
- Síntesis sencilla de nanocompuestos magnéticos funcionalizados en superficie para una adsorción selectiva eficaz de colorantes catiónicos
- Una solución inmersiva para baterías de vehículos eléctricos térmicamente más seguras



