Estudio de fotoluminiscencia de la influencia del hidróxido de amonio aditivo en nanocables de ZnO cultivados hidrotermalmente
Resumen
Reportamos la influencia del hidróxido de amonio (NH 4 OH), como aditivo de crecimiento, sobre nanomaterial de óxido de zinc a través de la respuesta óptica obtenida por fotoluminiscencia (PL). Se emplea un proceso hidrotermal de baja temperatura para el crecimiento de nanocables de ZnO (NW) en una superficie de Au sin semillas. Se demuestra un cambio de más de dos órdenes de magnitud en la densidad de ZnO NW mediante la adición cuidadosa de NH 4 OH en la solución de crecimiento. Además, mostramos mediante un estudio experimental sistemático y datos de caracterización PL que la adición de NH 4 El OH puede degradar la respuesta óptica de los ZnO NW producidos. El aumento de la basicidad de la solución de crecimiento con la adición de NH 4 El OH puede degradar lentamente la respuesta óptica de los NW grabando lentamente sus superficies, aumentando los defectos puntuales en los NW de ZnO. El presente estudio demuestra la importancia de los nutrientes de crecimiento para obtener ZnO NW ajustables de densidad controlada de calidad en sustratos conductores sin semillas.
Antecedentes
Los avances significativos en la síntesis de nanomateriales funcionales a través de enfoques ascendentes ahora ofrecen materiales de alta calidad para el desarrollo de dispositivos electrónicos eficientes de próxima generación [1, 2, 3, 4, 5]. El campo de investigación de ZnO ha mostrado un resurgimiento en el interés después de la demostración exitosa del crecimiento de nanoestructuras monocristalinas (nanocinturón) [6]. A partir de entonces, el uso de nanoestructuras de ZnO semiconductoras monocristalinas de alta calidad para el ensamblaje de componentes electrónicos de alto rendimiento continúa atrayendo un enorme interés de investigación en el campo de las pantallas [7, 8], los circuitos lógicos [9, 10], los sensores [ 11, 12] y optoelectrónica [13]. La renovación del interés en el material de ZnO ha sido impulsada en gran medida por su biocompatibilidad, fácil fabricación de nanoestructuras y gran familia de nanomorfologías alcanzables [14, 15]. Entre las distintas nanoarquitecturas de ZnO, los nanocables (NW) y las nanovarillas (NR) de ZnO unidimensionales (1D) se han investigado exhaustivamente como material semiconductor activo en dispositivos a nanoescala como los transistores de efecto de campo (FET) [16], los nanogeneradores ( NG) [17], o sensores [12].
Idealmente, un ZnO bien estequiométrico es un aislante. Sin embargo, en su forma no estequiométrica, puede comportarse como semiconductor o conductor dependiendo del número de defectos puntuales nativos creados y / o de la cantidad de dopante introducido. Se ha demostrado que, en el ZnO nanoestructurado, los defectos juegan un papel central en la definición de las prestaciones de los dispositivos electrónicos, como en el caso de los sensores [18] y / o nanogeneradores [17, 19], controlando la densidad de carga libre, el tiempo de vida de los portadores minoritarios y eficiencia de luminiscencia. Por ejemplo [18], se ha demostrado que se pueden obtener sensores UV de alta sensibilidad aumentando el número de defectos superficiales en ZnO NW. Estos defectos superficiales pueden actuar como centros de captura de electrones libres y dar como resultado la formación de una capa de agotamiento superficial. Cuanto mayor sea la profundidad de la región de agotamiento en la superficie NO, mayor será la sensibilidad a los rayos UV. Por otro lado, un número demasiado grande de defectos tiene efectos perjudiciales en el rendimiento del dispositivo NG [17, 19]. Por lo tanto, un control perfecto sobre la calidad del nanomaterial de ZnO producido es esencial para construir un dispositivo electrónico de alto rendimiento.
Diferentes técnicas de crecimiento de abajo hacia arriba, incluido el método de transporte de llama [20,21,22,23], vapor-líquido-sólido (VLS) [24], deposición electroquímica [25] y deposición hidrotermal y / o en baño químico [16, 26,27,28,29] se han utilizado para la síntesis de NW de 1D ZnO. Sin embargo, la mayoría de las técnicas están limitadas por su proceso de alta temperatura que no se puede ampliar en un área grande del dispositivo a un costo muy bajo, en sustratos de plástico, por ejemplo. La necesidad de una síntesis fácil, escalable industrialmente e independiente del sustrato de ZnO NWs ha visto avances significativos hacia el proceso de crecimiento hidrotermal [16, 17]. El crecimiento hidrotermal (HTG) es un proceso a baja temperatura en el que se puede producir material 1D monocristalino sobre diversos sustratos, incluidos plásticos o incluso fibras textiles [30]. En general, los NW de ZnO cultivados con HTG muestran un pico de banda de nivel de defecto intenso en los espectros de fotoemisión que se expande desde la emisión de longitud de onda de color azul a rojo dependiendo del tipo de defectos en el nanomaterial [31]. En la literatura, muchos defectos puntuales diferentes, como las vacantes de oxígeno y zinc (V O y V Zn ) e intersticial (O i y Zn i ), antisites (O Zn y Zn O ), y se identificó que las impurezas de hidrógeno son la causa de la banda de emisión del nivel de defecto en la fotoluminiscencia (PL) [32]. La banda PL visible consta de tres componentes gaussianos a 2.52, 2.23 y 2.03 eV, respectivamente etiquetados como azul I B , verde I G y naranja I O emisión máxima [33]. Sin embargo, incluso después de años de investigaciones, el origen de estos estados defectuosos sigue siendo objeto de debate. No obstante, independientemente de la causa de los defectos en ZnO, la relación entre la transición de banda a banda (emisión UV) y la intensidad máxima relacionada con el defecto en el espectro PL predice la respuesta óptica del nanomaterial producido [18, 34].
El proceso de crecimiento con una integración in situ de ZnO NW sobre un electrodo metálico sin ninguna capa de semilla de ZnO puede mejorar el proceso de transporte de carga a través de la interfaz de contacto metal-semiconductor (MS) y, en consecuencia, puede mejorar el rendimiento del dispositivo [35]. Hidróxido de amonio (NH 4 OH) se ha empleado a menudo para el crecimiento de ZnO NW en superficies metálicas de Au [35, 36]. Por ejemplo, en nuestro trabajo anterior, mostramos que NH 4 El OH se puede utilizar para el ajuste simultáneo de la densidad de NW y las propiedades eléctricas de los NW de ZnO cultivados en una superficie de Au sin semillas [5]. Sin embargo, informe que detalla el efecto de la adición de NH 4 El OH sobre la respuesta óptica del nanomaterial de ZnO producido en la superficie de Au rara vez se encuentra en la literatura. En el presente informe, estudiamos la respuesta óptica del material ZnO analizando la emisión relacionada con defectos y la emisión UV en el espectro PL de NW cultivados en diferentes NH 4 Concentraciones de OH. Dos picos dominantes, notados en el gráfico PL, están centrados en 3,24 eV (382 nm) y 2,23 eV (556 nm), respectivamente, denominados emisión ultravioleta (UV) (I UV ) y emisión de nivel de defecto verde (I G ) picos. La proporción extraída I UV / I G proporciona un índice cualitativo de la cantidad del defecto radiativo en el nanomaterial producido. El efecto de NH 4 La OH se confirma además mediante la realización de otra serie de experimentos y caracterizaciones de PL. En esta segunda serie de experimentos, hemos cultivado ZnO NW sin NH 4 OH y, a continuación, se realizó un tratamiento de poscrecimiento de NW en solución de amoniaco con diferente pH. Descubrimos una tendencia similar de disminución en la relación I UV / I G para ambas series de muestras, es decir, las cultivadas en diferentes NH 4 Concentración de OH y los demás postcrecimiento tratados en NH 4 OH.
Métodos
Los NW de ZnO se cultivan mediante un proceso de crecimiento hidrotermal en obleas de Si orientadas (100). Una muestra de 2 × 2 cm 2 El silicio rígido se limpia primero en una solución de piraña (1:1 H 2 SO 4 y H 2 O 2 ) durante 10 min seguido de una inmersión de 2 min en ácido fluorhídrico (50%) para eliminar el óxido fino formado durante la limpieza de pirañas y, finalmente, enjuague con agua desionizada (DI). A este paso de limpieza le sigue el secado con gas nitrógeno y se realiza un último paso de horneado a ~ 200 ° C para eliminar cualquier humedad adsorbida antes de la deposición del metal. A continuación, se deposita una capa de oro (~ 200 nm de espesor) mediante la técnica de pulverización catódica de corriente continua a temperatura ambiente. Para mejorar la adherencia entre el oro y el silicio, depositamos una capa de titanio (~ 100 nm) utilizando la misma técnica. El precursor de reactivo para HTG consiste en una proporción 1:1 de nitrato de zinc hexahidrato (Zn (NO 3 ) 2 ‚6H 2 O, 98% Sigma Aldrich) y hexametilentetramina (HMTA, Sigma Aldrich). Durante el crecimiento, los sustratos se sumergieron boca abajo en una copa de teflón, se sellaron dentro del reactor autoclave de acero inoxidable y se colocaron en un horno de convección precalentado a 85 ° C durante 15 h. El autoclave se saca del horno y se enfría de forma natural. Luego, los sustratos se enjuagan a fondo con agua desionizada y se secan en N 2 flujo de gas. En los experimentos, la concentración de NH 4 El OH varía de 0 a 50 mM. Se utiliza un sistema de microscopio electrónico de barrido (SEM) Hitachi S-4150 para la caracterización morfológica de los ZnO NW. Seguir la respuesta óptica de los NW obtenidos con diferentes NH 4 Se realizaron concentraciones de OH, mediciones de fotoluminiscencia (PL); A temperatura ambiente (RT), bombeando a 1,5 mW, la línea de 325 nm de un láser de He-Cd atravesó un modulador acústico-óptico a una frecuencia de 55 Hz. Se pueden encontrar más detalles experimentales para las mediciones de PL en la Ref [33].
Resultados y discusiones
Para ejecutar el presente estudio, se cultivan ZnO NW mediante el proceso HTG con diferentes NH 4 Concentración de OH a 85 ° C. Los parámetros del proceso de crecimiento se mencionan en la Tabla 1, y se pueden encontrar más detalles de crecimiento en la Ref. Boubenia y col. [5]. Los resultados de crecimiento obtenidos al variar NH 4 Las concentraciones de OH (de 0 a 50 mM por paso de 10 mM) en la solución de crecimiento se presentan en la Fig. 1a-f; que muestra imágenes típicas de SEM de sección transversal y vista superior adquiridas de las muestras de ZnO NW. Se obtiene un cambio de más de dos órdenes de magnitud en la densidad NW mediante la adición cuidadosa de NH 4 OH en la solución de crecimiento. El mecanismo detrás de la variación de densidad NW con NH 4 La adición de OH se puede encontrar en Boubenia et al. [5], donde los autores plantearon la hipótesis de que la cantidad de hidróxido de amonio tiene un efecto directo sobre la concentración de complejos de Zn (II) que afecta en gran medida la solubilidad del Zn en la solución. En consecuencia, se puede controlar la sobresaturación de la solución de crecimiento y, por tanto, el número de núcleos sobre el sustrato. Además, de acuerdo con la densidad, la relación de aspecto (AR) de las nanoestructuras determina / condiciona en gran medida su aplicación en la electrónica flexible donde se necesitan altas relaciones de superficie a volumen para una mayor absorción de la tensión. Además, el número de estados de defectos superficiales es directamente proporcional al AR de los NW, lo que tiene un impacto directo sobre la respuesta óptica del nanomaterial. Por lo tanto, la variación en la AR de NW, con el aumento de NH 4 La concentración de OH también se calcula utilizando imágenes SEM. La Figura 1g muestra un gráfico que muestra la tendencia de variación de densidad y AR con la adición de NH 4 OH en la solución de crecimiento. Puede verse, usando la Fig. 1g, que, como NH 4 La concentración de OH aumenta, tanto la densidad de NW como la AR aumentan hasta que los valores se saturan a una concentración de hidróxido de amonio de 40 mM. Mediciones de espectroscopía Raman a temperatura ambiente, realizadas en ZnO NW cultivados con diferentes NH 4 Concentraciones de OH, confirman la estructura cristalina de wurtzita del nanomaterial producido (Archivo adicional 1:Figura S1) [5].
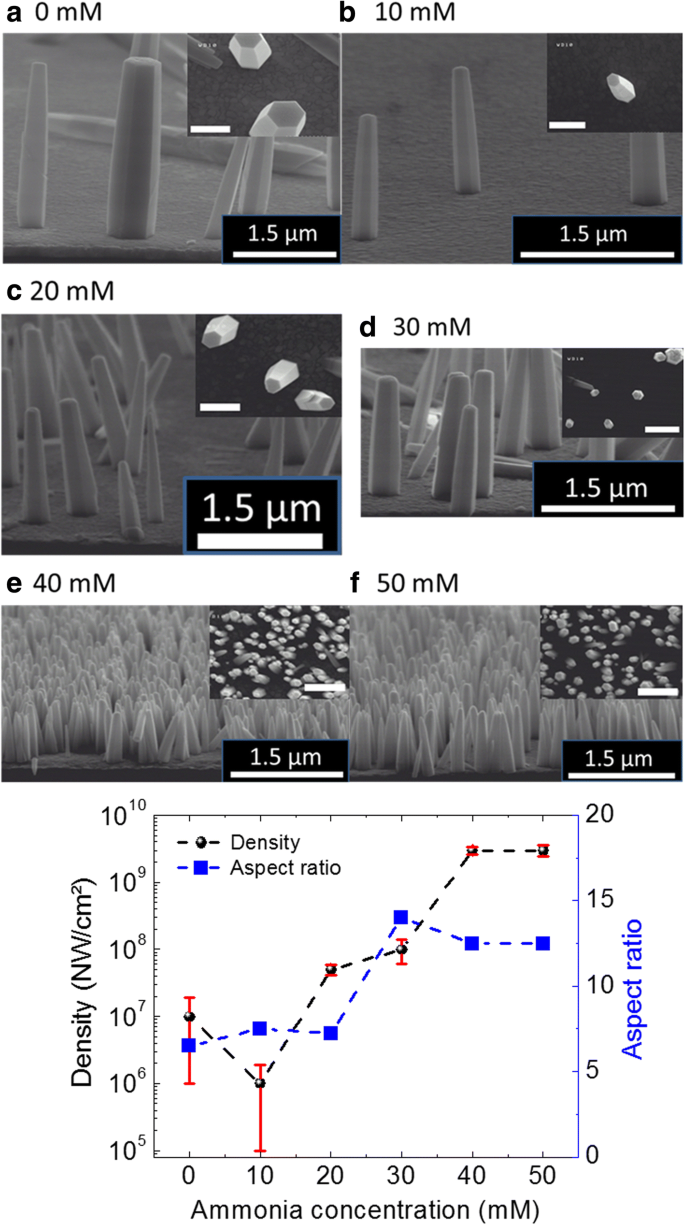
Imágenes SEM de NW cultivados para diferentes concentraciones de amoníaco. un 0 mM, b 10 mM, c 20 mM, d 30 mM, e 40 mM y f 50 mM. El recuadro de cada panel ( a - e ) muestra la imagen SEM de vista superior obtenida de la misma muestra. La barra de escala en el recuadro es 500 nm. g La variación de la densidad y la relación de aspecto de NW con el cambio en NH 4 Concentración de OH
La Figura 2a muestra los espectros PL medidos a TA para NW cultivados con diversas concentraciones de hidróxido de amonio. El espectro PL de ZnO NW presenta dos bandas de emisión:una emisión de luz cerca del borde de la banda (NBE) y una emisión amplia de nivel profundo (visible). La energía de excitación utilizada en el presente estudio es de 3,81 eV, lo que garantiza una población de portadores del mínimo de la banda de conducción. El pico de emisión de UV fuerte y estrecho, centrado en 3,24 eV para todos los casos, resulta de la fusión de las diversas emisiones relacionadas con excitones cerca del borde de la banda, incluida la recombinación de excitones libres y sus réplicas longitudinales ópticas (LO) -phonon, [37] transiciones de aceptor libres a neutrales, [38] y recombinación del par donante-aceptor [39], dependiendo de la configuración de la red local y la presencia de defectos [40,41,42]. En la Fig. 2a, también podemos observar un nivel de emisión visible amplio que se expande desde la longitud de onda de color verde a naranja. La presencia de un pico de emisión visible amplio puede explicarse con la hipótesis de la existencia de múltiples defectos y / o complejos de defectos que están predominantemente presentes en la superficie de las nanoestructuras de ZnO [34, 43]. Sin embargo, a pesar de varios informes sobre la presencia de emisión visible en el espectro PL de ZnO, no existe un consenso claro en la literatura sobre las posiciones de los picos en la región visible o sobre su origen. También hay que tener en cuenta que, debido a la gran variación en la densidad y la relación de aspecto de una muestra a otra (Fig. 1g), es difícil sondear la misma cantidad de material para muestras tan diferentes. Por lo tanto, no podemos comparar directamente la intensidad de emisión de estas muestras. Sin embargo, la relación de la magnitud de la intensidad máxima de emisión de UV con respecto a la intensidad máxima relacionada con el defecto, en el espectro PL, predice la respuesta óptica del nanomaterial producido. Todos los espectros visibles pueden ajustarse con éxito mediante tres estados de luminiscencia visible relacionados con defectos, a saber, azul, verde y naranja. Por ejemplo, la Fig. 2b traza el ajuste gaussiano de NH 4 40 mM Muestra de OH para los estados azul, verde y naranja, que se colorean en consecuencia para enfatizar sus diferencias relativas. Cabe señalar aquí, aunque la intensidad de PL para los picos de emisión tanto UV como visible varía debido a la diferencia en la masa producida para la variación de NH 4 OH en solución, la contribución porcentual para los estados azul, verde y naranja sigue siendo la misma. En la Fig. 2b, se presenta la contribución porcentual de cada estado de defecto, para la muestra de 40 mM, mostrando que la contribución principal de la emisión visible está relacionada con el estado de defecto verde. Por lo tanto, para hacer un seguimiento de la respuesta óptica de los nanomateriales producidos, es justo comparar la relación de intensidad de la emisión UV (I UV ) al estado de defecto verde (I G ), que parece tener la contribución porcentual más alta en los espectros visibles.
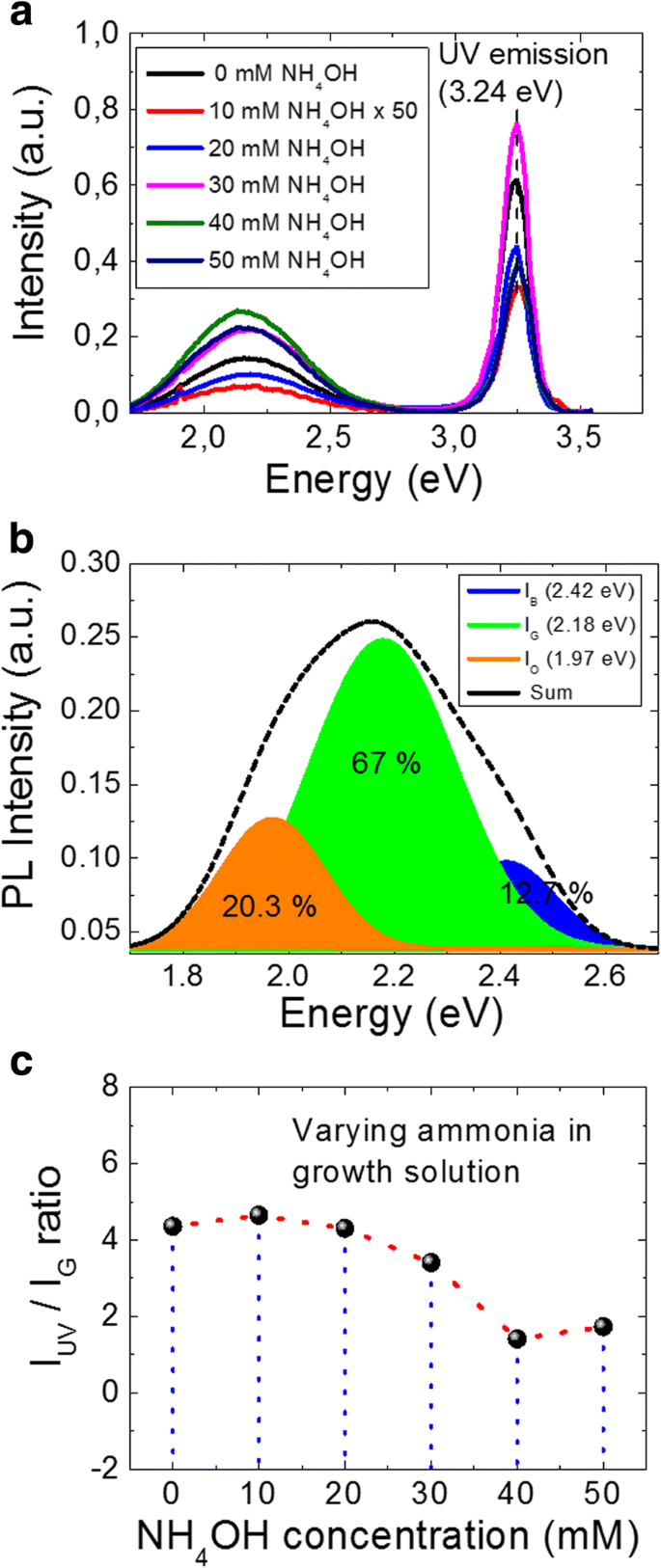
Los resultados de las mediciones de PL. un Los espectros PL de los ZnO NW cultivados bajo diferentes concentraciones de hidróxido de amonio. b Ajuste gaussiano deconvolucionado para la muestra de 40 mM a los estados de emisión azul, verde y naranja y sus contribuciones porcentuales en la emisión visible. c La relación de intensidad del pico de emisión verde y UV en función de NH 4 Concentración de OH
La Figura 2c traza el I UV extraído / I G relación para cada caso de NW cultivados con diferentes concentraciones de amoníaco, mientras que la Tabla 2 presenta los valores extraídos. Puede verse, usando la Fig. 2c, que el I UV / I G la proporción disminuye suavemente después de 20 mM de NH 4 OH en la solución de crecimiento. Por ejemplo, el I UV / I G El valor para el amoníaco 40 mM es tres veces menor que el de la muestra “sin amoníaco”, lo que indica un aumento de los estados de defectos visibles con la adición de amoníaco. De manera predominante, puede haber dos posibles razones para el aumento experimental observado de los estados de defecto de nivel visible:(i) aumento de la relación de aspecto y (ii) aumento de la basicidad de la solución con la adición de hidróxido de amonio. Teniendo en cuenta el primer punto, la relación de aspecto puede afectar en gran medida la intensidad del nivel de emisión visible. Por ejemplo, Djurisic et al. realizó un análisis PL en profundidad en nanoestructuras de ZnO y concluyó que la luminiscencia verde en los espectros de ZnO PL probablemente se origina en algunos defectos no paramagnéticos o complejos de defectos y que la mayor parte proviene de defectos superficiales [34]. Puede verse en la Fig. 1g que hay un fuerte aumento de la relación de aspecto ( L / d ) por encima de 20 mM de NH 4 OH además, donde L y d son la longitud y el diámetro del NO, respectivamente. Una AR grande significa un aumento considerable de la relación superficie / volumen, lo que conduce a una mayor emisión del nivel de defectos. En la Ref. [44] que conduce a una disminución de la I UV / Yo vis proporción. Sin embargo, los autores no están convencidos de que el aumento de AR pueda ser la única razón del aumento observado en la intensidad de emisión de defectos. Además, señalaron que los resultados obtenidos pueden ser muy sensibles a las condiciones experimentales como la densidad de excitación y el área de radiación [44].
Otra posible razón para el aumento observado en los estados de defecto en los NW puede ser la adición de NH 4 OH sí mismo. Chen y col. han demostrado que se pueden inducir varios defectos en NW de ZnO cultivados hidrotermalmente (utilizando la capa de semillas de ZnO) mediante la adición de NH 3 moléculas durante la etapa de crecimiento [45]. Aunque la adición de NH 4 OH no es crucial para el crecimiento de ZnO NW utilizando la capa de semillas de ZnO, para el crecimiento sin semillas de ZnO NW en superficies de Au, la adición de NH 4 OH juega un papel clave en el control del número de sitios de nucleación en la superficie de Au. Por ejemplo, Alenezi et al. explicó la variación de densidad de ZnO NW en la superficie desnuda de Au al afirmar que sin NH 4 OH, principalmente Zn 2+ Los iones están disponibles, mientras que el uso de hidróxido de amonio son limitados, lo que reduce significativamente la velocidad de nucleación homogénea y fomenta la heterogénea. Boubenia et al. [5], donde se pueden variar más de dos órdenes de densidad NW mediante un control cuidadoso de NH 4 Concentración de OH en la solución de crecimiento. Los autores afirman además un aumento de la densidad de portadores de carga gratuita, mientras que la movilidad de efecto de campo disminuye a medida que el NH 4 La concentración de OH aumenta, lo que sugiere la creación de defectos puntuales adicionales con la adición de NH 4 OH en la solución de crecimiento. Sin embargo, no se muestran datos de PL para confirmar los resultados eléctricos informados. Los resultados de PL que se muestran en la Fig. 2 están completamente de acuerdo con los resultados eléctricos informados por Boubenia et al. [5], como se menciona en la Tabla 2, donde la densidad de carga gratuita aumenta de 4,3 × 10 16 a 2 × 10 17 cm - 3 como NH 4 La concentración de OH aumenta de 0 a 40 mM en la solución de crecimiento. Por lo tanto, podemos plantear la hipótesis de que la adición de NH 4 El OH en la solución de crecimiento crea defectos puntuales adicionales en los ZnO NW. Sin embargo, para confirmar esta hipótesis, llevamos a cabo otra serie de experimentos donde los NW de ZnO tal como crecieron, sin adición de NH 4 OH, se tratan en solución con una basicidad creciente. Los detalles de los experimentos de tratamiento posterior al crecimiento se dan en la Tabla 3.
Los resultados experimentales obtenidos para el tratamiento posterior al crecimiento de NW en solución de amoniaco se muestran en las Figs. 3 y 4. La figura 3 muestra las imágenes SEM correspondientes de las muestras tratadas en diferentes NH 4 Concentraciones de OH. Se puede ver, a partir del presente conjunto de datos, que la superficie del NW comienza a ser más rugosa con el aumento de NH 4 Concentración de OH, que incluso conduce a la formación de nano-montículos en la superficie polar de ZnO NW para muestras tratadas de 100 y 200 mM. El peor de los casos puede verse en las muestras tratadas con 100 y 200 mM de NH 4 OH, donde algunos NW parecen haberse roto desde la base y yacen horizontalmente sobre el sustrato. Al aumentar aún más la molaridad de NH 4 Solución OH, más del 90% de los NW están rotos (datos no mostrados).

Imágenes SEM adquiridas de NW de ZnO en crecimiento (prístinos) y NW tratados después del crecimiento en diferentes NH 4 Concentraciones de OH
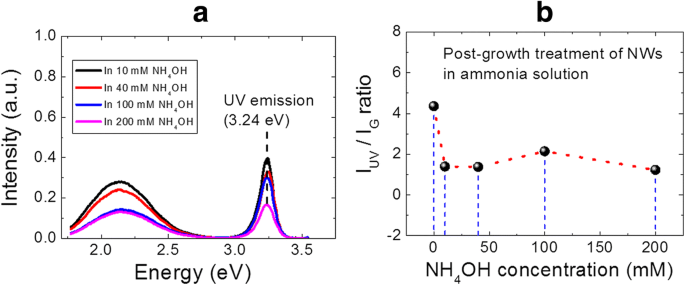
un Los espectros PL de los ZnO NW tratados en soluciones con diversas concentraciones de hidróxido de amonio. b La relación de intensidad de los picos de emisión verde y ultravioleta en función de NH 4 Concentración de OH, extraída de a
Los datos de PL resultantes que surgen de las muestras tratadas después del crecimiento se muestran en la Fig. 4. La Figura 4a muestra los espectros de PL medidos a TA para NW tratados con varias concentraciones de hidróxido de amonio, mientras que el I UV extraído / I G La gráfica se muestra en la Fig. 4b. Cabe señalar que la posición del pico para la emisión UV y visible no se ha cambiado después de NH 4 Tratamiento con OH, que indica que no se forma ningún defecto puntual adicional con diferente nivel de energía durante el NH 4 Tratamiento OH. La reducción continua en la intensidad PL del pico de emisión de UV, con el aumento de NH 4 La concentración de OH indica claramente la eliminación de nanomaterial de ZnO debido a un grabado lento de los NW en medio básico [46]. Además, es interesante notar, en la Fig. 4b, una clara y marcada disminución de la I UV / I G proporción, ya que los NW se tratan en NH 4 Solución de OH. Es importante mencionar aquí que, para el presente estudio, las condiciones experimentales como densidad de excitación, área de radiación, masa inicial de nanomaterial de ZnO, etc. son fijas. Por lo tanto, el I UV observado / I G La tendencia de la relación puede estar completamente relacionada con el efecto introducido por la adición de NH 4 OH y no a cambios en las condiciones experimentales [47]. Los resultados experimentales obtenidos apoyan claramente la hipótesis formulada en la sección anterior para la creación de defectos puntuales extra con la adición de NH 4 OH en la solución de crecimiento. Creemos que el aumento de la basicidad de la solución de crecimiento con la adición de NH 4 El OH puede degradar lentamente la respuesta óptica de los NW grabando lentamente sus superficies, lo que aumenta el nivel de defectos puntuales en los NW de ZnO.
Conclusiones
En resumen, demostramos un proceso ascendente fácil, de bajo costo y escalable para un crecimiento sin semillas de ZnO NW en superficies metálicas de Au. Con una cuidadosa adición de hidróxido de amonio en la solución de crecimiento, la densidad de ZnO NW se puede controlar en dos órdenes de magnitud. Consecuencias de la adición de NH 4 OH sobre la respuesta óptica de los NW obtenidos se estudiaron mediante la técnica de fotoluminiscencia. El espectro de emisión visible, para cada NH 4 La concentración de OH se deconvolucionó con éxito a los estados de defecto azul, verde y naranja. Además, también se presentó la contribución porcentual de cada estado de defecto, lo que muestra que la mayor contribución de la emisión visible proviene del estado de defecto verde. Por lo tanto, para hacer un seguimiento de la respuesta óptica de los nanomateriales producidos, comparamos la relación de intensidad de la emisión UV (I UV ) al estado de defecto verde (I G ). Se observó que el I UV / I G la proporción disminuye drásticamente después de la adición de 20 mM de NH 4 OH, insinuando la creación de defectos puntuales adicionales con la adición de NH 4 OH en la solución de crecimiento. Los resultados experimentales fueron bien respaldados por los datos de la literatura sobre el aumento de la densidad de carga gratuita con NH 4 OH además. Sin embargo, la hipótesis propuesta se confirmó aún más mediante la realización de otra serie de experimentos en los que los NW de ZnO recién crecidos, sin la adición de NH 4 OH, se trataron en soluciones con una basicidad creciente. Una clara y marcada disminución de la I UV / I G proporción, ya que los NW se trataron en NH 4 Solución de OH, mostró que el aumento de la basicidad de la solución de crecimiento con la adición de NH 4 El OH puede degradar lentamente la respuesta óptica de los NW grabando sus superficies, lo que aumenta el nivel de defectos puntuales en los NW de ZnO. El presente estudio es importante para controlar la respuesta óptica de ZnO NW que pueden cultivarse directamente en electrodos metálicos de Au para aplicaciones electrónicas y optoelectrónicas.
Nanomateriales
- El estudio de un nuevo sistema micelar similar a un gusano mejorado con nanopartículas
- Estudio de los primeros principios sobre la estabilidad y la imagen STM del borofeno
- Estudio in vitro de la influencia de nanopartículas de Au en las líneas celulares HT29 y SPEV
- Nanocables de silicio amorfo cultivados en película de óxido de silicio mediante recocido
- Influencia del agua en la estructura y propiedades dieléctricas de la microcristalina y nanocelulosa
- Ajuste de las morfologías de la superficie y las propiedades de las películas de ZnO mediante el diseño de la capa interfacial
- Una metodología de dos pasos para estudiar la influencia de la agregación / aglomeración de nanopartículas en el módulo de Young de nanocompuestos poliméricos
- Fabricación y caracterización de nanoclips de ZnO mediante el proceso mediado por poliol
- Influencia del sustrato en la longitud de onda y resistencia del acoplamiento LSP
- Crecimiento propio de MOCVD y fotoluminiscencia mejorada espectacularmente de nanocables de núcleo-carcasa de InGaAs / InP
- Mecanismos de formación de nanocables de InGaAs producidos por una deposición de vapor químico de dos pasos de fuente sólida



