Ruta de electrohilado de un paso de nanofibras de TiO2 de rutilo modificadas con SrTiO3 y sus propiedades fotocatalíticas
Resumen
El SrTiO 3 Rutilo modificado TiO 2 Las nanofibras compuestas se sintetizaron mediante una sencilla técnica de electrohilado. El resultado de XRD, SEM y TEM indica que el SrTiO 3 / TiO 2 La heterojucción se ha preparado con éxito. Comparado con el TiO 2 y SrTiO 3 , la actividad fotocatalítica del SrTiO 3 / TiO 2 (rutilo) para la degradación de naranja de metilo exhibe una mejora obvia bajo iluminación UV. que es casi 2 veces mayor que el TiO 2 desnudo (rutilo) nanofibras. Además, la alta cristalinidad y la separación del portador generado por fotones del SrTiO 3 / TiO 2 La heterojucción se considera la razón principal de esta mejora.
Antecedentes
Como semiconductor prototípico con propiedades fotoeléctricas elevadas y respetuosas con el medio ambiente, el óxido de titanio (TiO 2 ) es ampliamente utilizado en óptica, células solares, sensores, etc. [1, 2, 3, 4], y también se considera como un fotocatalizador más prometedor en el tratamiento de aguas residuales [5], debido a su bajo costo, alta estabilidad físico-química y no toxicidad. Como se informó en la literatura anterior, aunque la anatasa TiO 2 exhiben mejor fotocatálisis que el Rutilo TiO 2 , pero la banda prohibida de anatasa TiO 2 (3,2 eV) es más ancho que el rutilo TiO 2 (3,0 eV), que puede restringir la relación de utilización de energía luminosa en la aplicación fotocatalítica. Es más, compárelo con la anatasa TiO 2 metaestable , el rutilo TiO 2 exhiben una estabilidad físico-química más alta, lo que es beneficioso para la utilización cíclica en el tratamiento de la contaminación. Con estas ventajas únicas, cómo mejorar la eficiencia fotocatalítica del rutilo TiO 2 sería un problema importante. Como se sabe, la fotocatálisis depende principalmente del área de superficie específica o la movilidad y la vida útil de los portadores generados por fotones, por lo que se ha informado de mucho trabajo. Para una superficie específica, se han preparado montones de morfología excelente, como nanohojas [6], nanocinturones [7], nanobarras [8], nanofibras [9] y microflores [10], todas ellas con resultados inspiradores [11 , 12, 13, 14]. Por otro lado, la superficie de metal noble modificado o la preparación de heteroestructura se consideran formas útiles de ajustar la estructura de la banda para mejorar la movilidad y la vida útil de los portadores generados por fotones. Sin embargo, en comparación con el alto costo del metal noble modificado, la heteroestructura se considera una forma eficiente y de bajo costo. Se han informado muchas investigaciones relevantes, como ZnO / TiO 2 [15,16,17], CdS / ZnO [18,19,20], CeO 2 / grafeno, etc. [21]. Entre esos semiconductores, el titanato de estroncio (SrTiO 3 ) ha llamado la atención de los investigadores debido a la estabilidad térmica y la resistencia a la fotocorrosión [22], y se ha aplicado ampliamente en H 2 generación [23], eliminación de NO [24], disociación del agua [25] y descomposición del tinte por fotocatalizador [26,27,28]. En particular, dado que el fotocatalizador compuesto de heteroestructuras atrajo más atención, como Core-shell SrTiO 3 / TiO 2 y heteroestructuras SrTiO 3 / TiO 2 había mostrado una actividad fotocatalítica mucho mayor que el TiO 2 puro , que se atribuye a heteroestructuras promueven la separación de portadores fotogenerados [29, 30] . Entonces el SrTiO 3 se considera un buen candidato para acoplarse con la fase anatasa de TiO 2 para ajustar la estructura de la banda para mejorar su actividad fotocatalítica . Sin embargo, hay informes raros sobre SrTiO 3 -modificado Rutilo TiO 2 nanofibras compuestas para la degradación de los tintes contaminantes debido al engorroso proceso, entonces, cómo simplificar la preparación de SrTiO 3 / TiO 2 nano-heterounión sería un tema importante para su aplicación práctica. Como se sabe, el electroespinado es un método conveniente y eficiente para preparar nanomateriales, que podrían preparar fácilmente el precursor en nanofibras en la prelusión y luego formar una serie de nanoestructura en el recocido posterior, que se ha informado en muchas publicaciones [31,32,33 , 34,35,36].
En el presente estudio, informamos sobre una síntesis simple de un paso de SrTiO 3 Rutilo modificado TiO 2 nanoheterounión con alta fotocatálisis a través del electrohilado. Luego se ha estudiado el mecanismo de mejora fotocatalítica de la heterojucción.
Métodos
Materiales
Ácido acético de grado analítico, N, N-dimetilformamida (DMF, Aladdin, 99,5%), titanato de tetrabutilo (TBT, Aladdin, 99,0%), acetato de estroncio (Aladdin, 99,97%), polivinilpirrolidona (PVP, M W =1.300.000) se obtuvieron de Shanghai Macklin Biochemical Co. Ltd.
Preparación de SrTiO 3 / TiO 2 (rutilo) Nanofibra compuesta
SrTiO 3 / TiO 2 Las nanofibras compuestas (rutilo) se sintetizaron mediante electrohilado directo con el método de calcinaciones posteriores que se muestran en la Fig. 1. En primer lugar, la solución precursora se preparó disolviendo 2,2 g de PVP en 8 ml de DMF y 2 ml de ácido acético. Después de agitar durante 8 h, se añadieron 2 g de TBT a la solución precursora durante 4 h con un agitador magnético. Además, se añadió lentamente una cierta cantidad de acetato de estroncio a la mezcla anterior y se agitó hasta que la solución fue transparente. Los sol-geles preparados se cargaron en una jeringa de vidrio, se equiparon con una aguja de acero inoxidable de 0,5 mm de diámetro y se fijaron en una bomba de jeringa (0,6 ml / h, KDS-200, KD Scientific, Estados Unidos). Esta aguja está conectada al electrodo positivo de 15 kV (Modelo:ES40P-10 W, Gamma HighVoltage, Estados Unidos). Se mantuvo una distancia de 15 cm entre la punta de la aguja y el colector de papel de aluminio conectado a tierra. Durante el proceso de electrohilado, la humedad se mantuvo a <40% y la temperatura ambiente fue de 20 ° C. En consecuencia, se obtuvieron bandas de nanofibras no tejidas en el colector y se dejaron en un horno a 80 ° C secando durante 6 h. Las nanofibras electrohiladas se calcinaron en el aire a 700 ° C (5 ° C / min de calentamiento) durante 1 h para obtener la diferente ración de SrTiO 3 / TiO 2 (rutilo) nano-heterojucción. Es más, un simple TiO 2 nanofibras (rutilo) y SrTiO 3 se prepararon nanofibras para el contraste. La diferente ración de SrTiO 3 en SrTiO 3 / TiO 2 (rutilo) nano-heterojucción fue de 1% en peso, 3% en peso, 5% en peso y 10% en peso, y se marcó como ST-1, ST-3, ST-5, ST-10, respectivamente.
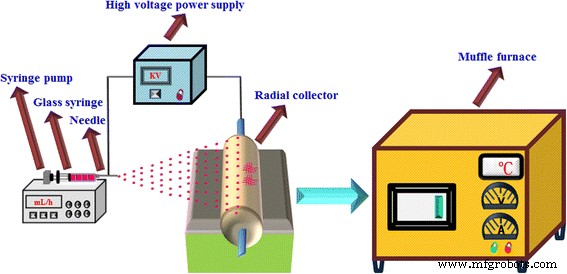
Diagrama esquemático del proceso de preparación del fotocatalizador
Caracterización
La morfología de la superficie de las muestras preparadas se investigó con el microscopio electrónico de barrido de emisión de campo (FESEM, Hitachi S-4800) equipado con espectroscopia de rayos X de dispersión de energía (EDS), y se determinó la microestructura de las muestras preparadas. observado por un microscopio electrónico de transmisión (TEM, JEM-2100, 200 kV); Las estructuras cristalinas de las muestras preparadas se caracterizaron mediante un avance de Bruker / D8 con radiación de Cu Kα (λ =1,518 Å) a una velocidad de exploración de 0,2 seg / paso en el rango de 10-80 °. El espectro de absorción de las muestras preparadas se registró utilizando un pectrofotómetro visible UV (U-3900Hitachi).
Medición de la actividad fotocatalítica
Se llenó en un reactor de cuarzo una solución de 50 ml de naranja de metilo (MO) con una concentración inicial de 15 mg / L en presencia de muestra (30 mg). La fuente de luz fue proporcionada por una lámpara de mercurio UV-C (Philips Holland, 25 W). Antes de la irradiación, la solución se mantuvo continuamente en la oscuridad durante 30 minutos para alcanzar un equilibrio de adsorción-desorción entre los sustratos orgánicos y los fotocatalizadores. A intervalos dados (t =10 min) de irradiación, se extrajeron y analizaron las muestras de la solución de reacción. Las concentraciones del tinte remanente se midieron con un espectrofotómetro a λ =464 nm.
Resultados y discusión
La Figura 2 muestra los patrones XRD de rutilo TiO 2 , SrTiO 3 y la diferente concentración de SrTiO 3 / TiO 2 (rutilo) nano-heterojucción. Es obvio que los picos de difracción en 2Ɵ =27.5, 36.1, 41.3 y 54.4 ° pueden indexarse a los planos cristalinos (110), (101), (111), (211) de rutilo TiO 2 (JCPDS78-1510). Los picos a 32,4, 40,0, 46,5 y 57,8 ° se atribuyen a los planos cristalinos (110), (111), (200) y (211) de Cubic SrTiO 3 (JCPDS 84–0443). El resultado indica que el SrTiO 3 / TiO 2 Las nanofibras compuestas (rutilo) con mayor cristalinidad se preparan con éxito bajo sinterización a 700 ° C (Fig. 2), lo que puede ser beneficioso para promover el transporte del portador generado por fotones para aumentar la fotocatálisis.
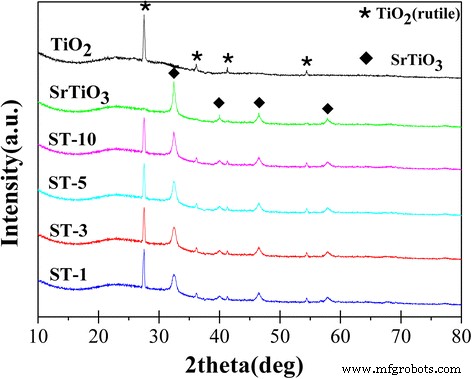
Patrones XRD del TiO desnudo 2 (Rutilo), desnudo SrTiO 3 , ST-10, ST-5, ST-3 y ST-1
La morfología de la superficie de la ST-3 recién hilada medida por FESEM se muestra en la Fig. 3 (a) - (d). La nanofibra compuesta preliminar ST-3 sin sinterizar se ilustró en la Fig. 3 (a). Como se muestra, la superficie de las nanofibras obtenidas con un diámetro de aproximadamente 300 nm es lisa y continua. Dado que el TBT podría hidrolizarse rápidamente por la humedad del aire, las redes continuas de TiO 2 Se formaron soles en las nanofibras una vez que se expulsaron de la punta de la aguja [37]. Como se presenta en la Fig. 3 (b), después de sinterizar a 700 ° C, el diámetro de las nanofibras disminuyó a aproximadamente 200 nm y las fibras siguen siendo continuas. Es interesante que la fibra después de la sinterización, las nanofibras se volvieron delgadas y rugosas, lo que podría generar un área de superficie mucho más específica para aumentar la fotocatálisis.

Imagen FESEM de ST-3. un ST-3 preparado, recuadro :SEM de gran aumento (sin sinterizar), ( b ) - ( d ) ST-3 (sinterizado)
Las imágenes TEM proporcionaron más información sobre la estructura cristalina de las nanofibras compuestas ST-3. La Figura 4a muestra una imagen TEM típica para ST-3, que se corresponde con el SEM. Se empleó HRTEM para iluminar aún más las estructuras cristalinas de las nanofibras compuestas de rutilo ST-3. Como se muestra en la Fig. 4b, la imagen HRTEM de gran aumento que revela claramente indica dos celosías distintivas de 0.324 nm y 0.275 nm respectivamente, que corresponden al plano (110) del rutilo TiO 2 y el plano (110) de SrTiO 3 . Este resultado también indica que la nano-heterounión se ha formado en el SrTiO 3 / TiO 2 nanofibras compuestas (rutilo) (Fig. 4b), que serían beneficiosas para separar pares de electrones-agujeros fotogenerados.
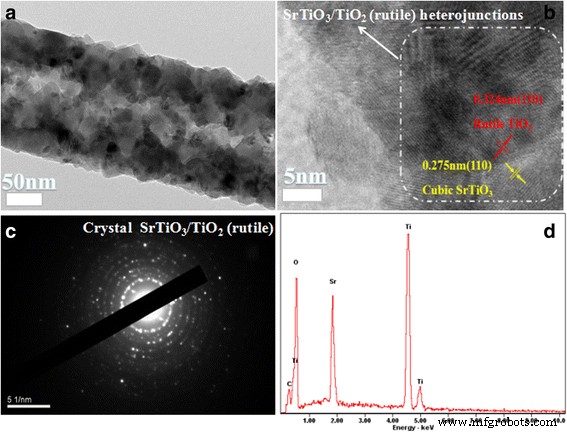
Imagen TEM y espectro EDS de ST-3. un Imagen TEM de ST-3, ( b ) HRTEM del área delimitada del rutilo TiO 2 y SrTiO 3, ( c ) SAED de ST-3, ( d ) EDS de ST-3
La difracción de electrones de área seleccionada (SAED) como se muestra en la Fig. 4c, que indica que la nano-heterojucción posee una alta cristalinidad. El FESEM EDX en la Fig. 4d además confirma que las heteroarquitecturas ST-3 contienen los elementos Ti, Sr, O y corresponden a la XRD.
El MO se utilizó como un contaminante de tinte modelo para estudiar la actividad fotocatalítica del TiO 2 desnudo (rutilo), desnudo SrTiO 3 y diferente SrTiO 3 / TiO 2 (rutilo) nanocompuestos, y los resultados se muestran en la Fig. 5. Después de 40 min de irradiación, el rutilo ST-1, ST-3, ST-5, ST-10, TiO 2 desnudo (rutilo) y SrTiO desnudo 3 las nanofibras se habían degradado aprox. 62%, 93%, 79%, 43%, 47% y 44% del colorante MO inicial, respectivamente (Fig. 5b). Es interesante que, con la creciente concentración de SrTiO 3 , la actividad fotocatalítica de SrTiO 3 / TiO 2 Las nanofibras compuestas (rutilo) exhiben una mejora obvia, lo que indica que la presencia de la heteroestructura en el fotocatalizador compuesto es beneficiosa para la fotocatálisis. Es más, como se muestra en la Fig. 5b, cuando hay un exceso de SrTiO 3 , los compuestos pueden exhibir una actividad fotocatalítica decreciente, lo que podría atribuirse a que la fotocatálisis del SrTiO 3 es mucho más débil que el TiO 2 , tan adecuado SrTiO 3 podría formar la heterojucción para mejorar la fotocatálisis de manera eficiente, pero el exceso de SrTiO 3 puede llevar a una disminución obvia.
Levantamiento de actividad fotocatalítica de diferentes muestras. un Espectros de absorción de ST-3 en fotocatálisis, ( b ) Curvas de degradación fotocatalítica con diferentes productos, ( c ) Reciclaje del ST-3, ( d ) Los espectros UV-Vis de diferentes productos
Para que sea conveniente para el uso fotocatalítico a largo plazo en el tratamiento de aguas residuales de tinte, la estabilidad cíclica es uno de los factores más importantes y se muestra en la Fig. 5c. Como se muestra en la Fig. 5c, después de 5 ciclos, hay una pérdida insignificante de fotodegradación de MO, que podría atribuirse a la pérdida de fotocatalizador en el proceso centrífugo e ilustra además que los fotocatalizadores compuestos ST-3 poseen una alta estabilidad y ciclicidad.
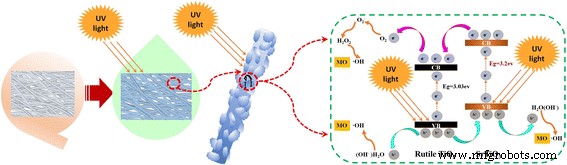
Como excelente fotocatálisis, el posible mecanismo para la actividad fotocatalítica mejorada del SrTiO 3 / TiO 2 Las nanofibras compuestas (rutilo) son muy importantes para su posterior modificación. Como se muestra en la Fig. 5d, la absorción de las diferentes muestras cambia poco, lo que significa que la actividad fotocatalítica es independiente de la absorción, lo que podría atribuirse a la nano-heterojucción única. El posible mecanismo se representa de la siguiente manera:cuando la luz ultravioleta irradia la superficie de las nanofibras compuestas, tanto el SrTiO 3 y el rutilo TiO 2 podría generar agujeros (h + ) y electrones (e - ) como se muestra en (1). Luego, los electrones generados se inmigran desde la banda de valencia (VB) de SrTiO 3 a las bandas de conducción (CB) de SrTiO 3 , y luego trasplantado en la banda de conducción (CB) de rutilo TiO 2. Por otro lado, los agujeros se transfieren a VB de SrTiO 3 de rutilo TiO 2 , que podría promover la separación de carga de manera eficiente para aumentar la vida útil de los portadores de carga y mejorar la eficiencia de la carga interfacial transferida para mejorar la actividad fotocatalítica del SrTiO 3 / TiO 2 heteroestructura (rutilo) (Fig. 6).

Un mecanismo propuesto para la degradación fotocatalítica de MO por el SrTiO 3 / TiO 2 (rutilo)
Mientras tanto, se proporcionó una fórmula probable de oxidación fotocatalítica de naranja de metilo de la siguiente manera:
$$ \ mathrm {SrTi} {\ mathrm {O}} _ 3 / \ mathrm {T} \ mathrm {i} {\ mathrm {O}} _ 2 \ left (\ mathrm {rutile} \ right) + \ mathrm {h } \ upnu \ to \ \ mathrm {SrTi} {\ mathrm {O}} _ 3 / \ mathrm {T} \ mathrm {i} {\ mathrm {O}} _ 2 \ left (\ mathrm {rutile} \ right) + {\ mathrm {h}} ^ {+} + {\ mathrm {e}} ^ {\ hbox {-}} $$ (1) $$ {\ mathrm {h}} ^ {+} + \ mathrm {O } {\ mathrm {H}} ^ {\ hbox {-}} \ to \ cdot p \ mathrm {O} \ mathrm {H} $$ (2) $$ {\ mathrm {h}} ^ {+} + {\ mathrm {H}} _ 2 \ mathrm {O} \ \ to \ cdot p \ mathrm {O} \ mathrm {H} + {\ mathrm {H}} ^ {+} $$ (3) $$ {\ mathrm {O}} _ 2 + {\ mathrm {e}} ^ {\ hbox {-}} \ to \ cdot p {{\ mathrm {O}} _ 2} ^ {\ hbox {-}} $$ (4) $$ \ cdotp {{\ mathrm {O}} _ 2} ^ {\ hbox {-}} + {\ mathrm {H}} _ 2 \ mathrm {O} \ to \ cdotp \ mathrm {O} \ mathrm {O} \ mathrm {H} + \ mathrm {O} {\ mathrm {H}} ^ {\ hbox {-}} $$ (5) $$ \ cdotp \ mathrm {O} \ mathrm {O} \ mathrm {H} + {\ mathrm {H}} _ 2 \ mathrm {O} + {\ mathrm {e}} ^ {\ hbox {-}} \ to {\ mathrm {H}} _ 2 {\ mathrm {O}} _ 2 + \ mathrm {O} {\ mathrm {H}} ^ {\ hbox {-}} $$ (6) $$ {\ mathrm {H}} _ 2 {\ mathrm {O}} _ 2 + {\ mathrm {e}} ^ {\ hbox {-}} \ to \ cdotp \ mathrm {O} \ mathrm {H} + \ mathrm {O} {\ mathrm {H}} ^ {\ hbox { -}} $$ (7) $$ \ cdotp \ mathrm {O} \ mathrm {H} + \ mathrm {M} \ mathrm {O} \ to \ mathrm {C} {\ mathrm {O}} _ 2 + {\ mathrm {H}} _ 2 \ mathrm {O} + \ mathrm {Otros} $$ (8) $$ \ cdotp {{\ mathrm {O}} _ 2} ^ {\ hbox {-}} + \ mathrm {M} \ mathrm {O} \ to \ mathrm {C} {\ mathrm {O}} _ 2 + {\ mathrm {H}} _ 2 \ mathrm {O} + \ mathrm {Otros} $$ (9) $$ \ cdotp \ mathrm {O} \ mathrm {O} \ mathrm {H} + \ mathrm {M} \ mathrm {O} \ to \ mathrm {C} {\ mathrm {O}} _ 2 + {\ mathrm {H}} _ 2 \ mathrm { O} + \ mathrm {Otros} $$ (10)Por lo tanto, el SrTiO 3 / TiO 2 Las nanofibras compuestas (rutilo) podrían considerarse como un fotocatalizador económico y continuo en aplicaciones futuras.
Conclusiones
En resumen, hemos preparado el SrTiO 3 / TiO 2 nanofibras compuestas (rutilo) a través de una ruta simple de electrohilado y mostraron su excelente capacidad para degradar el naranja de metilo, que podría atribuirse principalmente a la notable heterojucción y la alta cristalinidad. Además, la nueva estructura 3D podría aumentar el área de superficie específica de manera eficiente, lo que también es una razón importante para la fotocatálisis. Por lo tanto, un fotocatalizador excelente podría ofrecer una nueva visión para el diseño del catalizador futuro.
Nanomateriales
- Las 10 principales propiedades del aluminio y sus aplicaciones
- Propiedades del aluminio y características de la aleación
- Preparación y propiedades magnéticas de nanopartículas de espinela de FeMn2O4 dopadas con cobalto
- Hacia los nanofluidos de TiO2:Parte 1:Preparación y propiedades
- Compuesto híbrido Nanoestructurado de sílice / oro-celulosa-Amino-POSS mediante el proceso Sol-Gel y sus propiedades
- Hacia los nanofluidos de TiO2:Parte 2:Aplicaciones y desafíos
- Propiedades ópticas del infrarrojo cercano visible y estructural del TiO2 dopado con Cr para pigmentos fríos coloreados
- Síntesis sonoquímica de un solo paso y propiedades fotocatalíticas fáciles de compuestos de puntos cuánticos de grafeno / Ag3PO4
- Efecto del agente peptizante ácido sobre la relación anatasa-rutilo y el rendimiento fotocatalítico de nanopartículas de TiO2
- Fabricación y propiedad fotocatalítica de nuevos nanocompuestos SrTiO3 / Bi5O7I
- Un nuevo material de conversión ascendente de Ho3 + -Yb3 + -Mg2 + TiO2 tri-dopado y sus aplicaciones a las células solares de perovskita



