Aplicación de nanohojas de nitruro de boro exfoliado químicamente dopadas con Co para eliminar rápidamente los contaminantes orgánicos del agua textil
Resumen
Los materiales en capas bidimensionales dopados con metales de transición exhiben una magnetización mejorada y una estabilidad catalítica mejorada durante el tratamiento del agua, lo que conduce a posibles aplicaciones ambientales en varios sectores industriales. En el presente estudio, se exploraron nanohojas de nitruro de boro dopadas con cobalto (Co) (BN-NS) para tal aplicación. Se utilizó un proceso de exfoliación química para exfoliar BN-NS y se adoptó la ruta hidrotermal para incorporar el dopante de Co en varias concentraciones (por ejemplo, 2,5, 5, 7,5 y 10% en peso). El estudio de difracción de rayos X (XRD) indicó que la cristalinidad mejoró con el dopado con la formación de una fase hexagonal del material sintetizado. La difracción de electrones de área seleccionada (SAED) confirmó una cristalinidad mejorada, lo que corrobora los resultados de XRD. El espaciado entre capas se evaluó mediante un microscopio electrónico de transmisión de alta resolución (HR-TEM) equipado con el software de micrografía digital Gatan. El análisis de composición y grupo funcional se llevó a cabo con espectroscopía de rayos X de dispersión de energía (EDS) y de infrarrojos por transformada de Fourier (FTIR), respectivamente. Se utilizaron microscopio electrónico de barrido de emisión de campo (FE-SEM) y HR-TEM para sondear las morfologías de la superficie de las muestras preparadas. Los modos de unión en la muestra se identificaron mediante análisis Raman. Las propiedades ópticas se examinaron usando espectroscopía UV-vis. Se adquirieron espectros de fotoluminiscencia para estimar la separación y recombinación de excitones. Las propiedades magnéticas se estudiaron mediante el bucle de histéresis adquirido mediante mediciones de VSM. El colorante azul de metileno se degradó con el anfitrión preparado y se utilizaron nanohojas dopadas como catalizadores y se investigaron mediante espectros de absorción que iban de 250 a 800 nm. Los resultados experimentales de este estudio indican que el BN-NS codopado mostró propiedades magnéticas mejoradas y puede usarse para degradar los tintes presentes como efluentes en las aguas residuales industriales.
Introducción
Recientemente, el nitruro de boro (BN), un prometedor material en capas bidimensional similar al grafeno, disulfuro de tungsteno (WS 2 ) y disulfuro de molibdeno (MoS 2 ), ha atraído una atención considerable. El nitruro de boro existe típicamente en su forma cristalográfica más estable, es decir, nitruro de boro hexagonal (h-BN). Además, se encuentra como nitruro de boro cúbico (c-BN) que es estructuralmente análogo al diamante, nitruro de boro romboédrico (r-BN) y una fase amorfa [1]. El espaciado entre capas entre las capas de h-BN es 3.30 ~ 3.34 Å mientras que el grafito exhibe un espaciado de 3.33 ~ 3.35 Å. Además, h-BN es un buen aislante que posee una banda prohibida de ~ 5,9 eV [2, 3]. La estructura cristalina de h-BN se parece a la del grafeno, por lo que a veces se le denomina "grafeno blanco" y se le denomina "material gemelo" del grafeno. Curiosamente, los átomos de boro y nitrógeno están unidos covalentemente y dispuestos en un patrón en forma de panal [2, 4]. Además, el h-BN ofrece excelentes propiedades físicas, químicas, térmicas, eléctricas, ópticas y dieléctricas, que lo hacen atractivo para su uso en diversas aplicaciones [5,6,7]. Se han realizado estudios para alterar las características de aislamiento de BN mediante la sintonización de banda prohibida y las propiedades estructurales [3, 8]. Las nanoláminas de nitruro de boro (BN-NS) se prepararon inicialmente en 2004 exfoliando material a granel debido a su indisponibilidad en la naturaleza. Hasta la fecha, se han adoptado varios métodos para producir nanoláminas que incluyen exfoliación química [9], molienda de bolas [10], irradiación con haz de electrones [11] y técnica de vapor químico [12]. En la bibliografía también se describen otras rutas de exfoliación [13,14,15].
Las aplicaciones potenciales de BN-NS incluyen su uso en dispositivos optoelectrónicos y dispositivos de gestión térmica. Es particularmente adecuado para su uso como fotocatalizador y catalizador en el tratamiento de aguas residuales [3, 16, 17]. El agua juega un papel vital en la supervivencia y el desarrollo de todas las especies vivientes de la tierra, incluida la humanidad. Un suministro adecuado de agua de buena calidad durante todas las estaciones tiene un impacto importante en el medio ambiente y el crecimiento económico de una región [18, 19]. Además, la industria alimentaria en todo el mundo depende en gran medida de un suministro constante de agua limpia [20]. La disponibilidad de agua pura y dulce está influenciada por muchos factores, incluida la alta tasa de crecimiento de la población. Se estima que aproximadamente 2.700 millones de personas en numerosos países enfrentan escasez de agua potable [18, 21].
Según la literatura, una gran cantidad de tintes, incluidos el rojo congo, el amarillo Martius, el naranja de metilo, el rojo de metilo y el azul de metilo, se utilizan en una variedad de sectores industriales como el cuero, la construcción, el papel, la fabricación de metales y la impresión [22,23 , 24]. Los iones metálicos nocivos (Pb, Cr, Hg, Cu, etc.) producidos por el uso de estos colorantes provocan efectos nocivos en la vida humana y acuática. La exposición a colorantes no tratados e iones metálicos tóxicos puede provocar enfermedades graves como anemia, cáncer, encefalopatía y debilitamiento del sistema inmunológico [20, 25]. Además, la materia orgánica natural superflua puede aumentar el nivel de toxicidad y afectar negativamente a los sistemas de purificación de agua [26].
La sal y otras impurezas menores se pueden eliminar del agua mediante técnicas ampliamente disponibles; sin embargo, la remoción de tintes dañinos e iones de metales tóxicos es más desafiante. Se han utilizado diversas rutas para purificar el agua de estos contaminantes, incluida la fotocatálisis [16], la asistencia magnética [27], la eliminación de aceite [28] y la filtración y coagulación [29]. Entre estas técnicas, la catálisis ocupa un lugar importante, ya que se considera respetuosa con el medio ambiente, rentable y energéticamente eficiente. Además, la gran superficie y las propiedades químicas y físicas superiores de BN-NS lo hacen adecuado para su uso como catalizador en el tratamiento de aguas residuales [17].
En el presente estudio, también se investigan las propiedades magnéticas de muestras sintetizadas debido a su impacto potencial en el proceso de tratamiento de aguas residuales. Convencionalmente, los metales de transición que contienen electrones en capas 3d o 4f son responsables del origen del magnetismo. La literatura indica que la magnetización espontánea también se observa en elementos ligeros sin metales que contienen electrones en s y p orbital [30, 31]. Además, el origen del ferromagnetismo en semiconductores u óxidos magnéticos diluidos (DMS (O) s) es objeto de un intenso debate [32, 33]. El análisis teórico sugiere que los defectos periódicos en los nanomateriales basados en grafeno (2D), particularmente h-BN, inducen un orden magnético (ferromagnetismo, ferrimagnetismo y anti-ferromagnetismo) [34]. Además, estos defectos en h-BN actúan favorablemente para alterar su comportamiento diamagnético hacia el ferromagnetismo [35]. Los metales de transición (por ejemplo, Ni, Fe, Cu, Zn y Co) exhiben propiedades magnéticas satisfactorias; por lo tanto, el dopaje de estas especies en nanohojas de BN augura resultados prometedores. En consecuencia, el dopaje del metal de transición (Co) en h-BN da lugar a defectos extrínsecos que, junto con los defectos intrínsecos, sirven para mejorar sus propiedades magnéticas [36].
En el presente estudio, se utilizó una técnica hidrotermal simple para preparar nanohojas de BN codopadas con actividad catalítica mejorada y comportamiento magnético. El efecto del dopaje se investigó evaluando las propiedades estructurales, morfológicas, ópticas y magnéticas de BN-NS.
Métodos
El presente estudio tenía como objetivo sintetizar varias concentraciones de Co en nanohojas de h-BN a través de la ruta hidrotermal para eliminar los contaminantes orgánicos del agua textil y el comportamiento magnético.
Materiales
Polvo de BN a granel (98%), dimetilformamida (DMF) azul de metileno (MB) y borohidruro de sodio (NaBH 4 ) se adquirieron en Sigma-Aldrich Co. (Alemania). Cobalto (II) nitrato hexahidrato (CoH 12 N 2 O 12 ) (98%) se compró a VWR Chemicals (Reino Unido). Todos los productos químicos adquiridos para este estudio se utilizaron sin purificación adicional.
Exfoliación y síntesis de BN co-dopado
Se empleó la ruta de exfoliación química para sintetizar BN-NS. En primer lugar, se disolvieron 5 g de polvo de BN a granel en 200 ml de DMF y se agitó durante 20 min para obtener la solución madre. A esto le siguió una sonicación vigorosa durante 12 h. Después de la sonicación, se recogieron láminas de BN flotantes de la solución madre. El dopaje se llevó a cabo mediante un enfoque hidrotermal. En este método, se utilizó nitrato de cobalto (II) hexahidrato como dopante de Co. Se doparon varias relaciones en peso de hexahidrato de nitrato de cobalto (II) (2,5, 5, 7,5 y 10% en peso) en las nanohojas de BN recogidas. Posteriormente, se dispersaron BN-NS seleccionados y nitrato de cobalto (II) hexahidrato con diversas proporciones (1:0.25, 1:0.05, 1:0.075, 1:0.1) en 100 mL de agua desionizada bajo agitación continua durante 15 min. La suspensión se vertió en un autoclave de acero inoxidable, se colocó en un horno de vacío a 200ºC durante 10 h como se presenta esquemáticamente en la Fig. 1. Finalmente, el autoclave se retiró del horno y se enfrió a temperatura ambiente. El precursor se secó en una placa caliente a 100-120 ° C.
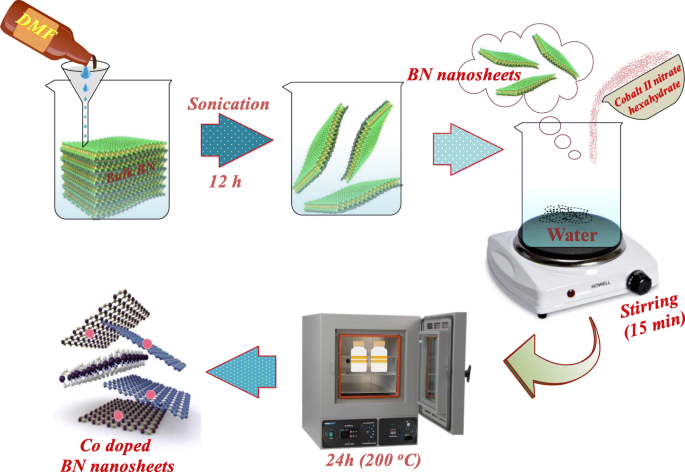
Ilustración esquemática de exfoliación y síntesis de BN-NS codopado
Actividad catalítica
Se midió la actividad catalítica de BN-NS puro y codopado para determinar el grado de degradación del colorante. Esto se llevó a cabo monitoreando la degradación de MB en una solución acuosa de NaBH 4 que sirve como agente reductor. Tanto MB como NaBH 4 se prepararon recientemente para garantizar la integridad de los datos experimentales. Habitualmente, el MB es el indicador redox empleado con más frecuencia en química analítica para regular la actividad catalítica durante una prueba de degradación del tinte. Además, el MB permanece azul en forma oxidada, mientras que parece neutral cuando se reduce [37]. Se realizaron dos experimentos catalíticos, el primero con 500 μL de NaBH 4 y 2 mg de catalizador y el segundo con 1000 μL de NaBH 4 y 4 mg de catalizador. En general, la concentración de un catalizador utilizado en un experimento es el factor más significativo que afecta la reacción química. Un catalizador reduce la energía de activación ( E a ) de una reacción, lo que sirve para mejorar su estabilidad y velocidad de reacción. El MB es principalmente un tinte tóxico que es peligroso para el medio ambiente. Puede reducirse con NaBH 4 que lo convierte en una especie no tóxica e incolora. Sin embargo, el proceso de reducción es relativamente lento en presencia de NaBH 4 . Los BN-NS sin dopar y codopados exhiben una gran superficie que, cuando se combina con un aumento de la reactividad de la reacción, sirve para acelerar la eficacia de reducción del colorante. La incorporación de un catalizador en MB en presencia de un agente reductor provoca adsorción. Además, una capa de reductor dispersa sobre los catalizadores también puede acelerar la adsorción debido a la reacción de oxidación-reducción entre el catalizador y el MB. La reacción de reducción por un catalizador ocurre transfiriendo e - del contenido del donante BH 4 - (por ejemplo, de NaBH 4 ) al MB de contenido del aceptador facilitado por BN-NS puro y dopado. Esto da como resultado la disminución de E a que sirve para estabilizar la reacción. La actividad catalítica se evaluó tomando 500 o 1000 μL de NaBH 4 diluido en 10 mL de solución MB en una cubeta de cuarzo. Posteriormente, se añadió catalizador (2 o 4 mg) para investigar la degradación del MB. La degradación del tinte se evaluó espectrofotométricamente como se ilustra esquemáticamente en la Fig. 2. Además, los espectros de absorción que variaban de 200 a 800 nm obtenidos con MB se usaron como referencia a temperatura ambiente. La degradación del tinte en presencia de catalizador puro y dopado confirmó una actividad catalítica mejorada, mientras que el NaBH 4 no pudo degradar MB.

Ilustración esquemática de la configuración experimental utilizada para evaluar la actividad catalítica
Caracterizaciones de materiales
Las muestras preparadas se analizaron utilizando una variedad de técnicas. La constitución de la fase y el grado de cristalinidad se evaluaron utilizando un difractómetro de rayos X (XRD) analítico PAN X-pert PRO con radiación Cu-Kα ( λ =1,5418 Å) y 2θ que oscilan entre 5 ° y 80 °. La espectroscopia de infrarrojos por transformada de Fourier (FTIR) se realizó utilizando un espectrómetro de Perkin Elmer para confirmar la presencia de grupos funcionales. Los espectros de emisión se obtuvieron a partir del espectroscopio de fotoluminiscencia (PL) utilizando el espectrofluorómetro JASCO FP-8200. Los espectros Raman se obtuvieron con un microscopio DXR Raman (Thermo Scientific) que tiene láser de diodo a 532 nm. El examen morfológico se realizó utilizando un microscopio electrónico de barrido de emisión de campo JSM-6460LV (FE-SEM) y un microscopio electrónico de transmisión de alta resolución Philips CM30 y JEOL JEM 2100F (HR-TEM). Las propiedades ópticas se registraron a través del espectrofotómetro UV-visible-Genesys 10S. Se utilizó espectroscopia de rayos X de dispersión de energía (EDS) para rastrear la composición elemental. Las propiedades magnéticas se midieron con un magnetómetro de muestra vibrante (VSM).
Resultados y discusión
Se utilizó XRD para analizar la fase y la estructura cristalina de las muestras preparadas, como se ilustra en la Fig. 3a. Se observaron picos de difracción a 26,8 °, 41,6 °, 43,52 ° y 50,2 ° que se indexaron como planos (002), (100), (101) y (102), respectivamente. Los reflejos observados confirman la presencia de una fase hexagonal de BN y concuerdan bien con JCPDS 00-034-0421 [38, 39]. Vale la pena señalar que la intensidad del pico característico de la muestra pura a la dopada aumenta, lo que sugiere que la cristalinidad se mejoró con la incorporación de Co. Además, los patrones de XRD indican un cambio de pico hacia un ángulo de difracción más alto, que se atribuye a la presencia de dopante. en las muestras [40]. Espaciado entre capas d 002 calculado con la ayuda de la ley de Bragg (nλ =2dsinθ) fue ~ 0.34 nm, que es consistente con los resultados HR-TEM [41].
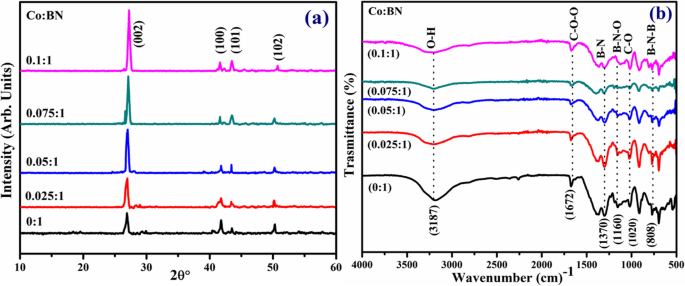
un Patrones de XRD de concentraciones prístinas y diversas (2,5, 5, 7,5 y 10% en peso) de BN-NS codopado. b Espectros FTIR
Se realizó FTIR para identificar huellas dactilares de infrarrojos en las nanohojas de control y dopadas, como se ilustra en la Fig. 3d. Se observaron espectros a ~ 808, 1020, 1160, 1370, 1672 y 3187 cm −1 . Se identificaron dos picos de núcleo a 808 y 1370 cm −1 que se cree que están asociados con B – N – B (vibraciones de flexión) y B – N (vibración de estiramiento). El último pico está asociado con la vibración de flexión A 2u modo (fuera del plano) mientras que el pico anterior coincide bien con la vibración de estiramiento E 1u modo (en el plano) [42, 43]. Además, los picos a 1020, 1160 y 1672 cm −1 fueron consistentes con el enlace C – O, B – N – O y C =O, respectivamente [44]. Otro pico centrado en 3187 cm −1 corresponde al enlace B – OH [45, 46].
La identificación de huellas dactilares estructurales se llevó a cabo mediante espectros Raman, como se ilustra en la Fig. 4a. Los espectros muestran una banda Raman característica centrada en 1370 cm −1 que se atribuye a E 2g modo fonón activo de h-BN y correlacionado con el pico G del grafeno [47]. La BN-NS exfoliada exhibe picos menores a 550 y 880 cm −1 que se atribuye al fondo fluorescente [48]. Además, se informa en la literatura que el h-BN monocristalino de alta calidad exhibe E 2g modo telefónico activo a 1367 cm −1 [40]. En este estudio, E 2g desplazada al rojo El modo de fonón activo se produce como resultado de una débil interacción entre las capas intermedias de BN. Además, los espectros Raman desplazados al rojo muestran la presencia de unas pocas nanoláminas en capas, lo que provoca un ligero alargamiento dentro de los enlaces de boro y nitrógeno (B – N) [49, 50]. En consecuencia, este alargamiento en el enlace B – N se debe al ablandamiento de los fonones y concuerda bien con los resultados citados anteriormente. Además, el dopaje elemental, el orden de las capas apiladas, el tamaño del dominio y la porosidad podrían provocar el ensanchamiento y desplazamiento de los picos [51].
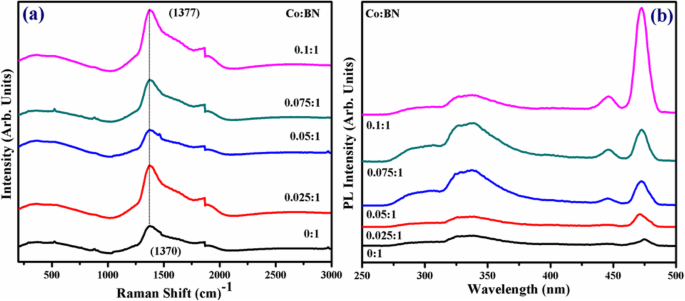
un Espectros de control Raman y BN-NS dopado. b Espectros PL
Se realizó espectroscopía PL para comprender la migración excitónica y la recombinación de pares de electrones-huecos, como se demuestra en la Fig. 4b. Los espectros se observaron con longitud de onda de excitación y emisión de λ ex =220 nm y λ em =310 nm, respectivamente. La banda característica observada a ~ 322–342 nm corresponde a la transición entre electrones y huecos debido al nivel de impurezas [52, 53]. Es de destacar que la banda excitónica aumenta pero no muestra un cambio de longitud de onda tras el dopaje. Los picos característicos a ~ 446 nm y ~ 471 nm indican que la intensidad de PL muestra un fuerte aumento de muestras puras a dopadas. Mientras tanto, el 10% en peso de BN-NS codopado tiene una intensidad PL máxima entre todas las muestras, lo que indica una recombinación máxima de huecos de electrones. La intensidad disminuye gradualmente debido a la concentración de dopaje que indica la separación de las cargas fotogeneradas [54]. Los espectros de emisión revelaron un comportamiento PL dependiente de la excitación que es consistente con los resultados reportados previamente [55].
Se empleó espectroscopía UV-vis para investigar los espectros de absorción y la banda prohibida de los productos preparados, como se muestra en la Fig. 5a. El pico de absorción característico del anfitrión BN-NS estaba en un umbral de ~ 205 nm en la región ultravioleta profunda (DUV) en referencia a la banda prohibida de ~ 5,7 eV como se presenta en la Fig. 5b. Vale la pena mencionar que la BN a granel induce un intervalo de banda de 5,2 a 5,4 eV, mientras que una monocapa expone un intervalo de banda de ~ 6,07 eV que coincide bien con los cálculos teóricos (por ejemplo, 6,0 eV). En el caso de bi / multicapas, el valor de la banda prohibida oscila entre 5,56 y 5,92 eV [43]. Siendo coherentes con una banda prohibida amplia en la Fig. 5b y el comportamiento de luminiscencia DUV en la Fig. 5a, las nanohojas de h-BN pueden considerarse como un nuevo candidato para una variedad de aplicaciones en la emisión de fotones, rayos ultravioleta y detectores DUV [56] . Además, el borde de absorción se desplazó hacia longitudes de onda más largas con concentraciones de dopaje crecientes (2,5 a 10% en peso), lo que demuestra un corrimiento al rojo (Fig. 5b) [57].
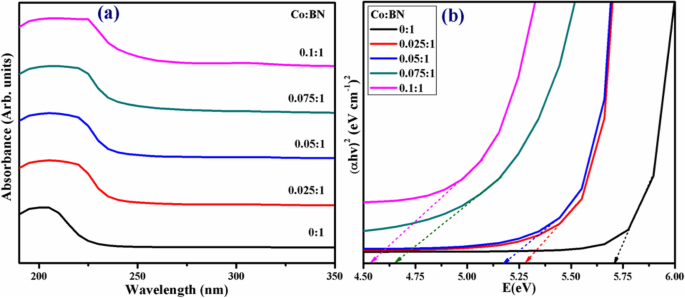
un Espectros UV-vis de BN-NS desnudos y co-dopados. b Gráfico de tauc para bandgap
La morfología y la composición del control y la BN-NS dopada se analizaron con FE-SEM como se muestra en la Fig. 6a. Las micrografías indican que las partículas obtenidas poseían una estructura agregada de nanolaminas con una superficie lisa y bordes curvos. La Figura 6 b – d muestra nanohojas BN cubiertas con cobalto. Se observó aglomeración en todas las muestras. Las micrografías FE-SEM revelan que las nanoláminas están plegadas con una estructura en capas compacta y poseen una forma y dimensión lateral no uniformes. La configuración y las dimensiones de las nanoláminas son consecuencia de la exfoliación del polvo de BN a granel. La morfología del producto obtenido se confirmó adicionalmente con análisis HR-TEM. A partir de las micrografías HR-TEM que se muestran en las Fig. 6a-d, se observó una morfología en forma de hoja de los productos preparados. Además, se observaron superficies compactas y rugosas de nanohojas con características ligeramente porosas que dan como resultado una actividad catalítica mejorada. Se observaron manchas esféricas oscuras que indican la incorporación exitosa del dopaje. Se registraron el apilamiento de minutos y los bordes curvados de las nanohojas, como se muestra en el análisis SEM en la Fig. 6a-d. Los resultados experimentales sugieren que los análisis FE-SEM y HR-TEM apuntan hacia la exfoliación exitosa de nanohojas de BN a partir de BN a granel.

un , a ’ Imágenes FE-SEM y HR-TEM de BN-NS puro. b - d FE-SEM de (2,5, 7,5 y 10% en peso) dopado de BN-NS. b ’ - d ’ HR-TEM de (2,5, 7,5 y 10% en peso) BN-NS dopado (recuadro 50 nm)
Se llevaron a cabo mediciones de espaciado entre capas de muestras desnudas y dopadas con IFFT (ver recuadro) inducido por medio de imágenes FFT de HR-TEM examinadas a través del software de micrografía digital Gatan para distinguir las franjas de celosía. Observado d -valor de espacio para BN-NS prístino y dopado al 2,5% en peso es 0,34 nm y 0,21 nm, que corresponde a d 002 y d 100 planos, respectivamente, como se ilustra en la Fig. 7a, c. Estos hallazgos concuerdan bien con el análisis de XRD y los datos estándar [58]. Además, los perfiles SAED se muestran en la Fig. 7b, d que significa anillos de difracción de puntos brillantes. Estos anillos de difracción se indexaron como originados en los planos (002), (100), (101) y (102) que concuerdan bien con los resultados de XRD. Los patrones SAED sugieren que todos los anillos pertenecen al BN hexagonal y validan la naturaleza altamente cristalina de las nanoláminas [58].
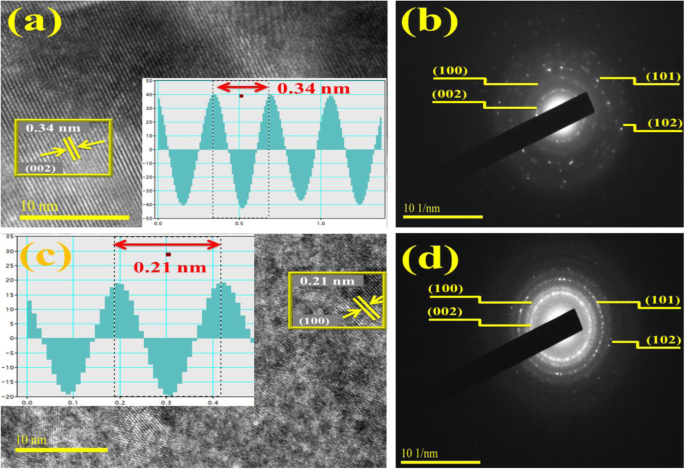
un , c d -análisis de espaciamiento del anfitrión y BN-NS dopado al 2,5% en peso. b , d Patrones de control SAED y BN-NS dopado al 2,5% en peso
La composición elemental de la superficie de BN-NS dopada se investigó mediante análisis EDS como se muestra en la Fig. 8a-d, respectivamente. Las micrografías obtenidas exhiben fuertes picos de boro (B) y nitrógeno (N) mientras que también se observó una señal menor para el cobalto (Co) en el espectro de EDS (Fig. 8a). Se observaron dos picos moderados de Co a 0.5 y 7 keV en muestras co-dopadas, que confirman la incorporación exitosa del dopante. Además, la señal de carbono por debajo de 1 keV se origina en las lengüetas de carbono que se utilizan para sujetar la muestra durante el análisis y / o se debe a los recuentos de fondo elevados en el detector SEM-EDS. De lo contrario, no había carbono en la muestra [59].

un - d Análisis EDS de varias concentraciones (2,5, 5, 7,5 y 10% en peso) de BN-NS codopado
Las propiedades magnéticas de BN-NS codopadas se evaluaron con la curva M – H utilizando mediciones de VSM. En el gráfico que se muestra en la Fig. 9, la apariencia sigmoidea de los bucles M – H demuestra que la BN-NS codopada se caracteriza por un momento magnético. El estudio de la literatura revela que la BN prístina muestra un comportamiento diamagnético con susceptibilidad (χ ≈ - 8,6 × 10 −7 emu / g) [31, 35]. Por el contrario, BN-NS codopado exhibe ferromagnetismo a temperatura ambiente (RT-FM) resultante de la interacción de intercambio entre Co +2 iones y dipolos no apareados que tienden a alinearse a lo largo del campo magnético aplicado. Se puede observar que el bucle de histéresis aparece más preciso y la concentración de dopaje aumenta, lo que afirma la pureza y la incorporación exitosa del dopante. La coercitividad, remanencia y magnetización de saturación de BN-NS codopado predicen la suavidad y dureza del material magnético. El codopaje en BN-NS da como resultado la formación de un material magnético blando. Los valores de la remanencia ( M r ), magnetización de saturación ( M s ) y coercitividad ( H C ) para varias concentraciones de dopaje (2,5, 5 y 7,5% en peso) se calcularon mediante la curva M – H como se muestra en la Tabla 1.
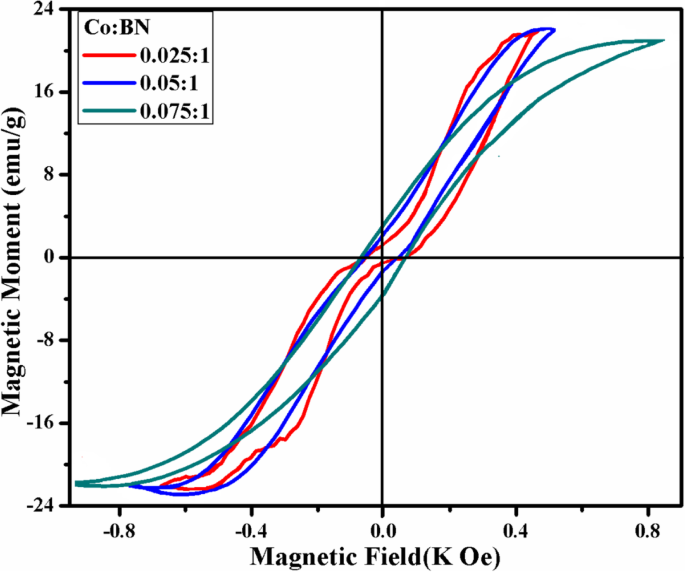
Curva M – H de diversas concentraciones (2,5, 5 y 7,5% en peso) de BN-NS codopado
La actividad catalítica de BN-NS prístina y codopada que funciona como catalizadores se expresó mediante la degradación de MB y se investigó mediante espectros de absorción controlados con espectrofotómetro UV-vis. Las Figuras 10 a – h muestran los resultados de la actividad catalítica utilizando 500 μL de NaBH 4 y 2 mg de catalizador. En la Fig. 10a, se puede ver que NaBH 4 no logra degradar el MB con éxito, ya que solo degrada el 8% del tinte después de 40 min. Incorporación de BN-NS puro en MB en presencia de NaBH 4 resultó en un 45% de degradación en 30 min (Fig. 10b). Además, la capacidad de degradación de BN-NS codopada (ver Fig. 10b-e) fue significativamente mayor. Varias concentraciones (2,5, 5, 7,5 y 10% en peso) de catalizador dopado demuestran una degradación del 58, 77, 90 y 97% en 13, 8, 3 y 2 min, respectivamente. Curiosamente, las nanohojas dopadas al 10% en peso producen una actividad catalítica superior y degradan el 97% de tinte en solo 2 minutos, lo que es más alto que las concentraciones dopadas (7.5, 5 y 2.5% en peso) y se observa una intensidad máxima característica a ~ 290 y 665 nm. Este incremento en la degradación del tinte se debe posiblemente a la mejora de la adsorción disponible, así como a los sitios catalíticos en los catalizadores. En este mecanismo, el estado 3d de Co interactúa bien con el estado 2p de los correspondientes sitios B o N disponibles en BN-NS. Esta fuerte interacción entre los estados 3d Co y 2p B o N aumenta la actividad catalítica y da como resultado una rápida degradación del tinte, lo que respalda favorablemente nuestros resultados [60].
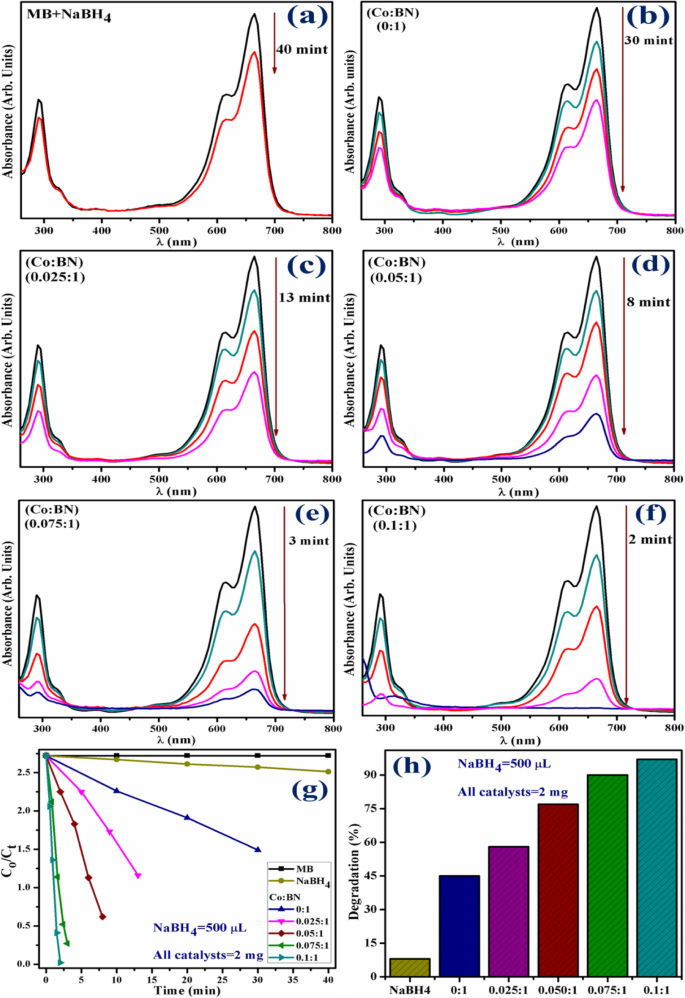
un Espectros UV-vis dependientes del tiempo de NaBH 4 . b prístina BN-NS. c - f Varias concentraciones (2,5, 5, 7,5 y 10% en peso) de BN-NS codopado. g Parcelas de C t / C o versus tiempo. h Comparación del porcentaje de degradación en varias concentraciones de BN-NS
El experimento catalítico se repitió usando 1000 μL de NaBH 4 y 4 mg de catalizador. Al aumentar la concentración del catalizador, la reacción avanza más rápidamente en comparación con el experimento mencionado anteriormente. Esta observación concuerda bien con la literatura. En el presente experimento, NaBH 4 todavía no degradó MB mientras tanto BN-NS prístino y varias concentraciones (2.5, 5, 7.5 y 10% en peso) de catalizador dopado degradaron 51, 65, 82, 95 y 99% en 27, 10, 6, 2 y 1 min, respectivamente, evaluado con un espectrofotómetro. Los resultados experimentales que miden la actividad catalítica se ilustran en la Fig. 11a, b.
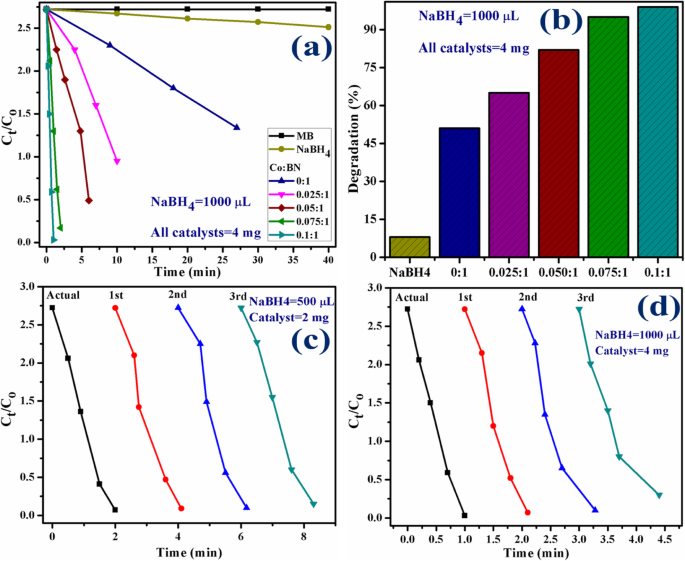
un Parcelas de C t / C o versus tiempo usando NaBH 4 =1000 μL y catalizadores =4 mg. b Comparación del porcentaje de degradación en varias concentraciones. c Parcelas de C t / C o frente al tiempo de reutilización del 10% en peso de BN-NS codopado. d Parcelas de C t / C o frente al tiempo de reutilización del 10% en peso de BN-NS codopado
Según la ley de Beer-Lambert, la relación entre la concentración de MB en un momento específico ( C t ) y concentración inicial de MB ( C o ), denominado C t / C o , se puede estimar mediante la relación de absorbancia paralela ( A t / A o ). Las figuras 10 f y 11 a representan el curso temporal de C t / C o utilizado para todos los catalizadores, mientras que las Fig. 10 gy 11 b indican el porcentaje de degradación de todos los catalizadores. El porcentaje de degradación fue evaluado por Eq. 1.
$$ \ mathrm {Degradación} \ \ left (\% \ right) =\ frac {Co- Ct} {Co} \ times 100 $$ (1)Además, el valor del pH es una variable operativa vital en el tratamiento de degradación del tinte. Además, el pH tiene un papel importante en el tratamiento de aguas residuales textiles y en los mecanismos de reacción que contribuyen a la degradación del tinte. Cabe mencionar que el porcentaje de degradación depende en gran medida del valor del pH. En el presente experimento, el valor de pH se fijó en 8,5. Significativamente, la degradación del tinte debido a la actividad catalítica demostró mejores resultados en un ambiente alcalino que apoya favorablemente nuestros hallazgos experimentales. Varios informes revelan que la mayor degradación del colorante por actividad catalítica se observó en un ambiente alcalino [61].
La estabilidad y reutilización (capacidad de reciclaje) de los catalizadores es una característica importante para evaluar un catalizador utilizado para la degradación del tinte. En el presente estudio, se evaluó la estabilidad de los catalizadores dejando que el experimento realizado permaneciera durante 48 h. Después de 48 h, los resultados fueron los mismos que los realizados inicialmente, es decir, la degradación todavía estaba en su condición anterior. La reutilización del catalizador se investigó reciclando un 10% en peso de catalizador codopado que sirvió como un catalizador superior en el presente estudio durante tres ciclos. Los espectros extraídos de actividad catalítica reciclada se evaluaron como se muestra en la Fig. 11c, d.
Además, se examinó la carga del catalizador antes y después de tres procesos de reciclado. En la primera y segunda actividad, se detectó una pérdida de peso menor de catalizador que variaba de 2 mg y 4 mg (antes) a 1,7 mg y 3,6 mg (después de tres ciclos) considerando una desviación de detección de ~ 5% en el presente experimento. Estos hallazgos indican que la BN-NS codopada exhibe una estabilidad sobresaliente mientras sirve como catalizador. Finally, this study suggests that Co-doped BN-NS exhibits an efficient and outstanding catalytic behavior toward dye degradation in industrial wastewater treatment.
Conclusion
In this study, boron nitride nanosheets (BN-NS) were synthesized through chemical exfoliation of bulk BN powder. Various concentrations (2.5, 5, 7.5, and 10 wt%) of Co were successfully incorporated via the hydrothermal approach. As prepared, pure and doped BN-NS were characterized by a variety of techniques to evaluate the effect of doping. XRD patterns confirm the presence of the hexagonal phase of BN with improved crystallinity from pure to doped samples. Furthermore, the peak shift indicates the successful incorporation of doping. FTIR spectra indicate sp 2 bonded B–N stretching vibrations consistent with E1g mode (in-plane) as well as B–N–B bending vibration associated with A2u mode (out plane). Raman spectroscopy affirmed E2g active phonon mode of h-BN while photoluminescence spectroscopy revealed emission spectra that were attributed to exciton migration and recombination. Host and Co-doped BN-NS displayed absorbance in the DUV region along with a redshift that causes a decrease in bandgap energy suggesting it to be a suitable material for degradation of dye from industrial wastewater and organic pollutants. Sheet-like morphology of obtained product was studied by means of FE-SEM and HR-TEM. Slightly porous features result in high catalytic activity due to available adsorption sites. EDS analysis showed the purity of the sample and confirmed the incorporation of dopant in nanosheets. The magnetic behavior of Co-doped BN-NS was investigated through VSM measurements that display strong ferromagnetic behavior while pristine BN-NS show diamagnetic behavior. Significantly, the sigmoidal appearance of the hysteresis loop becomes more precise from lower to a higher concentration of Co-doped BN-NS, which point toward the formation of a soft magnetic material. Lastly, pure and Co-doped BN-NS was utilized as a catalyst in dye degradation. The catalytic activity provides efficient results for most samples but 10 wt% Co-doped catalyst showed significant outcome with the highest dye degradation (99%) in 1 min, making it a novel catalyst in this study. Extracted results from pure and doped BN-NS can be used as a guideline to modify and enhance magnetic properties in order to improve reliability in modern optoelectronic technology. Finally, the synthesized material has the potential to be used as a stable, reusable, and superior nano-catalyst to replace conventional wastewater treatment methods.
Disponibilidad de datos y materiales
Todos los datos están completamente disponibles sin restricciones.
Abreviaturas
- BN-NS:
-
Boron nitride nanosheets
- Co:
-
Cobalt
- UV-vis:
-
Ultra-violet visible spectroscopy
- XRD:
-
Difracción de rayos X
- DUV:
-
Deep ultraviolet region
- FTIR:
-
Fourier transform infrared spectroscopy
- PL:
-
Fotoluminiscencia
- DMF:
-
Dimethylformamide
- MB:
-
Methylene blue
- NaBH4 :
-
Sodium borohydride
- EDS:
-
Espectroscopia de rayos X de dispersión de energía
- FE-SEM:
-
Field emission scanning electron microscopy
- HR-TEM:
-
Microscopía electrónica de transmisión de alta resolución
- JCPDS:
-
Joint committee on powder diffraction standards,
- VSM:
-
Vibrating sample magnetometer measurements
Nanomateriales
- Python elimina duplicados de una lista
- Estados electrónicos de nanocristales dopados con oxígeno y emisión visible en silicio negro Preparado por ns-Laser
- Nuevos nanocompuestos de poliestireno con polianilina dopado con ácido lauril sulfúrico
- Hacia cadenas de átomos individuales con telurio exfoliado
- Microesferas de carbono magnéticas como adsorbente reutilizable para la eliminación de sulfonamidas del agua
- Respuesta fotovoltaica pronunciada del fototransistor MoTe2 multicapa con formulario de contacto asimétrico
- Exfoliación líquida de alta eficiencia de nanoláminas de nitruro de boro utilizando una solución acuosa de alcanolamina
- Síntesis fácil y respetuosa con el medio ambiente de nanocables de Co3O4 y su prometedora aplicación con grafeno en baterías de iones de litio
- Síntesis y caracterización de BiOCl modificado y su aplicación en la adsorción de tintes de baja concentración a partir de una solución acuosa
- Eliminación de antibióticos del agua con una membrana de nanofiltración 3D totalmente de carbono
- Cómo eliminar la humedad del aire comprimido



