Síntesis en un solo recipiente del soporte jerárquico de la aleación de Pd-Cu similar a una flor en el grafeno hacia la oxidación del etanol
Resumen
El efecto sinérgico de la aleación y la morfología de los nanocatalizadores juegan un papel fundamental en la electrooxidación del etanol. En este trabajo, desarrollamos un electrocatalizador novedoso fabricado por síntesis en un solo recipiente de nanocatalizadores jerárquicos de aleación de paladio (Pd) -cobre (Cu) con forma de flor apoyados en óxido de grafeno reducido (Pd-Cu (F) / RGO) para pilas de combustible de etanol directo. Las estructuras de los catalizadores se caracterizaron mediante el uso de microscopía electrónica de barrido (SEM), microscopio electrónico de transmisión (TEM), difracción de rayos X (XRD) y espectrómetro de fotoelectrones de rayos X (XPS). El Pd-Cu (F) sintetizado Se encontró que el nanocatalizador / RGO exhibe mayores rendimientos electrocatalíticos hacia la reacción de electrooxidación de etanol en medio alcalino en contraste con el nanocatalizador de Pd soportado por RGO y el catalizador comercial de negro de Pd en electrolito alcalino, lo que podría atribuirse a la formación de aleación y la morfología de las nanopartículas. El alto rendimiento del nanocatalizador revela el gran potencial del diseño de la estructura de los materiales de soporte para la futura fabricación de nanocatalizadores.
Antecedentes
Las pilas de combustible de etanol directo (DEFC) se consideran fuentes de energía renovables económicas y respetuosas con el medio ambiente debido a la baja temperatura de funcionamiento, la renovabilidad, la baja toxicidad y la alta densidad energética [1, 2]. La actividad a largo plazo se ha mantenido como un gran desafío para la aplicación futura de DEFC, mientras que el envenenamiento se convierte en el cuello de botella para una mejora adicional. Entre todos los nanocatalizadores metálicos, el Pd atrae más atención no solo por su menor costo sino también por sus escasos efectos de envenenamiento por CO para la oxidación electroquímica del etanol [3, 4]. Además, se informa que la morfología y las estructuras de los materiales de soporte o nanopartículas podrían influir significativamente en sus propiedades electroquímicas [5, 6], y se han estudiado las siguientes:micro / nanohojas [7], nanoflores [6], nanocables [8] , microesferas huecas jerárquicas [9] y estructuras en forma de flor / hierba [10]. El cobre jerárquico similar a una flor se informó recientemente al cambiar la morfología del cobre para adquirir una gran superficie [5, 11, 12]. También se ha encontrado que el cobre no solo reduce el costo del electrocatalizador, sino que también puede ser más preferible para la adsorción de hidroxilos, lo que aumenta aún más la tasa de oxidación del alcohol [4, 13]. Además, las propiedades electrónicas cambiarían debido a los desplazamientos del centro de la banda d durante la formación de la aleación de Pd-Cu, y el efecto sinérgico de la composición aumentaría aún más la actividad electrocatalítica hacia el etanol [14, 15].
Además de los materiales metálicos, se espera que los materiales de soporte ideales de los electrocatalizadores tengan un área de superficie alta y buena conductividad eléctrica [16, 17], y recientemente, se han desarrollado series de grafeno y sus materiales complejos como materiales de soporte para los nanocatalizadores hacia la oxidación del etanol. Se informó que los metales podrían estar bien dispersos en el grafeno debido a la gran cantidad de grupos funcionales en las capas de grafeno que exhibían una alta actividad catalítica para la electrooxidación del alcohol [15, 16, 18]. Por lo tanto, sería prometedor desarrollar nanocatalizadores de aleación de Pd-Cu con forma de flor apoyados en óxido de grafeno reducido hacia la oxidación electroquímica del etanol.
En este documento, desarrollamos un enfoque hidrotermal sencillo en un solo recipiente para preparar nanopartículas de aleación de Pd-Cu con forma de flor apoyadas en óxido de grafeno reducido (RGO). La adición de solución de amoníaco no solo influye en la formación de la aleación de Pd-Cu sino que también conduce a la estructura jerárquica en forma de flor, adhiriéndose a la superficie RGO, aumentando sinérgicamente el área de superficie de los electrocatalizadores y adquiriendo más sitios activos disponibles [19]. El Pd-Cu (F) / El nanocatalizador RGO se caracterizó por microscopía electrónica de barrido (SEM), microscopio electrónico de transmisión (TEM), difracción de rayos X (XRD), espectrómetro de fotoelectrones de rayos X (XPS), espectroscopía de emisión óptica de plasma acoplado inductivamente (ICP-OES) y análisis termogravimétrico (TGA). Los estudios electroquímicos en medio alcalino muestran que el Pd-Cu (F) / El nanocatalizador RGO proporciona una mayor actividad y una actividad a largo plazo significativamente mejor hacia la electrooxidación de etanol que el nanocatalizador de Pd compatible con RGO y el negro de Pd comercial.
Métodos
Reactivos y químicos
Trihidrato de nitrato de cobre (II) (Cu (NO 3 ) 2 · 3H 2 O), cloruro de paladio (PdCl 2 ), etilenglicol (EG), etanol, polvo de grafito (S.P.), ácido sulfúrico (98% en peso de H 2 SO 4 ), permanganato de potasio (KMnO 4 ) y borohidruro de potasio (95% en peso de KBH 4 ) se adquirieron de Sinopharm Chemical Reagent Co., Ltd. Peróxido de hidrógeno (30% en peso de H 2 O 2 ) y la solución de amoníaco fueron proporcionados por Guangdong Guanghua Sci Tech Co., Ltd.Aladdin Industrial Inc. ofreció hidróxido de sodio (NaOH). Shanghai, China). El diez por ciento de Pd black fue proporcionado por HESEN Electric Co., Ltd. (Shanghai, China). El cinco por ciento en peso de solución de Nafion se obtuvo de Sigma Aldrich. Todos los productos químicos se utilizaron sin ninguna purificación adicional.
Preparación del Pd-Cu (F) / RGO
Preparación de óxido de grafeno (GO)
GO se preparó a partir de polvo de grafito según un método Hummers modificado [20].
Preparación de Pd-Cu (F) / RGO
En primer lugar, se preparó una solución mixta de 40 ml de EG y 40 ml de etanol, y se pusieron 160 mg de PVP en la solución bajo sonicación durante 30 min, luego se agregaron 0.01 mol L - 1 PdCl 2 y 0,02 mol L - 1 Cu (NO 3 ) 2 · 3H 2 O en la solución mezclada con agitación, luego agregando un cierto volumen de solución de amoníaco para ajustar el pH =10.0. A continuación, se dispersaron 30 mg de GO tal como se preparó en la solución mixta de 5 ml de EG y 5 ml de etanol en condiciones de sonicación para formar una suspensión de GO, luego se agregaron a la solución mencionada anteriormente con sonicación durante otros 60 min. Después de estos pasos, transferimos la solución de mezcla con 2 mL de KBH 4 (0,15 mg mL - 1 ) en un autoclave revestido de teflón de 50 ml y se mantuvo a 160 ° C durante 6 h. Después de enfriar a temperatura ambiente, el producto se centrifugó y se lavó varias veces con agua ultrapura y etanol. Por último, el producto se secó a 40 ° C al vacío durante la noche; el resultado se denominó Pd-Cu (F) / RGO.
También preparamos la partícula esférica Pd y Cu soportada en nanocatalizador RGO en el método similar mencionado anteriormente, mientras que la diferencia es que la solución de amoníaco fue reemplazada por Na 2 CO 3 solución. Los catalizadores obtenidos se marcaron como Pd-Cu (P) / RGO. Y el Pd (Pd / RGO) o Cu (Cu (F) compatible con RGO / RGO) también se prepararon nanocatalizadores en condiciones similares sin Cu (NO 3 ) 2 · 3H 2 O o PdCl 2 , respectivamente.
Mediciones electroquímicas
Las mediciones electroquímicas de la actividad electrocatalítica y la estabilidad de los catalizadores se realizaron en una estación de trabajo electroquímica CHI750D utilizando una celda de tres electrodos a temperatura ambiente. Se usó un electrodo de placa de platino como contraelectrodo, mientras que se usó un electrodo de calomelanos saturado (SCE) como electrodo de referencia. La preparación del electrodo de trabajo fue los siguientes pasos:2 mg de Pd-Cu (F) / Se añadió catalizador RGO a 2 ml de agua ultrapura bajo sonicación para formar una suspensión; luego, se esparcieron 10 μL de la suspensión de catalizador sobre la superficie de un electrodo de carbón vítreo (GCE, 5 mm de diámetro), que ha sido cuidadosamente pulido con alúmina y limpiado con agua ultrapura. Posteriormente, se vertieron 5 μL de solución de Nafion (5% en peso) sobre la superficie como una capa para cubrir las muestras. A modo de comparación, el Pd-Cu (P) Los catalizadores / RGO, Pd / RGO y negro de Pd comerciales también se modificaron para los electrodos en las mismas condiciones. En cada experimento, se usó nitrógeno de alta pureza para saturar el electrolito durante 30 minutos para eliminar el oxígeno.
Resultados y discusión
Se emplearon SEM y TEM para investigar el tamaño y la morfología de Pd-Cu (F) / RGO, Pd-Cu (P) / RGO, Cu (F) / RGO y catalizadores Pd / RGO. Como se muestra en la Fig. 1a, las nanopartículas de aleación de Pd-Cu están en ambos lados de la capa de grafeno. Obviamente se puede ver en la Fig. 1b, c que estos Pd-Cu (F) / Los nanocatalizadores RGO tienen una morfología similar a una flor que es diferente de la partícula Pd-Cu (P) / Nanopartículas RGO mostradas en la Fig. 1e, f. Y los tamaños de partícula promedio de estos dos catalizadores fueron de aproximadamente 80 ± 5 nm y 10 ± 2 nm, respectivamente. La morfología de Pd-Cu (F) / RGO está mucho más cerca de Cu (F) / RGO nanopartículas que se muestran en la Fig.1g en lugar de la estructura de partículas esféricas de las nanopartículas de Pd / RGO que se muestran en la Fig.1h, y esta morfología compacta jerárquica similar a una flor es tal como se informó en estudios anteriores, lo que sugiere que esta estructura es relevante para el impacto de Solución de Cu y amoniaco [21, 22]. Las nanopartículas de Pd-Cu con forma de flor sin grafeno también se fabricaron como se muestra en la Fig. 1d para afirmar el papel del grafeno en los electrocatalizadores. Se puede observar que las nanopartículas se dispersaron de manera desigual y algunas pequeñas nanopartículas se agregaron juntas. Compare con la morfología de Pd-Cu (F) / RGO, se puede concluir que el grafeno es un sustrato ideal para soportar y dispersar nanopartículas, lo cual es consistente con informes anteriores [17, 21].

SEM ( a , b ) y TEM ( c ) imágenes para Pd-Cu (F) / RGO. SEM ( d ) imagen para Pd-Cu (F) . SEM ( e ) y TEM ( f ) imágenes para Pd-Cu (P) / RGO. TEM ( g ) imagen de Cu (F) / RGO. SEM ( h ) imagen para Pd / RGO
Para investigar la distribución de elementos del Pd-Cu (F) / RGO, los espectros de espectroscopía de rayos X de dispersión de energía (EDX) se muestran en la Fig. 2a. Los resultados indicaron que las fracciones en peso de Pd y Cu de Pd-Cu (F) / RGO fue aproximadamente 1:1.4, lo que coincidió con las fracciones de peso alimenticio de Pd y Cu que fueron 1:1.3. Las fracciones de peso reales se midieron además mediante espectroscopía de emisión óptica de plasma acoplado inductivamente (ICP-OES), y el resultado del análisis reveló que Pd-Cu (F) / RGO contiene 15,8% en peso de Pd y 21,4% en peso de Cu, que era aproximadamente consistente con EDX. Los perfiles de escaneo STEM-EDS (Fig. 2b) también indicaron que los elementos Pd y Cu se cargaban en los catalizadores de manera homogénea.
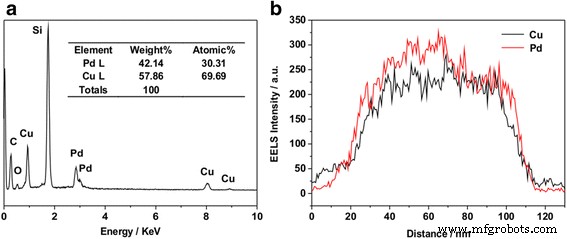
Espectros EDX ( a ) y perfiles STEM-EDS ( b ) de Pd-Cu (F) / RGO. El pico de Si proviene del sustrato de Si necesario
Los patrones XRD del Pd-Cu (F) / RGO, Pd-Cu (P) / RGO, Pd / RGO y Cu (F) Los catalizadores / RGO se presentaron en la Fig. 3. Para el Pd-Cu (P) / RGO, se detectaron tres picos de difracción a 40,1 °, 46,9 ° y 68,6 °, correspondientes a los planos de cristalito (111), (200) y (220) de Pd, que eran consistentes con los picos de Pd / RGO. Y el pico de difracción a 43,3 ° pertenece a los planos (111) del Cu, lo que sugiere la separación de fases entre Pd monometálico y Cu en Pd-Cu (P) / RGO. Las posiciones máximas del Pd-Cu (F) / RGO cambió en comparación con Pd / RGO, lo que sugiere la formación de aleaciones de Pd-Cu [12]. El experimento de control de Cu (F) / RGO sin carga de Pd muestra picos adicionales a 29,6 °, 42,4 °, 61,4 ° y 74,0 ° correspondientes a Cu 2 + 1 O (Cu 2 O con defectos de exceso de metal), lo que confirmó que el cobre se cargó en el RGO y se oxidó. Además, el pico ancho alrededor de 25 ° se detecta en cada línea, que se atribuye a los planos (002) de RGO, lo que sugiere la eliminación de los grupos funcionales que contienen oxígeno del GO [23].
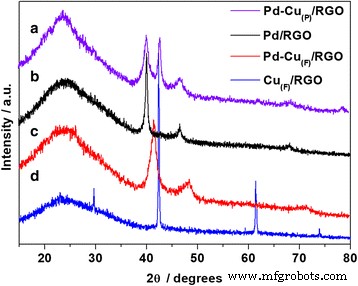
Patrones XRD del Pd-Cu (P) / RGO (curva a), Pd / RGO (curva b), Pd-Cu (F) / RGO (curva c) y Cu (F) / RGO (curva d)
Para determinar aún más la estructura, se realizó un análisis XPS para analizar los estados químicos de la superficie y los componentes de la muestra. Los espectros XPS de alta resolución de Pd 3 d , Cu 2 p regiones de Pd-Cu (F) / RGO se muestran en la Fig. 4a, b, respectivamente. El espectro XPS de Pd fue una combinación de cuatro picos que provienen de Pd a 340,6 y 335,2 eV y PdO a 341,6 y 336,2 eV [4]. En el espectro de Cu XPS, los picos de alrededor de 932,6 y 952,6 eV representaron Cu 2 p 3/2 y Cu 2 p 1/2, respectivamente. El Cu 2 p 3/2 y Cu 2 p 1/2 señales se ajustaron con seis picos que pueden deberse a Cu o Cu 2 O a 932,4 y 952,4 eV, CuO a 933,2 y 953,2 eV y Cu (OH) 2 en 934.4 y 955.2 eV, que fueron en parte consistentes con el resultado de XRD.
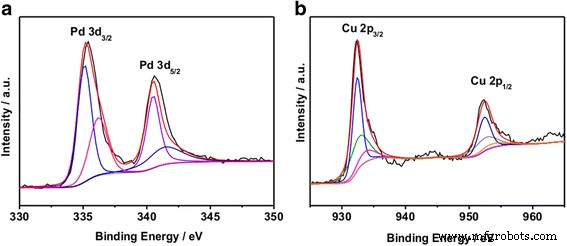
Levantamiento y espectros XPS de alta resolución de Pd 3 d ( a ) y Cu 2 p ( b ) de Pd-Cu (F) / RGO
Según los datos de XPS, propusimos el posible mecanismo de formación de la siguiente manera:En la solución de amoníaco, tanto Cu 2+ y Pd 2+ se coordinaron con el amoniaco, formando el [Cu (NH 3 ) 4 ] 2+ y [Pd (NH 3 ) 4 ] 2+ , respectivamente. Una fracción de los complejos combinada además con OH - para formar los óxidos metálicos [24], y la otra parte, se redujo en KBH 4 a nanopartículas. Durante este proceso, se formó la aleación Pd-Cu. Es posible que la adición de amoniaco favorezca la formación de la aleación Pd-Cu [25, 26]. Creemos que el PVP juega un papel crucial como agente director de la estructura durante la reducción, que es similar al sistema del Pt-Cu bajo la circunstancia del bromuro de cetiltrimetilamonio (CTAB). CTAB y PVP se utilizan generalmente para controlar la nucleación y el crecimiento de nanopartículas e influir en la velocidad de reacción, lo que da como resultado varias formas [27, 28, 29]. Mientras tanto, GO se redujo a RGO por KBH 4 y las nanopartículas de aleación de Pd-Cu en forma de flor se depositaron en el RGO debido a las fuertes interacciones entre las nanopartículas de metal u óxido metálico y los grupos funcionales de RGO [1]. El esquema de la preparación de Pd-Cu (F) Las nanoestructuras / RGO se muestran en la Fig. 5. En cuanto a Pd-Cu (P) / RGO, según los trabajos de Zhang QL et al. [1] y Lu L et al. [30], Pd 2 + y Cu 2+ se puede reducir en KBH 4 y depositado en el RGO, así como Na 2 CO 3 simplemente ajustando el pH del sistema.
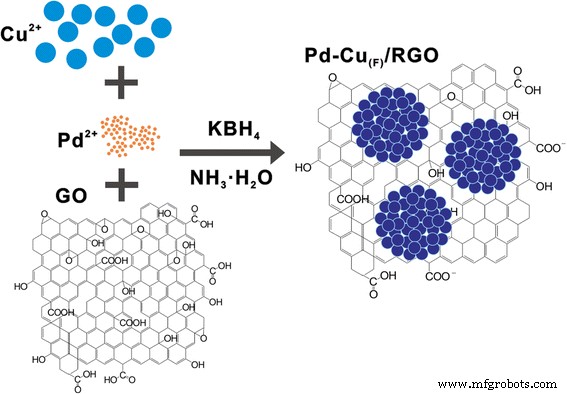
Ilustración esquemática de la preparación de Pd-Cu (F) / Nanoestructuras RGO
El análisis termogravimétrico (TGA) se realizó bajo un flujo de aire y las muestras se calentaron con una velocidad de calentamiento de 10 ° C min - 1 . El análisis se realizó en Pd-Cu (F) / RGO, Pd-Cu (P) / RGO, Pd / RGO y GO. Los resultados mostrados en la Fig.6 ilustraron que una pérdida de peso de aproximadamente el 6% de Pd-Cu (F) / RGO ocurrió entre 250 y 500 ° C, mientras que la pérdida de peso de Pd-Cu (P) / RGO fue de alrededor del 14% y Pd / RGO fue de alrededor del 22%. La pérdida de peso de los productos en una atmósfera de aire a alta temperatura probablemente se debió a la eliminación de los grupos funcionales restantes que contienen oxígeno. La pérdida de peso significativa de GO, alrededor del 28% entre 100 y 300 ° C, se debió principalmente a la eliminación de grupos funcionales que contienen oxígeno, al igual que C – O y C =O. Y la pérdida de peso dentro de los 100 ° C que provino del escape de moléculas de agua entre las nanohojas RGO, así como la pérdida de peso por encima de 500 ° C, se debió a la combustión del esqueleto de carbono [27, 31, 32]. El resultado indicó la eliminación de los grupos funcionales que contienen oxígeno en Pd-Cu (P) / RGO y Pd-Cu (F) / RGO, que confirma además que GO se redujo eficientemente a RGO durante la síntesis [23].
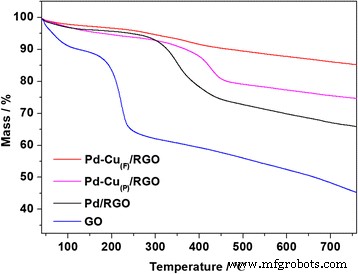
Curvas TGA de Pd-Cu (F) / RGO, Pd-Cu (P) / RGO, Pd / RGO y GO de 40 a 780 ° C en atmósfera de aire
Para evaluar el rendimiento de estos catalizadores para la electrooxidación de etanol en medio alcalino, se investigó el comportamiento electroquímico de estos catalizadores mediante voltamogramos cíclicos (CV) en solución de NaOH 0,5 M sin y con C 2 0,5 M H 5 OH. Los CV medidos en un N 2 -Solución de NaOH 0,5 M saturada a una velocidad de barrido de 50 mV s - 1 se muestran en la Fig. 7a. Las medidas de CV se realizaron entre - 0,8 y 0,2 V (vs.SCE), y los picos de - 0,2 a 0 V fueron aportados por la formación de especies oxigenadas en la superficie del Pd, y los picos entre - 0,4 y - 0,2 V se debieron principalmente a la reducción de PdO, que puede liberar sitios superficiales para la oxidación del etanol [2]. El área de superficie activa electroquímica (ECSA) se calculó mediante el área integral de la reducción de PdO. El ECSA se estimó en 151,90 m 2 g - 1 Pd para el Pd-Cu (F) / RGO, que era más grande que el de Pd-Cu (P) / RGO (123,36 m 2 g - 1 Pd), Pd / RGO (102,66 m 2 g - 1 Pd) y Pd negro (88,10 m 2 g - 1 Pd).
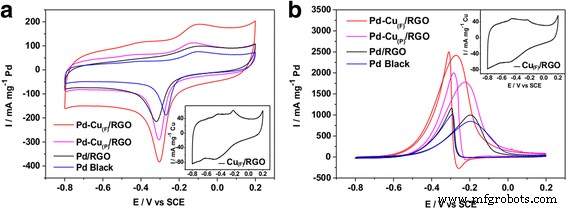
Voltamogramas cíclicos del Pd-Cu (F) / RGO, Pd-Cu (P) / RGO, Pd / RGO y Pd negro. Gráficos de CV en NaOH 0,5 M ( a ) y NaOH 0,5 M + C 2 0,5 M H 5 OH ( b ) a una velocidad de escaneo de 50 mV s - 1 . Las imágenes insertadas son los gráficos de voltamogramas cíclicos de Cu (F) / RGO en NaOH 0,5 M ( a ) y NaOH 0,5 M + C 2 0,5 M H 5 OH ( b ) a una velocidad de escaneo de 50 mV s - 1
Los CV de Pd-Cu (F) / RGO, Pd-Cu (P) / RGO, Pd / RGO y Pd negros en un N 2 saturado 0,5 M NaOH + 0,5 M C 2 H 5 La solución de OH se muestra en la Fig. 7b. La corriente de oxidación del etanol de Pd-Cu (F) / RGO (2416,25 mA mg - 1 Pd) fue más alta que la de Pd-Cu (P) / RGO (1779,09 mA mg - 1 Pd), y mucho más alto que Pd / RGO (997.70 mA mg - 1 Pd) y Pd negro (847,4 mA mg - 1 Pd), que significa Pd-Cu (F) / RGO tuvo una alta actividad de oxidación de etanol. También hubo diferentes potenciales de inicio de oxidación de etanol entre los cuatro catalizadores. El potencial de aparición de Pd-Cu (F) / RGO fue más negativo que el de Pd-Cu (P) / RGO aunque mucho más negativo que el de Pd / RGO y Pd black. Esta observación implicaba que las moléculas de etanol se pueden oxidar más fácilmente en Pd-Cu (F) / RGO. Podemos concluir que los catalizadores en forma de flor tal como se prepararon tuvieron un mejor desempeño electroquímico que los catalizadores sintéticos de partículas esféricas.
Para revelar el papel de Cu en el Pd-Cu (F) / RGO, un experimento de control de Cu (F) / RGO sin carga de Pd se realizó en las mismas condiciones. Como se muestra en el recuadro de la Fig. 7a, b, no hubo un pico obvio de oxidación de etanol en la talla CV de Cu (F) / RGO en 0,5 M NaOH + 0,5 M C 2 H 5 OH. Este resultado fue coherente con los informes anteriores [4, 12]. Las actividades electrocatalíticas ignorables hacia la oxidación del etanol de Cu (F) / RGO sugirió que el Pd actuaba como los sitios activos para la oxidación electrocatalítica hacia la electrooxidación del etanol, y la formación de la aleación Pd-Cu puede mejorar aún más la actividad electrocatalítica [33]. El papel de Cu en el Pd-Cu (F) / RGO en la reacción de electrooxidación puede explicarse por efecto bifuncional [12]. Cu es un átomo donante de electrones, mientras que Pd es un aceptor de electrones. El centro de la banda d se desplaza cuando se realiza la aleación entre Pd y Cu, y este fenómeno puede aumentar la oxidación electrocatalítica [18, 34, 35]. Por tanto, la formación de la aleación Pd-Cu favorecerá la electrooxidación del etanol. También es interesante que el cambio de morfología de una partícula a una estructura jerárquica similar a una flor también mejora aún más la electroactividad, que se debe principalmente a la gran superficie y al aumento del número de sitios catalíticos activos [36].
La prueba de durabilidad de estos cuatro catalizadores se midió en un N 2 saturado 0,5 M NaOH + 0,5 M C 2 H 5 Solución de OH durante 3000 sa un potencial de - 0.35 V, como se muestra en la Fig. 8. Debido a la formación de las especies intermedias, las corrientes iniciales cayeron rápidamente al principio [1], y la tasa de desintegración del Pd-Cu (F) / RGO fue significativamente más pequeño que el de Pd-Cu (P) / RGO. La corriente final después de 3000 s de Pd-Cu (F) / RGO fue mucho más alto que el de Pd-Cu (P) / RGO, Pd / RGO y Pd negro en las mismas condiciones, y los valores de densidad de corriente se enumeraron en la Tabla 1. Estos resultados ilustraron la actividad electrocatalítica a largo plazo más alta de Pd-Cu (F) / RGO entre los catalizadores investigados, lo que sugirió que la formación de una morfología jerárquica similar a una flor y la aleación mejoran significativamente la estabilidad de los catalizadores hacia la electrooxidación del etanol.
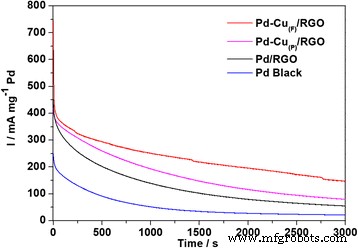
yo - T curvas del Pd-Cu (F) / RGO (curva a), Pd-Cu (P) / RGO (curva b), Pd / RGO (curva c) y Pd negro (curva d) en 0,5 M NaOH + 0,5 M C 2 H 5 OH hasta 3000 sa 25 ° C
Conclusiones
En resumen, desarrollamos un enfoque de síntesis en un solo recipiente para la preparación de un novedoso nanocatalizador de aleación de Pd-Cu similar a una flor y jerárquico apoyado en grafeno convertido químicamente. Se encuentra que la adición de solución de amoníaco durante la preparación de nanocatalizadores ofrece la oportunidad de ajustar la morfología de los nanocatalizadores e influir en la formación de la aleación, los cuales conducen a una actividad electrocatalítica altamente mejorada hacia la oxidación del etanol en medio alcalino y mejor a largo plazo. estabilidad de término de la estructura jerárquica similar a una flor de Pd-Cu (F) / RGO que el del Pd-Cu (P) / Catalizadores negros RGO, Pd / RGO y Pd. La actividad electrocatalítica y la durabilidad significativamente mejoradas que se benefician de la morfología jerárquica similar a una flor y la aleación de Pd-Cu sugieren que el Pd-Cu (F) / RGO podría estar prometiendo un electrocatalizador para la oxidación del etanol en DEFC, revelando el gran potencial del diseño de la estructura de los materiales de soporte para la fabricación futura de nanocatalizadores.
Abreviaturas
- Cu:
-
Cobre
- CV:
-
Voltamogramas cíclicos
- DEFC:
-
Pilas de combustible de etanol directo
- ECSA:
-
Área de superficie activa electroquímica
- GCE:
-
Electrodo de carbono vítreo
- GO:
-
Óxido de grafeno
- ICP-OES:
-
Espectroscopía de emisión óptica de plasma acoplado inductivamente
- Pd:
-
Paladio
- RGO:
-
Óxido de grafeno reducido
- SCE:
-
Electrodo de calomelanos saturado
- SEM:
-
Microscopía electrónica de barrido
- TEM:
-
Microscopio electrónico de transmisión
- TGA:
-
Análisis termogravimétrico
- XPS:
-
Espectrómetro de fotoelectrones de rayos X
- XRD:
-
Difracción de rayos X
Nanomateriales
- El grafeno pone los nanomateriales en su lugar
- Grafeno en altavoces y auriculares
- Nanocinta de grafeno
- Células solares de grafeno de alta eficiencia
- Síntesis verde en un recipiente de microesferas de SnO2 decoradas con Ag:un catalizador eficiente y reutilizable para la reducción de 4-nitrofenol
- Síntesis y actividad de oxidación del CO de óxido binario mixto 1D CeO2-LaO x catalizadores de oro soportados
- Síntesis de calentamiento de estado sólido de compuesto de poli (3,4-etilendioxitiofeno) / oro / grafeno y su aplicación para la determinación amperométrica de nitrito y yodato
- Síntesis en un solo recipiente de nanoplacas de Cu2ZnSnSe4 y su actividad fotocatalítica impulsada por la luz visible
- Evaluación de estructuras de grafeno / WO3 y grafeno / ceO x como electrodos para aplicaciones de supercondensadores
- Síntesis fácil y respetuosa con el medio ambiente de nanocables de Co3O4 y su prometedora aplicación con grafeno en baterías de iones de litio
- Síntesis sonoquímica de un solo paso y propiedades fotocatalíticas fáciles de compuestos de puntos cuánticos de grafeno / Ag3PO4



