La escoria de alto horno y su papel en la operación del horno
La escoria de alto horno y su papel en la operación del horno
La importancia de la escoria de alto horno (BF) para lograr un funcionamiento sin problemas del BF se ilustra con el viejo dicho "si se ocupa de la escoria, el horno se encargará del resto". Se ha realizado una gran cantidad de trabajo en la escoria BF estudiando las propiedades, los mecanismos de formación y los impactos en las operaciones del horno. Una escoria de buena calidad es necesaria para producir metal caliente de buena calidad en el BF.
Se requiere la práctica de escoria BF para cumplir con ciertos requisitos para una operación BF eficiente. Estos requisitos incluyen (i) debe absorber todos los componentes no volátiles no reducidos de la carga y eliminarlos del BF, (ii) debe ser líquido de baja viscosidad, (iii) debe poder absorber el azufre contenido principalmente en los combustibles, (iv) debe contener la menor cantidad posible de óxido de hierro para aumentar el rendimiento del metal caliente, (v) su volumen debe ser lo más bajo posible sin afectar la desulfuración, ( vi) el rango de temperatura en el que los componentes de la carga se vuelven cohesivos debe ser estrecho para garantizar una mejor permeabilidad de la columna de carga, y (vii) su calidad debe ser tal que pueda procesarse en material vendible. Estos requisitos son en parte complementarios y en parte mutuamente excluyentes. Por lo tanto, es necesario establecer prioridades.
Afortunadamente, existen relaciones generales que brindan una visión más práctica de la naturaleza de las escorias que se pueden usar a diario. Sin embargo, es importante tener una comprensión básica de la naturaleza fundamental de la escoria BF para comprender las relaciones generales.
Fundamentos de escoria BF
Los fundamentos de la escoria BF son complejos. Con alrededor del 40 %, el oxígeno es el elemento individual más grande en la escoria. La escoria es, por tanto, un sistema de óxido y de naturaleza iónica. Debido a la naturaleza del proceso BF, la formación de escoria es un proceso de varios pasos que implica cambios considerables en la composición y la temperatura. Los cuatro componentes principales de la escoria BF son SiO2 (sílice), CaO (cal), MgO (magnesia) y Al2O3 (alúmina). Estos cuatro componentes de la escoria BF forman numerosos compuestos que dan como resultado una amplia gama de propiedades químicas y físicas. Los componentes menores de la escoria son de particular interés con respecto a la química del metal caliente y el control del horno se suman a la complejidad de las propiedades fisicoquímicas de la escoria.
Los fundamentos de la escoria BF incluyen cuestiones relacionadas con el proceso BF. Estos temas incluyen la formación de escoria, el flujo en el hogar, la estructura molecular de la escoria y cómo la estructura relaciona los índices químicos conocidos como basicidad, solidificación de la escoria y el impacto de los cambios del estado térmico del horno en la composición de la escoria.
Formación de escoria – BF es un reactor de lecho empacado, gas-sólido-líquido, presurizado, intercambiador de calor a contracorriente, a reflujo. Tiene tres funciones principales, a saber (i) la reducción de óxidos de hierro a hierro metálico (ii) la fusión del hierro metálico y los óxidos, lo que proporciona (iii) la separación de las impurezas de la carga y el combustible del hierro líquido. Estas características del proceso conducen a la división del horno en tres zonas verticales con respecto a las escorias (i) a saber (i) zona granular, (ii) zona de formación de escoria y (iii) zonas de solera. Estas tres zonas y algunas reacciones específicas para cada zona se muestran en la figura 1.
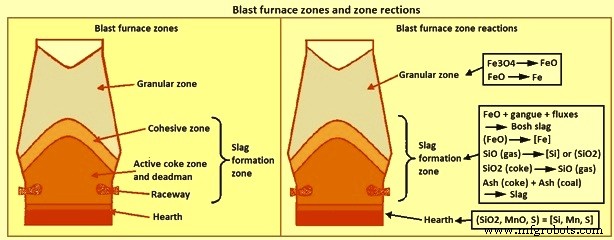
Fig. 1 Zonas de alto horno y reacciones de zona
La zona granular se ubica en la parte superior del horno donde todos los componentes cargados se encuentran en fase sólida. La zona granular está delimitada por la línea de stock en la parte superior y por el inicio de la formación de fases líquidas, la zona cohesiva, en la parte inferior. A medida que la carga desciende por la zona granular, es calentada por los gases de la parte inferior del horno y se realiza una parte de la reducción de los óxidos de hierro. La cantidad de reducción que ocurre en la zona granular es una función de la naturaleza de los materiales que contienen hierro, la distribución de la carga y la composición del gas y los patrones de flujo.
La zona de formación de escoria comienza en la zona cohesiva, donde comienza el ablandamiento de la carga, y continúa hasta debajo de la elevación de la tobera. Por lo tanto, la zona de formación de escoria incluye la zona cohesiva, la zona de coque activo, el hombre muerto y el camino de rodadura. La escoria formada en la parte superior de la zona de formación de escoria se denomina escoria "bosh" o "primaria", y la escoria que sale de la zona inferior es la escoria "de solera". Normalmente se supone que la escoria primaria está formada por todos los componentes de la escoria de carga, incluidos los óxidos de hierro no reducidos en la zona granular, pero no incluye las cenizas del coque o el carbón inyectado. La composición de la escoria cambia a medida que desciende en el horno debido a la absorción de las cenizas de coque y carbón, azufre y silicio del gas y la reducción del óxido de hierro. La temperatura de la escoria aumenta del orden de 500 ºC a medida que desciende hasta la altura de la tobera. Estos cambios en la composición y la temperatura pueden afectar considerablemente las propiedades físicas de la escoria, específicamente la temperatura de liquidus y la viscosidad.
La tercera zona es la capa de escoria en la solera del horno. La escoria producida en la zona de formación de escoria se acumula en la capa de escoria, llenando los vacíos en el coque del hogar y 'flotando' en la capa de metal caliente. El metal caliente pasa a través de la capa de escoria para llegar a la capa de metal caliente. La gran área superficial entre el metal caliente y la escoria cuando el metal caliente pasa a través de la capa de escoria mejora la cinética de las reacciones químicas. Estas reacciones dan como resultado cambios considerables en la química del metal caliente. En particular, los contenidos de [Si] y [S] antes de entrar en la capa de escoria son mucho más altos que los de la capa de metal caliente. La formación de escoria en la zona de formación de escoria es muy específica del horno debido al impacto de las propiedades de la carga y la operación del horno.
Estructura de escoria – La conceptualización de la estructura de la escoria (Fig. 2) se basa en la estructura formada por la sílice. A nivel molecular, el átomo de silicio está ubicado en el centro de un tetraedro rodeado por cuatro átomos de oxígeno, un átomo de oxígeno en cada esquina del tetraedro, como se muestra en la figura 2a. Cada átomo de oxígeno está unido a dos átomos de silicio y, por lo tanto, cada átomo de oxígeno es una esquina de dos tetraedros. El intercambio de átomos de oxígeno da como resultado un polímero o red en tres dimensiones en estado cristalino donde se comparten todas las esquinas (Fig. 2b). A medida que se calienta la sílice, algunos de los enlaces de las esquinas se rompen, pero la naturaleza polimérica de la estructura se mantiene incluso cuando se funde, como se muestra en la Fig. 2c.
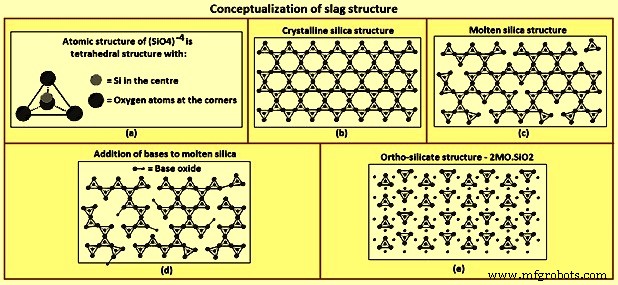
Fig. 2 Conceptualización de la estructura de la escoria
La adición de óxidos metálicos, como CaO y MgO, rompe la estructura del polímero. Estos óxidos actúan como donantes de oxígeno, reemplazando un átomo de oxígeno en una esquina de un tetraedro y rompiendo el enlace de la esquina de tetraedro a tetraedro (Fig. 2d). La descomposición de la estructura del polímero continúa con la adición de más óxidos metálicos hasta que la proporción molar de óxidos metálicos a sílice es igual a dos, momento en el que se rompen todos los enlaces de las esquinas de tetraedro a tetraedro (Fig. 2e). La relación molar de dos es la composición de ortosilicato, 2CaO-SiO2, 2MgO-SiO2 y CaO-MgO-SiO2. Al2O3 actúa de manera similar al SiO2 al formar polímeros y aceptar átomos de oxígeno de óxidos básicos. Los óxidos que aceptan oxígeno, SiO2 y Al2O3, se denominan óxidos ácidos. Los óxidos que donan oxígeno, CaO y MgO se denominan óxidos básicos.
Basicidad de la escoria – Es muy útil cuando se relacionan las propiedades de un sistema de múltiples componentes con su composición para desarrollar un índice basado en la composición. El problema al desarrollar un índice es cómo reflejar la importancia de cada componente del sistema en el índice. La diferente naturaleza de los óxidos ácidos (A) y los óxidos básicos (B) se ha utilizado en el desarrollo de índices de composición de escorias, normalmente denominados basicidades. Ejemplos de índices de basicidad que se han desarrollado son (i) exceso de bases ={(CaO) + (MgO)} – {(SiO2) + (Al2O3)}, (ii) basicidad (B/A) ={(CaO) + (MgO)} / {(SiO2) + (Al2O3)}, (iii) relación de campana ={(CaO) + 0.7(MgO)} / {0.94(SiO2)+ 0.18(Al2O3)}, y (iv) basicidad óptica ={(CaO) + 1,11(MgO) + 0,915(SiO2) + 1,03 (Al2O3)} / {(CaO) + 1,42(MgO) + 1,91(SiO2) + 1,69(Al2O3)}.
Los índices de basicidad se pueden agrupar en categorías generales, a saber (i) diferencias entre la cantidad de bases y ácidos, como se muestra en la ecuación (i) anterior, (ii) relaciones de bases a ácidos basadas en los porcentajes en peso, como se muestra en la ecuación (ii) anterior, (iii) proporciones de bases a ácidos basadas en las concentraciones molares, como se muestra en la ecuación (iii) anterior, y (iv) suma de la basicidad de cada componente y su concentración molar, como se muestra en la ecuación (iv) anterior. Como era de esperar en base a la descripción anterior de la estructura de la escoria, aquellos índices que reflejan la naturaleza molecular de la composición de la escoria, las ecuaciones (iii) y la ecuación (iv) tienden a ser mejores predictores de las propiedades de la escoria. Sin embargo, como el índice definido por la ecuación (ii) es probablemente la definición más utilizada.
Impacto de la temperatura:[Si], basicidad y volumen de escoria – Hay un aumento de la cantidad de [Si] con el aumento de la temperatura del metal caliente en el BF, como se muestra en la Fig. 3. La cantidad de aumento de [Si] para un aumento de temperatura dado varía de un horno a otro, pero la tendencia es la Lo mismo para todos los hornos. A medida que aumenta el [Si], el (SiO2) disminuye y, por lo tanto, aumenta la basicidad y disminuye el volumen de escoria. La cantidad de aumento en la basicidad para un aumento específico en [Si] es una función del volumen de escoria. La Fig. 3a muestra el cambio en B/A para volúmenes iniciales de escoria de 200 kg/tHM (kilogramos por tonelada de metal caliente) y 300 kg/tHM y para la relación entre [Si] y la temperatura del metal caliente que se muestra en la figura. La tendencia normal demostrada aquí es que cuanto mayor es el volumen de escoria, menor es el cambio en B/A para el mismo cambio en [Si] o temperatura del metal caliente.
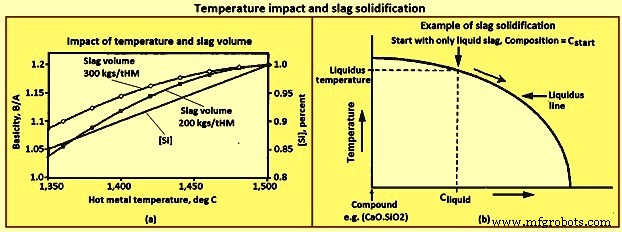
Fig. 3 Impacto de la temperatura y solidificación de la escoria
Solidificación de escorias – La definición común de temperatura de fusión solo se aplica a un sistema de un solo componente como el agua, donde solo existe agua líquida por encima de la temperatura de fusión y solo existe agua sólida por debajo de la temperatura de fusión. La escoria es un sistema de múltiples componentes y, por lo tanto, no tiene la definición común de temperatura de fusión excepto en composiciones específicas. La mayoría de las composiciones de escoria tienen fases tanto sólidas como líquidas presentes en un rango de temperaturas. La temperatura más baja a la que solo existe la fase líquida para una composición específica se denomina temperatura de liquidus.
La figura 3b muestra la ruta de solidificación de una escoria ilustrada en el diagrama de fase simplificado. Comience con escoria de composición C. Comience a temperaturas en las que solo exista escoria líquida. A medida que la escoria se enfría, moviéndose verticalmente hacia abajo en el diagrama, la composición de la escoria líquida no cambia hasta la intersección con la 'línea liquidus'. La intersección con la 'línea de liquidus' es la temperatura de liquidus para la composición Cstart. Una cantidad muy pequeña del compuesto sólido se forma a la temperatura de liquidus de la izquierda. Tres cambios continúan a medida que la temperatura se reduce aún más por debajo de la temperatura liquidus, a saber (i) se forma más compuesto sólido, (ii) la cantidad de escoria líquida disminuye, y (iii) la composición de la escoria líquida cambia, moviéndose hacia el justo a lo largo de la 'línea liquidus'. En el ejemplo, donde el compuesto formado es 2CaO.SiO2, la basicidad de la escoria líquida disminuye a medida que la escoria se enfría, ya que 2CaO.SiO2 contiene aproximadamente el doble de CaO que de SiO2.
La ruta de solidificación muestra cómo se puede formar un compuesto incluso cuando la composición de la escoria líquida es considerablemente diferente a la composición del compuesto. La relación en peso de CaO a SiO2 =1,86 para el compuesto de silicato dicálcico, 2CaO.SiO2. Si bien nunca se ha operado con éxito ningún BF utilizando escorias con un CaO a SiO2 cercano a 1,86, se pueden formar cantidades considerables de silicato dicálcico en las escorias de los BF operativos. La formación de suficiente silicato dicálcico da como resultado una escoria sólida que se descompone en polvo al enfriarse, conocida como escoria de "caída" o "polvo". La ruptura es causada por la expansión del volumen del 10 % del silicato dicálcico a medida que pasa por un cambio de fase a 675 °C. La pauta indicada para evitar una escoria 'caída' es (CaO) inferior a 0,9 (SiO2) + 0,6( A2O3) + 1,75(S).
Es importante recordar que los diagramas de fase se basan en condiciones de equilibrio. Las condiciones de equilibrio implican que la velocidad de enfriamiento es lenta en relación con la velocidad de las reacciones, como la formación de silicato dicálcico. La ruta de solidificación descrita anteriormente se "pasa por alto" si la velocidad de enfriamiento es muy alta, como en la granulación de escoria y, en menor medida, en la peletización de escoria. El enfriamiento rápido bloquea la composición en una fase de vidrio sólido, donde la cinética de las reacciones es demasiado lenta para que se formen los compuestos.
Flujo de escoria en el hogar – El control del nivel de escoria en el hogar es importante para mantener un funcionamiento estable del horno, especialmente porque se han incrementado las tasas de producción de metal caliente. Los altos niveles de escoria dan como resultado un aumento de la presión de explosión y el trabajo de la pared de bosh, e interrumpen el descenso uniforme de la carga. Uno de los problemas en el control del nivel de escoria es el flujo de escoria en el hogar durante la extracción. En el hogar, el flujo de escoria al orificio del grifo es más difícil que el flujo de metal caliente al orificio del grifo. El flujo de metal caliente tiene una fuerza impulsora mayor debido a la mayor densidad del metal caliente en comparación con la escoria. Se cree que la ruta del flujo de metal caliente es principalmente a través de regiones "libres de coque" debajo y/o alrededor del coque muerto. La ruta del flujo de escoria hacia el orificio del grifo es a través del coque de hombre muerto.
La figura 4 muestra la configuración de la solera y una posible secuencia de etapas de la solera durante la sangría que conducen a una falsa condición de solera seca al final de la sangría. Se cree que la superficie del metal caliente permanece relativamente plana en toda el área de la solera durante la sangría debido a la alta densidad del metal caliente y al camino "sin coque" hacia el orificio de la llave. La superficie de la escoria puede ser considerablemente más baja en la región alrededor del orificio del grifo que en otras regiones del hogar. Cuando la tasa de extracción de la escoria es más alta que la tasa de flujo de la escoria a través del hogar hacia la región del orificio del grifo, se produce un agotamiento de la escoria en la región del orificio del grifo y la superficie de la escoria comienza a curvarse hacia el orificio del grifo como se muestra en el paso 4 de Fig. 4. El agotamiento de la escoria continúa hasta que no hay escoria en el orificio del grifo y el horno parece estar seco cuando aún queda una cantidad considerable de escoria en el hogar, como se muestra en el paso 5 de la Fig. 4. Minimización de la resistencia al flujo de escoria en el hogar minimiza la escoria que queda en el hogar al final de un colado. La resistencia al flujo de escoria en el hogar se reduce a medida que aumenta la porosidad del lecho de coque del hogar y se reduce la viscosidad de la escoria.
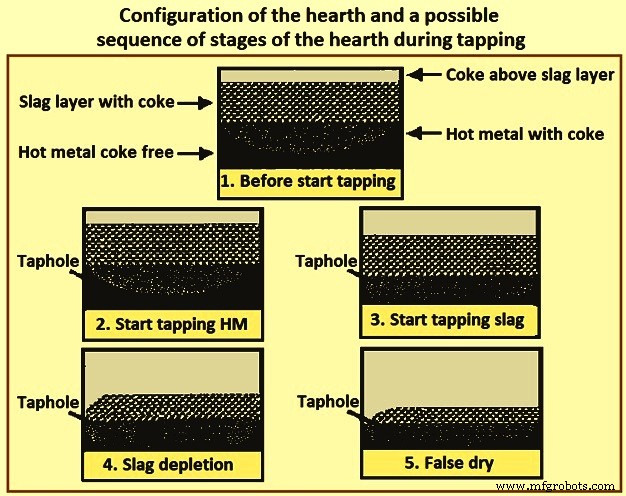
Fig. 4 Configuración del hogar y una posible secuencia de etapas del hogar durante la extracción
Sistema de óxido
Alrededor del 95 % de la escoria consiste en SiO2, CaO, MgO y Al2O3. El requisito de baja viscosidad se puede cumplir con una variedad de componentes en este sistema cuaternario. Ignorando la presencia de MgO, el diagrama de fase del sistema de óxido ternario CaO-Al2O3-SiO2 (Fig. 5) muestra una región de baja temperatura de fusión que es paralela al binario CaO-SiO2 con bajo contenido de Al2O3. Esta región se extiende desde un alto contenido de SiO2 hasta la isoterma de saturación para 2CaO.SiO2 y luego, para un contenido de CaO esencialmente constante, hacia un alto contenido de Al2O3. El contenido de MgO de la escoria no afecta sustancialmente la posición relativa de la región de baja temperatura de fusión y solo afecta los valores absolutos de las temperaturas de fusión.
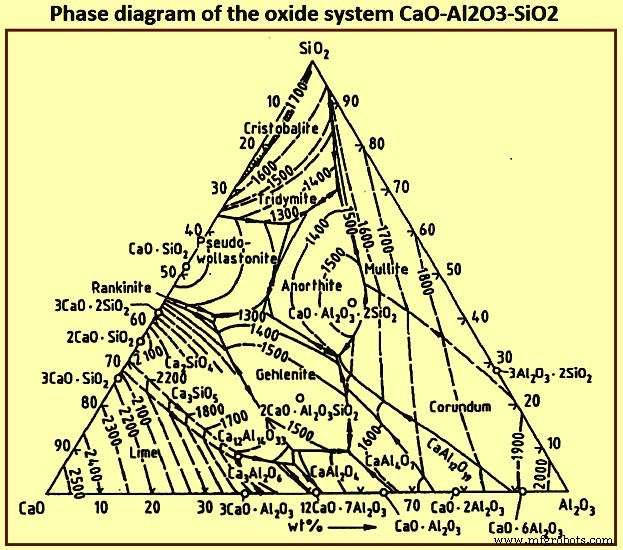
Fig. 5 Diagrama de fase del sistema de óxido CaO-Al2O3-SiO2
El sistema de óxidos que forma la base de las escorias BF es el sistema cal-sílice-alúmina (CaO-SiO2-Al2O3) modificado debido a la presencia de cierto porcentaje de MgO en la escoria. La figura 6 muestra el diagrama de fase del sistema CaO-Al2O3-SiO2-10 % MgO.
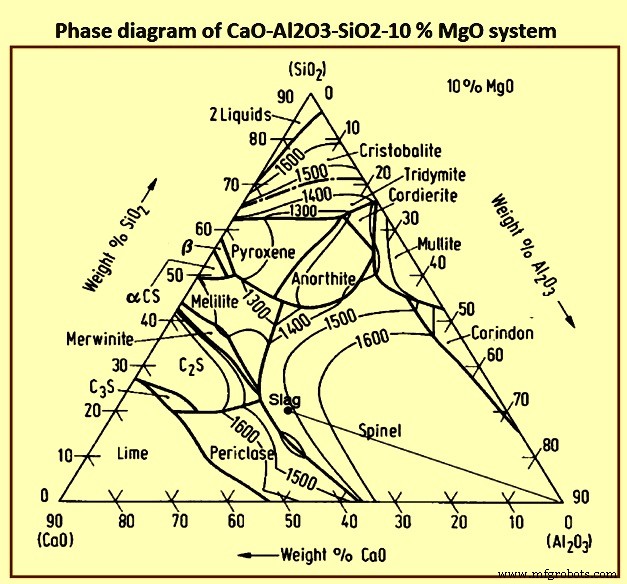
Fig. 6 Diagrama de fase del sistema CaO-Al2O3-SiO2-10 % MgO
En la Fig. 7 se muestran las composiciones de las escorias BF encontradas en varias condiciones de operación. La desulfuración del metal caliente aumenta con la basicidad de la escoria, es decir, con el aumento del contenido de CaO y/o MgO, la región 1 en la Fig. 7 puede, por lo tanto, usarse solo para procesamiento de baja carga de azufre. Dado que los constituyentes de la ganga normalmente forman una escoria de baja basicidad, la región 1 representa en gran medida la composición de la escoria sin adición de fundentes. El horno puede funcionar a una temperatura relativamente baja debido a los bajos puntos de fusión. La región 2 se alcanza para la carga de bajo contenido de hierro con constituyentes de ganga ácida. Este modo de operación prevalece y necesita una extensa desulfuración del metal caliente fuera del BF. El logro de una basicidad que resulte en una desulfuración adecuada dentro del horno necesita una gran adición de cal (CaO) que conduce a un alto volumen de escoria y por lo tanto a una mayor tasa de coque. La Región 3 representa las composiciones de escoria preferidas en todo el mundo para altos hornos grandes. En este caso, dependiendo del contenido de alúmina, se debe agregar dolomita para satisfacer los contenidos de MgO necesarios.
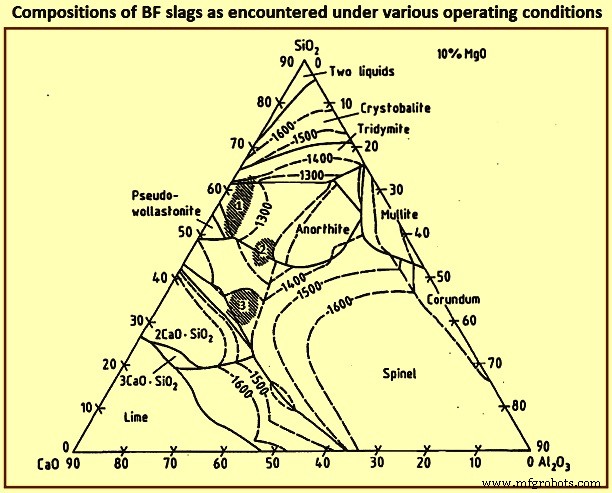
Fig. 7 Composiciones de escorias BF encontradas en varias condiciones de operación
La pestaña 1 muestra los componentes óptimos de la escoria BF. Las escorias con basicidades más altas (B) como se muestra en la pestaña 1 favorecen las condiciones óptimas de ablandamiento. El rango de ablandamiento y fusión de los constituyentes de la ganga es de alrededor de 80 °C a 130 °C para B =0,5, y alrededor de 20 °C a 50 °C para B =2. Debido a la temperatura de fusión más alta de la escoria altamente básica y de energía adicional necesaria debido a la mayor cantidad de adición de fundente, la basicidad de la escoria se mantiene por lo tanto en torno a 1,2.
| Tab 1 Composición óptima de la escoria BF | |||
| Al2O3 | CaO | MgO | SiO2 |
| % | % | % | % |
| 5 | 43 | 16 | 36 |
| 10 | 44 | 14 | 32 |
| 15 | 44 | 12,5 | 28,5 |
| 20 | 45 | 11 | 24 |
| 25 | 48 | 8 | 19 |
| 30 | 56 | 5 | 9 |
| 35 | 54 | 4 | 7 |
Propiedades de la escoria
Las propiedades físicas y químicas de las escorias son principalmente una función de la composición y temperatura de la escoria. A continuación se describen estas relaciones con el fin de desarrollar tendencias generales.
Temperaturas de líquidos – Las relaciones de temperatura de liquidus y composición de los cuatro componentes principales de la escoria se representan en un diagrama de fase cuaternario. La figura 8 se ha generado a partir de planos ternarios del diagrama de fase cuaternario. Las figuras 8a y 8b no son diagramas de fase. Hay dos tendencias generales derivadas de estas cifras. La primera es que las temperaturas de liquidus aumentan con aumentos en (Al2O3) y B/A, y la segunda es que el (MgO) en el rango de 8 % a 14 % tiende a minimizar el aumento de temperatura de liquidus causado por el aumento de ya sea (Al2O3) o B/A.
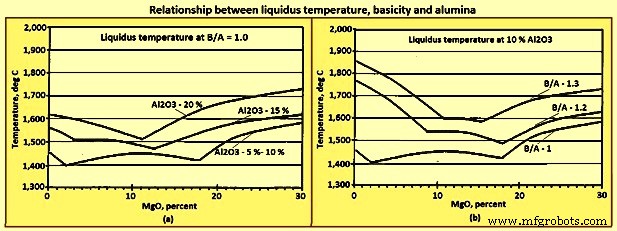
Fig. 8 Relación temperatura de liquidus, basicidad y alúmina
Viscosidad – La viscosidad es una medida de la cantidad de fuerza necesaria para cambiar la forma de un material y se informa en una unidad llamada 'poise'. Cuanto mayor sea la viscosidad, más fuerza se necesita para hacer que fluya un líquido. A efectos de comparación, considerando que a 20 ºC la viscosidad del agua es de 0,01002 poise, una viscosidad de escoria aceptable típica es de alrededor de 2 a 5 poise, y la viscosidad del SiO2 líquido es del orden de 100.000 poise. La alta viscosidad del SiO2 líquido es causada por la estructura del polímero. La descomposición de la estructura del polímero por los óxidos básicos reduce la viscosidad. La disminución de la viscosidad de todas las escorias líquidas al aumentar el B/A se muestra en la figura 9a. En general, la viscosidad de cualquier mezcla líquido/sólido aumenta a medida que aumenta la cantidad de sólidos en suspensión. El impacto de la temperatura en la viscosidad de la escoria es considerablemente mayor a temperaturas por debajo de la temperatura de liquidus que por encima de la temperatura de liquidus, como se muestra en la figura 9b.
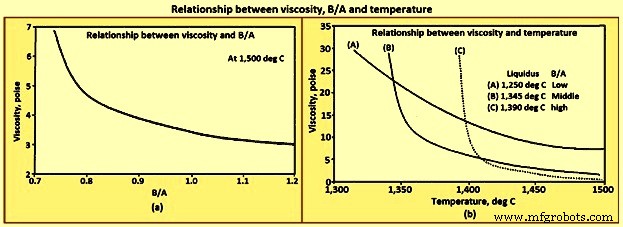
Fig. 9 Relación entre viscosidad, B/A y temperatura
Hay dos tendencias generales que se observan para la viscosidad. Por encima de la temperatura de liquidus, la viscosidad de las escorias líquidas disminuye al aumentar la temperatura y B/A. A temperaturas por debajo de la temperatura liquidus, la viscosidad disminuye con el aumento de la temperatura y la disminución de B/A.
Proporción de partición de azufre – La ferrería BF es un muy buen proceso de desulfuración en comparación con el proceso siderúrgico por la diferencia en el potencial de oxígeno de las escorias de los procesos. El efecto del potencial de oxígeno en la desulfuración se puede mostrar mediante la ecuación (CaO) + [S] =(CaS) + (FeO), donde el potencial de oxígeno se indica mediante (FeO). Cuanto mayor sea el (FeO), más se desplazará la reacción hacia la izquierda y mayor será la [S]. Las escorias siderúrgicas con (FeO) del 15 % al 25 % son, por tanto, escorias de desulfuración más débiles que las escorias de solera BF con (FeO) inferior al 1 %.
Esencialmente, todo el azufre en el BF sale del horno en el metal caliente y la escoria. Se puede desarrollar una relación para la predicción de [S] basada en un balance de masa de azufre para una tonelada de metal caliente, según la ecuación (i) a continuación, y el término definido partición de azufre según la ecuación (ii) a continuación. La predicción de [S], por la ecuación (iii) a continuación, se deriva de la sustitución de [S] de la ecuación (i) en la ecuación (ii) y luego resolviendo para [S].
La ecuación (i) es St =[S] /100 x 1,010 + (S) /100 x Svol donde 1,010 son los kg de metal caliente en una tonelada de metal caliente, incluida una pérdida de rendimiento del 1 %, St es la carga de azufre que es el peso total de azufre en kgs/tHM. Svol es el volumen de escoria que es el peso de la escoria en kgs/tHM. Ecuación (ii) Sp =(S) /[S] donde Sp es la relación de partición de azufre. La ecuación (iii) es [S] =St x 100 / (Sp x Svol + 1010).
La escoria Sp se puede predecir con base en la ecuación (iv) Sp =147.7 x BB + 37.7 x [Si] – 190 y la ecuación (v) BB ={(CaO) + 0.7(MgO)} / {0.94(SiO2) + 0.18 (Al2O3)}. Aquí BB es la basicidad definida por la relación de la campana. Cabe señalar que los coeficientes de la ecuación (iv) se han desarrollado a partir del análisis de regresión de un horno específico. La ecuación (iv) y la ecuación (v) se han utilizado para construir la figura 10(a), y la ecuación (iii), la ecuación (iv) y la ecuación (v) se han utilizado en la construcción de la figura 10 (b).
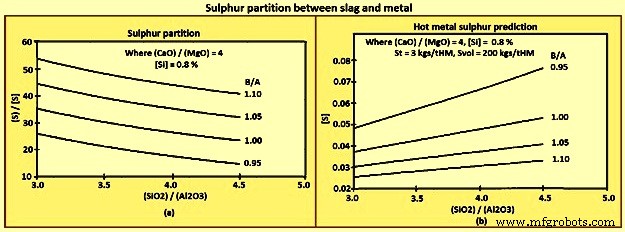
Fig. 10 Separación de azufre entre escoria y metal
Las tendencias generales que se pueden derivar de las ecuaciones y figuras anteriores son (i) [S] disminuye con la disminución de St y el aumento de Sp y Svol, (ii) sin embargo, Sp normalmente aumenta con B/A, (iii) CaO es un mejor desulfurante que el MgO, y (iv) el Al2O3 tiene un efecto menor sobre la Sp que el SiO2.
Capacidad alcalina – Se produce un fenómeno de “reflujo” o “reciclaje” en el BF debido al flujo a contracorriente de gases frente a sólidos/líquidos, en particular para azufre, zinc y álcalis. El reciclaje del potasio alcalino (K) se muestra en la Fig. 11a. El fenómeno de reciclaje es cuando un elemento viaja por el horno en una fase sólida o líquida, reacciona para formar especies gaseosas en las regiones de mayor temperatura del horno, luego viaja de regreso al horno como gases, donde reacciona y es absorbido por el sólido. / fases líquidas en la región de temperatura más baja del horno. El reciclado da como resultado concentraciones internas mucho más altas del elemento reciclado que la concentración que entra o sale del horno. Por ejemplo, la carga interna de K puede ser de 10 kg/tHM, cuando los materiales que se cargan contienen solo 2 kg/tHM.
Los álcalis no tienen efectos beneficiosos, pero tienen muchos efectos nocivos sobre el BF. Los álcalis son absorbidos por los refractarios, el coque y el mineral, lo que provoca la degradación de los refractarios, el coque y el hinchamiento del mineral. Los álcalis también pueden formar costras que pueden despegarse alterando las condiciones térmicas del horno, o acumularse y restringir la carga y el flujo de gas. Los álcalis no se pueden evitar ya que están contenidos en todos los carbones, coques y, en menor medida, minerales. La carga de álcali se debe minimizar siempre que sea posible.
Una parte de los álcalis abandona el horno en el gas superior, siendo la cantidad una función del perfil de temperatura superior. Los álcalis restantes deben eliminarse en la escoria. La capacidad de la escoria para eliminar los álcalis del horno se denomina capacidad alcalina de la escoria. Las relaciones entre la capacidad alcalina y la composición y temperatura de la escoria se muestran en la figura 11b. En general, la capacidad alcalina aumenta con un B/A más bajo y con una temperatura más baja.
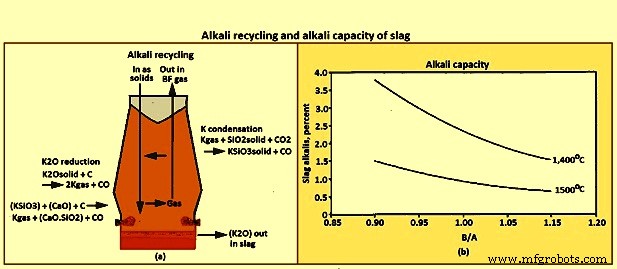
Fig. 11 Reciclado alcalino y capacidad alcalina de la escoria
Actividad de sílice – El [Si] producido depende de los materiales de carga, la operación del horno y la química de la escoria. El impacto de la química de la escoria se muestra en la ecuación [Si] =(SiO2) x GSiO2 / GSi x Keq / (P elevado a 2)co. Aquí CO es monóxido de carbono. Esta ecuación se desarrolla a partir de la constante de equilibrio, ecuación Keq ={ASi x (P elevado a la potencia 2)co} / { ASiO2 x Ac}, para la reacción dada en la ecuación (SiO2) + 2C =[Si] + 2COgas, la definiciones de las actividades de (SiO2) y [Si], ecuación ASiO2 =(SiO2) x GSiO2 y ecuación ASi =[Si] x GSi, y suponiendo que la actividad del carbón en el hogar es igual a uno. La tendencia implícita en la Ecuación [Si] =(SiO2) x GSiO2 / GSi x Keq / (P elevado a 2)co es que el [Si] disminuye a medida que disminuye el (SiO2).
Factores de diseño de escoria
En algunos de los BF, una composición típica de escoria que se forma a partir de la ganga en el mineral y la ceniza del coque es 9 % CaO, 5 % MgO, 75 % SiO2 y 10 % Al2O3. Una escoria de esta composición tiene una temperatura de liquidus del orden de 1.600 grados C y no fluye bien incluso por encima de su temperatura de liquidus. Hence, CaO and MgO are added to the burden to ‘flux’ the gangue and ash resulting in acceptable liquidus temperatures and flow characteristics.
Basic slag design is the selection of the types and quantities of fluxes to be used with a burden and coke to produce a slag of acceptable properties. Burden and coke selections are largely driven by economic issues such as local versus imported sources and degree of beneficiation. These economic driving forces have resulted in a wide range of slag compositions throughout the world.
The general factors to be considered in designing a slag for normal operation are (i) liquidus temperature, that is, the slag is to be completely liquid in the hearth and cast house, (ii) viscosity, that is, the slag is to have a low viscosity, high fluidity, so as to drain from the hearth and down the cast house runners, (iii) sulphur capacity that is the Sp is to be sufficient to produce hot metal with sulphur contents within specifications, (iv) alkali capacity, that is, the slag alkali capacity is to be sufficient to prevent alkali build up in the furnace, (v) hot metal silicon control, that is, the effect of the slag chemistry on the [Si] is to be considered, (vi) slag volume, that is, the slag volume is to be high enough to contribute to the stability of the slag properties and hot metal quality, but not so high as to require excessive fuel or contribute to furnace instability, (vii) robust properties, that is, the slag properties are to be as insensitive to variations in normal variations in furnace operation as possible, specifically hot metal temperature, and (viii) end use, that is, the requirements of the end use of the slag is to be considered.
Slag design is to recognize that the above factors are not independent and that the design always involves a balancing of the above factors to resolve the conflicting trends (Tab 2).
| Tab 2 Normal conflicting trends | ||
| Desired parameter | Basicity | Al2O3 |
| Lower liquidus temperature | Lower | Lower |
| Lower viscosity | Higher | |
| Higher K removal | Lower | Lower |
| Lower [S] | Higher | Higher |
| Lower [Si] | Higher | Higher |
Two examples of the slag design are described below. In the first example (Tab 3) , the issue is to increase the alkali removal without increasing the [S]. The resolution of the issue is to increase the slag volume through the use of additional SiO2 in the burden, while decreasing the slag basicity.
| Tab 3 Example of designing slag for increased K2O removal | |||||
| Basicity | Slag volume | K2O | K2O removed | (S) | S removed |
| B/A | kgs/tHM | % | kgs/tHM | % | kgs/tHM |
| 1.10 | 225 | 0.47 | 1.30 | 1.82 | 5.00 |
| 1.05 | 282 | 0.55 | 1.55 | 1.77 | 5.00 |
| 1.00 | 290 | 0.63 | 1.85 | 1.72 | 5.00 |
| 0.95 | 298 | 0.71 | 2.10 | 1.68 | 5.00 |
The issue in the second example (Tab 4) is to lower the [Si] without negatively impacting the other properties of slag and furnace operation. The resolution of the issue is to decrease the (SiO2) by increasing the (Al2O3) using quartzite, a high (Al2O3) burden material, while holding the (CaO) and (MgO) constant. The change in slag chemistry results into a decrease of both [Si] and [S].
| Tab 4 Example of designing slags with lower [Si] | |||||
| Period | Unit | Base | Number 1 | Number 2 | Number 3 |
| Basicity | 1.12 | 1.13 | 1.13 | 1.12 | |
| (MgO) | % | 11.8 | 11.5 | 11.7 | 11.5 |
| (Al2O3) | % | 7.8 | 10.2 | 10.3 | 11.7 |
| [Si] | % | 0.76 | 0.53 | 0.54 | 0.49 |
| [S] | % | 0.043 | 0.031 | 0.029 | 0.026 |
Slag after the BF
The use of BF slag is driven by the economics of processing and market demand. In the place, where the processing and marketing is performed by the organization producing the slag, the markets tend to be local in nature with minimal processing. As per the present trend, independent organizations take ownership of the liquid slag at the end of the slag runner which has led to wider markets with more extensive processing. The product slag can be classified by the rate of cooling.
Air-cooled slags are those produced with low cooling rates. These are slags which are solidified in pits and frequently cooled with water sprays. The largest uses for air cooled slag are in road construction, railroad ballast, and aggregate. Air-cooled slag has also been used in the production of cement, mineral wool insulation, roofing, and glass.
Pelletized and granulated slags are those produced with high cooling rates. Pelletized slag is produced by pouring liquid slag onto a rotating drum, sometimes with water. Granulated slags are produced by either pouring the liquid slag directly into a large slag pit of water or through the use of high pressure water sprays which breaks the slag up into droplets. Rapidly cooled slags have been used for the same applications as air-cooled slags. The high glass content of rapidly cooled slags makes it particularly suitable for Portland cement production.
Proceso de manufactura
- Sistema de control, medición y automatización de procesos de alto horno
- Generación y uso de gas de alto horno
- Granulación de escoria de alto horno en la fundición
- Productividad del alto horno y los parámetros que influyen
- Operación de alto horno y escoria con alto contenido de alúmina
- Irregularidades del alto horno durante la operación
- Tundish y su papel en la colada continua de acero
- Granulación en seco de escoria de alto horno para recuperación de energía
- Casa de Fundición de Alto Horno y su Operación
- Fabricación de hierro por alto horno y emisiones de dióxido de carbono
- Ingeniería de precisión y su papel en la fabricación



