Mejora de la ciclabilidad del ánodo de metal de litio mediante la construcción de un canal de iones interlaminares atómicos para baterías de azufre de litio
Resumen
La migración uniforme de iones de litio (Li) entre el separador y el ánodo de litio es fundamental para lograr una deposición de Li de buena calidad, que es de gran importancia para el funcionamiento de las baterías de metal de litio, especialmente para las baterías de Li-azufre (Li-S). Los separadores comerciales, como el polipropileno o el polietileno, se pueden preparar mediante procesos en húmedo o en seco, pero de hecho pueden causar abundantes porosidades, lo que da como resultado un decapado / revestimiento desigual de iones de litio y finalmente la formación de dendritas de Li. Desde allí, construimos un canal iónico interlaminar atómico mediante la introducción de montmorillonita en capas en la superficie del separador para guiar el flujo de iones de Li y lograr una deposición estable de Li. El canal iónico interlaminar atómico con un espaciado de 1,4 nm mostró una fuerte capacidad de absorción de electrolitos y una capacidad reservada para iones Li, promoviendo así la transferencia rápida de iones Li y dando como resultado una deposición uniforme de iones Li en el ánodo. Cuando se ensambló con el separador propuesto, la eficiencia de Coulombic de las baterías de Li || Cu fue del 98,2% después de 200 ciclos y se logró un recubrimiento / pelado estable incluso después de 800 h para las baterías simétricas de Li || Li. Es importante destacar que el separador propuesto permite un aumento de la capacidad específica del 140% después de 190 ciclos al emplear las baterías Li-S.
Introducción
Con una demanda cada vez mayor de aplicaciones electrónicas de alto rendimiento, como vehículos eléctricos y sistemas portátiles, la investigación centrada en dispositivos de almacenamiento de energía con alta densidad energética y ciclo de vida largo ha recibido una gran atención [1, 2, 3]. Específicamente, las baterías de metal de litio (LMB), como las baterías de litio azufre (Li-S), pueden ofrecer un excelente rendimiento de almacenamiento de energía debido a su alta densidad de energía, prospectiva para aplicaciones prácticas [4, 5, 6]. En particular, el metal de litio se ha empleado como un material de ánodo prometedor, ya que tiene una alta capacidad de almacenamiento teórico (~ 3860 mAh g −1 ), potencial estándar bajo (- 3,04 V frente al electrodo de hidrógeno estándar) y densidad de peso ligero (0,53 g cm −3 ). Sin embargo, la existencia de poros irregulares en los separadores comerciales puede conducir a una mala calidad del litio depositado, lo que puede resultar en la formación de dendríticas y consumir más metales de litio y electrolitos durante los repetidos procesos de decapado / decapado [7, 8].
En consecuencia, las dendritas de Li podrían formar el metal de Li "muerto" cuando se desprenden fácilmente del colector conductor, lo que da como resultado una baja eficiencia de Coulomb (CE) y una pérdida de capacidad irreversible [9, 10]. Además, las dendritas de litio podrían perforar el separador y, por lo tanto, provocar un cortocircuito en los LMB, lo que provocaría una fuga térmica, un incendio e incluso una posible explosión de las baterías recargables [11, 12]. Debido a tales obstáculos, el uso de LMB en baterías recargables se ha limitado en los últimos 20 años. Por lo tanto, prevenir la formación de dendritas de litio puede ser un enfoque eficaz para aprovechar al máximo las características prometedoras de las LMB [13]. Recientemente, los investigadores han propuesto varios métodos para resolver el problema anterior, incluida la optimización de la composición de electrolitos [5, 14], la construcción de la capa de interfase de electrolitos sólidos artificiales (SEI) en el ánodo de metal Li [15], el desarrollo del ánodo de Li compuesto tridimensional [ 16], y modificando el colector [17, 18]. Aunque esas estrategias se diseñaron para estabilizar la capa SEI y / o reducir la densidad de corriente aplicada efectiva de los metales de litio, se centraron principalmente en los electrolitos y metales de litio. Hasta la fecha, solo se han realizado unos pocos trabajos para abordar o mitigar los desafíos de las dendritas mediante la modificación del separador [19]. Evidentemente, regular el separador puede ser un método novedoso y factible para inhibir la formación de dendrita de litio.
Entre los componentes de los LMB, el separador no solo juega un papel clave para segmentar los electrodos de ánodo y cátodo para evitar cortocircuitos, sino que también afecta directamente el rendimiento de las baterías al autorizar la migración de iones de litio [9, 20, 21]. Por lo tanto, se ha informado que una simple modificación del separador usando una capa intermedia de polímero electrolítico semisólido [22], grafeno [23] o revestimiento de superficie de alto módulo [24] puede prevenir eficazmente la formación de dendritas y así mejorar el rendimiento de las LMB. Sin embargo, entre los enfoques informados anteriormente, las capas de barrera eran gruesas (> 10 µm) y tenían una alta carga de masa (varios miligramos), lo que inevitablemente puede impedir la rápida difusión de los iones Li y reducir la densidad de energía de las LIB. Además, la mayoría de los LMB que utilizan esos separadores funcionales solo pueden realizar ciclos con densidades de corriente bajas, por ejemplo, inferiores a 2 mA cm −2 . Para mejorar la densidad de corriente crítica de los LMB, la adición de partículas inorgánicas dentro del separador para mejorar la estructura porosa y aumentar la densidad de corriente crítica puede ser otro método eficaz. Sin embargo, la distribución desigual de los poros en el separador generalmente puede conducir a una difusión desordenada de los iones de Li durante el proceso de galvanoplastia / desmoldeo, lo que lleva a la deposición desigual de los iones de Li y la formación de dendritas de Li [7]. Por lo tanto, la microestructura del separador con un canal de transferencia de litio uniforme es muy beneficiosa para eliminar el problema encontrado de la dendrita durante los procesos de carga / descarga.
En este trabajo, con el objetivo de guiar la migración de iones Li de manera uniforme a través del separador, se fabrica un separador compuesto modificado con montmorillonita a base de Li (Li-MMT) mediante la construcción de canales iónicos interlaminares atómicos en el separador de PP. El separador preparado incrustado con un espaciado interlaminar (~ 1,4 nm) proporciona abundantes sitios activos para la difusión de iones de litio y la humectación de electrolitos [25]. Por lo tanto, se permite que el separador modificado logre una deposición uniforme de iones de Li en el ánodo de Li al unificar la dirección de los flujos de Li, lo que puede eliminar eficazmente los problemas de dendrita de Li en los procesos de carga / descarga. Como resultado, el separador Li-MMT permite que las baterías Li || Cu proporcionen un 98,2% de CE incluso después de 200 ciclos y garantiza que las baterías Li || Li simétricas actualicen un recubrimiento / pelado estable durante 800 ha 1 mA cm −2 con una capacidad de 1 mAh cm −2 . Además, las baterías con separadores Li-MMT @ PP también ofrecen una buena estabilidad de ciclo con un aumento de la capacidad específica del 140% en comparación con los separadores de PP después de 190 ciclos a 0,5 mA cm −2 con una carga de azufre de 1,5 mg cm −2 .
Métodos experimentales
Materiales y preparaciones
La montmorillonita (MMT), el fluoruro de polivinilideno (PVDF) y el hidróxido de litio (LiOH) se adquirieron de Aladdin. La N-metil pirrolidona (NMP) y el ácido sulfúrico (H 2 SO 3 ) se obtuvieron de Sinopharm Chemical Reagent Co., Ltd. El polvo de azufre (S) y el negro de acetileno (indicado como polvo C) se adquirieron de Alfa Aesar. Se utilizó Celgard 2500 como separador. El polvo de Li-MMT se preparó mediante intercambio catiónico. Normalmente, 0,2 M H 2 SO 3 Se usó una solución para convertir los cationes dentro de la capa intermedia de MMT en iones y luego se usó una solución de LiOH para preparar la solución a PH =7, así como convertir los iones de hidrógeno en iones de Li. Se utilizó tecnología de liofilización para recolectar el polvo de Li-MMT. Para la preparación del separador Li-MMT @ PP, solo un lado del separador se revistió con la suspensión de Li-MMT y el polvo de Li-MMT y PVDF con una relación de masa de 9:1 se dispersó uniformemente en la solución de NMP y la carga de masa promedio de Li-MMT es solo ~ 0,15 mg cm −2 .
Caracterización
Se empleó el espectro de difracción de rayos X (XRD) usando un difractómetro UltimaIV con radiación CuKα1 (λ =1.4506 Å) para investigar la estructura cristalina del polvo de Li-MMT. Se utilizó un microscopio electrónico de transmisión de alta resolución (HRTEM) para observar la capa intermedia de Li-MMT y el microscopio electrónico de barrido (SEM, FEI NANOSEI 450) se utilizó para analizar las morfologías de la superficie.
Mediciones electroquímicas
Para las pruebas de baterías Li || Cu y Li || Li, normalmente, las láminas de Cu se lavaron en primer lugar con agua desionizada y etanol tres veces para eliminar las posibles impurezas. Luego, la lámina de litio se cortó en círculos con un área de 1 cm −2 para utilizar como fuentes de Li. El electrolito era sal de litio de bistrifluorometanosulfonimida 1 M (LiTFSI) en una mezcla de 1,3-dioxaciclopentano (DOL) y 1,2-dimetoxietano (DME) (1:1 v / v) con 2% en peso de nitrato de litio (LiNO 3 ) como aditivo. Para las pruebas de batería Li-S, el cátodo S se preparó mediante nuestro método anterior en el que el polvo C y S se mezclaron y se calentaron a 155 ℃ durante 24 h con una relación de masa de 8:2 [26]. Y luego los polvos de compuestos C / S, C y PVDF con una relación de masa de 8:1:1 se dispersaron uniformemente en la solución de NMP para preparar el electrodo de azufre. La carga media de azufre es de 1,5 mg cm −2 que se revistió sobre la hoja de aluminio recubierta de carbono. Las baterías se ensamblaron mediante una batería de botón de acero inoxidable (CR2025) en una guantera llena de argón. Se utilizó lámina de Li como ánodo. Se usaron 20 µl de electrolito para humedecer el ánodo de litio y se usaron 20 µl adicionales para humedecer el separador y el cátodo. Antes de la prueba, las baterías de Li-S ensambladas reposaron 12 hy luego 0,2 mA cm −2 con 5 ciclos se utilizó para activar el rendimiento de la batería. El sistema de prueba electroquímica fue el sistema de prueba de batería CT2001A (LAND Electronic Co., China). El voltaje de corte fue de 1,7 a 2,7 V. La espectroscopia de impedancia electroquímica (EIS) fue probada por una estación de trabajo electroquímica (CHI660E, Chenhua Instruments Co., China).
Resultados y discusión
Para ilustrar el flujo de iones de litio a través del separador de PP comercial, los esquemas se muestran en la Fig. 1a, b, en la que la capa de Li-MMT de ~ 5 µm se revistió uniformemente sobre el separador de PP para guiar el flujo de iones de Li. Es bien sabido que el separador de PP comercial se prepara típicamente mediante procesos en seco o húmedo, y luego el separador se estira para generar abundantes vacíos para permitir el paso de iones de litio. Sin embargo, el separador de PP comercial muestra trayectorias desordenadas y poros apilados arbitrariamente (Fig. 1a), por lo que puede fallar en realizar una migración uniforme de iones de Li y finalmente causar dendritas de Li. Por lo tanto, el canal de iones atómicos Li-MMT se empleó como modulador para guiar un flujo uniforme de iones de Li (Fig. 1b) y lograr una deposición uniforme de Li. La estructura cristalina de MMT generalmente se compone de capas cargadas negativamente (NCL) separadas por espacio entre capas (> 1 nm), que alberga los iones catiónicos intercambiables, como Li + , Na + , Mg 2+ , Ca 2+ , etc. Por lo tanto, el método de intercambio catiónico es necesario para convertir los cationes del huésped en iones Li [25]. La estructura básica de los NCL es una capa T-O-T típica, donde "T" representa la hoja tetraédrica y "O" es la hoja octaédrica [25]. Con la estructura de capa intermedia única de Li-MMT, el electrolito puede penetrar eficazmente en la capa de Li-MMT, lo que resulta en el transporte sin obstáculos de iones de Li, logrando así la difusión eficiente de iones [7, 25]. La morfología de Li-MMT se muestra en la Fig. 1c, d que muestra claramente la estructura típica de nanoplacas 3D con una arquitectura apilada de forma cercana y arbitraria. Según la imagen HRTEM, se puede observar la estructura en capas de Li-MMT y muestra un espacio entre capas de ~ 1,39 nm.
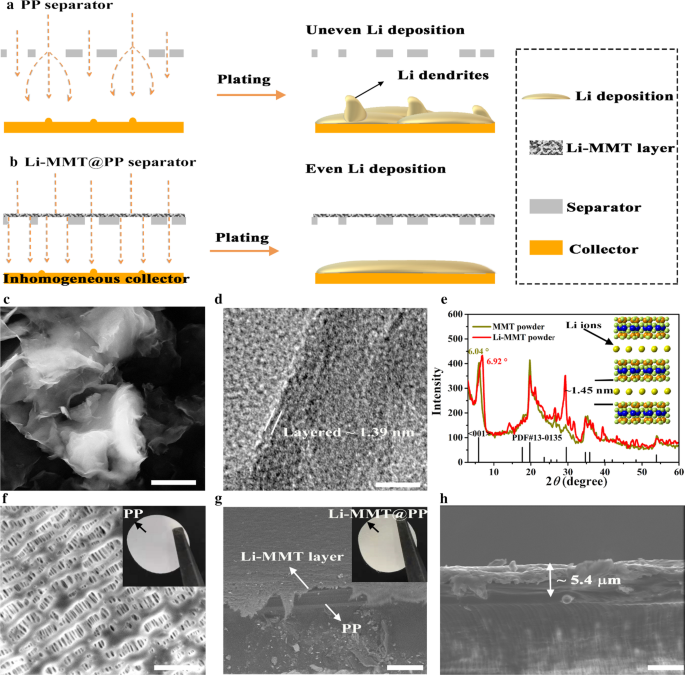
Preparación y caracterizaciones de polvos Li-MMT y separador Li-MMT @ PP. un , b Esquemas de conceptos de diseño con diferentes separadores. c Imagen SEM de Li-MMT. d Imagen HRTEM de Li-MMT. e Espectro XRD. f Imagen SEM del separador de PP, la imagen óptica insertada es un separador de PP. g Imagen SEM del separador Li-MMT @ PP y h perfil transversal correspondiente, la imagen óptica insertada en g es el separador Li-MMT @ PP. Barra de cicatrices: c 1,5 µm, d 5 millas náuticas, f 2,5 µm, g 25 µm, h 5 µm
La medición precisa del espacio entre capas de Li-MMT se muestra en la Fig. 1e. El MMT crudo con los cationes indeterminados en su capa intermedia presenta un pico alrededor de 6.04 °. Después del intercambio iónico, el pico ubicado a 6,92 ° puede confirmar el cambio de cationes indeterminados a iones Li. Dado que los cationes dentro de MMT en bruto son muy variables en tamaño y distribución, mientras que los iones Li son de tamaño más pequeño que otros cationes [25], la distancia entre capas disminuye gradualmente. Según la ley de Bragg, el espaciado entre capas de Li-MMT se puede estimar en ~ 1,4 nm, lo que puede proporcionar un canal amplio para el transporte de iones de litio y la humectación de electrolitos. La morfología porosa del separador de PP se presenta en la Fig. 1f. Después de recubrir la capa de Li-MMT, se puede encontrar que la porosidad del separador Li-MMT @ PP disminuye significativamente (Fig. 1g), lo que es beneficioso para el movimiento regular de iones. En este trabajo, la suspensión de Li-MMT se recubrió con una máquina de recubrimiento, que muestra potencial para la producción a gran escala. El espesor del recubrimiento es de solo 5 µm (Fig. 1h) con un aumento de masa insignificante.
Beneficiado del canal iónico interlaminar atómico mencionado anteriormente, el separador Li-MMT @ PP es eficaz para regular la deposición de Li y suprimir el crecimiento de dendrita de Li a escala atómica guiando el flujo de iones de Li. Las mediciones de Brunner-Emme-Teller (BET) muestran la distribución del tamaño de los poros del polvo de Li-MMT dentro del alcance de 1-3 nm (archivo adicional 1:Fig. S1). Como se muestra en la Fig. 2a, la batería Li || Cu se utilizó para estudiar la CE. Se encontró que el separador Li-MMT @ PP puede entregar la batería Li || Cu con un CE elevado y una estabilidad excelente incluso durante 200 ciclos a la densidad de corriente de 1 mA cm −2 con una capacidad de 1 mAh cm −2 . Durante las pruebas, se puede observar que todos los CE presentan una tendencia ascendente en los primeros 5 ciclos, provocada por la pasivación superficial de la deposición de Li. Sin embargo, un CE promedio más alto en los primeros 5 ciclos del separador Li-MMT @ PP destaca las ventajas de que el metal Li depositado sufre una reacción lateral más baja con el electrolito líquido junto con el separador Li-MMT @ PP. Con el revestimiento / pelado reduplicativo, la deficiencia del separador de PP se expone gradualmente que la batería de Li || Cu ensamblada solo aguanta ~ 50 ciclos y su CE disminuye bruscamente al 60% y casi a cero después de 150 ciclos. Por el contrario, la batería CE de Li || Cu ensamblada con separador Li-MMT @ PP aún ofrece ciclos estables con menor sobrepotencial (Fig.2b) y la batería aún mantiene 98.2% CE después de 200 ciclos, lo que indica el Li depositado el metal es más uniforme y no se produce dendrita de litio después de la regulación de la capa de Li-MMT.
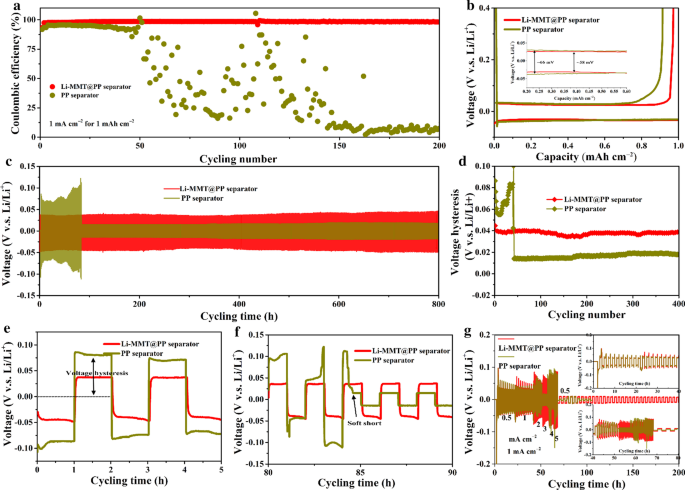
Rendimientos electroquímicos de baterías simétricas Li || Cu y Li || Li. un Curvas CE y b curvas de voltaje correspondientes. c Perfiles de voltaje-tiempo de las baterías Li || Li simétricas usando Li-MMT @ PP o separador PP a 1 mA cm −2 con una capacidad de 1 mAh cm −2 . d Histéresis de voltaje de baterías Li || Li simétricas. e , f Los perfiles de ampliación parcial de c . g Los rendimientos de frecuencia de Li || Li baterías simétricas
Para investigar más a fondo las ventajas del separador Li-MMT @ PP en la estabilidad cíclica de los ánodos de metal Li, también se fabrican baterías Li || Li simétricas con varios separadores. Como se muestra en la Fig. 2c, cuando la capacidad de ciclo es 1 mAh cm −2 a una densidad de corriente de 1 mA cm −2 , la batería con el separador Li-MMT @ PP ofrece una excelente estabilidad cíclica con mesetas de voltaje estables durante 400 ciclos (900 h) (Fig. 2d). En marcado contraste, la batería con el separador de PP presenta una fuerte histéresis de voltaje en las etapas iniciales. El sobrepotencial es casi dos veces mayor que el del separador Li-MMT @ PP (Fig. 2e). Después del lijado / pelado durante 84 h, se observa una caída repentina de voltaje para la batería con el separador de PP (Fig. 2f), que se puede atribuir a la conexión eléctrica entre los electrodos, dando como resultado el “corto suave”. Por lo tanto, las prestaciones de velocidad de la batería simétrica de Li se utilizaron además para evaluar la densidad de corriente en la supresión de las dendritas de Li. Como se muestra en la Fig. 2g, el separador Li-MMT @ PP bajo la densidad de corriente incluso tan alta como 5 mA cm −2 todavía exhibe comportamientos normales de enchapado / rayado. El separador de PP presenta fluctuaciones de voltaje significativas a medida que la densidad de corriente se cierra a 3 mA cm −2 . Especialmente cuando la densidad de corriente aumenta a 5 mA cm −2 , el voltaje se vuelve extremadamente inestable, lo que indica que la superficie del ánodo de Li sufre dendritas de Li graves. En comparación con trabajos anteriores (Archivo adicional 1:Tabla S1), el separador Li-MMT modificado muestra ventajas competitivas para suprimir eficazmente las dendritas de Li.
La correlación de iones de Li a través del separador antes y después de recubrir la capa de Li-MMT se propone en la Fig. 3a. Después del intercambio catiónico, la capa intermedia de Li-MMT proporciona el sitio activo para Li. El espaciado entre capas de 1,4 nm sirve como un canal de iones de Li único para permitir el flujo regular de iones de Li durante los procesos de decapado / decapado. Sin embargo, para el separador de PP, las trayectorias desordenadas (Fig. 3b) y los poros apilados arbitrariamente no permitirán la migración uniforme de iones de Li como a través del separador, lo que conducirá a la deposición heterogénea de iones de Li en los procesos electroquímicos, y provocando la formación de dendritas de litio. Por lo tanto, se investigan las morfologías de los ánodos de metal Li después de 20 ciclos para aclarar aún más el efecto del separador Li-MMT @ PP sobre la supresión de las dendritas de Li. Como se muestra en la Fig. 3c, e, después de revestir la capa de Li-MMT, se realiza una deposición de Li uniforme y densa y no se observa formación de dendrita de Li en la superficie del ánodo incluso después de 20 ciclos. Es importante destacar que el ánodo de metal de Li aún conserva una estructura relativamente densa y compacta con una superficie libre de dendrita, lo que destaca las ventajas de la capa de Li-MMT para un comportamiento favorable de decapado / decapado de Li sin dendrita. Sin embargo, para la celda con separador de PP, el ánodo de metal Li muestra dendritas de Li en forma de alambre obvias después de los ciclos (Fig. 3d), y apila libremente Li musgoso con una estructura altamente porosa (Fig. 3f).
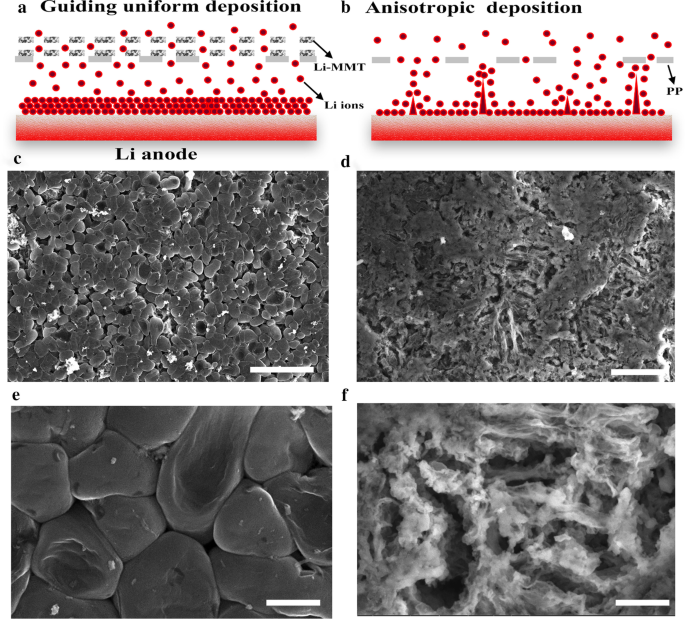
Imágenes SEM del ánodo de Li acoplado con Li-MMT @ PP o separador de PP después de 20 ciclos a 1 mA cm −2 con una capacidad de 1 mAh cm −2 . un , b Ilustración del mecanismo de separadores Li-MMT @ PP o PP. c , e Separador Li-MMT @ PP. d , f Separador de PP. Barras de escala: c 25 µm, d 10 µm, e , f 2,5 µm
Para demostrar el potencial del separador Li-MMT @ PP en la aplicación práctica de baterías de metal Li, el cátodo S con carga S de 1,5 mg cm −2 se empleó como electrodo. La interfaz electroquímica ensamblada con diferentes separadores se investigó mediante la medición de espectroscopía de impedancia electroquímica (EIS). Como se muestra en la Fig. 4a, típicamente, todos los separadores presentan semicírculos deprimidos a altas frecuencias, que corresponden a la resistencia de transferencia de carga interfacial. Aunque podemos ver que la resistencia de transferencia de carga de la batería ensamblada con separador Li-MMT @ PP es ligeramente mayor que la del separador PP, el rendimiento de la batería no se vio afectado después de la activación de baja densidad de corriente, lo que se ha afirmado en la sección experimental. Durante las regiones de baja frecuencia, las líneas inclinadas presentan la difusión de iones de litio dentro de los materiales activos. La Figura 4b muestra las mesetas de voltaje del cátodo compuesto C / S ensamblado con separadores Li-MMT @ PP o PP entre 1,7 y 2,8 V (V.S. Li / Li + ). Las pruebas de voltamperometría cíclica (CV) se realizaron y se presentan en el archivo adicional 1:Fig. S2. Aunque la mayor concentración de polisulfuros solo genera una polarización de concentración ligeramente mayor que el separador de PP, el área de pico del separador de Li-MMT @ PP es mucho mayor que la del separador de PP, lo que indica que se generan más polisulfuros cuando se usa la capa de recubrimiento de Li-MMT . De acuerdo con los mecanismos de reacción del cátodo S, la batería Li-S exhibe dos mesetas típicas durante los procesos de carga / descarga. En la primera etapa antes del punto de inflexión, el separador Li-MMT @ PP ofrece una alta capacidad de descarga de ~ 400 mAh g −1 con histéresis de voltaje insignificante. Sin embargo, para el separador PP, solo ~ 210 mAh g −1 Se observa capacidad, lo que indica que los polisulfuros de cadena larga parcialmente liberados (especialmente para el Li 2 S 8 ) no están involucrados en la reacción redox posterior para contribuir con la capacidad. La mayor capacidad de descarga durante la primera meseta implica que la capa de Li-MMT puede evitar eficazmente el transporte de polisulfuros solubles de cadena larga a la superficie del ánodo de Li. En los segundos pasos de conversión, obviamente, para el separador de PP, se forman pequeñas cantidades de polisulfuros de cadena corta debido a la existencia del efecto lanzadera dentro del electrolito a base de éter, lo que ha sido confirmado por nuestro trabajo previo [26]. Por el contrario, el separador Li-MMT @ PP tiene un diseño racional de que la superficie Li-MMT tiene una fuerte capacidad de anclaje para polisulfuros para evitar la lanzadera de polisulfuros [25]. Las excelentes propiedades de adsorción aseguran que se evite que los polisulfuros extiendan la superficie del ánodo de Li y pasiven la superficie de Li, lo que permite que la batería Li-S ensamblada con separador Li-MMT @ PP tenga una alta capacidad de descarga de 1283 mAh g -1 . Los ciclos a largo plazo con buena estabilidad son los principales objetivos de las baterías comerciales. La ciclabilidad a largo plazo de los separadores Li-MMT @ PP se muestra en la Fig. 4c. En los primeros 20 ciclos, se puede observar que las capacidades del separador Li-MMT @ PP y PP muestran una tendencia típica a la baja. Esto se debe a que, en el proceso de descarga inicial, se precipitarían abundantes polisulfuros del interior del material del cátodo C / S y se depositarían en la superficie del material del cátodo [26], lo que provocaría la pérdida de capacidad. Sin embargo, luego de estabilizar el ánodo de metal de litio, surgen los beneficios del separador Li-MMT @ PP que la retención de la capacidad de descarga se mantiene al 100% durante los ciclos posteriores y la CE también es del 100%.
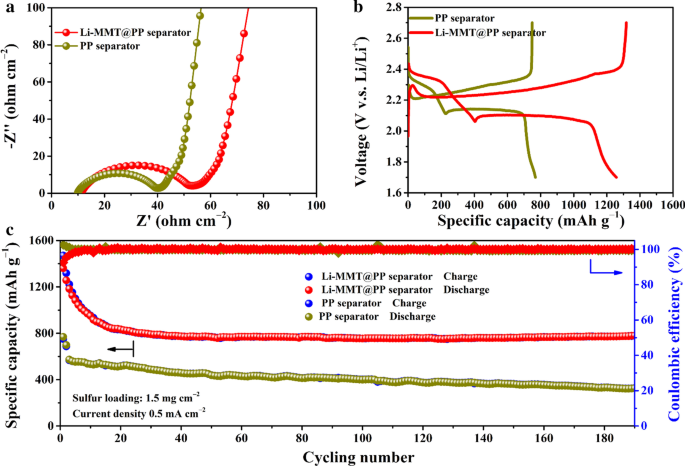
Rendimiento electroquímico de baterías Li-S con diferente separador. un Resultados de la EIS. b Las mesetas de carga / descarga con Li-MMT @ PP o separador de PP. c Rendimiento de ciclismo a largo plazo a 0,5 mA cm −2 con una carga de azufre de 1,5 mg cm −2
Conclusiones
En resumen, el canal de iones interatómico (Li-MMT) se construyó en el separador de PP poroso para modular el flujo de iones de Li y luego guiar la deposición uniforme de iones de Li en el ánodo de Li durante la galvanoplastia / decapado. Debido al amplio espacio entre capas (~ 1.4 nm) de Li-MMT, el separador Li-MMT @ PP asegura en gran medida la ciclabilidad del ánodo de metal Li al unificar la dirección de flujo de los iones de litio, lo que resulta en la deposición uniforme de iones de Li en el superficie del ánodo, formando así un ánodo de litio libre dendrítico. Como se ensambla con el separador Li-MMT @ PP, la batería Li-S exhibe una notable capacidad reversible de 776 mAh g −1 (casi 1,4 veces más grande que el separador de PP) con un 100% de CE después de 190 ciclos a la densidad de corriente de 0,5 mA cm −2 con una carga de azufre de 1,5 mg cm −2 .
Disponibilidad de datos y materiales
Todos los datos están completamente disponibles sin restricciones.
Abreviaturas
- Li:
-
Litio
- Li – S:
-
Azufre de litio
- PP:
-
Polipropileno
- PE:
-
Polietileno
- MMT:
-
Montmorillonita
- CE:
-
Eficiencia coulombica
- LMB:
-
Baterías de metal de litio
- SEI:
-
Interfase de electrolitos sólidos
- Li-MMT:
-
Montmorillonita a base de litio
- PVDF:
-
Fluoruro de polivinilideno
- LiOH:
-
Hidróxido de litio
- NMP:
-
N-metil pirrolidona
- H 2 SO 3 :
-
Ácido sulfúrico
- C:
-
Acetileno negro
- XRD:
-
Difracción de rayos X
- HRTEM:
-
Microscopio electrónico de transmisión de alta resolución
- LiTFSI:
-
Sal de litio de bistrifluorometanosulfonimida
- DOL:
-
1,3-dioxaciclopentano
- DME:
-
1,2-dimetoxietano
- LiNO 3 :
-
Nitrato de litio
- EIS:
-
Espectroscopia de impedancia electroquímica
- NCL:
-
Capas cargadas negativamente
- APUESTA:
-
Brunner – Emmet – Teller
- CV:
-
Voltamperometría cíclica
Nanomateriales
- Nanocristales de estaño para futuras baterías
- Nano y ánodo de batería:una revisión
- El reordenamiento atómico de múltiples pozos cuánticos basados en GaN en gas mixto H2 / NH3 para mejorar las propiedades estructurales y ópticas
- Investigaciones de la sorción de iones de metales pesados utilizando nanocompuestos de biocarbón modificado con hierro
- Efecto de diferentes aglutinantes sobre el rendimiento electroquímico del ánodo de óxido metálico para baterías de iones de litio
- Compuesto de aerogel / azufre de carbón activado recubierto de polianilina para batería de litio-azufre de alto rendimiento
- Transformación de lodo Si en estructura nano-Si / SiOx por difusión de oxígeno hacia el interior como precursor de ánodos de alto rendimiento en baterías de iones de litio
- Síntesis asistida por humato de nanocompuestos de MoS2 / C a través de la ruta de co-precipitación / calcinación para baterías de iones de litio de alto rendimiento
- Revisión:Membranas y filtros de metal poroso para la separación de aceite y agua
- Una novedosa batería flexible de iones de litio de celda completa basada en nanofibras de carbono electrohiladas a través de un paquete de plástico simple
- Tornos CNC para metal



