Preparación de micro / nanoesferas huecas de polianilina y su capacidad de eliminación de Cr (VI) de aguas residuales
Resumen
Las micro / nanoesferas de polianilina hueca (PANI) se obtienen mediante una simple polimerización de monómeros en solución alcalina con Triton X-100 Micelles como plantillas blandas. Las micro / nanoesferas huecas de PANI demuestran una capacidad de eliminación rápida y eficaz de cromo (VI) (Cr (VI)) en un amplio rango de pH, y la capacidad máxima de eliminación puede alcanzar 127,88 mg / g a pH 3. Después de tratarse con ácido, el Las micro / nanoesferas huecas de PANI usadas tienen una capacidad de eliminación similar de Cr (VI) de las aguas residuales.
Antecedentes
El ión de metal pesado cromo (VI) (Cr (VI)), que se origina en el cromado, el curtido de cuero, el acabado de metales y las industrias textiles, es muy peligroso para los ecosistemas y los organismos vivos debido a su carcinogenicidad y movilidad [1,2,3] . Los iones Cr (VI) no tratados pueden causar insuficiencia renal, congestión pulmonar, daño gástrico, cáncer de hígado, irritación de la piel, etc. [4, 5, 6]. En comparación con Cr (VI), los iones Cr (III) se precipitan o adsorben fácilmente [7,8,9]. Por tanto, convertir Cr (VI) en Cr (III) y precipitar Cr (III) en sólido son las técnicas habituales para la eliminación de Cr (VI) de la solución. Mientras que los reductores tradicionales como el dióxido de azufre, el metabisulfito de sodio y el sulfato ferroso, utilizados para la reducción de Cr (VI), no son reciclables ni reutilizables. Además, también conducen a la generación de productos de desecho secundarios, lo que aumenta los problemas ambientales [10, 11]. Por tanto, es fundamental explorar nuevos materiales para la eliminación de Cr (VI) del medio acuoso.
Desde que Rajeshwar y sus colaboradores informaron por primera vez de que los polímeros conductores podrían convertir Cr (VI) altamente tóxico en Cr (III) menos tóxico en 1993 [12], los polímeros conductores, especialmente la polianilina (PANI), han sido objeto de una gran preocupación [13,14, 15,16], debido a su fácil síntesis, bajo costo y mecanismo especial de dopaje / desdopado de protones. PANI, normalmente tiene tres estados de oxidación, que son pernigranilina (PB, que pertenece a la amina terciaria aromática), esmeralda (EB, que pertenece a la amina secundaria aromática) y leucoemeraldina (LB) [17, 18], contiene unidades benzenoides y quinonoides con abundantes grupos amina que pueden proporcionar electrones para la reducción de Cr (VI) [1, 10]. Sin embargo, la masa y la película de PANI con mala porosidad restringen su aplicación en la reducción de Cr (VI). Recientemente, las micro / nanoesferas huecas de PANI han recibido considerable atención debido a sus amplias aplicaciones potenciales en supercondensadores [19, 20], campos de biosensores electroquímicos [21], etc. Además, las micro / nanoesferas PANI huecas con cavidad interior pueden mejorar el área de superficie específica para mejorar la eliminación de la capacidad de Cr (VI) y la tasa de absorción. Recientemente, se están preparando microesferas huecas de PANI utilizando métodos de molde duro [19]; sin embargo, implican procedimientos complejos de preparación y eliminación, que conducen a una mala reproducibilidad y hacen que sea bastante difícil retener la estructura hueca después de la eliminación de la plantilla [22, 23]. En comparación con los métodos de plantilla rígida, los métodos de plantilla blanda son más económicos y eficaces. Más importante aún, la plantilla blanda se puede eliminar fácilmente con agua y etanol [1, 24]. Por lo tanto, un método de preparación simple, eficaz y de alto rendimiento de micro / nanoesferas PANI sigue siendo deseable en el campo de la eliminación de Cr (VI) tóxico.
En este artículo, se sintetiza una gran cantidad de micro / nanoesferas de PANI huecas reproducibles mediante una simple polimerización de monómeros en solución alcalina con Triton X-100 Micelles como plantillas blandas. Las micro / nanoesferas huecas reproducibles de PANI no son tóxicas y son seguras para los ecosistemas. Mientras tanto, las micro / nanoesferas huecas de PANI reproducibles tienen una alta capacidad de eliminación de Cr (VI) que puede alcanzar 127,88 mg / g a pH 3. El modelo de cinética de eliminación de Cr (VI) y la isoterma de absorción de las micro / nanoesferas de PANI huecas se ajustan a pseudo- modelo de cinética de segundo orden y modelo de isoterma de absorción de Langmuir, respectivamente. Las micro / nanoesferas huecas de PANI no solo eliminan el Cr (VI) rápidamente, sino que también pueden regenerarse fácilmente para su reutilización.
Métodos
El objetivo del estudio
Para resolver el problema de que el ion de metal pesado Cr (VI) en las aguas residuales genera un peligro letal para los ecosistemas y los organismos vivos, las micro / nanoesferas huecas reproducibles de PANI se preparan mediante una simple polimerización de monómeros en solución alcalina con Triton X-100 Micelas blandas. plantillas, con el fin de eliminar los residuos que contienen Cr (VI).
Materiales
La anilina (Sinopharm Co.Ltd), el hidróxido de sodio (NaOH, Sinopharm Co.Ltd), Triton X-100 (Alfa) y el persulfato de amonio (APS, Sinopharm Co.Ltd) son de grado analítico y se usan sin purificación adicional.
Síntesis de microesferas / nanoesferas PANI huecas
Se prepararon micro / nanoesferas de PANI huecas mediante una simple polimerización de monómero en solución alcalina con Triton X-100 Micelles como plantillas. En un proceso de síntesis típico, 32 mmol de anilina, 32 mmol de NaOH y 0,82 mmol de Triton X-100 se dispersaron directamente en 20 ml de agua desionizada con agitación magnética a temperatura ambiente durante 20 min, luego la solución de la mezcla se enfrió en hielo. baño de agua durante 5 min. Después de eso, se añadió la solución acuosa oxidante (20 ml) que contenía 32 mmol de APS preenfriada en el baño de agua helada durante 5 min a la solución de mezcla de anilina mencionada anteriormente en una porción, y la solución resultante se agitó durante otros 0,5 min para asegurar una mezcla completa y luego se procedió a la reacción en el baño de agua helada sin agitación durante 12 h. Finalmente, los productos se lavaron y centrifugaron con agua desionizada y etanol hasta que el filtrado se volvió incoloro y luego se secaron en un horno por 24 ha 60 ° C.
Caracterización
La morfología de los productos PANI resultantes se observó con microscopio electrónico de barrido de emisión de campo (FESEM, Sirion 200) y microscopio electrónico de transmisión (TEM, JEOL-2010). Las estructuras del PANI preparado se caracterizaron por difracción de rayos X (XRD, Philips X’Pert) y espectroscopia infrarroja por transformada de Fourier (FTIR, espectrofotómetro JASCO FT-IR 410). La concentración de Cr se analizó mediante espectrómetro de emisión de plasma (ICP) acoplado inductivamente y espectroscopía de absorción UV-Vis. El estado de oxidación del cromo adsorbido en la nanoestructura de PANI se determinó mediante espectroscopía de fotoelectrones de rayos X (XPS, ESCALAB 250). El potencial zeta y el tamaño de partícula se obtuvieron mediante Zetasizer 3000HSa.
Eliminación de Cr (VI) por esferas PANI huecas
La solución de Cr (VI) se preparó disolviendo dicromato de potasio (K 2 Cr 2 O 7 ) en agua desionizada. La solución madre (2 mmol L −1 ) se preparó disolviendo 1,177 g de K 2 Cr 2 O 7 en 2000 mL de agua desionizada. Todas las soluciones de trabajo con diversas concentraciones se obtuvieron mediante diluciones sucesivas. El polvo de PANI sintetizado (10 mg) se dispersó ultrasónicamente en 20 ml de solución de Cr (VI) (1,2 mmol L −1 ) con diferentes valores de pH, el cual se ajustó con solución de NaOH y HCl. Después de la reacción durante 3 h, la solución de reacción se centrifugó y los valores de pH del líquido sobrenadante se ajustaron en el rango de 7,5 a 8,5. Finalmente, las micro / nanoesferas huecas de PANI usadas se separaron y se aclararon varias veces con agua desionizada y se secaron. Las capacidades de eliminación de Cr (VI) de las micro / nanoesferas de PANI huecas en diferentes valores de pH se pueden calcular utilizando la siguiente ecuación:
$$ {q} _e =\ frac {\ left ({c} _0- {c} _e \ right) V} {m} $$ (1)donde q e es la cantidad de eliminación de Cr (VI) por gramo de micro / nanoesferas de PANI huecas en equilibrio (mg / g), V es el volumen de la solución (L), m es la masa de las micro / nanoesferas huecas de PANI (g) y c 0 y c e son la concentración de Cr (VI) inicial y de equilibrio (mg / L), respectivamente.
Medición de la cinética de eliminación
Para los experimentos de cinética de eliminación, se llevaron a cabo tres conjuntos de experimentos, en los que los valores de pH de la solución de Cr (VI) fueron 3, 4 y 5, respectivamente. El polvo de PANI sintetizado (10 mg) se dispersó ultrasónicamente en 20 ml de solución de Cr (VI) (1,2 mmol L −1 ) con diferentes valores de pH, y la mezcla se agitó magnéticamente. A intervalos predeterminados, se extrajo una cantidad apropiada de la solución de reacción y luego se centrifugó. El líquido sobrenadante se utilizó para analizar la concentración de Cr (VI) mediante espectroscopía de absorción UV-Vis a una longitud de onda de 350 nm. Las gráficas cinéticas teóricas se obtuvieron mediante la ecuación de pseudo-segundo orden:
$$ \ frac {t} {q_t} =\ frac {1} {k_2 {q} _e ^ 2} + \ frac {t} {q_e} $$ (2)donde q e y q t son las cantidades de Cr (VI) eliminadas por micro / nanoesferas PANI huecas en equilibrio y en el tiempo t (min) (mg / g) y k 2 es la constante de velocidad (g / mg min).
Medición de isotermas de eliminación
Para los experimentos de eliminación de isotermas, los procesos de operación son los mismos que los anteriores. También hicimos tres series de experimentos en diferentes valores de pH, 3, 4 y 5, respectivamente. En cada experimento, el polvo de PANI tal como se sintetizó (10 mg) se dispersó ultrasónicamente en 20 ml de solución de Cr (VI) con diferente concentración bajo agitación magnética. Cuando la solución alcanzó el equilibrio de eliminación, se centrifugaron y luego se analizó la concentración restante de Cr (VI) mediante espectroscopía de absorción UV-Vis. Las gráficas de Langmuir para la eliminación de Cr (VI) por micro / nanoesferas PANI huecas usando la ecuación de Langmuir:
$$ \ frac {c_e} {q_e} =\ frac {1} {q_m {k} _L} + \ frac {c_e} {q_m} $$ (3)donde q m es la capacidad máxima de eliminación (mg / g), q e son las cantidades de Cr (VI) en equilibrio (mg / g), c e es la concentración de Cr (VI) en equilibrio (mg / L), y k L es la constante de Langmuir.
Resultados y discusión
El PANI tal como se sintetizó se obtuvo mediante polimerización de monómeros con Triton X-100 Micelles como plantillas blandas. La morfología a través de la observación SEM y TEM se muestra en la Fig. 1. Se pueden observar claramente abundantes micro / nanoesferas PANI a partir de la imagen SEM de PANI en la Fig. 1a. Con cuidado, se observa un agujero en la superficie de las micro / nanoesferas, como se muestra en la imagen insertada de la Fig. 1a, que indica que las micro / nanoesferas son huecas. Este resultado se confirma más a través de la imagen TEM (Fig. 1b). Además, dos imágenes muestran que el diámetro de estas micro / nanoesferas está entre 0,5 y 2 μm.

un SEM y b Imágenes TEM de las micro / nanoesferas huecas PANI sintetizadas
La estructura molecular de micro / nanoesferas PANI huecas sintetizadas se caracteriza por espectroscopia FTIR y difracción de rayos X (XRD), mostradas en la Fig. 2. En la Fig. 2a se pueden observar claramente cinco picos característicos. Los picos característicos a 1569 cm −1 y 1496 cm −1 se atribuyen a la vibración de estiramiento C-N del anillo quinoide (Q) y el anillo bencenoide (B), respectivamente. El pico apareció a 1298 cm −1 se debe a la vibración de estiramiento C-H con conjugación aromática [1]. Pico a 1142 cm −1 corresponde a los modos de estiramiento N-Q-N y es un símbolo de la deslocalización de electrones en PANI [1]. Además, el pico de absorción a 824 cm −1 es característica de las vibraciones de flexión fuera del plano C-H del anillo de benceno para-sustituido [25]. Comparando los picos característicos del anillo bencenoide y el anillo quinoide, la intensidad de absorbancia relativa del anillo bencenoide es mayor que la del anillo quinoide. Entonces, se puede deducir que las micro / nanoesferas huecas de PANI están principalmente en forma de esmeralda. La Figura 2b muestra el patrón XRD de micro / nanoesferas PANI huecas sintetizadas, que muestra una alta cristalinidad inusual con picos de difracción centrados en 20.2 ° y 25.4 °, correspondientes a la periodicidad paralela y perpendicular a las cadenas de polímero [25].
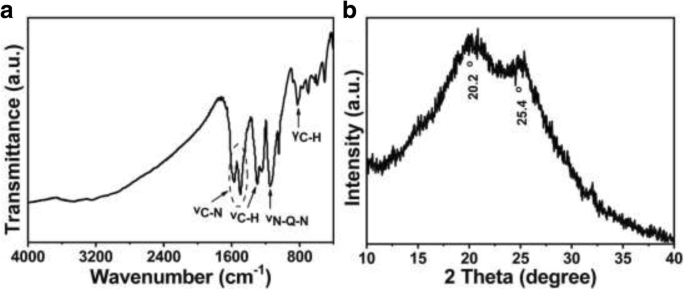
un Espectro FTIR y b Patrones XRD de las micro / nanoesferas PANI huecas sintetizadas
La Figura 3 muestra los resultados de la eliminación de Cr (VI) en diferentes momentos, en los que los valores de pH de la solución de Cr (VI) son 3, 4 y 5, respectivamente. Visto en la Fig. 3a, el color de la solución de Cr (VI) se vuelve más claro bajo el tratamiento con micro / nanoesferas de PANI huecas a medida que aumenta el tiempo. Especialmente, el líquido relativamente claro se obtiene después de 90 min cuando el pH es 3. Y los resultados de que la concentración de Cr (VI) se trató mediante micro / nanoesferas de PANI huecas se muestran directamente en la Fig. 3b. Estos resultados indican que las micro / nanoesferas huecas de PANI son un candidato eficiente para la eliminación de Cr (VI) de la solución en condiciones adecuadas.
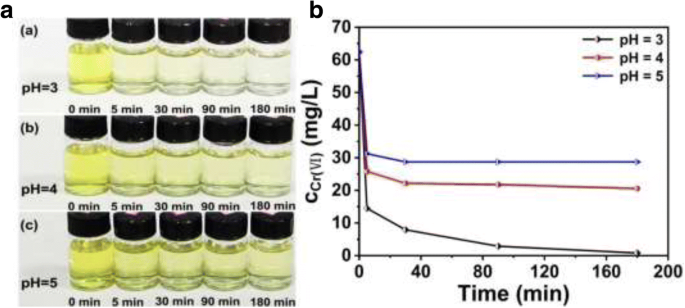
La solución de Cr (VI) después de tratada con micro / nanoesferas de PANI huecas en diferentes tiempos, pH de la solución respectivamente a a 3, b 4 y c 5 (concentración inicial de Cr (VI):1,2 mmol / L (62,4 mg / L)). un Las fotografías y b Concentración de Cr (VI) en la solución final
El valor de pH de la solución es un parámetro importante que afecta las propiedades químicas del Cr (VI) en solución o la protonación o desprotonación del PANI. Por lo tanto, se estudian las capacidades de remoción y reducción de Cr (VI) del PANI sintetizado en solución de diferente pH, como se muestra en la Fig. 4. La Figura 4a muestra los cambios de las concentraciones de Cr y Cr (VI) totales después del tratamiento con huecos. Micro / nanoesferas PANI a diferentes valores de pH, respectivamente. Las capacidades de eliminación de Cr (VI) de las micro / nanoesferas de PANI huecas en diferentes valores de pH se pueden calcular utilizando la Eq. (1). La relación correspondiente entre las capacidades de eliminación de Cr (VI) y los valores de pH se calcula a partir de los valores de la Fig. 4a mediante la Ec. (1) y se muestra en la Fig. 4b. La disminución obvia de la concentración de Cr (VI) como la disminución de los valores de pH de 12 a 1 muestra que las correspondientes capacidades de eliminación de Cr (VI) de las micro / nanoesferas huecas de PANI aumentan con el aumento de la acidez. Especialmente, la capacidad de eliminación de Cr (VI) muestra un rápido aumento cuando el pH es inferior a 4. Sin embargo, la concentración de Cr total muestra un rendimiento anormal cuando el valor de pH es inferior a 2, lo que indica que la concentración de Cr (III) aumenta drásticamente en la solución. Se informó que, a un pH más bajo (pH por debajo de 2), el Cr (III) reducido existía predominantemente en Cr 3+ forma, y la literatura informó que el grado de protonación de las micro / nanoesferas huecas PANI usadas aumentaba rápidamente con la disminución del pH en el pH ácido 1-2 [26, 27]. Por lo tanto, los resultados del experimento anterior se pueden atribuir a que la repulsión electrostática aumenta entre las microesferas huecas de PANI utilizadas y el Cr (III) reducido, lo que supera la interacción de quelación entre ellas, de modo que el Cr (III) entre en solución desde la superficie de PANI, cuando el pH es inferior a 2. Cuando el pH es superior a 2, la tendencia al cambio de la concentración de Cr total es similar a la de Cr (VI) (Fig. 4a), lo que indica que se elimina la mayor parte del Cr (III) reducido de la solución. Afirma que las micro / nanoesferas huecas de PANI son un buen candidato para la eliminación de Cr (VI) cuando el valor de pH está entre 2 y 4.
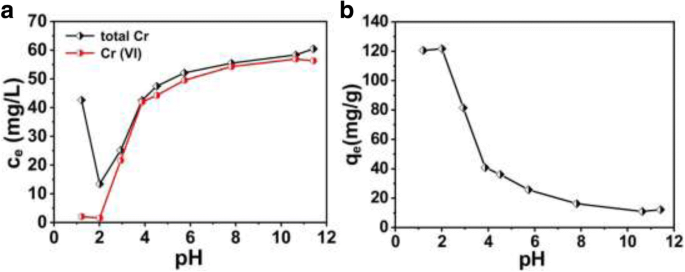
un Los cambios de la concentración de Cr bajo diferentes pH de la solución, y b las capacidades de eliminación de Cr (VI) correspondientes (concentración inicial de Cr (VI):1,2 mmol / L (62,4 mg / L))
Las microesferas huecas de PANI después de la reacción con una solución de Cr (VI) a pH 3, 4 y 5 se investigan más. La Figura 5a-c muestra el análisis de mapeo de elementos de las micro / nanoesferas PANI huecas utilizadas, en las que se observó el elemento Cr además de los elementos C y N. Demuestra directamente que los iones Cr fueron adsorbidos de hecho por micro / nanoesferas huecas PANI. La Figura 5d muestra los espectros XPS de las microesferas huecas PANI usadas a pH 3, 4 y 5, respectivamente, que exhiben la energía de unión del Cr 2p. En los espectros XPS, se pueden observar dos picos; el primero corresponde a 2p 1/2 , el posterior a 2p 3/2 . Comparando las tres líneas del espectro XPS, la energía de enlace del Cr 2p 3/2 se ubica en 577.4 eV y no tiene nada que ver con el valor de pH. Se informó que las bandas de 577,4 eV se pueden atribuir al Cr (III) por analogía con otros compuestos de cromo [12, 28]. Por lo tanto, el Cr adsorbido está principalmente en forma de Cr (III).
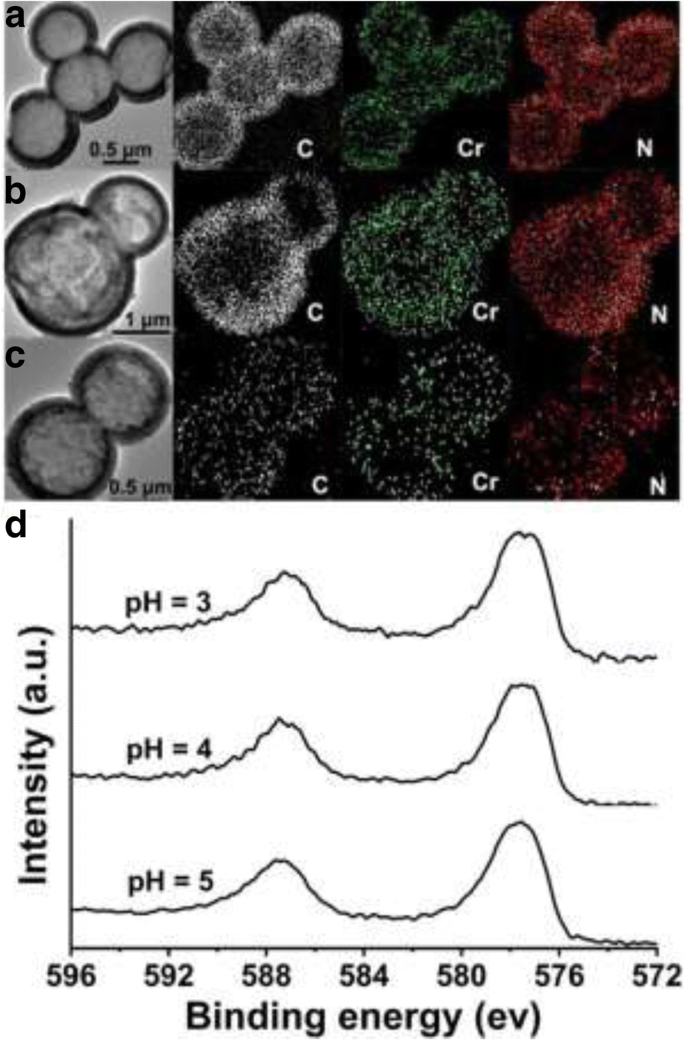
un - c Mapeo de elementos y d Espectros de Cr 2p XPS de las micro / nanoesferas huecas de PANI después de la reacción con Cr (VI) (concentración inicial de Cr (VI):1,2 mmol / L (62,4 mg / L); pH de la solución respectivamente a 3, 4 y 5)
Con base en todos estos resultados, puede resumir el mecanismo de eliminación de Cr (VI) con micro / nanoesferas de PANI huecas de la siguiente manera:el Cr (VI) se absorbe en la superficie de micro / nanoesferas de PANI (EB) huecas y prístinas. Luego, el Cr (VI) absorbido se reduce a Cr (III). Mientras tanto, el PANI prístino (EB) se oxida a la forma de pernigranilina (PB). El Cr (VI) en solución existe en forma de ion cromato ácido (HCrO 4 - ) dentro del rango de pH (2-6) [25]. En este rango de pH, una porción de EB PANI está protonada y el grupo amina (-NH-) de sus moléculas existe como grupo amina (-NH 2 + -). Por lo tanto, el Cr (VI) adsorbido por micro / nanoesferas PANI huecas se logra a través de la interacción electrostática entre PANI de carga positiva y HCrO de carga negativa 4 - . El potencial zeta y el tamaño de partícula de las muestras se midieron con Zetasizer 3000HSa, y los resultados muestran que el potencial zeta es 38,6 mV y 32,9 mV, y el tamaño de partícula es de aproximadamente 990 nm y 630 nm para PANI antes y después de Cr (VI). eliminación a pH 3, respectivamente. Significa que el PANI de antes y después de la eliminación de Cr (VI) puede existir de forma estable en la solución. Comparando la estructura molecular de EB y PB PANI, se puede encontrar que la solvatación de EB PANI de amina secundaria aromática es mayor que la de PB PANI de amina terciaria aromática, porque la amina secundaria lleva un átomo de hidrógeno más que la amina terciaria [ 29]. Por lo tanto, el tamaño de partícula aparente de EB PANI es mayor que el de PB PANI.
Como sabemos, la capacidad de eliminación de Cr (VI) depende principalmente del área de superficie específica de las micro / nanoesferas huecas de PANI. El área de superficie específica de micro / nanoesferas de PANI huecas se puede obtener mediante análisis de adsorción-desorción de nitrógeno (que se muestra en la Fig. 6), y el área de superficie BET se puede calcular en 32,813 m 2 / g, lo que indica una mayor superficie específica de micro / nanoesferas de PANI huecas.
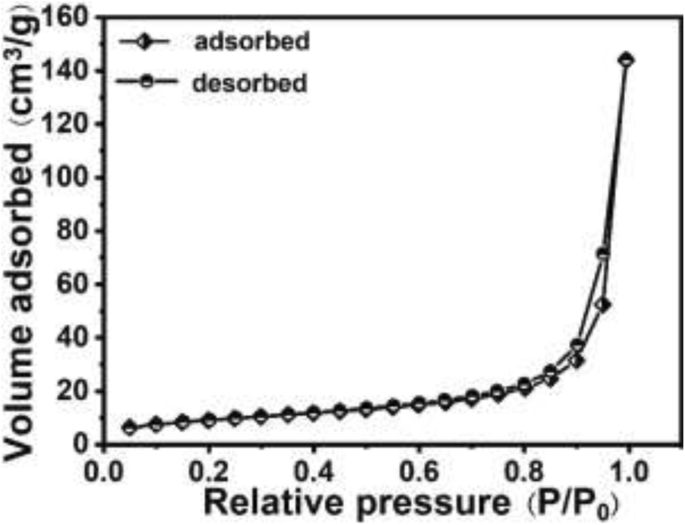
Isotermas de adsorción-desorción de nitrógeno de las micro / nanoesferas huecas PANI sintetizadas
La Figura 7a muestra la relación entre la capacidad de remoción q t de Cr (VI) y el tiempo t para solución con diferentes valores de pH. La capacidad de eliminación aumenta rápidamente en la etapa inicial (0 ~ 5 min) y luego continúa aumentando lentamente hasta el equilibrio después de aproximadamente 120 min. Indica que la remoción inicial ocurre en la superficie de micro / nanoesferas PANI huecas y luego procede hacia la parte interna [25].
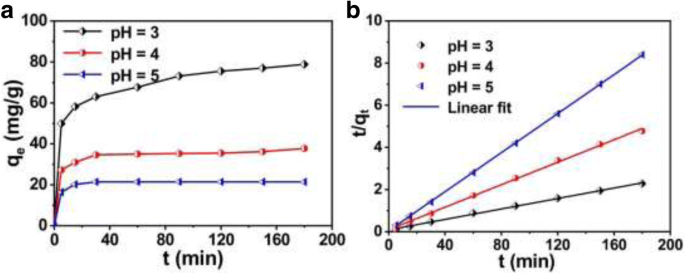
un Cambios en la concentración de Cr (VI) en diferentes momentos (concentración inicial de Cr (VI):1,2 mmol / L (62,4 mg / L), pH de la solución respectivamente a 3, 4 y 5) y b los modelos de pseudo-segundo orden sobre la cinética de eliminación de Cr (VI) con micro / nanoesferas PANI huecas
Para explorar la cinética de eliminación de Cr (VI) con micro / nanoesferas PANI huecas, se emplean algunos modelos que contienen los modelos de pseudo-primer orden y pseudo-segundo orden para interpretar los datos del experimento. Aquí, el pseudo-segundo orden es el modelo más apropiado para ajustar los datos experimentales, comparando los datos del experimento con estos modelos teóricos. La Figura 7b muestra las gráficas cinéticas teóricas de acuerdo con la ecuación de pseudo-segundo orden. (2). El resultado muestra que t / q t versus t eran lineales y los coeficientes de correlación R 2 corresponden a 0,99788, 0,99817 y 0,99994, para pH 3, 4 y 5, respectivamente. Además, los valores de q e se puede calcular a partir de la pendiente, es decir, 80,654, 37,48 y 21,56 mg / g correspondientes a un valor de pH de 3, 4 y 5, respectivamente, que se acercan a los valores experimentales que se muestran en la Fig. 7a.
Las capacidades de eliminación de Cr (VI) de las micro / nanoesferas huecas de PANI también están relacionadas con la concentración de Cr (VI). Por tanto, es importante investigar el efecto de la concentración de Cr (VI) sobre las capacidades de eliminación de micro / nanoesferas huecas PANI. El experimento se llevó a cabo a pH 3, 4 y 5, respectivamente, con varias concentraciones iniciales de Cr (VI). La Figura 8a muestra los cambios de la capacidad de eliminación de Cr (VI) ( q e (mg / g)) versus concentración de equilibrio ( c e (mg / L)). Como se muestra en la Fig. 8a, la capacidad de eliminación aumenta más rápidamente a una concentración más baja de Cr (VI) y tiende a ser un valor constante a una concentración más alta, es decir, se logra la capacidad máxima de eliminación de Cr (VI) de las micro / nanoesferas huecas de PANI. Para describir el resultado experimental de la isoterma de eliminación de Cr (VI), se seleccionan tres modelos de isotermas importantes, que son los modelos de Langmuir, Freundlich y Temkin. Sin embargo, solo el modelo de Langmuir puede ajustarse a los datos experimentales. La Figura 8b muestra las gráficas de Langmuir para la eliminación de Cr (VI) por micro / nanoesferas PANI huecas, el Langmuir Eq. (3). El resultado muestra que c e / q e versus c e es lineal a pH 3, 4 y 5, respectivamente (coeficiente de correlación R 2 =0,99950, 0,99875 y 0,99962 a pH 3, 4 y 5). Además, los valores de q m que se calcula a partir de la pendiente son 25,61, 43,20 y 127,88 mg / ga pH 5, 4 y 3, respectivamente, que están cerca de los valores experimentales que se muestran en la Fig. 8a. La isoterma de Langmuir se basa en el supuesto de que no hay interacción entre el adsorbente de estructura homogénea y la cobertura monocapa. La eliminación de Cr (VI) de la solución en la micro / nanoesfera PANI hueca coincide con el modo monocapa. Puede afirmar que no se puede producir más adsorción cuando los sitios activos en la superficie de las micro / nanoesferas huecas de PANI están ocupados por Cr (VI).
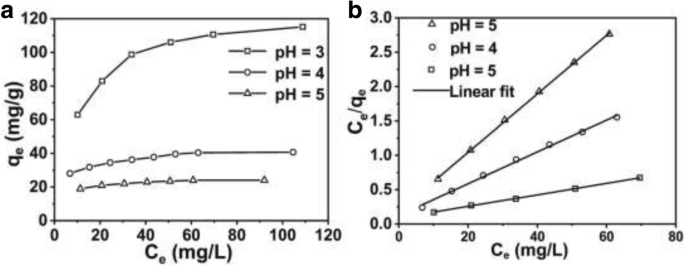
un La capacidad de eliminación de Cr (VI) a diferentes concentraciones de equilibrio (pH de la solución respectivamente a 3, 4 y 5) y b modelo de isoterma de eliminación de Langmuir correspondiente
La comparación de la capacidad máxima de remoción de Cr (VI) de las micro / nanoesferas huecas de PANI sintetizadas en este estudio con lo reportado en la literatura se muestra en la Tabla 1. Puede verse que las micro / nanoesferas huecas de polianilina exhiben Cr (VI ) capacidad de eliminación que la de muchos otros removedores. Estos resultados sugieren que las micro / nanoesferas huecas de PANI pueden considerarse un material prometedor para la eliminación de Cr (VI) de una solución acuosa.
Sobre la base de los resultados antes mencionados, el proceso de eliminación de Cr (VI) se puede explicar como sigue. La solución inicial contiene Cl - , H + , HCrO 4 - iones, etc. (Fig. 9a). En condiciones de medio ácido, el estado de oxidación de la esmeralda de los iones PANI (EB) y Cr (VI) se oxidan y reducen al estado de pernigranilina (PB) y Cr 3+ iones, respectivamente (Fig. 9b). El procedimiento de reacción principal se puede demostrar de la siguiente manera en solución ácida [36]:
$$ 3 \ mathrm {PANI} \ \ left (\ mathrm {EB} \ right) +6 {\ mathrm {Cl}} ^ {\ hbox {-} 1} \ hbox {-} 6 {\ mathrm {e} } ^ {\ hbox {-} 1} \ to 3 \ mathrm {PANI} {\ left (\ mathrm {Cl} \ right)} _ 2 \ left (\ mathrm {PB} \ right) $$ (4) $$ 2 {{\ mathrm {H} \ mathrm {CrO}} _ 4} ^ {\ hbox {-} 1} \ kern0.5em +14 {\ mathrm {H}} ^ {+} \ kern0.5em +6 {\ mathrm {e}} ^ {\ hbox {-} 1} \ kern0.5em \ to 2 {\ mathrm {Cr}} ^ {3 +} \ kern0.5em + \ kern0.5em 8 {\ mathrm {H}} _2 \ mathrm {O} $$ (5)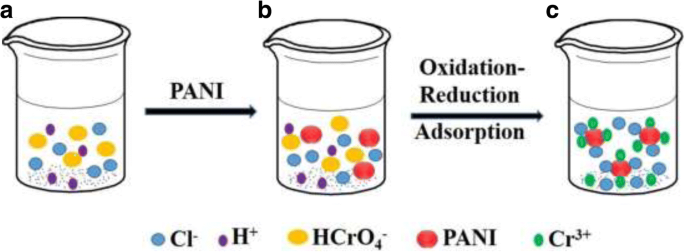
El diagrama esquemático de la eliminación de Cr (VI). un Aguas residuales que contienen Cr (VI) en condiciones ácidas, b agregar PANI a las aguas residuales que contienen Cr (VI) y c eliminación de aguas residuales de Cr (VI)
Esta reacción ocurre simultáneamente en la superficie de PANI. El Cr 3+ resultante Los iones se absorben en la superficie de las micro / nanoesferas PANI (Fig. 9c). Como se mencionó anteriormente, las micro / nanoesferas PANI son esferas huecas, y la mayoría de las esferas huecas tienen muchos agujeros, por lo que la superficie exterior e interior de las micro / nanoesferas PANI pueden absorber una gran cantidad de Cr 3+ iones debido a la estructura hueca (Fig. 1).
Se informó que la pernigranilina es inestable en condiciones ambientales y se reduce fácilmente al estado de oxidación de esmeralda en una solución ácida fuerte, como HCl y H 2 SO 4 [26]. Esto indica que las micro / nanoesferas huecas de PANI usadas se pueden regenerar fácilmente mediante tratamiento con ácido. La conversión entre el estado de pernigranilina y esmeralda se puede mostrar como el Esquema 1. Por ejemplo, las micro / nanoesferas de PANI huecas usadas se tratan adicionalmente con HCl 1 M durante 0,5 hy luego se reutilizan para la eliminación de Cr (VI). Se puede encontrar en la Tabla 2 que la capacidad de remoción de las primeras micro / nanoesferas de PANI huecas reutilizadas probablemente esté cerca de la capacidad de remoción de PANI inicial [26, 37]. Se puede concluir que las micro / nanoesferas huecas de PANI son un material reproducible para la eliminación de Cr (VI).
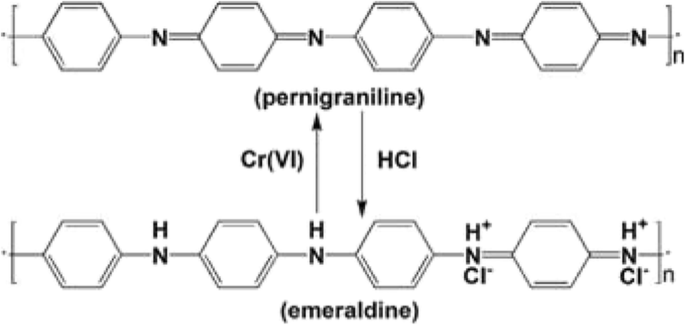
Ilustración esquemática de la conversión entre pernigranilina y esmeralda de PANI
Conclusiones
Se ha fabricado una gran cantidad de micro / nanoesferas de PANI huecas mediante una simple polimerización de monómero en solución alcalina con Triton X-100 Micelles como plantillas. Las micro / nanoesferas huecas pueden eliminar rápida y eficazmente el Cr (VI) en un amplio rango de pH. Los datos de la cinética de eliminación se ajustan al pozo del modelo de pseudo-segundo orden y la isoterma de eliminación de Cr (VI) se puede describir mediante el modelo de isoterma de Langmuir. La capacidad máxima de eliminación de las micro / nanoesferas huecas de PANI puede alcanzar 127,88 mg / ga pH 3. Además, las micro / nanoesferas huecas de PANI usadas pueden regenerarse fácilmente mediante tratamiento con solución ácida, manteniendo aproximadamente la misma eliminación de Cr (VI) capacidad. El presente trabajo indica que las micro / nanoesferas huecas de PANI son un material eficaz y reproducible para eliminar el Cr (VI) tóxico de las aguas residuales.
Abreviaturas
- APS:
-
Persulfato de amonio
- B:
-
Anillo benzenoide
- EB:
-
Esmeralda
- FESEM:
-
Microscopio electrónico de barrido por emisión de campo
- FTIR:
-
Espectroscopía infrarroja por transformada de Fourier
- ICP:
-
Espectrómetro de emisión de plasma acoplado inductivamente
- LB:
-
Leucoemeraldina
- PANI:
-
Polianilina
- PB:
-
Pernigranilina
- P:
-
Anillo de quinoide
- TEM:
-
Microscopio electrónico de transmisión
- XPS:
-
Espectroscopia de fotoelectrones de rayos X
- XRD:
-
Difracción de rayos X
Nanomateriales
- Tanto Tesla como Panasonic eliminarán el cobalto de sus baterías
- La transmisión de deportes atrae a más espectadores (y capacidad de red) en 2019
- Justificación de la automatización en su fábrica:lo que debe hacer, lo que no debe hacer y los consejos de los expertos
- Cómo Ingram Micro aporta valor del canal a socios y clientes
- Eliminación por adsorción de iones de cobre (II) de una solución acuosa utilizando un nano-adsorbente de magnetita de residuos de cascarilla de molino:síntesis, caracterización, adsorción y mode…
- Preparación y propiedades magnéticas de nanopartículas de espinela de FeMn2O4 dopadas con cobalto
- Preparación de nanopartículas de mPEG-ICA cargadas con ICA y su aplicación en el tratamiento del daño celular H9c2 inducido por LPS
- Hacia los nanofluidos de TiO2:Parte 1:Preparación y propiedades
- Preparación de nanobarras de alúmina a partir de lodos de alúmina que contienen cromo
- Preparación y rendimiento fotocatalítico de fotocatalizadores LiNb3O8 de estructura hueca
- Preparación de micromateriales híbridos de MnO2 recubiertos de PPy y su rendimiento cíclico mejorado como ánodo para baterías de iones de litio



