Efecto de los tensioactivos sobre las microestructuras de las nanoflores en flor de SnO2 jerárquicas y sus propiedades de detección de gases
Resumen
SnO 2 jerárquico Las nanoflores en flor se fabricaron con éxito mediante un método hidrotermal simple pero fácil con la ayuda de diferentes tensioactivos. Aquí nos enfocamos en explorar los efectos de promoción de los surfactantes en el autoensamblaje de 2D SnO 2 nanohojas en 3D SnO 2 estructuras similares a flores, así como sus funciones de detección de gases. El SnO 2 con forma de flor poliporosa El sensor exhibe un excelente rendimiento de detección de gas frente al etanol y H 2 S gas debido a la alta porosidad cuando se añade polivinilpirrolidona a la solución precursora como tensioactivo. Los tiempos de respuesta / recuperación fueron de aproximadamente 5 s / 8 s para 100 ppm de etanol y 4 s / 20 s para 100 ppm de H 2 S, respectivamente. Especialmente, el valor de respuesta máximo de H 2 Se estima que S es 368 a 180 ° C, que es uno o dos órdenes de magnitud más alto que el de otros gases de prueba en este estudio. Eso indica que el sensor fabricado con la ayuda de polivinilpirrolidona tiene una buena selectividad para H 2 S.
Antecedentes
Los sensores de gas han atraído una atención generalizada debido a sus posibles aplicaciones en la detección de gases tóxicos, nocivos, inflamables y explosivos [1]. En la actualidad, los semiconductores de óxido metálico ocupan una posición importante en varios sensores debido a su sencillo proceso de preparación, menor costo y mayor sensibilidad a los gases objetivo [2, 3, 4]. Dióxido de estaño (SnO 2 ), un material multifuncional de tipo n con una banda prohibida directa de 3,6 eV [5], se ha utilizado ampliamente tanto en estudios fundamentales como en aplicaciones prácticas, como sensores de gas [6], catálisis [7] y dispositivos optoelectrónicos [8 ]. Especialmente, SnO 2 ha sido considerado como el material de detección con mayor potencial debido a su no estequiometría natural [9], alta sensibilidad, rápida respuesta / velocidad de recuperación y alta estabilidad química [10].
Es bien sabido que el mecanismo de detección de gas de los óxidos metálicos está relacionado con los procesos de adsorción y desorción del gas objetivo en la superficie del sensor, dando lugar a un cambio de la conductividad eléctrica [11]. Estos procesos dependen en gran medida del tamaño, morfología y dimensión, así como de la estructura cristalina de las muestras [12]. Hay dos formas principales de mejorar eficazmente el rendimiento de detección de SnO 2 [13]. Uno es sintetizar materiales compuestos basados en SnO 2 , como la fabricación de uniones p-n, decoración de superficies o dopaje [14]. La otra es preparar varios SnO 2 puros materiales que incluyen nanotubos [15], nanobarras [16], nanoesferas [17], estructuras huecas [14] y nanoflores [18], que tienen nanoestructuras únicas, una gran superficie específica y una gran capacidad de captura de electrones [19]. Recientemente, SnO 2 jerárquico tridimensional (3D) Las nanoestructuras han llamado mucho la atención debido a su mejor rendimiento de detección de gas causado por una gran superficie específica y una rápida difusión gaseosa en comparación con las nanoestructuras 1D y 2D [20]. Se han utilizado varias técnicas para fabricar nanoestructuras 3D de SnO 2 [21], como la deposición química en fase de vapor [22], el método sintético solvotermal [23], el método molde [24], el método sol-gel [25] y la ruta hidrotermal [26]. Entre ellos, las rutas solvotermales e hidrotermales con bajo costo [27], altos rendimientos y manipulación simple han demostrado ser los métodos prometedores para sintetizar SnO jerárquico 3D 2 nanoestructuras. Por ejemplo, Dong et al. SnO hueco preparado 2 nanoesferas con un diámetro que varía de 200 a 400 nm utilizando un método de síntesis solvotermal [28]. Li y col. fabricó un novedoso SnO 2 similar a un copo de nieve Arquitectura jerárquica con excelentes propiedades de detección de gases a través de un método hidrotermal fácil [29]. Además, Chen et al. Sintetizado con éxito SnO 2 similar a una flor jerárquica nanoflores florecientes construidas mediante el autoensamblaje de muchas nanohojas de forma regular mediante un método hidrotermal convencional [30].
La aplicación práctica de SnO 2 sensores todavía está limitado en cierta medida debido a la temperatura de trabajo relativamente más alta y la selectividad más pobre para los gases de prueba [31]. Para mejorar las propiedades de detección de gases, los investigadores han prestado atención a la síntesis controlable de SnO 2 similar a una flor en 3D nanoestructuras con efectos tensioactivos [32], sin embargo, se plantea un desafío importante debido a la variedad de tensioactivos.
En el presente estudio, informamos una optimización bien controlada de SnO 2 jerárquico 3D nanoflores basadas en el autoensamblaje de nanoláminas delgadas con la ayuda de diferentes tensioactivos en condiciones hidrotermales. Nuestro estudio sistemáticamente comparativo de detección de gas entre sensores fabricados se centra en el efecto de promoción de los tensioactivos en el comportamiento de los sensores. Los resultados muestran que los tensioactivos anfifílicos no iónicos, como PVP y Triton X-100, pueden ser candidatos potenciales para optimizar la morfología de nanoflores 3D con alta porosidad y gran superficie específica. En particular, el sensor basado en PVP presenta una alta respuesta, un tiempo de respuesta rápido y una buena selectividad para H 2 S a una temperatura relativamente más baja. Además, un posible mecanismo de crecimiento bien controlado de SnO 2 Se proponen nanoestructuras.
Métodos / Experimental
Se utilizaron citrato trisódico dihidrato y cloruro de estaño dihidrato de Sinopharm Chemical Reagent Co., Ltd. como precursores para SnO 2 síntesis. Se adquirieron polietilenimina, hexametilen tetramina, TritonX-100 y polivinilpirrolidona de Aldrich Chemistry y se utilizaron como agentes directores de estructura. Se utilizó agua destilada a lo largo de los experimentos. Todos los productos químicos eran de calidad analítica y se usaron tal como se compraron sin ninguna purificación adicional.
Síntesis de SnO 2 Nanoflores con diferentes arquitecturas
Un procedimiento de síntesis típico con un método hidrotermal simple se puede describir como sigue (Fig.1):en primer lugar, se añadieron 5 mmol de NaOH a una mezcla de 80 ml de etanol anhidro y agua desionizada (1:1) con agitación magnética. Luego, 20 mmol de Na 3 C 6 H 5 O 7 · 2H 2 O y 10 mmol de SnCl 2 · 2H 2 Se disolvieron O en la solución mixta sucesivamente con agitación vigorosa durante 1 ha temperatura ambiente. La solución mezclada se transfirió luego a un autoclave de acero inoxidable revestido con teflón de 100 ml y se mantuvo a 180 ° C durante 12 h, y luego se enfrió a temperatura ambiente de forma natural. Después de la reacción, el precipitado obtenido se recogió por centrifugación, se lavó con agua desionizada y etanol anhidro varias veces y se secó a 60 ° C durante 6 h. El SnO 2 Las nanoflores finalmente se obtuvieron después de calcinar el precipitado en un horno de mufla en condiciones de aire ambiente a 500 ° C durante 2 h. Para sintetizar SnO 2 nanoflores con diferentes microestructuras, diferentes agentes tensioactivos (1,0 g) se introdujeron en la solución respectivamente antes de la disolución de Na 3 C 6 H 5 O 7 · 2H 2 O. En este trabajo, se utilizaron cuatro tipos diferentes de tensioactivos, incluidos PVP, PEI, HMT y TritonX-100, y los productos finales correspondientes se denominan S PVP , S PEI , S HMT y S TritonX-100 , respectivamente, mientras que el producto sin tensioactivo está firmado como S 0 .
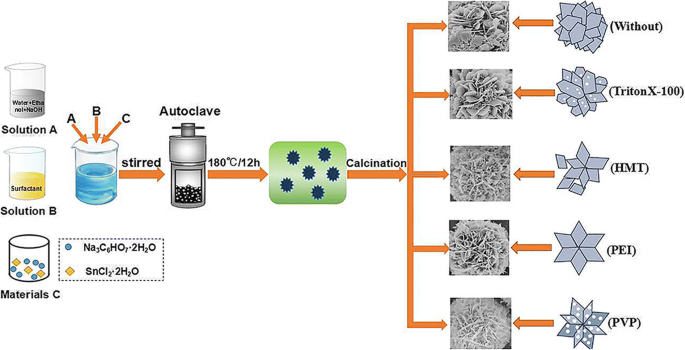
Ilustración esquemática del proceso de formación del SnO 2 jerárquico con forma de flor nanoestructuras que utilizan diferentes tipos de tensioactivos
Caracterizaciones
Es bien sabido que las propiedades de detección de gas de los sensores de gas están muy relacionadas con la morfología, el tamaño y la dispersabilidad de los nanomateriales. Los productos preparados se analizaron en términos de sus estructuras y morfologías mediante difracción de rayos X policristalina (XRD, Alemania Bruker AXS D8 Advance), microscopía electrónica de barrido (SEM, USA FEI Sirion 200) y microscopía electrónica de transmisión de campo. (FETEM, EE. UU. Tecnai G2 F20 S-TWIN). El área de la superficie se mide con el analizador elemental (EE. UU. ASAP 2460) basado en el método Brunauer-Emmett-Teller (BET).
Prueba de detección de gas y fabricación de sensores
El sensor de gas se fabricó usando el método de serigrafía en la parte superior de un tubo de alúmina (visto en la Fig. 2a). Típicamente, en primer lugar se mezcló una cantidad adecuada de polvo tal como se preparó con etanol anhidro para formar una suspensión espesa. Posteriormente, la suspensión de lodo se revistió sobre el tubo de alúmina mediante un cepillo pequeño, que está soportado por dos electrodos de Au y cuatro alambres conductores de Pt. A continuación, se insertó un alambre calefactor de Ni-Cr en el tubo de alúmina para controlar la temperatura de trabajo ajustando el voltaje de calentamiento. Finalmente, el producto se envejeció a 80 ° C durante 72 h antes de la prueba.

un Diagrama esquemático de la configuración del sensor de gas. b Diagrama de circuito eléctrico del dispositivo sensor
Las propiedades de detección de gas se midieron utilizando un sistema de análisis inteligente de detección de gas con sensor químico de gas 4, temperatura, presión, pequeño (CGS-4TP) (Beijing Elliott Technology Co., Ltd., China) en condiciones de laboratorio. La Figura 2b muestra el circuito eléctrico esquemático típico. R s es la resistencia del sensor y R l es la resistencia de carga y un voltaje de calentamiento (V h ) se utiliza para ajustar la temperatura de trabajo. En el presente trabajo, la respuesta del sensor se definió como S =(R s - R g ) / R g , donde Rs es la resistencia inicial y Rg es la resistencia después de la inyección de gases. Los tiempos de respuesta y recuperación se definen como el tiempo que tarda el sensor en alcanzar el 90% del cambio de resistencia total en el caso de adsorción y desorción, respectivamente.
Resultados y discusión
Caracterización estructural y morfológica
La fase cristalina del SnO 2 preparado Los productos se identificaron mediante difracción de rayos X de potencia como se muestra en la Fig. 3. A partir del patrón XRD, todos los picos de difracción observados se pueden asignar fácilmente a la estructura tetragonal de rutilo de SnO 2 puro con la tarjeta de archivo JCPDS estándar no. 41-1445, y no se pueden identificar otros picos debido a impurezas. Los picos agudos indican el alto grado de cristalinidad de nuestro SnO 2 muestras, y no se detecta ningún cambio notable en los picos de difracción, lo que revela que las muestras son de alta pureza.
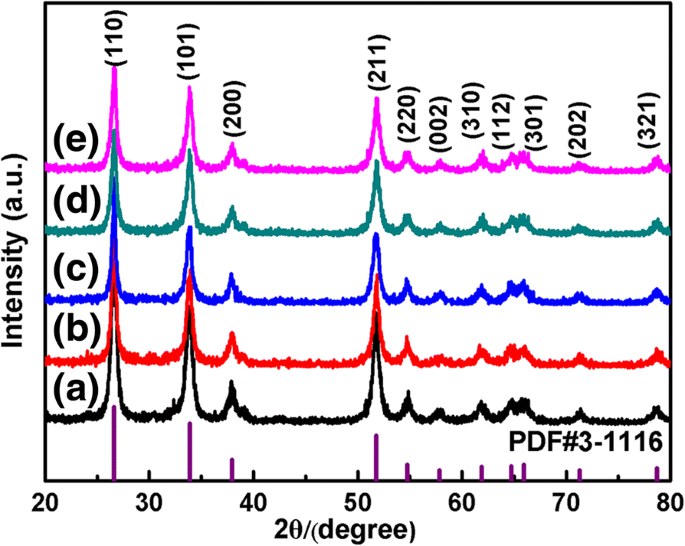
Patrones XRD del SnO 2 muestras con diferentes morfologías. un S 0 , b S TritonX100 , c S HMT , d S PEI y e S PVP
La Figura 4a muestra la imagen SEM del producto sin tensioactivo. Se puede observar una arquitectura jerárquica similar a una flor y las nanoflores únicas se ensamblan mediante nanohojas ultrafinas con un grosor promedio de 20 nm alrededor. Desafortunadamente, estas nanohojas están muy escalonadas entre sí, lo que resulta en una fuerte disminución de sus espacios de reacción. La Figura 4b-e muestra las morfologías de los productos obtenidos mediante la introducción de diferentes agentes tensioactivos manteniendo inalteradas otras condiciones experimentales. Se puede ver que tras la adición de tensioactivo TritonX-100 (Fig. 4b), las nanohojas se entrecruzan libremente entre sí, y algunos mesoporos se forman en el borde de las nanohojas. Cuando se añadió HMT a la mezcla de reacción como agentes tensioactivos (Fig. 4c), se puede ver que las nanohojas están dispuestas al azar y se forman varias nanohojas más pequeñas entre nanohojas ultrafinas. La Figura 4d muestra las imágenes SEM de los productos obtenidos al introducir el surfactante PEI en la solución precursora, lo que revela que las nanohojas con superficies lisas están dispuestas ordenadamente y se intersecan verticalmente entre sí, dejando un mayor espacio de reacción. La Figura 4e, f presenta las imágenes típicas de SEM de los productos obtenidos tras la adición de tensioactivo PVP en las mismas condiciones. Se puede ver que las nanohojas se distribuyen uniformemente a lo largo del radio en toda la muestra para formar una estructura similar a una flor. Además, en comparación con otras estructuras de S TritonX-100 , S HMT y S PEI , las nanohojas de S PVP están encerrados en un cono triangular invertido con un espacio hueco relativamente mayor (Fig. 4e). Una imagen más ampliada revela que las arquitecturas en forma de flor están ensambladas por nanohojas mesoporosas para formar una estructura jerárquica porosa abierta, y cada nanohoja se fabricó con numerosos mesoporos (Fig. 4f).

Las imágenes SEM del SnO 2 nanoflores con diferentes morfologías. un S 0 , b S TritonX-100 , c S HMT , d S PEI y e , f S PVP
Para investigar más a fondo las microestructuras y las propiedades cristalinas de las nanoflores, se emplean TEM de bajo aumento y HRTEM típico combinados con las técnicas de análisis de difracción de electrones de área seleccionada (SAED). De las imágenes TEM (Fig. 5a-e), se puede ver que las nanoflores con un diámetro promedio de 3 μm están ensambladas de numerosas nanohojas individuales, y su morfología y tamaño son similares a las imágenes SEM. Especialmente, la imagen TEM de S PVP (Fig. 5e) muestra que la estructura más parecida a una flor con el color oscuro uniforme en la región media se construye a partir de la dispersión del pozo de numerosas nanoláminas uniformes a lo largo de la dirección del radio. Combinando las mediciones de SEM con TEM, se puede llegar a la conclusión de que las estructuras obtenidas tras la adición de tensioactivo PVP son las más estables. Las imágenes TEM de alta resolución (HRTEM) muestran que para las muestras S 0 , S HMT , S PEI y S PVP , el espaciado de celosía de 0.335 nm observado es consistente con el plano de celosía (110) del rutilo tetragonal SnO 2 (La Fig. 5f solo muestra una imagen típica de HRTEM para S HMT como representante). La exposición del plano reticular (110) revela que el plano reticular (110) es el plano más estable para SnO 2 en el aire, lo cual es consistente con el estudio teórico. Cabe señalar que S TritonX-100 es un caso especial en este trabajo (Fig. 5b). Tras la adición del tensioactivo TritonX-100, el crecimiento y la dispersión de las nanohojas conducen aleatoriamente a un diámetro relativamente mayor (3 ~ 4 μm) de las nanoflores en comparación con otras muestras. Además, su imagen HRTEM muestra que el espaciado de celosía calculado es 0.264 nm, que corresponde al plano de celosía (101) de la estructura tetragonal de rutilo de SnO 2 . Además, el patrón SAED revela que S PVP tiene una estructura monocristalina casi perfecta, y los puntos de difracción corresponden a (110), (\ (1 \; \ overline {1} \; 0 \)), (\ (\ overline {1} \; 1 \; 0 \)) y (200) planos de celosía de SnO 2 (Figura 5h). Por el contrario, para otras muestras como S 0 , S HMT , S PEI y S TritonX-100 , el patrón SAED muestra una estructura policristalina, y el anillo de difracción está indexado a los planos (110), (101) y (211) de la estructura tetragonal de rutilo de SnO 2 (Figura 5g).
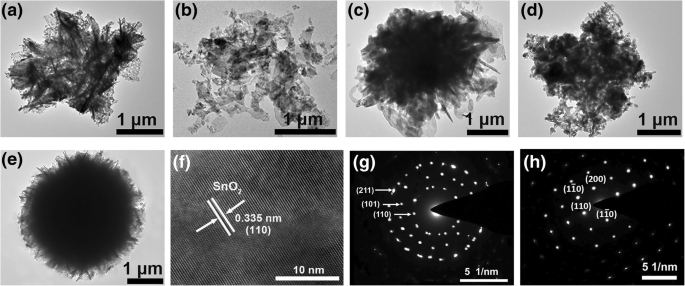
Imágenes TEM de bajo aumento de SnO 2 muestras. un S 0 , b S TritonX-100 , c S HMT , d S PEI y e S PVP . f Micrografía HRTEM que muestra imágenes de celosía agrandadas de S HMT . g Patrones SAED de S 0 . h Patrones SAED de S PVP
Mecanismo de crecimiento del SnO 2 Nanoflores
Según las observaciones experimentales y el análisis anterior, se cree que los tensioactivos desempeñan un papel importante en la formación de varios SnO 2 nanoflores [33]. El posible mecanismo de crecimiento de SnO 2 jerárquico de hoja-flor nanoestructuras se ilustra brevemente en la Fig. 1. En este trabajo, todos los SnO 2 las nanoflores se sintetizan utilizando SnCl 2 como precursor [34]. En condiciones hidrotermales, la reacción general para el crecimiento de SnO 2 Los cristales con alta temperatura y presión se pueden expresar de la siguiente manera [35]:
$$ {\ mathrm {SnCl}} _ 2 + 2 {\ mathrm {OH}} ^ {-} \ to \ mathrm {Sn} {\ left (\ mathrm {OH} \ right)} _ 2 + 2 {\ mathrm { Cl}} ^ {-} $$ (1) $$ \ mathrm {Sn} {\ left (\ mathrm {OH} \ right)} _ 2 \ to \ mathrm {Sn} \ mathrm {O} + {\ mathrm { H}} _ 2 \ mathrm {O} $$ (2) $$ \ mathrm {SnO} + \ frac {1} {2} {\ mathrm {O}} _ 2 \ to {\ mathrm {SnO}} _ 2 $$ (3) $$ \ mathrm {Sn} {\ left (\ mathrm {OH} \ right)} _ 2+ \ frac {1} {2} {\ mathrm {O}} _ 2 + {\ mathrm {H}} _ 2 \ mathrm {O} \ to \ mathrm {Sn} {\ left (\ mathrm {OH} \ right)} _ 4 \ to {\ mathrm {SnO}} _ 2 + 2 {\ mathrm {H}} _ 2 \ mathrm {O} $ $ (4)Durante todo el proceso, tres sustancias químicas afectan en gran medida el crecimiento morfológico del SnO 2 nanoflores, incluido NaOH, citrato de sodio y el tensioactivo. En primer lugar, se formaron varios nanocristales primarios diminutos debido a la hidrólisis de Sn 2+ en una solución básica de etanol-agua, así como su rápida reacción con OH - iones de NaOH. Cabe señalar que el entorno básico de etanol-agua es importante para estimular el SnO 2 nucleación y crecimiento [36]. La adición de citrato de sodio juega un papel crucial en la distribución espacial de los precursores debido a su fuerte capacidad de coordinación, que puede promover una anisotropía en el rápido crecimiento y agregación de SnO 2 nanohojas con la fuerza impulsora de la energía superficial decreciente y acelerar el ensamblaje de nanohojas en las nanoflores florecientes jerárquicas estables [37].
Generalmente, la adición de tensioactivos favorece la ampliación de la superficie así como la mejora de la actividad superficial [38]. Entre los tensioactivos utilizados en este trabajo, el PEI es un tipo de tensioactivos catiónicos. Cuando se agrega PEI a las soluciones de reacción, debido al N + existente iones con una cola hidrófila, PEI se adsorberá preferentemente en una determinada faceta del cristal, lo que conduce a la nucleación de SnO 2 nanocristales, así como el crecimiento ordenado de SnO 2 nanohojas con selectividad direccional. Tanto PVP como TritonX-100 son tensioactivos anfifílicos no iónicos, que pueden servir como una plantilla blanda en la fabricación de materiales mesoporosos. Tomemos PVP, por ejemplo, para explicar el mecanismo de crecimiento de estructuras porosas en SnO 2 nanohojas de la siguiente manera:cuando se agrega PVP a la solución, las moléculas de PVP se autoensamblan en micelas esféricas debido a la fuerte atracción hidrófoba entre las colas de alquilo rectas. Debido a su anfifilicidad, el radical hidrófilo se moverá hacia la dirección de la solución acuosa, y el radical hidrófobo se moverá en la dirección opuesta, conduciendo a la formación de dominios inorgánicos alrededor de las micelas de PVP dispuestas periódicamente. Entonces, Sn 2+ y OH - Los iones se adsorben fácilmente en las superficies externas de estas micelas a través de interacciones electrostáticas hasta que SnCl 2 se oxida en SnO 2 nanohojas, que son seguidas por el autoensamblaje de nanohojas en nanoflores florecientes con la ayuda de citrato de sodio. Finalmente, las micelas de PVP de plantilla blanda se eliminan durante el proceso de calcinación, produciendo SnO 2 jerárquico nanoflores con estructuras mesoporosas. Aunque tanto PVP como Triton X-100 contribuyeron a la formación de estructuras porosas, cabe señalar que PVP también puede desempeñar un papel de agente dispersante, lo que hace que el SnO 2 las nanohojas crecen de manera más uniforme y separada debido a las interacciones fuertes y las distancias de interacción electrostática cortas entre el SnO 2 nanohojas y PVP.
Propiedades de detección de gas
Como se informó anteriormente, las nanoestructuras similares a flores jerárquicas fueron favorables para la absorción y difusión de los gases de la sonda en los materiales del sensor. Para arrojar luz sobre el efecto de promoción de los tensioactivos y la morfología correspondiente sobre el comportamiento del sensor, en este trabajo se realiza un estudio sistemáticamente comparativo de detección de gas entre sensores fabricados.
Comportamientos de detección de gas de sensores fabricados a etanol
La temperatura de funcionamiento óptima es un factor clave para la aplicación de sensores de gas de óxido semiconductor. En primer lugar, se prueban las respuestas de los sensores a 100 ppm de gas etanol a diversas temperaturas de funcionamiento de 180 a 360 ° C como se muestra en la Fig. 6a. Se observa claramente que todos estos sensores exhiben un comportamiento de detección de gas similar, es decir, los valores de respuesta primero aumentan con un aumento de temperatura, alcanzan un valor máximo a 270 ° C y luego disminuyen gradualmente con un aumento adicional de temperatura. Por lo tanto, se puede elegir 270 ° C como la temperatura de funcionamiento optimizada para el estudio de detección de gas de todo SnO 2 similar a una flor fabricado sensores en nuestro trabajo. El motivo de la dependencia de la respuesta de la temperatura es el siguiente:cuando la temperatura de funcionamiento es demasiado baja, se asigna un valor de respuesta relativamente menor a la respuesta inerte debido a la activación química, mientras que para una temperatura de funcionamiento demasiado alta, el objetivo de gas absorbido las moléculas pueden escapar de los sensores antes de las reacciones, lo que también da como resultado una respuesta deficiente. Además, se puede ver en la Fig. 6a que de los cinco SnO 2 sensores basados en diferentes tensioactivos, S PVP muestra la mayor respuesta al gas etanol y el mayor valor de respuesta al gas (38). Los valores máximos de respuesta de otros cuatro sensores son 27 para S PEI , 16 para S HMT , 11 para S TritonX-100 y 8 para S 0 .
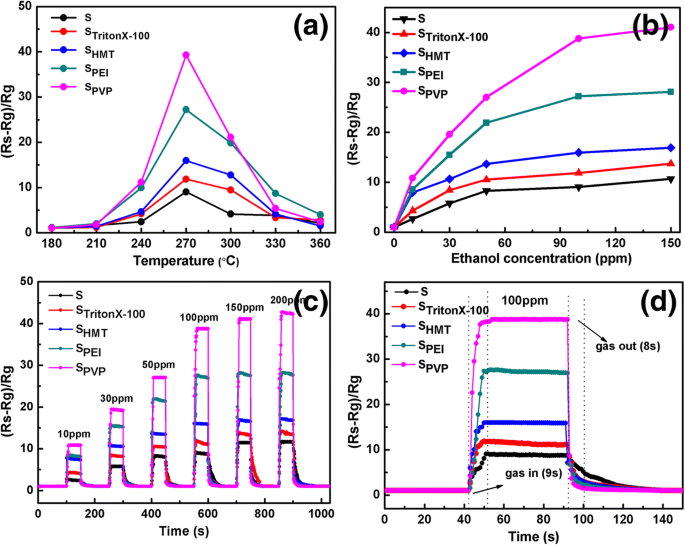
un La respuesta de los sensores a 100 ppm de etanol bajo diferentes temperaturas de funcionamiento (180–360 ° C). b Las curvas de respuesta dinámica de los sensores al etanol con diferentes concentraciones (10–150 ppm) a 270 ° C. c Curvas de respuesta versus tiempo de los sensores a 10–200 ppm de etanol consecutivamente a 270 ° C. d Transitorio de detección dinámica de los sensores a 100 ppm de etanol a 270 ° C
La Figura 6b muestra la respuesta de todos los SnO 2 sensores hacia el etanol en el rango de concentración de 10 ~ 150 ppm a la temperatura de trabajo óptima 270 ° C. Se puede observar claramente que la respuesta de todos los sensores aumenta rápidamente con la concentración de gas por debajo de 50 ppm, y esta tendencia se vuelve suave de 50 a 150 ppm, tendiendo a saturarse a alrededor de 100 ppm. Como era de esperar, los tensioactivos y las morfologías inducidas pueden producir una gran influencia en la detección de gases de los sensores fabricados. Entre estos sensores fabricados, el S PVP El sensor exhibe el mejor comportamiento de detección hacia el gas etanol y S PEI viene en segundo lugar. Para obtener una visión profunda del mecanismo de detección de gas, también se realiza la adsorción-desorción de nitrógeno BET (Brunaure-Emmett-Teller) para determinar las áreas de superficie específicas de estas muestras, como se muestra en la Tabla 1. Se puede ver que S PEI tiene la mayor superficie específica (38,4 m 2 g −1 ) con mayoría absoluta. Cabe señalar que a pesar de la superficie relativamente más pequeña (15,5 m 2 g −1 ), S PVP es el mejor candidato para el sensor de gas de etanol debido a su perfecta arquitectura similar a una flor con autoensamblaje de apilamiento ordenado y una porosidad relativamente más alta, lo que proporciona sitios de adsorción más activos para las moléculas de etanol. Incluso a concentraciones bajas de etanol de 10 ppm, la sensibilidad de S 0 , S TritonX-100 , S HMT , S PEI y S PVP Los sensores pueden alcanzar 2, 4, 7, 9 y 11, respectivamente, lo que indica su posible aplicación para sensores de etanol incluso a bajas concentraciones.
La Figura 6c muestra la respuesta dinámica de detección de gas y las curvas de recuperación de los sensores fabricados hacia el etanol con una temperatura de funcionamiento de 270 ° C, a partir de la cual se puede ver que las respuestas de todos los sensores fabricados aumentan al aumentar la concentración de etanol y una notable modulación de la resistencia. se alcanza a aproximadamente 100 ppm. Las respuestas muestran un aumento drástico una vez que el sensor fue expuesto a los gases objetivo y luego cayó a su valor inicial en el aire. Como se muestra en la Fig. 6d, la respuesta y el tiempo de recuperación a 100 ppm de etanol son aproximadamente 16 sy 28 s para S 0 , 14 sy 18 s para S TritonX-100 , 11 sy 15 s para S HMT , 9 sy 11 s para S PEI y 5 sy 8 s para S PVP , respectivamente. Es obvio que el S PVP El sensor tiene las mejores características de respuesta / recuperación en comparación con otros sensores.
La Tabla 2 muestra una comparación de los rendimientos de detección de etanol basados en diferentes SnO 2 enfoques fabricados informados en otras publicaciones y este trabajo a la concentración de 100 ppm. Se puede ver que nuestro Polyporoso SnO 2 nanoflower presenta comportamientos de detección de etanol notablemente con una temperatura de funcionamiento óptima más baja y un valor de respuesta más alto, así como un tiempo de respuesta-recuperación más rápido, lo que podría atribuirse a la presencia de numerosos mesoporos en el sensor SPVP, lo que lleva a una alta porosidad a favor de la adsorción y difusión de gas etanol.
Comportamientos de detección de gas de sensores fabricados a H 2 S
Como se discutió en la subsección anterior, S PVP El sensor exhibe la mejor propiedad de detección de gas a 100 ppm de etanol debido a su alta porosidad. Para encontrar su gas de detección óptimo, probamos la respuesta de S PVP sensor hacia diferentes gases, incluidos acetona, metanol, formaldehído y H 2 S, con una concentración de 100 ppm a varias temperaturas de funcionamiento (como se muestra en la Fig. 7a, b). Se puede notar que la respuesta óptima aparece a 330 ° C de metanol, a 210 ° C de formaldehído, a 360 ° C de acetona y a 180 ° C de H 2 S. Además, el valor de respuesta máximo de S PVP a H 2 Se estima que S es 368, que es uno o dos órdenes de magnitud (\ ({\ mathrm {S}} _ {{\ mathrm {H}} _ 2 \ mathrm {S}} / {\ mathrm {S}} _ {\ mathrm {etanol}} =9 \), \ ({\ mathrm {S}} _ {{\ mathrm {H}} _ 2 \ mathrm {S}} / {\ mathrm {S}} _ {\ mathrm { formaldehído}} =45 \)) más alto que el de otros gases de prueba. La temperatura de trabajo óptima más baja, así como el mejor valor de respuesta, indican S PVP tiene la excelente selectividad para H 2 S.
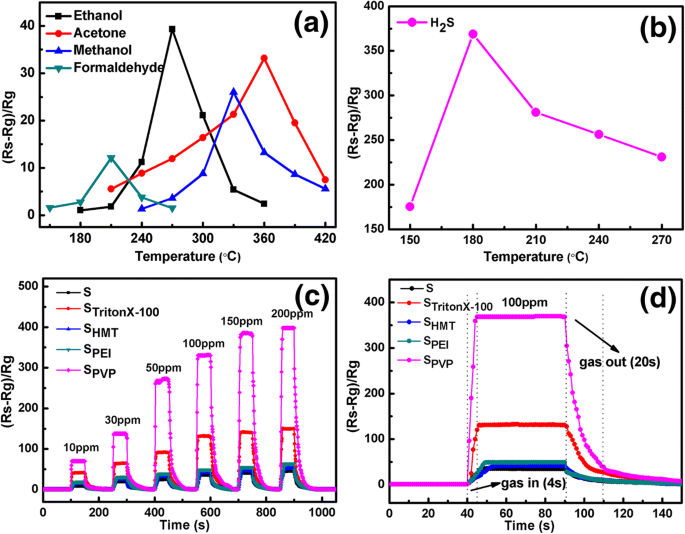
un Respuesta de S PVP sensor a 100 ppm de etanol, acetona, metanol y formaldehído a diferentes temperaturas de funcionamiento. b Respuesta de S PVP sensor a 100 ppm H 2 S a diferentes temperaturas de funcionamiento. c Curvas de respuesta en función del tiempo de los sensores a 10-200 ppm H 2 S consecutivamente a 180 ° C. d Transitorio de detección dinámica de los sensores a 100 ppm H 2 S a 180 ° C
Considerando la alta respuesta de S PVP sensor a H 2 S, también realizamos una medición sistemática de detección de gas de todos los demás sensores. Una respuesta dinámica de detección de gas y curvas de recuperación de sensores fabricados hacia H 2 S a 180 ° C se muestran en la Fig. 7c. Obviamente, los valores de respuesta de todos los sensores fabricados muestran una función creciente monótona de H 2 Concentración de S. Para 100 ppm de H 2 S, el tiempo de respuesta y recuperación es de aproximadamente 9 sy 43 s para S 0 , 5 sy 30 s para S TritonX-100 , 14 sy 40 s para S HMT , 8 sy 38 s para S PEI y 4 sy 20 s para S PVP , mientras que los valores máximos de respuesta son 35, 132, 41, 49 y 368 para S 0 , S TritonX-100 , S HMT , S PEI y S PVP , respectivamente. Es obvio que el S PVP El sensor tiene las mejores características de respuesta / recuperación y la respuesta más alta a H 2 S gas en comparación con otros sensores, mientras que S TritonX-100 logra el segundo.
La Figura 8 muestra el gráfico de barras de la respuesta de cinco sensores fabricados al formaldehído, metanol, etanol, acetona y H2 2 S. Todos los gases se probaron con una concentración de 100 ppm a la temperatura de funcionamiento óptima. S TritonX-100 y S PVP mostrar una respuesta distinta a H 2 S, mientras que S PEI muestra la respuesta de gas más alta al metanol y la acetona. Cabe mencionar que el área de superficie específica y la porosidad son dos factores importantes para los sensores de gas. El área de superficie específica más grande proporcionará sitios más activos para la adsorción y desorción de los gases de prueba, mientras que la porosidad más grande induciría una mayor velocidad de difusión del gas debido a la presencia de mesoporos. En comparación, S PEI posee un área de superficie específica relativamente más grande que otros (visto en la Tabla 1), que muestra la respuesta de gas más alta al metanol y la acetona (Fig. 8), mientras que S PVP y S TritonX-100 exhiben la respuesta de gas más alta a H 2 S debido a sus nanoestructuras similares a flores poliporosas, lo que demuestra una buena selectividad de S TritonX-100 y S PVP hacia H 2 S. La buena selectividad de las muestras a H 2 S se puede explicar de la siguiente manera:cuando el SnO 2 el sensor está expuesto en H 2 S gas, both chemisorbed oxygen species and SnO2 nanostructure react with H2 S during sensing measurement to form SO2 and SnS2 , respectivamente. Compared with SnO2 , the body resistance of SnS2 is relatively smaller, leading to the sensitivity enhancement of the gas sensor [39]. On the contrary, the SnO2 sensor does not react with any other target gases, such as formaldehyde, methanol, ethanol, and acetone.
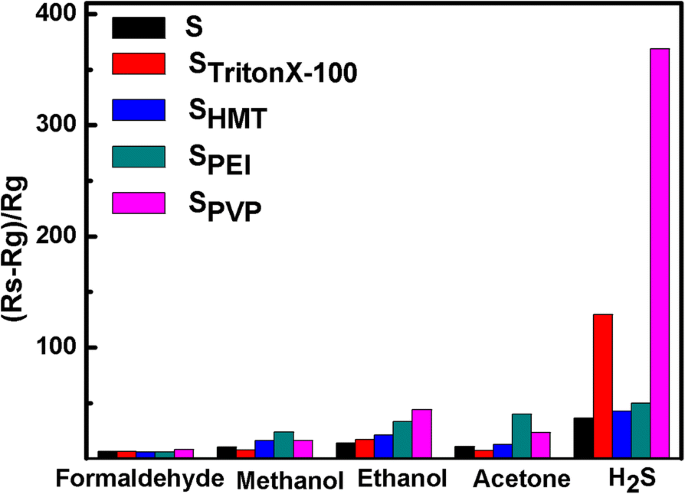
The comparison among sensor response of SnO2 nanomaterials to 100 ppm of various gases at the optimal operating temperature
Good stability and long service duration are expected from the viewpoint of practical application. To verify the stability of the sensor, the successive gas-sensing behavior of SPVP to 100 ppm ethanol was tested under the same conditions after 1 month. The samples were stored in the vacuum drying vessel during the 1-month interval. It can be seen from Fig. 9 that SPVP exhibits an excellent repeatability and stability even after 1 month. The three cyclic curves are similar to that measured 1 month ago, including the response value as well as the response-recovery time.
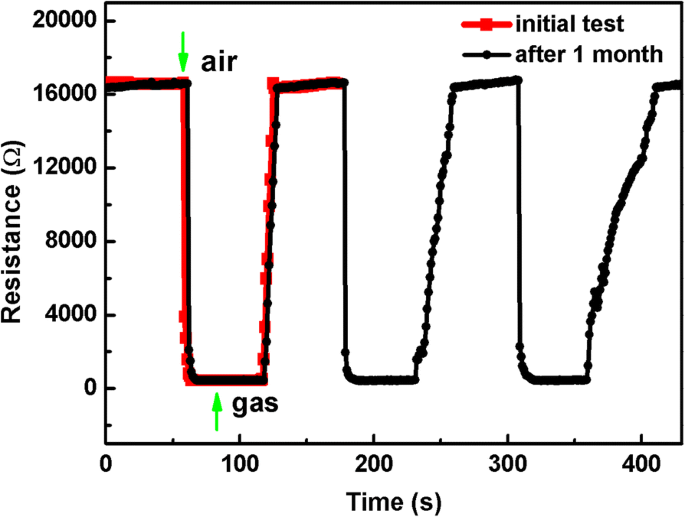
Stability of SPVP over 1 month of aging for 100 ppm ethanol at 270 °C
Gas-Sensing Mechanism
Up to now, the most widely accepted gas-sensing mechanism of semiconductor oxide is the model based on the electron transfer dynamics during an adsorption–oxidation–desorption process, which can change the resistance value of the sensors [40]. The response of typical n-type semiconductor greatly depends on the electron concentration. As shown in Fig. 10, at elevated temperature, electrons in the valence band are thermally excited to the conductive band. Once the SnO2 sensor is exposed to ambient air, oxygen molecules will be chemisorbed on the surface of SnO2 nanoflowers. Oxygen ions (O2 − , O − , and O 2− ) are then formed by capturing electrons from the conductive band of SnO2 [41], which is accompanied by an effective enlargement of electron-depleted layer. As a typical n-type semiconductor, the broadening of electron-depleted region means the decrease of carrier concentration within SnO2 nanoflowers, which will lead to the increase of resistance of the sensors. Conversely, when the SnO2 sensor is exposed in the reductive ambient, the absorbed oxygen species will quickly react with the target gas, which results in releasing the trapped electrons back to the conduction band and a reduction of the resistance of the sensors. Among the sensors fabricated in this work, SPEI and SPVP show relative better gas-sensing performances. The underlying physical mechanisms are as follows:the gas sensing properties are strongly dependent on the surface special area and the porosity. In comparison, SPEI possesses a relative larger specific surface area than others, which will provide more active sites for adsorption and desorption of test gases. SPVP exhibits a relative higher porosity due to the polyporous flower-like nanostructures, which is favorable to the rapid diffusion of gas (as shown in Fig. 10).
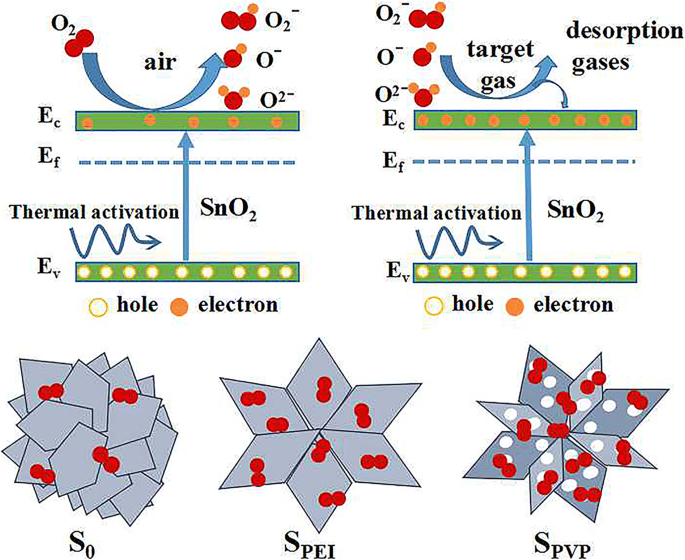
Schematic diagrams on the gas-sensing mechanism of flower-like SnO2 hierarchical nanostructures
Conclusiones
We have successfully prepared the 3D hierarchical flower-like SnO2 nanostructures through a simple and low-cost facile hydrothermal route with the assistance of different surfactants. The images of SEM and TEM showed that the fabricated 3D hierarchical SnO2 nanoflowers with an average diameter of 2~4 μm were composed of many 2D nanosheets. The addition of surfactant plays an important role in the formation of nanoflowers. Based on the experimental observations, the possible growth process and gas-sensing mechanism of SnO2 nanoflowers were proposed. As a cationic surfactant, the addition of PEI is conducive to the nucleation of SnO2 nanocrystals as well as the orderly growth of SnO2 nanosheets, leading to a relative larger specific surface area. As amphiphilic non-ionic surfactants, PVP and TritonX-100 can make the nanosheets grow more uniformly and separately, which can serve as a soft template in the synthesis of advanced material, especially in the fabrication of mesoporous materials. In comparison, the sensor with the help of PVP (SPVP ) exhibits excellent gas-sensing performances to ethanol and H2 S due to its relative higher porosity. Especially, SPVP shows a high response (368), fast response/recovery time (4 s/20 s), and good selectivity toward H2 S gas. In addition, it is found that NaOH and sodium citrate are also important for the morphological formation of SnO2 nanoflowers.
Abreviaturas
- 1D:
-
Unidimensional
- 2D:
-
Bidimensional
- 3D:
-
Tridimensional
- BET:
-
Brunauer-Emmett-Teller
- FETEM:
-
Field emission transmission electron microscopy
- HMT:
-
Hexamethylene tetramine
- Na3 C6 H 5 O 7 · 2H 2 O:
-
Trisodium citrate dihydrate
- PEI:
-
Polyethyleneimine
- PVP:
-
Polivinilpirrolidona
- SAED:
-
Difracción de electrones de área seleccionada
- SEM:
-
Microscopía electrónica de barrido
- XRD:
-
Difracción de rayos X
Nanomateriales
- El efecto del plasma de no equilibrio por contacto sobre las propiedades estructurales y magnéticas de Mn Х Fe3 - X О4 Espinelas
- Propiedades paramagnéticas de nanomateriales derivados del fullereno y sus compuestos poliméricos:efecto de bombeo drástico
- Propiedades de las oscilaciones electromagnéticas longitudinales en metales y su excitación en superficies planas y esféricas
- Influencia del agua en la estructura y propiedades dieléctricas de la microcristalina y nanocelulosa
- Ajuste de las morfologías de la superficie y las propiedades de las películas de ZnO mediante el diseño de la capa interfacial
- Nanocompuestos magnéticos de poli (N-isopropilacrilamida):efecto del método de preparación sobre las propiedades antibacterianas
- Síntesis de puntos cuánticos de sulfuro de antimonio solubles en agua y sus propiedades fotoeléctricas
- Síntesis fácil de óxido de estaño mesoporoso similar a un agujero de gusano a través del autoensamblaje inducido por evaporación y las propiedades mejoradas de detección de gas
- Efecto del método de síntesis de nanopartículas de manganita La1 - xSr x MnO3 en sus propiedades
- Prueba de las propiedades estructurales, electrónicas y magnéticas de Ag n V (n =1–12) Clusters
- Tipos de metales y sus propiedades.



