Análisis de metales por espectroscopia de emisión óptica
Análisis de metales por espectroscopia de emisión óptica
Las técnicas espectroscópicas de emisión óptica se originaron en experimentos realizados a mediados del siglo XIX, pero siguen siendo algunos de los medios más útiles y flexibles para realizar análisis elementales. Los átomos libres emiten luz en una serie de estrechos intervalos de longitud de onda, cuando se colocan en un entorno energético. Estos intervalos, denominados líneas de emisión, forman un patrón conocido como espectro de emisión, que es la característica del átomo que lo produce. Las intensidades de las líneas son normalmente proporcionales al número de átomos que las producen. La presencia de un elemento en una muestra se indica por la presencia en la luz de la fuente de excitación de una o más de sus líneas características. La concentración de este elemento se puede determinar midiendo las intensidades de las líneas. Así, el espectro de emisión característico forma la base del análisis elemental cualitativo, y la medición de las intensidades de las líneas de emisión forma la base del análisis elemental cuantitativo. Los espectros de emisión para el hierro y el litio se muestran en la Fig. 1.

Fig. 1 Espectro de emisión para hierro y litio
El espectroscopio de emisión óptica, también conocido como espectrómetro de emisión óptica, se usa normalmente para (i) la determinación cuantitativa de los constituyentes principales y de elementos traza en varios tipos de muestras, y (ii) el análisis elemental cualitativo. Los ejemplos de aplicación incluyen (i) determinación rápida de concentraciones de elementos de aleación en aceros y otras aleaciones, (ii) análisis elemental de materiales geológicos, (iii) determinación de concentraciones de trazas de impurezas en materiales semiconductores, (iv) análisis de metales de desgaste en aceites, (v) determinación de concentraciones de álcalis y alcalinotérreos en muestras acuosas, y (vi) determinación de calcio en cemento.
Las muestras se encuentran en forma de sólidos conductores (arcos, chispas y descargas luminiscentes), polvos (arcos) y soluciones (llamas). El tamaño de la muestra depende de la técnica específica que varía de alrededor de 0,000001 gramos a varios gramos. La preparación de la muestra se realiza mediante mecanizado o molienda (metales), disolución (para llamas) y digestión o incineración (muestras orgánicas).
Las limitaciones de las técnicas espectroscópicas de emisión óptica son (i) algunos elementos son difíciles o imposibles de determinar, como nitrógeno, oxígeno, hidrógeno, halógenos y gases nobles, (ii) la forma de la muestra debe ser compatible con la técnica específica y (iii) ) todos los métodos proporcionan respuestas dependientes de la matriz. El tiempo de análisis estimado oscila entre 30 segundos y varias horas, según los requisitos de preparación de la muestra.
Las capacidades de las técnicas relacionadas incluyen (i) la fluorescencia de rayos X es para el análisis elemental de componentes menores y a granel y necesita una reducción de datos sofisticada para el análisis cuantitativo y no es útil para elementos ligeros (número atómico 9), (ii) plasma acoplado inductivamente (ICP) la espectroscopia de emisión es para el análisis elemental cuantitativo rápido con límites de detección de partes por billón, con muestras en solución y no es útil para hidrógeno, nitrógeno, oxígeno, haluros y gases nobles, (iii) la espectroscopia de emisión de plasma de corriente continua es similar en el rendimiento de la espectroscopia de emisión ICP, y (iv) la espectroscopia de absorción atómica es una técnica de un solo canal, ineficiente para el análisis de múltiples elementos, pero tiene una sensibilidad y precisión favorables para la mayoría de los elementos.
En un sentido más amplio, la espectroscopia de emisión óptica incluye la espectroscopia de emisión óptica ICP, que utiliza un ICP como fuente de excitación. Sin embargo, los términos "espectroscopia de emisión óptica" y "espectroscopia de emisión óptica" normalmente se refieren a la espectroscopia de emisión óptica que utiliza descarga de chispa, descarga de arco de corriente continua, descarga luminiscente o fuente de llama para generar la descarga de excitación. En este artículo se analiza la espectroscopia óptica con descarga de chispa, ya que se está utilizando en la industria del acero.
Muchos espectroscopios de emisión óptica cuentan con "Análisis de distribución de pulsos" (PDA) para mejorar la reproducibilidad (precisión) de la medición. Este método implica el procesamiento estadístico de los espectros de emisión generados por pulsos de chispa obtenidos a partir de descargas de chispas en una atmósfera de argón. El espectroscopio de emisión óptica ofrece un análisis elemental rápido de muestras de metales sólidos, lo que lo hace indispensable para el control de calidad en los procesos de fabricación de acero
Principios generales
El espectro característico que produce un átomo refleja la estructura electrónica del átomo. Los cambios en la energía de los electrones de valencia o de la capa exterior dan como resultado las líneas atómicas utilizadas en la espectroscopia de emisión. Cada átomo tiene un estado fundamental en el que todos sus electrones ocupan posiciones de mínima energía potencial. A medida que un átomo absorbe energía, uno o más de los electrones externos pueden promoverse a energías más altas, produciendo un estado excitado. La energía de un estado atómico es una función de las energías de los electrones individuales y de los cambios de energía resultantes de las interacciones entre los electrones. Cada combinación posible de configuraciones electrónicas produce un término espectroscópico que describe el estado del átomo. La figura 2 muestra el principio del espectro de emisión tomando como ejemplo un átomo de litio.
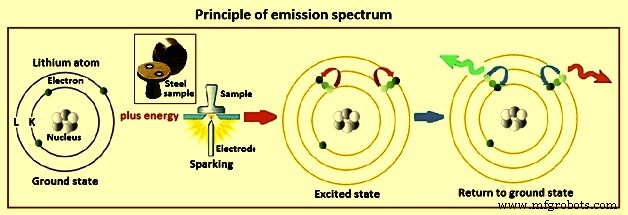
Fig. 2 Principio del espectro de emisión
Niveles de energía de los electrones – Los átomos más simples, como el hidrógeno y los metales alcalinos, tienen un solo electrón fuera de una capa llena. Las configuraciones electrónicas simples de estos átomos producen varios términos posibles. Las líneas de emisión atómica se producen cuando el átomo experimenta una transición espontánea de un estado excitado a otro estado de menor energía. No todas las combinaciones posibles de estados producen líneas de emisión. Solo las transiciones que obedecen las reglas de selección derivadas de la mecánica cuántica ocurren espontáneamente. Diversos factores controlan las intensidades relativas de las líneas. Esas transiciones entre un estado excitado bajo y el estado fundamental, denominadas transiciones de resonancia, generalmente producen la emisión más intensa.
La energía del electrón excitado aumenta al disminuir el espacio entre los estados excitados hasta que alcanza un límite de ionización. En este punto, el electrón ya no está ligado al átomo y puede asumir un rango continuo de energías. Dichos electrones no enlazados pueden sufrir transiciones a estados enlazados. Dado que el estado superior de la transición no se limita a valores discretos, la luz de dichas transiciones se propaga continuamente en un rango de longitudes de onda.
El límite de ionización para el átomo corresponde al estado fundamental del ion con una sola carga. La excitación de los electrones enlazados restantes produce un nuevo sistema de términos y un nuevo conjunto de líneas. La ionización y la excitación pueden continuar hasta que un átomo sea completamente despojado de sus electrones. En las fuentes de emisión prácticas, la ionización rara vez avanza más allá de la eliminación de dos electrones y, en la mayoría de los casos, solo es necesario considerar la primera etapa de ionización. Sin embargo, normalmente se usa una línea del primer espectro de iones en el análisis en lugar de una línea atómica neutra.
Superposición espectral – El uso de la emisión atómica para el análisis elemental necesita la mensurabilidad de la intensidad de emisión de una línea de interés independiente de la superposición de emisiones de otras especies en la muestra. La probabilidad de superposición no deseada depende del número de líneas en el espectro y de la extensión de la longitud de onda o ancho de línea de cada transición. Si todos los sistemas de términos atómicos son tan simples como el que se muestra para el litio en la Fig. 2, la probabilidad de superposición espectral será baja. Sin embargo, el litio es uno de los átomos más simples.
Los átomos con estructuras electrónicas más complejas producen espectros de emisión correspondientemente complejos. El espectro de hierro (que se muestra en la Fig. 1), ejemplifica tal complejidad espectral. El espectro de una etapa de ionización de un solo elemento puede, dada la energía de excitación suficiente, consistir en cientos de líneas de emisión. La complejidad se agrava cuando varios elementos están presentes en una muestra, cada uno generando espectros neutros e iónicos.
Ampliación de línea – La complejidad espectral no debe ser un problema si, en la práctica, cada línea de emisión es estrictamente monocromática y se dispone de instrumentos con resolución espectral infinita. La energía asociada con un término electrónico no se define con exactitud, sino que se distribuye en un rango de valores. La incertidumbre en los niveles de energía aparece en el espectro de emisión como un ensanchamiento de la longitud de onda de las líneas de emisión. Varios factores dictan la magnitud de la dispersión de energía. Los más importantes para la espectroscopia de emisión son las colisiones frecuentes del átomo o ion emisor con otras especies en la fuente de excitación y la colocación del emisor en un campo eléctrico no homogéneo.
El primer tipo de ensanchamiento de línea es el ensanchamiento por colisión, mientras que el segundo es el ensanchamiento Stark. Un tercer tipo, el ensanchamiento Doppler, resulta del movimiento de las especies emisoras en relación con el dispositivo que detecta la emisión. Para la energía de transición fija, la emisión registrada por un átomo que se mueve hacia el detector tiene longitudes de onda más cortas que la registrada por un átomo en reposo. La emisión de un átomo que se aleja del detector tiene longitudes de onda más largas. La magnitud relativa de estas tres contribuciones de ensanchamiento de línea depende en gran medida del tipo de fuente que excita la emisión. La contribución de la colisión al ancho de la línea es principalmente una función de la fuente de presión. La contribución Doppler para un elemento dado depende de la temperatura de la fuente. La magnitud de la contribución de Stark depende de la densidad de las especies cargadas cerca del emisor.
Ensimismamiento – Los perfiles de línea atómica producidos por cualquiera de los efectos anteriores pueden verse alterados por la autoabsorción. A altas concentraciones de átomos en la fuente espectroscópica, la probabilidad es razonable de que la radiación que emite un átomo sea absorbida por otro átomo del mismo tipo. La probabilidad de absorción es mayor en las longitudes de onda cercanas al centro del perfil de la línea que en las longitudes de onda cercanas a las alas. Los perfiles de emisión observados en tales condiciones son más planos y amplios que los observados en ausencia de autoabsorción. Si los átomos absorbentes están a temperaturas más bajas que los átomos emisores, el perfil lineal es similar al que se muestra en la figura 3. El perfil de absorción Doppler de los absorbentes de baja temperatura es más estrecho que el perfil de emisión de los emisores más calientes. Esto se llama autorreversión.
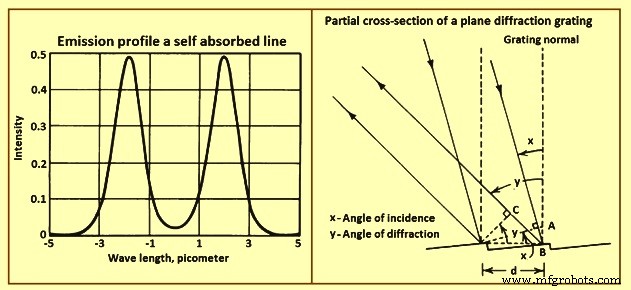
Fig. 3 Perfil de emisión de una línea autoabsorbida y sección transversal parcial de una rejilla de difracción plana
Emisión molecular – El volumen de emisión energética de una fuente espectroscópica puede contener moléculas pequeñas además de átomos libres. Al igual que los átomos, las moléculas producen emisión óptica que refleja cambios en las energías de los electrones externos de la molécula. A diferencia de los átomos, las moléculas tienen numerosos niveles de vibración y rotación asociados con cada estado electrónico. Cada transición electrónica en la molécula produce una banda de emisión compuesta por líneas individuales que reflejan la estructura vibracional y rotacional de los estados electrónicos involucrados en la transición.
Las bandas moleculares aparecen en un espectro registrado como bordes intensos, fuera de los cuales se desarrollan líneas menos intensas a longitudes de onda más altas o más bajas con un espaciado que aumenta con la distancia desde el borde. El borde es la cabeza de la banda. Compuestas por muchas líneas estrechamente espaciadas, las bandas moleculares pueden dominar una región del espectro, lo que complica la detección de emisiones de otras especies en esa región. Las fuentes de emisión se diseñan con frecuencia para minimizar la emisión molecular. Con menos frecuencia, las intensidades de banda se utilizan en lugar de las intensidades de línea atómica para medir la concentración.
Sistemas ópticos
La emisión atómica es analíticamente útil solo en la medida en que la emisión de una especie atómica puede medirse y su intensidad puede registrarse independientemente de la emisión de otras fuentes. Esta detección y cuantificación necesita instrumentación de clasificación de longitud de onda de alta resolución. Además, antes de que la luz pueda clasificarse, debe recolectarse de manera eficiente, a veces solo de una región aislada en una fuente de emisión espacialmente heterogénea.
Instrumentos de clasificación de longitud de onda – El elemento clave en los instrumentos modernos de clasificación de longitudes de onda es la rejilla de difracción, una superficie reflectante de forma precisa que tiene muchas ranuras paralelas muy juntas. En la figura 3 se muestra una sección transversal parcial de una rejilla de difracción. Los rayos de luz paralelos inciden en las ranuras adyacentes de la rejilla. Los rayos incidentes están en fase entre sí. Los rayos esparcidos por la rejilla han recorrido diferentes caminos. La diferencia en las longitudes de los caminos es AB + BC.
En ángulos que producen una diferencia de trayectoria que es un número entero de longitudes de onda, los rayos que salen están en fase y la luz se difracta en ese ángulo. En otros ángulos, los rayos que salen están desfasados y se produce una interferencia destructiva. Los ángulos en los que tiene lugar la difracción para una longitud de onda dada se pueden determinar observando que AB =d sen x y BC =d sen y donde d es la separación entre ranuras de la rejilla de difracción, x es el ángulo de incidencia e y es el ángulo de difracción. La condición de difracción viene dada por la ecuación m.lambda =d.(sen x +/- sen y). El signo menos entra cuando los haces incidente y difractado están en lados opuestos de la rejilla normal.
Normalmente se utilizan dos tipos de dispositivos de clasificación de longitud de onda (Fig. 4) para la espectroscopia de emisión. El primero, el monocromador de rejilla, se utiliza para la detección de radiación de un solo canal. La figura 4 muestra la trayectoria de la luz a través de un monocromador Czerny-Turner, una configuración típica. La luz ingresa al monocromador a través de la rendija de entrada y pasa al espejo colimador. La luz colimada incide en la rejilla de difracción plana y se difracta en un ángulo que depende de su longitud de onda. Parte de la luz se difracta en ángulos tales que golpea el espejo de enfoque. Luego se enfoca para formar una matriz de imágenes de rendija de entrada en el plano focal del monocromador. La posición en la matriz de una imagen de hendidura depende del ángulo en el que la luz que la forma sale de la rejilla. La longitud de onda de la imagen centrada en la rendija de salida viene dada por la ecuación m. lambda =2d.sin q.cos p donde q es el ángulo a través del cual gira la rejilla, y p es el ángulo del instrumento y es el ángulo que forma una línea que pasa por el centro de la rejilla y el centro de cualquiera de los espejos con la línea central del instrumento Las relaciones entre q y p y los ángulos x e y utilizados en la primera ecuación se muestran en la Fig. 4. A medida que se gira la rejilla, las imágenes de diferentes longitudes de onda pasan secuencialmente a través de la rendija de salida y son detectadas por un tubo fotomultiplicador.
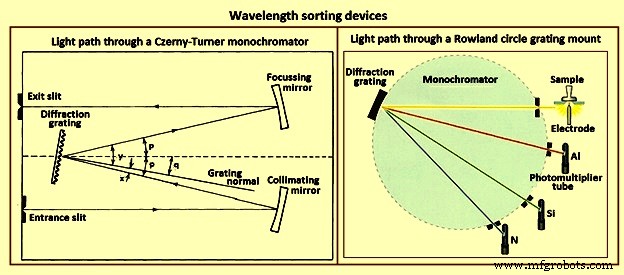
Fig. 4 Dispositivo de clasificación de longitud de onda
El segundo tipo general de clasificador de longitud de onda es el policromático. La mayoría de los policromadores son variaciones de la montura circular de Rowland (Fig. 4). La rejilla de difracción es cóncava, con un radio de curvatura R. Si una rendija de entrada se ubica en un círculo de radio R/2 tangente a la cara de la rejilla, las imágenes difractadas de la rendija se enfocan alrededor del círculo. Las rendijas de salida y los tubos fotomultiplicadores se pueden colocar en posiciones de la curva focal correspondientes a las longitudes de onda de las líneas de varios elementos. Se pueden determinar simultáneamente intensidades de línea de 40 a más de 60 elementos, dependiendo de la capacidad del instrumento.
Alternativamente, se puede colocar una tira de película o una placa fotográfica en la curva focal en lugar de las rendijas y los tubos fotomultiplicadores, convirtiendo el policromador en un espectrógrafo. Se puede registrar un espectro de emisión completo en poco tiempo en una placa o en un trozo de película. La detección fotográfica permite una mayor flexibilidad en la selección de líneas y proporciona más información que la combinación de rendijas fijas y tubos fotomultiplicadores. Sin embargo, el tiempo necesario para procesar el medio fotográfico, ubicar las líneas de interés y registrar sus intensidades hace que el uso de instrumentos fotográficos sea tedioso. Los avances en las capacidades de adquisición y procesamiento de datos de los policromadores computarizados están dejando en desuso a los instrumentos espectrográficos.
La óptica de colección para un instrumento espectroscópico transfiere la energía radiante de la fuente al detector con la máxima eficiencia y resuelve o, en algunos casos, mezcla las heterogeneidades espaciales en la emisión de la fuente. El primer requisito se cumple si la radiación de la fuente llena la rendija de entrada y la óptica de colimación del espectrómetro. Se puede usar una lente simple de tamaño adecuado para obtener imágenes de la fuente en la rendija de entrada con un aumento suficiente para llenarla. El tamaño de la lente se selecciona de tal manera que la radiación que pasa a través de la rendija solo llene la óptica de colimación. La rendija de entrada, entonces, define el área de la fuente vista por el sistema, y cualquier falta de uniformidad de la fuente dentro de esa área se transfiere al detector. La detección fotográfica frecuentemente necesita uniformidad espacial de las imágenes de hendidura. La uniformidad deseada se logra si la fuente se refleja en la óptica de colimación mediante una lente cerca de la rendija. Luego se utilizan otras lentes para generar una imagen intermedia de la fuente en una apertura para proporcionar resolución espacial.
Fuentes de emisión
Una fuente de luz de emisión consiste en descomponer la muestra de alguna forma fácilmente preparada en un vapor atómico, y luego excitar el vapor con suficiente eficiencia para producir una señal de emisión medible de los componentes de interés de la muestra. Cada uno de los cuatro tipos de fuentes de emisión (arcos, chispas de alto voltaje, descargas luminiscentes y llamas) tiene un conjunto de características físicas con los correspondientes activos y pasivos analíticos.
Mecanismos de excitación – La propiedad de una fuente de emisión más estrechamente ligada a sus características de excitación es la temperatura. La temperatura indica la cantidad de energía accesible en la fuente. Dado que la energía se puede repartir de diversas formas entre diferentes especies, las diferentes temperaturas pueden reflejar esa partición. La temperatura cinética del gas y la temperatura del electrón indican las energías cinéticas de las partículas pesadas y los electrones, respectivamente. Las temperaturas de excitación e ionización reflejan el contenido de energía electrónica de las especies atómicas y moleculares.
Además, las moléculas almacenan energía en modos de rotación y vibración, que se expresa como temperaturas de vibración y rotación. En muchos entornos de fuentes, el exceso de energía en un modo se intercambia o transfiere rápidamente a otro. En tales casos, todas las temperaturas anteriores son iguales y la fuente está en equilibrio termodinámico local (LTE). Cuando existe LTE, las condiciones de excitación se pueden describir sin comprender los mecanismos microscópicos de transferencia de energía. La distribución de la población entre los posibles estados excitados para una especie determinada viene dada por la ecuación de Boltzmann.
Cuando LTE no existe, entonces una descripción completa de la excitación en tales casos debe tener en cuenta los procesos de colisión microscópicos que pueden excitar o desexcitar un nivel de energía dado con una eficiencia muy diferente a la predicha usando LTE. Por ejemplo, en descargas de baja presión, una pequeña porción de la población de electrones puede tener una temperatura mucho más alta que la temperatura del gas en la descarga. Estos electrones rápidos pueden producir átomos o iones altamente excitados en cantidades mucho mayores que las generadas en condiciones LTE. La eficiencia de excitación en fuentes que no son LTE depende con frecuencia de coincidencias cercanas en la energía cinética o interna de las especies en colisión y, por lo tanto, muestra variaciones pronunciadas a medida que cambia la composición química de la región de excitación.
Fuente de emisión ideal – La fuente de emisión ideal toma muestras de todos los materiales de manera eficiente, independientemente de su forma, y entrega vapor a la zona de excitación con una composición directamente proporcional a la composición de la muestra. La excitación es uniformemente eficiente para todos los elementos. Produce espectros simples, con toda la energía de excitación concentrada en unos pocos estados excitados. La fuente no genera espectro de fondo. Por lo tanto, los resultados analíticos para concentraciones iguales de elementos en dos muestras son idénticos, independientemente de las diferencias en la concentración de otros constituyentes de la muestra. Es decir, el muestreo y la excitación no dependen de la matriz.
Fuentes de chispa – La chispa de alto voltaje es una descarga eléctrica intermitente caracterizada por voltajes operativos suficientes para causar la ruptura espontánea de un espacio analítico y altas corrientes resultantes de la energía almacenada capacitivamente en el circuito de descarga. La Fig. 5 muestra una fuente de chispas de forma de onda controlada que consta de un circuito de carga de alto voltaje, un circuito de tanque de condensador de inductor con un interruptor de alto voltaje y un circuito de forma de onda que incorpora el espacio analítico.
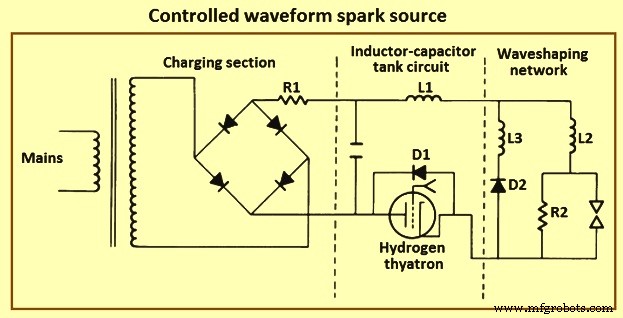
Fig. 5 Fuente de chispa de forma de onda controlada
El circuito genera una serie de descargas de chispas idénticas con un control preciso sobre la magnitud y dirección de la corriente, así como la duración de la descarga. En la práctica, la sección de carga del circuito es simplemente un transformador de alto voltaje y un rectificador de onda completa. La chispa se dispara en momentos retrasados desde el cruce por cero de la forma de onda de carga de corriente alterna (CA) seleccionada para producir el mismo voltaje del capacitor al comienzo de cada descarga. El disparador suele ser un tiratrón de hidrógeno o un rectificador controlado por silicio de alto voltaje. Para un voltaje de descarga dado, los valores relativos de las inductancias y la capacitancia dictan la forma y la amplitud de la forma de onda actual en el tanque y las secciones de formación de onda del circuito. Para la operación analítica, los valores de los componentes normalmente se seleccionan para proporcionar una corriente de descarga unidireccional con amplitudes máximas de 50 A a 200 A y duraciones de 50 microsegundos a 150 microsegundos.
Limitaciones del análisis – La vía de chispas analítica consta típicamente de un ánodo de tungsteno y un cátodo del material a analizar. Dado que la muestra forma uno de los electrodos, el análisis por espectroscopia de emisión de chispas se limita a las muestras que son conductoras o que pueden serlo. El análisis normalmente se lleva a cabo en una atmósfera inerte, que se proporciona en una cámara cerrada o como una capa de gas que fluye. A menos que se estabilicen, las chispas individuales en un tren golpean diferentes lugares en el electrodo de muestra, generando un patrón de quemado de varios milímetros de ancho en una muestra plana. Con una capa de argón que fluye del ánodo al cátodo, las chispas golpean de manera mucho más reproducible y el área de combustión se reduce en un factor de diez.
Cuando una chispa golpea el electrodo de muestra, el calentamiento local rápido expulsa el material del electrodo al espacio de chispas. En una chispa no estabilizada, la trayectoria del material expulsado es aleatoria. En una chispa estabilizada, el material se propaga hacia arriba a través del espacio como un cilindro en expansión alrededor del eje entre electrodos. En cualquier caso, el vapor se somete a varias condiciones de excitación durante una sola chispa. Primero pasa por el punto del cátodo energético, donde puede sufrir varias etapas de ionización. A medida que continúa hacia arriba, el vapor en el canal de la chispa conductora de corriente permanece muy excitado; el vapor extraído del eje entre electrodos experimenta condiciones mucho menos energéticas. La corriente en la descarga aumenta y disminuye, alterando notablemente las condiciones de excitación, coincidiendo en el tiempo con el movimiento del vapor de muestra a través del espacio.
La falta de homogeneidad temporal y espacial de la chispa impide su caracterización en términos de temperatura de excitación. La emisión se genera en diferentes momentos y lugares a partir de varias etapas de ionización del material de muestra y el gas atmosférico. La forma dominante de emisión es frecuentemente el primer espectro de iones. Las líneas del ion cargado individualmente se denominan tradicionalmente líneas de chispa.
Los cambios en la emisión de chispas ocurren en microsegundos. La emisión de un tren de chispas también varía en cuestión de minutos. Este cambio a largo plazo en la intensidad de la emisión, el efecto de chispas, es principalmente un reflejo del cambio en el electrodo de muestra causado por chispas repetidas en su superficie. Los cambios químicos y físicos en el electrodo contribuyen al efecto de chispa. Por lo tanto, la naturaleza exacta de las curvas de chispas depende en gran medida de las condiciones experimentales.
Los parámetros de la fuente de chispas (capacitancia, voltaje, inductancia y tasa de repetición), la composición de la muestra, la estructura de la fase de la muestra, la condición de la superficie de la muestra, la atmósfera de chispas y el área de combustión se deben considerar al describir el comportamiento de chispas. De particular importancia son las dependencias de la composición de la muestra y la estructura de la fase, lo que indica que los resultados de emisión de un elemento dependen en gran medida de la matriz. Esto es importante cuando la chispa se utiliza como fuente de emisión analítica.
Minimizar las características indeseables – Se han adoptado diversos procedimientos en el análisis de chispas para minimizar el efecto de las no idealidades de la fuente. Los efectos de chispas se tratan tradicionalmente registrando las emisiones solo después de que se hayan producido los mayores cambios de intensidad asociados con una quema. La luz que llega al detector se bloquea durante un período de precombustión que suele durar alrededor de 1 minuto, durante el cual la chispa acondiciona la superficie del electrodo fresco. Si la chispa es inestable posicionalmente y toma muestras de un área grande, la emisión que sigue al período de precombustión, para la mayoría de los elementos, permanece bastante constante durante los 30 segundos necesarios para registrar un espectro de emisión.
Las chispas posicionalmente estables generan curvas de chispas comprimidas en el tiempo en comparación con las producidas por descargas inestables. En lugar de aumentar a un valor de estado estable, la intensidad de emisión aumenta a un máximo en unos pocos segundos y luego disminuye a un valor relativamente bajo. La emisión se vuelve progresivamente más errática a medida que continúa la quema. El pico de emisión durante los primeros 2 minutos de la quema contiene información sobre la concentración de un elemento en una muestra y el tipo de matriz en la que se encuentra el elemento.
Una compensación adicional por la no idealidad de la fuente de chispa es el uso de relaciones de intensidad en lugar de intensidades de emisión no modificadas para indicar la concentración elemental. Las intensidades de las líneas de los constituyentes menores se relacionan con las intensidades de un constituyente principal de la matriz. Por ejemplo, en el análisis del acero, las intensidades de línea de los elementos de aleación se relacionan con la intensidad de una línea de hierro. Este procedimiento compensa en cierta medida las variaciones en la eficiencia de muestreo y excitación de una muestra a otra. Implica la suposición implícita de que el muestreo y la excitación del componente de referencia representan los mismos procesos para los constituyentes menores. Este no siempre es el caso, especialmente si la muestra contiene inclusiones que difieren significativamente en la concentración de la mayor parte de la muestra.
Las medidas anteriores no producen resultados analíticos satisfactorios a menos que el espectrómetro de chispa esté calibrado utilizando estándares que coincidan estrechamente con la muestra desconocida en composición química y forma física. Los laboratorios que utilicen la chispa para el análisis deben tener conjuntos de normas para cada tipo de material a analizar. Los estándares para investigaciones de chispas no se producen fácilmente y, por lo general, deben comprarse.
Muestreo y preparación de muestras
La excitación de fuente de chispa es el método más rápido para obtener un análisis elemental de un metal o aleación. Las muestras se toman de acero líquido, chapa fina, productos semiacabados o acabados. La velocidad es crítica en la industria del acero, para la cual se debe muestrear y analizar una masa fundida de un horno de producción y ajustar las concentraciones de elementos de aleación dentro de rangos predeterminados.
Cuando se toman muestras de acero líquido, se utiliza una sonda de muestreo o se vierten en un molde de fundición pequeñas cantidades de acero líquido recogidas con una cuchara de muestreo. La muestra se enfría. Las partes innecesarias de la muestra se eliminan con un molinillo o un cortador. Si no se investigan los elementos traza, se puede usar una amoladora o una lijadora de banda. Se muele o lija una superficie plana sobre la muestra enfriada y luego se coloca sin preparación adicional en una fuente de chispas. Sin embargo, para minimizar la contaminación, la muela abrasiva o la correa deben cambiarse para cada muestra. Se realiza el análisis y los resultados se envían inmediatamente al horno, donde se realizan los ajustes apropiados en la composición del calor. El muestreo y el análisis necesitan como máximo unos minutos. Las muestras tomadas de los productos semiacabados o acabados deberán tener un diámetro mínimo de 12 mm. Las muestras pequeñas en forma de varilla se pueden analizar con un equipo especial. La figura 6 muestra esquemáticamente el muestreo, la preparación de muestras y el análisis mediante el espectroscopio de emisión óptica.
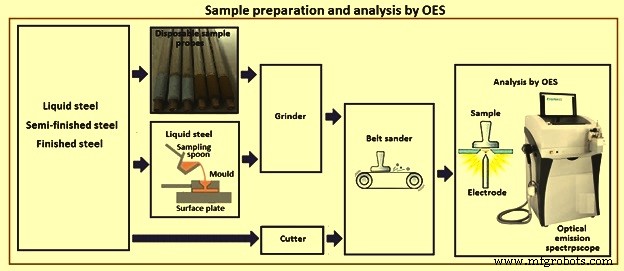
Fig. 6 Preparación y análisis de muestras por OES
Proceso de manufactura
- Filtro de cerámica
- 16 técnicas de herrería
- Análisis de emisiones fotoinducidas para identificar contaminantes superficiales
- Espectroscopia utilizando un microscopio óptico
- Corte de metal
- Rentabilidad del punzonado de chapa
- ¿Qué es el punzonado de chapa?
- Máquina de metal perforado y aplicaciones
- ¿Qué es una Fundición?
- Una descripción general de la chapa fina
- ¿Qué es enderezar chapa?



