Optimización de la nanoencapsulación en grupos de células parecidas a islotes porcinos neonatales utilizando polimerosomas
Resumen
Investiga métodos para probar la nanoencapsulación de grupos de células similares a islotes porcinos neonatales (NPCC) utilizando polimerosomas (PSomes) formados utilizando polímeros de polietilenglicol-bloque-polilactida. Aquí, nuestros estudios presentan un procedimiento de nanoencapsulación eficiente con daño mínimo y pérdida de NPCC. Usamos N-hidroxisuccinimida (NHS) en el N-terminal de los PSomas para inducir la unión de grupos amina en la matriz extracelular que rodea a los NPCC. Se utilizó medio de cultivo F-10 con albúmina de suero bovino en el procedimiento de nanoencapsulación para minimizar el daño y la pérdida de NPCC. Finalmente, indujimos el entrecruzamiento entre PSomes bifuncionales (NHS- / NH 2 -PSomes). El medio de cultivo F-10 que contenía BSA al 0,25% con un pH de 7,3 minimizó el daño y la pérdida de NPCC después de la nanoencapsulación en comparación con el uso de tampón HBSS básico (pH 8,0). Además, indujimos la nanoencapsulación eficiente a través de la conjugación de PSomes utilizando PSomes bifuncionales (NHS- / NH 2 -PSomes).
Introducción
El uso del trasplante de alo-islotes en el tratamiento de la diabetes tipo 1 es limitado debido a la falta de donantes adecuados. En cambio, hay un aumento gradual en el uso de islotes de animales en el trasplante de xeno-islotes, y los cerdos emergen como especies donantes óptimas [1]. Cuando se utilizan cerdos como donantes durante el trasplante, se pueden utilizar islotes separados, según la edad de los cerdos. A menudo, los grupos de células parecidas a islotes porcinos neonatales (NPCC) se prefieren a los islotes porcinos adultos (API) debido a su asequibilidad y facilidad de aislamiento. Además, los NPCC pueden proliferar gradualmente después del trasplante, prolongando su función in vivo [1, 2]. Sin embargo, cuando los NPCC se trasplantan en las venas porta de primates humanos o no humanos (NHP), las variaciones entre especies pueden causar reacciones inmunes como la reacción inflamatoria instantánea mediada por sangre (IBMIR) o el rechazo hiperagudo, lo que lleva a la pérdida temprana del injerto [3]. Para resolver este problema, se requiere la encapsulación de NPCC que pueden inhibir diversas respuestas inmunes. Hay tres tipos de encapsulación:macro, micro y nanoencapsulación. La macroencapsulación utiliza un dispositivo que contiene islotes, que luego se implanta alrededor de los vasos sanguíneos para liberar insulina a través de una membrana semipermeable en respuesta a los niveles de glucosa en sangre. La microencapsulación empaqueta una pequeña cantidad de islotes en una cápsula porosa. Aunque estas encapsulaciones pueden proteger a los islotes del rechazo inmunitario, en ensayos in vivo se han informado efectos secundarios como el colapso de la membrana o la generación de trombos. Los islotes también alteran el flujo de hormonas, nutrientes u oxígeno debido al aumento de la distancia de difusión. La nanoencapsulación es la estrategia de modificación de la superficie celular que induce la unión entre las células y las proteínas exógenas, principalmente polietilenglicol (PEG), en la transfusión de sangre [4].
La nanoencapsulación con PEG se ha utilizado ampliamente como método de modificación para mejorar la eficacia y las propiedades fisicoquímicas de las proteínas o péptidos diana [5]. En particular, la nanoencapsulación de islotes puede tener efectos inhibidores en respuesta al ataque de células inmunes y al reconocimiento de anticuerpos. El PEG se utiliza ampliamente para el recubrimiento celular debido a sus propiedades biocompatibles, como la no inmunogenicidad, el enmascaramiento de antígenos y el efecto no incrustante [6]. Entre las nanopartículas utilizadas para la nanoencapsulación de NPCC, los "polimerosomas" (PSomas) basados en PEG-bloque-polilactida (PEG-b-PLA) son los más adecuados porque son estables y fáciles de modificar; también pueden incorporar reactivos hidrófilos e hidrófobos en su ensamblaje [7, 8]. La modificación de la superficie de los islotes utilizando polímeros (que contienen PEG) se logra mediante la unión covalente o no covalente entre la matriz extracelular (MEC) del islote y el polímero conjugado con el grupo funcional [9].
En estudios anteriores, se utilizó una solución salina equilibrada básica de Hank (HBSS, pH 8,0) como tampón de reacción de nanoencapsulación de islotes debido a su capacidad para facilitar la N-hidroxisuccinimida (NHS) -NH 2 unión [10,11,12]. Sin embargo, para minimizar el daño celular a los NPCC durante la nanoencapsulación, utilizamos medio F-10 (medio de cultivo NPCC) con pH fisiológico (pH 7,3). Además, debido a que preservar la cantidad de NPCC después de la nanoencapsulación es importante para el trasplante de la cantidad correcta de células, agregamos albúmina de suero bovino (BSA), que recubre el fondo de la placa de cultivo celular con un polímero de cadena larga, para aumentar la recuperación. tasa [13]. En nuestro estudio anterior, la nanoencapsulación de NPCC con PSomes se llevó a cabo a través de grupos funcionales únicos, como NHS o NH 2 , que se utilizan para inducir unión covalente o interacción electrostática con ECM de NPCC, respectivamente. Sin embargo, a medida que la afinidad de unión disminuye con el tiempo, se necesitan estrategias para aumentar la eficiencia de la unión [14]. Se pueden usar algunos que tienen grupos bifuncionales como candidato para aumentar la eficiencia del recubrimiento debido a su capacidad de agregación. Por lo tanto, indujimos un entrecruzamiento entre los PSomas que contienen grupos bifuncionales (NHS- / NH 2 -PSome) que puede unirse no solo al ECM de NPCC, sino también a cada PSome a través de interacción covalente o interacción electrostática, aumentando así la eficiencia de nanoencapsulación.
En este estudio, investigamos la posible aplicación de la nanoencapsulación en NPCC mediante un método optimizado en el campo del xenotrasplante de islotes porcinos.
Materiales y métodos
Animales
Todos los experimentos con animales fueron aprobados por el Comité Institucional de Uso y Cuidado de Animales del Instituto de MGENPLUS co. limitado. (# 2019–1), y todos los procedimientos se llevaron a cabo de acuerdo con las pautas establecidas por el comité. La cirugía se realizó bajo anestesia general y se hicieron esfuerzos para asegurar que los animales experimentaran un dolor mínimo. Los cerdos fueron sacrificados antes de la pancreatectomía.
Aislamiento de grupos de células parecidas a islotes porcinos neonatales (NPCC)
Se aislaron NPCC de lechones de 3 a 5 días de edad. Brevemente, los lechones fueron anestesiados con ketamina (10 mg / kg, Yuhan, Seúl, Corea) e hidrocloruro de xilazina (1 mg / kg, Rompun; Bayer Corea, Seúl, Corea) inyectados en el músculo femoral y luego sacrificados inyectando cloruro de potasio ( Sigma-Aldrich, MO, EE. UU.) En el corazón. El páncreas se expuso a través de una incisión abdominal, se recogió y se sumergió en la solución salina equilibrada de Hank (HBSS, Biosesang, Gyeonggi-do, Corea) con bicarbonato de sodio 8,3 mM, N- (2-hidroxietil) piperazina-N ′ - ( Ácido 2-etanosulfónico) (HEPES) (Sigma-Aldrich, MO, EE. UU.) Y 0,5% de antibiótico-antimicótico (Biowest, MO, EE. UU.). El páncreas se cortó en 1 a 2 mm 3 fragmentos y digeridos en colagenasa tipo V (1 mg / ml, Sigma-Aldrich, MO, EE.UU.) en HBSS durante 10 min. Se añadió HBSS frío que contenía suero bovino fetal (FBS) al 10% (Biowest, MO, EE.UU.) al tejido de páncreas digerido para detener la actividad enzimática. Los tejidos del páncreas digeridos se lavaron en HBSS y, después de la resuspensión, los tejidos se filtraron a través de un pluriStrainer 500 µm (pluriSelect, Leipzig, Alemania) y se lavaron en HBSS. Finalmente, los NPCC se sembraron y cultivaron en 5% de CO 2 a 37 ° C en medio F-10 (Gibco, CA, EE. UU.) suplementado con albúmina de suero bovino (BSA) al 0,25% (genDepot, TX, EE. UU.), nicotinamida 10 mM, D-glucosa 10 mM, L-glutamina 2 mM, 2 mM de cloruro de calcio dihidrato, 50 µM de isobutilmetilxantina (IBMX), 20 µg / ml de ciprofloxacina (Sigma-Aldrich, MO, EE. UU.) Y 1% de antibiótico-antimicótico. Los NPCC se cultivaron durante 5 días [15], con la adición de exendina-4 10 nM (Prospec, Ness-Ziona, Israel) a los medios de cultivo todos los días.
Evaluación in vitro de NPCC y NPCC nanoencapsuladas
Después del cultivo, el número de NPCC se contó como equivalente de islote (IEQ) utilizando la retícula del ocular en el ocular. La viabilidad se evaluó mediante tinción con naranja de acridina (AO, 0,67 μM, Sigma-Aldrich, MO, EE. UU.) Y yoduro de propidio (PI, 75 μM, Sigma-Aldrich, MO, EE. UU.). Para realizar el ensayo de secreción de insulina estimulada por glucosa (GSIS), se recogieron 20-30 NPCC y se preincubaron con una concentración baja de D-glucosa (2,8 mM) en tampón de bicarbonato de Krebs-Ringer (KRBB) durante 1 h. A continuación, los NPCC se incubaron con D-glucosa baja (2,8 mM) en tampón KRBB durante 1 h, seguido de solución de D-glucosa alta (28,0 mM) en KRBB durante 1 h. Se recogieron los sobrenadantes para medir la secreción de insulina en concentraciones altas y bajas de glucosa [11]. La cantidad de insulina secretada de cada muestra se midió usando un kit ELISA Quantikine de insulina humana / canina / porcina (R&D systems, MN, EE. UU.). El índice de estimulación (IS) se calculó dividiendo las cantidades de insulina en concentraciones altas de glucosa (28,0 mM) por las de concentraciones bajas de glucosa (2,8 mM).
Preparación de Polymersome (PSome)
Para preparar PSomas, copolímeros de N-hidroxisuccinimida-poli (etilenglicol) -bloque-poli (lactida) (10 mg / ml, NHS-PEG-b-PLA) o amina-poli (etilenglicol) -bloque-poli (lactida) ) copolímeros (10 mg / ml, NH 2 -PEG-b-PLA; Nanosoft Polymers, NC, EE. UU.) Se disolvieron en 1 ml de dimetilsulfóxido (DMSO, Sigma-Aldrich, MO, EE. UU.). Además de preparar PSome bifuncional, cada copolímero (NHS o NH 2 -PEG-b-PLA) disuelto en DMSO se mezcló en proporciones. Se añadió agua destilada (DH2O) a la solución de polímero para obtener una concentración final de 1 mg / ml. La solución de polímero se sometió a ultrasonidos en un ultrasonicador (Sea han ultrasónico, Seúl, Corea) durante 5 min. Se añadió 1,1'-dioctadecil-3,3,3 ', 3'-tetrametilindodicarbocianina, sal de 4-clorobencenosulfonato (DiD; Biotium, CA, EE. UU.) A la solución de polímero durante la sonicación para permitir la visualización. Finalmente, la mezcla se dializó en DH2O durante 3 días.
Nanoencapsulación
El PSome se diluyó en tampón de reacción de nanoencapsulación (ya sea HBSS (pH 7.3 o pH 8.0) o medio F-10 simple sin suplementos (pH 7.3 o pH 8.0), con o sin BSA al 0.25%). La nanoencapsulación se realizó agregando el PSome a NPCC en medios de cultivo. Para hacer esto, se sembraron 10,000 IEQ de NPCC en una placa de cultivo celular de 6 pocillos (SPL, Gyeonggi-do, Corea), y se añadió PSome diluido a los NPCC y se incubó en 5% de CO 2 a 37 ° C durante 1 h. Se incubó un grupo de control negativo (NC) (NPCC no recubiertos sin PSomas) en las mismas condiciones que el grupo experimental. Después de la incubación, los NPCC nanoencapsulados se recolectaron y cultivaron en medios de cultivo F-10.
Eficiencia de NPCC nanoencapsuladas
Los NPCC nanoencapsulados de PSome conjugados con DiD se visualizaron utilizando microscopía de fluorescencia (Leica, Wetzlar, Alemania) o microscopía de barrido láser confocal (CLSM; Carl Zeiss, Oberkochen, Alemania). La intensidad de los NPCC unidos a PSoma conjugado con DiD se cuantificó calculando la intensidad de fluorescencia media (MFI) utilizando el software ImageJ (NIH, Bethesda, EE. UU.). Los núcleos de la célula se contratiñeron con 4 ', 6-diamidino-2-fenilindol (DAPI).
Ensayo de permeabilidad polimérica
Los NPCC nanoencapsulados NHS-PSome en F-10 o F-10 (0,25% BSA) se incubaron con dextrano conjugado con isotiocianato de fluoresceína (FITC) de diferentes pesos moleculares (10, 20, 70 y 250 kDa) durante 2 h. . La penetración de dextrano conjugado con FITC en NPCC nanoencapsuladas NHS-PSome se confirmó para cada peso molecular mediante un microscopio de escaneo láser confocal.
Ensayo de viabilidad celular polimerizado
El THP-1 nanoencapsulado de NHS-PSome (línea celular monocítica humana) en RPMI 1640 (Biowest, MO, EE. UU.) Se incubó durante 1 h. La viabilidad de THP-1 nanoencapsulado en NHS-PSome se midió de acuerdo con el protocolo presentado en el kit de ensayo de proliferación celular MTT (iNtRon Biotechnology, Seongnam-si, Corea).
Análisis estadístico
La prueba t para datos no apareados se realizó en GraphPad Prism 6.0. La significancia estadística se expresó como *, ** *** y **** indicando la P valor de ≤ 0.05, ≤ 0.01, ≤ 0.001 y ≤ 0.0001.
Resultados
Evaluación cultural y funcional de los NPCC
Los NPCC se cultivaron durante 5 días y se realizaron controles de calidad, incluida la viabilidad y el GSIS. El número total de NPCC fue de 21.014,0 IEQ / g / páncreas. La viabilidad, usando tinción AO / PI, fue del 89,9%. GSIS, que se realizó para confirmar la capacidad de respuesta de los NPCC a la concentración de glucosa, dio un índice de estimulación promedio (SI) de 2,3 (Tabla 1, Archivo adicional 1:Fig. S1).
Se requiere concentración de PSome para una nanoencapsulación eficiente de NPCC
Para determinar la concentración de PSome requerida para una nanoencapsulación eficiente, agregamos concentraciones variables de NHS-PSome a los NPCC. NHS-PSome se almacenó a una concentración de 1 mg / ml en DH 2 O y diluido a 1:5, 1:10, 1:20 y 1:40 para dar concentraciones finales que oscilan entre 0,2 y 0,025 mg / ml. La eficiencia de la nanoencapsulación se midió mediante MFI de NPCC nanoencapsuladas de PSome cargadas con DiD. La concentración final de 0,1 mg / ml (dilución 1:10) mostró la mayor intensidad de fluorescencia 2 días después de la nanoencapsulación (Fig. 1a yb) y la nanoencapsulación posterior de NPCC se realizó a esta concentración.
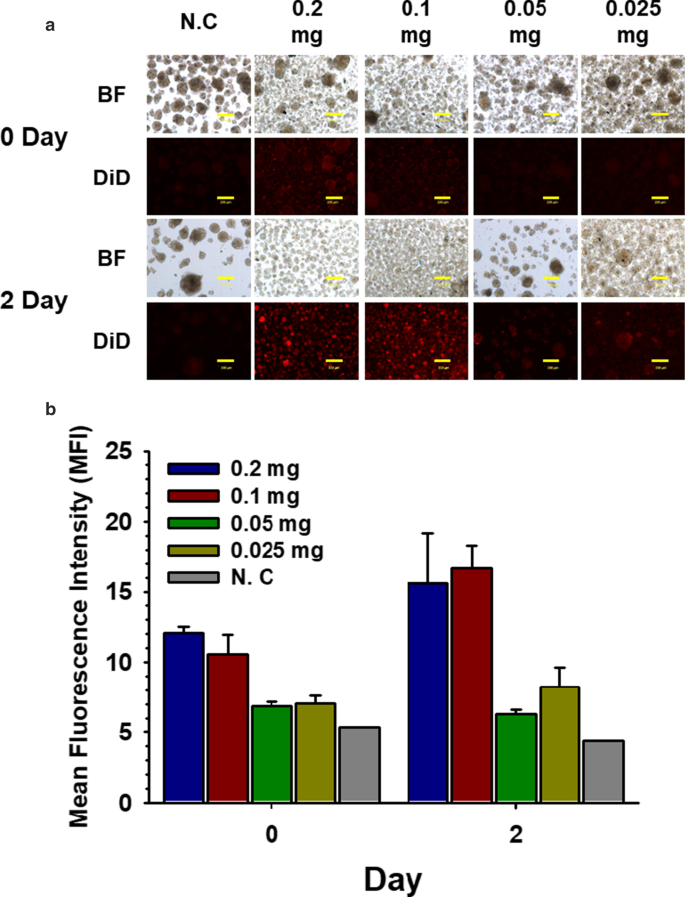
Optimización de la concentración de PSome para una nanoencapsulación eficaz a los 0 y 2 días. Optimización de la concentración de PSome para una nanoencapsulación eficaz. un NHS-PSoma cargado con DiD se trató en NPCC a diversas concentraciones (BF; campo brillante). Las barras de escala representan 200 μm. b MFI de NPCC nanoencapsuladas PSome cargadas con DiD ( n =3) y control NC ( n =1)
Eficiencia mejorada de nanoencapsulación en medios F-10 con pH fisiológico
La nanoencapsulación de islotes pancreáticos (que contienen NPCC) se realiza a menudo en tampón HBSS básico (pH 8,0 o superior) para mejorar la afinidad de unión entre NH2 en ECM de islotes y NHS conjugado en polímero. Sin embargo, la nanoencapsulación en tampón HBSS básico puede dañar potencialmente los NPCC. Por lo tanto, para minimizar el daño de los NPCC y determinar el efecto del pH en NHS-NH 2 de unión, los NPCC se nanoencapsularon a través de NHS-PSome en tampones HBSS o medios de cultivo F-10 simples (utilizados en este estudio para cultivar NPCC) con pH 7,3 (fisiológico) o pH 8,0 (básico), respectivamente. Cuando los NPCC se nanoencapsularon en F-10, se mantuvo la morfología normal de los NPCC (Fig.2a) y la eficiencia de la nanoencapsulación basada en MFI aumentó significativamente en comparación con la del grupo HBSS independientemente del pH en los días 0 y 6 (Fig. 2b). Aunque los grupos HBSS mostraron una diferencia significativa entre pH 7,3 y 8,0 el día 6, la intensidad de la nanoencapsulación disminuyó significativamente en comparación con la del grupo F-10. Por lo tanto, utilizamos medio de cultivo fisiológico F-10 (pH 7,3) como tampón de reacción de nanoencapsulación en experimentos posteriores para minimizar el daño potencial de los NPCC.
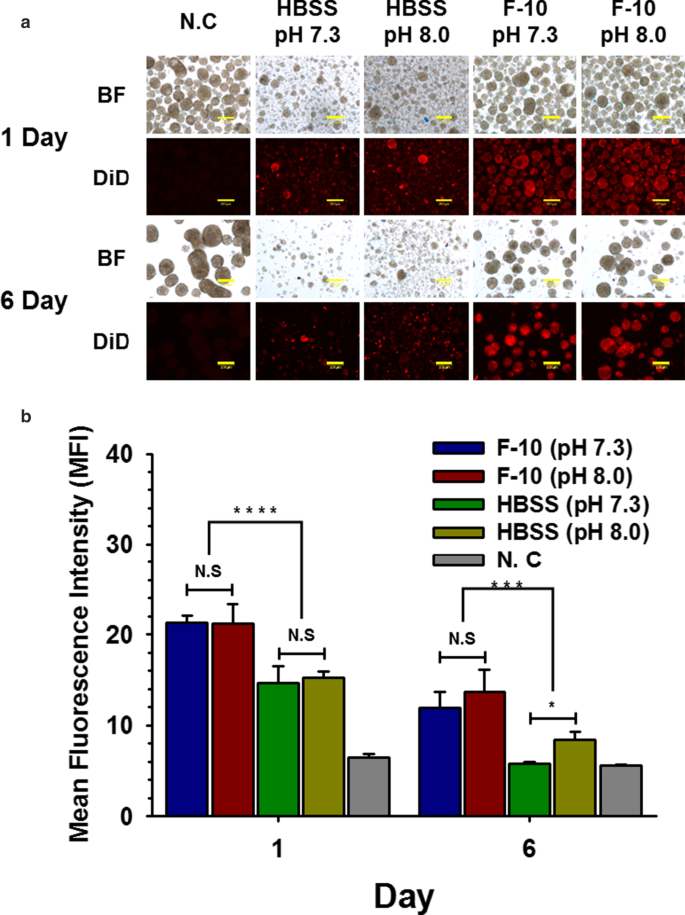
Comparaciones de la eficiencia del recubrimiento de nanoencapsulación en varios tampones de reacción a 1 y 6 días. Comparaciones de la eficiencia del recubrimiento de nanoencapsulación en varios tampones de reacción. un NPCC nanoencapsuladas en HBSS (pH 7,3 y pH 8,0) o F-10 (pH 7,3 y pH 8,0) usando NHS-PSome conjugado con DiD (BF; campo brillante). Las barras de escala representan 200 um; b MFI de NPCC nanoencapsulados en HBSS (pH 7.3 y pH 8.0) o F-10 (pH 7.3 y pH 8.0) usando NHS-PSome conjugado con DiD (todos los grupos; n =3). Los datos representan la media ± S.D. * p <0.05, *** p <0.001 y **** p <0,0001 frente a otros grupos
Mayor tasa de recuperación de NPCC después de la nanoencapsulación
Aunque el daño celular de los NPCC se redujo al mínimo en F-10, la cantidad de NPCC recolectada después de la nanoencapsulación se redujo notablemente. Para resolver este problema, agregamos 0,25% de BSA al medio F-10 durante el cultivo y la nanoencapsulación de NPCC utilizando NHS-PSome. Inicialmente confirmamos si la adición de 0,25% de BSA en el medio F-10 afecta la eficiencia del recubrimiento y la permeabilidad selectiva, permitiendo el paso de moléculas pequeñas (dextrano conjugado con FITC de 10 y 20 kDa) mientras bloquea las moléculas más grandes (conjugado con FITC de 70 y 250 kDa). dextrano), como función esencial de PSome. Como resultado, el revestimiento de conformación se mostró en imágenes de CLSM (Fig.3a, Mid) y la permeabilidad selectiva se mantuvo normalmente (Fig.3b, dextrano conjugado con FITC) en NPCC nanoencapsuladas NHS-PSome con F-10 que contenía 0.25 % BSA en comparación con F-10, aunque el MFI se redujo ligeramente (Fig. 3b). Las cantidades de NPCC recolectadas después de la nanoencapsulación mostraron una tasa de recuperación significativamente mayor (71,9%) en F-10 con 0,25% de BSA que en F-10 sin BSA (42,3%) (Fig. 3c). La viabilidad (NC:89,5%, NHS-PSome:90,3%) y la secreción de insulina estimulada por glucosa (NC:2,1, NHS-PSome:1,6) de NPCC en F-10 con 0,25% BSA también se mantuvieron después de la nanoencapsulación (Fig. .4a, b, archivo adicional 1:Fig. S2). Nuestros resultados indican que la adición de 0,25% de BSA puede mejorar significativamente la tasa de recuperación de NPCC después de la nanoencapsulación y no afectó la eficacia del recubrimiento o la función de PSome.
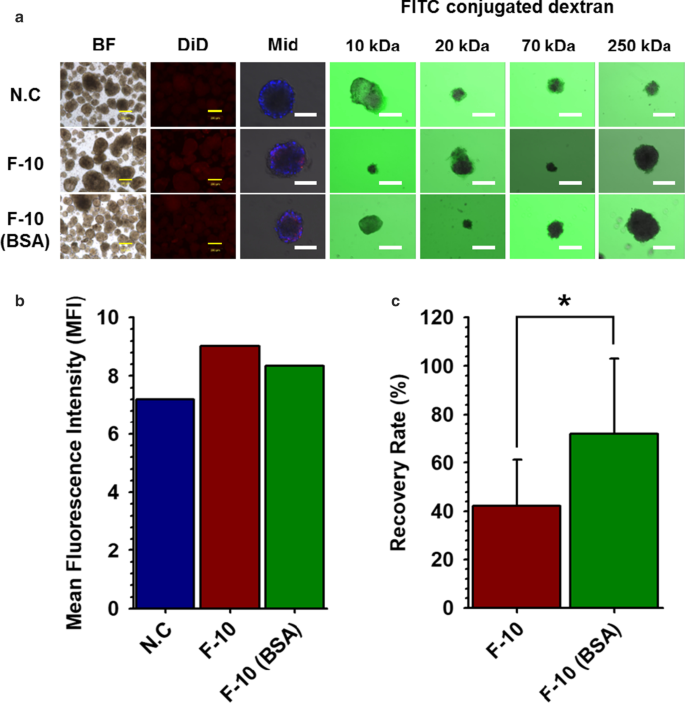
Comparaciones de la eficiencia del recubrimiento después de la adición de BSA al 0,25% en tampones de reacción de nanoencapsulación para aumentar la tasa de recuperación. Comparaciones de la eficiencia del recubrimiento después de la adición de BSA al 0,25% en tampones de reacción de nanoencapsulación para aumentar la tasa de recuperación. un Eficacia de recubrimiento y permeabilidad selectiva de NPCC nanoencapsuladas con NHS-PSome en F-10 o F-10 con 0,25% BSA (BF; campo brillante, medio; imagen media usando CLSM de NPCC nanoencapsuladas NHS-PSome conjugadas con DiD, Dextrano conjugado con FITC; imagen del medio usando CLSM de dextrano conjugado con FITC en NPCC nanoencapsuladas NHS-PSome). El azul en el medio representa la célula a través de la tinción DAPI. Las barras de escala son 200 (BF y DiD) y 100 (dextrano conjugado con FITC y medio) µm; b MFI de NPCC nanoencapsuladas usando NHS-PSome conjugado con DiD; c Tasa de recuperación de NPCC después de la nanoencapsulación en F-10 ( n =12) o F-10 con 0,25% de BSA ( n =12). Los datos representan la media ± S.D. * p <0.05 frente a F-10
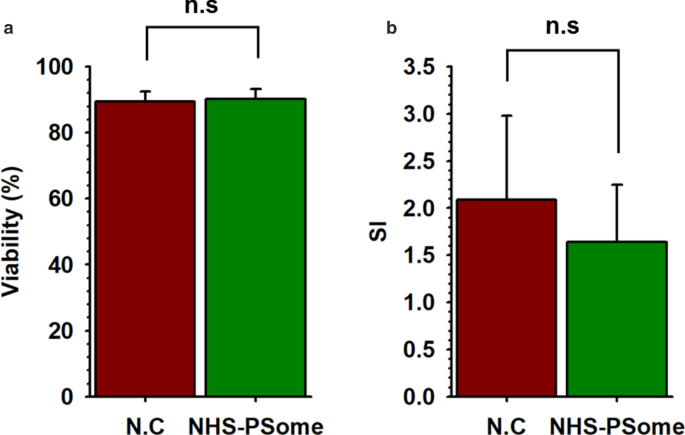
Viabilidad y funcionalidad de los NPCC nanoencapsulados NHS-PSome que utilizan F-10 con 0,25% de BSA. Viabilidad y funcionalidad de los NPCC nanoencapsulados NHS-PSome que utilizan F-10 con 0,25% de BSA. un Viabilidad de los NPCC nanoencapsulados NHS-PSome ( n =6) y control NC ( n =6); b SI de NPCC nanoencapsulados NHS-PSome ( n =5) y control NC ( n =5). Los datos representan la media ± S.D
Estabilidad mejorada de la nanoencapsulación a través de enlaces cruzados PSomes
Para inducir una nanoencapsulación más estable de NPCC, intentamos conjugar PSomes que tienen dos grupos funcionales diferentes. Primero, llevamos a cabo nanoencapsulación de los NPCC agregando simultáneamente diferentes proporciones de PSomes que contienen NHS y NH 2 grupos bifuncionales (NHS- / NH 2 -PSome) en un PSome (esquema 1). La eficacia de la nanoencapsulación fue confirmada por el MFI de DiD conjugado en NPCC nanoencapsuladas de PSome. Las imágenes resultantes de la microscopía de fluorescencia no mostraron diferencias significativas entre los grupos 9:1, 5:5 y 1:9 de NPCC nanoencapsuladas NHS- / NH2-PSome (9:1, 5:5, 1:9) el día 0 y día (Fig. 5a). Sin embargo, en los resultados de CLSM, el grupo 5:5 parecía estar sobrerrevestido y 1:9 mostró un recubrimiento insuficiente mientras que el grupo 9:1 formó un recubrimiento conformal, el día 1 (Fig. 5b). Por lo tanto, determinamos que la proporción óptima de NHS- / NH2 en PSome es de 9:1. Cuando se realizaron ensayos funcionales para el grupo 9:1, nuestros resultados mostraron que la viabilidad del grupo 9:1 disminuyó significativamente en comparación con la del control NC (92,1%), pero la viabilidad se mantuvo en niveles normales (87,8%). %). La función SI del grupo 9:1 fue normal (3.0) en comparación con la del control NC (3.7) (Fig. 5c, d).
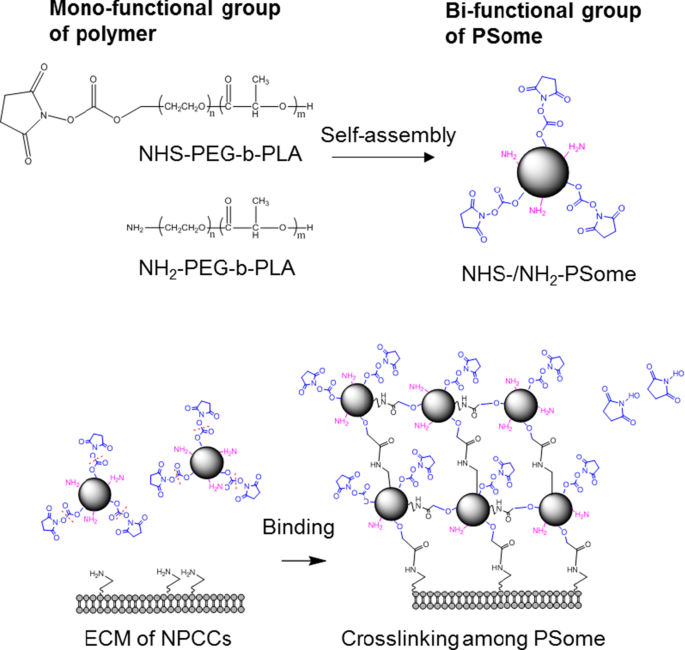
La ilustración de la estabilidad mejorada de la nanoencapsulación por reticulación de PSomas
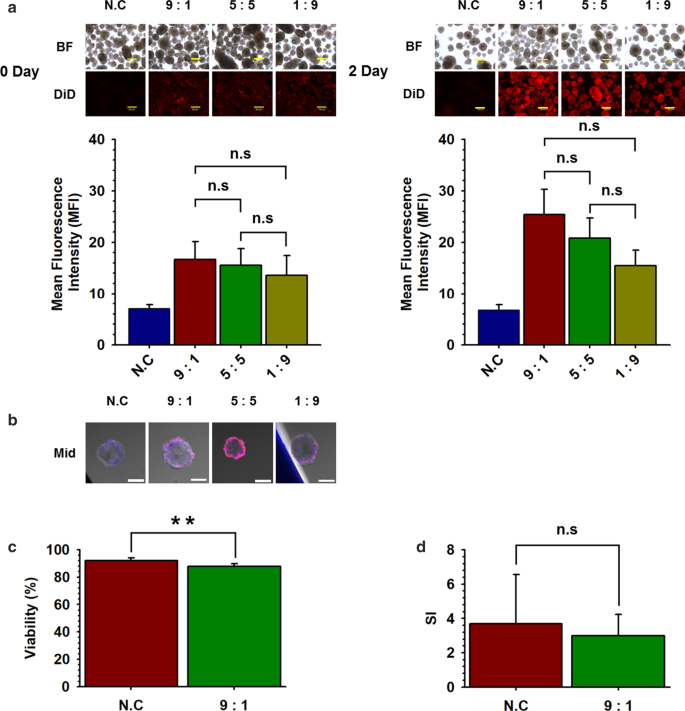
Revestimiento de eficacia y funcionalidad de NHS- / NH 2 -Algunos NPCC nanoencapsulados. Revestimiento de eficacia y funcionalidad de NHS- / NH 2 -Algunos NPCC nanoencapsulados. un DiD conjugado 9:1, 5:5, 1:9 de NHS- / NH 2 -Algunos NPCC nanoencapsulados (9:1, 5:5, 1:9) (NC; NPCC sin recubrimiento). MFI muestra la intensidad de los NPCC nanoencapsulados de PSome conjugados con DiD ( n =3) y control NC ( n =3). Las barras de escala representan 200 um; b CLSM de NHS- / NH 2 conjugado con DiD -Algunos NPCC nanoencapsulados (imagen media; media con CLSM de NHS- / NH 2 conjugado con DiD -Algunos NPCC nanoencapsulados). El azul en el medio representa la célula a través de la tinción DAPI. Las barras de escala representan 100 um; C. Viabilidad de 9:1 ( n =9) y control NC ( n =3). Los datos representan la media ± S.D. ** p <0,01 frente a NC; D. SI de 9:1 ( n =9) y control NC ( n =3). Los datos representan la media ± S.D
Discusión
La diabetes mellitus, comúnmente conocida como diabetes, es una enfermedad metabólica caracterizada por niveles altos de glucosa en sangre. La diabetes tipo 1 se debe a que las células beta del páncreas no producen suficiente insulina [16]. El trasplante de islotes pancreáticos que contienen células β productoras de insulina se ha utilizado recientemente para curar la diabetes tipo 1. Sin embargo, el trasplante de alo-islotes es limitado debido a la escasez de donantes; en cambio, el xenotrasplante que utiliza islotes de animales no humanos ha surgido como una fuente alternativa de tejido de donantes. Debido a sus similitudes fisiológicas con los humanos, la facilidad de cría en masa y la disponibilidad de cría en instalaciones libres de patógenos, los cerdos se consideran un modelo animal óptimo para el trasplante de xeno-islotes [1]. Especialmente, los NPCC se han utilizado valiosamente tan bien como las API. Aunque la madurez de los NPCC es menor que la de los API, los NPCC tienen algunas ventajas sobre los API, como tener un procedimiento de aislamiento de islotes relativamente simple y económico, la capacidad de desarrollar resistencia a entornos hipóxicos y la proliferación in vivo después del trasplante [1, 2, 3] . Por estas razones, utilizamos cerdos recién nacidos de 3-5 días como fuente de islotes en este estudio.
Desafortunadamente, una vez que los islotes de cerdos se implantan en los vasos sanguíneos de primates humanos o no humanos, a menudo ocurren reacciones inmunes graves como IBMIR o rechazo hiperagudo. IBMIR generalmente ocurre debido a varios factores tisulares (TF) expresados en islotes porcinos que median la coagulación en los vasos sanguíneos humanos a través de la activación de una vía extrínseca. Los antígenos alfa-galactosa o no gal expresados en la superficie de las células de cerdo también pueden ser objetivos de anticuerpos humanos naturales, seguidos de una activación en cascada complementaria llamada rechazo hiperagudo. Como resultado, los injertos se pierden después de la hipoxia por la formación de coágulos de la vía de la coagulación y la muerte celular por la activación del complemento en el huésped [3]. Para resolver estos problemas, se ha probado la encapsulación, un método de recubrimiento de islotes pancreáticos con materiales biocompatibles para protegerlos contra el ataque de reacciones de anticuerpos o del complemento. En primer lugar, la macroencapsulación utiliza un dispositivo con una membrana semipermeable que contiene el islote y se implanta junto a los vasos sanguíneos donde libera insulina en el torrente sanguíneo en respuesta a los niveles de glucosa en sangre [4]. En segundo lugar, la microencapsulación, que utiliza principalmente alginato, tiene una permeabilidad selectiva y puede permitir que el oxígeno y los nutrientes pasen a través de su superficie porosa, mientras bloquea múltiples citocinas y la infiltración de células inmunitarias. Sin embargo, debido a que usan el mismo tamaño de cápsulas independientemente del tamaño de los islotes, es difícil recubrir los islotes de manera conformada. Además, puede producirse fibrosis que encierre el injerto después del trasplante [17]. Por último, la modificación de la superficie de los islotes (nanoencapsulación) utiliza principalmente polietilenglicol (PEG) que tiene la propiedad de "efecto sigiloso" que bloquea la interacción de materiales recubiertos con polímero "sigiloso" (PEG) y componentes en la sangre (células inmunes) en vivo [11, 18]. Nuestra estrategia de nanoencapsulación de NPCC utiliza los copolímeros de PEG modificados (PEG-b-PLA, Polymersome, PSome). Además, Psome tiene propiedades hidrofílicas e hidrofóbicas y puede incorporar inmunosupresores o factores involucrados en la diferenciación o crecimiento celular [8].
La nanoencapsulación de islotes con PEG se ha realizado en tampón HBSS básico (pH 8,0 o superior) para mejorar la afinidad de unión entre NHS en PEG y NH 2 en ECM del islote [10,11,12]. Sin embargo, dado que estas condiciones no pueden proporcionar un entorno de cultivo celular adecuado, intentamos la nanoencapsulación en un entorno que imita la condición de cultivo de NPCC. Para abordar los problemas anteriores, probamos medios F-10 simples, medio de base de cultivo NPCC, con pH fisiológico (sin ningún suplemento) utilizado como tampón de reacción de nanoencapsulación. La nanoencapsulación en F-10 con pH fisiológico mostró una eficiencia de recubrimiento similar y mantuvo la morfología normal de los NPCC en comparación con las condiciones de cultivo usando tampón HBSS básico (Fig. 3). Por lo tanto, podemos proponer una plataforma que minimice el daño de NPCC durante la nanoencapsulación en un entorno de imitación de cultivo de NPCC.
Aunque se estableció el método de nanoencapsulación para minimizar el daño de NPCC, la cantidad residual de NPCC recolectadas después de la nanoencapsulación disminuyó cuando la nanoencapsulación se realizó en placas de Petri. Esto significa que necesita más NPCC para nanoencapsulación para trasplantes. Según informes anteriores, los rendimientos de los islotes se mejoraron en algunas cepas de ratón mediante el uso de BSA durante el aislamiento [19]. Además, se utilizó BSA como cultivo en suspensión mediante el recubrimiento previo de la superficie de las placas de cultivo celular en cultivos de células de hepatoma de rata [13]. Por lo tanto, para aumentar la cantidad de NPCC después de la nanoencapsulación, se agregó 0,25% de BSA en tampón de reacción de nanoencapsulación F-10, lo mismo que la concentración de BSA utilizada para cultivar NPCC. Como resultado, la tasa de recuperación de NPCC aumentó significativamente después de la nanoencapsulación (Fig. 4). Esto significa que se puede predecir y trasplantar el número correcto de islotes (que contienen NPCC) después de la nanoencapsulación minimizando la pérdida de islotes (que contienen NPCC). En resumen, este estudio que utilizó F-10 con 0,25% de BSA para nanoencapsulación mostró que (i) se mantuvo la morfología normal de los NPCC, (ii) no se interfirió la unión entre el PSome conjugado con NHS y el NH2 en la ECM de los NPCC y (iii) aumentó la tasa de recuperación de NPCC después de la nanoencapsulación.
Finalmente, intentamos mejorar la estabilidad de la nanoencapsulación a través de (i) conjugación entre PSomes y (ii) unión entre PSomes y ECM de NPCC. Primero, los polímeros NHS- y NH2-PEG-b-PLA se mezclaron proporcionalmente para formar el PSome bifuncional (NHS- / NH2-PSome) que puede unirse tanto al PSome como al ECM de los NPCC. Postulamos que la conjugación podría lograrse de manera eficiente mediante grupos bifuncionales dentro de un PSome en lugar de conjugar dos PSomes con grupos monofuncionales debido a la posible interrupción causada por la unión entre PSomes con el mismo grupo funcional (NHS-NHS y NH2-NH2). Como se ve en los resultados, el revestimiento conformal de NPCC se logró en una proporción de 9:1 de NPCC nanoencapsuladas de NHS- / NH2-PSome, y se mantuvo la viabilidad y la funcionalidad (Fig. 5). Sin embargo, se necesitan más estudios para cuantificar la fuerza del enlace PSome, para demostrar que la nanoencapsulación con PSomes bifuncionales resultó en una encapsulación más estable que la del PSome monofuncional. Por lo tanto, sugerimos que nuestras condiciones efectivas de nanoencapsulación que imitan el entorno de cultivo NPCC se pueden utilizar en la estrategia de nanoencapsulación utilizando islotes que contienen NPCC (archivo adicional 1).
Conclusión
Este estudio se realizó para determinar un método óptimo de nanoencapsulación de islotes pancreáticos (NPCC) utilizando polimerosomas basados en PEG (PSomes). En primer lugar, el uso de medio de cultivo F-10 con pH de 7,3 puede mantener la morfología normal de los NPCC después de la nanoencapsulación en comparación con el uso de tampón HBSS básico (pH 8,0), minimizando así el daño a los NPCC durante la encapsulación. En segundo lugar, la adición de 0,25% de BSA al medio F-10 mejoró el rendimiento de NPCC en aproximadamente 1,7 veces después de la nanoencapsulación. Finalmente, indujimos una nanoencapsulación más estable a través de la conjugación de PSomes bifuncionales (NHS- / NH2-PSomes). Los métodos de nanoencapsulación presentados en este documento pueden ser aplicables en la nanoencapsulación de islotes pancreáticos utilizando nanopartículas basadas en PEG.
Disponibilidad de datos y materiales
No aplica.
Abreviaturas
- DiD:
-
1,1′-Dioctadecyl-3,3,3′,3′-tetramethylindodicarbocyanine, 4-chlorobenzenesulfonate salt
- AO:
-
Acridine orange
- APIs:
-
Adult porcine islets
- BSA:
-
Albúmina de suero bovino
- BF:
-
Campo brillante
- CLSM:
-
Microscopía de escaneo láser confocal
- DAPI:
-
4′,6-Diamidino-2- phenylindole
- DMSO:
-
Dimetilsulfóxido
- DH2O:
-
Distilled water
- ELISA:
-
Ensayo inmunoabsorbente ligado a enzimas
- FBS:
-
Suero fetal bovino
- FITC:
-
Isotiocianato de fluoresceína
- GSIS:
-
Glucose-stimulated insulin secretion
- HBSS:
-
Hank’s balanced salt solution
- IBMIR:
-
Instant blood-mediated inflammatory reaction
- IEQ:
-
Islet equivalent
- IBMX:
-
Isobutylmethylxanthine
- KRBB:
-
Krebs–Ringer bicarbonate buffer
- MFI:
-
Mean fluorescence intensity
- HEPES:
-
N-(2-Hydroxyethyl)piperazine-N′-(2-ethanesulfonic acid)
- NC:
-
Control negativo
- NPCCs:
-
Neonatal porcine islet like cell clusters
- NHS:
-
N-hidroxisuccinimida
- NHP:
-
Non-human primate
- PLA:
-
Poly lactide
- PEG:
-
Polietilenglicol
- PSomes:
-
Polymersomes
- PI:
-
Yoduro de propidio
- SI:
-
Stimulation index
- TF:
-
Tissue factor
Nanomateriales
- C # usando
- Avanzando hacia 7nm
- Uso de ángulos para mejorar el futuro de la electrónica
- Hormigón inteligente con nanopartículas
- Optimización de película fina altamente reflectante para micro-LED de ángulo completo
- Fabricación de alto rendimiento de nanofibras de calidad utilizando un electrohilado de superficie libre modificado
- La optimización de programación de DRAM 1T sin capacitor basada en TFET de doble puerta
- Efecto catalítico de los clústeres de Pd en la combustión de poli (N-vinil-2-pirrolidona)
- Prueba de las propiedades estructurales, electrónicas y magnéticas de Ag n V (n =1–12) Clusters
- Optimización de celdas solares de matriz de unión de pines de nanocables GaAs mediante el uso de heterouniones AlGaAs / GaAs
- Absorción de luz eficaz utilizando rejillas piramidales de doble cara para células solares de silicio de película delgada



