Síntesis controlada de BaYF5:Er3 +, Yb3 + con morfología diferente para la mejora de la luminiscencia de conversión ascendente
Resumen
En este trabajo, Er 3+ / Yb 3+ -codoped BaYF 5 con diferentes tamaños y formas se han sintetizado mediante un sencillo método solvotermal. Al cambiar la fuente de fluoruro, el valor de pH, el disolvente, los tensioactivos, Yb 3+ concentración, temperatura y tiempo de reacción, las condiciones óptimas de síntesis de BaYF 5 :Er 3+ , Yb 3+ se encontró que mejoran las propiedades luminiscentes de conversión ascendente. Se encuentra que la intensidad de emisión de la luz verde y roja se mejora varias veces mediante el uso de NaBF 4 como fuente de fluoruro con la comparación de NH 4 F y NaF. Además, los efectos de diferentes tensioactivos no son los mismos. La adición de 5% de polieterimida (PEI) como tensioactivo también puede mejorar la emisión de conversión ascendente. Por el contrario, cuando se usó citrato de sodio (CIT) como otro surfactante para agregar, los tamaños de los nanocristales aumentaron gradualmente y las propiedades luminosas también disminuyeron.
Antecedentes
En los últimos años, los nanofosforos de conversión ascendente (UCNP) han atraído cada vez más atención debido a su uso en muchos campos, como dispositivos láser de estado sólido, imágenes de sonda fluorescente, bioaplicación, pantalla tridimensional estereoscópica, contador cuántico infrarrojo, sensor de temperatura y antifalsificación. [1,2,3,4,5,6,7,8,9,10,11]. Las UCNP suelen estar compuestas por material de matriz, activador y sensibilizador [12]. Debido a su baja energía fonética y su excelente estabilidad química, los fluoruros se utilizan a menudo como materiales de matriz para la preparación de UCNP. NaYF 4 [13] Las nanopartículas con una buena emisión de conversión ascendente tienen una estructura de fase hexagonal, mientras que la fase cúbica produce una emisión de conversión ascendente deficiente. Recientemente, algunos de los materiales de UC basados en BREF 5 (B =Mg, Ba, Ca, Sr) también se han estudiado y estos cristales recientemente desarrollados resultaron adecuados para aplicaciones de UC [14, 15]. Er 3+ -dopado BaYF 5 extremadamente exhibe la fuerte capacidad de luminiscencia UC. La intensidad de luminiscencia de Er 3+ -dopado BaYF 5 es ocho veces mayor que Er 3+ -dopado LaF 3 [dieciséis]. Cuando Er 3+ se utiliza como activador, Yb 3+ es un sensibilizador de luminiscencia UC representativo debido a su eficiente transferencia de energía [17, 18, 19, 20, 21]. Además, los tamaños de carga de Er 3+ y Y 3+ coinciden, y sus radios son similares (Er 3+ el radio es de 0,1 nm, Y 3+ el radio es de 0,101 nm) [22]. Por lo tanto, BaYF 5 se considera un anfitrión apropiado para Er 3+ iones.
Los principales factores que afectan las propiedades de luminiscencia son el tamaño de partícula, la morfología, la estructura y otros [23, 24]. Para obtener materiales luminiscentes UC con alta eficiencia, la síntesis controlada de las partículas esféricas con tamaño adecuado es beneficiosa para lograr una alta acumulación de densidad y dispersión de luz. En este trabajo, muestras de Yb 3+ / Er 3+ -codoped BaYF 5 se fabrican mediante un método solvotermal. Bajo las diferentes condiciones de reacción, se sintetizaron las muestras con diferentes morfologías y propiedades. NaBF 4 ya que la fuente de fluoruro tiene una mayor intensidad luminosa de UC en relación con el NH 4 F y NaF. Quizás pueda liberar lentamente F - ; por lo tanto, es más propicio para hacer el crecimiento de cristales y promover la luminiscencia de UC. Además, la influencia del disolvente, los tensioactivos, Yb 3+ También se informó la concentración, el pH de la solución inicial, la temperatura y el tiempo de reacción. Entre la eficiencia luminosa de UC y varias condiciones de reacción, se han investigado la regularidad y el mecanismo.
Experimental
Todos los productos químicos son de grado analítico, como Ba (OH) 2 · XH 2 O, Y (NO 3 ) 3 · 6H 2 O, Yb 2 O 3 , (CH 3 CO 2 ) 3 Er, NaBF 4 , NH 4 F, NaF, ácido oleico y HNO 3 y se utilizó etanol absoluto. Se utilizó agua desionizada en todo momento. Todos los materiales químicos se utilizaron tal como se recibieron sin purificación adicional.
Preparación de BaYF sintético 5 :Er 3+ , Yb 3+
Yb 2 O 3 se disolvió en HNO 3 diluido calentando la solución para obtener el Yb (NO 3 ) 3 solución. En una ruta sintética típica, Ba (OH) 2 · XH 2 O, Y (NO 3 ) 3 · 6H 2 O, (CH 3 CO 2 ) 3 Er y NaBF 4 se disolvieron por separado en agua desionizada. Según la relación de BaY 1-x-y F 5 :xEr 3+ , yYb 3+ , la solución de Ba (OH) 2 · XH 2 O, Y (NO 3 ) 3 · 6H 2 O, (CH 3 CO 2 ) 3 Er, Yb (NO 3 ) 3, y NaBF 4 se pusieron en una taza de teflón. Se agregaron ácido oleico y etanol a la mezcla para que correspondiera a una cierta proporción. El valor de pH de la solución mezclada se ajustó a 9 utilizando NH 3 · H 2 O. Después de agitar magnéticamente durante 30 min, la copa de teflón se mantuvo en un autoclave de sellado de acero inoxidable y se calentó a 200 ° C durante 16 h. Cuando el autoclave se enfrió naturalmente a temperatura ambiente, el producto se centrifugó con etanol y agua desionizada tres veces respectivamente y se secó a 60 ° C durante 12 h.
Caracterización
La difracción de rayos X (XRD) se obtuvo en el avance BrukerD8 a una velocidad de escaneo de 10 ° / min en el 2 θ oscilan entre 10 y 70 con radiación Cu Kα. La espectroscopía de fotoluminiscencia (PL) se registró en un espectrómetro de fluorescencia (FLS920, Edinburgh Instruments) tras la excitación de onda continua de un diodo láser de 980 nm. El microscopio electrónico de barrido (SEM) y el espectrómetro de dispersión de energía (EDS) se registraron en S-3400N-II.
Resultados y discusión
La Figura 1i presenta los patrones XRD del BaYF 5 :20% Yb 3+ , 2% Er 3+ sintetizado por diferentes condiciones. Los picos de difracción de todas las muestras se pueden indexar fácilmente a la fase tetragonal estándar BaYF 5 (JCPDS n. ° 46-0039) a excepción de la Fig. 1i (a) debido a la generación de fase adicional BaF 2 al valor de pH de 4 . Cuando el pH aumentó de 4 a 9, se mejoró el cristalino de la muestra. Mientras tanto, el BaF 2 fase desapareció también. No aparecieron picos adicionales de otra fase, lo que revela que las condiciones experimentales variables tienen poca influencia en la estructura cristalina de la muestra. Cabe señalar que todos los picos de difracción se desplazan a 2 θ superiores lado, lo que indica que la constante de celosía se vuelve más pequeña porque los radios de Er 3+ o Yb 3+ son más pequeños que los de Y 3+ [25, 26]. Además, es fácil encontrar las reglas de que cuando aumenta el tiempo de reacción, la intensidad de los picos de difracción aumenta simultáneamente. Se extraen conclusiones similares cuando aumentan las temperaturas. Concluye que las condiciones de reacción anteriores pueden promover el crecimiento de BaYF 5 cristales. El análisis del espectro EDS de una muestra específica se indicó en la Fig. 1ii. Como se muestra en el diagrama, se confirmó la presencia de los elementos de Ba, Y, F, Yb y Er en la muestra dada. Según los resultados de XRD y EDS, Er 3+ y Yb 3+ fueron dopados con éxito en BaYF 5 . La Figura 1v muestra las imágenes SEM de BaYF 5 sintetizados en diferentes condiciones. Las muestras preparadas que se muestran en la Fig. 1v (A) son microesferas con un tamaño de aproximadamente 45 nm. Sin embargo, no están finamente dispersos ni agregados hasta cierto punto. De acuerdo con su diagrama XRD en la Fig. 1i (c), el tamaño del cristal se puede calcular aproximadamente mediante la ecuación de Scherrer:
$$ D =K \ gamma / B \ \ cos \ theta $$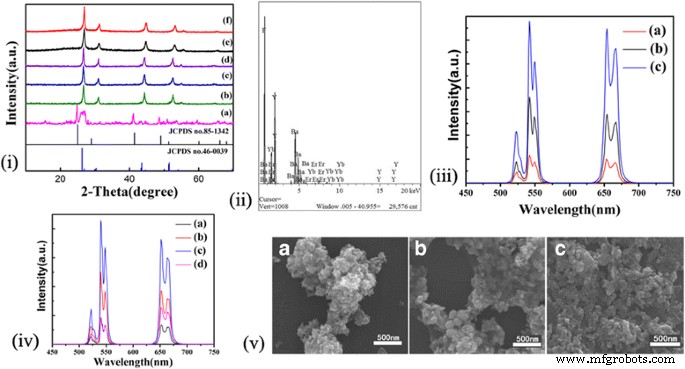
yo Patrones XRD del 2% Er 3+ preparado , 20% Yb 3+ -codoped BaYF 5 , el pH es igual a 9 excepto (a), cuyo pH es igual a 4. (a) 200 ° C, 16 h. (b) 200 ° C, 12 h. (c) 200 ° C, 16 h. (d) 200 ° C, 24 h. (e) 180 ° C, 16 h. (f) 220 ° C, 16 h. El patrón XRD estándar de BaYF 5 (JCPDS n. ° 46-0039) y BaF 2 (JCPDS n. ° 85-1342) también se proporciona a modo de comparación. ii EDS del producto correspondiente a XRD (d). iii Espectros de emisión de UC de las muestras sintetizadas a 200 ° C, (a) 12 h, (b) 16 h, (c) 24 h. iv Espectros de emisión de UC de los productos sintetizados durante 16 h. (a) 180 ° C, pH =9. (b) 200 ° C, pH =9. (c) 220 ° C, pH =9. (d) 200 ° C, pH =4. v Imágenes SEM del BaYF 5 preparado sintetizados en diferentes condiciones. (A) 200 ° C, 16 h. (B) 220 ° C, 16 h. (C) 200 ° C, 24 h
donde K es la constante de Scherrer ( K es igual a 0,89), γ es la longitud de onda de los rayos X ( γ es igual a 0,15405 nm), B es el ancho completo a la mitad del máximo de los picos de difracción de las muestras, y θ es el ángulo de difracción del pico observado [27, 28]. La intensidad más fuerte del pico de difracción a 2 θ =26,689 ° se utilizó para calcular el tamaño medio del cristal. Se estima que el tamaño medio del cristal es de 41,7 nm, que se cierra al tamaño (45 nm) mediante la observación del gráfico SEM. Como se representa en la Fig. 1v (B), cuando la temperatura de reacción se incrementó a 220 ° C, las dispersiones de las partículas se volvieron relativamente altas. Sin embargo, el tamaño del cristal era desigual y aparecieron algunas partículas más grandes con un tamaño de aproximadamente 180 nm. Cuando el tiempo de reacción se prolongó a 24 h, los nanocristales se dispersaron relativamente bien con una morfología de partículas uniforme. Los tamaños son de aproximadamente 30 nm, que son básicamente consistentes con las estimaciones (24,9 nm) de los datos XRD. La Figura 1iii, iv muestra los espectros de luminiscencia UC de BaYF 5 :Er 3+ / Yb 3+ sintetizado a través de diferentes condiciones experimentales bajo excitación a 980 nm. La banda de emisión principal de Er 3+ es 520, 540 y 654 nm como resultado de 2 H 2/11 → 4 Yo 15/2 (verde), 4 S 3/2 → 4 Yo 15/2 (verde) y 4 F 2/9 → 4 Yo 15/2 (rojo) transiciones, respectivamente. En la Fig. 1iii, iv, a medida que aumenta la temperatura, es beneficioso para el crecimiento de cristales del producto, mientras que se prolonga el tiempo de reacción, el aumento del pH tiene el mismo efecto. La intensidad de luminiscencia de UC se puede mejorar debido a la formación de cristales más altos. Cuando se prolongó el tiempo de reacción o se ajustó el pH de 4 a 9, las nanopartículas tienen mejor cristalización debido a sus mayores dispersiones y tamaños más uniformes.
La Figura 2i muestra los patrones XRD de BaYF 5 : x Yb, 2% Er ( x =10%, 30%). Todos los picos de difracción coinciden perfectamente con el patrón estándar de BaYF 5 cristales (JCPDS no 46-0039). Muestra que el dopaje de iones de tierras raras no afecta el crecimiento de cristales. Como se muestra en la Fig.2ii, cuando Yb 3+ La concentración aumenta del 10 al 20%, la intensidad de luminiscencia UC aumenta rápidamente hasta que Yb 3+ la concentración supera el 20% debido a la extinción de la concentración. Se concluye que la concentración del 20% es la concentración óptima.
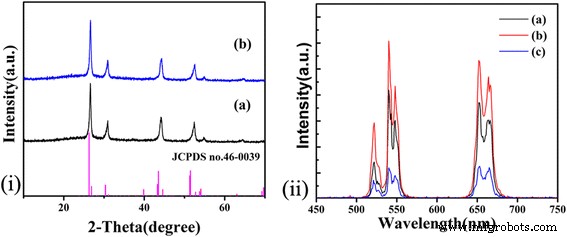
yo Patrones XRD del 2% Er 3+ preparado , Yb 3+ -codoped BaYF 5 sintetizado a 200 ° C durante 16 h con diferentes Yb 3+ concentraciones, (a) 10% Yb 3+ y (b) 30% Yb 3+ , el patrón XRD estándar de BaYF 5 (JCPDS n. ° 46-0039) también se proporciona a modo de comparación. ii Espectros de emisión de UC de las muestras sintetizadas a 200 ° C durante 16 h con diferentes Yb 3+ concentraciones. (a) 10% Yb 3+ , (b) 20% Yb 3+ , (c) 30% Yb 3+
La Figura 3i muestra los patrones XRD de BaYF 5 :Yb 3+ / Er 3+ nanocristales obtenidos mediante la adición de diferentes tensioactivos. Todos los picos de difracción se combinan perfectamente con la tarjeta estándar de fase tetragonal BaYF 5 (JCPDS no 46-0039). Cuando se agregó 5% de polieterimida (PEI), la intensidad de los picos de difracción aumenta, lo que indica que PEI puede promover el crecimiento de BaYF 5 cristales. Además, después de la adición de ácido cítrico, los picos de difracción se desplazan a un ángulo más bajo. Esto prueba que cuando se agregó citrato (CIT), el volumen celular de la muestra aumenta gradualmente. La otra razón puede ser que el ácido cítrico está cubierto en la superficie del cristal, los iones de tierras raras son difíciles de adultar en las redes del huésped. Además, los picos de difracción se vuelven diferentes a los demás con un pequeño defecto como el CIT / Y =4:1. La razón concebible radica en la alta concentración de CIT que conduce al BaYF 5 cambio de parámetro de celda unitaria y distorsión de celosía. Como se ilustra en la Fig. 3iii (A), cuando se añadió 5% de PEI en etanol, los nanocristales se convirtieron en grumos masivos que consisten en un gran número de partículas esféricas con una distribución de tamaño estrecha. La Figura 3iii (B) y (C) muestra que cuando se añadió el tensioactivo con una concentración de CIT / Y =1:1, el tamaño total del cristal se hizo relativamente mayor. Como puede verse en el diagrama, la muestra tiende a agregarse sin límites obvios en algunas áreas. A medida que la relación de concentración de tensioactivo aumenta a 4:1, el tamaño máximo de las partículas aumenta a 4 um con la superficie cubierta por algunas otras partículas esféricas más pequeñas. A medida que aumenta la concentración de tensioactivo, se mejora la capacidad de cobertura de CIT [29], lo que conduce a la formación de grupos de cristales. Como se muestra en la Fig. 3ii, tanto la emisión verde como la emisión roja se mejoran después de agregar 5% de PEI en etanol. Los grupos amino de cadena larga de PEI pueden formar estructuras complejas con iones metálicos por coordinación. PEI puede inhibir el crecimiento de partículas envolviendo firmemente la superficie para mejorar el cristalino. Por el contrario, después de agregar ácido cítrico, la emisión de luminiscencia de UC disminuyó en gran medida debido al aumento del tamaño del cristal y la disminución del contenido de iones de tierras raras.
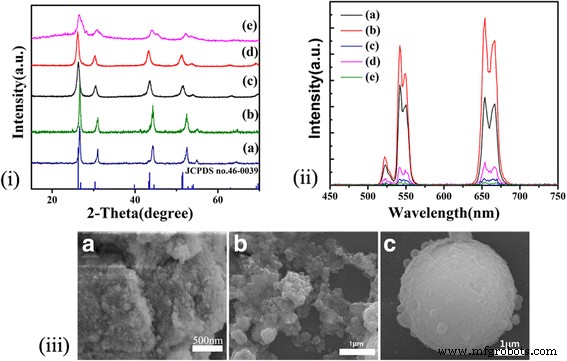
yo Patrones XRD del 2% Er 3+ preparado , 20% Yb 3+ -codoped BaYF 5 sintetizado a 200 ° C durante 24 h, (a) el solvente es etanol, (b) el solvente consiste en 95% de etanol y 5% de PEI, (c) - (e) se agregó ácido cítrico como surfactante, la proporción de CIT a Y es 1:1, 2:1 y 4:1, respectivamente. El patrón XRD estándar de BaYF 5 (JCPDS n. ° 46-0039) también se proporciona para realizar la comparación. ii Espectros de emisión de UC de BaYF 5 preparado. (a) El solvente es etanol, (b) el solvente consiste en 95% de etanol y 5% de PEI, (c) CIT / Y =1:1, (d) CIT / Y =2:1, (e) CIT / Y =4:1. iii Imágenes SEM de las muestras sintetizadas mediante la adición de diferentes tensioactivos con diferentes concentraciones. (A) 5% PEI, (B) CIT / Y =1:1, (C) CIT / Y =4:1
La Figura 4i muestra el patrón XRD de productos obtenidos de diferentes fuentes de fluoruro. No aparecen picos de impurezas, lo que demuestra que el cambio de fuentes de fluoruro no afecta la cristalización de BaYF 5 . Vale la pena señalar que hay menos cambios de los picos de difracción de las muestras obtenidas de NH 4 F o NaF que los de las muestras obtenidas de NaBF 4 . Esto indica que NH 4 F y NaF lanzaron F - desordenada y rápidamente, resultando en la dificultad del control de la síntesis de cristales [30]. Como consecuencia, los iones de tierras raras se vuelven difíciles de ingresar a las redes del anfitrión. La Figura 4iii representa las imágenes SEM de la muestra usando NH 4 F y NaF como fuentes de fluoruro. Las partículas son similares a los nanocristales que se sintetizan agregando un 5% de PEI. Sin embargo, las formas son más irregulares en relación con las obtenidas de NaBF 4 . Como puede verse en la Fig. 4ii, la muestra que utilizó NaBF 4 como fuente de fluoruro muestra la mayor eficiencia de emisión de UC debido a los beneficios del crecimiento del cristal que genera una forma de esfera uniforme. Las partículas en tamaños más pequeños tendrán más Er 3+ en la superficie submicrométrica, provocando más vibraciones superficiales para conducir la aceleración en la emisión roja y verde. Además, la distancia entre Er 3+ se vuelve más pequeño y ocurre una relajación cruzada ( 2 H 2/11 + 4 Yo 15/2 → 4 Yo 2/9 + 4 Yo 13/2 ). Como resultado, la banda verde ( 2 H 2/11 , 4 S 3/2 → 4 Yo 15/2 ) se vuelve fácil de apagar en tamaños más pequeños, pero la banda roja ( 4 F 2/9 - 4 Yo 15/2 ) se vuelve más difícil de apagar [24, 31].
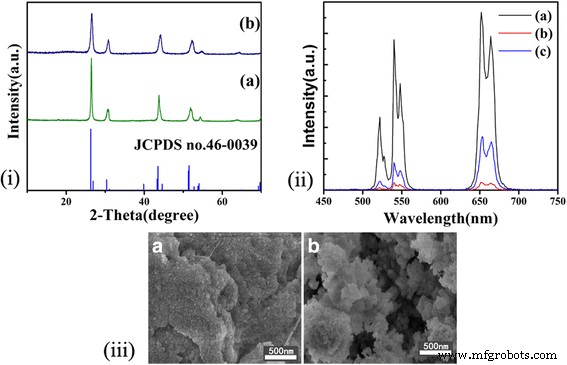
yo Patrones XRD del 2% Er 3+ preparado , 20% Yb 3+ -codoped BaYF 5 sintetizado a 200 ° C durante 24 h; Se añadió 5% de PEI para realizar una comparación conveniente. (a) y (b) la fuente de fluoruro era NH 4 F y NaF, respectivamente. El patrón XRD estándar de BaYF 5 (JCPDS n. ° 46-0039) también se proporciona para realizar la comparación. ii Espectros de emisión de UC de muestras. (a) NaBF 4 . (b) NH 4 F. (c) NaF. iii Imágenes SEM de los productos (A) NH 4 F. (B) NaF
La Figura 5 muestra los niveles de energía esquemáticos de Yb 3+ y Er 3+ . Mientras tanto, describe los mecanismos del proceso de luminiscencia UC que explican la generación de emisiones verdes y rojas bajo excitación láser de 980 nm. En el Yb 3+ / Er 3+ -codoped BaYF 5 sistema, mediante la absorción del primer fotón de 980 nm, Yb 3+ ion en el 2 F 7/2 el estado fundamental se transfiere al estado excitado 2 F 5/2 . Cuando vuelve al estado fundamental, la energía se transfiere a Er 3+ ion para poblar el 4 Yo 2/11 Expresar. El segundo fotón de 980 nm o transferencia de energía de otro Yb 3+ excitado , puede bombear Er 3+ ion en 4 F 7/2 nivel. Los estados de menor energía 2 H 2/11 y 4 S 3/2 puede ser poblado por 4 en descomposición no radiativa F 7/2 Expresar. Las transmisiones del electrón desde 2 H 2/11 y 4 S 3/2 al 4 Yo 15/2 el estado fundamental emite emisiones verdes. Alternativamente, Er 3+ ion en el 4 Yo 2/11 El estado también puede relajarse no radiativamente a 4 Yo 13/2 Expresar. 4 F 2/9 estado de Er 3+ se puede poblar por absorción de fotones o transferencia de energía de Yb 3+ . Las emisiones de UC rojo se producen a través de la transición de 4 F 2/9 a 4 Yo 15/2 . Algunos electrones en el 4 F 2/9 el nivel puede estar emocionado a 2 H 2/9 mediante un proceso de transferencia de energía asistido por fonones, y se pueden observar las emisiones azules. Las bandas de emisión a 520, 540 y 654 nm podrían corresponder a la transferencia de electrones desde el nivel excitado 2 H 2/11 , 4 S 3/2 y 4 F 2/9 al estado fundamental 4 Yo 15/2 de Er 3+ , respectivamente [19, 32, 33].
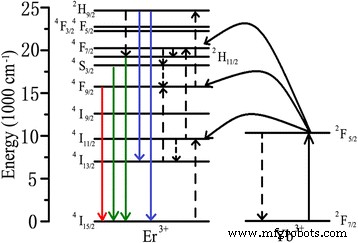
Diagrama esquemático de niveles de energía entre Er 3+ y Yb 3+
Conclusión
En resumen, BaYF 5 :20% Yb 3+ , 2% Er 3+ se han sintetizado con éxito mediante un método solvotermal conveniente. Se encuentra que el uso de NaBF 4 como fuente de fluoruro o la adición de PEI al 5% como tensioactivo puede mejorar eficazmente la dispersión cristalina y de partículas que pueden promover la emisión de UC. En comparación con PEI, a medida que aumenta la concentración de CIT, las nanopartículas se vuelven gradualmente más grandes, lo que es inversamente proporcional a las propiedades luminosas. Es obvio que los nanocristales a través de 220 ° C de temperatura de tratamiento térmico durante 24 h son una condición de reacción óptima de las excelentes propiedades de luminiscencia. Estos comportamientos pueden atribuirse a sus grandes tamaños uniformes, su buena dispersión y su alta cristalinidad.
Nanomateriales
- Los diferentes tipos de manijas para pasadores de liberación rápida
- En sintonía con el corazón de un átomo de cobre
- El potencial para integrar datos visuales con IoT
- MoS2 con espesor controlado para evolución electrocatalítica de hidrógeno
- Síntesis y propiedades electroquímicas de materiales de cátodo LiNi0.5Mn1.5O4 con dopaje compuesto Cr3 + y F− para baterías de iones de litio
- Síntesis fácil de nanocables de plata con diferentes relaciones de aspecto y utilizados como electrodos transparentes flexibles de alto rendimiento
- Biosensor ultrasensible para la detección de ADN de Vibrio cholerae con nanoesferas compuestas de poliestireno-co-ácido acrílico
- Método de postratamiento para la síntesis de nanopartículas de FePt-Fe3O4 binarias monodispersas
- Polímero poroso funcional a base de trifenilfosfina como catalizador heterogéneo eficiente para la síntesis de carbonatos cíclicos a partir de CO2
- ¿Cuáles son las diferentes opciones para el acabado de metales?
- 11 tipos diferentes de procesos de soldadura con la ayuda del diagrama



