Desfosforación de Aceros
Desfosforación de Aceros
Los efectos del fósforo (P) en las propiedades de los aceros se resumen en la Pestaña 1. Se puede ver que el P tiene efectos tanto positivos como negativos en las propiedades del acero.
| Tab 1 Efectos del fósforo en las propiedades de los aceros | ||
| Sl.No. | Propiedad | Efecto del fósforo |
| 1 | Fuerza | Fuerte positivo (refuerza la ferrita) |
| 2 | Endurecimiento al horno | Positivo |
| 3 | Ductilidad | Negativo fuerte |
| 4 | Recocido galvánico | Puede mejorar la resistencia al polvo |
| 5 | Fosfatabilidad | Positivo |
| 6 | Esmaltado | |
| a. Descamación de pescado | Negativo | |
| b. Decapado | Positivo | |
| 7 | Soldabilidad | No perjudicial para contenidos inferiores al 0,1 % |
| 8 | Pérdida de núcleo en laminación del motor | Negativo fuerte |
| 9 | Resistencia a la fractura | Negativo fuerte |
Los aceros con bajo contenido de P son necesarios para aplicaciones donde se necesita alta ductilidad, como láminas delgadas, acero de embutición profunda y tuberías, etc. En los primeros días, el control de P no se consideraba un gran desafío en la producción de acero, ya que los minerales de hierro con bajo Los contenidos de P estaban disponibles fácil y económicamente. Sin embargo, en el pasado reciente, debido a los altos precios del mineral de hierro, se están utilizando minerales de hierro de menor precio de fuentes que normalmente tienen un mayor contenido de P y esto ha hecho que el control de P sea una actividad importante durante la fabricación de acero.
Además del P de los minerales de hierro, el P también ingresa al acero líquido debido al reciclaje de la escoria BOF (horno de oxígeno básico). El reciclaje de la escoria BOF se realiza a través de la planta de sinterización o directamente en el alto horno para recuperar el contenido de hierro y cal de la escoria y minimizar los problemas relacionados con la eliminación de la escoria. El sinterizado o la escoria BOF alimentada al alto horno inevitablemente aumenta el contenido de P del metal caliente y, por lo tanto, las cargas de P en el proceso de fabricación de acero.
En las plantas siderúrgicas integradas, la eliminación de P normalmente tiene lugar durante el proceso primario de fabricación de acero, generalmente el proceso BOF. Para cumplir con las nuevas demandas de control de P, es necesario mejorar la comprensión de la termodinámica y la cinética de la reacción de partición de P entre la escoria y las masas fundidas de metal durante el proceso de fabricación de acero.
La desfosforación de aceros se ha convertido en una técnica metalúrgica muy importante en el proceso de fabricación de acero para producir aceros de alta calidad. Como el contenido de P está controlado por las reacciones en BOF, la técnica de doble escoria se ha aplicado generalmente para obtener aceros calmados con bajo contenido de P. Sin embargo, esta técnica va acompañada del aumento del tiempo de operación y la disminución del rendimiento del acero. Además de los problemas de productividad con esta técnica, también se genera una enorme cantidad de escoria BOF durante la operación del BOF.
El fósforo también se puede eliminar durante el proceso de refinación del acero. De hecho, más del 90 % de la entrada de P en la masa fundida se puede eliminar en el BOF. La capacidad de refinación de la escoria depende de muchas variables, como la composición de la escoria y del metal, la temperatura, el tiempo y la intensidad de la agitación de la escoria/metal.
El contenido de P en el acero líquido durante el colado, la desoxidación, el soplado con gas inerte y la colada puede aumentar gradualmente debido a su introducción con desoxidantes y reducción a partir de una escoria. Esta posibilidad se debe tener en cuenta para mantener las condiciones de desfosforación en el acero líquido. Como resultado de las reacciones entre el acero, la escoria y los desoxidantes, el equilibrio de P se desplaza hacia un aumento del contenido de P en el acero a pesar de una disminución significativa de la temperatura. En este caso, la desfosforación depende sustancialmente de la relación entre el acero y el peso de la escoria. El papel de estos factores se puede deducir de la siguiente ecuación de balance de P.
(Contenido de P en la escoria de la cuchara) + (Contenido de P en el acero de la cuchara) =(Contenido de P en el metal colado) + (Contenido de P en la escoria atrapada por el acero en la cuchara) + (P de los desoxidantes).
Reacción del fósforo y equilibrio termodinámico
Los estudios integrales iniciales sobre la desfosforación se realizaron durante la década de 1940. Estos estudios observaron que el FeO y el CaO son componentes necesarios de la escoria para la desfosforación del acero. Estos estudios también mostraron que la reacción de desfosforación es exotérmica y que la capacidad de desfosforación de la escoria disminuye con la temperatura. Los estudios también han observado que la desfosforación se ve reforzada por una disminución de la temperatura y un aumento en el contenido de FeO y la basicidad de la escoria.
Se han desarrollado muchas correlaciones para predecir la relación de partición de P en función de la composición del metal y la escoria, así como de la temperatura. Sin embargo, todavía hay desacuerdos en los datos de laboratorio y la partición P de equilibrio que se puede predecir.
Aunque la cuantificación del equilibrio P es extremadamente importante, muchos de los hornos siderúrgicos no funcionan en equilibrio, normalmente debido a la formación de escoria líquida, la cinética y las limitaciones de tiempo. Por lo tanto, es importante saber qué tan cerca del equilibrio operan los hornos de fabricación de acero para sugerir composiciones de escoria óptimas para promover la desfosforación.
Durante los primeros estudios se observó que las condiciones de agitación y la composición de la escoria son dos variables clave para permitir una eliminación óptima de P. Además, la saturación excesiva de la escoria con CaO y MgO no parece beneficiar el proceso en ninguna medida.
Durante estos estudios se descubrió que es probable que los fenómenos interfaciales dinámicos en la interfaz metal-escoria desempeñen un papel importante en el comportamiento cinético del sistema, debido al intercambio de elementos activos de superficie, como el oxígeno (O2), que reduce drásticamente la tensión interfacial y provocar la emulsificación espontánea. También se encontró que el P no juega un papel en la emulsificación espontánea y se elimina rápidamente antes del inicio de los fenómenos interfaciales dinámicos. La emulsificación es causada quizás por la desoxidación del metal después de que se ha eliminado el P y el metal se ha supersaturado con O2 por una razón desconocida. El área superficial estimada aumenta rápidamente en más de un orden de magnitud durante los períodos inicial e intermedio de la reacción. La gota de metal se rompe en cientos de pequeñas gotas, emulsionando efectivamente el metal en la escoria. Con el tiempo, el área superficial disminuye y las gotas de metal se unen. Se observaron resultados similares para una gota de hierro (Fe) oxidada.
En la década de 1950, se propuso que es satisfactorio considerar que la reacción tiene lugar en su forma más simple, como se indica a continuación.
2P + 5O =P2O5 (líquido)
La energía libre asociada con la reacción se evaluó utilizando una estimación de la entropía de fusión de P2O5, de modo que
Delta G =– 740375+535,365 T J/mol
En T más de 1382 grados K, ¿Delta G? se vuelve positivo, lo que da como resultado la descomposición de P2O5 en P y O. Por lo tanto, la eliminación de P requiere que se reduzca el P2O5. El coeficiente de actividad del P2O5 aumenta con la sílice (SiO2) y disminuye con los óxidos básicos como el CaO y el MgO.
Durante la década de 1980 se llevaron a cabo más estudios sobre la partición de P en varios sistemas de escoria. Estos estudios han indicado que la relación de distribución de P aumenta con el aumento del contenido de CaO en la escoria y con la disminución de la temperatura. También se ve que el efecto del CaF2 sobre la desfosforación es el mismo que el del CaO sin elevar el punto de fusión de la escoria. También se estudiaron los efectos del óxido de bario (BaO) y el óxido de sodio (Na2O) en la partición de P. Estos estudios concluyeron que las equivalencias de CaO de Na2O y BaO son 1,2 y 0,9 en porcentaje en peso, respectivamente.
La distribución de P en los diferentes sistemas de escoria se ha estudiado en numerosas ocasiones y se han desarrollado varias correlaciones. Las diversas conclusiones de estos estudios se resumen a continuación.
- Los contenidos de CaO, MgO, SiO2, P2O5, FeO y MnO de la escoria tienen influencia en la partición de P.
- La escoria líquida está completamente ionizada y el P en la escoria existe como un ion fosfato.
- El logaritmo de la partición P aumenta con un 2,5 log % de FeO como predice la termodinámica y ese aumento de la basicidad de la escoria también aumenta el coeficiente de partición.
- Aumentar la basicidad de la escoria (CaO/SiO2) hasta 2,0 tiene un fuerte efecto creciente en la partición P. Sin embargo, el aumento es mucho menos pronunciado con basicidades superiores a 2,5.
- La relación de partición P aumenta inicialmente con el aumento del contenido de FeO, pero luego disminuye después de alcanzar un cierto nivel. Este nivel es función de la basicidad y la temperatura de la escoria. Estas conclusiones también son válidas para contenidos de FeO en la escoria entre el 15 % y el 25 %. Más concretamente, la partición P es independiente de contenidos de FeO superiores al 19 %. Además, la partición de P parece ser menor con un aumento del contenido de MgO a temperaturas de 1600 °C y 1650 °C.
- Para las escorias que contienen del 0,2 % al 1,0 % de P2O5, el logaritmo del coeficiente de actividad de P2O5 es una función lineal del contenido de CaO y MgO y no depende de la temperatura. Para la escoria que contiene P2O5 en más del 1 %, el logaritmo del coeficiente de actividad de P2O5 también es una función lineal de CaO pero también depende de la temperatura.
- Los aumentos en las concentraciones de Ca2+, Fe2+ y Mg2+ dan como resultado una disminución del coeficiente de actividad de P2O5 mientras que (SiO4)4- tiene el efecto contrario.
- La polimerización de P no ocurre mucho en las escorias que normalmente se encuentran en la fabricación de acero.
También se han probado otros enfoques para la partición del modelo P entre el acero y la escoria. En 2011, se desarrolló un modelo termodinámico exhaustivo basado en la teoría de la coexistencia de iones y moléculas (IMCT) para predecir la relación de distribución de P entre las escorias de CaO-SiO2-FeO-Fe2O3-MnO-Al2O3-P2O5 y el acero líquido. El IMCT asume que la escoria está compuesta de iones simples, como Ca2+, Fe2+, Mg2+ y O2-; moléculas simples, P2O5, SiO2 y Al2O3; silicatos, aluminatos y muchos otros como moléculas complejas. Todas las especies iónicas participan en reacciones para formar moléculas complejas a partir de pares de iones (Me2+ y O2-) y moléculas simples y se encuentran en equilibrio termodinámico. Las posibles moléculas de P tenidas en cuenta son P2O5, 3FeO.P2O5, 4FeO.P2O5, 2CaO.P2O5, 3CaO.P2O5, 4CaO.P2O5, 2MgO.P2O5, 3MgO.P2O5 y 3MnO.P2O5. Se ha encontrado que 3CaO.P2O5 y 4CaO.P2O5 tienen una contribución a la partición de P medida del 96 % y 4 % respectivamente.
La discusión hasta ahora involucró el equilibrio P entre el acero líquido y la escoria líquida. Sin embargo, debido a la naturaleza multicomponente de las escorias siderúrgicas, no es raro tener posibles fases sólidas en equilibrio con la escoria líquida. Se han llevado a cabo estudios sustanciales sobre fases sólidas específicas que son comunes en las escorias siderúrgicas. Más específicamente, los estudios se han centrado en las escorias que contienen partículas de 2CaO.SiO2 y CaO. Estas fases sólidas normalmente están presentes en las escorias siderúrgicas durante el proceso BOF y pueden desempeñar un papel en la desfosforación ya que los fosfatos se pueden disolver en ellas.
Refinado de fósforo en proceso BOF
Un buen productor de acero también es un buen productor de escoria”, es un dicho popular entre el personal de fabricación de acero y es muy relevante en el contexto del proceso BOF. Tener un buen control sobre la formación y composición de la escoria permite una refinación óptima y minimiza el riesgo de tener que volver a soplar el O2 o hacer adiciones adicionales al final de la colada. Durante el comienzo del golpe, la lanza se mantiene muy por encima de la superficie del metal. Durante los primeros 3 a 4 minutos, el Si (silicio) del metal se oxida rápidamente junto con el Fe formando una escoria rica en FeO y SiO2. Se añaden cantidades sustanciales de cal y cal dolomítica al BOF. A medida que continúa el golpe, la cal sólida se disuelve continuamente en la escoria líquida aumentando la masa y la basicidad de la escoria. A medida que continúa la descarburación, la escoria comienza a formar espuma y el gas CO generado reduce el contenido de FeO en la escoria. Cerca del final del golpe, la tasa de descarburación disminuye y la oxidación de Fe vuelve a ser significativa. A lo largo del golpe, la temperatura del metal aumenta constantemente de 1350 °C a 1650 °C y la temperatura de la escoria es generalmente 50 °C más alta que la del metal al final del golpe.
El mecanismo de disolución de la cal es muy relevante para el proceso BOF y la eliminación de P. Lograr una disolución rápida de la cal durante el proceso BOF brinda una buena oportunidad para aumentar la productividad y reducir el tiempo y el costo del proceso. El mecanismo de disolución de la cal es función de la composición de la escoria y del nivel de saturación del silicato dicálcico (2CaO.SiO2). La escoria inicial es rica en FeO y SiO2. Cuando se agrega cal por primera vez y comienza a disolverse, se forma una capa de 2CaO.SiO2 alrededor de las partículas sólidas y disminuye la velocidad de disolución de la cal. Esta capa sólida puede romperse y la escoria puede penetrar aún más en los poros de la partícula de cal y continuar la disolución. La penetración de la escoria es función de la viscosidad y el tamaño de poro de la partícula sólida.
Dado que en el proceso BOF frecuentemente coexisten algunas fases sólidas de óxido con la escoria, es importante comprender cómo las partículas sólidas pueden influir en la eliminación de P. Varios estudios han analizado la solubilidad del P en diferentes partículas sólidas como CaO, 2CaO.SiO2 y 3CaO.SiO2. Las siguientes son algunas de las inferencias de estos estudios.
- La partición de fósforo entre las partículas de 2CaO.SiO2 y la escoria varía entre 2 y 70 a medida que aumenta el contenido de FetO y la basicidad de la escoria. Se encuentra que la dependencia de la temperatura de la distribución de P es muy débil y las partículas aisladas de 2CaO.SiO2 muestran una transformación uniforme completa a 2CaO.SiO2-3CaO.P2O5 en 5 segundos.
- Al entrar en contacto con la escoria de CaO-FetO-SiO2-P2O5, la partícula de CaO se encapsula rápidamente por una capa de 2CaO.SiO2-3CaO.P2O5 y una escoria de CaO-FetO sin que se forme P2O5 entre la partícula de CaO y el 2CaO .Solución sólida de SiO2-3CaO.P2O5.
- Hay dos rutas posibles para la transferencia de P de la escoria al 2CaO.SiO2. En la primera ruta, 2CaO.SiO2-3CaO.P2O5 precipitaría de la escoria líquida después de que el P se transfiera de la fase metálica. En la segunda ruta posible, las partículas de 2CaO.SiO2 ya presentes en la escoria antes de que el P se transfiera del metal. Luego, el P se difunde en la partícula de 2CaO.SiO2 precipitada, libre de P. Se ha encontrado que la tasa de transferencia de P por la ruta de precipitación es mucho más rápida que por la ruta de difusión. Esto señala el hecho de que tener partículas de 2SiO2.SiO2 preexistentes no necesariamente mejora la eliminación de P.
Durante el proceso de soplado en BOF se crea un entorno muy dinámico. A medida que el chorro de O2 golpea la superficie de la escoria y, posteriormente, el metal líquido, crea una emulsión trifásica de gas-escoria-metal, lo que aumenta significativamente el área interfacial total disponible para que ocurran varias reacciones químicas entre las fases. Las gotas de metal se expulsan continuamente del baño de metal a granel a la mezcla de escoria y gas, donde pueden reaccionar durante un período de tiempo determinado. La generación de estas gotas de metal es muy importante para la cinética dentro del BOF.
La tasa de refinación, durante el proceso BOF, no es solo una función de la cinética química sino también una función del tiempo de residencia que una gota de metal dada pasa en la escoria. El tiempo de residencia calculado de una gota de metal que se expulsa del metal a granel que viaja en una trayectoria balística a través de la escoria es inferior a 1 segundo, que es demasiado corto para que una gota determinada reaccione de manera significativa. Sin embargo, durante el estudio del comportamiento de las gotas de Fe-C en la escoria, se ha observado que la formación de un "halo" de gas mientras se produce la descarburación mantiene la gota de metal suspendida en la escoria de 50 a 200 segundos. Sobre la base de estas observaciones, el modelo se modifica para incluir el efecto de la descarburación en la densidad aparente de una gota de metal y es capaz de predecir los tiempos de residencia de consistencia.
El informe titulado 'Imphos:Improving Phosphorus Refining' publicado en 2011 ha analizado, entre otros temas, los perfiles de relación metal/escoria, la distribución del tamaño de las gotas de metal en la emulsión escoria/metal, la distribución de P en la interfaz escoria-metal y la disolución de la cal. El informe ha definido cinco perfiles de eliminación de P, como se muestra en la Fig. 1. Estos perfiles son (i) un perfil de P casi constante, (ii) un perfil de reversión de P, (iii) un perfil de alta eliminación de P, (iv) un perfil de reversión y desaceleración de P, y (v) reversión con perfil de eliminación rápida de P. Para cada uno de estos perfiles se ha estudiado la cantidad de metal y su composición química para la emulsión escoria/metal y para el baño a granel. Se ha encontrado que el contenido de P de las gotas de metal en la escoria suele ser menor o igual que el del baño a granel, lo que indica que la eliminación de P es impulsada por la desfosforación de las gotas de metal presentes en la emulsión de escoria/metal en lugar de en la emulsión de escoria/metal. baño a granel. Una observación interesante en el informe es que, durante las primeras etapas del golpe, la eliminación de P en las gotitas emulsionadas ocurrió mucho más rápido que la descarburación.
Se encuentra que las gotas de metal están extremadamente empobrecidas en P (mucho menos de 100 ppm) mientras que hay más del 1 % de C en el baño. Esto está potencialmente relacionado con el 'halo' de gas y la emulsificación, que pueden aumentar el tiempo de residencia de las gotas durante las primeras etapas del golpe, lo que les da tiempo suficiente para reaccionar con la escoria altamente oxidante presente, lo que resulta en una rápida eliminación de P si el tamaño de la gota es apropiado. Dado que la eliminación de P está fuertemente relacionada con la generación de gotas de metal, hay una altura de lanza ideal durante cada etapa del soplado para maximizar la generación de gotas y crear una buena emulsión de escoria/metal/gas. Se observa que a medida que disminuye la altura de la lanza, se generan menos gotas de metal.
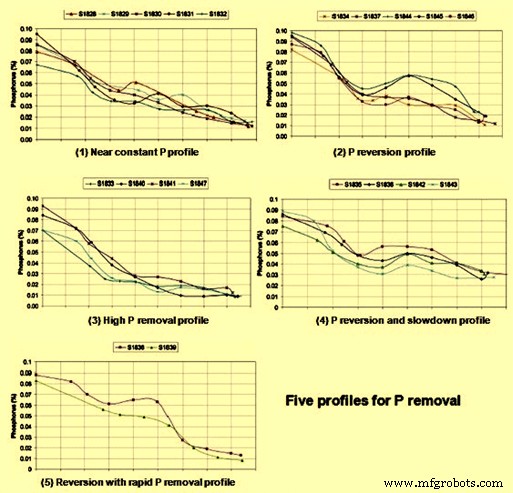
Fig. 1 Diferentes perfiles de eliminación de P
El mecanismo de desfosforación en el proceso BOF se puede resumir a continuación.
- Durante el comienzo del golpe, donde la lanza de O2 se mantiene alta, se logra una buena expulsión de gotas y la eliminación de P ocurre rápidamente.
- A medida que continúa el golpe y la descarburación comienza a generar gas CO, el FeO en la escoria se reduce y la escoria puede dejar de oxidarse lo suficiente. Esto puede resultar en la reversión de P al fundido a medida que las gotas se vuelven a fosforar y regresan al metal a granel. Esto es especialmente importante si la disolución de la cal no es óptima.
- Más cerca del final del golpe, la descarburación se ralentiza y el contenido de FeO en la escoria aumenta favoreciendo nuevamente la desfosforación. Sin embargo, esto puede no ser suficiente para compensar la posible reversión que ocurrió antes.
- Se pueden lograr resultados óptimos al monitorear de cerca el FeO y el CaO en la escoria. Las adiciones de mineral de hierro pueden ser útiles para mantener el contenido ideal de FeO para continuar con la oxidación de P en paralelo con la descarburación.
Cinética de eliminación de fósforo
Aunque el equilibrio de P se ha estudiado ampliamente, la cinética de la eliminación de P no se ha estudiado hasta ese punto. Sin embargo, se aplican los mismos principios para otras reacciones metalúrgicas a alta temperatura. Cuando el P disuelto en Fe entra en contacto con la escoria, durante la reacción de desfosforación tienen lugar varios pasos que proporcionan una ilustración básica del fenómeno. Estos pasos son los siguientes.
- Transferencia de masa en la fase metálica de [P] y [O] hacia la interfase escoria-metal
- Transferencia de masa en la fase de escoria de (O2-) hacia la interfase escoria-metal
- Reacción química en la interfase escoria-metal para la formación de (PO4)3-
- Transferencia de masa en la fase de escoria de (PO4)3- lejos de la interfaz de reacción
Dado que la desfosforación ocurre a altas temperaturas, es razonable suponer que la reacción química en la interfase es rápida y en equilibrio. Por lo tanto, los posibles pasos limitantes de la velocidad son la transferencia de masa en las fases de metal o escoria o ambas, si se supone que no hay fases sólidas presentes en la escoria capaces de absorber fósforo.
Uno de los estudios sobre la cinética de desfosforación de Fe-C(sat)-P metal caliente por escorias oxidantes, muestra que uno de los principales retos en la desfosforación de metal líquido es cuantificar correctamente la fuerza impulsora de la reacción debido a la no -Potencial de equilibrio de O2 en la interfase escoria/metal. Este desequilibrio se produce debido a la descarburación del metal líquido que reduce el potencial de O2 en el metal. En tales casos, la escoria tiene un potencial de O2 alto mientras que el metal tiene un potencial de O2 bajo. Durante el estudio se encontró que la reacción de desfosforación sigue una tasa cinética de primer orden con respecto a la concentración de P en el metal y que los contenidos más altos de FeO aumentan el coeficiente de transferencia de masa de la escoria debido a una disminución en la viscosidad, aunque el FeO también puede tener un impacto positivo o negativamente la fuerza motriz de la reacción. El estudio también indicó que el transporte de masa en la fase de escoria es el paso limitante de la velocidad en la desfosforación del metal.
Más recientemente, otro estudio utilizó un enfoque matemático para cuantificar la transferencia de masa de P entre el metal y la escoria. El estudio ha demostrado que el coeficiente de transferencia de masa aparente parece ser una función de la tensión interfacial, que se ve afectada por el flujo de masa de un elemento tensioactivo, como el O2, especialmente en condiciones de transferencia de masa rápida. Los cambios en el parámetro de transferencia de masa están relacionados con el fenómeno interfacial dinámico que mejora la transferencia de masa durante períodos de alto flujo de O2 a través de la interfaz. Se sugiere que este alto flujo de O2 disminuya la tensión interfacial durante la reacción, lo que conduce a un aumento en el área interfacial o el coeficiente de transferencia de masa, o ambos.
Varios estudios han demostrado que la emulsificación espontánea puede ocurrir durante períodos de intensa transferencia de masa de elementos tensioactivos debido a una reducción muy pronunciada en la tensión interfacial entre dos líquidos inmiscibles. Además, para la tensión interfacial de equilibrio, los contenidos de O2 y S (azufre) en el metal juegan un papel importante en la tensión de equilibrio observada. La adición de CaF2 y Na2O eleva la tensión interfacial pero las adiciones de MnO tienden a disminuirla. Uno de los estudios ha demostrado que cuando el flujo de O2 se vuelve mayor que aproximadamente 0,1 g átomo/seg, la tensión interfacial se aproxima a un valor cercano a cero. Cuando el flujo de O2 es inferior a 0,01 átomos g/seg, la tensión interfacial aumenta rápidamente hasta un valor cercano a la tensión de equilibrio.
La cinética de desfosforación ha sido mucho menos estudiada que el equilibrio P entre metal-escoria. Hay desacuerdos sobre si la transferencia de masa en el metal, la escoria o ambos controla la velocidad de la reacción. Debido a la naturaleza de la reacción, un fenómeno de interfase dinámica parece tener un papel importante en la velocidad global de la reacción. La emulsificación espontánea parece ocurrir cuando tiene lugar una rápida transferencia de masa de O2 en la interfase de los sistemas de metal-escoria. Esto da como resultado una disminución sustancial de la tensión interfacial, aumentando así el área de reacción y su velocidad global. Sin embargo, el cálculo directo de los cambios en el área de reacción debido a la emulsificación espontánea sigue siendo muy difícil.
Proceso de manufactura
- Materiales metálicos de impresión 3D
- Inconel vs acero inoxidable
- Grados comunes de acero para herramientas
- Inclusiones, Ingeniería de Inclusión y Aceros Limpios
- Granulación de escoria de alto horno en la fundición
- Operación de alto horno y escoria con alto contenido de alúmina
- Nitrógeno en Aceros
- Enjuague con argón de aceros
- Laminación en frío de aceros
- ¿Qué es la escoria?
- Comprensión de la soldadura por electroescoria (ESW)



