Matrices de nanopilares de GaAs con tapa de Au fabricadas mediante grabado químico asistido por metal
Resumen
Las matrices de nanopilares de GaAs se fabricaron con éxito mediante grabado químico asistido por metal utilizando matrices de nanopilares de Au. Las matrices de nanodot se formaron sobre sustratos mediante deposición al vacío a través de una máscara de alúmina porosa con una matriz ordenada de aberturas. Mediante el uso de un grabador con una alta concentración de ácido y una baja concentración de oxidante a una temperatura relativamente baja, el área que rodea la interfaz Au / GaAs se podría grabar de forma selectiva. En las condiciones óptimas, se formaron matrices de nanopilares de GaAs con capa de Au con una periodicidad ordenada de 100 nm y alturas de pilar de 50 nm.
Antecedentes
Los semiconductores compuestos III-V han atraído la atención como materiales de próxima generación y como posibles alternativas a los semiconductores basados en silicio debido a sus excelentes propiedades, incluida la movilidad superior del portador y la banda prohibida directa. Las nanoestructuras con periodicidad ordenada y / o alta relación de aspecto se consideran un elemento importante en diversas aplicaciones, incluidos los dispositivos ópticos y optoelectrónicos, debido a su bajo costo y alta eficiencia de conversión en comparación con los dispositivos convencionales basados en película delgada [1, 2, 3, 4] . En general, para fabricar semiconductores de baja dimensión (p. Ej., Nanocables), se utilizan procesos secos como la epitaxia de haz molecular, la epitaxia de vapor-líquido-sólido y la epitaxia de fase de vapor organometálica [1, 5, 6, 7]. Aunque estos métodos tienen muchas ventajas, incluida una alta precisión de modelado, sus inconvenientes incluyen el alto costo y las limitaciones de tamaño del área de modelado en aplicaciones prácticas. Por lo tanto, se necesitan métodos alternativos que permitan la fabricación simple y rentable de nanoestructuras.
El grabado químico asistido por metal, propuesto por Li y Bohn en 2000 [8], es un método de fabricación comúnmente utilizado debido a su relativa simplicidad y bajo costo. Estudios recientes han demostrado que el grabado químico asistido por metal se puede aplicar para fabricar nanoestructuras complejas como nanoporos rectos profundos, nanoporos helicoidales, canales inclinados, cicloides y espirales [4, 9, 10, 11, 12]. Sin embargo, desde el informe de Li et al., La mayoría de los estudios han informado de la fabricación de nanoestructuras de silicio; Pocas investigaciones se han centrado en la nanofabricación de semiconductores compuestos III-V [13, 14], y la formación de estructuras ordenadas a escala nanométrica en sustratos de GaAs es particularmente poco conocida. Para ampliar la gama de aplicaciones del grabado químico asistido por metales, es deseable desarrollar un método de nanofabricación para semiconductores compuestos III-V que no dependa de las dimensiones de los patrones resultantes.
En un estudio anterior, fabricamos matrices de microbombas de InP [15] y patrones de línea y matrices de pilares de GaAs [16] utilizando grabado químico asistido por metal. Sin embargo, las dimensiones de los patrones resultantes (por ejemplo, la periodicidad y los anchos de los patrones de línea) oscilaron entre varios micrómetros y varias decenas de micrómetros. Hasta donde sabemos, ningún estudio ha informado la formación de nanoestructuras de GaAs ordenadas con una escala submicrónica o una periodicidad menor utilizando grabado químico asistido por metales por las siguientes razones:(1) es difícil controlar la forma y el tamaño de los metales nobles utilizado como catalizador a escala nanométrica y (2) el fenómeno de grabado de GaAs es menos conocido en comparación con el caso del silicio. Por lo tanto, intentamos aclarar el mecanismo de grabado de GaAs en la escala nanométrica. En este estudio, demostramos que las matrices de nanopilares ordenadas con una periodicidad de 100 nm se pueden fabricar en sustratos de GaAs utilizando grabado químico asistido por metal con un catalizador de Au con patrón. También se investigan los efectos de la composición del grabador y el tiempo de grabado sobre la morfología del sustrato de GaAs grabado.
Métodos
El principio de fabricación de matrices de nanopilares de GaAs mediante grabado químico asistido por metal se muestra esquemáticamente en la Fig. 1. Se preparó una máscara de alúmina porosa de orificio pasante con una matriz ordenada de aberturas mediante anodización en dos pasos seguida de anodización en dos capas [ 17]. La primera anodización se realizó sobre aluminio pulido electroquímicamente (99,99% de pureza) a un voltaje constante de 40 V en 0,3 mol dm −3 ácido oxálico a 30 ° C durante 3 h. El voltaje de anodización de 40 V está bien establecido como una condición de autoorden que produce una disposición de poros altamente ordenada en alúmina anódica [18].
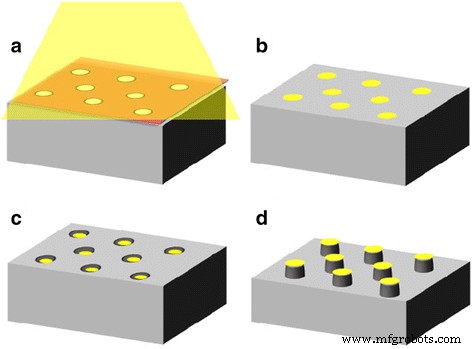
Modelo esquemático de la fabricación de matrices de nanopilares de GaAs. un Deposición al vacío de Au sobre un sustrato de GaAs a través de una máscara de alúmina porosa. b Retirada de la mascarilla. c , d Grabado químico de GaAs utilizando matrices de nanopuntos de Au como catalizador
Después de la primera anodización, se eliminó la primera capa de alúmina anodizada en una solución mixta de ácido fosfórico y ácido crómico a 80 ° C. Posteriormente, se llevó a cabo la segunda anodización durante 1,5 min en las mismas condiciones que la primera anodización. Basado en el principio de anodización de dos capas, la muestra se anodizó nuevamente a un voltaje constante de 40 V en 12 mol dm −3 ácido sulfúrico a 5 ° C durante 8 min para preparar una capa de alúmina de sacrificio. La máscara de alúmina porosa de orificio pasante se formó disolviendo la capa de alúmina de sacrificio en ácido fosfórico al 2% en peso a 30ºC durante 20 min. Se realizó un grabado químico adicional en ácido fosfórico al 5% en peso a 30 ° C durante 15 min para aumentar el diámetro de los poros de la máscara de alúmina.
Después de enjuagar la máscara de alúmina en agua destilada, la máscara de alúmina obtenida se colocó sobre un sustrato de GaAs de tipo n [dopado con Si, 2,35–2,67 × 10 −3 Ω cm, (100) orientación del cristal]. Posteriormente, se evaporó una capa de Au de 30 nm de espesor a través de la máscara de alúmina utilizando un sistema de deposición al vacío mediante la fórmula de calentamiento por resistencia (ULVAC KIKO Inc., VPC-410) con una presión por debajo de 1 x 10 -3 Pa (figura 1a). El grosor de la capa de Au se midió utilizando una microbalanza de cristal de cuarzo y la tasa de deposición de Au fue de 0,02 nm s −1 . Después de la deposición del metal, la máscara de alúmina se retiró en ácido fosfórico al 5% en peso a 25 ° C durante 30 min (Fig. 1b).
El sustrato de GaAs recubierto de Au se grabó químicamente en HF que contenía KMnO 4 (Figura 1c). KMnO 4 actúa como un agente oxidante en una solución ácida [19,20,21,22]. Las morfologías de la máscara de alúmina, la capa de Au depositada y el sustrato de GaAs grabado se evaluaron mediante microscopía electrónica de barrido de emisión de campo (FE-SEM; JEOL JSM-6701F). La composición química del sustrato de GaAs grabado se evaluó mediante espectroscopía electrónica de barrena (AES; JEOL JAMP-9500F). Los espectros de electrones de barrena se adquieren fácilmente a partir de puntos o áreas seleccionados de la superficie. Aquí, la imagen de mapeo elemental AES se adquirió con un voltaje de aceleración y una corriente de emisión de 30 kV y 15 nA, respectivamente.
Resultados y discusión
En el grabado químico asistido por metal, es esencial controlar con precisión las dimensiones del catalizador metálico para obtener el diseño deseado en la superficie del sustrato. Debido a que la morfología de la estructura resultante depende del patrón geométrico inicial y las dimensiones del catalizador metálico, se requiere un catalizador metálico modelado para fabricar nanoestructuras ordenadas en superficies semiconductoras. En este estudio, se utilizó una máscara de alúmina con una serie ordenada de aberturas para controlar el tamaño y la disposición del catalizador metálico. Para un proceso de deposición de metal seco, el grosor de la máscara es crítico porque la deposición de metal a través de una máscara gruesa con aberturas estrechas es físicamente difícil. En el caso de la alúmina porosa, el grosor de la máscara se puede ajustar con alta reproducibilidad cambiando el tiempo de anodización. Aquí, se preparó una máscara de alúmina porosa de orificio pasante de aproximadamente 300 nm de espesor sobre un sustrato de GaAs. La máscara de alúmina se colocó con su superficie hacia arriba. Los diámetros superior e inferior de las aberturas en la máscara de alúmina fueron de aproximadamente 80 y 70 nm, respectivamente. El diámetro ligeramente mayor de la abertura superior en comparación con la abertura inferior se atribuyó al ataque químico durante la preparación de la máscara de alúmina.
La Figura 2 muestra una matriz típica de nanodottos de Au bien ordenada sobre un sustrato de GaAs. La matriz de nanodot corresponde a la configuración de la matriz de poros autoordenada en la máscara de alúmina anódica, como se muestra en la Fig. 2a. Aunque la capacidad de control de la deposición de Au debería mejorarse aún más, la deposición de metal a través de la máscara de alúmina que se muestra en este documento es adecuada para la producción a gran escala de patrones de puntos de metales nobles ordenados sobre sustratos semiconductores en términos de simplicidad y eficiencia del proceso de fabricación. Tenga en cuenta que cada nanodoto de Au tenía casi el mismo diámetro de aproximadamente 70 nm; este diámetro fue determinado por el tamaño de poro de la parte inferior de la máscara de alúmina, mientras que las alturas de los nanodots de Au fueron determinadas principalmente por el tiempo de deposición. En este estudio, la altura de cada nanodot de Au se ajustó a ~ 30 nm, como se muestra en la Fig. 2b.

un Superficie y b Imágenes SEM de sección transversal de una matriz de nanodottos de Au formada sobre un sustrato de GaAs a través de una máscara de alúmina porosa anódica
Después de la formación de matrices de Au dot sobre sustratos de GaAs, las muestras se sumergieron en una solución de HF y KMnO 4 para grabado químico asistido por metales. En el grabado químico convencional asistido por metal, el grabado procede localmente en la interfaz entre el catalizador y el sustrato subyacente, lo que resulta en la formación de poros o zanjas en la dirección perpendicular al sustrato, y el catalizador metálico se hunde en el semiconductor como se muestra en Figura 1c. Se considera que el uso de un grabador compuesto por una alta concentración de ácido y una baja concentración de oxidante promueve el consumo suave de los agujeros positivos generados (h + ) en la interfaz metal / semiconductor. En este estudio, se espera que la oxidación de GaAs en la interfaz Au / GaAs proceda directamente por el h + generado .
La Figura 3 muestra una imagen SEM típica de la superficie de GaAs grabada usando el catalizador de Au con patrón. El grabado químico se realizó en una solución que contenía 0,001 mol dm −3 KMnO 4 y 20 mol dm −3 HF a una temperatura relativamente alta de 45 ° C. En este estudio, la concentración de KMnO 4 fue bajo (0.001 mol dm −3 ) para suprimir el grabado lateral. Según informes anteriores de DeJarld et al. y Cheung et al., la tasa de grabado lateral aumentó con el aumento del agente oxidante (KMnO 4 ) concentración [19, 21].

Imagen SEM de la superficie superior del sustrato de GaAs después de un grabado químico asistido por Au en una solución que contiene 0,001 mol dm −3 KMnO 4 y 20 mol dm −3 HF durante 600 sa 45 ° C
Los catalizadores de Au, que se detectaron como puntos brillantes circulares, se observaron dentro de los poros en muchas áreas del sustrato de GaAs, como se muestra en la Fig. 3. El diámetro de los poros observados en la Fig. 3 coincidió con los tamaños de los nanodots de Au depositados que se muestran en la Fig. 2. Estos resultados indican que el ataque químico convencional asistido por metal, que se muestra esquemáticamente en la Fig. 1c, ocurrió solo en la interfaz Au / GaAs y procedió anisotrópicamente perpendicular al sustrato, es decir, en la dirección <100>.
En el grabado químico asistido por metales, la composición del grabador y la temperatura de grabado afectan la dinámica de la difusión del portador, la oxidación y la eliminación del producto [19]. Para abrir nuevas aplicaciones del sustrato de GaAs grabado, intentamos fabricar matrices de nanopilares de GaAs cambiando las condiciones del grabado químico asistido por metal. La Figura 4 muestra imágenes típicas de SEM en sección transversal de superficies de GaAs grabadas obtenidas usando el catalizador de Au modelado. Aumentando la concentración de KMnO 4 , la morfología de la estructura resultante podría cambiarse. En todos los casos se obtuvieron nanopilares de GaAs dispuestos hexagonalmente sobre toda el área de la muestra. Las puntas de los pilares se estrecharon ligeramente como resultado del grabado lateral. Las periodicidades de las matrices de nanopilares de GaAs fueron de aproximadamente 100 nm, correspondientes a las de las matrices de puntos de Au utilizadas como catalizador y los poros de la alúmina porosa utilizada como máscara inicial. Hasta donde sabemos, las dimensiones (por ejemplo, periodicidad) de las estructuras obtenidas en GaAs mediante grabado químico asistido por metal en este estudio son más pequeñas que las informadas para otras estructuras de GaAs [19,20,21,22].

Imágenes SEM de matrices de nanopilares de GaAs fabricadas mediante grabado químico asistido por Au en soluciones que contienen 0,01 mol dm −3 KMnO 4 y 5, 10 o 20 mol dm −3 HF durante 5 s en a 20 y b 45 ° C
Cuando el ataque químico se realizó a una temperatura relativamente baja de 20 ° C, se observó catalizador de Au en la punta de cada pilar, como indican las flechas. La Figura 4a muestra que la velocidad de ataque aumentó al aumentar la concentración de HF a la misma concentración de oxidante. A la alta concentración de HF de 20 mol dm −3 , la altura residual del pilar de GaAs fue la más alta.
Contrariamente a la expectativa de que la oxidación de GaAs en la interfaz Au / GaAs procede por el h + generado , no se observó disolución química en el área de contacto entre el catalizador de Au y el sustrato de GaAs subyacente en el caso de la Fig. 4. Se considera que el patrón de grabado depende de la temperatura del grabador. A baja temperatura (p. Ej., 20 ° C), la velocidad de h + Se cree que el consumo en la interfaz Au / GaAs es menor que la tasa de h + inyección; por tanto, h + difundido en el área que rodea los GaAs recubiertos de Au. Finalmente, se formó un nanopilar de GaAs bajo el área de contacto entre el catalizador de Au y el sustrato de GaAs subyacente debido a que se produjo un ataque selectivo del sitio en la superficie de GaAs expuesta. En otras palabras, los nanodots de Au también actuaron como una máscara protectora para evitar la disolución del sustrato de GaAs. Este fenómeno de grabado, como se muestra esquemáticamente en la Fig. 1d, se denomina grabado químico asistido por metal inverso [19, 22]. En 2010, también demostramos la formación de matrices de microbombas InP utilizando grabado químico asistido por metal inverso bajo irradiación UV [15]. A diferencia del grabado químico asistido por metal convencional, el grabado químico asistido por metal inverso se produce en las superficies de semiconductores compuestos III-V expuestas alrededor de las áreas recubiertas de metal mediante la difusión de h + del catalizador metálico y el posterior grabado químico selectivo del sitio. No se ha observado un comportamiento de grabado tan único en materiales de silicio.
Cuando el grabado químico asistido por metal se realiza a una temperatura alta de 45 ° C, el h + generado Se espera que se consuma tan pronto como alcance el límite entre Au, GaAs y grabador, lo que resultará en la promoción del grabado vertical. Incluso en este caso, sin embargo, se produjo un ataque químico asistido por metal inverso. Como se muestra en la Fig. 4b, la velocidad de grabado aumentó al aumentar la concentración de HF de la misma forma que el comportamiento de grabado de la Fig. 4a. Sin embargo, a una alta temperatura de grabado de 45 ° C y una alta concentración de HF de 20 mol dm −3 , los catalizadores de Au se separaron de las puntas de los pilares de GaAs porque el exceso de h + generado por la temperatura relativamente alta, incluso en el corto tiempo de ataque de 5 s, promovió el ataque lateral de GaAs en presencia del catalizador de Au. La capacidad de control de la forma de los pilares se mejorará mediante la optimización adicional de las condiciones de grabado (por ejemplo, composición, concentración y temperatura del grabador). Intenta aclarar los efectos de la concentración de agente oxidante sobre la generación de h + y la morfología de los GaAs grabados actualmente.
Para examinar el efecto del tiempo de grabado en la geometría de la estructura de GaAs grabada, el grabado químico se prolongó en 20 mol dm −3 HF y 0,01 mol dm −3 KMnO 4 a una temperatura relativamente baja de 20 ° C. Como se muestra en la imagen de sección transversal en la Fig. 5a, la profundidad de los nanopilares de GaAs alcanzó ~ 50 nm. Una de las características notables de las matrices de nanopilares de GaAs obtenidas en este estudio es que la punta de cada pilar estaba cubierta con Au, como se muestra en el recuadro de la Fig. 5a. La Figura 6 muestra el análisis elemental AES del mismo espécimen. Los mapas de AES para Ga y Au de los GaAs grabados indican la presencia de Au en la punta de cada pilar incluso después del grabado químico asistido por metal durante 10 s.

Imágenes SEM transversales de una matriz de nanopilares de GaAs fabricada mediante grabado químico asistido por Au a 20 ° C para a 10 y b 60 s en una solución que contiene 20 mol dm −3 HF y 0,01 mol dm −3 KMnO 4 . Recuadro muestra una imagen de la superficie de una matriz de nanopilares de GaAs con capa de Au

un Imagen del sustrato de GaAs después del grabado químico asistido por Au y los mapas AES correspondientes para b Ga y c Au. Las condiciones de grabado fueron las mismas que las de la Fig. 5a
Debido a que la altura del pilar se determinó principalmente por el tiempo de grabado, el grabado se prolongó aún más de 10 sa 1 min para formar matrices de pilares más altos en GaAs. Sin embargo, el tiempo de grabado prolongado de 1 min dio como resultado una disminución de la altura del pilar, como se muestra en la Fig. 5b. La disminución en la altura del pilar se atribuyó al ataque lateral en presencia de catalizador de Au y al desprendimiento posterior de los puntos de Au utilizados como catalizador.
Aunque el grabado químico asistido por metal, que controla con precisión la difusión de h + del catalizador metálico, aún no se ha logrado por completo, la nanofabricación de semiconductores compuestos III-V utilizando grabado químico asistido por metal ofrece una alternativa prometedora para el diseño de estructuras tridimensionales ordenadas sin el uso de procesos secos. Además, las matrices de nanopilares de GaAs con Au-capped obtenidas tienen aplicaciones tecnológicas y científicas potenciales en dispositivos optoelectrónicos como las células solares que emplean nanoestructuras plasmónicas para mejorar la captura de luz [23, 24].
Conclusiones
En resumen, hemos demostrado la fabricación de matrices de nanopilares de GaAs ordenadas en sustratos de GaAs (100) mediante grabado químico asistido por Au. Se formaron matrices de au nanodot con patrones de celosía hexagonal y periodicidades ordenadas de 100 nm mediante deposición al vacío a través de una máscara de alúmina porosa. Los nanodots de Au tenían diámetros de aproximadamente 70 nm, correspondientes al diámetro de la parte inferior de la máscara de alúmina, y sirvieron como catalizador y máscara protectora. A una temperatura relativamente baja, las matrices de nanopilares de GaAs cubiertas con Au podrían formarse mediante grabado selectivo en el sitio en la superficie de GaAs expuesta circundante. Estos hallazgos proporcionan la primera evidencia para el control más preciso de las nanoestructuras en sustratos de GaAs utilizando un enfoque factible basado en el grabado químico asistido por metales. La técnica de litografía no convencional para la nanofabricación de semiconductores compuestos III-V presentada en esta comunicación supera los inconvenientes de los métodos convencionales y tiene aplicaciones tecnológicas y científicas potenciales en varios campos de investigación.
Abreviaturas
- AES:
-
Espectroscopía de electrones Auger
- FE-SEM:
-
Microscopía electrónica de barrido por emisión de campo
Nanomateriales
- Propiedades químicas del titanio
- Matrices de C#
- Matrices C++
- Matrices C
- C Matrices multidimensionales
- Matrices de Java
- Desentrañar la evolución morfológica y la cinética de grabado de nanocables de silicio poroso durante el grabado químico asistido por metales
- Efectos del pH microambiental de los liposomas sobre la estabilidad química del fármaco cargado
- Biocompatibilidad mejorada en matrices anódicas TaO x nanotubos
- Matrices de nanotubos de TiO2:fabricadas con una plantilla blanda-dura y la dependencia del tamaño de grano del rendimiento de las emisiones de campo
- MATLAB - Matrices



