Nanopartículas cargadas de fármaco de donepezilo emulsionado 80 de polisorbato dirigido al cerebro para neuroprotección
Resumen
La mayoría de los medicamentos para la enfermedad de Alzheimer no funcionan de manera eficiente debido a la barrera hematoencefálica. Por lo tanto, diseñamos un nuevo nanopreparado (PS-DZP-CHP):nanopartícula de pululano modificado con colesterol (CHP) con cobertura de superficie de polisorbato 80 (PS), como portador de donepezilo (DZP) para realizar la entrega de tejido cerebral. Mediante análisis de tamaño y calorimetría de titulación isotérmica, elegimos la relación de dosificación óptima del fármaco con nanomateriales (1:5) y diseñamos una serie de experimentos para verificar la eficacia de las nanopartículas. Los resultados de los experimentos de liberación in vitro mostraron que las nanopartículas pueden lograr una liberación continua del fármaco en 72 h. Los resultados de la observación de fluorescencia en ratones mostraron un buen direccionamiento cerebral de nanopartículas de PS-DZP-CHP. Además, la nanopartícula puede mejorar la concentración del fármaco en el tejido cerebral en ratones. Se utilizaron nanopartículas de DZP-CHP para pretratar las células nerviosas con daño de la proteína Aβ. La concentración de lactato deshidrogenasa se determinó mediante tinción con MTT, rodamina 123 y AO-EB, que demostró que las nanopartículas de DZP-CHP tenían un efecto protector sobre la neurotoxicidad inducida por Aβ 25–35 y fueron superiores al donepezil libre. La prueba del medidor de movimiento perpetuo microtérmico mostró que las nanopartículas de PS-DZP-CHP tienen afinidad con la apolipoproteína E, que puede ser vital para que esta nanopartícula se dirija al tejido cerebral.
Introducción
La EA es una enfermedad del sistema nervioso central con complicados mecanismos patológicos que causa disfunción cognitiva progresiva, pero es muy difícil de tratar debido a la dificultad en la administración de fármacos y la baja concentración de fármaco que puede llegar al tejido cerebral [1, 2]. La aprobación de la BBB se ha convertido en una dificultad importante en la investigación del sistema de administración de fármacos (DDS) [3, 4]. La mayoría de los medicamentos abren la BBB a través de medios biológicos, químicos o físicos; entre ellos, los métodos físicos se utilizan ahora con mayor frecuencia clínicamente [5]. Debido a los defectos insuperables en la administración intracraneal de fármacos basados en tecnología invasiva, la producción de profármacos lipófilos o sustratos de transporte activo a través de la modificación química de la superficie del fármaco tiene más ventajas [6]. Entre ellas, las nanopartículas son una de las mejores opciones para lograr la administración intracraneal de fármacos al dirigirse activamente a la BHE [7,8,9].
Los nano-DDS se han convertido en el foco de la investigación dirigida al cerebro e incluyen nanopartículas de polímeros, nanopartículas orgánicas, liposomas, nanofibras y micelas que se han diseñado para proporcionar tratamientos y diagnósticos [6, 10, 11, 12]. Tanto las nanopartículas cargadas de fármaco como los fármacos lipofílicos de molécula pequeña pueden pasar a través de la BHE. La diferencia es que es más probable que las nanopartículas cargadas con fármacos pasen por difusión pasiva por adsorción en la pared capilar del cerebro. Además, los fármacos libres se enfrentan a una segunda barrera, la barrera sangre-líquido cefalorraquídeo (B-CSF) [13]. A diferencia de otras contrapartes de barrera, la mayoría de los fármacos son relativamente permeables a través del LCR y se difunden hacia el parénquima cerebral. Sin embargo, debido al proceso de difusión muy lento, la concentración de fármacos libres en el LCR es mucho más alta que en el parénquima cerebral, y la alta concentración en el LCR provocará cierta toxicidad [14, 15]. En este proceso, las nanopartículas tienen ventajas únicas y significativas. Si la superficie del nanoportador está recubierta con un tensioactivo hidrófilo, la ApoE se adsorberá en la superficie y el LCR puede promover el movimiento de nanopartículas hacia el parénquima cerebral a través del espacio alrededor de los vasos sanguíneos [16]. Nanopartículas recubiertas con el tensioactivo no iónico polisorbato 80 preparado por Kreuter et al. [17] fueron los primeros fármacos administrados con éxito al sistema cerebral y transportados a través de la adsorción de la proteína sérica ApoE en el plasma. Por lo tanto, la modificación del polisorbato 80 en la superficie de las nanopartículas para formar un compuesto específico del fármaco permite el reconocimiento del fármaco y del receptor de BHE endógeno, aumentando en gran medida la biodisponibilidad de los fármacos [18,19,20].
En la actualidad, el inhibidor de la acetilcolinesterasa (AChE) donepezil (DZP) se usa comúnmente para el tratamiento de la EA moderada, pero debido a su solubilidad en grasas, se disuelve deficientemente en vivo , y la baja biodisponibilidad oral, los comprimidos convencionales de donepezilo deben tomarse diariamente para mantener el efecto terapéutico [21, 22]. Debido a que la capacidad cognitiva de los pacientes con EA está gravemente afectada, lo que causa grandes inconvenientes en el mantenimiento de un programa de medicación, es urgente el desarrollo de una preparación de DZP de liberación sostenida de acción prolongada. La hipótesis de la cascada de amiloide sugiere que la causa de la EA es el depósito de placas amiloides alrededor del parénquima cerebral y las paredes cerebrovasculares. También se observa un gran número de manchas difusas en áreas del cerebro, que están compuestas por depósitos extracelulares de Aβ amorfos, altamente fibróticos e insolubles [23, 24]. Boridy y col. encontraron que las nanopartículas de polisacárido de pululano que no son tóxicas y fácilmente degradables pueden formar un complejo con la proteína Aβ y prevenir eficazmente la agregación de proteínas y pueden eliminarse rápidamente de las células para inhibir la toxicidad celular [25]. El pululano modificado hidrofóbicamente con colesterol (CHP) es una sustancia anfifílica que puede autoensamblarse en una nanoestructura con un núcleo hidrofóbico y una capa hidrofílica de cadena de azúcar en una solución acuosa [26, 27]. Al mismo tiempo, las nanopartículas de CHP pueden adsorber la proteína Aβ para evitar su deposición y agregación, desempeñando un papel sinérgico. Como nanoportador, CHP tiene una superioridad significativa.
Sobre la base del conocimiento anterior, el equipo de investigación diseñó una nanopreparación DZP-CHP en la etapa inicial y determinó la proporción de dosificación óptima del fármaco al nanoportador. Luego, se adsorbió polisorbato en la superficie de las nanopartículas para apuntar activamente al paso a través de la BBB para lograr el enriquecimiento del cerebro. En este estudio, se caracterizó una serie de nanosoluciones de DZP-CHP y se exploró y estudió el proceso de liberación del fármaco in vitro. Después de que las nanopartículas se prepararon con éxito, se utilizó Aβ25-35 para inducir el daño de las células nerviosas para establecer un modelo de células AD [28, 29]. Luego, se investigó el efecto protector de la nanosolución DZP-CHP en modelos de células PC12 y SH-SY5Y.
Materiales y métodos
Materiales
Se utilizaron los siguientes:pululano (hecho en casa) modificado hidrofóbicamente con colesterol [30]; donepezil (Shanghai Ziqi Biotechnology Co., Ltd.); polisorbato 80 (Tianjin Fuchen Reagent Institute); colorante verde de indocianina (ICG) (Tianjin Baiying Biological Technology Co., Ltd.); polisorbato 80 (Tween 80, PS) (Oficina de reactivos Tianjin Fuchen); ratones negros (Hunan Slake Jingda Laboratory Animal Co., Ltd.); Aβ25-35 (US Sigma); sal de tetrametil azol (MTT) (US Sigma); suero bovino recién nacido (U.S. Gibco); kit de lactato deshidrogenasa (LDH) (Nanjing Jiancheng Biological Co., Ltd.); Kit de fluorescencia de tinción doble AO / EB (Sino Pharmaceutical Group Chemical Reagent Co., Ltd.); y células PC12 (células de feocromocitoma suprarrenal de rata) obtenidas del Departamento de Neurología, Second Xiangya Hospital, Central South University. Las células SH-SY5Y (células de neuroblastoma de médula ósea humana) se adquirieron del ATCC Cell Bank (Manassas, VA, EE. UU.).
Preparación de nanopartículas
Tres tipos de nanopartículas con diferentes proporciones de DZP y CHP (p / p) (10:20, 4:20 y 2:20) se prepararon con éxito primero mediante diálisis de agua de acuerdo con los métodos descritos en la literatura [31]. Se añadió una cierta concentración de nanopartículas de DZP-CHP a un vaso de precipitados con un volumen constante de 10 ml y luego se succionó en otro vaso de precipitados que contenía emulsionante polisorbato 80 (PS) (concentración 0,7 mmol) para sedimentar durante 1 h. A continuación, la mezcla se colocó en un tubo EP y se sonicó durante 3 min (potencia de salida 100 W, modo de trabajo de pulso intermitente:ancho de pulso 2,0 s, tiempo intermitente 2,0 s). La operación se repitió tres veces hasta que se obtuvo una dispersión uniforme [32]. Las nanopartículas cargadas con fármaco de donepezilo emulsionado de polisorbato 80 (PS-DZP-CHP) finalmente se obtuvieron después de que se eliminaron las impurezas mediante filtración.
Caracterización de nanopartículas
Morfología de nanopartículas
La forma, morfología de la superficie y tamaño de las nanopartículas de DZP-CHP (DCP) con relaciones DZP a CHP de 1:2, 1:5 y 1:10 se analizaron con un microscopio electrónico de transmisión Tecnai F20. Se colocó una gota de nanopartículas de CHP, DZP-CHP y PS-DZP-CHP sobre una malla de cobre recubierta de carbono para formar una fina película líquida. Luego, se usó una solución de ácido fosfotúngstico al 2% (p / v) para obtener una tinción negativa de la muestra después del secado natural de la película. La solución acuosa de nanopartículas recién preparada se agregó gota a gota a una oblea de silicio limpia, se secó a temperatura ambiente y luego se colocó bajo un microscopio electrónico de barrido de emisión de campo JSM-6700F para observar la estructura de la superficie.
Tamaño de nanopartículas y potencial Zeta
El tamaño, el coeficiente de polidispersidad (PDI) y el potencial zeta de las nanopartículas de DZP-CHP y PS-DZP-CHP se analizaron utilizando dispersión dinámica de luz (DLS). El tamaño de partícula promedio y la distribución del tamaño de la suspensión homogénea obtenida se midieron tres veces cada uno.
Liberación de fármacos in vitro
La liberación de donepezil se midió mediante diálisis dinámica de agua. Se disolvió un miligramo de nanopartículas de DZP-CHP y PS-DZP-CHP en 5 ml de solución salina tamponada con fosfato (PBS, pH 7,4, concentración 0,01 M) y luego se transfirió a una bolsa de diálisis, que se mantuvo en la misma solución a temperatura constante de 37 ° C con agitación magnética. Se diluyeron cuatro mililitros de PBS a 0, 0,5, 1, 2, 4, 8, 12, 24, 48 y 72 h con el mismo volumen de PBS al mismo pH. Se utilizó espectrofotometría ultravioleta-visible para detectar la absorbancia del dializado a 312 nm en diferentes momentos; el contenido de la solución se determinó con una curva estándar y la prueba de liberación se repitió tres veces in vitro. El porcentaje de liberación de donepezil se calculó de acuerdo con la siguiente fórmula:
$$ Q \% ={{(C {\ text {n}} \ times V + V {\ text {n}} \ sum \ nolimits _ {{{\ text {t}} ={0}}} ^ { {\ text {n}}} {{\ text {Ci}}})} \ mathord {\ left / {\ vphantom {{(C {\ text {n}} \ times V + V {\ text {n} } \ sum \ nolimits _ {{{\ text {t}} ={0}}} ^ {{\ text {n}}} {{\ text {Ci}}})} {(WNP \ times LC \%} }} \ right. \ kern- \ nulldelimiterspace} {(WNP \ times LC \%}}) $$Cn es la concentración de la muestra en el momento Tn, μg / mL; V es el volumen total de solución de liberación de PBS, mL; Vn es el volumen de líquido liberado de PBS en el punto de tiempo Ti, mL; y Ci es la concentración de donepezil en el punto de tiempo Ti, μg / mL.
Calorimetría de titulación isotérmica (ITC)
Se goteó una cierta concentración de solución de PS sobre soluciones de nanopartículas de CHP y se midieron los cambios de calor con ITC (vip-itc, Microcal, Northampton, MA, EE. UU.). La solución de nanopartículas de CHP incluía tres tipos de nanopartículas con diferentes proporciones de DZP a CHP (1:2, 1:5 y 1:10). Todas las soluciones se desgasificaron antes de la titulación. La temperatura de todo el sistema se mantuvo constante a 25 ° C.
Experimentos con animales para observar la focalización en el cerebro
Preparación de nanopartículas de CHP de donepezilo marcadas con ICG
Se pesaron cuatrocientos miligramos de CHP-DZP y 20 mg de ICG usando una balanza analítica, y se añadió una cantidad apropiada de DMSO para mezclar y disolver completamente. Luego, la solución obtenida anteriormente se añadió gota a gota a la bolsa de diálisis con una pipeta, y el agua destilada se reemplazó una vez cada hora. Tres horas más tarde, el agua destilada se reemplazó cada 2 h, y se agregaron 400 a 800 ml de agua destilada cada vez durante 48 h hasta que el DMSO se dializó por completo. Posteriormente, la solución anterior se transfirió con una pipeta a un matraz aforado para obtener un volumen constante y luego se trató con una onda de ultrasonido durante 2 min. La filtración a través de una membrana de filtro de 0,45 μm dio como resultado nanopartículas DZP-CHP etiquetadas con ICG (ICG-DZP-CHP), que se empacaron por separado y se almacenaron en un refrigerador a 4 ° C para su uso futuro.
Preparación de nanopartículas de CHP de donepezilo fluorescente emulsionado
Se colocó una cantidad apropiada de ICG-DZP-CHP en un vaso de precipitados de 10 ml y se añadió 1 l (v / v) de emulsionante polisorbato 80 (PS). El vaso de precipitados se mantuvo durante 1 hora y luego se transfirió a un tubo EP para ultrasonidos durante 2 minutos a 100 W. La operación anterior se repitió tres veces hasta que se obtuvo una nanosolución uniforme. Finalmente, se obtuvieron nanopartículas cargadas con fármaco de donepezilo emulsionado y etiquetado con ICG (PS-ICG-DZP-CHP).
Experimentos MST para verificar la unión del APOE a nanopartículas
Todos los experimentos de MST se realizaron en un sistema Monolith NT.115 (201810-BR-N024). Todas las soluciones se prepararon con agua desionizada y reactivos de grado analítico. Los tampones se prepararon y almacenaron a temperatura ambiente. Las muestras de proteínas se mantuvieron en hielo hasta su uso [33]. Se diluyeron nanopartículas de PS-ICG-CHP (55,6 µM) a 40 nM con agua desionizada y se cargó ICG para la fluorescencia. Se preparó una solución de APOE (30 µl, 55,6 µM) y se marcaron 16 tubos capilares del 1 al 16; Primero, se agregaron 20 µl de APOE al tubo 1, y se agregaron 10 µl a los tubos 2 a 16. Luego, se transfirieron 10 µl de solución del tubo 1 al tubo 2 y se mezclaron completamente. Después de eso, se retiraron 10 µl de solución del tubo 2 y se transfirieron al tubo 3. Esta operación se repitió hasta que finalmente se retiraron 10 µl de solución del tubo 16 para asegurar que la solución en cada tubo fuera del mismo volumen. Se agregaron diez microlitros de nanopartículas diluidas a cada tubo y se mezclaron completamente para comenzar la medición. Los datos de la prueba MST se analizaron con el software de análisis NT y el ajuste de KD se realizó de acuerdo con la ley de acción masiva siguiendo las instrucciones del software.
Tecnología de imágenes de fluorescencia in vivo para la observación dirigida al cerebro
Se eligió un lote de ratones negros sanos que pesaban aproximadamente entre 18 y 22 g cada uno y se dividieron al azar en 2 grupos:el grupo PS-ICG-DZP-CHP y el grupo ICG-DZP-CHP. A cada ratón se le inyectaron 200 µl de 200 µg / ml de los fármacos del grupo anterior a través de la vena de la cola, y 0,5 h más tarde, los ratones se anestesiaron con pentobarbital sódico al 1% (50 mg / kg). Después de eso, todos los ratones se colocaron en el área de fotografía del generador de imágenes en vivo con los parámetros de imagen establecidos en una longitud de onda de excitación de 765 nm-815 nm y una longitud de onda de absorción de 815 nm-845 nm para obtener una imagen de fluorescencia de todo el animal. . Después de la obtención de imágenes, se diseccionaron todos los ratones y se extrajeron el riñón, el corazón, el bazo, el pulmón, el hígado y el cerebro para obtener imágenes de fluorescencia. Los parámetros de imagen fueron consistentes con los descritos anteriormente.
Estudio sobre distribución tisular de nanopartículas
Agrupación y muestreo de ratones
Cuarenta y cinco ratones C57BL / 6 se dividieron aleatoriamente en 15 grupos:5 grupos fueron inyectados con donepezil libre (grupo libre), 5 con nanopartículas de donepezil (grupo nano) y otros 5 con nanopartículas de donepezil modificadas con PS (grupo PS) en 0,25 mg / kg a través de la cola de la vena. Luego, se extrajo sangre 1 h, 3 hy 6 h después de la inyección. Después de eso, se sacrificaron todos los animales y se recogieron y trituraron los tejidos del corazón, el cerebro, el hígado y los riñones. Luego, se pesaron con precisión 0,2 g del tejido anterior y se añadieron a aproximadamente 1 ml de solución de NaCl al 0,9% y se homogeneizaron con un homogeneizador (65 Hz, 150 s). Se extrajeron con precisión cien microlitros de homogeneizado de tejido en un tubo EP de 1,5 ml con 0,7 ml de metanol, se agitaron en vórtex para mezclar durante 30 s para la precipitación de proteínas y luego se centrifugaron a 12.000 r · min −1 durante 10 min. Finalmente, se transfirieron 100 μL de sobrenadante a una botella de inyección para su análisis.
Método de determinación
La HPLC se utilizó por primera vez para el examen, pero la sensibilidad no fue lo suficientemente alta. Por lo tanto, se realizaron experimentos de seguimiento LC-MS, que mostraron una fuerte especificidad y ninguna sustancia endógena que interfiriera con la determinación del fármaco. El protocolo LC-MS cumplió con las pautas para la determinación de muestras biológicas. Las condiciones cromatográficas fueron las siguientes:fase móvil A, agua (que contiene ácido fórmico al 0,1%); fase móvil B, metanol (que contiene ácido fórmico al 0,1%); elución isocrática:A30% -B70%; caudal, 0,3 ml · min −1 ; temperatura de la columna, 35 ° C; volumen de inyección, 10 μL. Las condiciones de colisión fueron las siguientes:temperatura de la fuente de ionización por electropulverización (ESI), 150ºC; caudal de gas de desolación, 550 L · h −1 ; temperatura del gas de desolación, 500 ° C. Las condiciones para la detección de iones positivos fueron las siguientes:voltaje capilar, 3 kV; voltaje de cono, 30 V; modo de escaneo, monitoreo de reacciones múltiples (MRM).
Experimentos celulares
Cultivo celular y pasaje
Se cultivaron células PC12 y SH-SY5Y en DMEM con alto contenido de azúcar complementado con suero bovino fetal (FBS) inactivado por calor al 10% (v / v) y penicilina y estreptomicina al 1% (v / v) y luego se mantuvieron en una incubadora que contenía 5 % CO 2 a 37 ° C. Las células se utilizaron en varios experimentos o se pasaron tan pronto como alcanzaron el 80% de confluencia. Antes de los experimentos, las células PC12 y SH-SY5Y se sembraron en placas prerrevestidas de colágeno tipo I a la densidad celular requerida de acuerdo con la escala experimental.
Criopreservación celular
Cuando se observó que crecían hasta la fase logarítmica bajo un microscopio, las células PC12 y SH-SY5Y se congelaron y se lavaron dos veces con PBS, se tripsinizaron para formar una suspensión celular y se colocaron en un tubo de centrífuga estéril para la recolección por centrifugación (1000 r × min - 1 , 3 min). Luego, se añadió la solución de crioconservación de células y las células se guardaron en un tubo con el nombre de la célula y la fecha marcada. Las células se colocaron en un refrigerador a 4 ° C durante 1 h, - 20 ° C durante 2 h, - 80 ° C (congeladas) durante la noche y finalmente se transfirieron a un tanque de nitrógeno líquido.
Método MTT para detectar la tasa de supervivencia celular
La viabilidad celular se midió usando un ensayo de reducción de MTT. Brevemente, las células PC12 y SH-SY5Y se sembraron en placas de 96 pocillos (prerrevestidas con colágeno tipo I) a una densidad de 1 × 10 4 células / ml para permitir que las células se adhieran a cada pocillo. Después de la incubación durante 24 h, las células se preincubaron con diferentes concentraciones de nanosolución de CHP de donepezilo o solución de donepezilo libre durante 2 h. Posteriormente, se añadió Aβ25-35 (concentración final 20 µM) a cada pocillo. La placa de 96 pocillos tratada se incubó a 37 ° C durante 24 h. Después de eso, se agregó MTT (50 μL, 5 mg / mL) y se incubó con las células tratadas a 37 ° C durante 4 h. Finalmente, el medio se retiró con cuidado y los cristales de formazán se disolvieron en 150 μL de DMSO. La absorbancia se obtuvo a 490 nm utilizando un lector de microplacas. La viabilidad celular se expresa como el porcentaje de células vivas en el grupo tratado y el porcentaje de células vivas en el grupo de control no tratado.
Determinación de la actividad de LDH en el sobrenadante celular
Se sembraron células PC12 y SH-SY5Y en placas de cultivo de 96 pocillos (prerrevestidas con colágeno tipo I) a densidades de 2 x 10 5 y 3 × 10 5 células / mL, respectivamente. Después de la incubación durante 24 h, las células se preincubaron con diferentes concentraciones de nanosolución de CHP de donepezilo o solución de donepezilo libre durante 2 h. Posteriormente, se añadió Aβ25-35 (concentración final 20 µM) a cada pocillo. La actividad de LDH se midió de acuerdo con las instrucciones proporcionadas por el kit. Brevemente, se recogieron las células cultivadas con medio y luego se centrifugaron a 3500 rpm. El sobrenadante (50 µl) se mezcló con un volumen igual de reactivo para iniciar la reacción de LDH. La absorbancia se obtuvo a 450 nm utilizando un lector de microplacas y se calculó la actividad de LDH.
Método de tinción AO / EB para observar la morfología de la apoptosis
Se utilizó colorante fluorescente AO / EB para evaluar las características de las células apoptóticas. Se sembraron células PC12 y SH-SY5Y en placas de cultivo negras de 12 pocillos (prerrevestidas con colágeno tipo I) a densidades de 3 x 10 5 y 4 × 10 5 células / pocillo, respectivamente. Después de la incubación durante 24 h, las células se preincubaron con diferentes concentraciones de nanosolución de CHP de donepezilo o solución de donepezilo libre durante 2 h. Posteriormente, se añadió Aβ25-35 (concentración final 20 µM) a cada pocillo. Después del tratamiento, las operaciones se realizaron según el kit. Se evitó la luz durante todo el experimento. Finalmente, se observó la morfología celular.
Método de tinción con rodamina 123 para la detección del potencial de membrana mitocondrial
La MMP se midió utilizando un tinte fluorescente rodamina 123 (Rh123), un tinte catiónico permeable a las células que se distribuye preferentemente en las mitocondrias debido a sus propiedades altamente negativas. Se sembraron células PC12 y SH-SY5Y en placas de cultivo negras de 24 pocillos (prerrevestidas con colágeno tipo I) a densidades de 2 × 10 5 y 3 × 10 5 células / pocillo, respectivamente. Después de la incubación durante 24 h, las células se preincubaron con diferentes concentraciones de nanosolución de CHP de donepezilo o solución de donepezilo libre durante 2 h. Posteriormente, se añadió Aβ25-35 (concentración final 20 µM) a cada pocillo. Después del tratamiento, las células se lavaron con PBS y se incubaron con 10 μg / mL de rodamina 123 durante 30 min en la oscuridad a 37 ° C. Después de la incubación, las células se lavaron 3 veces con PBS y se midió la intensidad de la fluorescencia a 488 nm y 510 nm utilizando un lector de placas de fluorescencia.
Procesamiento estadístico y análisis de datos
Todos los experimentos se repitieron tres veces y los resultados se expresan como la media ± desviación estándar. Se utilizó el software estadístico GraphPad Prism y ANOVA unidireccional, Student's t Se utilizaron pruebas y otros métodos para el análisis estadístico. P <0.05 indica que una diferencia es estadísticamente significativa.
Resultados
Características de las nanopartículas
La cogeneración se autoagrega para formar nanopartículas con núcleos hidrófobos, que se pueden cargar con DZP. Las nanopartículas de CHP cargadas con DZP (DCN) con relaciones de fármaco a nanomaterial de 1:2, 1:5 y 1:10 se denominaron DCN1, DCN2 y DCN3. Según los resultados de la microscopía electrónica de barrido, las nanopartículas de CHP mostraron una estructura esférica y, después de la carga de DZP, las DCN también fueron esféricas, como se muestra en la Fig. 1. El tamaño medio y el potencial zeta de las nanopartículas de CHP fueron de 257 ± 3,05 nm y -2,81 ± 0,27 mV, respectivamente. Después de la carga de DZP, los tamaños medios fueron 273 ± 3,72, 260,7 ± 1,76 y 266,8 ± 4,56 nm, y los potenciales zeta fueron -6,20 ± 0,40, - 5,75 ± 0,64 y -9,30 ± 0,39 mV para DCN1, DCN2 y DCN3, respectivamente , como se muestra en la Tabla 1. Los porcentajes de atrapamiento de fármaco fueron 42,00 ± 5,65%, 86,54 ± 1,31% y 59,71 ± 4,43%, y los porcentajes de carga de fármaco fueron 12,02 ± 1,90%, 13,42 ± 2,03% y 7,40 ± 1,72%, respectivamente.
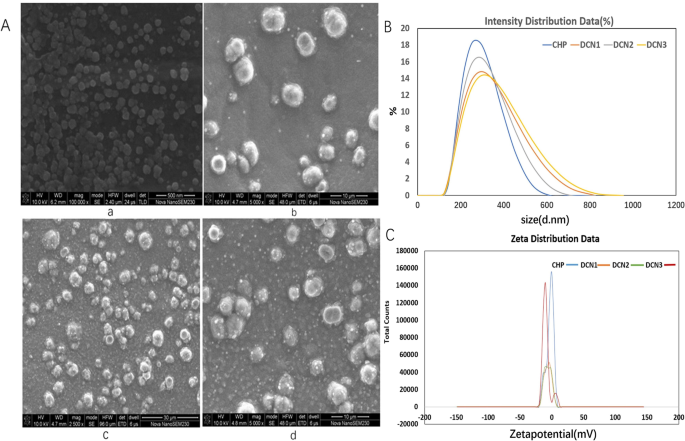
Imágenes de microscopía electrónica de barrido ( a , a-CHP, b-DCN1, c-DCN2, d-DCN3), distribución de tamaño ( b a-CHP, b-DCN1, c-DCN2, d-DCN3) y potencial zeta ( c a-CHP, b-DCN1, c-DCN2, d-DCN3) de nanopartículas
Medición de ITC
Para las DCN, durante todo el proceso de reacción, la reacción mostró principalmente un pico ascendente (Fig. 2) y la reacción fue endotérmica porque el pico ascendente indica una reacción de liberación de calor. Por lo tanto, el PS se puede adsorber espontáneamente en la superficie de DCN. La afinidad de PS fue (14,7 ± 2,76) × 10 4 M −1 , (29,8 ± 1,66) × 10 4 M −1 y (36,7 ± 3,84) × 10 4 M −1 , y el grado de cobertura de PS fue de 2,65 ± 0,193, 2,70 ± 0,372 y 1,49 ± 0,434 para DCN1, DCN2 y DCN3, respectivamente. Este resultado indica que el PS se adsorbió a la superficie de DCN con una alta afinidad y tenía una mayor cantidad de cobertura en DCN2. ∆H > 0 y ∆S > 0 indica que las tres partículas se unieron principalmente a través de interacciones hidrofóbicas con PS.
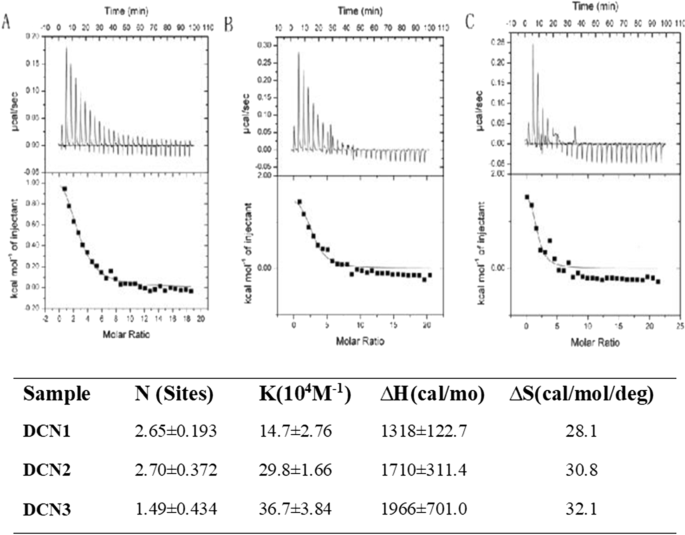
Datos de calorimetría isotérmica para titulación de PS (0,9 mM) en a DCN1, b DCN2 y c Soluciones de DCN3 (0,02 mM) a 25 ° C. Grado de cobertura, afinidad (KA) y cambios de entalpía y entropía para la unión de PS con nanopartículas (NP) después de la titulación en soluciones de NP
Caracterización de los tres tipos de nanopartículas
Las NP de CHP y las DCN preparadas por diálisis mostraron una forma esférica uniforme (Fig. 3a). Según el estudio anterior, elegimos las nanopartículas DZP-CHP con una proporción de fármaco a nanomateriales de 1:5 como sujetos del siguiente experimento. Las nanopartículas de DZP-CHP tenían un tamaño de partícula relativamente uniforme de 260,7 ± 1,76 nm y el índice de dispersión era de 0,196 ± 0,019. Aunque el tamaño de partícula permaneció relativamente estable después de la carga del fármaco, aumentó bruscamente a 335,2 ± 5,46 nm después de la adsorción de PS. El potencial zeta de las nanopartículas de DZP-CHP fue - 0,66 ± 0,04 mV, y después de recubrir con polisorbato 80, el potencial zeta cayó a - 2,22 ± 0,86 mV (Fig. 3b).
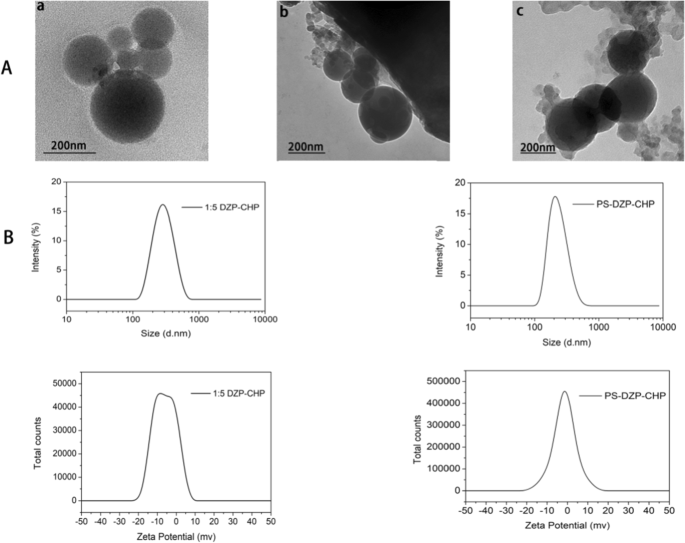
Caracterización de diferentes nanopartículas. un a Fotografía de microscopía electrónica de transmisión de NP de CHP, b Fotografía de microscopía electrónica de transmisión de NP DZP-CHP, c Fotografía de microscopía electrónica de transmisión de NP de PS-DZP-CHP. B:Diagrama de tamaño de partículas y diagrama de potencial zeta de NP de CHP-DZP (proporción de alimentación 1:5) y NP de DZP-CHP modificadas con polisorbato 80 (proporción de alimentación 1:5)
Liberación de nanopartículas de fármacos in vitro
Los resultados mostraron que, en comparación con el donepezil libre, las NP de DZP-CHP y las NP de PS-DZP-CHP liberaron DZP durante 72 h con efectos obvios de liberación controlada. La velocidad de liberación rápida temprana de las nanopartículas cargadas de fármaco puede deberse a la rápida disolución y liberación de las moléculas de fármaco, y luego, la ralentización puede deberse a la disminución de la concentración de fármaco, que solo puede verse afectada por la disolución y la difusión. Luego se estudió la liberación de fármaco in vitro de NP de DZP-CHP recubiertas y no recubiertas con polisorbato 80. La razón de la liberación más lenta de los NP de PS-DZP-CHP puede deberse a una fuerte adsorción de polisorbato 80 a pequeños fármacos moleculares hidrófobos (Fig. 4).
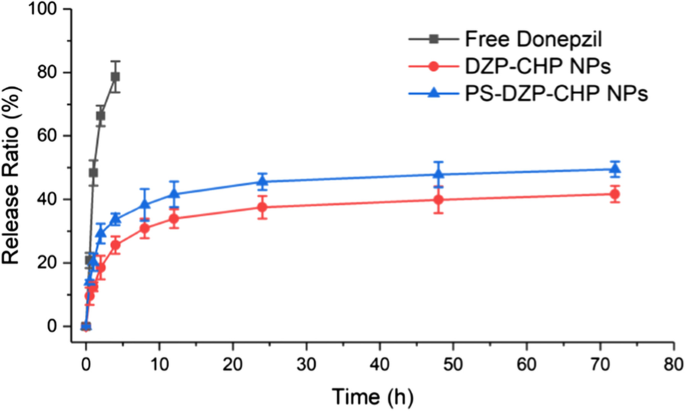
Curvas de liberación de fármacos in vitro para NP DZP, DZP-CHP (1:5) y NP PS-DZP-CHP
Efecto de focalización del cerebro de nanopartículas
Observación de la focalización del cerebro utilizando tecnología de imágenes de fluorescencia en vivo
Los cerebros de los ratones inyectados con ICG libre no mostraron fluorescencia, pero los cerebros inyectados con nanopartículas emulsionadas con PS presentaron una fluorescencia más fuerte en el cerebro que los inyectados con nanopartículas no emulsionadas porque ambas nanopartículas pudieron llegar al cerebro después de la inyección a través de la vena de la cola (Fig. . 5a). Para verificar esto, diseccionamos los ratones 30 minutos después de la inyección intravenosa de soluciones ICG-DZP-CHP y PS-ICG-DZP-CHP, extrajimos todos los órganos necesarios para el estudio y luego realizamos imágenes de fluorescencia. Las nanopartículas de PS-ICG-DZP-CHP presentaron una fuerte fluorescencia en el cerebro, pero no se observó ninguna en otros órganos (Fig. 5b). Las imágenes mostraron que las nanopartículas modificadas con PS presentaban la fluorescencia más fuerte en el tejido cerebral, mientras que las no modificadas mostraban una fluorescencia débil. No se observó fluorescencia en el tejido cerebral de ratones inyectados con ICG libre (Fig. 5c).
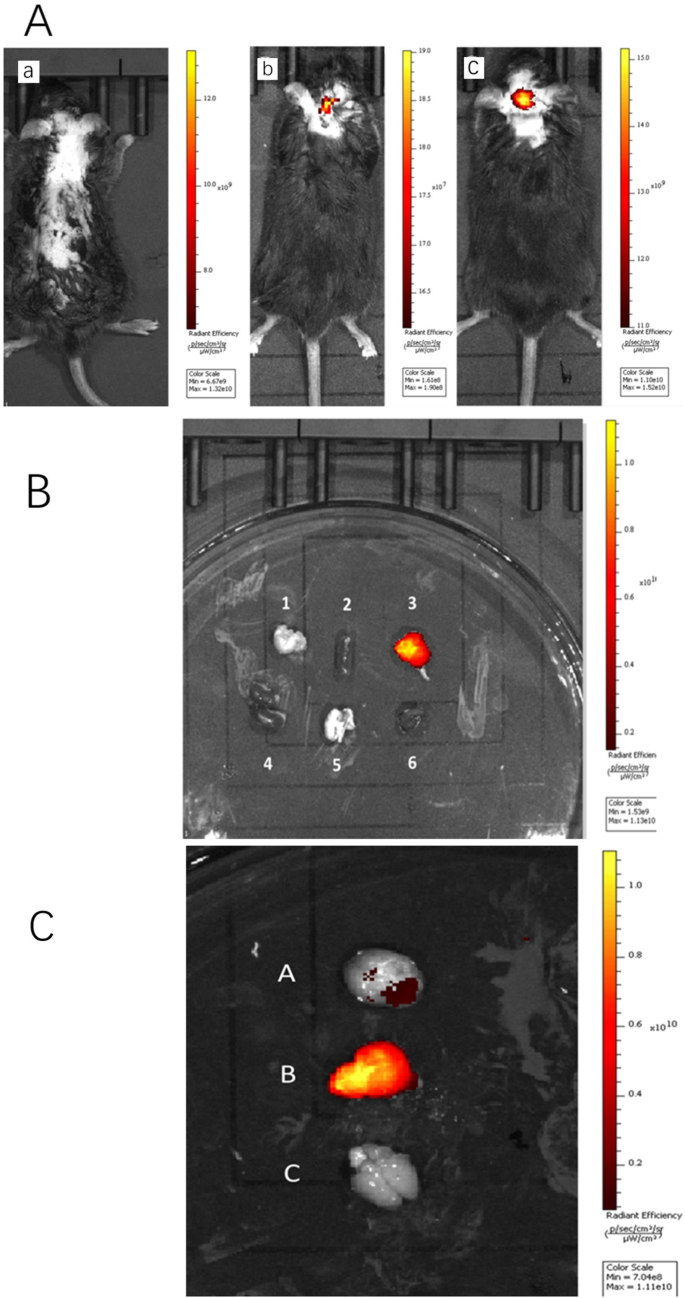
Imágenes de fluorescencia in vivo después de inyectar diferentes soluciones a través de la vena de la cola. un Imágenes de fluorescencia de animales enteros inyectados a través de la vena de la cola con 200 μg / ml de nanopartículas de DZP-CHP o PS-DZP-CHP cargadas con ICG como tinción. una solución de ICG libre (intensidad de fluorescencia × 10 9 ), b ICG-DZP-CHP nanoparticles (fluorescence intensity × 10 7 ), c ICG-DZP-CHP nanoparticles modified by PS (fluorescence intensity × 109). b Fluorescence images of various organs after injection of DZP-CHP nanoparticles modified by PS via the tail vein. c Fluorescence images of the brain after dissection. d Brain of mice injected with ICG-PS-DZP-CHP nanoparticles, e brain of mice injected with ICG-DZP-CHP nanoparticles modified with PS, f brain of mice injected with free ICG
Tissue Distribution of Nanoparticles in Mice
Donepezil was distributed in various tissues and mainly in the brain after injection of PS-DZP-CHP nanoparticles. Because it is metabolized through the kidney, the concentration of donepezil is very high in the kidney at certain times (Fig. 6a). In the brain, the concentration of free donepezil reached a peak in a very short time and then decreased rapidly. However, the concentration of donepezil nanoparticles reached a peak much more slowly and then decreased, especially nanoparticles modified with PS, which indicates a sustained-release effect with a delayed peak and prolonged retention time. Obviously, the nanoparticles improved the bioavailability of the drug (Fig. 6b).
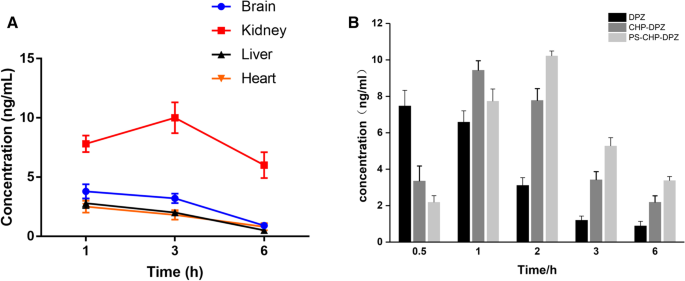
a The concentration of donepezil in the brain, heart, liver and kidney at different times. b The concentrations of free DZP, DZP-CHP nanosolution and DZP-CHP nanosolution modified with PS in brain tissue at different times
MST Results
MST results showed that the thermal surge changed regularly with increasing ligand concentration, and the KD value was 3.63 μM, indicating that the ligand effectively binds to the target protein, which verifies that PS can bind to Apo E and is relatively stable. After surface modification with PS, CHP nanoparticles can promote adsorption of Apo E, theoretically confirming that the nanoparticles we designed can specifically target brain tissue because the nanoparticles adsorbed Apo E, which may mediate passage through the blood–brain barrier (Fig. 7).
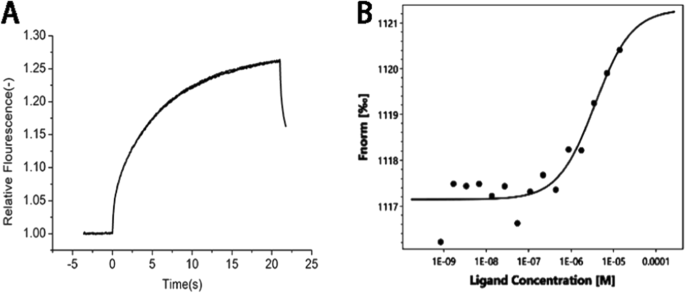
a Raw MST data. The fluorescently labeled molecules were observed for 5 s. At this time, the infrared laser was turned on, and a small part of the capillary tube was heated to 2–5 °C. The molecules migrated along a thermal gradient, resulting in changes in fluorescence intensity. When the infrared laser is turned off, the molecules diffuse along the concentration gradient. b The binding curve is generated by the difference between the initial fluorescence intensity and the intensity in the presence of heat, and the curve conforms to the standard 1:1 binding model
Establishment of a Nerve Injury Model Induced by Aβ25–35
MTT tests were used to detect the effect of different concentrations of Aβ25-35 on the activity of PC12 and SH-SY5Y cells [Fig. 8a (i), Fig. 8b (i)], and the results showed that with increasing Aβ25–35 concentration, PC12 and SH-SY5Y cell proliferation activity gradually decreased compared with that in the normal control group. When PC12 and SH-SY5Y cells were treated with 20 μM Aβ25–35 , PC12 cell activity decreased to 49.5 ± 3.3% that observed in the control group (P < 0.01), and SH-SY5Y cell activity decreased to 49.7 ± 0.8% (P < 0.01). An LDH kit was used to detect the effect of different concentrations of Aβ25–35 on LDH activity in both cell supernatants. Colorimetric tests showed that activity in both supernatants increased gradually with increasing Aβ25–35 concentration. After treatment of the cells with 20 μM Aβ25–35 , PC12 cell LDH release increased to 359.3 ± 18.3% that in the control group (P < 0.01), and SH-SY5Y cell LDH release increased to 360.0 ± 18.2% (P < 0.01). Rhodamine 123 staining was used to detect the effect of different concentrations of Aβ25– 35 on the mitochondrial membrane potential in both cell lines [Fig. 8a (ii), b (ii)]. The test showed that the mitochondrial membrane potential in both cell lines decreased gradually with increasing Aβ25– 35 concentration (5, 10, 20, 40 μmol/L). Treatment of the cells with 20 μM Aβ25–35 decreased the PC12 cell mitochondrial membrane potential to 51.3 ± 1.6% that in the control group (P < 0.01); for SH-SY5Y cells, the MMP decreased to 47.9 ± 1.7% that in the control group (P < 0.01).
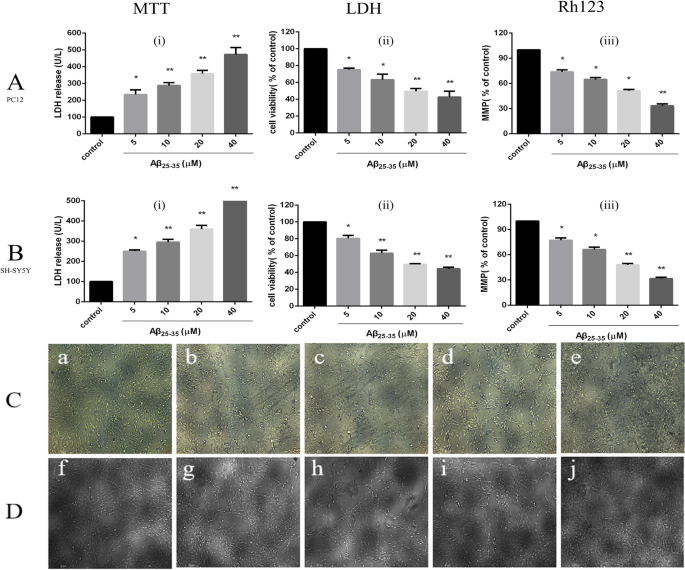
Effects of different concentrations of Aβ25–35 on injury to PC12 and SH-SY5Y cells. a , b The effect of different concentrations of Aβ25–35 on the cell survival rate, LDH activity and cell mitochondrial membrane potential in PC12 cells and SH-SY5Y cells (*P < 0.05, ** P < 0.01 vs control group). c The effect of different concentrations of Aβ25– 35 on damage to the morphology of PC12 cells:a control group, b Aβ25– 35 (5 μM) injury group, c Aβ25– 35 (10 μM) injury group, d Aβ25– 35 (20 μM) injury group, e Aβ25– 35 (40 μM) injury group. D:the effect of different concentrations of Aβ25– 35 on injury to the morphology of SH-SY5Y cells:f—control group, g Aβ25– 35 (5 μM) injury group, h—Aβ25– 35 (10 μM) injury group, i—Aβ25– 35 (20 μM) injury group, j—Aβ25– 35 (40 μM) injury group
Inverted fluorescence microscopy was used to observe morphological changes of PC12 and SH-SY5Y cells injured by different concentrations of Aβ25– 35 (Fig. 8c, d). The PC12 and SH-SY5Y cells in the control group had higher density, fusiform shapes, fuller cell bodies and longer protrusions. As the concentration of Aβ25– 35 increased (5, 10, 20, 40 μmol/L), the number of cells in both cell lines gradually decreased, the cell bodies shrank slightly, and the protrusions began to shrink sharply. When the concentration of Aβ25– 35 was increased to 40 μmol/L, the protrusions broke significantly, most of the cells contracted sharply, their shape became irregular, and some cells detached and became suspended in the solution.
Therefore, we treated PC12 and SH-SY5Y cells with 20 μM Aβ25-35 for 24 h to establish a nerve injury model.
Neuroprotective Effect of Drug-Loaded Nanoparticles (DZP-CHP)
MTT assays were used to detect the activity of different concentrations of DZP and DZP-CHP (2.5 μM, 5 μM, 10 μM) in PC12 and SH-SY5Y cells [Fig. 9a (i), b(i)]. Tests showed that treatment of PC12 cells with 20 μM Aβ25-35 alone resulted in a significant reduction in cell viability to 48.4 ± 2.8% that in the control group (P < 0.01). However, after pretreatment with DZP and DZP-CHP (2.5 μM, 5 μM, 10 μM) solutions, the viability of PC12 cells increased significantly. The viability of PC12 cells in the DZP-CHP group was higher than that in the DZP group (P < 0.05). Similarly, treatment of SH-SY5Y cells with 20 μM Aβ25– 35 alone resulted in a significant reduction in cell viability to 48.5 ± 4.0% that in the control group (P < 0.01), while after pretreatment with DZP and DZP-CHP solution (2.5 μM, 5 μM, 10 μM, respectively), the viability of SH-SY5Y cells increased significantly. The viability of SH-SY5Y cells in the DZP-CHP group was higher than that in the DZP group (P < 0.05).
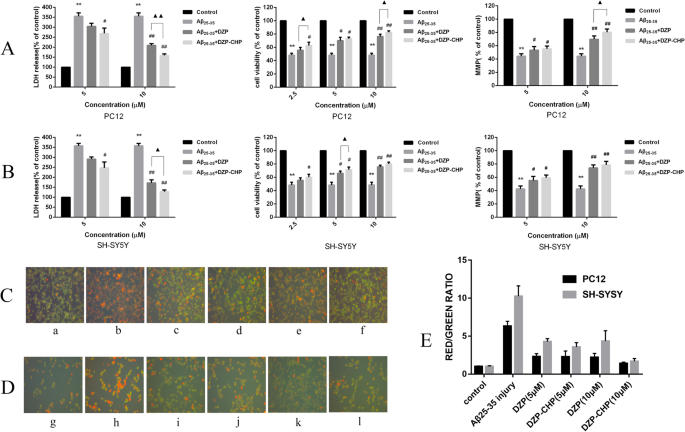
Effect of DZP-CHP on Aβ25-35-injured PC12 and SH-SY5Y cells. a and b The effects of DZP-CHP on the cell survival rate, LDH activity, and mitochondrial membrane potential of PC12 and SH-SY5Y cells injured by Aβ25-35 (#P < 0.05, ## P < 0.01 vs Aβ25-35 group; ▲ P < 0.05 vs DZP group). c The effect of DZP-CHP on the apoptosis morphology of PC12 cells injured by Aβ25-35; a—control group, b—Aβ25-35 injury group, c—DZP (5 µM), d—DZP -CHP (5 µM), e—DZP (10 µM), f—DZP-CHP (10 µM). D:the effect of DZP-CHP on the apoptosis morphology of SH-SY5Y cells injured by Aβ25-35; g—control group, h—Aβ25-35 injury group, i—DZP (5 µM), j—DZP-CHP (5 µM), k—DZP (10 µM), l—DZP-CHP (10 µM). E:red/green fluorescence ratio
LDH kits were used to detect the effects of different concentrations of DZP and DZP-CHP (5 μM and 10 μM) on the release of LDH from PC12 and SH-SY5Y cells into the culture medium [Fig. 9a (ii), b (ii)]. Colorimetric measurements showed that the release of LDH from PC12 cells that were exposed to 20 μM Aβ25-35 alone increased significantly by 355.1 ± 16.6% (P < 0.01). In the presence of DZP and DZP-CHP (5 μM and 10 μM), LDH release from PC12 cells dropped significantly. The effect in the DZP-CHP group was higher than that in the DZP group (P < 0.01). Similarly, the release of LDH from SH-SY5Y cells exposed to 20 μM Aβ25-35 increased significantly to 357.8 ± 12.5% (P < 0.01). However, after pretreatment with DZP and DZP-CHP (5 μM and 10 μM), LDH release from SH-SY5Y cells decreased significantly. The effect in the DZP-CHP group was higher than that in the DZP group (P < 0.05).
According to previous reports, depolarization of the MMP leads to loss of Rh123 from mitochondria, which in turn leads to a decline in intracellular fluorescence. Therefore, to characterize changes in the mitochondrial membrane potential in PC12 and SH-SY5Y cells treated with Aβ25-35, DZP, and DZP-CHP (5 μM, 10 μM), rhodamine 123 was used for detection [Fig. 9a (iii), b (iii)]. The results showed that the fluorescence intensity of rhodamine 123 decreased significantly to 44.3 ± 3.8% (P < 0.01) after incubation of PC12 cells with 20 μM Aβ25-35 for 24 h. However, pretreatment with DZP and DZP-CHP (5 μM, 10 μM) solutions resulted in a significant increase in fluorescence intensity in a dose-dependent manner, and the effect in the DZP-CHP group was higher than that in the DZP group (P < 0.05). Similarly, after treatment of SH-SY5Y cells with 20 μM Aβ25-35 for 24 h, the fluorescence intensity of rhodamine 123 significantly decreased to 42.5 ± 4.6% (P < 0.01). However, after pretreatment with DZP and DZP-CHP (5 μM, 10 μM), the fluorescence intensity increased significantly, and the effect in the DZP-CHP group was higher than that in the DZP group.
An AO-EB double staining kit was used to detect morphological changes of PC12 and SH-SY5Y cells treated with different concentrations of DZP and DZP-CHP (5 μM and 10 μM) (Fig. 9c, d). After AO-EB double staining, the nuclei of living cells presented green fluorescence under a fluorescence, and the fluorescence of apoptotic cells was orange-red; the higher the degree of apoptosis is, the brighter the fluorescence. Compared with the untreated control group, PC12 and SH-SY5Y cells treated with Aβ25-35 alone showed typical apoptotic characteristics, such as highly condensed and broken nuclei and obvious cell injury. However, pretreatment with DZP and DZP-CHP solution (5 μM and 10 μM) significantly inhibited cell damage and improved cell morphology.
Discussion
Although nanoparticles have been shown to be an effective delivery medium for nervous system diseases, the complexity of their structure and performance makes it challenging to detect and evaluate their physical–chemical properties and biological safety [34,35,36]. Therefore, after nanodrugs are designed, experiments to verify the safety and effectiveness of the nanomaterials at the cell and animal levels are extremely necessary. In the early laboratory stage, PS-DZP-CHP nanoparticles were successfully synthesized, and the optimal dosing ratio of the drug to CHP was set at 1:5. Due to the stable adsorption of PS to apolipoproteins ApoB and ApoE, brain targeting of nanoparticles can be achieved by permeation through the BBB [37]. The expected goal is that nanoparticles begin to decompose after reaching the brain; DZP is released and increases the concentration of cholinesterase; CHP reduces Aβ protein deposition and improves the brain environment; and administration frequency decreases because of the sustained release from nanoparticles [38,39,40,41].
Therefore, this study conducted an in vitro drug release test to assess the sustained release effect of nanoparticles. Compared with free DZP, nanoparticles achieved local sustained release in the brain, and PS can adsorb plasma proteins and reduce the loss of nanoparticles and prolong the release time to achieve a long cycle. After injection of ICG-labeled DZP-CHP and PS-DZP-CHP nanoparticles into rats, emulsified nanoparticles showed stronger fluorescence in the brain than those not emulsified with Tween 80. After organ biopsy, fluorescence imaging of various organs revealed that only the brain presented strong fluorescence, while other organs did not, indicating that nanoparticles did not release the drug until they reached the brain, which met the expected goal. In addition, nanoparticles modified with polysorbate 80 adsorbed ApoE to the surface and simulated low-density lipoprotein to bind to lipoprotein receptors on the surface of endothelial cells and enter the brain through LDLR induction [42, 43]. Moreover, the mechanisms by which nanoparticles regulate the tight junctions between endothelial cells and the inhibition of P-glycoprotein may produce a synergistic effect on their transcellular transport into the brain parenchyma [44]. However, since polysorbate 80 is prone to produce toxic substances, which cause untoward reactions, such as hypotension, dyspnea and shock, the dosage should be strictly controlled [45, 46]. Although a large number of nanodrugs have been developed for treatment of CNS diseases, most have shown poor effects [4]. In this study, we built a brain model of AD patients to evaluate the protective effect of nanoparticles on the brain. Because the toxicity of the Aβ protein to nerve cells varies with the concentration, it is better to screen an appropriate concentration to better simulate the brain environment of AD patients. The model was treated with DZP and DZP-CHP nanosolutions in advance to investigate the protective effect of DZP-CHP against PC12 and SH-SY5Y cell damage induced by Aβ25-35. The results showed that both solutions improved the cell proliferation activity caused by Aβ25-35, LDH release declined, and the mitochondrial potential rose. The inhibitory effect of the DZP-CHP nanosolution on cell damage induced by Aβ25-35 was significantly better than that of free DZP solution, and a concentration of 10 M DZP-CHP nanosolution proved to be the best, which may be due to the optimal drug concentration approach.
Basically, this study deduced the activity process of nanoparticles in vivo , verifying that PS-DZP-CHP nanoparticles have strong brain targeting, a good sustained release effect and a good AD therapeutic effect, thus demonstrating that they are clinically promising nanodrugs. The difficulty of treating the brain with medication has always been a major problem for researchers. The BBB leads to difficulty in curing CNS diseases, such as Parkinson's disease, brain tumors and brain stroke [47]. PS-DZP-CHP nanoparticles can effectively pass the BBB without destroying it, and DZP can be replaced as a model drug. Loading other drugs with high fat solubility and poor dissolution in vivo into the hydrophobic center of the NPs can not only increase brain targeting but also improve the water solubility of the drug. In addition, the design of CHP nanoparticle solutions is simple, and the drug dosage of the hydrophobic center can be flexibly controlled to ensure the best therapeutic effect while minimizing cytotoxicity [48, 49]. In future work, we will conduct in vivo research on DZP-CHP nanoparticles, such as evaluation of drug metabolism and side effects. These studies supplied a new strategy for brain drug delivery, and it is advantageous to clinical application of nanodrug with AD treatment.
Conclusion
DZP-CHP nanoparticles showed an optimal drug to nanomaterials dosing ratio of 1:5, which led to higher PS coverage and drug loading. DZP-CHP nanoparticles with PS adsorption exhibited slow release and significant brain targeting. Nanoparticle surface modification with PS can promote adsorption of Apo E and thus is vital for brain targeting. DZP-CHP nanoparticles had a protective effect on neurotoxicity and were superior to free donepezil.
Availability of Data and Materials
Not applicable.
Nanomateriales
- Los científicos de IBM son los primeros en hacer una demostración de los motores brownianos oscilantes para nanopartículas
- Nanopartículas de oro para sensores de quimioterapia
- Nanopartículas de oro multifuncionales para aplicaciones terapéuticas y diagnósticas mejoradas:una revisión
- Nanopartículas para la terapia del cáncer:avances y desafíos actuales
- Pez cebra:un sistema modelo en tiempo real prometedor para la administración de fármacos neuroespecíficos mediada por nanotecnología
- Nanopartículas cargadas de fármaco de donepezilo emulsionado 80 de polisorbato dirigido al cerebro para neuroprotección
- Nanofibras poliméricas electrohiladas decoradas con nanopartículas de metales nobles para detección química
- Membranas compuestas que contienen nanopartículas de intercambiadores de iones inorgánicos para la desalación electrodialítica de glicerol
- Nuevas nanopartículas de Au Nanostars @ PEG biocompatibles para la obtención de imágenes de TC in vivo y las propiedades de depuración renal
- Nanopartículas de sílice para la administración intracelular de proteínas:un nuevo enfoque de síntesis que utiliza proteína verde fluorescente
- Simulaciones por computadora para enfermedades neurodegenerativas



