El diagrama de fase de hierro-carbono
Diagrama de fase hierro-carbono
Los diagramas de fase son herramientas muy importantes en el estudio de aleaciones para la solución de muchos problemas prácticos en metalurgia. Estos diagramas definen las regiones de estabilidad de una fase que puede existir en un sistema de aleación en condiciones de presión atmosférica constante. Para un sistema binario, las coordenadas de estos diagramas son temperatura y composición. Las interrelaciones entre las fases, la temperatura y la composición en un sistema de aleación normalmente se presentan por diagrama de fase solo en condiciones de equilibrio. Tales condiciones ocurren durante velocidades lentas de calentamiento y enfriamiento de las aleaciones, cuando la cinética de las transformaciones no juega un papel importante.
En su forma más simple, el hierro y los aceros son aleaciones de hierro (Fe) y carbono (C). Hay tres tipos de aleaciones ferrosas. Estas aleaciones consisten en (i) hierro con un contenido de C inferior al 0,0008 % a temperatura ambiente, (ii) aceros con un contenido de C que oscila entre el 0,008 % y el 2,14 % (normalmente menos del 1 %) y con una microestructura formada por ferrita y cementita ), y (iii) hierro fundido con un contenido de C que oscila entre el 2,14 % y el 6,7 % (normalmente menos del 4,5 %). El estudio de la constitución y estructura del hierro y los aceros comienza con el diagrama de fase hierro-carbono (Fe-C) (Fig. 1). El diagrama de fase Fe-C también se utiliza como base para la comprensión de los procesos de tratamiento térmico.
Muchas de las características básicas del sistema Fe-C influyen en el comportamiento incluso de las aleaciones de hierro y acero más complejas. Por ejemplo, las fases que se encuentran en el sistema binario simple Fe-C persisten en aceros complejos, pero es necesario examinar los efectos que tienen los elementos de aleación en la formación y propiedades de estas fases. El diagrama Fe-C proporciona una base valiosa sobre la cual se puede construir el conocimiento de los aceros al carbono y aleados.
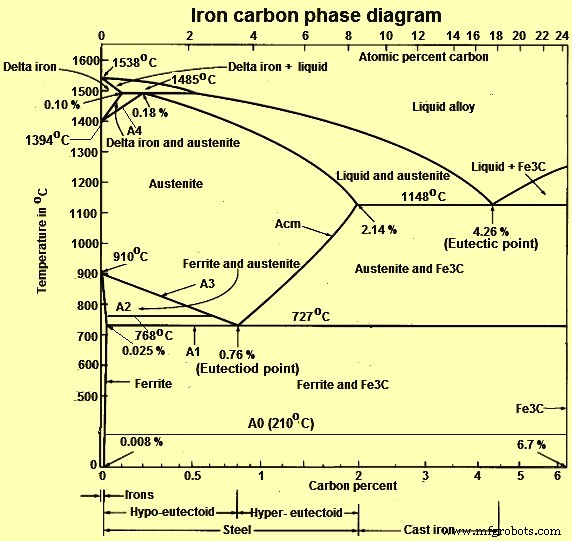
Fig. 1 Diagrama de fase de carbono de hierro
C es una impureza intersticial en Fe. Forma una solución sólida con las fases alfa, gamma y delta del hierro. La solubilidad máxima de C en el hierro alfa es de 0,025 % a 727 °C. El hierro cúbico centrado en el cuerpo (BCC) tiene posiciones intersticiales relativamente pequeñas. La solubilidad máxima de C en el hierro gamma cúbico centrado en la cara (FCC) es de 2,14 % a 1148 °C. El hierro FCC tiene posiciones intersticiales más grandes. Las propiedades mecánicas de las aleaciones de hierro-carbono (hierro y aceros) dependen de su microestructura, es decir, de cómo se mezclan las diferentes fases.
El diagrama de fase de hierro-carbono en la Fig. 2 en realidad muestra dos diagramas, a saber (i) el diagrama estable de hierro-grafito (líneas rojas), (ii) y el diagrama metaestable de Fe-Fe3C. La cementita es metaestable y el verdadero equilibrio debe estar entre el hierro y el grafito (C). Aunque el grafito se presenta ampliamente en los hierros fundidos, por lo general es difícil obtener esta fase de equilibrio en los aceros. La condición estable suele tardar mucho tiempo en desarrollarse, especialmente en el rango de baja temperatura y bajo contenido de carbono. Por lo tanto, el diagrama de equilibrio normal que generalmente se usa es el diagrama metaestable Fe-Fe3C porque es relevante para el comportamiento de la mayoría de los aceros en la práctica.
Los detalles de los diagramas de fase estable y metaestable del sistema Fe-C, especialmente en el lado rico en Fe, se conocen mucho mejor que cualquier otro sistema binario con una complejidad similar. Sin embargo, todavía hay áreas sustanciales donde el diagrama de fase no se ha establecido bien, como en los rangos de temperatura, composición y presión que no están directamente relacionados con la fabricación de hierro y acero.
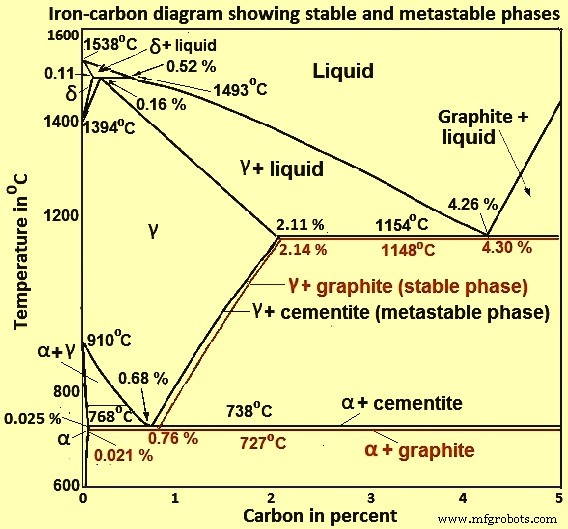
Fig. 2 Diagrama de hierro-carbono que muestra las fases estable y metaestable
Hay algunas fases metalúrgicas importantes y microcomponentes en el sistema de carbono de hierro. En el sistema Fe-Fe3C , el carbono es una impureza intersticial en Fe. Forma una solución sólida con las fases de hierro alfa (ferrita alfa), gamma (austenita) y delta (ferrita delta). Estas son fases importantes en el diagrama de fases Fe - Fe3C. Entre los campos monofásicos se encuentran regiones con mezclas de dos fases, como ferrita y cementita, austenita y cementita, y ferrita y austenita. A las temperaturas más altas, se puede encontrar el campo de fase líquida y por debajo de este se encuentran los campos de dos fases líquido y austenita, líquido y cementita, y líquido y ferrita. En el tratamiento térmico de aceros, siempre se evita la fase líquida. En el punto eutéctico (4,26 % C), la aleación líquida al enfriarse se convierte directamente en austenita y cementita sin ningún campo bifásico. De manera similar, en el punto eutectoide (0,76 % C), la fase austenita al enfriarse se convierte directamente en ferrita y cementita sin ningún campo bifásico. Algunos límites importantes en campos monofásicos han recibido nombres especiales que facilitan la comprensión del diagrama.
Las principales fases del hierro y los aceros en equilibrio son las siguientes fases.
- Ferrita o fase de hierro alfa:es una forma estable de hierro a temperatura ambiente. Es una fase de baja temperatura relativamente blanda y es una fase de equilibrio estable. Se transforma en austenita FCC (fase gamma) a 910 °C. La ferrita es un componente común en los aceros y tiene una estructura BCC, que está menos densamente empaquetada que la estructura FCC. Es suave y bastante dúctil. Es magnético por debajo de 768 grados C. Tiene baja resistencia y buena tenacidad.
- Austenita o fase de hierro gamma:la austenita es una fase de alta temperatura. Es una solución sólida de C en el hierro FCC. Por lo tanto, tiene una estructura FCC, que es una estructura compacta. Es una fase no magnética y dúctil. Se transforma en ferrita delta BCC a 1394 grados C. No es estable por debajo de la temperatura eutéctica (727 grados C) a menos que se enfríe rápidamente. La austenita tiene buena resistencia y tenacidad.
- Fase de ferrita delta:es una solución sólida de C en hierro BCC. Es estable solo a temperaturas superiores a 1394 ºC. Se funde a 1538 ºC. Tiene propiedades paramagnéticas.
- Cementita:es Fe3C o carburo de hierro. Es un compuesto intermetálico de Fe y C. Tiene una estructura ortorrómbica compleja y es una fase metaestable. Es una fase dura y quebradiza. Tiene baja resistencia a la tracción, buena resistencia a la compresión y baja tenacidad. Se descompone (muy lentamente, dentro de varios años) en ferrita alfa y C (grafito) en el rango de temperatura de 650 °C a 700 °C.
Al comparar la austenita con la ferrita, la solubilidad del carbono es mayor en la austenita con un valor máximo de 2,14 % a 1148 °C. Esta alta solubilidad del carbono en la austenita es extremadamente importante en el tratamiento térmico, cuando el tratamiento de disolución en la austenita seguido de un enfriamiento rápido a temperatura ambiente permite la formación de una solución sólida sobresaturada de carbono en hierro. La fase de ferrita está restringida con una solubilidad máxima de carbono de 0,025 % a 727 °C. Dado que el rango de carbono disponible en los aceros comunes es de 0,05 % a 1,5 %, la ferrita normalmente se asocia con cementita en una u otra forma. Del mismo modo, la fase delta es muy restringida y se encuentra en el rango de temperatura entre 1394 °C y 1538 °C/ Desaparece por completo cuando el contenido de carbono alcanza el 0,5 %.
La aleación de composición eutectoide (0,76 % C) cuando se enfría lentamente forma perlita, que es una estructura en capas de dos fases, a saber, alfaferrita y cementita. La perlita es la mezcla de fases de ferrita-cementita. Tiene un aspecto característico y puede tratarse como una entidad microestructural o un microconstituyente. Es un agregado de láminas alternas de ferrita y cementita que degenera (se esferoidiza o engrosa) en partículas de cementita dispersas con una matriz de ferrita después de un mantenimiento prolongado por debajo de 727 °C. Es un eutectoide y tiene una estructura BCC. Es una solución parcialmente soluble de Fe y C. Mecánicamente, la perlita tiene propiedades intermedias a ferrita blanda y dúctil y cementita dura y quebradiza. Tiene alta resistencia y baja tenacidad.
Las aleaciones hipo-eutectoides contienen ferrita pro-eutectoide (formada por encima de la temperatura eutectoide) junto con la perlita eutectoide que contiene ferrita eutectoide y cementita. Las aleaciones hipereutectoides contienen cementita pro-eutectoide (formada por encima de la temperatura eutectoide junto con perlita que contiene ferrita eutectoide y cementita).
En caso de solidificación fuera del equilibrio del sistema Fe-C, también se pueden formar algún tipo adicional de microestructuras. Algunas de estas microestructuras se dan a continuación.
- Bainita – Es una fase entre perlita y martensita. Es un microconstituyente metaestable duro y consiste en una mezcla no laminar de ferrita y cementita en una escala extremadamente fina. La bainita superior se forma a temperaturas más altas y tiene un aspecto plumoso. La bainita inferior se forma a temperaturas más bajas y tiene un aspecto acicular. La dureza de la bainita aumenta con la disminución de la temperatura de su formación. Tiene buena resistencia y tenacidad.
- Martensita:es una forma muy dura de estructura cristalina de acero. Lleva el nombre del metalúrgico alemán Adolf Martens. Se forma por enfriamiento rápido y es duro y quebradizo. Es una forma de hierro tetragonal centrada en el cuerpo (BCT) en la que se disuelve algo de carbono. Se forma durante el enfriamiento, cuando la red cúbica de austenita centrada en la cara se distorsiona en la estructura tetragonal centrada en el cuerpo sin la pérdida de los átomos de carbono que contiene en cementita y ferrita. Es una solución súper saturada de átomos de C en ferrita. Es una fase metaestable dura. Tiene morfología de listón cuando C es inferior al 0,6 %, morfología de placa cuando C es superior al 1 % y una mezcla de los intermedios. Tiene alta resistencia y dureza y baja tenacidad.
- Sorbita/troostita:las estructuras de la etapa inferior de perlita con escamas muy finas se denominan sorbita y troostita. Son las estructuras de transformación de la etapa de perlita las que corresponden a las tasas de enfriamiento crecientes. Sin embargo, cambia la relación de estructura y la formación de perlita con respecto a la distancia de las escamas. La estructura no se puede ver con un microscopio óptico.
- Ferrita Widmanstatten:se obtiene cuando el acero al carbono simple hipoeutectoide se enfría rápidamente a una temperatura superior a la temperatura A3. Debido al rápido enfriamiento, hay poco tiempo disponible para que los cristales de ferrita se nuclearen no solo en el límite de grano sino también dentro de los grandes granos de austenita. Crecen rápidamente en alguna dirección de cristal preferida dentro del grano y, por lo tanto, se vuelven más largos. La estructura tiene forma de agujas (listones) o placas que tienden a alinearse en la misma dirección dentro de un grano.
Hay muchas temperaturas y puntos críticos en el diagrama Hierro-C que son importantes tanto desde el punto de vista básico como práctico. Estas son las temperaturas cuando durante el enfriamiento, o el calentamiento, se producen en ellas las transformaciones tanto de fase como magnéticas. Las temperaturas a las que se producen las transformaciones en el estado sólido se denominan temperaturas críticas o puntos críticos. A continuación se indican las temperaturas principales y los puntos críticos.
- Temperatura A0:es la temperatura de Curie cuando se produce el cambio magnético a no magnético de la cementita al calentarse. La estructura puede desarrollar defectos tales como dislocaciones, fallas y vacantes. La cementita es metálica y ferromagnética con una temperatura de Curie de alrededor de 210 grados C. Cuando se alea, los solutos metálicos sustituyen a los sitios de hierro; átomos más pequeños como el boro reemplazan al carbono en los sitios intersticiales.
- Temperatura A1:es la temperatura (727 °C) cuando se produce la transformación eutectoide. A esta temperatura, la perlita cambia a austenita al calentarla y viceversa
- Temperatura A2:se denomina temperatura de Curie de la ferrita (768 °C), donde la ferrita ferromagnética al calentarse cambia a paramagnética. A esta temperatura no se produce ningún cambio en la microestructura
- Temperatura A3:es la temperatura a la que la ferrita comienza a formarse a partir de la austenita, al enfriarse el acero hipoeutectoide o los últimos rastros de ferrita libre se transforman en austenita, al calentarse. Por lo tanto, es la temperatura correspondiente al límite de fase gamma + alfa / gamma para el acero hipoeutectoide y es una función del contenido de carbono del acero, ya que disminuye de 910 °C al 0 % C a 727 °C al 0,76 % C. También se le llama temperatura crítica superior de los aceros hipoeutectoides. El intervalo de temperatura entre las temperaturas A1 y A3 se denomina rango crítico en el que la austenita existe en equilibrio con la ferrita.
- Temperatura Acm:es la temperatura, en un acero hipereutectoide, a la que la cementita proeutectoide comienza a formarse (al enfriarse) a partir de la austenita. Representa la temperatura del límite de fase gamma/gamma + Fe3C y es una función del carbono. La línea Acm ilustra que la solubilidad sólida del carbono en la austenita disminuye muy rápidamente desde un máximo de 2,14 % a 1148 °C hasta un máximo de 0,76 % a 727 °C, debido a la mayor estabilidad de la cementita a temperaturas más bajas. El carbono extra precipita de la austenita como cementita pro-eutectoide en aceros hipereutectoides (también llamada cementita secundaria en hierros fundidos). La separación de la cementita de la austenita (al enfriarse) también va acompañada de la evolución del calor.
- Temperatura A4:es la temperatura a la que la austenita se transforma en hierro delta. El valor más bajo para esta temperatura es 1394 grados C, que es en el caso de hierro puro. Esta temperatura aumenta a medida que aumenta el porcentaje de carbono.
- Temperatura Ms:es la temperatura a la que comienza la transformación de austenita en martensita durante el enfriamiento.
- Temperatura Mf – Es la temperatura a la cual termina la formación de martensita durante el enfriamiento. Todos los cambios, excepto la formación de martensita, ocurren a temperaturas más bajas durante el enfriamiento que durante el calentamiento y dependen de la tasa de cambio de temperatura.
Transformación austenita-ferrita – En condiciones de equilibrio, se forma ferrita proeutectoide en aleaciones de hierro-carbono que contienen hasta un 0,76 % de carbono. La reacción ocurre a 910 °C en hierro puro, pero tiene lugar entre 910 °C y 727 °C en aleaciones de hierro y carbono. Sin embargo, al enfriar el estado austenítico a temperaturas por debajo de la temperatura eutectoide, la ferrita se puede formar a temperaturas tan bajas como 600 °C. Hay cambios morfológicos pronunciados a medida que se reduce la temperatura de transformación, que normalmente se aplican en general a hipo-eutectoide. y fases hipereutectoide, aunque en cada caso hay variaciones debido a la cristalografía precisa de las fases involucradas. Por ejemplo, los mismos principios se aplican a la formación de cementita a partir de austenita, pero no es difícil distinguir morfológicamente la ferrita de la cementita.
Transformación austenita-cementita – Existen diferentes morfologías de cementita que se forman a temperaturas de transformación progresivamente más bajas. El desarrollo inicial de los alotriomorfos de límite de grano es muy similar al de la ferrita y el crecimiento de las placas laterales o de la cementita de Widmanstatten sigue el mismo patrón. El alotriomorfo tiene una forma que no refleja su simetría cristalina interna. Esto se debe a que tiende a nuclearse en las superficies de los granos de austenita, formando así capas que siguen los contornos de los límites de los granos. Las placas de cementita tienen una forma cristalográfica más rigurosa, a pesar de que la relación de orientación con la austenita es más compleja. Como en el caso de la ferrita, la mayoría de las placas laterales se originan a partir de alotriomorfos en los límites de grano, pero en la reacción de cementita se nuclean más placas laterales en los límites gemelos en la austenita.
Reacción austenita-perlita – La perlita es la microestructura más familiar en el diagrama de fase de carbono de hierro. Fue descubierto por Sorby hace más de un siglo, quien asumió correctamente que se trataba de una mezcla laminar de hierro y carburo de hierro. Es un componente muy común de una amplia variedad de aceros, donde proporciona una contribución sustancial a la resistencia. Las estructuras eutectoides lamelares de este tipo están muy extendidas en la metalurgia de los aceros. Estas estructuras tienen mucho en común con las reacciones de precipitación celular. Ambos tipos de reacción se producen por nucleación y crecimiento y, por lo tanto, están controladas por difusión. Los núcleos de perlita ocurren en los límites de grano de austenita, pero está claro que también pueden estar asociados tanto con ferrita pro-eutectoide como con cementita. En los aceros comerciales, los nódulos de perlita pueden nuclearse en las inclusiones.
Proceso de manufactura
- Hierro vs acero:¿Cuál es la diferencia?
- ¿Qué son los metales ferrosos? Obtenga los hechos
- Hierro
- Cómo 5G dirigirá la próxima fase de la Industria 4.0
- ¿Qué es el diagrama de fase hierro-carbono?
- Cómo elegir el grado correcto de hierro fundido dúctil
- Las grandes empresas de fundición de hierro
- ¿Por qué el hierro gris es el material de forja más popular?
- Las múltiples ventajas de la fundición gris
- ¿Cuáles son los beneficios de usar tuberías de hierro dúctil?
- 11 tipos diferentes de procesos de soldadura con la ayuda del diagrama



