Adsorción de productos descompuestos de SF6 en C3N modificado con ZnO:un estudio teórico
Resumen
SF 6 , como un excelente medio de aislamiento, es ampliamente utilizado en los dispositivos de aislamiento de alto voltaje, lo que garantiza el funcionamiento seguro del sistema eléctrico. Sin embargo, la inevitable descarga parcial en un dispositivo de larga duración provoca la descomposición de SF 6 y deteriora su rendimiento de aislamiento. En este trabajo, se realizaron cálculos de DFT para estudiar las propiedades de adsorción y detección de C 3 modificado con ZnO N (ZnO-C 3 N) nanohoja hacia SF 6 productos descompuestos, con el fin de proponer un nuevo nanocandidato para evaluar el estado de funcionamiento de SF 6 dispositivos de aislamiento. Primero investigamos la estructura de ZnO-C 3 N monocapa y luego simuló su comportamiento de adsorción en cuatro SF 6 típicos especies descompuestas, a saber, H 2 S, SO 2 , SOF 2 y SO 2 F 2 . Se encuentra que el ZnO-C 3 La monocapa N puede exhibir una reactividad y sensibilidad deseables en SO 2 , SOF 2 y SO 2 F 2 , lo que lleva a la intensa deformación de las moléculas de gas y grandes energías de adsorción. Estas consecuencias permiten la posible aplicación de un gas adsorbente basado en ZnO-C 3 N monocapa para eliminar los gases de impurezas de SF 6 equipo de aislamiento. Según el análisis, se supone que ZnO-C 3 N monocapa está calificado para ser utilizado para mantener la resistencia del aislamiento y garantizar el funcionamiento seguro del sistema de energía.
Introducción
Con el rápido desarrollo de la nanotecnología, la aplicación de sensores basados en nanomateriales novedosos está aumentando en los últimos años. En virtud de su rápida respuesta, bajo consumo, bajo costo y alta sensibilidad, el nano-sensor ha sido estudiado exclusivamente en el campo médico, militar, de detección de gases y monitoreo ambiental [1, 2, 3, 4]. El sensor de tipo de resistencia, como uno de los sensores más utilizados, es el preferido por los estudiosos debido a su estructura simple y mecanismo de trabajo. En la etapa inicial, el grafeno es un material atractivo en la detección de gases por su excelente rendimiento físico y químico, como una gran superficie específica, alta movilidad del portador y conductividad térmica favorable [5,6,7,8]. Sin embargo, el grafeno está limitado en la aplicación de reconocimiento de gases debido a su característica de banda prohibida cero [9, 10], con un rendimiento inferior en la identificación de gases comunes como CO, CO 2 , CH 4 , N 2 , NO 2 , NH 3 , H 2 y H 2 O [11]. Posteriormente, con el esfuerzo conjunto de los estudiosos, numerosos nanomateriales novedosos con las mismas propiedades que el grafeno pero sin bandgap cero han surgido en el campo de la detección de gases, incluidos, entre otros, los dicalcogenuros de metales de transición (TMD) [12,13,14 ], carburos y nitruros metálicos [15], semiconductores estratificados del grupo III-VI [16, 17] y nitruros del grupo III-V [18,19,20].
Entre los nuevos materiales similares al grafeno que surgieron, C 3 El N se sintetiza mediante la pirólisis directa de monocristales de trihidrocloruro de hexaaminobenceno o la polimerización de 2, 3-diaminofenazina [21, 22], que ha atraído una atención considerable como adsorbente de gas [23,24,25]. El C 3 N es intrínsecamente un semiconductor indirecto con un intervalo de banda de 0,39 eV que puede sintonizarse mediante la fabricación de puntos cuánticos con diferentes diámetros [22]. En micro apariencia, C 3 El N se puede considerar como una supercélula de grafeno 2 × 2 sustituida por dos átomos de nitrógeno, que posee una red en forma de panal plana con seis átomos de carbono y dos átomos de nitrógeno. Como resultado de los átomos de N añadidos, el C 3 intrínseco N muestra una actividad química más fuerte y una mayor movilidad del portador, pero mantiene una estabilidad estructural similar en comparación con el grafeno, lo que hace que el C 3 La monocapa N es un candidato competitivo para la detección de gases [26]. En términos de capacidad de adsorción, los investigadores han demostrado que el C 3 intrínseco N tiene una selectividad y sensibilidad excelentes [27] en la detección de NO 2 y SO 2 , mientras que para otros gases, no hay un efecto de adsorción obvio. Sin embargo, la investigación deja en claro que la reactividad superficial del C 3 El N podría promoverse en gran medida mediante la modificación de partículas de impurezas. Por ejemplo, Pashangpour y Peyghan [28] llevaron a cabo un experimento comparativo sobre la capacidad de adsorción de CO del C 3 intrínseco y dopado. N nanohoja; sus resultados ilustran que el dopante Al puede provocar una interacción de unión mucho más fuerte que el C 3 prístino N. Más tarde, Zargham Bagheri [29] estudió teóricamente el C 3 dopado con Si N para la adsorción de acetona, y se encuentra reemplazando un átomo de C con un átomo de Si, la energía de adsorción puede aumentar de - 9,7 a - 67,4 kcal / mol, y la sensibilidad aumenta a medida que se sustituyen más átomos de C.
El óxido de metal es una alternativa comúnmente utilizada en la modificación de superficies para mejorar la reactividad química de las interacciones de los gases. Como uno de los semiconductores de óxido metálico, el ZnO tiene una banda prohibida de aproximadamente 3,37 eV con una excitante energía de enlace de aproximadamente 60 meV, estabilidad química, excelentes propiedades fotocatalíticas y alta actividad para algunos gases específicos [30]. De acuerdo con Ref [31], ZnO puede crecer en morfologías de nanoestructura 0-dimensional (0D), unidimensional (1D) y bidimensional (2D), con ejemplos de cada clase que incluyen nanoclusters, nanocables / nanotubos y nanohojas / nanocintas, respectivamente. Dada la característica de tamaño y morfología fácilmente controlados [32, 33], la nanopartícula de ZnO es un material prometedor en su trabajo como dopante para mejorar el rendimiento de detección de nano-superficies [34,35,36]. Recientemente, algunos académicos han propuesto estudios teóricos sobre la mejora de la actividad superficial de los nanomateriales mediante el uso de un dopante de óxido metálico de una sola molécula. E. Mohammadi-Manesh y col. [37] investigó la capacidad de adsorción del grafeno decorado con Cu y CuO sobre H 2 S teóricamente y descubrió que la conductividad del grafeno modificado cambió significativamente en comparación con la del grafeno intrínseco después de la adsorción de H 2 S. Asadi y Vaezzadeh [38] diseñaron una hoja de grafeno decorada con B y CuO para detectar H 2 S y CO basados en la teoría funcional de la densidad (DFT). La simulación en estos trabajos fue realizada por DFT y sus códigos computacionales extienden la estructura atómica o molecular periódicamente en base a la supercélula definida y luego calculan las propiedades físicas de todo el sistema. Con base en este método, la adsorción de un átomo o molécula sobre el sustrato como sensor se utiliza para estudiar nanoestructuras. Los informes anteriores nos estimulan a realizar investigaciones relacionadas y adicionales sobre este tema sobre el dopaje de moléculas de óxido de metal único; aquí, dopamos C 3 N con molécula de ZnO en lugar de nanopartículas de ZnO como simplificación para explorar el efecto del ZnO en la detección de gases.
SF 6 es un medio ampliamente utilizado en aparamenta aislada en gas (GIS) con destacadas propiedades aislantes y extintoras de arcos [39]. Los inevitables defectos internos del accidente, como la descarga parcial (DP) en GIS, descompondrán SF 6 a algunos sulfuros con bajo contenido de fluoruro como SF 4 , SF 3 y SF 2 [40]. Estos subproductos reaccionarían aún más con las trazas de humedad y oxígeno, generando algunas sustancias químicas estables como H 2 S, SO 2 , SOF 2 y SO 2 F 2 [41]. La fiabilidad de aislamiento de estos subproductos es mucho menor que SF 6 y su existencia acelerará la evolución de la EP si se deja solo. Por tanto, para garantizar el funcionamiento seguro del GIS, es fundamental detectar o barrer estos gases. En este artículo, elegimos ZnO como dopante y construimos el modelo de C 3 modificado con ZnO N (ZnO-C 3 N) monocapa para estudiar su rendimiento de adsorción en SF 6 típico especies descompuestas (H 2 S, SO 2 , SOF 2 y SO 2 F 2 ) teóricamente. Al analizar los cambios estructurales, el comportamiento de transferencia de electrones, la estructura de la banda y la densidad de estado (DOS), el impacto del dopante ZnO en la interacción entre el C 3 Se estudiaron exhaustivamente las moléculas de N de superficie y de gas. El propósito de nuestro trabajo es brindar un mecanismo detallado de adsorción y detección de ZnO-C 3 N monocapa para una aplicación potencial para detectar o eliminar los gases de impureza en el SF 6 dispositivos de aislamiento.
Detalles computacionales
Todos los cálculos basados en DFT se realizaron en Dmol 3 paquete [42]. Con el fin de describir mejor la densidad de electrones no uniforme de un sistema realista, empleamos la aproximación de gradiente generalizada (GGA [43]) dentro de la función Perdew-Burke-Ernzerhof (PBE) y la corrección de dispersión de TS para tratar con el electrón. términos de correlación de cambio [44, 45]. Se indujeron los pseudopots de semi-núcleo DFT (DSSP) para el tratamiento del núcleo y se eligió la base numérica doble con polarización (DNP) como el conjunto de bases orbitales atómicas [46]. Paquete Monkhorst k -Se definieron puntos de mallas de 6 × 6 × 1 tanto en la optimización geométrica como en los cálculos de estructura electrónica [47]. La tolerancia de convergencia de energía, la fuerza máxima y el desplazamiento máximo en la optimización geométrica se establecieron respectivamente en 1.0 × 10 −5 Ha, 0,002 Ha / Å y 0,005 Å [48]. Además, la monocapa y su imagen vecina fueron separadas por un espacio de vacío de 15 Å para evitar la interacción entre ellas.
Como se ilustra en la Fig.1, la supercélula 2 × 2 × 1 de C 3 La monocapa de N y las moléculas de gas se establecieron y optimizaron antes del proceso de dopaje y adsorción. El enlace C-N (1.422 Å) en la monocapa optimizada es ligeramente más largo que el enlace C-C (1.418 Å) como consecuencia del radio más grande del átomo de N en comparación con el átomo de C. La constante de celosía obtenida en este trabajo es 4.92 Å, similar a los resultados reportados en la Ref. [25, 49]. Calculamos la transferencia de carga entre la molécula y la monocapa mediante análisis de Hirshfeld y definimos Q T para representar el cambio de carga en la molécula de gas. Un Q positivo T indica el comportamiento de liberación de electrones de la molécula de gas. Por el contrario, sugiere el comportamiento de recepción de electrones de la molécula de gas.
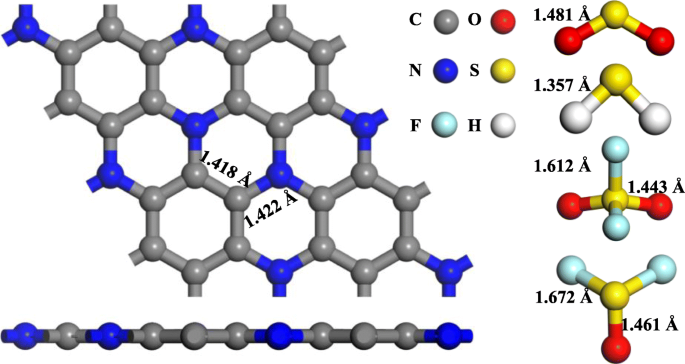
Estructura optimizada de C 3 N monocapa, H 2 S, SO 2 , SOF 2 y SO 2 F 2
Resultados y discusión
Análisis de C 3 modificado con ZnO N monocapa
Después de la optimización geométrica, el ZnO se colocó en la superficie de C 3 N monocapa en diferentes orientaciones y posiciones para explorar la configuración más razonable de ZnO-C 3 N. Según la Fig. 2a, la partícula de ZnO se acerca a C 3 N monocapa a través de la vertical (O 1 , O 2 ) y paralelo (O 3 ) orientaciones al plano en la posición del centro de la estructura hexagonal (P H1 , P H2 ), el punto medio de los enlaces C-C y C-N (P B1 , P B2 ) y justo encima del átomo de C (P C ) y átomo de N. Definimos la energía de formación ( E formulario ) para evaluar la estabilidad de ZnO-C 3 N monocapa, calculada de la siguiente manera:
$$ {E} _ {\ mathrm {formulario}} ={E} _ {\ mathrm {ZnO} \ hbox {-} {\ mathrm {C}} _ 3 \ mathrm {N}} - {E} _ {\ mathrm {ZnO}} - {E} _ {{\ mathrm {C}} _ 3 \ mathrm {N}} $$ (1)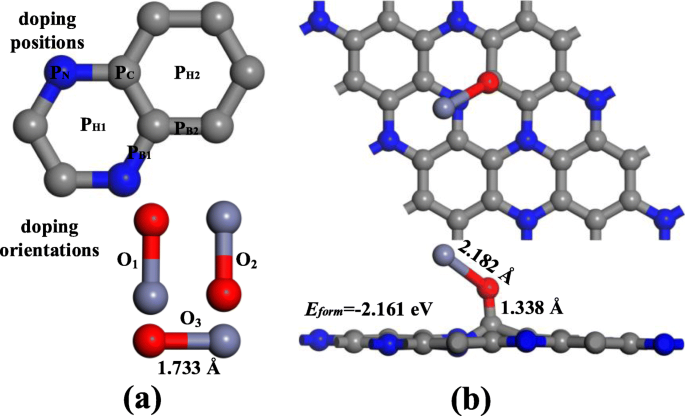
un Las posiciones y orientaciones de aproximación de la molécula de ZnO. b La configuración más estable de ZnO-C 3 N
donde E ZnO y \ ({E} _ {{\ mathrm {C}} _ 3 \ mathrm {N}} \) son la energía de la molécula de ZnO y C 3 N monocapa antes del dopaje, y \ ({E} _ {\ mathrm {ZnO} - {\ mathrm {C}} _ 3 \ mathrm {N}} \) es la energía de ZnO-C 3 Estructura N. Cuando el "enlace" de rango cercano entre átomos ocurre en la estructura atómica extendida, la energía total se reduce y resulta en una E negativa. formulario [50]; la estructura con la E más grande formulario se selecciona para adsorción y análisis adicional.
Todas las configuraciones de ZnO-C 3 N monocapa se muestran en la Figura S1, S2, S3. Estos resultados demuestran que la mayoría de las estructuras con grandes E formulario están en O 2 orientación y la partícula de ZnO prefiere acercarse al C 3 Superficie N por posición orientada a O y atrapada por un átomo de C. Además, cada proceso de modificación en este estudio es espontáneo ya que el E formulario es negativo y el máximo E formulario se obtiene colocando la partícula de ZnO en S C en O 2 orientación. Como se puede ver en la Fig. 2b, la molécula diatómica está unida a C 3 N con una inclinación de 40 °. El enlace Zn-O se alarga de 1.733 Å a 2.182 Å y el enlace C-O se mide como 1.338 Å. Bajo el efecto de ZnO, la superficie de C 3 N ya no es plano, pero se produce un cierto grado de distorsión y, mientras tanto, el átomo de C más cercano al átomo de O se extrae de la superficie. Para una discusión más detallada del comportamiento electrónico de ZnO-C 3 N monocapa, la densidad de carga de deformación (DCD) y la densidad de estado (DOS) se muestran en la Fig. 3. En la Fig. 3a, la región roja corresponde a un aumento en la densidad de carga y la disminución se representa en azul. Cuando la molécula de ZnO se adsorbe, extrae 0,255 e del C 3 Se puede reconocer una monocapa N y un área roja distinta alrededor del átomo de O. Mientras que el átomo de Zn está rodeado por un área azul, lo que significa la diferencia de electronegatividad entre el átomo de O y el átomo de Zn. Además, el aumento significativo de la densidad de carga entre el átomo de O y el átomo de C sugiere la formación de un enlace C-O que también puede ser apoyado por la intensa hibridación entre los estados del orbital O 2p y el del orbital C 2p, como se muestra en la Fig. 3c. De la curva de DOS en la Fig. 3b, es obvio que la introducción de ZnO conduce a un aumento en el DOS sistémico y la aparición de varios picos novedosos. Se puede identificar que los nuevos picos pequeños emergidos son aportados por el átomo de O en aproximadamente -2,5 eV y el más grande ubicado en -5,6 eV aparentemente resultó del orbital Zn 3d. Los cambios en DOS y la hibridación entre orbitales confirmaron el hecho de que la partícula de ZnO se ha adsorbido firmemente en la superficie de C 3 N y ejerció un gran impacto en la estructura electrónica de todo el sistema.
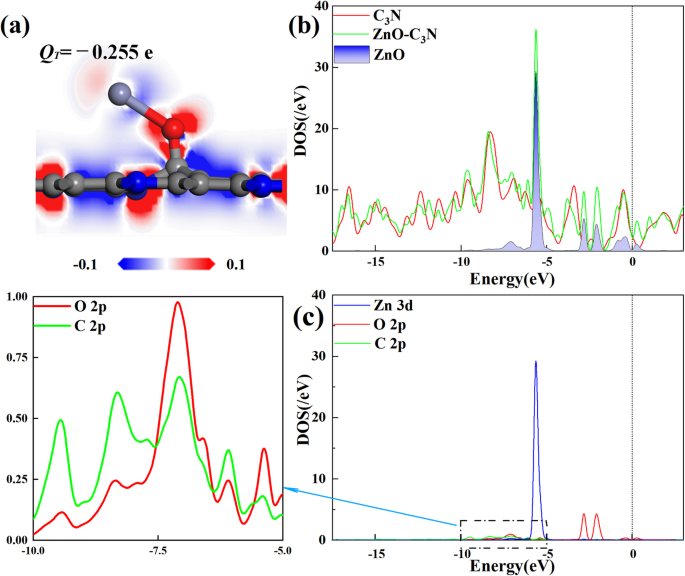
un DCD y b , c DOS y PDOS de ZnO-C 3 N monocapa
Comportamiento de adsorción de ZnO-C 3 N monocapa
Para comparar completamente los posibles parámetros de adsorción y seleccionar la configuración más deseable para el análisis, colocamos cada molécula de gas sobre la superficie de ZnO-C 3 N monocapa en varias orientaciones. Por ejemplo, para moléculas triatómicas, a saber, H 2 S y SO 2 , hicimos el plano compuesto por los tres átomos paralelo o vertical a la superficie con el átomo de S hacia arriba o hacia abajo. La energía de adsorción ( E anuncios ) se emplea para describir los cambios de energía de diferentes estructuras de adsorción y se calcula como
$$ {E} _ {\ mathrm {ads}} ={E} _ {\ mathrm {ZnO} \ hbox {-} {\ mathrm {C}} _ 3 \ mathrm {N} / \ mathrm {gas}} - {E} _ {\ mathrm {ZnO} \ hbox {-} {\ mathrm {C}} _ 3 \ mathrm {N}} - {E} _ {\ mathrm {gas}} $$ (2)donde E gas y \ ({E} _ {\ mathrm {ZnO} - {\ mathrm {C}} _ 3 \ mathrm {N}} \) son la energía de la molécula de gas aislada y el ZnO-C 3 N monocapa antes de la adsorción, \ ({E} _ {\ mathrm {ZnO} - {\ mathrm {C}} _ 3 \ mathrm {N} / \ mathrm {gas}} \) representa la energía del sistema con gas adsorbido. Después de obtener la energía total mínima local de cada situación, solo la estructura con el máximo E anuncios se eligió para una mayor discusión, como se muestra en la Fig. 4, y la diferencia de densidad de electrones (EDD) se muestra en la Fig. 5 para una mejor comprensión del mecanismo de transferencia de carga.
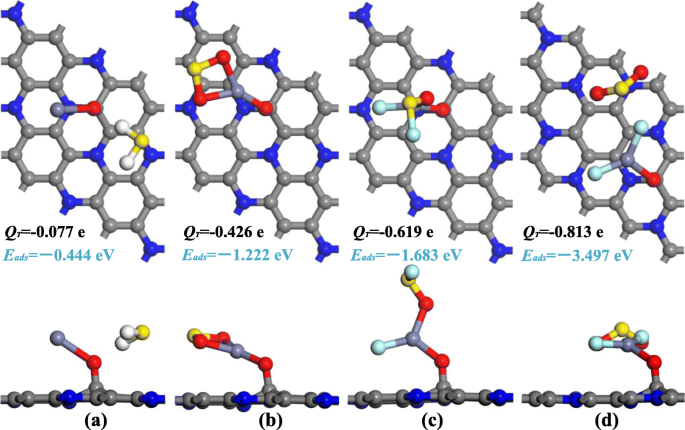
La configuración de adsorción de a H 2 Sistema S, b SO 2 sistema, c SOF 2 sistema y d SO 2 F 2 sistema
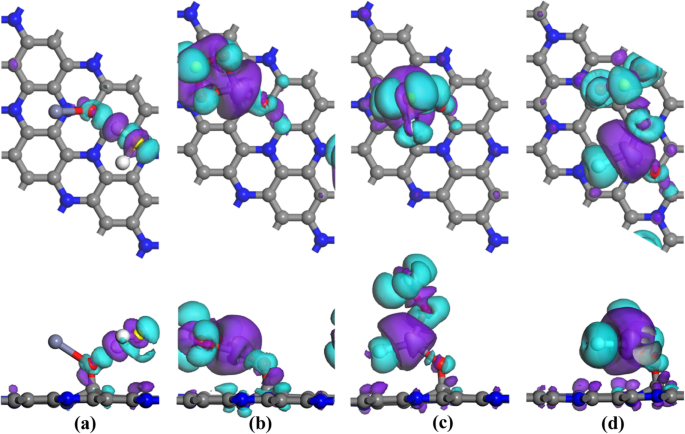
El EDD de a H 2 Sistema S, b SO 2 sistema, c SOF 2 sistema y d SO 2 F 2 sistema
El H 2 El sistema de adsorción de S se muestra en la Fig. 4a, donde H 2 La molécula S se adsorbe en posición paralela y la distancia atómica más cercana entre H 2 molécula (átomo de H) y dopante de ZnO (átomo de O) se mide como 2,042 Å. El enlace H-S del átomo de captura H se alarga a 1.374 Å en comparación con el 1.357 Å en su estado aislado, mientras que el otro H-S permanece sin cambios durante el proceso de adsorción. La ligera deformación de la configuración geométrica sugiere la interacción entre H 2 Molécula S y ZnO-C 3 La monocapa N es débil. Combinado con el E anuncios (- 0,444 eV) y Q T (- 0.077 e), está claro que H 2 La molécula S no puede adherirse de manera estable a ZnO-C 3 N monocapa; asumimos que ZnO-C 3 La monocapa N no es adecuada para detectar H 2 S. Para SO 2 molécula que se muestra en la Fig. 4b, ambos átomos de O están atrapados por un átomo de Zn con una distancia de 2.020 y 2.031 Å, respectivamente. La partícula de ZnO se dobla más cerca de la superficie y el ángulo formado por Zn-O-C se reduce de 129 a 118 ° debido a la presencia de SO 2 . Al mismo tiempo, del análisis de Hirshfeld, encontramos que el átomo de S actúa como un donador de electrones con una pérdida de 0.164 e y su efecto de adsorción a los átomos de O se debilita, resultando en la extensión de los enlaces SO de 1.481 a 1.619 Å [ 51]. A la inversa, la fuerza interatómica reforzada, debido al aumento de electrones (0,292 e) en el átomo de O de ZnO, ha acortado el enlace Zn-O de 2,182 a 1,869 Å. Aparte de las variaciones geométricas y la transferencia de electrones, el E anuncios hasta - 1.222 eV es otra evidencia de una fuerte interacción durante el proceso de adsorción, lo que indica una posible aplicación de ZnO-C 3 N monocapa en la detección de SO 2 . En cuanto al SOF 2 y SO 2 F 2 sistema de adsorción dado en la Fig. 4c yd, se puede ver que las moléculas diana han sufrido un cambio dramático en la morfología. El átomo de F en SOF 2 se deshace de la restricción del enlace S-F y es adsorbido por un átomo de Zn a una distancia de 1.830 Å. Se puede observar un cambio aún más drástico en SO 2 F 2 donde ambos enlaces S-F se rompieron y formaron enlaces Zn-F con longitudes de 1.802 y 1.883 Å. Además de la formación del enlace Zn-F, el grupo SOF restante en SOF 2 El sistema también está atrapado por el átomo de Zn a través del enlace Zn-O. Pero en el caso de SO 2 F 2 sistema, es interesante notar que el SO 2 grupo generado por la descomposición de SO 2 F 2 no se captura pero mantiene una distancia del átomo de Zn, y con sus enlaces S-O calculados de la misma manera que el SO aislado 2 en longitud. La deformación pronunciada de las moléculas de gas está asociada con la gran E anuncios calculado tan grande como - 1,683 eV en SOF 2 sistema y - 3.497 eV en SO 2 F 2 sistema. En base a esto, la adsorción de SOF 2 y SO 2 F 2 sobre ZnO-C 3 N puede determinarse como una fuerte quimisorción acompañada de una gran cantidad de transferencia de carga en este proceso, lo que indica la posible existencia de una hibridación orbital de electrones significativa. Con la gran E anuncios y Q T , ZnO-C 3 La monocapa N puede proporcionar una adsorción más estable al SO 2 , SOF 2 y SO 2 F 2 que otros nanomateriales, como se enumera en la Tabla 1, la configuración de adsorción de ZnO-C 3 La monocapa de N es más grande que los nanomateriales enumerados en 0.358–3.281 eV y 0.038–0.811 e, lo que garantiza el rendimiento de adsorción de este material cuando se usa en la detección de gas, mientras que especulamos que es difícil para estas moléculas de gas (SO 2 , SOF 2 y SO 2 F 2 ) para deshacerse de la fuerte fuerza de interacción como consecuencia de los grandes anuncios E . Por lo tanto, para evitar la degradación del rendimiento causada por el envenenamiento del sensor, se deben tomar medidas como el recocido a alta temperatura o la radiación ultravioleta para mejorar el rendimiento de desorción del ZnO-C 3 N monocapa. El análisis de rendimiento de desorción específico se proporcionará en la sección "Evaluación del rendimiento de detección de gas".
En términos de la EDD que se muestra en la Fig. 5, la parte azul indica la región de acumulación de electrones y la otra parte en violeta es la región de agotamiento de electrones. Para H 2 S, se puede encontrar una pequeña región de acumulación entre el átomo de H y el átomo de O, mientras que la mayoría de las regiones de acumulación y agotamiento se encuentran alrededor del H 2 Molécula S, lo que sugiere la pequeña transferencia de carga y la redistribución de orbitales moleculares en H 2 Molécula S. En el SO 2 sistema de adsorción, hay regiones de agotamiento obvias que rodean el átomo de S y el átomo de Zn, mientras que las regiones de acumulación se distribuyen principalmente alrededor de los átomos de O y por encima del átomo de S. Este fenómeno confirma la función de receptor de electrones de SO 2 molécula, de acuerdo con la Q T (-0,426 e) obtenido del análisis de Hirshfeld. En SOF 2 y SO 2 F 2 sistemas, a juzgar por la gran escala de regiones de acumulación y agotamiento, hay transferencias de carga e hibridación de electrones notables en ambos sistemas. Las regiones de acumulación se distribuyen entre los átomos del gas objetivo, mientras que las regiones de agotamiento se localizan principalmente alrededor del átomo de Zn, lo que refleja la propiedad distinta de donación de electrones del átomo de Zn. Como resultado, estos comportamientos electrónicos suponen que el ZnO-C 3 La monocapa de N tiene una fuerte adsorción a las moléculas de gas más persuasiva.
Propiedades electrónicas de ZnO-C 3 N monocapa sobre adsorción de gas
Como se informó en grafeno- [56], SWCNT- [57] y MoSe 2 - [58] basado en investigaciones de detección de gases, DOS es otro parámetro importante en la investigación del comportamiento electrónico entre los gases y la nanoestructura. Puede verse en la Fig. 6a que la redistribución de los orbitales moleculares en H 2 S está de acuerdo con la conclusión derivada del EDD en la Fig. 5a. La hibridación entre los orbitales H 1s y O 2p está disponible cerca de - 4 y - 6 eV pero de un grado bajo, lo que demuestra la interacción débil y la pequeña posibilidad de formar un nuevo enlace H-O. En cuanto al SO 2 En la Fig. 6c, el orbital antienlazante se mueve ligeramente cerca del nivel de Fermi y parte de los orbitales se transforma de separación a conexión, manifestando la aparente redistribución de la estructura electrónica en SO 2 molécula. Para la interacción entre los átomos en la Fig. 6d, los orbitales O 2p, Zn 4s y Zn 3d se encuentran hibridados en múltiples niveles de energía, tales como - 6, - 4 y - 2 eV. La hibridación significa la fuerte interacción química entre el átomo de O y el átomo de Zn y apoya eficazmente la formación del enlace Zn-O calculado en la estructura optimizada. En el SO 2 F y SO 2 F 2 sistema, debido a la deformación dramática en la estructura, los orbitales moleculares se activan fuertemente y se redistribuyen con muchos orbitales formados nuevos. Los orbitales F 2p y O 2p en SOF 2 se hibridan intensamente con los orbitales Zn 4s y 3d en - 8, - 7 y + 3 eV. La hibridación entre átomos de F y átomos de Zn se puede identificar cerca de - 7, - 5 y + 3,5 eV. La aparente hibridación entre el átomo de Zn y los átomos de F, O atrapados es la evidencia de la formación de enlaces químicos estables, a saber, los enlaces Zn-F y Zn-O, que pueden ser una explicación del fuerte efecto de adsorción entre ZnO-C 3 N monocapa y los dos gases. Combinado con los resultados obtenidos de cuatro sistemas de adsorción, excepto para H 2 Molécula S, las otras tres moléculas (SO 2 , SO 2 F y SO 2 F 2 ) se puede adsorber firmemente cuando se expone al ZnO-C 3 N monocapa. Esta conclusión prueba que la sustancia tiene la potencial aplicación de eliminación de gas en el equipo de alto voltaje.
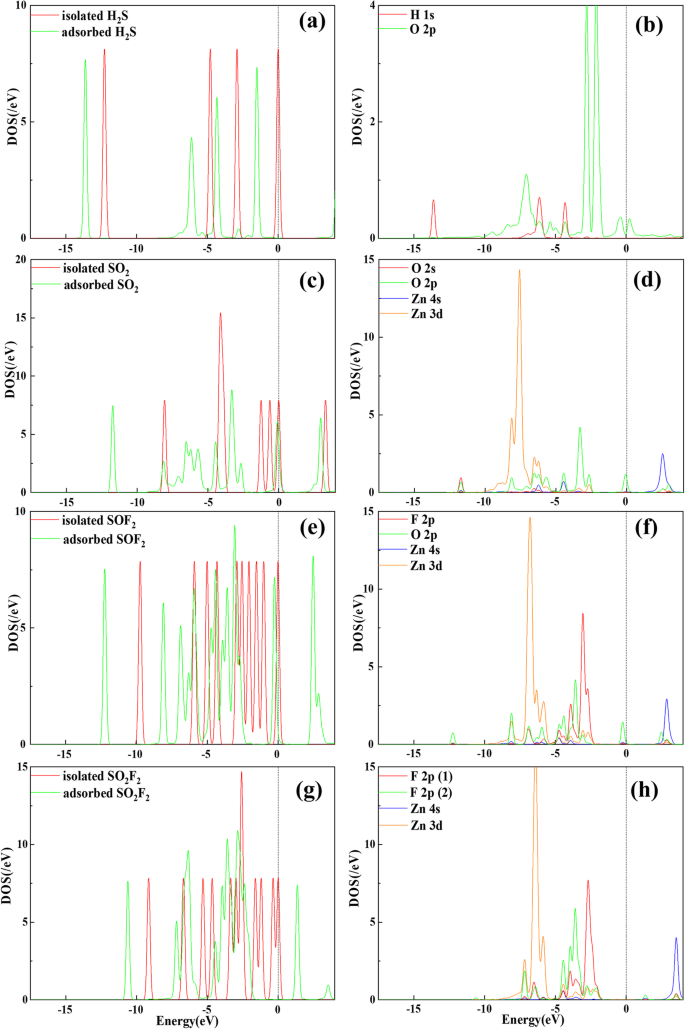
DOS y PDOS de la molécula de gas adsorbida en ZnO-C 3 N monocapa. un , b H 2 Sistema S. c , d SO 2 sistema. e , f SOF 2 sistema. g , h SO 2 F 2 sistema
Evaluación del rendimiento de detección de gas
Para lograr la detección de gas, es necesario un cambio moderado en la conductividad para los dispositivos de tipo resistivo de post-adsorción. La conductividad de un determinado sistema está relacionada con su banda prohibida de acuerdo con la siguiente ecuación [59]:
$$ \ sigma =A \ times {e} ^ {- {E} _g / 2 {k} _BT} $$ (3)donde A es una cierta constante, k B es la constante de Boltzmann (8,62 × 10 −5 eV K −1 ) y T es la temperatura. Se puede reconocer una relación inversamente proporcional entre la conductividad y la banda prohibida, cuanto más ancha es la banda prohibida, más difícil es para el electrón cruzar la banda prohibida. La Figura 7a demuestra que la banda prohibida en ZnO-C 3 N monocapa es bastante pequeña como 0.168 eV, que es menos de la mitad de la banda prohibida en C 3 prístino N (0,39 eV), mientras que las propiedades del semiconductor y del bandgap indirecto siguen siendo las mismas, lo que se puede juzgar a partir de la ubicación diferente de la parte inferior de la banda de conducción (M) y la parte superior de la banda de valencia (Γ). Con respecto a la banda prohibida de los sistemas de adsorción, se pueden encontrar diferentes variaciones en la Fig. 7b – d. En H 2 S, la banda prohibida disminuye a 0,125 eV debido al movimiento descendente en la parte inferior de la banda de conducción. En otros sistemas, el nivel de impureza novedoso que aparece en la parte superior de la banda de valencia se encuentra con el nivel de Fermi cerca del punto M y da como resultado la banda prohibida cero de estos sistemas, que puede considerarse un fuerte dopaje de tipo p para el ZnO-C 3 N monocapa [43, 60]. Aunque la naturaleza semiconductora de las estructuras adsorbidas puede estar cubierta por su propiedad de tipo metálico de banda prohibida cero [61], la banda prohibida cero podría proporcionar una mejora visible en la conductividad. Es muy importante mejorar el rendimiento de respuesta de los dispositivos basados en ZnO-C 3 N monocapa. Para ampliar el análisis adicional de la respuesta ( R ) rendimiento, aquí lo calculamos con base en la siguiente ecuación [62]:
$$ R =\ frac {\ left | \ frac {1} {\ sigma _ {\ mathrm {gas}}} - \ frac {1} {\ sigma _ {\ mathrm {gas}}} \ right |} {\ frac {1} {\ sigma _ {\ mathrm {puro}}}} =\ left | \ frac {\ sigma _ {\ mathrm {puro}} - {\ sigma} _ {\ mathrm {gas}}} {\ sigma _ {\ mathrm {gas}}} \ right | $$ (4)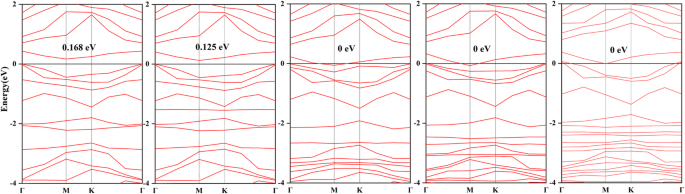
Estructura de bandas de a ZnO-C 3 N monocapa, b H 2 Sistema S, c SO 2 sistema, d SOF 2 system y e SO 2 F 2 sistema
donde σ puro y σ gas representan la conductividad del ZnO-C 3 Sistema N antes y después de la adsorción, respectivamente. Según los cálculos, la R para el H 2 El sistema S y los tres sistemas restantes son 0.567 y 0.962, es decir, la conductividad aumentaría en 56.7% y 96.2% cuando la adsorción ocurre en la superficie de ZnO-C 3 N monocapa; en este caso, es posible detectar la existencia de estos gases.
El tiempo de recuperación ( τ ) es otro parámetro importante para estimar la propiedad de los sensores utilizados en la detección de gas, que indica el tiempo empleado en eliminar las moléculas de gas adsorbidas. Al revisar la literatura, τ podría calcularse mediante la ecuación de van’t Hoff Arrhenius [63]:
$$ \ tau ={F} ^ {- 1} {e} ^ {- {E} _ {\ mathrm {a}} / {k} _ {\ mathrm {B}} T} $$ (5)donde F es la frecuencia de intentos y se define como 10 12 s −1 en este estudio. E a es la barrera de energía para la desorción que se asume igual que el valor de E anuncios aquí, k B y T se definen igual que en la Ec. (3). De la Eq. (5), la desorción de los gases adsorbidos sería más difícil ya que E anuncios aumentando de tamaño, pero también se puede controlar elevando la temperatura de trabajo.
La Tabla 2 enumera el tiempo de recuperación requerido para que los cuatro gases se eliminen de la superficie de ZnO-C 3 N monocapa. Para el H 2 Molécula S, la pequeña E anuncios Indudablemente refleja la barrera de baja energía para la desorción, lo que provoca el tiempo de recuperación extra corto en microsegundos. Mientras tanto, para los sistemas con E más grandes anuncios , parece imposible separar la molécula de gas de la superficie a la temperatura de trabajo ya que la desorción tardará varios días. When it reaches 498 K and 598 K which can rarely occur in the electrical equipment, the desorption process could be accelerated to the minutes scale for SO2 and SOF2 , respectivamente. The extremely strong adsorption between the gas molecules (SO2 , SOF2 , and SO2 F2 ) and the surface reveals the potential application of the ZnO-C3 N monolayer as a gas scavenger to remove the SF6 decomposition species and maintain the good insulation state inside the power system. In addition, in the actual structure, given the high quantity of ZnO nanocrystals on C3 N, the effect is expected to be substantially enhanced. Besides, comparing to the original configuration, the activity of the gases releasing from the ZnO-C3 N monolayer is greatly impaired and can hardly exert impact on the system because of the severe deformation of the molecular structures (SOF2 and SO2 F2 ). In terms of the H2 S, it is supposed that the unstable interaction and extremely short recovery time of ZnO-C3 N monolayer towards H2 S are unable to provide an effective detection as the adsorption density is supposed to be small.
Conclusiones
In this paper, a model of ZnO-modified C3 N is established and the optimal structure is investigated by placing the ZnO particle on the surface of C3 N in various orientations and position. Thus, the adsorption parameters of the ZnO-C3 N monolayer on four SF6 decomposition species, namely H2 S, SO2 , SOF2 , and SO2 F2 , were obtained by analysing the E ads , DOS, Q T , and band structure before and after adsorption. It is found that the H2 S molecule can hardly adsorb stably on the nanostructure; at the same time, the other gases are strongly trapped in the ZnO particle. These results confirmed that the adsorption performance of ZnO-C3 N monolayer allows its potential application as gas scavenger to sweep SO2 , SOF2 , and SO2 F2 from the high-voltage equipment, which keeps the insulation strength and the safe operation of power system. Plus, the frontier molecular orbital theory implies that ZnO-C3 N monolayer possesses the possibility to estimate the dielectric state of SF6 insulation equipment as an indicator, given the obvious changes in conductivity caused by the adsorption of the abovementioned gases.
Disponibilidad de datos y materiales
All the data and material are provided in the manuscript and supplementary file.
Nanomateriales
- Jabón antibacteriano
- Innovación en Mar-Bal
- Industrias en las que trabajamos
- Efecto superficial sobre el transporte de petróleo en nanocanales:un estudio de dinámica molecular
- El estudio de un nuevo sistema micelar similar a un gusano mejorado con nanopartículas
- Investigación teórica de nanocables de germanio tensados biaxialmente por tracción
- Estudio numérico de un absorbedor solar eficiente que consta de nanopartículas metálicas
- Estudio antitumoral de nanogeles de condroitina sulfato-metotrexato
- Estudios teóricos sobre fotodiodos de avalancha de InGaAs / InAlAs SAGCM
- Reacción de reducción de oxígeno en nanocatalizador de PtCo:Envenenamiento por aniones (bi) sulfato
- Investigación de los primeros principios de los comportamientos de adsorción de moléculas pequeñas en pentagrafeno



