La influencia de los materiales, la heteroestructura y la orientación de los nanohíbridos en la actividad fotocatalítica
Resumen
En este trabajo, diferentes estructuras basadas en nanobarras de ZnO tipo n electrodepositadas y Cu 2 tipo p Las nanoestructuras de O, CuSCN y NiO se fabrican para la degradación del naranja de metilo (MO). Se discute por primera vez la influencia de los materiales, la heteroestructura y la orientación de los nanohíbridos en la actividad fotocatalítica. Las estructuras de heterounión muestran una mejora notable en comparación con el semiconductor desnudo. La morfología de la nanoestructura influye principalmente en la actividad fotocatalítica. NiO tiene la actividad catalítica más alta entre las cuatro nanoestructuras semiconductoras prístinas de ZnO, Cu 2 O, CuSCN y NiO. La mayor mejora de la actividad fotocatalítica se obtiene utilizando una heteroestructura de ZnO / NiO (1 min) atribuida a la estructura de heterounión y un área de superficie específica extremadamente mayor, que puede degradar el MO (20 mg / L) a incoloro en 20 min con el fotocatalítico más rápido. velocidad entre estructuras de heterounión homogénea. Mientras tanto, la metodología y el análisis de datos descritos en este documento servirán como un enfoque eficaz para el diseño de nanoestructuras híbridas para la aplicación de energía solar, y los nanohíbridos apropiados tendrán un potencial significativo para resolver los problemas ambientales y energéticos.
Antecedentes
Los nanomateriales híbridos con excelentes propiedades ópticas, electrónicas y magnéticas han atraído mucho interés en los últimos años debido a sus aplicaciones generalizadas en la remediación del medio ambiente [1, 2] y la conversión de energía solar [3, 4]. En los últimos años, se han desarrollado varias variedades de nanohíbridos, por ejemplo, nanocompuestos de óxido de grafeno [5], TiO 2 / BiVO 4 nanocompuestos [6], nanocompuestos de hidrogel impresos en 3D [7] y Ru / Li 2 O nanocomposites [8]. Entre los diferentes tipos de nanomateriales, las heterouniones basadas en diferentes nano-semiconductores se han convertido en un área de investigación importante debido a sus atractivas propiedades fotocatalíticas [9,10,11] y fotovoltaicas [12,13,14]. Recientemente, se han realizado varios trabajos de investigación sobre diversas aplicaciones catalíticas de la degradación del tinte, como el organocatalizador de membrana nanohíbrida [15], el catalizador nanohíbrido bioinorgánico [16] y el catalizador nanohíbrido verde [17]. Debido a la toxicidad, los colorantes orgánicos en las aguas residuales representan una seria amenaza para la salud humana [18, 19]. Por tanto, la conversión de colorantes orgánicos en sustancias inocuas es fundamental para la vida humana y el desarrollo sostenible. Se han explorado una variedad de materiales semiconductores inorgánicos con diferentes morfologías como fotocatalizadores para la purificación de aguas residuales bajo radiación UV o luz visible [20,21,22], especialmente óxido de zinc (ZnO) y dióxido de titanio (TiO 2 ) nanomateriales unidimensionales (1D). Hasta ahora, los nanomateriales de ZnO obtuvieron la investigación más amplia entre varios semiconductores, lo que podría atribuirse a su rendimiento eficiente en la transferencia de electrones [23], que proporciona orificios fotogenerados para una oxidación fuerte, mejor característica respetuosa con el medio ambiente, no toxicidad, bajo costo y buena estabilidad. y estar muy extendido en la tierra [24, 25]. Sin embargo, la actividad fotocatalítica de ZnO está severamente limitada por sus defectos internos:respuesta más estrecha de la región UV-visible debido a su gran banda prohibida y alta eventualidad de recombinación de pares de electrones-huecos fotogenerados [26, 27]. Para superar estas limitaciones, se han tomado numerosas medidas, como el dopaje [28], metales nobles compuestos, como Au [29, 30] y Ag [31]; y combinar con otros semiconductores, como CdS [32], ZnSe [33], CdSe [34, 35] y PbS [36, 37]. Se ha demostrado que la obtención de heterouniones basadas en ZnO y otros semiconductores es una forma viable de mejorar la respuesta a la luz visible y la eficiencia de degradación de las aguas residuales. Recientemente, se han desarrollado varias heterouniones basadas en nanomateriales de ZnO y nano-semiconductores de tipo p sobre degradación. Recientemente, el Cu 2 Las heteroestructuras de O-ZnO en la fotocatálisis fueron informadas por Wang et al. [38] y Yu et al. [39]. Luo y colaboradores informaron de la heteroarquitectura ZnO / CNF / NiO para la fotocatálisis de alto rendimiento [40]. Liu y col. reportaron heterouniones de nanofibras electrohiladas NiO / ZnO con actividad fotocatalítica mejorada [41]. La estructura de ZnO / CdS también tiene una mayor actividad fotocatalítica que los materiales prístinos [42]. Estos informes indican que las heteroestructuras poseían una mayor actividad fotocatalítica de descomposición del tinte que los semiconductores prístinos. Sin embargo, la eficiencia de la degradación fotocatalítica del naranja de metilo (MO) necesita mejoras adicionales. Además, el diseño de la estructura de heterounión necesita más investigación, por ejemplo, reducir el costo al deshacerse del metal noble y usar un método simple como la electrodeposición y una temperatura de reacción más baja. En este estudio, ZnO, Cu 2 Las nanoestructuras de O, CuSCN y NiO se preparan mediante un método de electrodeposición simple y de bajo costo a temperatura ambiente. Se fabrican estructuras de heterounión de diferentes materiales y diferentes orientaciones basadas en nanobarras de ZnO de tipo n y Cu 2 de tipo p Nanoestructuras de O, CuSCN y NiO. Las heteroestructuras exhiben un rendimiento fotocatalítico mucho mejor para la degradación fotocatalítica de MO que el material prístino de tipo n o el material de tipo p. La influencia sobre la orientación de la heterounión depende de la calidad del cristal del material superior de la heterounión. La influencia sobre el material de diferentes condiciones de reacción depende de la morfología y la calidad de las nanoestructuras. Entre los tres materiales de tipo p utilizados en nuestro trabajo, NiO tiene el rendimiento fotocatalítico más excelente. El ZnO / NiO (1 min) puede descomponer la solución acuosa de MO (20 mg / L) de naranja a incolora en 20 min. Revela que tanto el material como la orientación pueden tener un efecto sobre el rendimiento fotocatalítico, lo que tiene un significado de gran importancia para la descomposición de contaminantes orgánicos; Además, este estudio es el primer estudio exhaustivo de la influencia de los materiales, la orientación y la heteroestructura en la actividad fotocatalítica y puede promover más investigaciones sobre más nanohíbridos para obtener una mayor eficiencia fotocatalítica.
Métodos
Materiales experimentales
Vidrio recubierto de óxido de indio y estaño (ITO) (CSG Holding Co., Ltd., 15 Ω / sq), nitrato de zinc (Zn (NO 3 ) · 6H 2 O), hexametilentetramina (HMT), sulfato de cobre (II) pentahidratado, hidróxido de sodio, ácido láctico, tiocianato de potasio, ácido etilendiaminotetraacético, trietanolamina y nitrato de níquel hexahidrato, todos adquiridos de Sinopharm Chemical Reagent Co., Ltd. Todos estos materiales son de grado analítico y utilizado tal como se recibió sin purificación adicional.
Preparación de nanoestructuras
El método de electrodeposición rentable se utiliza en este trabajo para la preparación de la gran área de nanoestructuras debido al procesamiento a baja temperatura, formas de sustrato arbitrarias y control preciso del tamaño de las nanoestructuras [43]. Todas las deposiciones se llevan a cabo en una celda de vidrio configurada en la que un sustrato ITO, una placa de platino y un electrodo Ag / AgCl en KCl saturado o electrodo de calomelanos saturado (SCE) sirven como electrodo de trabajo, contraelectrodo y electrodo de referencia. , respectivamente. Las condiciones de reacción detalladas para la fabricación de todas las nanoestructuras por electrodeposición se muestran en la Tabla 1. El valor de pH de Cu 2 La solución de reacción O se regula de 10 a 12 por NaOH. El valor de pH de la solución de reacción de CuSCN es de alrededor de 1,5. Finalmente, todas las muestras depositadas anteriormente se enjuagan con agua desionizada para eliminar el electrolito y se secan al aire de forma natural. No se emplea recocido posterior a la deposición.
Caracterizaciones
Los patrones de difracción de rayos X (XRD) se miden con un difractómetro Rigaku D / Max-2500 usando radiación Cu Kα ( λ =1,54 Å) a temperatura ambiente. La velocidad de escaneo es de 10 ° / min. El voltaje y la corriente son 40 kV y 40 mA. La superficie y la estructura en sección transversal de las muestras se caracterizan por microscopía electrónica de barrido (SEM) utilizando un Philips-FEI XL 30-SFEG a temperatura ambiente sin ningún recubrimiento de superficie. El voltaje de aceleración es de 10 a 20 kV. Las propiedades ópticas de las muestras se investigan mediante espectrometría de reflectancia difusa UV-vis (UV-vis DRS) utilizando un espectrofotómetro UV-vis Shimadzu UV-3101PC a temperatura ambiente.
Experimentos de descomposición fotocatalítica
Las actividades fotocatalíticas de las muestras preparadas se evalúan hacia la degradación de MO en solución acuosa. Una lámpara Xe de 500 W es una fuente de luz de dispositivos de reacción fotocatalítica. En un proceso de fotodegradación, la muestra se coloca en un reactor de cuarzo lleno con 3 mL de solución acuosa de MO (20 mg / L). Antes de la irradiación, la solución acuosa se mantiene en la oscuridad durante 60 min para alcanzar el equilibrio de adsorción de MO. Después de un tiempo de irradiación específico, el rendimiento de la descomposición fotocatalítica se analiza midiendo la absorbancia de la solución de MO en su longitud de onda característica (465 nm) con un espectrofotómetro UV-vis. Todas las muestras se realizan en experimentos independientes y se llevan a cabo a temperatura ambiente.
Resultados y discusión
Preparación de nanoestructuras y análisis de composición
Todo el ZnO, Cu 2 Las nanoestructuras de O, CuSCN y NiO se sintetizan mediante el método de electrodeposición rentable a temperatura ambiente. La electrodeposición se realiza en una celda electroquímica estándar de tres electrodos en el modo potenciostático. Las texturas cristalinas de ZnO, Cu 2 Las nanoestructuras de O, CuSCN y NiO se caracterizan mediante perfiles XRD. Las imágenes XRD de ZnO, Cu 2 Las nanoestructuras de O, CuSCN y NiO preparadas mediante el método de electrodeposición se muestran en la Fig. 1. Un conjunto de picos en la Fig. 1a aparece en 2 θ de ca. 34,36 °, 36,12 ° y 47,48 ° para las nanovarillas de ZnO, que se asignan a los cristales (002), (101) y (102) de ZnO, respectivamente. Todos los picos en las nanovarillas de ZnO se pueden indexar a la estructura de wurtzita hexagonal de ZnO, y no existen otras fases detectables en las nanoestructuras de ZnO, que son similares a los perfiles XRD en Ref. [39]. Además, el pico fuerte de ZnO (002) indica que se obtienen nanobarras orientadas con alta cristalinidad. Tres picos en la Fig. 1b a 2 θ de ca. Se observan 29,78 °, 36,81 ° y 42,89 ° para el Cu 2 electrodepositado Película O sobre sustrato ITO, que se asignan a (110), (111) y (200) de Cu 2 O cristales, respectivamente, lo que indica que Cu 2 O tiene la estructura cúbica cúprica pura con una orientación preferida (111), que es la misma que los perfiles XRD en la Ref. [38]. La difracción de picos en la Fig. 1c aparece en 2 θ de aproximadamente 16,21 °, 27,20 ° y 32,69 ° y se pueden asignar a los planos (003), (101) y (006) de los cristales de CuSCN, respectivamente, que pueden indexarse a una estructura romboédrica β -CuSCN [44]. Los patrones de XRD en la Fig.1d se asignan a los tres picos principales de NiO a 37.52 °, 43.26 ° y 62.86 °, que se refieren a los planos (111), (200) y (220), respectivamente, tan similares como XRD perfiles en Ref. [39]. Todos los patrones de XRD revelan que no se detecta ninguna de las otras fases y que las nanoestructuras no tienen impurezas. La Figura 1 e muestra los espectros de absorbancia de ZnO, Cu 2 Nanoestructuras de O, CuSCN y NiO preparadas por el método de electrodeposición. Como se muestra en la Fig. 1e, las nanobarras de ZnO solo pueden absorber la luz de alta energía con una longitud de onda menor a 370 nm. Se puede observar un borde de la banda de absorbancia a 600 nm para Cu 2 O, como se muestra en la Fig. 1e, que es consistente con la banda prohibida de Cu 2 O (2,1 eV). Como se muestra en la Fig. 1e, CuSCN tiene una absorción baja y amplia con una longitud de onda superior a 350 nm y NiO tiene una absorción entre 350 y 500 nm pero una absorción baja con una longitud de onda superior a 500 nm. Toda la absorción de ZnO, Cu 2 Las nanoestructuras de O, CuSCN y NiO se encuentran en el rango ultravioleta y visible, y esto garantizará la absorción de la luz ultravioleta bajo la irradiación de la lámpara Xe en los experimentos de descomposición fotocatalítica y la consecuente generación de pares de electrones-huecos.
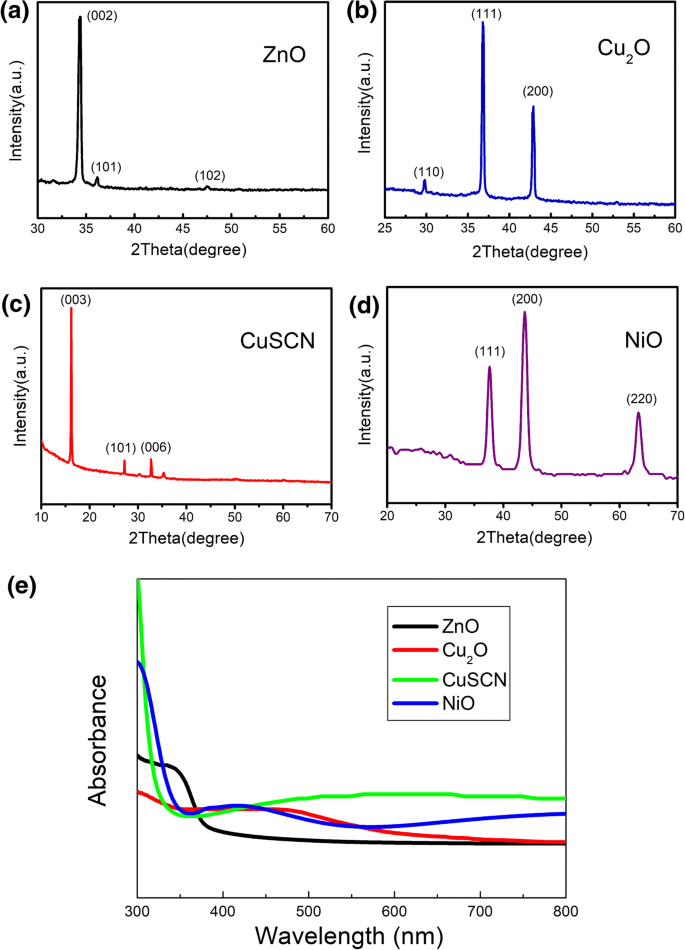
Espectros de fotoelectrones de rayos X de ZnO ( a ), Cu 2 O (pH 10, 20 min) ( b ), CuSCN (3D) ( c ) y NiO (1 min) ( d ) nanoestructuras preparadas mediante el método de electrodeposición y los espectros de absorbancia ( e ) de ZnO, Cu 2 Nanoestructuras de O (pH 10, 20 min), CuSCN (3D) y NiO (1 min) preparadas mediante el método de electrodeposición
Diseño y morfología de las heteroestructuras
Diferentes heterouniones basadas en nanobarras de ZnO tipo n y Cu 2 tipo p Se fabrican nanoestructuras de O, CuSCN y NiO con diferente orientación. En primer lugar, el ZnO, Cu 2 O, ZnO / Cu 2 O y Cu 2 O / ZnO se preparan para la degradación fotocatalítica de MO. La Figura 2 muestra la imagen SEM de la vista superior de nanobarras de ZnO (a), ZnO / Cu 2 O (pH 12, 20 min) heterounión (b), Cu 2 O (pH 12, 20 min) (c) y Cu 2 O (pH 12, 20 min) / heterounión ZnO (d). Archivo adicional 1:La Figura S1 muestra la vista en sección transversal de estas cuatro estructuras. La Figura 3 muestra la imagen SEM de la vista superior de ZnO / Cu 2 O (pH 10, 20 min) heterounión (a), ZnO / Cu 2 O (pH 10, 40 min) heterounión (b), Cu 2 O (pH 10, 20 min) / heterounión ZnO (c), Cu 2 O (pH 10, 40 min) / heterounión ZnO (d), Cu 2 O (pH 10, 20 min) (e) y Cu 2 O (pH 10, 40 min) (f). Archivo adicional 1:La Figura S2 muestra la vista en sección transversal de estas seis estructuras. Como se ve desde la vista superior que se muestra en la Fig. 2a y la vista en sección transversal en el archivo adicional 1:Figura S1 (a), las nanovarillas de ZnO obtenidas por el método de electrodeposición son casi la estructura de un prisma hexagonal. El diámetro y la longitud de las nanovarillas se encuentran en los rangos de 200–300 nm y 800–1200 nm, respectivamente. Como se muestra en las Figs. 2c y 3e yf, se puede observar que el Cu 2 Los cristales de O crecen de cubos a octaedros cuando el valor de pH de la solución de electrodeposición cambia de 10 a 12. Los cristales obtenidos a pH ~ 10 con el tiempo de reacción de 20 y 40 min no son todos los cubos perfectos debido a la diferente disolución del cristal en la solución de reacción [45]. También se puede ver claramente que el Cu 2 Los cristales de O se hacen más grandes y densos según el tiempo, y el Cu 2 Los cristales O se amontonarán y agregarán cuando el tiempo de reacción sea más largo. En el proceso de agregación, el Cu 2 Los cristales O se deformarán debido a la gran densidad. Como se muestra en las Figs. 2b y 3a yb, se puede concluir que Cu 2 Los cristales de O que crecen en las nanovarillas de ZnO son tan compactos como el Cu 2 Cristales de O que crecen en el sustrato de vidrio ITO desnudo y son algunos más pequeños que el Cu 2 Cristales de O crecidos en vidrio ITO debido al diferente punto de nucleación. Cuando el valor de pH de la solución de reacción es 10, las nanovarillas de ZnO crecen en el Cu 2 Los cristales de O son más compactos que las nanovarillas de ZnO cultivadas en vidrio ITO, y el diámetro y la longitud de las nanovarillas de ZnO cultivadas en Cu 2 Los cristales de O son casi iguales con las nanovarillas de ZnO cultivadas en vidrio ITO, como se muestra en la Fig. 3c y d. Las nanovarillas de ZnO cultivadas en Cu 2 Los cristales de O (pH 10, 40 min) son un poco más densos que las nanovarillas de ZnO cultivadas en Cu 2 En la capa de las nanovarillas de ZnO aparecerán cristales de O (pH 10, 20 min) y barras de ZnO mucho más grandes. Como se muestra en la Fig. 2d, las nanovarillas de ZnO crecidas en el Cu 2 Los cristales de O (pH 12, 20 min) son mucho más escasos que las nanovarillas de ZnO que crecen en el vidrio ITO. El diámetro y la longitud de las nanovarillas de ZnO cultivadas en Cu 2 Los cristales de O (pH 12, 20 min) no son homogéneos en un rango amplio.

La imagen SEM de la vista superior de nanobarras de ZnO ( a ), ZnO / Cu 2 O (pH 12, 20 min) heterounión ( b ), Cu 2 O (pH 12, 20 min) ( c ) y Cu 2 O (pH 12, 20 min) / heterounión ZnO ( d )

La imagen SEM de la vista superior de ZnO / Cu 2 O (pH 10, 20 min) heterounión ( a ), ZnO / Cu 2 O (pH 10, 40 min) heterounión ( b ), Cu 2 O (pH 10, 20 min) / heterounión ZnO ( c ), Cu 2 O (pH 10, 40 min) / heterounión ZnO ( d ), Cu 2 O (pH 10, 20 min) ( e ) y Cu 2 O (pH 10, 40 min) ( f )
En segundo lugar, se preparan ZnO, CuSCN, ZnO / CuSCN y CuSCN / ZnO para la degradación fotocatalítica de MO. Se preparan dos nanoestructuras de CuSCN diferentes, estructuras de tipo prisma hexagonal (3D) y de nanocables (NW), mediante el método de electrodeposición. La Figura 4 muestra la imagen SEM de la vista superior de la heterounión ZnO / CuSCN (3D) (a), la heterounión ZnO / CuSCN (NWs) (b), la heterounión CuSCN (3D) / ZnO (c), la heterounión CuSCN (NWs) / ZnO ( d), CuSCN (3D) (e) y CuSCN (NW) (f). Archivo adicional 1:La Figura S3 muestra la vista en sección transversal de estas seis estructuras. Las estructuras CuSCN (3D) y CuSCN (NWs) electrodepositadas sobre nanobarras de ZnO son más densas que las del vidrio ITO, como se muestra en la Fig. 4a y b. Las nanovarillas de ZnO bajo estructuras de CuSCN (3D) están parcialmente grabadas por la solución de reacción de CuSCN con un pH erosivo de 1,5, como se muestra en la Fig. 4a y el archivo adicional 1:Figura S3 (a). Las nanovarillas de ZnO bajo estructuras de CuSCN (NW) se graban principalmente con la solución de reacción de CuSCN con un pH de 1,5, pero el contorno de las nanovarillas de ZnO se mantiene después de la electrodeposición de las estructuras de CuSCN (NW), como se muestra en la Fig. 4b y el archivo adicional 1:Figura S3 (b). El CuSCN (3D) en las nanobarras de ZnO es mucho más intensivo que las estructuras de CuSCN (NW) en las nanobarras de ZnO, y las nanobarras de ZnO debajo de las estructuras de CuSCN (NW) casi desaparecen solo quedando el vestigio del prisma hexagonal de ZnO. Las nanovarillas de ZnO preparadas en la capa de CuSCN son más compactas que las nanovarillas de ZnO cultivadas en vidrio ITO, y el diámetro y la longitud de las nanovarillas de ZnO cultivadas en CuSCN son más pequeñas que las nanovarillas de ZnO cultivadas en vidrio ITO debido a los diferentes puntos de nucleación , como se muestra en la Fig. 4c y d. Las estructuras CuSCN (3D) y CuSCN (NWs) preparadas por el método de electrodeposición en vidrio ITO están orientadas con alta densidad y casi vertical al sustrato con un diámetro de aproximadamente 100 nm y 80 nm, respectivamente, como se muestra en la Fig. 4e y f.

La imagen SEM de la vista superior de la heterounión ZnO / CuSCN (3D) ( a ), Heterounión ZnO / CuSCN (NWs) ( b ), Heterounión CuSCN (3D) / ZnO ( c ), Heterounión CuSCN (NWs) / ZnO ( d ), CuSCN (3D) ( e ) y CuSCN (NW) ( f )
Finalmente, el ZnO, NiO, ZnO / NiO y NiO / ZnO se preparan para la degradación fotocatalítica de MO. La Figura 5 muestra la imagen SEM de la vista superior de la heterounión ZnO / NiO (1 min) (a), la heterounión ZnO / NiO (10 min) (b), la heterounión NiO (1 min) / ZnO (c), NiO (10 min) / Heterounión de ZnO (d), NiO (1 min) (e) y NiO (10 min) (f). Archivo adicional 1:La Figura S4 muestra la vista en sección transversal de estas seis estructuras. La nanoestructura de NiO electrodepositada en nanobarras de ZnO durante 1 min es una malla intersectada con nanobarras de ZnO, como se muestra en la Fig. 5a y el archivo adicional 1:Figura S4 (a). Las nanovarillas de ZnO electrodepositadas sobre la nanoestructura de NiO (1 min) se exponen parcialmente creciendo a través de la malla de NiO (1 min), y la parte remanente de las nanovarillas de ZnO permanece en la malla que no se puede ver en las imágenes SEM de la vista superior. como se muestra en la Fig. 5c y archivo adicional 1:Figura S4 (c). La nanoestructura de NiO electrodepositada en vidrio ITO durante 1 min es la malla intercalada multicapa distribuida uniformemente sobre el vidrio ITO con una superficie específica alta, como se muestra en la Fig. 5e y el archivo adicional 1:Figura S4 (e). La nanoestructura de NiO electrodepositada en nanobarras de ZnO durante 10 min es flores consta de muchas partículas, como se muestra en la Fig. 5b y archivo adicional 1:Figura S4 (b). La nanoestructura de NiO electrodeposited sobre vidrio ITO durante 10 min consta de muchas partículas de NiO que pueden formar una capa compacta sobre el vidrio ITO y una capa de partículas sobre la capa compacta, como se muestra en la Fig.5f y archivo adicional 1:Figura S4 (f ). Desde la vista en sección transversal de SEM en el archivo adicional 1:Figura S4 (f), se pueden encontrar algunas grietas en la capa compacta del vidrio ITO debido a la fuerza de extrusión generada por las partículas de NiO. Cuando se electrodeposita ZnO sobre NiO (10 min), las nanovarillas de ZnO más pequeñas (en comparación con las del vidrio ITO) crecen en la capa de partículas de NiO, y la forma de las partículas de NiO desaparece solo quedando la morfología de las nanovarillas de ZnO, como que se muestra en la Fig. 5d y archivo adicional 1:Figura S4 (d). Las grietas en la capa compacta de NiO en el vidrio ITO también se pueden ver en el archivo adicional 1:Figura S4 (d), y algunas grietas en la estructura de las nanovarillas de ZnO son generadas por las grietas en la capa compacta.

La imagen SEM de la vista superior de la heterounión ZnO / NiO (1 min) ( a ), Heterounión ZnO / NiO (10 min) ( b ), Heterounión NiO (1 min) / ZnO ( c ), Heterounión NiO (10 min) / ZnO ( d ), NiO (1 min) ( e ) y NiO (10 min) ( f )
Actividad fotocatalítica
Las propiedades fotocatalíticas se investigan mediante la degradación del MO, un contaminante orgánico común [46, 47]. Tres sistemas de ZnO / Cu 2 Se discuten O, ZnO / CuSCN y ZnO / NiO, incluido el ZnO prístino, el Cu 2 prístino O (o CuSCN o NiO), ZnO / Cu 2 O (o CuSCN o NiO) y Cu 2 O (o CuSCN o NiO) con cuatro estructuras en cada sistema. Aunque el método de electrodeposición utilizado en este trabajo para la preparación de las nanoestructuras es ecológico y ambiental, el método de preparación puede requerir una cantidad considerable de productos químicos indeseables que socavan el verdor de los métodos. El problema, como la recuperación sostenible de sustancias químicas por membranas, puede resolverse mediante un proceso híbrido continuo que comprende un reactor de flujo y una unidad de nanofiltración posterior para el reciclaje in situ de disolvente y reactivo que fue desarrollado por Szekely et al. [48]. Archivo adicional 1:Figura S5 y Figura S6 exhiben los cambios de concentración de MO en ausencia y en presencia de diferentes fotocatalizadores. Obviamente, el contenido de MO tiene pocos cambios en ausencia del catalizador en comparación con la adición del catalizador. Bajo irradiación de luz visible, sólo el 15% de MO se descompone después de 40 min en ausencia del catalizador, como se muestra en el archivo adicional 1:Figura S5 (a). Las nanovarillas de ZnO prístinas exhiben un cierto grado de actividad fotocatalítica para la descomposición de MO. Sin embargo, debido a las limitaciones de los defectos internos (gran banda prohibida y fácil recombinación de pares de agujeros de electrones) y el área de superficie específica, el rendimiento fotocatalítico sigue siendo deficiente, como se muestra en el archivo adicional 1:Figura S6 (a), Figura S6 ( b) y Figura S6 (c). La comparación del área de superficie específica de las nanoestructuras se conjetura a partir del tamaño y densidad de la superficie mediante imagen SEM [49,50,51]. Los cambios de concentración de MO con ZnO, Cu 2 O (pH 10, 20 min), Cu 2 O (pH 10, 40 min), Cu 2 O (pH 12, 20 min), ZnO / Cu 2 O (pH 10, 20 min), ZnO / Cu 2 O (pH 10, 40 min), ZnO / Cu 2 O (pH 12, 20 min), Cu 2 O (pH 10, 20 min) / ZnO, Cu 2 O (pH 10, 40 min) / ZnO y Cu 2 O (pH 12, 20 min) / ZnO como los catalizadores se muestran en el archivo adicional 1:Figura S6 (a). La intensidad del pico de absorción disminuye gradualmente y se desplaza al azul a medida que aumenta el tiempo de irradiación de 0 a 40 min. El desplazamiento al azul se puede atribuir a la desalquilación [52]. El rendimiento fotocatalítico de tres Cu 2 diferentes O, Cu 2 O (pH 10, 20 min), Cu 2 O (pH 10, 40 min) y Cu 2 O (pH 12, 20 min), es similar debido a la morfología similar y al área de superficie específica, como se muestra en las Figs. 2c y 3a y b. El rendimiento fotocatalítico del Cu 2 prístino El O es más pobre que el de las nanobarras de ZnO prístinas debido a un límite cristalino más grande, una menor movilidad del portador, un área de superficie específica más pequeña y una recombinación más fácil de electrones y huecos. El rendimiento fotocatalítico de ZnO / Cu 2 O (pH 10, 20 min), ZnO / Cu 2 O (pH 10, 40 min) y ZnO / Cu 2 O (pH 12, 20 min) es casi el mismo debido a la morfología similar y al área de superficie específica de la capa superior Cu 2 O, como se muestra en las Figs. 2b y 3e y f. El rendimiento fotocatalítico de tres heterouniones de ZnO / Cu 2 O es más bajo que el de las nanovarillas de ZnO prístinas debido a la menor superficie específica de la capa superior Cu 2 O como una conexión directa a la solución MO pero es más alta que la del Cu 2 prístino Debido al efecto de la heterounión de ZnO y Cu 2 O. El rendimiento fotocatalítico de Cu 2 La arquitectura O / ZnO es la más alta en ZnO / Cu 2 O sistema debido a su estructura de heterounión y mayor área de superficie específica de la capa superior ZnO. En comparación con las escasas nanovarillas de ZnO en Cu 2 O (pH 12, 20 min) y demasiadas nanovarillas de ZnO en Cu 2 O (pH 10, 40 min), Cu 2 O (pH 10, 20 min) / ZnO tiene el mejor rendimiento fotocatalítico entre tres Cu 2 Arquitecturas O / ZnO como resultado de nanoestructuras perfectas de ZnO cultivadas en Cu 2 O (pH 10, 20 min), como se muestra en las Figs. 2d y 3c y d. Se discute la influencia en el pH de la reacción, el tiempo de reacción y la orientación de la heterounión y, en conclusión, el tiempo de reacción tiene poco efecto sobre el rendimiento fotocatalítico en el ZnO / Cu 2 O sistema. En resumen, en el ZnO / Cu 2 O sistema, Cu 2 O (pH 10, 20 min) / ZnO tiene el mejor rendimiento fotocatalítico.
Los cambios de concentración de MO con ZnO, CuSCN (3D), CuSCN (NWs), ZnO / CuSCN (3D), ZnO / CuSCN (NWs), CuSCN (3D) / ZnO y CuSCN (NWs) / ZnO como catalizadores son se muestra en el archivo adicional 1:Figura S6 (b). El rendimiento fotocatalítico de CuSCN prístino es más pobre que el de nanobarras de ZnO prístino debido a una superficie específica más pequeña, menor movilidad del portador y una recombinación más fácil de electrones y huecos. El rendimiento fotocatalítico de CuSCN (NW) es mejor que el de CuSCN (3D) debido a la mayor superficie específica de las nanoestructuras de CuSCN, como se muestra en la Fig. 4e y f. El rendimiento fotocatalítico de CuSCN (3D) / ZnO y CuSCN (NWs) / ZnO es mejor que el de ZnO debido a su estructura de heterounión y mayor área de superficie específica. CuSCN (NWs) / ZnO tiene el mejor rendimiento fotocatalítico que CuSCN (3D) / ZnO debido a las nanovarillas de ZnO más pequeñas y mejor distribuidas que crecen en la nanoestructura de CuSCN y la consecuente mayor área de superficie específica. En el sistema ZnO / CuSCN, la arquitectura ZnO / CuSCN tiene el mejor rendimiento fotocatalítico entre ZnO, CuSCN, ZnO / CuSCN y CuSCN / ZnO como resultado de la estructura de heterounión, mayor área de superficie específica del material superior de la heterounión, y el área de contacto más grande con la solución MO. Las nanovarillas de ZnO bajo estructuras de CuSCN (3D) están parcialmente grabadas por la solución de reacción de CuSCN con un pH erosivo, y las nanovarillas de ZnO bajo estructuras de CuSCN (NWs) son grabadas principalmente por la solución de reacción de CuSCN con un pH de 1,5 manteniendo solo el contorno y muy pocos restos de nanovarillas de ZnO, como se muestra en la Fig. 4a yb y archivo adicional 1:Figura S3 (a, b). Aunque las nanovarillas de ZnO bajo estructuras CuSCN (3D) están parcialmente grabadas, el espacio entre las nanovarillas se vuelve más grande que entre las nanovarillas de ZnO prístinas con la consecuente área de superficie específica más grande y es más claro y ordenado que las nanovarillas de ZnO bajo estructuras de CuSCN (NWs) con grabado casi completo. Entonces, el rendimiento fotocatalítico de ZnO / CuSCN (3D) es mejor que el de ZnO / CuSCN (NW). Se discute la influencia en la morfología de la nanoestructura y la orientación de la heterounión, y ambos pueden afectar el rendimiento fotocatalítico en el sistema ZnO / CuSCN. En resumen, ZnO / CuSCN (3D) tiene el mejor rendimiento fotocatalítico en el sistema ZnO / CuSCN.
Archivo adicional 1:La Figura S6 (c) muestra los cambios de concentración de MO con ZnO, NiO (1 min), NiO (10 min), ZnO / NiO (1 min), ZnO / NiO (10 min), NiO (1 min) ) / ZnO y NiO (10 min) / ZnO como catalizador. El rendimiento fotocatalítico de NiO prístino (10 min) es más pobre que el de nanobarras de ZnO prístino debido a la nanoestructura más grande, la consecuente área de superficie específica más pequeña, menor movilidad del portador y una recombinación más fácil de electrones y huecos. El rendimiento fotocatalítico de NiO (1 min) es mejor que NiO (10 min) y ZnO debido a la superficie específica mucho mayor de las nanoestructuras de NiO, como se muestra en la Fig. 5e y f. The photocatalytic performance of NiO (10 min)/ZnO is poorer than that of ZnO as a result of the even bigger nanostructure of the upper layer NiO (10 min) and the smaller specific surface area. As shown in Fig. 5c, ZnO nanorods are partially exposed growing through the meshwork of NiO (1 min) and the remnant part of the ZnO nanorods are remained in the meshwork. NiO (1 min) nanostructures are the multi-layer interspersed meshwork uniformly distributed on the ITO glass with much higher specific surface area, as shown in Fig. 5e. So, NiO (1 min)/ZnO has a little better photocatalytic performance than ZnO and a lower photocatalytic action than NiO (1 min). The photocatalytic performance of ZnO/NiO (1 min) and ZnO/NiO (10 min) is better than others due to their heterojunction structure and larger specific surface area. ZnO/NiO(1 min) architecture has the best photocatalytic performance in the ZnO/NiO system as a result of the heterojunction structure, extremely higher specific surface area of the upper material in the heterojunction, and the consequent larger contact area with the MO solution. The influence on reaction time and orientation of the heterojunction are discussed and both will give an effect on the photocatalytic performance in the ZnO/NiO system. In summary, ZnO/NiO (1 min) has the best photocatalytic performance in the ZnO/NiO system.
Figure 6a and b show the concentration changes of MO and the UV-vis absorption spectra of MO aqueous solution with ZnO, Cu2 O (pH 10, 20 min), CuSCN (3D), NiO (1 min), Cu2 O (pH 10, 20 min)/ZnO, ZnO/CuSCN (3D), and ZnO/NiO (1 min) as the catalysts. Among the four semiconductor nanostructures ZnO, Cu2 O (pH 10, 20 min), CuSCN (3D), and NiO (1 min), NiO has the most excellent photocatalytic performance owing to the multi-layer interspersed meshwork uniformly distributed and the consequent extremely higher specific surface area. ZnO has the bigger mobility and bigger specific surface area than Cu2 O and CuSCN so that ZnO has the better photocatalytic performance. Cu2 O has the better photocatalytic performance than CuSCN due to the bigger specific surface area. ZnO/NiO (1 min) heterostructure has the most excellent photocatalytic performance among all the heterostructures based on n-type ZnO and p-type Cu2 O, CuSCN, and NiO. It is owing to more charge transfer caused by heterojunction structure, more photo-generated carrier as a result of higher specific surface area caused by the meshwork nanostructure of the upper NiO directly contacting to MO, and less carrier recombination caused by more compact contact of NiO/ZnO than Cu2 O/ZnO and CuSCN/ZnO, as shown in Additional file 1:Figure S2(c), Figure S3(a), and Figure S4(a). In summary, NiO is the most suitable material for photocatalytic degradation of MO among the four semiconductor nanostructures of ZnO, Cu2 O, CuSCN, and NiO. The photocatalytic performance of the semiconductor can be affected both by the mobility and the specific surface caused by the nanostructure. ZnO/NiO (1 min) heterostructure has the most excellent photocatalytic performance among all the architectures based on ZnO, Cu2 O, CuSCN, and NiO. Influencing factor on the photocatalytic performance of all these architectures can be summarized as the inherent mobility of the material, the heterojunction architecture, and the morphology of nanostructure. The scheme of the photocatalysis mechanism using heterostructure photocatalyst is shown in Additional file 1:Figure S7. The mechanisms for improved photocatalytic properties are demonstrated in Additional file 1. To further assess the photocatalytic activity, we have compared the degradation ability of our best heterojunction in every system with other nanohybrids in Table 2. Compared with other catalysts, ZnO/NiO (1 min) demonstrated the best photocatalytic performance.
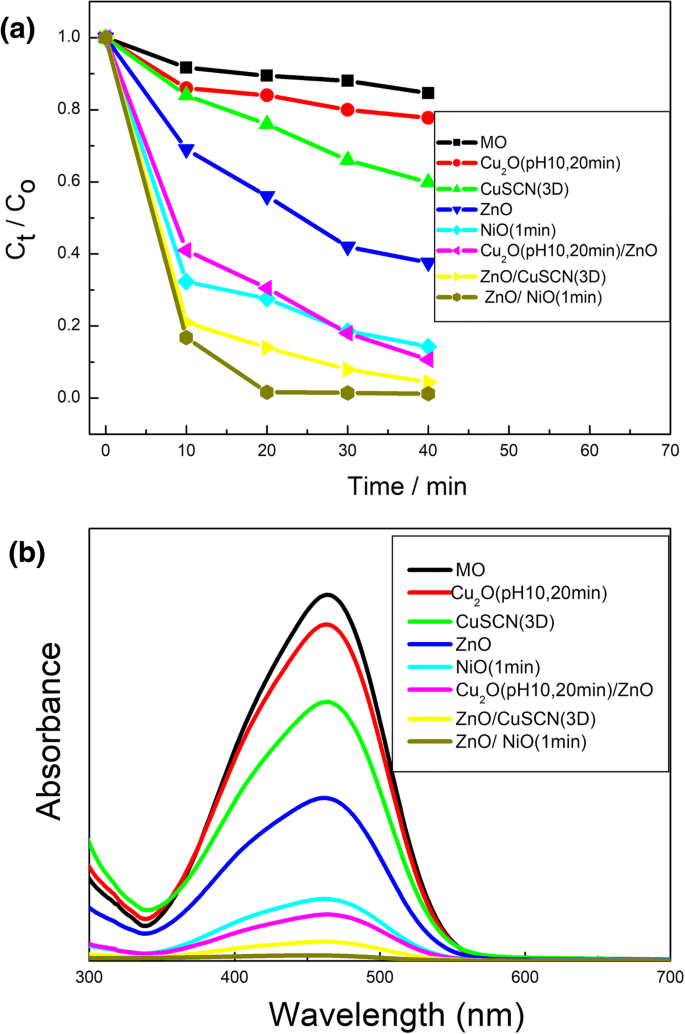
un The relative concentration (Ct /C0 ) of MO versus time under light irradiation in the absence and presence of various photocatalysts:ZnO, Cu2 O (pH 10, 20 min), CuSCN (3D), NiO (1 min), Cu2 O (pH 10, 20 min)/ZnO, ZnO/CuSCN (3D), and ZnO/NiO(1 min); b The UV-vis absorption spectra of MO aqueous solution with different photocatalysts:ZnO, Cu2 O (pH 10, 20 min), CuSCN (3D), NiO (1 min), Cu2 O (pH 10, 20 min)/ZnO, ZnO/CuSCN (3D), and ZnO/NiO(1 min)
Conclusiones
In summary, different heterojunctions based on n-type ZnO nanorods and p-type Cu2 O, CuSCN, and NiO nanostructures with different orientations are fabricated. All these structures exhibit certain photocatalytic activity for the degradation of MO. Several conclusions can be summarized with analysis of these photocatalytic data as follows:the morphology of nanostructure has significant influence on photocatalytic activity; the photocatalytic activity of heterojunction structure is better than pristine semiconductor except consideration of the influence of the nanostructure morphology; the orientation of the heterojunction has no remarkable influence on photocatalytic activity; NiO has the best photocatalytic activity among the four pristine semiconductor nanostructures ZnO, Cu2 O, CuSCN, and NiO; and ZnO/NiO (1 min) heterostructure has the most excellent photocatalytic performance among all the architectures. The great enhancement of the photocatalytic activity is obtained using ZnO/NiO (1 min) heterostructure attributed to the heterojunction structure and extremely higher specific surface area. The study on the influence of materials, nanostructure morphology, and orientation in heterostructure on photocatalytic activity can provide a theoretical direction for the photocatalyst research with application in the energy and environment fields, and it can be concluded with a perspective on the future photocatalyst and a bright prospect of these controllable nanohybrid materials.
Abreviaturas
- 1D:
-
Unidimensional
- EDTA:
-
Ácido etilendiaminotetraacético
- HMT:
-
Hexametilentetramina
- MO:
-
Methyl orange
- NW:
-
Nanowire
- SCE:
-
Electrodo de calomelanos saturado
- SEM:
-
Microscopía electrónica de barrido
- UV-vis DRS:
-
UV-vis diffuse reflectance spectrometry
- XRD:
-
Difracción de rayos X
Nanomateriales
- La evolución de SLS:nuevas tecnologías, materiales y aplicaciones
- La fórmula perfecta para alinear operaciones y mantenimiento
- Los mejores materiales de impresión 3D de metal para la fabricación aditiva
- Presentación de la estructura atómica y electrónica de las nanofibras de carbono de copa apilada
- Influencia del agua en la estructura y propiedades dieléctricas de la microcristalina y nanocelulosa
- Síntesis en un solo recipiente de nanoplacas de Cu2ZnSnSe4 y su actividad fotocatalítica impulsada por la luz visible
- Materiales y diseño de PCB para alta tensión
- Los mejores materiales para prototipos seguros para alimentos
- Los mejores materiales para sus prototipos médicos
- Un método escalable para la integración de áreas grandes de materiales 2D
- Frenos, embragues y materiales de fricción para la industria del petróleo y el gas



