Conjugación química de amina-aldehído en una superficie de ELISA de poliestireno tratado con hidróxido de potasio para nanosensar un antígeno p24 del VIH
Resumen
El ensayo inmunoabsorbente ligado a enzimas (ELISA) se ha utilizado ampliamente para la vigilancia de enfermedades y la detección de fármacos debido a su precisión y sensibilidad relativamente más altas. El ajuste fino del ELISA es obligatorio para elevar la detección específica de biomoléculas a una abundancia menor. Con este fin, la captura molecular más alta en la superficie de ELISA de poliestireno (PS) es crucial para una detección eficiente, y podría lograrse inmovilizando las moléculas en la orientación correcta. Es un gran desafío inmovilizar moléculas de proteína de una manera bien alineada en una superficie de ELISA debido a variaciones de carga. Empleamos una estrategia química de superficie de PS acoplada con 3- (aminopropil) trietoxisilano (APTES) y glutaraldehído (GLU) para demostrar el alto rendimiento con ELISA. Se encontró que un tratamiento con hidróxido de potasio seguido de una proporción igual de 1% de APTES y unión de GLU era óptimo, y una incubación más prolongada con GLU favoreció la máxima sensibilidad. p24 es un antígeno de secreción temprana vital para el diagnóstico del virus de la inmunodeficiencia humana (VIH), y se ha utilizado para una detección eficaz con la química anterior. Se siguieron tres procedimientos diferentes, que condujeron a la detección mejorada del antígeno p24 del VIH a 1 nM, que es un nivel 30 veces mayor en comparación con una superficie de ELISA convencional. La funcionalización química de la superficie que se muestra aquí también muestra una mayor especificidad con suero humano y VIH-TAT. El enfoque anterior con la química de superficie diseñada también podría recomendarse para el diagnóstico de enfermedades en otras superficies de detección que involucren la interacción de la sonda y el analito en muestras de prueba heterogéneas.
Antecedentes
La detección de biomarcadores de enfermedades y antígenos de superficie en patógenos intactos es necesaria en el campo del diagnóstico médico para prolongar la esperanza de vida de las personas y mantener una vida más sana. Hay diferentes sistemas de detección disponibles para diagnosticar patógenos y enfermedades potencialmente mortales, incluidos los cánceres [1, 2, 3, 4]. Se ha demostrado que la gama de sondas y estrategias de detección identifica varias enfermedades [5, 6]. Entre estos resultados, el ensayo de inmunoabsorción ligado a enzimas (ELISA) es una estrategia bien establecida para detectar y diagnosticar enfermedades importantes, incluido el VIH, y ELISA se ha considerado una prueba de control de calidad [7,8,9,10]. Como inmunoensayo, ELISA detecta el antígeno utilizando el anticuerpo apropiado. Para cumplir esta función, el antígeno se inmoviliza en una superficie de poliestireno (PS) y luego interactúa con el anticuerpo asociado (anticuerpo primario), seguido por el anticuerpo específico del hospedador (anticuerpo secundario) con la enzima conjugada, que se permite unirse a el anticuerpo primario. Finalmente, estas interacciones moleculares son controladas por un sustrato adecuado. Los investigadores han utilizado diferentes enfoques basados en ELISA, incluido el método sándwich con anticuerpos poli- y monoclonales adecuados o combinaciones de aptámero-anticuerpo para mejorar las detecciones [11,12,13,14].
La sensibilidad de un ELISA depende de parámetros como la interacción entre el antígeno y el anticuerpo, la temperatura, el pH y la eficacia de la unión del antígeno en la superficie de la PS. Entre estos factores, la inmovilización del antígeno o anticuerpo en la placa PS juega un papel crucial en la mejora del límite de detección. Además, la limitación planteada por la unión y la distribución no uniforme de la proteína en la superficie de la PS afecta en gran medida la sensibilidad del ensayo [5]. Una mayor cantidad con la inmovilización adecuada de proteínas ayuda a lograr la orientación correcta en la superficie de la PS para posibles mejoras en la detección. Se han empleado diferentes estrategias para inmovilizar adecuadamente las proteínas en la superficie de la PS. Una proteína o un anticuerpo tiene la capacidad de inmovilizarse en la placa de PS simplemente por adsorción química o física o interacción electrostática. Bora y col. [15] inmovilizó proteína en la superficie de PS mediante fotoquímica, y encontraron mejoras de hasta 1,5 a 2 veces más en comparación con la superficie sin tratar. En otro estudio, se demostró la inmovilización eficiente de proteínas en la placa de PS con un polímero llamado polivinil bencil lactonoilamida (PVLA) [16]. Los polímeros a base de polietilenglicol (PEG) también han proporcionado la inmovilización eficaz de biomoléculas en las superficies de detección. Lakshmipriya y col. [17] desarrolló una detección mejorada del factor IX de la proteína de coagulación inmovilizando su oligómero tiolado junto con dos polímeros (PEG-b-PAAc y N6-PEG) en una superficie recubierta de oro.
En la superficie de la placa ELISA, el PS está compuesto por una cadena de carbono alifático con anillos de benceno colgantes en cada carbono y proporciona una superficie hidrófoba. El grupo carboxilo de la superficie de la PS se une al antígeno o anticuerpo a través de una interacción electrostática con sus grupos amina expuestos. Sin embargo, esta estrategia de unión tiene desventajas, como la menor unión de proteínas y el posicionamiento irregular de las moléculas. Las proteínas y péptidos de menor tamaño con un menor número de composiciones de aminoácidos son especialmente difíciles de unir en la superficie de la PS debido a la disponibilidad de menos epítopos. Además, se ha demostrado que si las moléculas del sustrato sensor están apiñadas, entonces la distancia entre las sondas está demasiado alterada para participar en una interacción genuina. Por esa razón, aumentar la unión de una proteína o un anticuerpo en la placa de PS con la orientación adecuada mejora el límite de detección. En general, las proteínas se inmovilizan directamente en la superficie de ELISA y los investigadores se centran en mejorar la inmovilización de proteínas en la superficie de ELISA para desarrollar una detección de alto rendimiento. En particular, varios investigadores han observado la inmovilización de proteínas mediante funcionalización química en la superficie del PS para mejorar esta estrategia. La modificación química basada en amina es eficaz para inmovilizar diferentes anticuerpos a través del reticulante apropiado. El 3- (aminopropil) trietoxisilano (APTES) se usa comúnmente para modificar la superficie de detección para su uso con aminas. El anticuerpo puede inmovilizarse en la superficie de APTES modificada con amina a través de su grupo COOH. Sin embargo, la inmovilización de la proteína no se puede unir directamente a la superficie de la amina como el anticuerpo; en particular, las proteínas de menor tamaño requieren un agente de reticulación adecuado. Aquí, presentamos un paso simple de inmovilización de proteínas mediante una modificación química con APTES y glutaraldehído (GLU). Inmovilizamos las proteínas covalentemente en la superficie modificada con amina y las unimos usando GLU. GLU es un compuesto orgánico con la fórmula CH 2 (CH 2 CHO) 2 , y se ha descubierto que es uno de los agentes de entrecruzamiento de proteínas más eficaces [4, 18, 19, 20]. Tiene dos grupos aldehído en sus extremos; un extremo se une a la superficie ELISA modificada con amina y el otro extremo está libre para unirse a la proteína o al anticuerpo. En general, la inmovilización de proteínas o péptidos de menor tamaño en la superficie de ELISA es un verdadero desafío debido a la presencia de menos aminas en su superficie. Con la estrategia de funcionalización química, existe la posibilidad de utilizar proteínas o péptidos de menor tamaño para inmovilizar fuertemente el material en la placa ELISA PS. Para nuestro método, usamos APTES-GLU como enlazador; Al usar esta modificación, podemos inmovilizar cualquier tipo de anticuerpos, proteínas y péptidos. Las mejoras de señal y sensibilidad bajo esta estrategia son mayores en comparación con otras estrategias químicas exploradas en el pasado [3, 4].
Para demostrar la ventaja de estas químicas, elegimos la detección de una de las principales proteínas del virus de la inmunodeficiencia humana (VIH) (p24), que se expresa en la etapa más temprana de la infección por VIH. El antígeno p24 está formado por el núcleo viral y está presente en un nivel más alto durante la primera semana de infección. Por lo tanto, es ideal generar un sistema sensible utilizando p24 para una detección más temprana del VIH. Aquí, la detección de p24 se generó usando la superficie ELISA modificada químicamente mencionada anteriormente. Esta estrategia de funcionalización química ha mejorado la detección de p24 en la superficie de PS ELISA en varios pliegues y puede recomendarse para detectar otros biomarcadores clínicos importantes.
Materiales y métodos
Reactivos y biomoléculas
Las proteínas recombinantes VIH-p24 y Tat y el anticuerpo p24 se adquirieron de Abcam (Malasia). El 3- (aminopropil) trietoxisilano (APTES), el glutaraldehído (GLU) y el suero humano se adquirieron en Sigma-Aldrich (EE. UU.). La peroxidasa de rábano picante conjugada con anti-IgG de ratón (inmunoglobulina anti-ratón HRP) se obtuvo de Thermo Scientific (EE. UU.). Se adquirió una placa ELISA de Becton Dickinson (Francia). Se obtuvo un tampón de recubrimiento ELISA 5X de Biolegend (Reino Unido). La albúmina de suero bovino (BSA) y el sustrato de HRP [3,3 ', 5,5'-tetrametilbencidina (TMB)] se obtuvieron de Promega (EE. UU.). El lector de ELISA analítico se obtuvo de Fisher Scientific (Malasia).
Niveles óptimos de APTES y GLU para la funcionalización en la superficie PS
La optimización de los niveles de APTES y GLU para usar en la superficie de PS se realizó con el antígeno p24 del VIH dirigido. Para decidir las concentraciones adecuadas de APTES y GLU, la superficie de ELISA se activó primero con hidróxido de potasio al 1% durante 10 min. Luego, se dejaron unir tres cantidades diferentes de APTES (0,5, 1 y 2%) sobre la superficie de ELISA y se incubaron durante la noche a temperatura ambiente (TA). Después de eso, se aplicaron dos cantidades diferentes de GLU (1 y 2%) a la superficie de PS modificada con amina. En ese momento, se dejó que el VIH-p24 a una concentración de 250 nM se uniera a la superficie modificada con GLU, y la superficie restante de GLU se bloqueó con BSA al 2%. El anticuerpo p24 se introdujo a una dilución de 1:1000, y luego se dejó que la IgG-HRP anti-ratón se uniera al anticuerpo p24. Finalmente, estas interacciones se monitorearon agregando el sustrato (3,3 ', 5,5'-tetrametilbencidina, TMB) para HRP. Después de que se añadió la cantidad óptima de sustrato (100 mM), se leyó la absorbancia con un lector ELISA a 405 nm. Los experimentos de control se realizaron en ausencia de la diana HIV-p24.
Optimización del enlace de aldehído con el grupo de amina
Para determinar el tiempo de incubación adecuado para que GLU uniera las superficies modificadas con amina, se observaron dos tiempos de incubación diferentes. Después de que se modificó la superficie de ELISA PS con APTES, se inmovilizó el GLU durante 3 hy se incubó independientemente durante la noche, y luego se inmovilizó el antígeno p24 del VIH 250 nM sobre las superficies modificadas con GLU. Los pasos restantes se siguieron como se muestra en el experimento anterior.
Detecciones comparativas entre el antígeno del VIH-p24 en la superficie modificada con GLU y las uniones del antígeno del VIH-p24 premezclado con GLU
Para detectar el antígeno p24 del VIH en la superficie de ELISA, comparamos dos enfoques diferentes de modificación de la superficie utilizando GLU. En el primero (método 1:amina-GLU-p24), la superficie de PS se modificó inicialmente con una amina usando APTES al 2%, se agregó GLU al 2% a la superficie para unir la superficie de la placa con un grupo aldehído, y luego 100 Se añadió antígeno nM de VIH-p24. En el segundo enfoque (método 2:p24 premezclado de amina-GLU), después de que la superficie fuera modificada por una amina, se mezcló GLU-p24 (2% de GLU con 100 nM de antígeno de VIH-p24 y se mantuvo a TA durante 30 min). adicional. Finalmente, la detección se realizó utilizando el anticuerpo p24. Los otros pasos se realizaron como se explicó anteriormente. Los experimentos de control se realizaron en ausencia del VIH-p24 diana.
Límite de detección:ELISA convencional frente a ELISA modificado químicamente
Para comprobar el límite de detección, se titularon diferentes concentraciones de p24 de 0,5 a 500 nM, y se evaluaron utilizando los métodos y métodos convencionales 1 y 2.
Método convencional
El antígeno p24 del VIH se diluyó inicialmente con tampón de revestimiento de ELISA al 1%, se añadió a la superficie de ELISA y se mantuvo a 4 ° C durante la noche, y luego las áreas restantes se bloquearon con BSA al 2% durante 1 ha TA. Después de eso, se añadió una dilución 1:1000 de anticuerpo p24 y se incubó durante 1 h, y luego se añadió una dilución 1:1000 de anti-IgG-HRP de ratón a la superficie de ELISA y se dejó reposar durante 1 h. Finalmente, se agregó el sustrato HRP (TMB) y se midió a una longitud de onda de 405 nm utilizando el lector ELISA.
Método 1
Se agregaron diferentes concentraciones de antígeno p24 del VIH a las superficies modificadas con APTES y GLU. Una vez inmovilizado el antígeno, se siguieron los pasos restantes como se indica en el ELISA convencional. Los lavados se realizaron cinco veces entre cada paso de inmovilización. La absorbancia se registró a una longitud de onda de 405 nm utilizando el lector ELISA y se tomaron fotografías.
Método 2
En la placa ELISA modificada con APTES, se inmovilizaron diferentes concentraciones de p24 premezcladas con GLU. Se siguieron todos los demás pasos utilizados para el ELISA convencional. Los lavados se realizaron cinco veces entre cada paso de inmovilización. Se registró la absorbancia a una longitud de onda de 405 nm usando el lector ELISA y se registraron fotografías. Los experimentos de control se realizaron en ausencia del VIH-p24 diana.
Detección específica del antígeno p24 del VIH en la superficie modificada por APTES
Para comprobar la especificidad del ensayo, realizamos dos experimentos de control diferentes. En lugar del antígeno VIH-p24, usamos suero humano o proteína VIH-TAT premezclada con GLU al 1% y los agregamos a la superficie modificada con APTES. Todos los demás pasos se siguieron como se explicó anteriormente. Los experimentos de control se realizaron en ausencia de la diana HIV-p24.
Resultados y discusión
El ensayo inmunoabsorbente ligado a enzimas (ELISA) es un inmunoensayo eficaz que ayuda a los investigadores a identificar diferentes biomoléculas utilizando los anticuerpos adecuados. Una alta inmovilización de analitos (proteínas, péptidos, anticuerpos y aptámeros) [21,22,23] y la capacidad de capturar moléculas (anticuerpos monoclonales, anticuerpos policlonales y regiones Fc de anticuerpos) [24, 25] pueden mejorar drásticamente la límite de detección y ayudar a respaldar la especificidad del análisis. Teniendo esto en cuenta, varios tipos de investigación se centran en modificar químicamente la superficie de ELISA para capturar la sonda o analito correctamente orientado en una cantidad mayor. En general, un anticuerpo o proteína se inmoviliza en la superficie de ELISA PS a través de una interacción electrostática entre el grupo carboxilo en el PS y los grupos amina en la proteína o anticuerpo. Sin embargo, este método no es lo suficientemente eficaz para lograr una mayor sensibilidad y especificidad debido a su limitación de unión. Para superar este problema fundamental, durante la presente investigación, preparamos una superficie de ELISA químicamente funcionalizada utilizando 3- (aminopropil) trietoxisilano (APTES) y glutaraldehído (GLU) para la inmovilización de proteínas eficiente. Como se muestra en la Fig. 1a, una superficie de PS activada con hidróxido de potasio se modificó con una amina usando APTES y luego se reticuló con GLU para unir la proteína. En ausencia de un tratamiento con hidróxido de potasio, el nivel óptimo de APTES unido a la superficie de PS es significativamente menor debido a la ausencia de un aceptor de enlace de hidrógeno polar que mejora la adsorción inicial y desencadenará la unión más alta de APTES. La Figura 1b muestra la detección propuesta de proteína inmovilizada en la superficie ELISA modificada químicamente con su anticuerpo asociado.
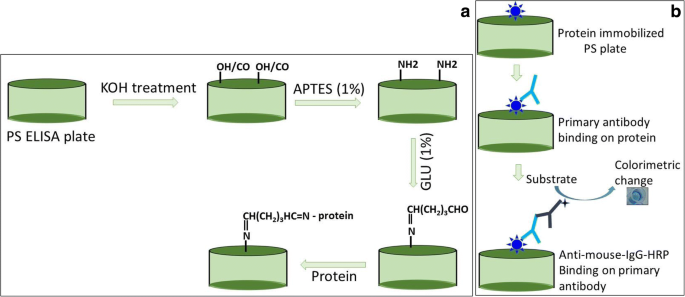
Representación esquemática de ELISA químicamente modificado ( a ). La superficie de ELISA se modificó químicamente usando APTES y GLU después del tratamiento con hidróxido de potasio. El antígeno se inmovilizó sobre la superficie modificada con GLU. b El antígeno inmovilizado fue detectado por su anticuerpo asociado
Para recopilar evidencia sobre esta estrategia de detección, queríamos utilizar una proteína importante del virus de la inmunodeficiencia humana (VIH) llamada p24. El antígeno p24 del VIH es una de las proteínas que podría expresarse durante la etapa temprana de la infección por VIH y se multiplica en el sistema huésped como se revela en otros sistemas virales (Fig. 2). El VIH intacto tiene glucoproteínas en la envoltura que cubre la cápside y el antígeno p24 del VIH reside en la región de la cápside (Fig. 3a). Antes de detectar el antígeno p24 del VIH, optimizamos inicialmente la concentración del enlazador químico para capturar el antígeno p24 del VIH en la superficie de ELISA. Exploramos diferentes concentraciones y combinaciones de APTES y GLU en la superficie de ELISA y evaluamos los resultados utilizando una concentración constante de 250 nM de antígeno VIH-p24. Como se muestra en las Fig. 3b yc, la aplicación de APTES y GLU al 1% mostró un nivel saturado de unión al antígeno p24 del VIH. Si APTES estaba presente en menos del 1%, la absorbancia de unión (DO) era menor, al mismo nivel de tiempo que la de APTES al 2%, debido a un aumento en la inespecificidad (en referencia al experimento de control). Para GLU, el nivel del 2% muestra una buena detección del antígeno del VIH-p24 a una absorbancia de 0,25 y, simultáneamente, el experimento de control (sin VIH-p24) muestra la mayor absorbancia (0,16). El APTES y GLU óptimos al 1% muestran la absorbancia más baja en el experimento de control (0,08) y la absorbancia más alta (0,22) durante la detección específica del antígeno p24 del VIH. Este resultado se produjo porque, con el aumento de APTES y GLU, es posible capturar el anticuerpo en las superficies restantes de amina libre (que se origina en APTES) y superficies de aldehído (que se origina en GLU). Este resultado es el mismo incluso cuando las regiones de la superficie libre se bloquearon con BSA en los casos anteriores. Para ajustar aún más el método, también intentamos aumentar la concentración de BSA para minimizar la señal de fondo. Sin embargo, incluso a la concentración más alta de APTES y GLU, hubo bioincrustación. Según estos resultados, la condición optimizada es APTES y GLU al 1%, como se utilizó en los experimentos.
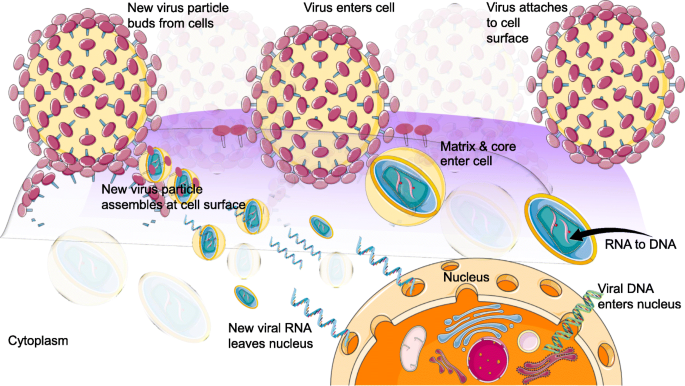
Interacción entre el VIH y la célula huésped. Se muestra la estrategia general de multiplicación del VIH
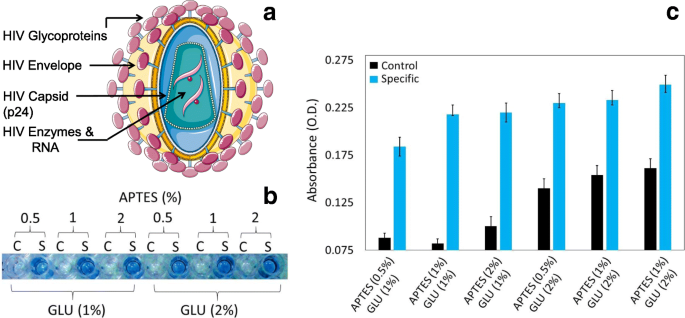
un Estructura intacta del VIH. Se indica el antígeno p24. b La optimización de APTES y GLU. Se utilizaron APTES (0,5, 1 y 2%) y GLU (1 y 2%) con diferentes combinaciones para detectar la concentración constante (250 nM) del antígeno p24 del VIH
Después de la optimización de APTES y GLU, también ajustamos el tiempo de incubación para unir el GLU a la superficie modificada por APTES. Como se muestra en la Fig. 4a, la incubación de GLU durante la noche conduce a la mayor absorbancia en comparación con el tiempo de incubación más corto (3 h). Este resultado se produce debido al tiempo de incubación insuficiente para que GLU se vincule a la superficie modificada por APTES; en última instancia, el anticuerpo puede unirse a las superficies restantes de APTES. Con un mayor tiempo de incubación para GLU, este compuesto tiene la posibilidad de cubrir la superficie APTES por completo. Esta saturación aumenta la inmovilización de proteínas en la superficie de GLU y mejora la sensibilidad del ensayo. A la concentración de 250 nM de VIH-p24, hay casi el doble de absorbancia con la incubación durante la noche de GLU (Fig. 4a).
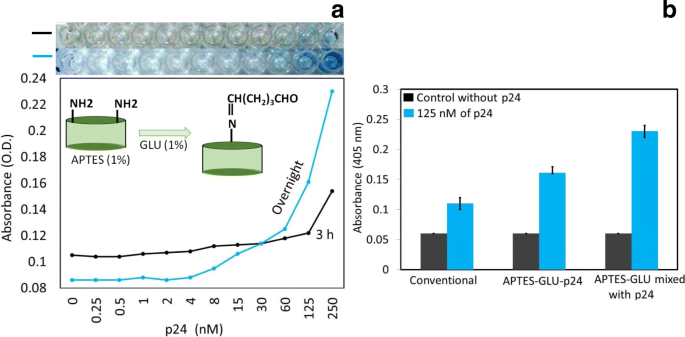
Optimización del período de incubación de GLU. un Optimizado para tener un período de incubación de 3 hy una incubación durante la noche utilizando GLU al 1% en una superficie modificada con APTES al 1%. b Detección de p24 125 nM mediante tres enfoques diferentes, convencional, APTES-GLU-p24 (método 1) y p24 premezclado con APTES-GLU (método 2)
Debido a la señal genuina más alta después de la incubación durante la noche de GLU con el aumento de la absorbancia y la detección específica de p24, usamos una condición similar para experimentos adicionales. En este caso, inmovilizamos el GLU en la superficie modificada con APTES y luego unimos la proteína (método 1). También probamos otro enfoque; En primer lugar, mezclamos GLU al 1% con antígeno VIH-p24 125 nM y luego añadimos esta mezcla a la superficie de PS modificada con amina (método 2). Sorprendentemente, hubo un aumento de la absorbancia con la misma concentración de antígeno p24 del VIH (de DO 0.161 a 0.23) que la concentración utilizada en el método 2. Cuando permitimos que la proteína se uniera a la GLU como premezcla, casi todas las proteínas estaban capaz de unir el GLU, y luego esta mezcla se adsorbió fácilmente sobre la superficie modificada con amina. Sin embargo, cuando se permitió que la proteína se uniera a la superficie de GLU preinmovilizada, la mayoría de los grupos aldehído de GLU no estaban disponibles. La Figura 4b indica que el método de mezcla muestra la detección de una concentración similar (125 nM) de antígeno p24 del VIH con una mayor absorbancia. Además, los métodos 1 y 2 mostraron una mayor absorbancia en comparación con el método convencional con la misma concentración de antígeno p24 del VIH.
Después de la optimización completa de los pasos de detección, para encontrar el límite de detección, titulamos el antígeno p24 del VIH de picomolar a rangos nanomolares (500 pM a 500 nM). Comparamos tres métodos diferentes, a saber, el convencional, APTES-GLU-p24 (método 1:p24 inmovilizado en APTES seguido de modificación GLU), y VIH-p24 premezclado con APTES-GLU (método 2:se siguió la premezcla de p24 y GLU por inmovilización en APTES) con la misma concentración de p24. Como se muestra en la Fig. 5, se encontró que el límite de detección para p24 era 30 nM para el ELISA convencional. En el método 1, el límite de detección se mejoró ocho veces (4 nM) en comparación con el ELISA convencional. Este resultado se produjo porque cuando usamos la superficie de PS químicamente modificada, la inmovilización de proteínas fue estable bajo la disposición uniforme y la tasa de inmovilización también fue bastante alta en comparación con la adsorción convencional de proteínas en la superficie de ELISA. Vashist y col. [12] ya mostró que la mayor inmovilización de un anticuerpo en la superficie ELISA modificada con APTES se asoció con un nivel de detección drásticamente mejorado en comparación con el ELISA convencional [12]. En su trabajo, la amina en APTES puede unirse a grupos carboxilo en el anticuerpo y, de esa manera, inmovilizaron el anticuerpo químicamente en la superficie de ELISA. Con este método, solo podemos inmovilizar los anticuerpos en la superficie de ELISA a través de sus grupos carboxilo, pero la inmovilización de antígenos basada en proteínas no es posible en APTES. Para ello, introdujimos el enlazador GLU para inmovilizar la proteína en la superficie ELISA PS. Con estos enlazadores químicos, no sólo se enlazó químicamente una proteína sino también un anticuerpo mediante el acoplamiento de amina al aldehído en el glutaraldehído. La unión inespecífica de biomoléculas sobre el sustrato de ELISA se controló usando los experimentos de control. Se realizó un experimento de control sin la molécula diana (VIH-p24). Sin la diana, el anticuerpo específico para p24 no puede unirse en la superficie y, por tanto, el anticuerpo secundario conjugado con enzima tampoco se inmoviliza en la superficie de ELISA. En este caso, cuando agregamos el sustrato (TMB), no podemos encontrar ningún cambio en la absorbancia.
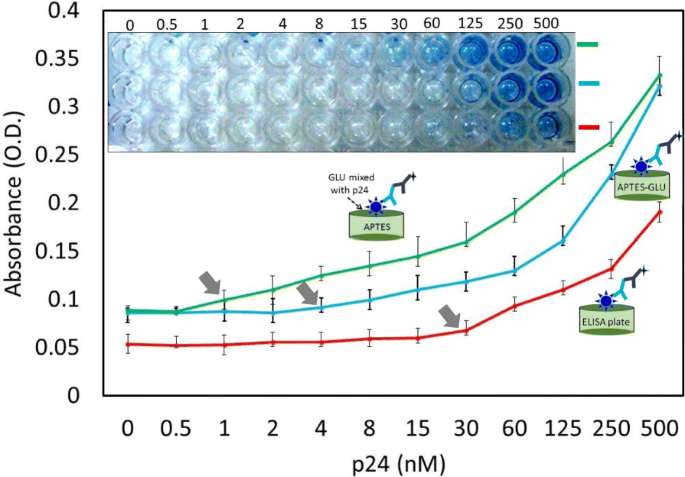
Límite de detección del antígeno p24 del VIH. La p24 se valoró de 0,5 a 500 nM. Se siguieron tres enfoques diferentes, el convencional y los métodos 1 y 2
Para mejorar el límite de detección, intentamos premezclar GLU y el antígeno p24 del VIH antes del paso de inmovilización en la superficie modificada con APTES. Se esperaba que la premezcla de GLU y antígeno p24 del VIH mejorara con la mayor inmovilización de proteínas en la superficie de ELISA. Cuando premezclamos GLU con el antígeno p24 del VIH, la relación de unión del aldehído a GLU es alta. Cuando agregamos esta mezcla a la superficie ELISA, mejora la tasa de inmovilización. Dixit y col. encontraron que cuando premezclaban el anticuerpo y APTES antes de la inmovilización en la placa ELISA, su enfoque mejoraba la inmovilización del anticuerpo en la superficie ELISA y aumentaba el límite de detección [12]. En nuestro estudio, como era de esperar, cuando premezclamos el antígeno GLU y VIH-p24 antes de la inmovilización, el límite de detección mejoró a 1 nM y fue 30 veces mayor que el del ELISA convencional, que mostró un límite de detección de 30 Nuevo Méjico. Nuestra estrategia no solo tuvo un límite de detección mejorado, sino que también mejoró la absorbancia para todas las concentraciones de antígeno p24 del VIH. A p24 250 nM, observamos que la absorbancia era de 0,35, que es casi el doble de la del ELISA convencional con la misma concentración de antígeno p24 del VIH. Con todas las concentraciones de antígeno p24 del VIH, se observó una gran diferencia en la absorbancia en comparación con el ELISA convencional (Fig. 5), como se evidencia en la detección confiable del antígeno p24 del VIH.
Para evaluar la especificidad del ensayo, realizamos la prueba con dos experimentos de control diferentes. Elegimos suero humano y HIV-TAT y lo mezclamos con GLU en lugar del antígeno HIV-p24 antes de su uso, y evaluamos su especificidad. Como se muestra en la Fig. 6, en el caso de suero humano y VIH-TAT, no hay absorbancia significativa; sin embargo, el antígeno p24 del VIH 250 nM mostró un claro aumento en la absorbancia. Este resultado confirma la detección específica del antígeno p24 del VIH en la superficie de ELISA modificada químicamente con una mayor sensibilidad.
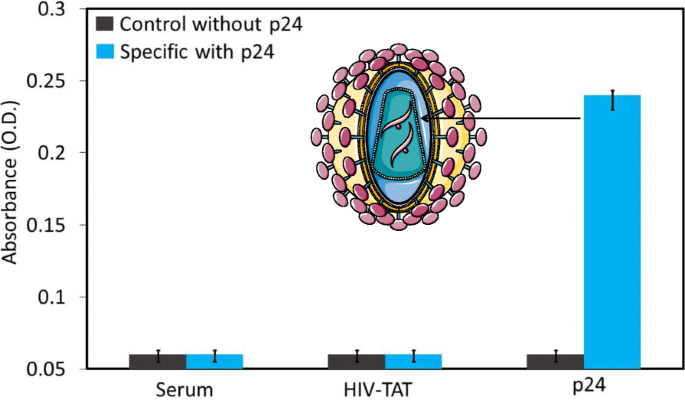
Detección específica del antígeno p24 del VIH. En lugar de HIV-p24, se utilizaron el suero humano y la proteína HIV-TAT para comprobar la especificidad
Conclusiones
Una inmovilización más alta y adecuada de una proteína o un anticuerpo en la superficie de ELISA mejora drásticamente el límite de detección. Aquí, hemos introducido un método de funcionalización química interesante para inmovilizar la cantidad de proteína o anticuerpo que se une a la superficie de ELISA PS, con la ayuda de APTES y GLU. Para demostrar la detección, utilizamos el antígeno p24 del VIH. El límite de detección se mejoró 30 veces en comparación con el ELISA convencional. Los desarrollos adicionales de la presente investigación podrían conducir a mejoras químicas similares en otras superficies de detección y serían útiles para detectar diferentes antígenos en una menor abundancia, lo que representaría un avance en los diagnósticos médicos.
Abreviaturas
- APTES:
-
3- (aminopropil) trietoxisilano
- BSA:
-
Albúmina de suero bovino
- COOH:
-
Carboxilo
- ELISA:
-
Ensayo inmunoabsorbente ligado a enzimas
- Fc:
-
Fragmento cristalizable
- GLU:
-
Glutaraldehído
- VIH:
-
Virus de inmunodeficiencia humana
- HRP:
-
Peroxidasa de rábano picante
- IgG:
-
Inmunoglobulina
- OD:
-
Una densidad óptica
- PEG:
-
Polietilenglicol
- PD:
-
Poliestireno
- PVLA:
-
Polivinil bencil lactonoilamida
- TMB:
-
3,3 ′, 5,5′-tetrametilbencidina
Nanomateriales
- Tecnologías avanzadas de deposición de capas atómicas para micro-LED y VCSEL
- Nanofibras poliméricas electrohiladas decoradas con nanopartículas de metales nobles para detección química
- Un nuevo inmunosensor magnetoelástico para la detección ultrasensible del antígeno carcinoembrionario
- Preparación de una superficie de Cu ultra suave para una síntesis de grafeno de alta calidad
- Tipos de acabados superficiales para productos moldeados
- Revestimiento de conversión de película química para chapa metálica
- Estrategias para la preparación adecuada de soldaduras
- Sistema de detección química para bajos niveles de concentración
- 5 casos de uso únicos para maquinaria de acabado
- Selección de la rugosidad superficial adecuada para el mecanizado CNC
- ¡Hay un robot para eso!



