Mini revisión sobre la estructura y propiedades (fotocatálisis) y técnicas de preparación de partículas de nanopartículas de nitruro de carbono grafítico y sus aplicaciones
Resumen
Nitruro de carbono de grafito (g-C 3 N 4 ) es bien conocido como uno de los materiales más prometedores para actividades fotocatalíticas, como el CO 2 reducción y fraccionamiento del agua, y remediación ambiental mediante la eliminación de contaminantes orgánicos. Por otro lado, el nitruro de carbono también presenta propiedades sobresalientes y pronósticos de aplicación extensivos en el aspecto de las propiedades de emisión de campo. En esta mini revisión, las novedosas técnicas de estructura, síntesis y preparación de g-C 3 con mucho cuerpo N 4 -se revelaron compuestos y películas. Esta mini revisión analizó los avances contemporáneos en la estructura, síntesis y diversos métodos utilizados para preparar g-C 3 N 4 materiales nanoestructurados. El presente estudio da cuenta del pleno conocimiento del uso de las excepcionales propiedades estructurales y de las técnicas de preparación de nitruro de carbono de grafito (g-C 3 N 4 ) y sus aplicaciones.
Introducción
La fuente de energía central eufórica del espacio extraterrestre, las capacidades de energía solar para superar la demanda de energía del mundo del almanaque por una gran frontera [1]. Dada la era de pronósticos largos del Sol, la energía solar también se considera la última fuente renovable que se puede recolectar en el planeta Tierra [2, 3]. Sin embargo, la naturaleza interminable y discontinua de esta fuente de energía presenta desafíos clave en las relaciones de recolección, almacenamiento y utilización [4]. Por el momento, hay una medida de tecnologías implementadas que pueden usarse para enfrentarlos. La energía solar puede recolectarse, transformarse y conservarse de manera flexible en forma de calor, que puede distribuir el calor a la residencia o convertirse en electricidad, así como en otras formas de energía [5]. Las tecnologías investigadas más innovadoras relacionadas con la obtención de fotones solares pueden ser las de fotocatálisis, como las describe Edmond Becquerel, 1839 [5].
Predominantemente, las aguas residuales son la principal fuente de contaminación, específicamente las aguas residuales producidas debido a la industrialización química, porque estas aguas residuales contienen una concentración pronunciada de grandes fragmentos orgánicos que son tremendamente venenosos y cancerígenos por naturaleza [3]. Anteriormente, la tecnología de remediación ambiental (que comprende adsorción, oxidación biológica, oxidación química e incineración) se ha utilizado en el tratamiento de todo tipo de aguas residuales orgánicas y tóxicas y también tiene su aplicación efectiva en la utilización de energía solar, tratamiento ambiental y aplicaciones biomédicas y de detección. Fujishima y Honda revelaron el conocimiento excepcional sobre la división fotoquímica del agua en hidrógeno y oxígeno en presencia de TiO 2 en 1972; El interés de la investigación se ha centrado en la fotocatálisis heterogénea [3, 4, 5]. La aceleración de la fotorreacción en la existencia de un catalizador se describe como fotocatálisis. Se sabe que la reacción de fotocatálisis se lleva a cabo en medios tales como fase gaseosa, fases líquidas orgánicas puras o soluciones acuosas. Además, en la mayoría de los métodos de degradación química, la degradación fotocatalítica frente a los fotones y un catalizador se identifica a menudo como la mejor opción para controlar las aguas residuales orgánicas, la utilización de la energía solar, el tratamiento ambiental y las aplicaciones biomédicas y de detección [3, 5]. Por lo tanto, la tecnología más avanzada utilizada para el tratamiento de aguas residuales orgánicas y aplicaciones relacionadas se atribuye a los fotocatalizadores impulsados por luz solar en evolución [3].
Los fotocatalizadores semiconductores se pueden utilizar para la eliminación de concentraciones ambientales de especies orgánicas e inorgánicas de sistemas de fase acuosa o gaseosa en el tratamiento de agua potable, limpieza ambiental y aplicaciones industriales y sanitarias. Esto se debe a la enorme capacidad de estos semiconductores (g-C 3 N 4, TiO 2 - y ZnO) para oxidar sustratos orgánicos e inorgánicos en el aire y el agua a través de procesos redox para su aplicación efectiva en la utilización de energía solar, aguas residuales y tratamiento ambiental, aplicaciones biomédicas y de detección sin ninguna segunda contaminación.
Nitruro de carbono grafítico polimérico (g-C 3 N 4 ) se ha convertido en el principal centro a considerar en la investigación de la fotocatálisis [6]. g-C 3 N 4 es un elemento de respuesta a la luz visible con un intervalo de banda de 2,7 eV, y la ubicación de energía de CB y VB está en -1,1 y 1,6 eV a través de un electrodo de hidrógeno normal, respectivamente [Wang et al. 2009]. Además, g-C 3 N 4 tiene la capacidad de resistir los ataques del calor, los ácidos fuertes y las soluciones alcalinas fuertes [7]. g-C 3 N 4 tiene una capacidad única de ser preparado simplemente mediante policondensación térmica de precursores ricos en N baratos, como dicianamida, cianamida, melamina, cianurato de melamina y urea, y esto es diferente a otros fotocatalizadores que contienen metales que requieren sales metálicas costosas para su preparación [ 6, 8]. La condensación térmica, solvotermal, la deposición química de vapor, la polimerización asistida por microondas y la síntesis hidrotermal son ejemplos de estrategias preparativas (Tabla 2) que se han aplicado de manera encomiable en la preparación de nitruro de carbono para propósitos distintivos y análisis en el área de fotocatálisis y otros. [9].
Debido a estas excelentes propiedades de g-C 3 N 4 , el uso de este prometedor g-C 3 N 4 en agua, CO 2 La fotorreducción, la purificación de contaminantes orgánicos, la síntesis orgánica catalítica y las pilas de combustible son más eficientes y eficaces [6]. La cantidad de investigaciones y reseñas admirables sobre g-C 3 N 4 La estructura y preparación en los últimos años ha aumentado enormemente [10]. Los autores destacaron principalmente los avances más contemporáneos en la estructura, síntesis y técnicas de preparación de g-C 3 N 4 y nitruro de carbono (CN x ) películas vívidamente en esta mini reseña concisa. La estructura única y las novedosas técnicas de síntesis y preparación de g-C 3 N 4 y CN X las películas están bien presentadas y los conceptos ilustrados sobre cómo extender la preparación de g-C 3 N 4 en esta mini revisión se enfatizan luego. Además, los autores discutieron las aplicaciones en g-C 3 N 4 , y también se defendieron las perspectivas en futuras investigaciones.
Revisión
Fotocatálisis y nitruro de carbono grafítico
La fotocatálisis se refiere mejor a la aceleración de conversiones químicas (oxidaciones y reducciones) provocadas por la activación de un catalizador. Esta reacción involucra un semiconductor ya sea solo o en combinación con promotores metal / orgánicos / organometálicos, a través de la absorción de luz, luego de la transferencia de carga o energía para ser adsorbida, lo que puede conducir a la transformación fotocatalítica de un contaminante. Durante un mecanismo de fotocatálisis, hay una ocurrencia simultánea de al menos dos acciones principales que ayudan a una producción exitosa de especies oxidantes reactivas (Fig. 2). Estas reacciones son oxidación de H 2 adsorbido disociativamente. O generado principalmente por huecos fotogenerados y reducción de un aceptor de electrones también creado por electrones fotoexcitados (Fig. 2). Por tanto, estas reacciones producen un anión radical hidroxilo y superóxido, respectivamente [11]. Durante la reacción de fotocatálisis, es obvio que hay una generación asistida por fotones de especies catalíticamente activas en lugar de la acción de la luz como catalizador en una reacción [12, 13, 14, 15, 16]. Considerablemente, la recolección de luz visible, principalmente de la luz solar, por catalizador (fotocatalizador) para iniciar transformaciones químicas (Fig. 1) se describe como fotocatálisis. Aplicación de C 3 N 4 El fotocatalizador para el tratamiento de aguas residuales, la utilización de energía solar, el tratamiento ambiental y las aplicaciones biomédicas y de detección se ha discutido en muchas áreas de la ciencia.
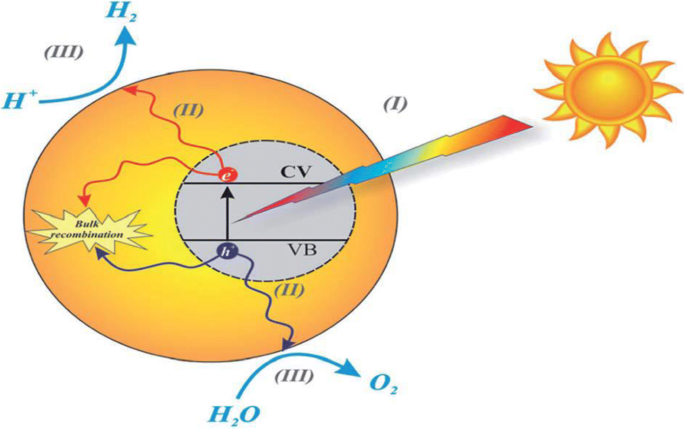
Diagrama esquemático de los mecanismos básicos de la actividad fotocatalítica del desdoblamiento del agua. Reproducido con autorización [113, 114]. Copyright 2015 y 2018. La Real Sociedad de Química
Iluminación de un catalizador semiconductor, como TiO 2 , ZnO, ZrO 2 y CeO 2 , con fotones que transportan energía igual o superior a su banda prohibida, creando un par de huecos de electrones similar a la transferencia de electrones fotoinducida y la absorción de luz promueve un electrón en la banda de conducción. El óxido puede transferir su electrón (Fig. 2) a cualquier aceptor de electrones adsorbido (promoviendo así su reducción), mientras que el hueco (o la vacante de electrones) puede aceptar un electrón de un donante adsorbido (promoviendo su oxidación). g-C 3 N 4 es capaz de catalizar el desprendimiento de hidrógeno / oxígeno y CO 2 reducción bajo excitación de banda prohibida y en presencia de co-catalizadores y / o agentes de sacrificio adecuados.
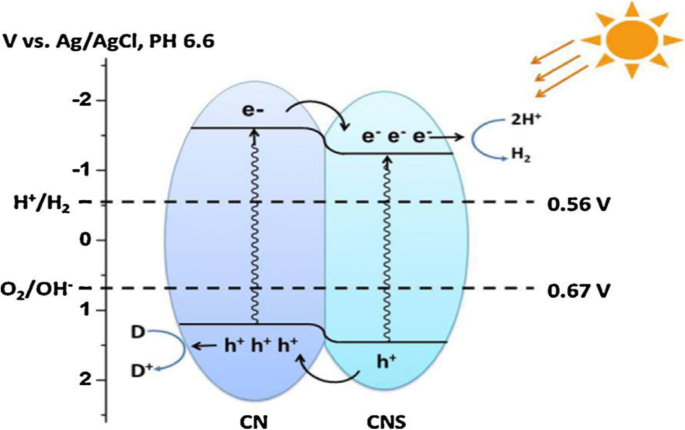
Ilustración esquemática de la heterounión orgánica formada entre g-C3N4 y g-C3N4 dopado con S. Reproducido de Ref. [115]. Copyright 2015. Elsevier
Partícula de nanopartículas de nitruro de carbono grafítico
Los materiales con nanoestructuras 1D que tienen distintas propiedades electrónicas, químicas y ópticas podrían tener su tamaño y morfología ajustados. Esta capacidad de los materiales nanoestructurados 1D ha llevado a un avance novedoso de diversos enfoques para mejorar su actividad fotocatalítica [17]. Además, existe una guía del movimiento de los electrones en la dirección axial y el confinamiento lateral de los electrones por estas nanoestructuras 1D. Ha habido un avance de materiales 2D desde el grafeno a nanohojas de óxido metálico y calcogenuro metálico y luego a estructuras orgánicas covalentes 2D (g-C3N4).
Los medios apropiados de selección de precursores y métodos de condensación habían dado lugar a dos tipos principales de g-C 3 N 4 polimorfos estructurales y esto incluye, en primer lugar, el g-C 3 N 4 consisten en unidades de s-triazina condensadas (anillo de C 3 N 3 ) con una serie periódica de vacantes de carbono único. El segundo tipo de g-C 3 N 4 consiste en tri-s-triazina condensada (tri-anillo de C 6 N 7 ) subunidades acopladas a través de grupos amino terciarios planos, y esto tiene mayores vacantes periódicas en la red. El g-C 3 N 4 Las redes consisten principalmente en segmentos a base de melón (el segundo tipo de estructura; este consiste en la unidad de tri-s-triazina, Fig. 3a) que es termodinámicamente más estable en comparación con los arreglos a base de melamina (el primer tipo de estructura; este compuesto de la s-triazina, Fig. 3b) como se describe en los cálculos de la teoría funcional (DFT) [18]. Por lo tanto, se cree ampliamente que el núcleo de tri-s-triazina es los bloques de construcción fundamentales para la formación de g-C 3 N 4 red.
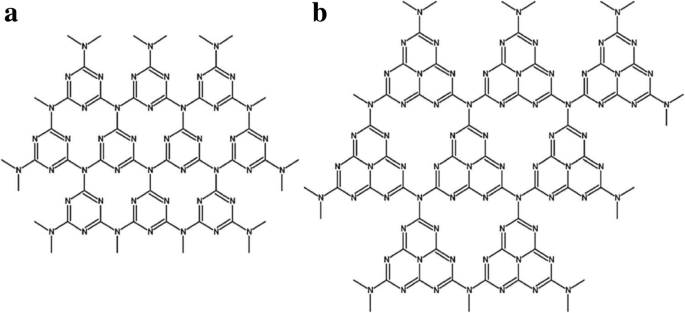
un Tri-s-triazina y b tri-s- triazina como estructuras unitarias de g-C 3 N 4 . Reproducido con autorización [25, 31]. Copyright 2008 Real Sociedad de Química
Estructura de la partícula grafítica a base de nanopartículas de nitruro de carbono
g-C 3 N 4 son una clase de materiales poliméricos bidimensionales (2D) que comprenden en su totalidad un enlace covalente, sp 2 -Átomos de carbono y nitrógeno hibridados. El carbono y el nitrógeno tienen la distinción de varios estados de valencia que forman enlaces; por lo tanto, en g-C 3 N 4 , hay diversas estructuras de enlaces de valencia. Los trabajos de investigación han iniciado que algunos C 3 N 4 estructuras defectuosas y estructuras amorfas de g-C 3 N 4 siguen siendo las estructuras metaestables, pero con el repunte de N vacantes, estos dos tipos de configuración de g-C 3 N 4 el material generalmente disminuye en módulo de volumen. Las características estructurales, la composición de los materiales y la cristalinidad de g-C 3 N 4 se puede caracterizar y evaluar mediante técnicas XRD, XPS y Raman. En 1830, Berzelius describió la fórmula general (C 3 N 3 H) ny Liebig también idearon la notación “melón”, y estas predicciones llevaron a más investigación centrada en oligómeros y polímeros de nitruro de carbono [19, 20]. Además, estas estructuras cristalinas se han encontrado y declarado en experimentos [21, 22, 23]. El α-C 3 N 4 fue encontrado anteriormente por Yu y colaboradores [24]. Una estructura 2D cargada similar al grafito del grafito C 3 N 4 generalmente se observa como una estructura de grafito sustituida con heteroátomos de nitrógeno que incluye principalmente planos grafíticos conjugados con p, y es con sp 2 hibridación de átomos de carbono y nitrógeno. El grafito cristalino es un 3% menos denso que el g-C 3 N 4 . Cambiar la localización de los electrones y luego consolidar los enlaces que se encuentran entre las capas debido a la sustitución del heteroátomo de nitrógeno puede ayudar a aclarar la distancia entre capas de g-C 3 N 4 [25].
Estructura electrónica y propiedades de g-C 3 N 4
Actualmente, el g-C3N4 se considera un fotocatalizador de nueva generación para recuperar la actividad fotocatalítica de fotocatalizadores tradicionales como TiO 2 , ZnO y WO3. Se supone que g-C3N4 tiene una estructura similar al grafito [26, 27, 28, 29, 30]. El método de policondensación térmica se usa generalmente para preparar g-C3N4 y, por lo tanto, para investigar la estructura electrónica de g-C3N4.
El α-C 3 N 4 fue encontrado anteriormente por Yu y colaboradores [24]. Estos científicos utilizaron el procedimiento de cálculo del modelo de clústeres de mecánica cuántica y desarrollaron α-C 3 N 4 mediante la optimización de la estructura electrónica de g-C 3 N 4 para fotocatálisis y otros. En la estructura de alpha-C 3 N 4 , Átomos de C y N unidos por sp 3 La clave fue utilizar el diseño de la estructura tetraedro de g-C3N4. Liu y Cohen anticiparon la existencia de beta-C 3 N 4 mediante concepto de banda de primeros principios y preparado beta-C 3 N 4 basado en β -Si 3 N 4 estructura electrónica. Liu y Cohen luego revelaron que la estructura de β -C 3 N 4 era hexagonal y abarcaba 14 átomos por cada celda unitaria.
La destacada predicción anticipada por Liu y Cohen en 1989 de que el b-polimorfo C 3 N 4 tendría valores de dureza excepcionalmente altos en comparación con el diamante, ha entusiasmado la investigación científica hasta la fecha [26]. En 1993, C 3 N 4 películas delgadas mediante la inhalación de magnetrón de un objetivo de grafito sobre sustratos de Si (100) y Zr policristalino bajo un ambiente de nitrógeno puro y consideración de la estructura de C 3 N 4 con microscopía electrónica analítica y espectroscopía Raman fueron sintetizados por Chen y sus coautores [27, 31]. Los científicos, Teter y Hemley [28], predijeron que alfa-C 3 N 4 , beta-C 3 N 4 , cubic-C 3 N 4 , pseudocúbico-C 3 N 4 y grafito C 3 N 4 muestran una dureza pronunciada que se acerca a la del diamante en su experimento que realizaron 3 años después, como ya se describió de acuerdo con los cálculos del primer principio de la estabilidad relativa, la estructura y las propiedades físicas de los polimorfos de nitruro de carbono.
Wang y colaboradores [26, 32] aplicaron búsquedas de estructuras de algoritmos evolutivos ab initio para calcular la estructura precisa de g-C3N4 preparada por métodos de policondensación térmica y síntesis de fusión de sal para una fotocatálisis mejorada sensible a la luz visible. La estructura más estable 1-3 se predijo para g-C3N4 basado en heptazina. El orden de estabilidad de fase fue 1> 2> 3. A diferencia de otras estructuras en capas, las fases distorsionadas en g-C3N4 basado en heptazina (ver Fig. 3) fueron las más estables. Esta estructura contribuye a la actividad fotocatalítica mejorada de la promesa. En g-C3N4, los electrones de un par solitario de nitrógeno son principalmente responsables de la estructura de la banda y el desarrollo de la banda de valencia.
Preparación de partículas de nanopartículas de nitruro de carbono grafítico
Síntesis
La interesante naturaleza tribológica y electrónica de los nitruros de carbono grafíticos permite desarrollar un método para depositar capas de nitruros de carbono grafíticos de forma controlada; por tanto, se puede obtener nitruro de grafeno. Considerablemente, la partícula de referencia para la comparación es el voluminoso g-C3N4. Esta partícula se puede lograr mejor mediante la selección de precursores ricos en nitrógeno sin enlace C-C directo, como cianamida, diciandiamida, melamina, tiourea, urea o mezclas a través de varios métodos preparativos (Tablas 1, 2 y 3), para condensación térmica instantánea [33]. Los materiales de nitruro de carbono son en su mayoría recursos a granel con una pequeña superficie, por lo general menos de 10 m 2 g −1 cuando se preparan o sintetizan por condensación directa de los precursores orgánicos que contienen nitrógeno [34].
La estructura mesoporosa, cuando se mineraliza y el área de superficie específica se amplifica, ayuda a afinar las propiedades fisicoquímicas y luego aumenta el rendimiento fotocatalítico del nitruro de carbono de grafito (g-C 3 N 4 ). La nanocolada / replicación de matrices de sílice mesoporosa es el primer método utilizado para preparar nitruro de carbono de grafito (g-C 3 N 4 ), eran famosos por su cohorte de nanoestructuras de carbono correspondientes [35]. Luego se realizaron grandes esfuerzos para desarrollar esquemas más innovadores para g-C 3 N 4 modificación, que fue entusiasmada por el método de plantilla dura (Tabla 1). Liu y Cohen luego descubrieron la (Tabla 1) técnica de plantilla blanda [26], y la otra g-C 3 N 4 También se descubrieron esquemas de modificación como la impregnación en solución ácida, el método de dispersión ultrasónica y la funcionalización química [26]. Estos métodos, como se describió anteriormente, fueron buenos signos del principio de modificación de las propiedades químicas de la superficie y la textura de g-C 3 N 4 , solo con sus potenciales electrónicos.
Los tratamientos térmicos, como la deposición física de vapor (PVD) [36], la deposición química de vapor (CVD) [37], el método solvotermal [38] y la reacción en estado sólido [38], se utilizan para polimerizar abundantes cantidades de nitrógeno y oxígeno. -precursores de compuestos libres que comprenden estructuras centrales de C – N previamente unidas (derivados de triazina y heptazina), y estos sirven como técnicas básicas para el nitruro de carbono de grafito (gC 3 N 4 ) síntesis. Los precursores comúnmente utilizados para la preparación de nitruro de carbono de grafito (g-C 3 N 4 ) mediante polimerización incluyen cianamida [39], diciandiamida [40], melamina [41], urea [42], tiourea [43], cloruro de guanidinio [44] y tiocianato de guanidina [45]. El uso de elementos logrados directamente es realmente un desafío en muchas áreas; esto se debe a la débil dispersión y la naturaleza ordinaria del g-C 3 a granel N 4 . El uso de amplias micro / nanoestructuras y morfologías para preparar diferentes tipos de g-C 3 N 4 ha sido intensamente investigado por científicos durante los últimos años de estudios de fotocatálisis. Por ejemplo, ultradelgado g-C 3 N 4 nanohojas que se prepararon exfoliando g-C 3 a granel N 4 Los materiales [46,47,48] tenían carga negativa y podían dispersarse bien en agua.
La exfoliación por oxidación térmica, la exfoliación ultrasónica y la exfoliación química son bien conocidos como los principales métodos de exfoliación utilizados para preparar g-C 3 N 4 materiales. Meso-g-C 3 N 4 Los materiales tienen un gran rendimiento, como una gran actividad fotocatalítica debido a su mayor superficie específica (hasta 830 m 2 g −1 ) y mayor porosidad (hasta 1,25 cm 3 g −1 ); Además, el mayor número de sitios activos presentes en la superficie y una mayor selectividad de tamaño o forma mejora sus excelentes resultados. Las vías más esenciales para la preparación de meso-g-C 3 N 4 incluyen métodos de plantillas blandas (autoensamblaje) [49, 50] y plantillas duras (nano-fundición) [51] (Tabla 1 y Fig. 4). Tamaños más pequeños, conocidos popularmente como g-C 3 N 4 puntos cuánticos (QD), fueron utilizados por muchos grandes científicos de investigación en sus investigaciones para la síntesis de g-C 3 N 4 [52,53,54,55]. Dos enfoques principales para sintetizar 2D g-C 3 N 4 nanohojas son delaminación de capas de g-C 3 N 4 sólidos en nanohojas independientes, principalmente conocida como estrategia de arriba hacia abajo (Fig. 5) y el ensamblaje anisotrópico de moléculas orgánicas en una forma 2D (Fig. 6), también llamada estrategia de abajo hacia arriba. [56] Sorprendentemente para la estructura química diversa y la estructura de banda electrónica de las nanohojas de CN, las nanohojas de CN preparadas revelaron una respuesta de emisión de electroquimioluminiscencia (ECL) única a numerosos iones metálicos. Debido a esto, ha habido un desarrollo exitoso del sensor ECL con detección rápida de numerosos iones metálicos.

Imágenes TEM de TCN ( a y b ) y MCN ( c y d ) utilizando un enfoque de plantillas estrictas. Reproducido con permiso de [120]. Copyright 2015. Elsevier
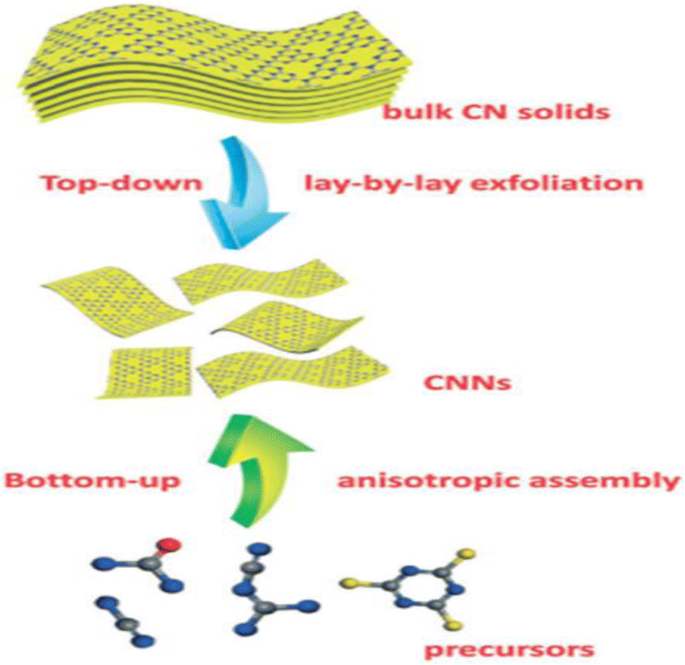
Ilustración esquemática de la síntesis de CNN mediante el uso de estrategias de arriba hacia abajo y de abajo hacia arriba (reproducida de la referencia [121] con permiso de la Royal Society of Chemistry)
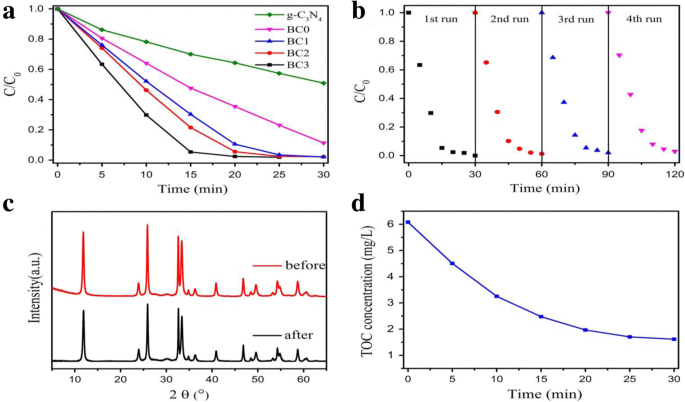
Diagrama esquemático de la preparación y fotocatalizador de luz visible mejorado por la disminución de RhB por diferentes fotocatalizadores en función del tiempo de irradiación de luz visible (carga de fotocatalizadores, 0,5 g / L; concentración inicial de RhB, aproximadamente 10 mg / L, sin modulación de pH). Los fotocatalizadores utilizados fueron g-C3N4 puro y a serie de híbridos g-C3N4 / BiOCl, b degradación cíclica de RhB sobre BC3, c Patrones XRD de fotocatalizadores BC3 antes y después del proceso fotocatalítico, y d gráficos de TOC versus tiempo de degradación. (Reproducido de la ref. [122] con permiso de Springer-Verlag GmbH Alemania 2017)
Técnicas utilizadas en la preparación de nanopartículas de nitruro de carbono grafítico
El estudio sobre la síntesis de nitruro de carbono (g-C 3 N 4 y CN x ) ha despertado la curiosidad de investigadores de todo el mundo. g-C 3 N 4 y se han sintetizado películas con propiedades fotocatalíticas precisas [57, 58]. La condensación térmica, la solvotermia, la deposición química en fase de vapor, la polimerización asistida por microondas y la síntesis hidrotermal abordadas son métodos (Cuadro 2) que se han utilizado eficazmente en la preparación de nitruro de carbono para diferentes propósitos y análisis en el área de fotocatálisis y otros [9 ].
Métodos de tratamiento térmico y solvotermal
Basándose en la reacción de policondensación entre melamina y cloruro cianúrico en presencia de polvo de níquel, Li y el equipo de investigación [41] propusieron dos métodos principales para la síntesis de nitruros de carbono grafíticos ricos en nitrógeno. Estos dos métodos fueron métodos solvotermales usando benceno como solvente y vía de reacción sólida libre de solvente con tratamiento térmico (Fig. 7). Otros trabajos de muchos científicos [59, 60, 61, 62, 63] sugirieron que las reacciones solvotermales suelen producir cristalino después del lavado y secado, y no requieren tratamiento posterior al recocido. Estos científicos también propusieron actividades fotocatalíticas mejoradas con este método (Fig. 8).

Imágenes SEM de la muestra B:( a ) partículas de alúmina recubiertas de nitruro de carbono; ( b ) detalle de las hendiduras salientes de nitruro de carbono. Es posible observar la forma irregular de las láminas de nitruro de carbono obtenidas por pirólisis. Imágenes SEM de la muestra A:( c ) y ( d ) vistas de partículas de alúmina recubiertas con nitruro de carbono. Reproducido de [60]

Imágenes TEM y un patrón de difracción de electrones de mp-C3N4 después de la eliminación de las nanopartículas de sílice. Reproducido con autorización [123]. Copyright John Wiley &Sons Inc., 2006
Niu y compañía también informó de los cambios morfológicos cuando se utilizó la técnica solvotermal [64]. Loumagne et al. [65] testificaron las posesiones fisicoquímicas de los depósitos a base de SiC, obtenidos mediante la descomposición térmica de CH3SiCl3 en hidrógeno. Kelly y el grupo [66] informaron de la síntesis de TaC mediante el uso de reactivos cloruro de tantalio (V) y carbono mezclados en una caja de guantes llena de argón a través del proceso térmico. Sucesivamente, el método de condensación térmica, que consiste principalmente en un sistema de heptazina aromática conjugada con características de ensamblaje grafítico, se ha utilizado varios momentos para preparar g-C 3 N 4 [36]. El uso de la técnica solvotermal para g-C 3 N 4 La síntesis tiene grandes remuneraciones, como la formación de partículas finas y uniformes, un bajo consumo de energía y una mayor viabilidad económica en comparación con el anticuado método de condensación térmica. Por el contrario, estos métodos todavía requieren mucho tiempo, y en cierta medida requieren unas pocas horas para completar la formación y cristalización de las partículas.
Deposición de vapor químico
La investigación de Roberto y colaboradores [60] sugirió que el uso de la deposición química en fase de vapor (CVD) para la síntesis de nitruro de carbono grafítico mediante la reacción entre la melamina y el ácido úrico tiene una alta actividad fotocatalítica. Se encontró que el nitruro de carbono grafítico formado tenía una estructura basada en bloques de heptazina.
Roberto y sus colaboradores propusieron entonces que la naturaleza de estos nitruros de carbono revelaba una forma irregular (Fig. 7), cristalinidad y una textura nanométrica. Kelly y col. [66] ha informado de la síntesis de TaC mediante el uso de reactivos cloruro de tantalio (V) y carbono mezclados en una caja de guantes llena de argón mediante una técnica térmica y luego transformados en nanopartículas de TaC mediante una técnica química. La CVD es uno de los métodos más útiles para preparar grafeno monocapa de alta calidad estructural para su uso en diferentes dispositivos para actividades catalíticas [67]. Wang y el grupo [26, 32] obtuvieron películas de CN 푥 sobre sustrato de Ni utilizando el método HFCVD en primer lugar. Debido a que es más probable que la preparación de estas películas produzca enlaces C – H y N – H en las condiciones de CVD, la mayoría de las películas CN 푥 son amorfas. De estudios anteriores, los procedimientos de CVD se utilizan para preparar nitruros de carbono, la elección de los materiales del sustrato es muy crítica para ser considerada. Se pueden preparar muestras de áreas grandes exponiendo un metal a diferentes precursores de hidrocarburos a altas temperaturas. Hay diferentes tipos de métodos de CVD disponibles, como CVD realzado por plasma, CVD térmico y CVD de pared caliente / fría. Los métodos de CVD consisten principalmente en resonancia de ciclotrón de electrones, descarga luminiscente de CC asistida por filamento caliente, descarga de radiofrecuencia y deposición de vapor químico por plasma de microondas. El sesgo de la deposición de vapor químico de filamento caliente auxiliar (HFCVD) es una de las herramientas locales utilizadas en la deposición de películas de diamante y otras. El mecanismo exacto de formación de grafeno depende del sustrato de crecimiento, pero normalmente se inicia con el crecimiento de átomos de carbono que se nuclean en el metal después de la descomposición de los hidrocarburos, y los núcleos crecen luego en grandes dominios [68]. Recientemente, el grafeno monocapa de alta calidad producido mediante el uso de CVD de pared fría de calentamiento resistivo también fue 100 veces más rápido que el CVD convencional.
Síntesis de sol-gel
La técnica sintética sol-gel es un proceso mediante el cual se forma un producto sólido o un nanomaterial a partir de una solución después de la transformación del gel intermedio. En este método de síntesis, los reactivos se mezclan a nivel molecular permitiendo reacciones rápidas y conducen a productos más homogéneos con mayor área de superficie. Sorprendentemente, esta técnica se ha utilizado para sintetizar diferentes tipos de nanopartículas, incluidos los procesos de carburo metálico y nitruro para fotocatálisis [69]. La síntesis de nitruro metálico mediante procesos sol-gel se remonta al uso de compuestos organometálicos (sintetizados a partir de elementos metálicos y dialquilamina) [70].
Calefacción por microondas
En los últimos tiempos, el calentamiento por microondas se ha utilizado ampliamente para la preparación de productos químicos y farmacéuticos finos en comparación con los métodos descritos anteriormente, porque permite un rango de reacción completo y un tiempo de reacción corto, que son apropiados para la producción a escala industrial [71]. Wang y sus colaboradores adoptaron una técnica simple para sintetizar g-C 3 N 4 utilizando un precursor rico en nitrógeno barato / menos costoso que luego puede ser activo como fotocatalizador para la generación de H 2 y O 2 bajo irradiación de luz visible para su investigación. La radiación de microondas acelera la reacción química y disminuye la energía consumida, penetrando consecuentemente en el recipiente de reacción y haciendo disponible energía abiertamente a los reactivos y al solvente con una gran tasa de transferencia de calor. La técnica de calentamiento por microondas es diferente a las técnicas tradicionales como los baños de aceite y las cámaras de calentamiento; este método es más efectivo y confiable. Radiación de microondas, con respecto al sistema de reacción cerrado y presurizado solvotérmicamente por calor, los reactivos pueden reaccionar y transformarse en productos mucho más rápidamente que usando el método convencional. Dai y sus compañeros de trabajo propusieron un proceso económico y que ahorra tiempo para la síntesis de g-C 3 N 4 utilizando polimerización asistida por microondas recientemente. Dai y sus compañeros de trabajo descubrieron que el g-C 3 N 4 muestra lograda, mostrando submicrosferas y una alta superficie de 90 m 2 g −1 , (Fig. 9) y se sintetizó con éxito a 180 ° C en condiciones de irradiación de microondas durante solo 30 minutos, lo que reveló un rendimiento fotocatalítico mejorado [71]. Los experimentos realizados por Hu y sus compañeros de trabajo también revelaron que el g-C 3 sintetizado por microondas N 4 tiene una buena estabilidad química y térmica y una fuerte intensidad de emisión que las del convencional [71]. Hu y sus colaboradores también afirmaron que el microondas sintetizaba g-C 3 N 4 se desempeñó mejor en fotocatálisis sensible a la luz visible.
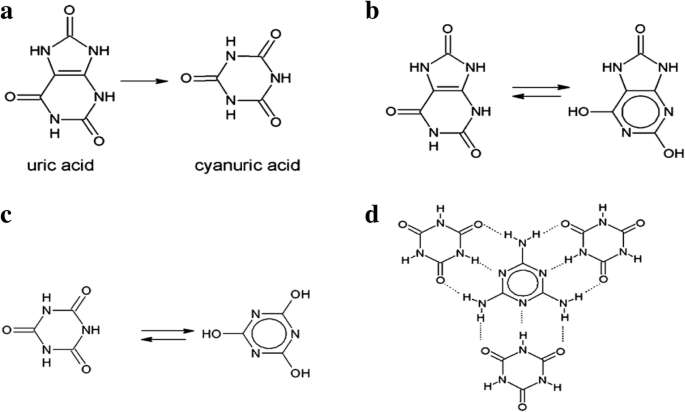
( a ) Descomposición térmica del ácido úrico en ácido cianúrico; ( b ) tautómeros de ácido úrico; ( c ) tautómeros de ácido cianúrico; ( d ) representación esquemática de un fragmento de capa del aducto llamado cianurato de melamina
Deposición física de vapor
Consiste en la pulverización catódica con magnetrón, la deposición por haz de iones (IBD), la pulverización catódica por reacción y la deposición por láser pulsado, etc. La pulverización catódica de reacción es el método elemental para la preparación de materiales compuestos. Cuando se usa esta técnica para preparar g-C 3 N 4 , la fracción másica de nitrógeno suele ser inferior al 40%. Por el contrario, para formar 훽 -C 3 N 4 , el sistema debe constar de una cantidad adecuada de nitrógeno y la relación estequiométrica debe alcanzar el 57%. Niu y su grupo [72] lograron el g-C 3 N 4 sobre sustrato de silicio mediante el uso de un objetivo de evaporación por láser de pulso C, deposición auxiliar de nitrógeno atómico. Niu y col. Los estudios encontraron que la cantidad de N alcanzaba el 40% en las películas y luego los átomos de C, N combinados con un enlace covalente no polar. Sucesivamente, Sharma et al. [73] y Zhang et al. [74] también hizo algunos estudios críticos y luego obtuvo películas CN 푥 mediante un método similar al que se ha comentado. Mihailescu y colaboradores [75] también usaron amoníaco en lugar de N 2 -Fabricado películas duras de CN 푥 con enlaces simples, dobles y triples de carbono-nitrógeno y luego descubrió que su banda prohibida óptica es de 4,5 eV. A partir del estudio reciente, lo que los científicos obtienen con frecuencia son películas de mezcla que comprenden varias fases cristalinas.
Considerar la eficacia de g-C 3 preparado N 4 , Takanabe y su grupo propusieron el desprendimiento de hidrógeno fotocatalítico utilizando nitruros de carbono cristalinos (CN) [76]. Takanabe y col. adquirieron nitruros de carbono mediante agregación supramolecular (Tabla 3) que se controló adicionalmente mediante (Tabla 3) policondensación de fusión iónica (IMP) usando melamina y 2, 4, 6-triaminopirimidina como dopante. Hay otros pocos métodos similares a los que Takanabe y su grupo usaron en su experimento, consulte la Tabla 3.
Aplicaciones del nitruro de carbono grafítico
Hay varias aplicaciones emergentes de este nitruro de carbono grafítico y tales aplicaciones incluyen detección basada, aplicaciones biomédicas, tratamiento de aguas residuales y ambiental, utilización de energía solar y uso en la fabricación de dispositivos.
Utilización de energía solar
Incrementar la actividad sensible visible del nitruro de carbono no solo depende del control de las estructuras moleculares, síntesis y técnicas de preparación de CN, sino que también depende de la capacidad de alterar las estructuras electrónicas de estos materiales. Por lo general, bajo irradiaciones de luz visible, los nitruros de carbono se pueden usar para producir fotoelectrodos y, por lo tanto, generar fotocorriente. Esta habilidad de g-C 3 N 4 se debe a la excepcional naturaleza reversible de protonación y desprotonación. Uno de los mejores enfoques es el uso de combustible solar a partir de CO 2 y agua (producida por la mayoría de los fotocatalizadores) para producir H 2 , hidrocarburos y gas de síntesis para energía y otros [77, 78]. Se propuso que g-C 3 N 4 tiene el potencial de ser fotocatalizadores escalables y libres de metales para uso en luz visible según la estructura, síntesis y técnica de preparación aplicada. Un trabajo reciente de Liu y su equipo [79] ha sugerido un desarrollo novedoso del método de creación de plantillas de sacrificio para formular g-C 3 mesoporoso N 4 esferas y un esquema de alto rendimiento. Esta técnica propuesta se puede utilizar para sintetizar g-C 3 N 4 varillas, y esto es mejor para la regeneración de NADH (Fig. 10a-c) para la producción exitosa de energía y otros.
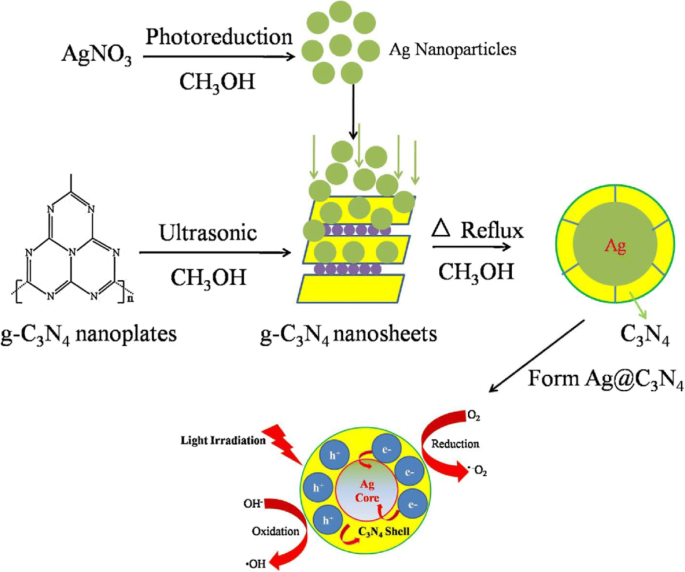
Dibujo esquemático que ilustra la ruta sintética (método de plantilla) y el mecanismo de separación de carga y el proceso fotocatalítico sobre fotocatalizadores C3N4 y Ag @ C3N4 bajo irradiación de luz. Reproducido con autorización [124]. Copyright 2014 Elsevier.
Tratamiento de aguas residuales y medioambiental
La mayoría de los procesos industriales petroquímicos, petroquímicos, textiles y alimentarios provocan contaminación en el medio ambiente, para ser precisos, los cuerpos de agua [80]. En la producción de textiles, materiales fotográficos y materiales de impresión, se utilizan tintes orgánicos y estos tintes se filtran en la mayor parte del medio acuático durante el proceso de teñido [81]. A pesar del impacto nocivo de estos tintes en la salud humana y animal, su degradación biológica y química es un desafío [82, 83]. Debido a esta amenaza, existe la necesidad de desarrollar un proceso de oxidación superior para el tratamiento de agua potable contaminada y materiales no degradables [84, 85]. La mayoría de las investigaciones [86,87,88,89,90] han demostrado que el uso de semiconductores como g-C 3 N 4 para fotocatálisis es el mejor método para el tratamiento de aguas residuales y el medio ambiente debido a su naturaleza menos nociva [86,87,88,89,90]. g-C 3 N 4 es más conocido por ser los fotocatalizadores potenciales para la degradación de numerosos contaminantes [16, 90, 91], con los potenciales fotofísicos del nitruro original alterados por dopaje con heteroátomos, formación de heterouniones con otros materiales y mejoras de textura para expandir la superficie y la porosidad . La estructura, síntesis y técnicas de preparación de g-C 3 N 4 Las nanohojas también determinan la eficiencia del fotocatalizador y su aplicación en relación con el tratamiento de aguas residuales. Ultrafino g-C 3 N 4 nanohojas derivadas de g-C a granel 3 N 4 por exfoliación en metanol revelan una mayor actividad fotocatalítica (Fig. 11) para la degradación del azul de metileno (MB) [92]. Sintetizar y preparar el candidato mediante el dopado de metales como Cu y Fe [93,94,95, 96] y no metales como B, C, O o S [97,98,99,100], y el codopaje [ 101,102,103] ha sido ampliamente utilizado por muchos científicos para el tratamiento del agua y el medio ambiente. Una solución prometedora para la descontaminación ambiental [104,105,106] es la combinación de metales nobles y g-C 3 N 4 [107,108,109,110,111,112].
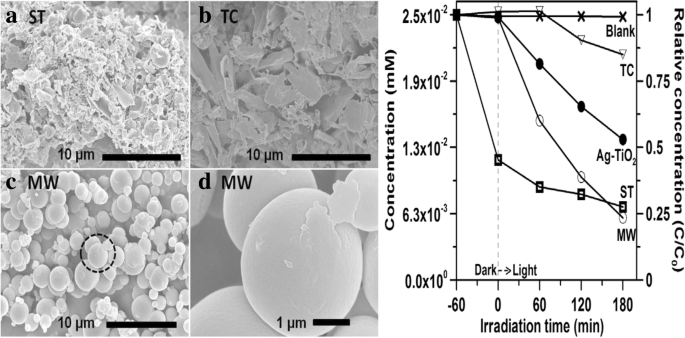
Imágenes SEM de (a) ST, (b) condensación térmica (TC) y (c) muestras de síntesis asistida por microondas (MW); (d) aumento de la muestra de MW; Degradación fotocatalítica de la solución de MO sobre muestras de MW, ST, TC C3N4 y Ag-TiO2 irradiadas con luz visible. En el experimento, se realizó una prueba en blanco en la que se irradió la solución sin añadir catalizador. Reproducido con autorización [125]. Copyright 2017 Elsevier
En resumen, las aplicaciones inviables en las aguas residuales y la contaminación ambiental de la mayoría de los fotocatalizadores mejor versados se deben a algunos de sus disuasivos deméritos, que incluyen, alto costo, pequeña escala, poca actividad fotocatalítica y reciclaje que invita a la reflexión. Razonablemente, en el área de remediación ambiental, g-C 3 N 4 , TiO 2 -, y nanomaterial a base de ZnO exhiben las aplicaciones más prometedoras como resultado de su bajo costo, alta actividad fotocatalítica y ninguna segunda contaminación en el medio ambiente [3].
Aplicaciones biomédicas y de detección
Para aumentar la capacidad de g-C 3 N 4 para el uso de detección, bioterapia y bioimagen, existe la necesidad de alterar la estructura molecular, mejorando así la manipulación del material en el agua. Debido a la fotoluminiscencia de luz, muy recomendable para uso relacionado con la biología, g-C 3 N 4 El nanomaterial es un candidato muy esencial para aplicaciones biomédicas y de detección. La aplicación de g-C 3 N 4 para la detección, la bioterapia y la bioimagen considera principalmente su estructura, síntesis y mecanismos preparativos. Zhang y colaboradores [53] propusieron que las nanohojas ultrafinas de g-C3N4 podrían usarse como biomarcadores para el etiquetado de las membranas celulares. g-C 3 N 4 Lin y compañía también han sugerido. para ser fotosensibilizadores potenciales y nanoportadores de fármacos sensibles al pH para la obtención de imágenes y la terapia del cáncer.
Perspectivas futuras
A partir de la discusión, la investigación futura del nanocompuesto g-C3N4 puede enfocarse en sintetizar la innovadora partícula nano-basada g-C3N4 que responda al monitoreo de la morfología, evaluando la practicidad y eficacia de la fotocatálisis de la síntesis tradicional y las estrategias preparativas de g- Nano compuesto C3N4, y luego explorando las aplicaciones de diversas nanopartículas g-C3N4 en el tratamiento de aguas residuales comerciales, su aplicación efectiva en la utilización de energía solar, tratamiento ambiental, aplicaciones biomédicas y de detección mediante la evaluación completa de su capacidad fotocatalítica, costo y energía. consumo y reutilización.
Conclusiones
En conclusión, esta mini revisión culmina los avances actuales en la estructura y técnicas de preparación de g-C 3 con cuerpo N 4 material de base nano. Comprensiblemente, g-C 3 N 4 ha demostrado ser uno de los mejores competidores adecuados para diseñar y ensamblar fotocatalizadores compuestos innovadores. Por lo tanto, hay poca incertidumbre de que el avance masivo de g-C 3 N 4 Las nanopartículas de base durarán para desarrollarse en un futuro próximo. En vista de eso, también se necesitan más estudios para hacer un uso completo de las excepcionales propiedades estructurales, de síntesis, y de las técnicas de preparación de g-C 3 N 4 partícula de base nano.
Abreviaturas
- g-C 3 N 4 :
-
Nitruro de carbono de grafito
- TiO 2 :
-
Óxido de titanio
- ZnO:
-
Óxido de zinc
Nanomateriales
- Las 10 principales propiedades del aluminio y sus aplicaciones
- Óxido de hafnio y su estructura y aplicaciones
- Las propiedades de los compuestos de resina y fibra y por qué son beneficiosos
- ¿Cuáles son las aplicaciones y propiedades del acero al manganeso?
- Preparación y propiedades magnéticas de nanopartículas de espinela de FeMn2O4 dopadas con cobalto
- Presentación de la estructura atómica y electrónica de las nanofibras de carbono de copa apilada
- Hacia los nanofluidos de TiO2:Parte 1:Preparación y propiedades
- Compuestos de grafeno y polímeros para aplicaciones de supercapacitores:una revisión
- Influencia del agua en la estructura y propiedades dieléctricas de la microcristalina y nanocelulosa
- La preparación de la nanoestructura yema-cáscara de Au @ TiO2 y sus aplicaciones para la degradación y detección del azul de metileno
- Preparación y rendimiento fotocatalítico de fotocatalizadores LiNb3O8 de estructura hueca



