Peculiaridades estructurales de los compuestos poliméricos orgánicos-inorgánicos conductores de iones a base de resina epoxi alifática y sal de perclorato de litio
Resumen
El artículo se refiere a polímeros híbridos amorfos sintetizados basándose en oligómero epoxi de éster alifático diglicida de polietilenglicol que fue curado por polietilen poliamina y sal de perclorato de litio. Las peculiaridades estructurales de los compuestos poliméricos orgánicos-inorgánicos se estudiaron mediante calorimetría diferencial de barrido, espectros de rayos X de gran angular, espectroscopía infrarroja, microscopía electrónica de barrido, análisis elemental y microscopía óptica reflectante y de transmisión. Por un lado, los resultados mostraron que la introducción de LiClO 4 la sal en polímero epoxi conduce a la formación de complejos coordinativos de metal-polímero de tipo donante-aceptor entre el centro Li + ion y ligando. Por otro lado, también se encontró la aparición de microinclusiones amorfas, probablemente de naturaleza inorgánica.
Antecedentes
Los electrolitos líquidos se utilizan comúnmente en baterías de litio o de iones de litio a temperatura ambiente con una conductividad iónica de 10 −3 a 10 −2 S / cm [1, 2].
Sería útil que las baterías pudieran funcionar a temperaturas más altas, ya que no será necesario utilizar un circuito de refrigeración independiente a nivel del sistema, o tal necesidad se reducirá significativamente [3]. Sin embargo, las altas temperaturas crean dificultades debido a la rápida degradación de los electrolitos líquidos [3]. Además, existen dos problemas principales que dificultan el desarrollo de electrolitos líquidos. En primer lugar, la formación de dendritas de litio en los electrodos conlleva un peligro grave debido a la posibilidad potencial de cortocircuitos internos. En segundo lugar, la inestabilidad electroquímica de los electrodos de litio provoca un ciclo de vida insignificante de las baterías durante los procesos repetidos de carga / descarga [4].
Además, la primera generación de prototipos de baterías, que utilizaba electrolitos líquidos, tiene un alto riesgo de fugas que afecten a la fiabilidad de un dispositivo [1]. La seguridad es uno de los problemas más urgentes relacionados con el mayor progreso en el desarrollo de las baterías de próxima generación. Eso hace que los electrolitos sólidos sean uno de los candidatos más prometedores para el reemplazo de electrolitos líquidos inflamables y potencialmente peligrosos [5].
Los electrolitos de polímero sólido (SPE) se han utilizado en diferentes aplicaciones como conductores de iones en varios dispositivos electroquímicos como baterías de litio, ultracondensadores, pilas de combustible y células solares [6]. Las baterías recargables de litio y de iones de litio desempeñan un papel importante en el mercado de los dispositivos de almacenamiento de energía electroquímica, ya que se utilizan ampliamente para la carga de dispositivos electrónicos portátiles y para dispositivos de control autónomos [2]. Por lo tanto, recientemente, el desarrollo de nuevos electrolitos de polímeros sólidos fue un objetivo importante, ya que aún no se ha logrado el equilibrio óptimo entre la alta conductividad iónica y las condiciones tecnológicas del material [7, 8]. Los SPE tienen propiedades tales como buena compatibilidad con electrodos, baja tasa de autodescarga, fácil procesamiento para varias formas y tamaños, falta de fugas, flexibilidad y autosuficiencia para cambios de forma durante los ciclos de carga y descarga [7,8,9,10 ].
El óxido de polietileno (PEO) [11, 12] es uno de los oligómeros más estudiados, que se utilizan para la creación de SPE debido a la coordinación eficaz de los iones metálicos en él debido a la distancia y orientación óptimas de los átomos de oxígeno del éter en sus cadenas moleculares [ 12]. La desventaja del PEO es la estructura cristalina amorfa [4, 13, 14] que conduce a la conductividad a través del área amorfa de un polímero solo [11, 15] por encima de la temperatura de transición vítrea T g [6, 12, 16] y, como resultado, el PEO tiene una conductividad iónica baja a temperatura ambiente debido a la presencia de una fase cristalina alta [4, 14, 17].
Hoy en día, por regla general, los electrolitos poliméricos sólidos incluyen sales inorgánicas que se disuelven en oligómeros que, a su vez, forman una matriz sólida con la conductividad iónica [10, 12, 18, 19]. La sal añadida sirve como fuente de iones y contribuye a su movimiento a lo largo de las cadenas del polímero, de modo que desempeña un papel crucial en el transporte de iones en los electrolitos del polímero [16]. Por lo tanto, la concentración y la movilidad de los iones son parámetros importantes que afectan la conductividad en los electrolitos del polímero [14, 17]. La comprensión del mecanismo del transporte de iones en un polímero requiere el estudio de las interacciones ion-ion e ion-polímero que es de gran interés [10, 14]. Se han realizado muchos estudios del transporte de iones en electrolitos de polímeros utilizando varios tipos de cationes como Na + , Li + , Ag + y Mg + [20]. Sin embargo, preferentemente se estudian los composites basados en sales de litio, porque el Li + Los cationes son los más pequeños y pueden moverse fácilmente en una matriz de polímero [17, 20]. Otra característica importante es la estabilidad térmica de los iones y su inercia para los componentes de la celda [21].
Se puede lograr una alta conductividad iónica aumentando la concentración de sal en el polímero [6]; sin embargo, los autores [9] han demostrado que la conductividad de los compuestos basados en PEO está limitada por cierto valor de la concentración de sal. A mayor concentración de sal, la conductividad disminuye debido a la formación de complejos iónicos, lo que, a su vez, provoca la reducción de la movilidad iónica y el número de portadores de carga [10].
Para su aplicación como electrolitos, los polímeros deben tener ciertas propiedades, como amorfo, presencia de éter oxígeno en su estructura, baja temperatura de transición vítrea, alta estabilidad dimensional, resistencia mecánica y capacidad para formar películas delgadas [9, 18]. Uno de los materiales adecuados que satisface estos requisitos es el oligómero epoxi alifático, a saber, el éster alifático diglicida de polietilenglicol. Tiene una estructura de cadena idéntica a la del óxido de polietileno, sin embargo, es amorfa y es capaz de disolver la alta concentración de sal de perclorato de litio de manera similar a la PEO.
Por tanto, el objetivo del presente trabajo es la síntesis de compuestos poliméricos sólidos amorfos basados en oligómeros epoxi alifáticos y el estudio de la influencia de las sales de perclorato de litio en su estructura.
Métodos
Materiales y síntesis
El oligómero epoxi (éster alifático diglicida de polietilenglicol (DEG-1)) y perclorato de litio (LiClO 4 ) sal se utilizaron para la síntesis de compuestos poliméricos epoxi conductores de iones. Estos componentes fueron previamente presecados al vacío a 80 ° C durante 24 h. Después de secar, la sal se disolvió en el oligómero DEG-1. Soluciones de DEG-1-LiClO 4 se prepararon con LiClO 4 contenido de 0 a 50 phr de DEG-1. Se ha utilizado un endurecedor de 10 phr de polietilen poliamina (PEPA) como agente de curado para la síntesis de los compuestos.
Las características térmicas se estudiaron mediante calorimetría diferencial de barrido (DSC) con TA Instruments DSC Q2000 en el rango de temperatura de -70 a +150 ° C con una velocidad de calentamiento de 10 ° C / min. Temperatura de transición vítrea ( T g ) se determinó a partir de las curvas de DSC en el segundo calentamiento. El error experimental de determinación de las temperaturas de transición vítrea fue de ± 1 ° C.
Las características eléctricas y dieléctricas fueron investigadas por el analizador dieléctrico de banda ancha “Novocontrol Alpha” con Novocontrol Quatro Cryosystem (Novocontrol Technologies, Montabaur, Alemania) que estaba equipado con un circuito de dos electrodos, en el rango de frecuencia de 10 −1 a 10 7 Hz y el rango de temperatura de −60 a +200 ° C. La tensión aplicada a una muestra fue igual a 0,5 V. Las muestras de ensayo tenían un diámetro de 20 mm y un espesor de 0,5 mm y fueron recubiertas previamente con una capa de aluminio al vacío. Los datos obtenidos se analizaron mediante el software “Novocontrol WinDeta 3.8”.
La organización estructural y las características del ordenamiento macromolecular de los sistemas poliméricos sintetizados se investigaron mediante espectros de rayos X de gran angular (WAXS) utilizando el difractómetro de rayos X DRON-4.7. El esquema óptico de rayos X se realizó mediante el método Debye-Scherer al pasar el rayo primario a través del polímero de muestra de polímero usando CuK α emisión ( λ =1,54 Å) que se hizo monocromático mediante un filtro de Ni. Las investigaciones se llevaron a cabo mediante escaneo automático por pasos en el rango de ángulos de dispersión (2 θ ) de 2,6 ° a 40 °, y el tiempo de exposición fue de 5 s.
Se han realizado estudios espectroscópicos de infrarrojos (IR) utilizando un espectrómetro con transformación de Fourier “Tensor-37” de Bruker Corp. en el rango de números de onda 600 ° -3800 ° cm −1 . Según el pasaporte del dispositivo, el error de medición relativo es <2%.
Las características morfológicas de los compuestos sintetizados se estudiaron utilizando el método de microscopía óptica reflectante (ROM) por microscopio de polarización Unicorn NJF 120A en ángulos de polarización de 0 ° a 90 °. El análisis de microfotografías se realizó utilizando el software Carl Zeiss Imaging Solutions AxioVision V4.7.1.
Las características estructurales de los compuestos sintetizados se han estudiado utilizando métodos de microscopía electrónica (SEM) por microscopio electrónico de transmisión JEOL 100-CX II, equipado con sistema de barrido. El análisis elemental de las inclusiones se realizó utilizando un complejo analítico que consta de un microscopio electrónico de barrido JEOL JSM-35CF y un espectrómetro de rayos X con cuantos de rayos X de energía dispersiva (Modelo INCA Energy-350 de “Oxford Instruments”). Una característica importante de este análisis con microsonda electrónica es su ubicación:el tamaño máximo del área de excitación es de 2 μm. De acuerdo con las características morfológicas y la composición química en base al análisis espectral de dispersión de energía, se ha realizado la separación automática de inclusiones por tipos (composición elemental) y medición de sus tamaños. Los resultados se analizaron utilizando un programa especial para la distribución de fases cuantitativas y la investigación de inclusión. Todos los resultados se presentan en porcentaje en peso. El error experimental fue del 0,1%.
Los estudios WAXS, IR, ROM y SEM y el análisis elemental se llevaron a cabo a la temperatura T =20 ± 2 ° C.
Resultados y discusión
El análisis de los estudios de DSC, así como de las investigaciones dieléctricas y eléctricas de los compuestos sintetizados con un contenido de sal de perclorato de litio de 0 a 20 phr, se presentó previamente en nuestro artículo [22]. Ampliación adicional de LiClO 4 el contenido (de 0 a 50 phr) mantiene un aumento lineal de la temperatura de transición vítrea T g de −10 a 64 ° C (Fig. 1a). Eso puede ser el resultado de interacciones electrostáticas entre cationes de litio Li + y la cadena macromolecular de DEG-1 con formación de complejos coordinativos, que se acompañan de desplazamiento de la densidad electrónica de los átomos de oxígeno y su polarización parcial. Se refleja en una reducción sustancial de la movilidad segmentaria de las cadenas DEG-1 dentro de los complejos formados que se muestra en el aumento de la temperatura de transición vítrea de la matriz del polímero.
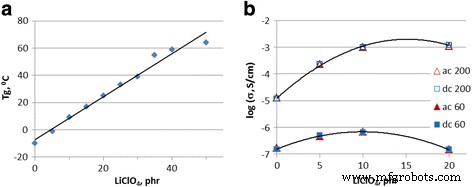
Características térmicas y eléctricas de los composites. un Dependencia de la temperatura de transición vítrea T g ( a ) y conductividad σ a 60 y 200 ° C ( b ) en LiClO 4 contenido de sal
La figura 1b muestra el cambio de conductividad σ con crecimiento de LiClO 4 contenido en compuesto. A baja temperatura (60 ° C), el valor máximo de σ se alcanza a 10 phr de sal y el σ valor de compuesto con 20 phr de LiClO 4 es igual a eso en DEG-1 puro. A alta temperatura (200 ° C), el σ los valores son tres órdenes de magnitud más altos con un máximo de 15 phr de LiClO 4 . Tal carácter de dependencia de la conductividad de LiClO 4 El contenido puede explicarse por la existencia de dos procesos competitivos opuestos. En primer lugar, el aumento del contenido de sal en el material compuesto aumenta el número de portadores y aumenta la conductividad. En segundo lugar, el crecimiento de T g refleja la restricción de los movimientos moleculares de DEG-1 que reduce la movilidad de los portadores. A temperaturas más altas, el aumento de los movimientos moleculares compensa este mecanismo y la conductividad se vuelve esencialmente más alta.
El análisis de los patrones de difracción de rayos X de gran angular de los sistemas ha demostrado que todos ellos son amorfos (Fig. 2). El valor medio del período ( d ) de un orden molecular de corto alcance de segmentos moleculares internodales DEG-1 / PEPA ubicados en el volumen del polímero se puede calcular usando la ecuación de Bragg:
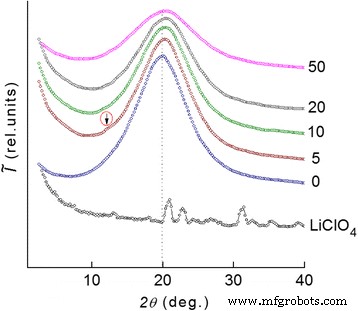
Los estudios WAXS del DEG-1 / LiClO 4 sistemas. Los patrones de difracción de rayos X de gran angular de una sal de perclorato de litio LiClO 4 y sistemas con diferentes contenidos de sal (mostrados cerca de las curvas)
$$ d =l {\ left (2 \ sin {\ theta} _m \ right)} ^ {- 1} $$donde λ es la longitud de onda de la emisión característica de rayos X ( λ =1,54 Å para CuK α emisión) y equivale a 4,44 Å.
Sin embargo, la introducción de LiClO 4 la sal que tiene una estructura cristalina en la resina epoxi va acompañada de cambios en el patrón de difracción. Eso se evidencia por la presencia de un pico de difracción sutil del tipo difuso en 2 θ m ≈ 12,2 ° en el fondo del halo amorfo, que es similar a la posición angular del DEG-1 en 2 θ m ≈ 20,0 ° ( d ≈ 4,39 Å). Este pico de difracción caracteriza la existencia de complejos metal-polímero del tipo donante-aceptor, en nuestro caso, entre iones centrales (Li + ) y el oxígeno del éter de las cadenas epoxi en el volumen intermolecular de la resina epoxi, y esto confirma las suposiciones hechas por el análisis de los datos de DSC. Basado en la posición angular de este pico de difracción en compuesto con 50 phr de LiClO 4 , la distancia media de Bragg d entre las cadenas moleculares coordinadas por los cationes Li + es 4,30 Å.
La estructura de los compuestos poliméricos se ha investigado mediante espectroscopía infrarroja. Las principales bandas de absorción de LiClO 4 , DEG-1 y PEPA con los grupos relevantes se presentan en la Tabla 1. Estas bandas de absorción se interpretaron de acuerdo con [23,24,25], respectivamente.
Como se puede ver, las bandas de absorción características del anillo de epoxis están ausentes en los espectros (Fig. 3, 0 phr LiClO 4 contenido) que indica el curado completo del componente epoxi. Estas bandas de absorción también están ausentes en los espectros de IR (Fig. 3, 5-50 phr) de los composites curados. Las bandas de absorción en el rango de números de onda 1300-1520 y 1000-1190 cm −1 , que corresponden respectivamente a las fluctuaciones de –CH 2 - y los grupos (C – O – C y C – NC), se expanden y cambian a la región de baja frecuencia con LiClO 4 aumento de contenido. Se sabe que esto puede estar asociado con la formación de enlaces de coordinación entre Li + cationes y ClO 4 - aniones y cadenas poliméricas [26, 27]. Generalmente se acepta que Li + Los cationes pueden formar fácilmente complejos con enlaces de éter de polietileno [23, 24, 27,28,29,30], así como con poliaminas [31]. La banda de absorción a 1637 cm −1 en el espectro IR de LiClO 4 indica su estado no disociado (Tabla 1) [23, 24]. Cabe señalar que esta banda en los espectros de infrarrojos de 5-50 muestras está ausente. Esto indica que la forma pura (no disociada) de LiClO 4 en los compuestos no está contenido. De acuerdo con esto, en la Fig.4 las posibles interacciones ion-dipolo de Li + ion con el enlace éter del fragmento de óxido de polietileno y el grupo OH del anillo epoxi descrito de DEG-1 (Fig. 4a-d) y con el grupo amina secundaria de PEPA (Fig. 4e), con el grupo amina secundaria o terciaria y el enlace éter simultáneamente (Fig. 4e-g), se muestran. Como ejemplo de ClO 4 coordinado - ion, la Fig. 4h representa el esquema de esta interacción aniónica con un átomo de carbono cargado positivamente que se encuentra cerca del átomo de oxígeno electronegativo.
Los espectros de infrarrojos de los compuestos. La espectroscopia infrarroja de los sistemas con los diferentes contenidos de sal de perclorato de litio (los números cerca de las curvas)

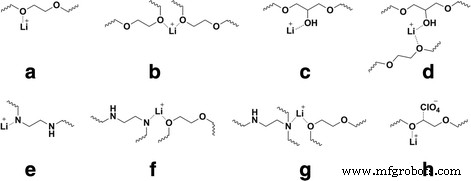
un - h Esquemas de complejos. Complejos que posiblemente existan en los sistemas LiClO 4 / DEG-1 / PEPA
Cabe señalar que en la muestra con adición de perclorato de litio 5 phr y después de la solidificación, una nueva banda de absorción a 864 cm −1 aparece en su espectro IR, que mantiene en las muestras un contenido de sal de 10–50 phr. Teniendo en cuenta que la mayoría de las bandas de absorción de los complejos metálicos se encuentran en la región de baja frecuencia [32], es obvio que esta banda de absorción está asociada a complejos que involucran LiClO 4 . La interacción de PEO y LiClO 4 se estudia ampliamente en la literatura y en los materiales presentados, la banda de absorción alrededor de 860 cm −1 está ausente [23, 24, 27, 28, 29, 30]. Probablemente, esta banda se refiere a la formación de un complejo amino de litio, cuya presencia influye en las fluctuaciones de los grupos metileno ubicados en las cercanías. Esto se confirma con la aparición de una nueva banda de absorción en el espectro IR del compuesto con 5 phr de LiClO 4 a 1525 cm −1 (Fig. 3), que se desplaza a la región de baja frecuencia con el aumento del contenido de sal hasta 50 phr. De acuerdo con [26], esto se debe al creciente número de enlaces de coordinación. Es importante tener en cuenta que cuando se toman muestras de película con 5–50 phr de LiClO 4 se trituraron en un polvo y se moldearon en las tabletas de KBr, las bandas de absorción descritas en ≤1525 y 860–864 cm −1 desapareció, ya que el aplastamiento conduce a la destrucción de los débiles enlaces de coordinación. Eso también confirma la naturaleza de coordinación de estas bandas. Como ejemplo, la Fig. 5 muestra los espectros de IR de las muestras con 5 y 30 phr de LiClO 4 contenido.
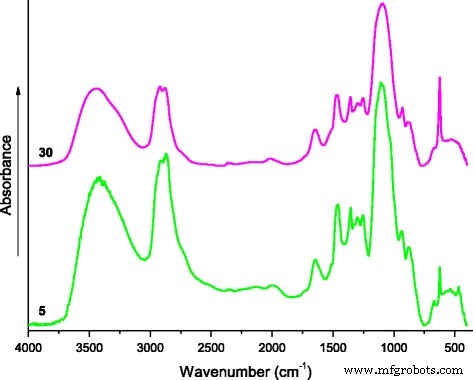
Los espectros de IR (en tabletas de KBr). Los espectros de IR de los compuestos con diferentes LiClO 4 contenido (marcado con números cerca de las curvas)
Generalmente, la cantidad creciente de LiClO 4 conduce al aumento de los enlaces de coordinación, que reducen la movilidad de las cadenas macromoleculares [28]. La Figura 3 muestra una disminución gradual en la intensidad de las bandas de absorción asociadas con las fluctuaciones de valencia de OH–, NH– y –CH 2 - grupos. En la destrucción de los enlaces de coordinación en las muestras moldeadas en las tabletas de KBr, estos enlaces de valencia se manifiestan claramente (Fig. 5).
Además de los enlaces de coordinación, deben indicarse otros factores importantes que influyen en la estructura de los composites obtenidos. Por tanto, la reacción entre DEG-1 y PEPA en presencia de LiClO 4 ocurre más completamente, aparentemente (hasta un cierto límite de sal), ya que se sabe que LiClO 4 es un catalizador de aminólisis eficaz del anillo de oxiranos [33]. Otro factor de formación de estructura se puede realizar como una red de enlaces de hidrógeno, incluidos los que tienen la participación de ClO 4 - iones [30].
En nuestro caso, los complejos de Li + Los iones con número máximo de coordinación 2 se presentan en la Fig. 4, pero el número de coordinación de iones puede llegar a 8 [31]. Debido al pequeño radio (0,6 A), el Li + Los iones son altamente móviles, por lo que pueden crear y destruir los complejos fácilmente [29, 31], y debido a eso, es difícil definir una estructura compleja que involucre la sal de perclorato de litio que se formó durante la reacción de curado.
La Figura 6 presenta las micrografías de microscopios ópticos reflectantes de los compuestos sintetizados con diferente contenido de sal de perclorato de litio. Se observó la formación de estructuras ordenadas en los compuestos con la adición de la sal al sistema. En este caso, la microscopía óptica reflectante utilizada en modo polarizado reveló la presencia de las inclusiones distribuidas, probablemente, de naturaleza inorgánica con tamaños que oscilan entre 2 y 20 μm. Con el fin de confirmar la presencia de inclusiones en los compuestos, se llevó a cabo la investigación estructural que utilizó microscopía electrónica de barrido. Los resultados se presentan en la Fig. 7. Se puede ver la presencia de las inclusiones observadas por ROM (para las muestras con algo de LiClO 4 contenido) y el aumento de su número y tamaño con el aumento de LiClO 4 contenido en los compuestos. Para determinar la naturaleza de las inclusiones encontradas, el análisis elemental de nueve áreas diferentes de la superficie del compuesto con 50 phr LiClO 4 se ha cumplido (Fig. 8). La distribución de masa normalizada de elementos en las microáreas mostradas en la Fig. 8 se presenta en la Tabla 2. Es evidente que el contenido de elementos en los espectros es diferente. Es importante que las inclusiones identificadas por ROM (Fig.6) y SEM (Fig.7) se caractericen por la disminución del contenido de carbono y el aumento del contenido de oxígeno y cloro, que entran en la composición de LiClO 4 (espectros 3-5), en comparación con los espectros de la matriz polimérica (espectros 7-9). Eso se puede explicar por la agregación de átomos de oxígeno y cloro y, quizás, también por la agregación de átomos de litio (sin embargo, fue imposible determinar dicha agregación con las investigaciones realizadas) a partir de las sales de perclorato de litio disueltas en DEG-1 durante su síntesis. La presencia de varios átomos de carbono (incluso en el espectro 3-5 de las inclusiones) puede explicarse por la superposición de su alto contenido en cadenas macromoleculares de matriz polimérica que pueden cubrir parcialmente las inclusiones.

Resultados de microscopía óptica reflectante. ROM del polímero epoxi con a 0, b 10, c 20 y d 50 phr LiClO 4 sal
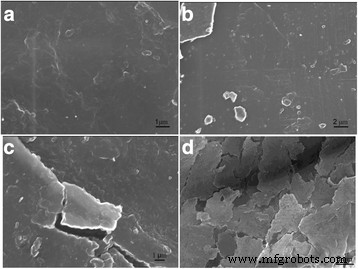
Resultados de la microscopía electrónica de barrido. SEM de los compuestos con a 0, b 10, c 20 y d 50 phr LiClO 4 sal

SEM con análisis elemental. SEM del compuesto con 50 phr LiClO 4 superficie con el nombramiento de espectros de análisis elemental
También se determinó la composición elemental de la sal de perclorato de litio inicial. Se encontró que el cloro en la sal es 41.61% wt y el oxígeno es 58,39% wt . No se pudo determinar el contenido de litio.
Mapa elemental resumen (Fig. 9d) del compuesto con 20 phr de LiClO 4 se construyó a partir de mapas elementales de elementos individuales (carbono — Fig. 9a; oxígeno — Fig. 9, b; cloro — Fig. 9c) para determinar la distribución de elementos en su superficie. Los cálculos han demostrado que el contenido de los elementos en la superficie del compuesto son los siguientes:carbono es 51,57% en peso, oxígeno es 43,79% en peso y cloro es 4,64% en peso, mientras que su distribución coincide con el orden de las inclusiones identificadas por los medios de microscopía óptica y electrónica. Esto permite concluir que la naturaleza de estas inclusiones con saturación de oxígeno y cloro es inorgánica.
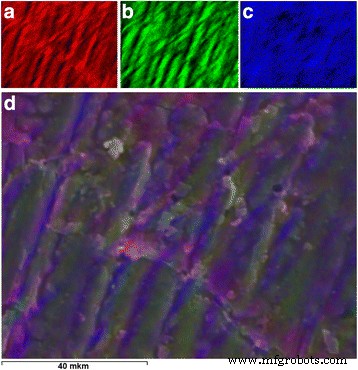
Los resultados del análisis elemental. El mapa elemental de la superficie del compuesto con 20 phr LiClO 4 : a C, b O, c Cl y el d mapa combinado
Conclusiones
El estudio integral de composites basados en oligómeros epoxi alifáticos (DEG-1) que contienen diferentes cantidades de LiClO 4 sal (0-50 phr) reveló la creación de interacciones entre los cationes de litio Li + y la cadena macromolecular de DEG-1 con formación de complejos coordinativos. Se refleja en una reducción sustancial de la movilidad segmentaria de las cadenas DEG-1 dentro de los complejos formados que aumentan linealmente la temperatura de transición vítrea T g de matriz de polímero con el contenido de sal.
Se encontró que a mayor temperatura (200 versus 60 ° C), los valores de conductividad σ son tres órdenes de magnitud más altos con un máximo de 15 phr de LiClO 4 . Tal comportamiento de conductividad se explica por la existencia de dos procesos competitivos opuestos, a saber, el crecimiento del contenido de sal en el material compuesto da lugar al aumento del número de portadores y al aumento de la conductividad. Por otro lado, la restricción de los movimientos moleculares de DEG-1 debido a la formación de los complejos coordinativos reduce la movilidad del portador. A temperaturas más altas, el aumento de los movimientos moleculares compensa este mecanismo y la conductividad se vuelve esencialmente más alta.
El estudio detallado de espectroscopia IR permitió sugerir el esquema de LiClO 4 interacción con cadenas de polímeros, es decir, las posibles interacciones ion-dipolo de Li + ion con el enlace éter del fragmento de óxido de polietileno y el grupo OH del anillo epoxi de DEG-1 descrito, con un grupo amina secundaria o un grupo amina terciaria de PEPA y un enlace éter simultáneamente.
Los resultados de estudios morfológicos y estructurales mediante microscopios ópticos y electrónicos, así como por análisis elemental, han revelado la presencia de inclusiones con tamaños desde nanómetros hasta ~ 20 μm, probablemente, de naturaleza inorgánica distribuidas en la matriz polimérica.
Abreviaturas
- DEG-1:
-
Epoxi oligómero de diglicida éster alifático de polietilenglicol
- DSC:
-
Calorimetría diferencial de barrido
- IR:
-
Infrarrojos
- LiClO 4 :
-
Sal de perclorato de litio
- PEO:
-
Óxido de polietileno
- PEPA:
-
Polietileno poliamina
- ROM:
-
Microscopía óptica reflectante
- SEM:
-
Microscopía electrónica de barrido
- SPE:
-
Electrolitos de polímero sólido
- T g :
-
Temperatura de transición vítrea
- TOM:
-
Microscopía óptica de transmisión
- CERA:
-
Espectroscopia de rayos X de gran angular
Nanomateriales
- Las propiedades de los compuestos de resina y fibra y por qué son beneficiosos
- La historia de la resina epoxi
- Carpintería y resina epoxi
- La resina epoxi como pasatiempo
- Impresione a sus amigos y familiares con proyectos de resina epoxi
- Nano y ánodo de batería:una revisión
- El aditivo PES aumenta la resistencia a la fractura y al micro-agrietamiento en compuestos epoxi
- Sino Polymer desarrolla un preimpregnado de resina epoxi de alto rendimiento
- Resina epoxi estructural T26 (cinta EP-UD)
- Resina epoxi estructural T26 (EP-PCF)
- Resina Epoxi Estructural T26 (EP-CF)



