Progreso de la investigación del hidrogel termosensible en la terapia de tumores
Resumen
En comparación con las estrategias tradicionales de terapia tumoral, el hidrogel como sistema de depósito de fármaco puede realizar la liberación de fármaco a demanda y la capacidad de penetración en los tejidos profundos. También exhibe una gran retención del sitio del tumor para mejorar la permeabilidad y el efecto de retención del tratamiento del tumor. Esto puede superar significativamente la resistencia del fármaco y los efectos secundarios graves. El hidrogel compuesto inorgánico / orgánico ha atraído una gran atención debido a sus efectos combinados, mejorando los efectos terapéuticos contra varios tipos de tumores. El hidrogel inyectable in situ puede restringir de forma segura los medicamentos en los sitios de la lesión sin fugas y garantizar una mejor bioseguridad. Además, el hidrogel posee macroporos interconectados que pueden proporcionar suficiente espacio para el transporte de nutrientes, la actividad celular y las interacciones célula-célula. La terapia térmica es una estrategia eficaz para la terapia tumoral debido a su mínima invasividad y alta selectividad. Debido a que la temperatura del lugar se puede controlar con precisión y ayuda a evitar los riesgos de destruir el sistema inmunológico del cuerpo y eliminar las células normales, la terapia térmica presenta resultados de tratamiento significativos. No obstante, cuando la temperatura celular alcanza aproximadamente los 43 ° C, provoca una inactivación celular a largo plazo. Con base en estos méritos, la formulación de hidrogel termosensible con funciones adaptativas muestra una eficacia excelente, una capacidad de penetración tisular ilimitada y pocos efectos secundarios deletéreos. Además, el hidrogel termosensible tiene propiedades físicas únicas bajo los estímulos externos, que es el sistema de administración de fármacos ideal para la liberación a demanda en el tratamiento de tumores. Este artículo revisará el estado del hidrogel termosensible en la aplicación clínica para la terapia del cáncer.
Introducción
En los últimos años, los investigadores han centrado su atención en los biomateriales 3D, ya que los macroporos reticulados proporcionan suficiente espacio para el transporte de nutrientes, la actividad celular y las interacciones célula-célula [1]. Como portadores de fármacos ideales, el hidrogel tiene una invasividad mínima. Puede formar las formas deseadas para cumplir con los requisitos de los sitios de lesión irregulares en la terapia del cáncer [2]. El hidrogel tradicional generalmente se fabrica mediante la interacción física o la unión química del polímero constituyente, lo que tiene efectos mínimos sobre su función [3]. El hidrogel como sistema de administración de fármacos debe responder a estímulos endógenos / exógenos, asegurando así la liberación del fármaco a demanda en los sitios de la lesión y reduciendo los efectos secundarios innecesarios en los tejidos normales [4]. El nanomaterial inorgánico funcional incorporado en el hidrogel puede superar significativamente los límites intrínsecos, lo que tiene otras propiedades fascinantes y mejora notablemente la eficacia terapéutica sensible a los estímulos [5,6,7].
La terapia térmica tiene las ventajas del control de la temperatura local y la mínima invasividad, que se convirtió en un enfoque terapéutico novedoso después de la quimioterapia, la radioterapia y la intervención quirúrgica en el tratamiento tumoral actual [8]. Basado en termoterapia mediada por material inorgánico de hidrogel con la característica física única bajo ciertos estímulos, es la plataforma de administración de agentes ideal para la terapia de dosis de fármaco a demanda en los sitios de la lesión [9,10,11]. En comparación con los enfoques terapéuticos sinérgicos tradicionales (quimio / radioterapia, terapia quimio / fotodinámica y terapia fotodinámica / fototérmica), hidrogel termosensible cargado con fármacos antitumorales. Esto puede ayudar a que los medicamentos penetren en los tejidos profundos, formar las formas deseadas para rellenar los tejidos irregulares y promover la cicatrización de las heridas [12]. Además, el calentamiento a temperatura leve puede mejorar los resultados de la quimioterapia al mejorar la permeabilidad de la citomembrana para aumentar la captación celular de fármacos y controlar la liberación de fármacos del hidrogel. Cuando la temperatura celular supera los 41 ° C, se produce la desnaturalización de las proteínas y la inactivación celular temporal, que dura varias horas. Cuando la temperatura alcanza aproximadamente los 43 ° C, provoca la inactivación celular a largo plazo [13]. Además, la inyección de hidrogel termosensible in situ en los sitios de la lesión puede evitar el riesgo de acumulación de fármaco en el hígado y el bazo para mejorar los resultados de la terapia y garantizar una mejor bioseguridad in vivo [14].
El beneficio del hidrogel termosensible en la clínica puede facilitar la administración, mejorar la eficacia terapéutica en la región de la lesión y reducir el daño innecesario a los tejidos normales, mejorando así el cumplimiento del paciente. Este artículo resumirá algunos hidrogeles termosensibles para mejorar el tratamiento de enfermedades y establecer el estado actual del hidrogel en la aplicación clínica.
Hidrogel de hipertermia magnética
Es bien sabido que la concentración de dopaje de nanopartículas inorgánicas en el hidrogel puede afectar inevitablemente a las propiedades intrínsecas del hidrogel, que por lo general muestra dependencia de la dosis [15]. La alta concentración de agentes potenciaría la eficacia terapéutica. Sin embargo, deteriora innecesariamente las propiedades reológicas del hidrogel, lo que da como resultado una liberación repentina, un tratamiento incontrolado y efectos secundarios graves en los tejidos normales [16].
Es un desafío fabricar un hidrogel de nanopartículas de alto rendimiento, que debería equilibrar las propiedades intrínsecas del hidrogel y asociar las funciones asociadas con el proceso de carga de nanopartículas inorgánicas. Esta contradicción es muy obvia en el diseño de hidrogel magnético en la termoquimioterapia sinérgica para un tratamiento posquirúrgico altamente eficaz [17]. Esta deficiencia se superaría eficazmente, proporcionando buenas propiedades reológicas y suficiente eficiencia de calentamiento. Esto se basa en glicol-quitosano, poli (etilenglicol) telequélico difuncional (DT-PEG) y óxido de hierro ferromagnético con dominio de vórtice (FVIO) como materias primas (Fig. 1) [18]. En comparación con el hidrogel magnético tradicional, el hidrogel magnético obtenido supera los efectos secundarios y exhibe propiedades reológicas notables y una alta capacidad de conversión de calor en un campo magnético alterno [19]. Además, este hidrogel magnético autoadaptable regula el fármaco de forma sostenible a largo plazo. Se dirige directamente a los sitios de la lesión. La hipertermia magnética puede promover la internalización de un fármaco, eventualmente provoca la apoptosis de las células cancerosas y reduce el tamaño del tumor. El hidrogel incorporado con FVIO tiene las características de autocuración, gelificación rápida y capacidad de autoconfirmación, que puede satisfacer la termoquimioterapia sinérgica y proporcionar una estrategia alternativa para abordar la necesidad clínica insatisfecha. Este trabajo subraya la promesa potencial de la precisión de los lugares de inyección. Mejora la eficacia de la hipertermia magnética para el tratamiento de tumores de xenoinjerto.
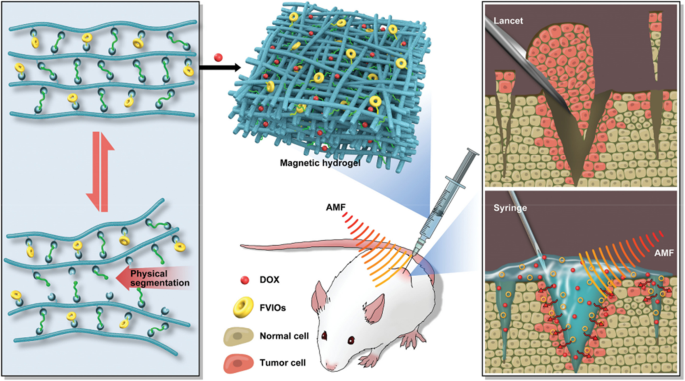
Ilustra el hidrogel magnético funcionalizado con FVIO con funciones de adaptación óptimas para la prevención de la recurrencia posoperatoria del cáncer de mama [18]. Copyright 2019 Adv. Mater de salud
Hidrogel de absorción de luz en el infrarrojo cercano
La terapia fototérmica (PTT) ha atraído una gran atención debido a sus ventajas inmejorables en el tratamiento del cáncer, incluido el tratamiento de control y los resultados satisfactorios de erradicación del cáncer [20,21,22]. Sin embargo, el PTT convencional tiene poca penetración en el sitio de las lesiones profundas, lo que trae efectos nocivos sobre la terapia. La quimioterapia y la estrategia sinérgica de PTT podrían ser un buen candidato para mejorar la eficacia terapéutica del tumor [23].
Varios materiales fototérmicos han sido ampliamente explotados como portadores de administración de fármacos o reactivos de acoplamiento para la terapia del cáncer, incluidos los armazones organometálicos y los puntos de carbono [24,25,26,27]. Entre estos materiales, los puntos poliméricos conjugados (Pdots) son biomateriales biocompatibles, degradables y no tóxicos con fácil funcionalización. Son de tamaño pequeño y propiedades fotofísicas extraordinarias [28,29,30,31]. Más importante aún, los puntos P con fuertes propiedades de absorción óptica y fotoestabilidades en la ventana de luz del infrarrojo cercano (NIR) son agentes satisfactorios para el PTT y la formación de imágenes fotoacústicas (PAI) [32,33,34]. El iohexol es un agente de contraste eficaz y seguro aprobado por la Administración de Drogas y Alimentos de los Estados Unidos para la obtención de imágenes de tomografía computarizada (TC) corporal [35]. Sin embargo, el tiempo del iohexol para la obtención de imágenes por TC es muy corto, y esta deficiencia inevitable limita el iohexol ampliamente utilizado en la clínica [26]. Rallar iohexol en hidrogel termosensible basado en Pdots-DOX puede superar con éxito esta desventaja del iohexol para mejorar la capacidad de obtención de imágenes por TC. Esto hace que el hidrogel sea un candidato excelente utilizado en la teranóstica del cáncer.
Con base en estos méritos, Men et al. introdujo una plataforma multifunción de administración de medicamentos de hidrogel Pdots @ con buena biodegradabilidad, fuerte capacidad de absorción NIR, alta eficiencia de conversión fototérmica y control de la liberación de medicamentos, capacidad de obtención de imágenes de CT / PA / fluorescencia satisfactoria y mejores resultados terapéuticos tumorales (Fig. 2) [ 36]. El sistema de hidrogel Pdots-DOX-iohexol @ mediado por luz NIR obtenido exhibe fuertes efectos fototérmicos. Logró quimioterapia de control de dosis mediante irradiación de luz NIR de intervalo, penetración tisular superior e invasión mínima en el tratamiento del cáncer, inhibiendo así el crecimiento tumoral. Más importante aún, la modalidad de nanoingeniería para el hidrogel Pdots-DOX-iohexol @ posee una excelente capacidad para obtener imágenes de CT / FL / PA y una alta biocompatibilidad para la detección del cáncer. Por lo tanto, el concepto de integrar varios agentes de diagnóstico / terapéuticos en un sistema puede potencialmente aplicarse a varias perspectivas de la terapia de enfermedades en la clínica.
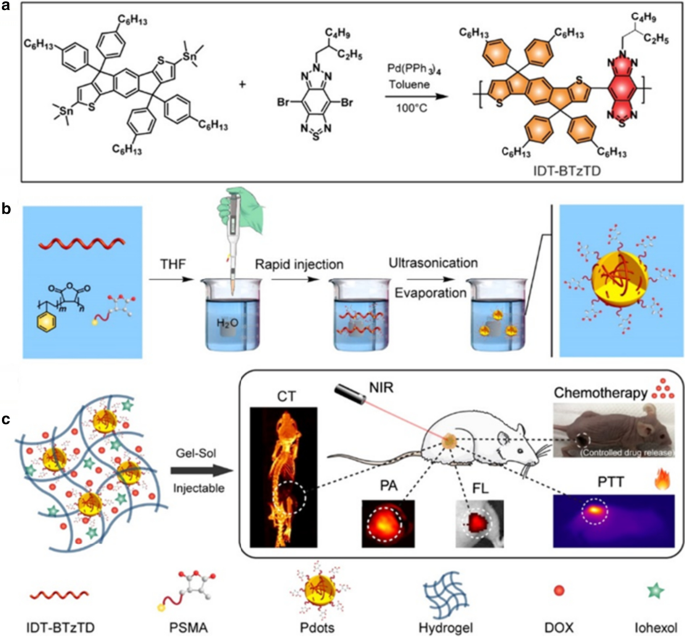
un Esquema de la fabricación de polímero conjugado IDT - BTzTD. b Esquema de la fabricación de IDT - BTzTD Pdots. b Esquema del hidrogel Pdots - DOX - iohexol @ para la terapia del cáncer quimio-fototérmica sinérgica guiada por imágenes trimodales FL / PA / CT [36]. Copyright 2020 ACS Appl. Mater. Interfaces
Hidrogel bifuncional de efectos fototérmicos
En la actualidad, el tratamiento de los tumores óseos depende principalmente de la intervención quirúrgica y los enfoques sinérgicos de quimio / radioterapia, lo que mejora significativamente la tasa de supervivencia de los pacientes [37]. Sin embargo, la intervención quirúrgica siempre provoca defectos óseos. Elimina de manera incompleta las células tumorales, lo que dificulta la curación de los tejidos óseos por sí mismos y las células cancerosas residuales proliferan en varios días. Por lo tanto, es importante desarrollar un biomaterial con terapia tumoral y, al mismo tiempo, promover la regeneración ósea después de la cirugía.
El hidrogel inyectable como un enfoque alternativo prometedor puede formar las formas deseadas para rellenar los tejidos defectuosos. Sus componentes son muy similares a los tejidos óseos para mejorar la capacidad osteogénica [38]. El hidrogel inyectable aplicado en la ingeniería de tejido óseo debe ser lo suficientemente lento para adaptarse a la manipulación quirúrgica y, al mismo tiempo, lo suficientemente rápido para lograr la estabilidad y la función después de la inyección in vivo [39]. Para resolver estos problemas, Luo y sus colaboradores proporcionaron un nuevo hidrogel inyectable bifuncional. Este hidrogel utilizó polidopamina (PDA) para modificar nanohidroxiapatita (n-HA) e inmovilizar cisplatino (DDP) para fabricar partículas de PHA-DDP. Luego se introdujeron partículas de PHA-DDP en el Schiff basándose en el sistema de reacción entre el quitosano (CS) y el alginato de sodio oxidado (OSA) (Fig. 3) [40]. La nanohidroxiapatita (n-HA) desempeñó un papel importante en la formación de hueso, que es el principal material inorgánico de los tejidos óseos y está compuesto por elementos de calcio y fósforo [41]. El PDA inspirado en el mejillón como candidato ideal para agentes fototérmicos tiene buena biocompatibilidad y biodegradabilidad y tiene abundantes grupos funcionales. El CAP inspirado en mejillones se deposita fácilmente en diversas sustancias, como la carga de fármacos antitumorales (cisplatino, DDP) a través de enlaces de hidrógeno u otras interacciones [42,43,44]. Además, n-HA se modificó en PDA para obtener n-HA decorado con PDA (PHA), mejorando la adhesión y proliferación celular [45].
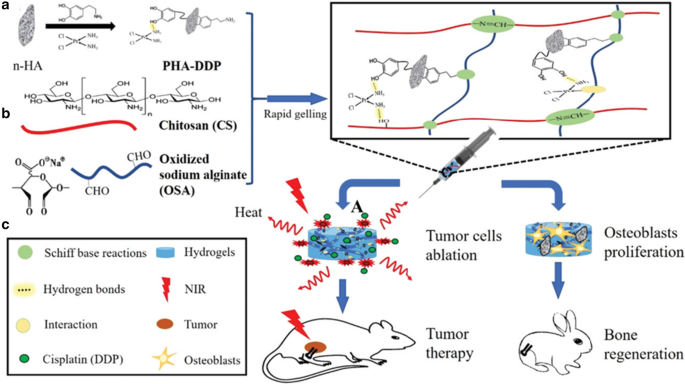
Ilustración esquemática de la formación de hidrogeles bifuncionales OSA-CS-PHA-DDP y bioaplicación [40]. Copyright 2019 Macromol. Biosci
El hidrogel inyectable OSA-CS-PHA-DDP obtenido con éxito tiene excelentes efectos fototérmicos PDA de inhibir el crecimiento tumoral a través de la hipertermia local bajo irradiación láser. Además, los efectos fototérmicos leves pueden mejorar la permeabilidad de la citomembrancia para aumentar la captación celular de fármacos antitumorales. Pueden destruir las interacciones de los enlaces de hidrógeno entre DDP y PDA para mejorar la liberación del fármaco y potenciar los efectos del tratamiento tumoral. Más importante aún, el abundante grupo funcional de PDA puede promover la proliferación y adhesión de células madre mesenquimales óseas y facilitar aún más la formación de tejido óseo nuevo. Este hidrogel bifuncional integra el tratamiento tumoral con la regeneración ósea en base a estas propiedades. Muestra un enfoque prometedor para los defectos óseos relacionados con tumores en la clínica.
Hidrogel de agarosa sensible a PTT / PDT
La vascularización del tumor tiene una estructura deficiente, lo que da como resultado un suministro de oxígeno insuficiente en las regiones tumorales. Condición de hipoxia que causa un microambiente tumoral ácido al aumentar la producción de ácido láctico a través de la glucólisis anaeróbica [46]. Por lo tanto, la hipoxia y el pH bajo son características comunes del microambiente tumoral que comprometen gravemente la eficacia terapéutica.
La terapia fototérmica destruye los tejidos tumorales basándose en la hipertermia local mediada por agentes fototérmicos bajo irradiación con láser [47]. Por lo tanto, se han desarrollado varios tipos de agentes fototérmicos para satisfacer el rendimiento de PTT [48]. Sin embargo, la mayoría de ellos todavía tienen algunos inconvenientes en la aplicación clínica, como la no degradabilidad, la baja bioseguridad y el progreso de síntesis compleja. El ácido húmico (HA) tiene una excelente capacidad de conversión fototérmica y de formación de imágenes fotoacústicas (PA), que se extrae de la humificación bioquímica de materia animal y vegetal y ha atraído una atención cada vez mayor en el PTT [49]. Mientras tanto, la terapia fotodinámica (TFD) es otra estrategia eficaz para la terapia tumoral mediante la utilización de especies reactivas al oxígeno (ROS) generadas a partir de moléculas de oxígeno en presencia de fotosensibilizadores (PS) bajo excitación láser [50]. La clorina e6 tiene un alto rendimiento de producción de ROS y una baja toxicidad en la oscuridad, que se ha utilizado ampliamente en la TFD [51]. Pero, el microambiente de hipoxia intrínseca puede comprometer los efectos terapéuticos durante el progreso de la TFD.
El hidrogel de agarosa LMP se funde a una temperatura superior a 65 ° C y la transición de sol a gel comienza a una temperatura inferior a 25 ° C durante el proceso de enfriamiento, lo que muestra un gran potencial para la administración de fármacos a demanda al regular con precisión varias temperaturas [7, 52 ]. Por lo tanto, el hidrogel de agarosa LMP funcionalizado y diseñado racionalmente es un enfoque prometedor para lograr una alta biodisponibilidad del fármaco y mejorar el resultado terapéutico a través de una sola inyección. Como se muestra en la Fig. 4, Hou et al. proporcionó un enfoque novedoso "co-atrapado" al incorporar simultáneamente SH, Ce6 y MnO 2 nanopartículas en agarosa de bajo punto de fusión (LMP) y la agarosa obtenida @ SH / MnO 2 / El hidrogel híbrido Ce6 se utilizó con éxito para mejorar la PTT / TFD mediante la mejora del entorno de hipoxia tumoral [53]. Después, se inyectó hidrogel híbrido tal como se sintetizó en las áreas tumorales, exhibiendo una excelente biocompatibilidad y biodegradabilidad, especialmente cuando se introdujo con precisión en la parte más interna. Además, MnO 2 y el Ce6 se puede impregnar continuamente en el entorno circundante suavizando e hidrolizando el hidrogel híbrido. Más importante aún, el SH como absorbente de luz convierte la luz en térmica bajo irradiación láser, por lo que el propio hidrogel se puede aplicar en PTT. Además, MnO 2 liberado del hidrogel puede catalizar el exceso de H 2 O 2 en tejidos tumorales para generar oxígeno, lo que puede mejorar los resultados de la TFD al ser expuesto a láser de 660 nm y atenuar el entorno de hipoxia tumoral. Esta agarosa multifunción @ SH / MnO 2 / El hidrogel híbrido Ce6 se inyectó en los sitios del tumor sin ingresar al sistema circulatorio, lo que ayuda a evitar un posible riesgo biológico y a ser eliminado por el sistema inmunológico del cuerpo. Por lo tanto, logra "una inyección, múltiples terapias" y nos inspira a explotar enfoques adecuados basados en hidrogel para diversas terapias de enfermedades en la clínica.
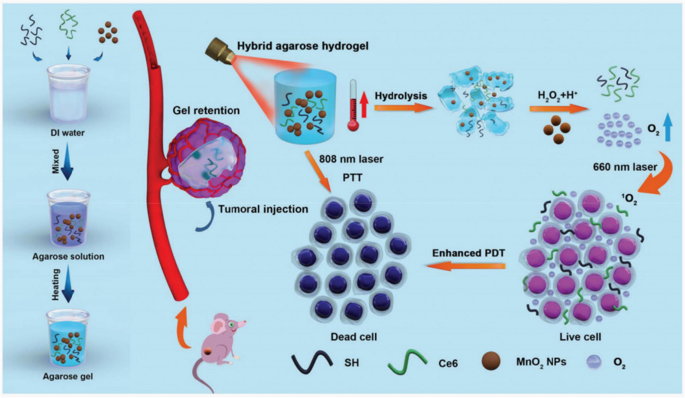
Diagrama esquemático del proceso de síntesis y principio de funcionamiento de la agarosa @ SH / MnO 2 / Hidrogel Ce6. La inhibición tumoral eficaz se logró mediante una terapia tumoral fotoinducida mejorada sobre la base del alivio de la hipoxia tumoral [53]. Copyright 2020 Biomater Sci
Perspectivas
La terapia térmica tiene las ventajas de una mínima invasividad y una alta selectividad, que es una estrategia eficaz para la terapia tumoral en la clínica [54, 55]. En comparación con los enfoques convencionales, la terapia térmica puede controlar con precisión la temperatura local y evitar eficazmente efectos secundarios innecesarios, como dañar los problemas normales y destruir el sistema inmunológico del cuerpo [56]. Cuando la temperatura de la célula alcanza los 41 ° C, la célula se vuelve temporalmente inactiva y provoca la desnaturalización de las proteínas, y esta condición dura varias horas. Cuando la temperatura llega a los 43 ° C, puede provocar la inactivación de las células a largo plazo. Aunque la terapia térmica ha logrado un progreso muy interesante en el campo de la terapia tumoral, todavía hay una falta de agentes fototérmicos o portadores de fármacos seguros y eficaces con buena biocompatibilidad y biodegradabilidad.
El hidrogel es el candidato ideal como portador de fármacos con buena biocompatibilidad y biodegradabilidad en el tratamiento actual de tumores. La incorporación de inorgánicos / orgánicos en hidrogel ha atraído una gran atención debido a sus efectos cooperativos que pueden mejorar los efectos de la terapia contra el tumor. Entre varios hidrogel sensibles, el hidrogel termosensible puede controlar de forma precisa y continua la liberación del fármaco a través del estímulo de temperatura en los tejidos tumorales. En comparación con los métodos de inyección percutánea e intravenosa, el hidrogel de administración inyectado en el lugar exacto dentro de los agentes tiene una mejor bioseguridad in vivo [57].
Conclusiones
A pesar de los importantes méritos del hidrogel, la aplicación clínica ha sido limitada debido a la biodistribución insatisfactoria, la escasa biocompatibilidad y la escasa capacidad de penetración tumoral. En este artículo, el hidrogel termosensible tiene las ventajas de una mejor biocompatibilidad, una excelente capacidad de inhibición de tumores y la ausencia de efectos secundarios innecesarios. Estos méritos promoverán aún más su aplicación en la clínica para el tratamiento de diversas enfermedades.
Disponibilidad de datos y materiales
No aplica.
Abreviaturas
- DT-PEG:
-
Polietilenglicol telequélico difuncional
- FVIO:
-
Óxido de hierro ferromagnético con dominio de vórtice (FVIO)
- PTT:
-
Terapia fototérmica
- Puntos:
-
Puntos de polímero
- NIR:
-
Infrarrojo cercano
- PAI:
-
Imágenes fotoacústicas
- CT:
-
Tomografía computarizada
- PDA:
-
Polidopamina
- N-HA:
-
Nanohidroxiapatita (n-HA)
- DDP:
-
Inmovilizar cisplatino
- CS:
-
Quitosano (CS)
- OSA:
-
Alginato de sodio oxidado
- DDP:
-
Cisplatino
- HA:
-
Ácido húmico
- HA:
-
Ácido húmico
- PDT:
-
Terapia fotodinámica
- ROS:
-
Especies reactivas al oxígeno
- PD:
-
Fotosensibilizadores
- LMP:
-
Punto de fusión bajo
- SH:
-
Humato de sodio
- Ce6:
-
Cloro e6
- MnO 2 :
-
Óxido de manganeso
Nanomateriales
- AI respalda el proyecto de investigación de iluminación inteligente
- Acelerando la detección temprana de enfermedades con nanobiotecnología
- Los investigadores de IBM se llevan el premio a la innovación en investigación de semiconductores
- El Consejo Europeo de Investigación financia la investigación de dispositivos de una sola molécula mediante la manipulación de átomos
- Nanopartículas para la terapia del cáncer:avances y desafíos actuales
- Nanorods de oro recubiertos con BSA para la terapia fototérmica NIR-II
- Adaptación de la toxicidad de las especies reactivas del oxígeno a la terapia tumoral avanzada
- Marcos metal-orgánicos sensibles al medio ambiente como sistema de administración de fármacos para la terapia tumoral
- Progreso en nanoestructuras basadas en óxidos de hierro para aplicaciones en almacenamiento de energía
- Un breve informe de progreso sobre las células solares de perovskita de alta eficiencia
- Nanopartículas de albúmina cargadas con resveratrol con circulación sanguínea prolongada y biocompatibilidad mejorada para una terapia de tumores pancreáticos dirigida altamente eficaz



