Thiacalix [4] arenes Elimina los efectos inhibidores de los cationes de Zn en la actividad de la miosina ATPasa
Resumen
Numerosas anomalías reproductivas femeninas son causadas por trastornos del músculo liso uterino (miometrio). Los metales pesados tienen un efecto adverso sobre la contractilidad del músculo liso uterino. Aunque el zinc es un elemento biogénico esencial para la mayoría de los organismos, las dosis altas de este elemento son tóxicas. El estudio de 0,5−5 mM Zn 2+ efecto sobre la actividad de la ATPasa de miosina S1 del útero encontró que 5 mM Zn 2+ Los cationes tienen el efecto inhibidor más pronunciado. El cálculo de los parámetros cinéticos ( K m y V máx , ATP ) reveló que la velocidad máxima aparente del ATP de hidrólisis catalizada por miosina en presencia de Zn 2+ 5 mM disminuyó en 1.6 veces. El valor de К m para la hidrólisis de ATP por miosina S1 en presencia de Zn 2+ no cambia estadísticamente, aunque tiende a disminuir. Se determinó que la actividad de ATPasa de miosina S1 uterina no depende de la concentración de Mg 2+ en presencia de Zn 2+ 5 mM . Además, se demostró que el tetrahidroxitiacalix [4] areno-tetrasulfosfonato (C-798) y el tetrahidroxitiacalix [4] areno-tetrafosfonato (C-800) restauraron la actividad de la miosina S1 ATPasa al nivel de control en presencia de 5 mM de Zn 2+ . Uno de los mecanismos más probables de restaurar la acción del efecto protector de estos tiacalix [4] arenos se basa en su capacidad para quelar los cationes de metales pesados del medio de incubación. El acoplamiento molecular de C-798 y C-800 en la región de miosina S1 mostró que estos tiacalix [4] arenos podrían interactuar con el enlace catiónico Zn por residuos de aminoácidos de miosina cerca del sitio activo de ATPasa. Por tanto, los tiacalix [4] arenos pueden debilitar la interacción entre este catión y la miosina S1. Se especuló que los resultados obtenidos podrían ser utilizados para futuras investigaciones con el objetivo de utilizar estos tiacalix [4] arenos como compuestos farmacológicos en el caso de intoxicaciones con altas concentraciones de zinc.
Antecedentes
Es relevante el problema de la contaminación del medio ambiente con metales pesados y la búsqueda de formas de reducir su impacto en los objetos vivos [1, 2].
El zinc es un elemento biogénico esencial para la mayoría de los organismos. [3]. Los iones de zinc forman complejos con múltiples proteínas que llevan a cabo funciones metabólicas vitales. El ion zinc es un componente de al menos 300 metaloenzimas que catalizan más de 50 reacciones bioquímicas (fisiológicas) diferentes [4, 5] .
Sin embargo, el zinc es un metal pesado. Se puede encontrar en el grupo IIb de la tabla periódica de los elementos, junto con los dos metales tóxicos cadmio y mercurio. Sin embargo, el zinc se considera relativamente no tóxico para los seres humanos [6]. Este elemento es nocivo solo en dosis excesivas [7].
El LD oral 50 para el zinc está cerca de 3 g / kg de peso corporal según la base de datos TOXNET de la Biblioteca Nacional de Medicina de EE. UU. Es más de 10 veces mayor que el cadmio y 50 veces mayor que el mercurio [6]. El exceso de la concentración normal de este microelemento en humanos es causado más comúnmente por la ingesta de medicamentos y aditivos biológicamente activos que contienen zinc redundante en su composición. Se registró como casos individuales de intoxicación con zinc como resultado de ingerir alimentos almacenados en recipientes recubiertos de zinc o completamente de zinc. El óxido de zinc, el cloruro y el sulfato de zinc se se utilizan ampliamente en la industria para la producción de vidrio; en la fabricación de fibras artificiales, pinturas de zinc, cerámicas, fósforos y cemento dental; en la industria de la pulpa y el papel, para la conservación de la madera y para el estañado y la soldadura.
Una alta concentración de zinc altera la respuesta inmunitaria [8]. Los niveles elevados de Zn, Al, Cu y Fe en el cerebro pueden facilitar el desarrollo o la progresión de la enfermedad de Alzheimer según algunos estudios epidemiológicos [9, 10].
Los metales pesados pueden afectar la reproducción femenina en diferentes etapas como el inicio de la vida fetal, el desarrollo temprano y la maduración. Los cationes de metales pesados también pueden ser la causa de subfertilidad, infertilidad, retraso del crecimiento intrauterino, abortos espontáneos, malformaciones, defectos de nacimiento, muerte posnatal, envejecimiento prematuro y trastornos del aprendizaje y la conducta [11, 12].
La función contráctil uterina está asociada con la actividad del complejo proteico (actomiosina) en el que la miosina exhibe actividad enzimática, es decir, la capacidad de hidrolizar ATP. La miosina ATPasa localizada en el dominio catalítico del subfragmento-1 (S1 o cabeza) transforma la energía química depositada en los enlaces macroérgicos de ATP en movimiento mecánico. Como resultado, la miosina se mueve a lo largo del filamento de actina, provocando la contracción muscular. Por tanto, la hidrólisis de ATP catalizada por miosina se considera uno de los procesos esenciales en el mecanismo molecular de la función miometrial [13, 14].
El subfragmento 1 de miosina es una parte N-terminal de la cadena pesada de miosina que consta de dos dominios:el dominio motor globular N-terminal (catalítico) que contiene el sitio de ATP-asa y el sitio de unión de actina, y el dominio regulador, o brazo de palanca responsable del movimiento de la miosina a lo largo de los filamentos de actina. El núcleo del dominio motor de la miosina está formado por una hoja β central de siete hebras que está rodeada por hélices α. Un gran dominio estructural que representa seis de las siete hebras de la hoja β central generalmente se denomina dominio superior de 50 kDa (U50). Una gran hendidura separa el dominio superior de 50 kDa del dominio estructural inferior de 50 kDa bien definido (L50) que está formado por residuos de aminoácidos de 465 a 590. La región de unión de actina y el sitio de unión de nucleótidos de la miosina están en lados opuestos de la hoja β de siete hebras con el resto fosfato del nucleótido en la parte posterior del bolsillo de unión al nucleótido. El lazo P, el interruptor 1 y el interruptor 2 están ubicados en el dominio superior de 50 kDa cerca del vértice de la hendidura grande. Los tres motivos de unión a nucleótidos entran en contacto con la fracción fosfato del nucleótido en la parte posterior del bolsillo de unión a nucleótidos y actúan como sensores de γ-fosfato [15].
En nuestros estudios anteriores se descubrió que los cationes de metales pesados inhibían la actividad de la miosina ATPasa del músculo liso uterino [16, 17] que puede afectar negativamente las propiedades contráctiles del miometrio.
El impacto adverso de los metales pesados sobre la contractilidad uterina requiere el desarrollo de sustancias farmacológicas que puedan eliminar estos efectos nocivos.
Los calixarenos han atraído actualmente la atención de los investigadores como posibles efectores artificiales de diferentes procesos bioquímicos. Estos compuestos son oligómeros fenólicos macrocíclicos sintéticos que tienen una estructura en forma de copa. Sus bordes superior e inferior se pueden funcionalizar con varios sustituyentes químicos. Los arenos de Calix [4] están formados por cuatro fragmentos de arenos funcionalizados y se caracterizan por una conformación de macrociclo bastante flexible. Calix [4] arenos mostró una baja toxicidad de la matriz y la capacidad de penetrar en las células. Por tanto, estos compuestos se consideran agentes prometedores para el desarrollo de nuevos fármacos eficaces [18, 19].
Una clase prometedora de tales sustancias son los tiacalixarenos [18] solubles en agua que poseen los grupos metálicos complejantes en la plataforma molecular macrocíclica. Los calixarenos, debido a su capacidad para formar complejos supramoleculares con cationes (bio) metálicos, también se han utilizado en la investigación biomédica como extractores de metales pesados [20,21,22].
Hemos demostrado anteriormente que el tetrahidroxitiacalix [4] areno-tetrasulfonato (С-798) eliminó los efectos inhibidores de Pb 2+ , Cd 2+ y Ni 2+ sobre la hidrólisis de ATP catalizada por la miosina S1 del miometrio porcino [23].
Este estudio tuvo como objetivo investigar el efecto de altas concentraciones de cationes de zinc y su acción conjunta con tetrahidroxi-tiacalix [4] areno-tetrasulfonato (С-798) y tetrahidroxi-tiacalix [4] areno-tetrafosfonato (C-800) sobre la miosina Actividad de la ATPasa S1 del útero. Este estudio fue necesario para probar la capacidad de estos tiacalixarenos para eliminar los efectos adversos de las altas concentraciones de zinc sobre la actividad enzimática de la miosina uterina.
Los tiacalix [4] arenos C-798 y C-800 consisten en una copa formada por cuatro fragmentos fenólicos modificados en el borde superior con cuatro grupos sulfonato aniónico y cuatro fosfonato, respectivamente. Ambos tiacalix [4] arenos tienen grupos hidroxilo y átomos de azufre bivalentes densamente ubicados en el borde inferior, lo que les permite quelar metales pesados con la formación de complejos metálicos estables [21] (Fig. 1).
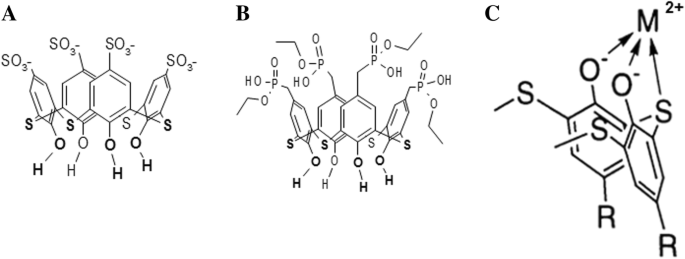
La estructura química del tetrahidroxitiacalix [4] areno-tetrasulfonato (C-798) ( a ), tetrahidroxitiacalix [4] areno-tetrafosfonato (C-800) ( b ), y el esquema del complejo quelante del tiacalixareno con catión metálico en el borde inferior (posición invertida) ( c )
Este trabajo es el resultado de un proyecto conjunto del Instituto Palladin de Bioquímica y el Instituto de Química Orgánica de NAS de Ucrania centrado en la interacción de la miosina ATPasa del miometrio con calix [4] arenos que son inhibidores o activadores (efectores) de la miosina ATPasa uterina.
Resultados
Dependencia de la actividad de la ATPasa de miosina S1 en Zn 2+ Concentración
Se encontró que el efecto inhibidor más pronunciado sobre la actividad de la ATPasa de miosina S1 del útero fue de 5 mM (43 ± 8%, M ± SD) para los cationes Zn. El rango de concentración de Zn 2+ era 0,5-5 mM en el medio de incubación (que contenía ATP 3 mM, Mg 2+ 5 mM y 0,01 mM Ca 2+ ). El cien por ciento es el valor de la actividad ATPasa sin la adición de cationes Zn (control) (Fig. 2). Por lo tanto, los efectos adversos de los cationes Zn sobre la hidrólisis de ATP de miosina S1 se estudiaron más a fondo con 5 mM de Zn 2+ .
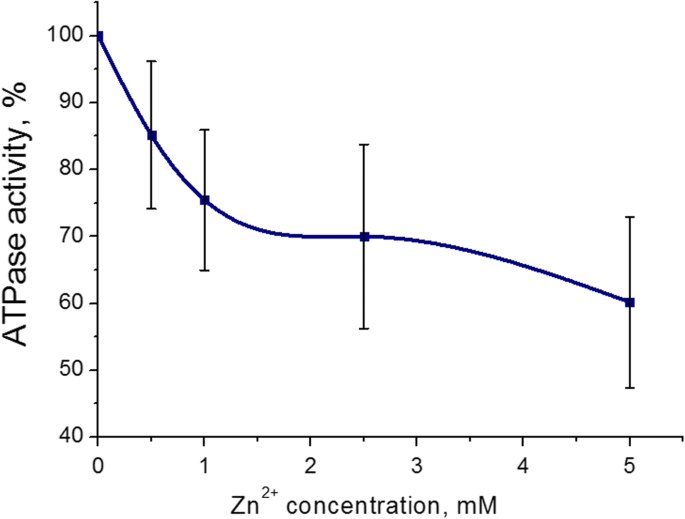
Actividad de ATPasa de miosina S1 del miometrio en presencia de concentraciones de cationes Zn de 0,5 a 5,0 mM (M ± SD, n =6). El 100% es el valor de la actividad de la ATPasa sin la adición de cationes Zn
Dependencia de la actividad de la ATPasa de miosina S1 de la concentración de ATP en presencia 5 mM Zn 2+
El Zn 2+ Se investigó el efecto sobre la afinidad de la actividad ATPasa de miosina S1 a su sustrato (ATP). Aumentar la concentración de ATP en el medio de incubación de 0,5 a 5 mM a un MgCl 2 fijo concentración (5 mM) tanto en el control como en presencia de Zn 2+ 5 mM dio como resultado un gráfico en forma de cúpula con un valor máximo de actividad de ATPasa a 3 mM de ATP. El valor de la actividad enzimática en este pico en presencia de zinc fue un 30% menor que el del control (Fig. 3). Los gráficos de la dependencia de la actividad ATPasa de miosina S1 de la concentración de ATP en el control y la presencia de Zn 2+ 5 mM en la parte ascendente se linealizaron según el método Lineweaver-Burk [27]. El cálculo de los parámetros cinéticos es decir, la constante imaginaria de Michaelis ( K m ) y la tasa máxima de ATPasa de miosina S1 para ATP ( V máx., ATP ) reveló que V máx., ATP de la actividad enzimática de la miosina en presencia de Zn 2+ 5 mM disminuyó 1,6 veces (38 ± 7 y 22 ± 6 nmol Pi / min por 1 mg de proteína en el control y la presencia de Zn 2+ respectivamente, n =5). El valor de К m para la hidrólisis de ATP por miosina S1 no cambia estadísticamente, aunque tiende a disminuir (0,49 ± 0,15 mM en el control, 0,38 ± 0,12 mM en presencia de Zn 2+ ; M ± SD; n =5).
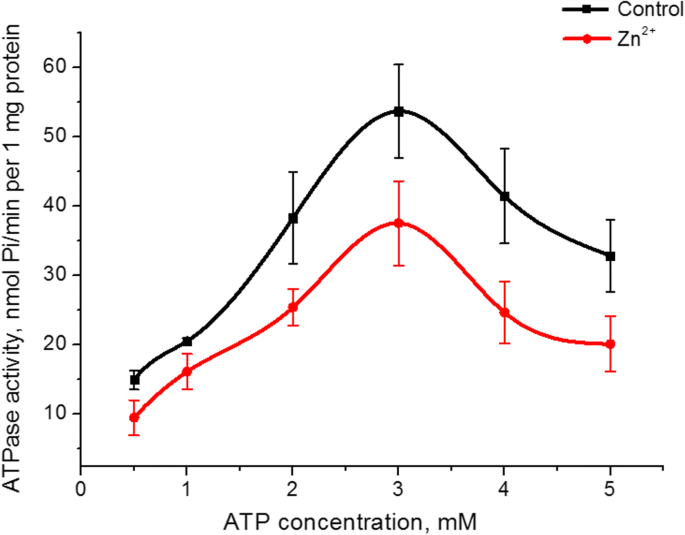
La influencia de ATP 0,5 a 5 mM en la actividad ATPasa de miosina S1 del útero en presencia de Zn 2+ 5 mM en comparación con un control (M ± SD, n =5)
Dependencia de la actividad de la ATPasa de miosina S1 en Mg 2+ Concentración en presencia 5 mM Zn 2+
El efecto de 5 mM Zn 2+ en Mg 2+ Se estudió la dependencia de la concentración de la actividad ATPasa de la miosina uterina. Aumentando el Mg 2+ concentración en el medio de incubación de 0,5 a 5 mM a una concentración fija de ATP (3 mM) en presencia de Zn 2+ 5 mM no da como resultado un cambio de la actividad ATPasa de miosina S1. Al mismo tiempo, el Mg 2+ Se detectó dependencia de la concentración de la actividad de ATPasa en el control (en las condiciones estándar). El nivel más alto de hidrólisis de ATP de miosina en el control se logró a 3 mM de Mg 2+ (Figura 4). Por lo tanto, la actividad de la enzima miosina S1 del útero no depende de la concentración de Mg 2+ en presencia de altas concentraciones de Zn (5 mM).
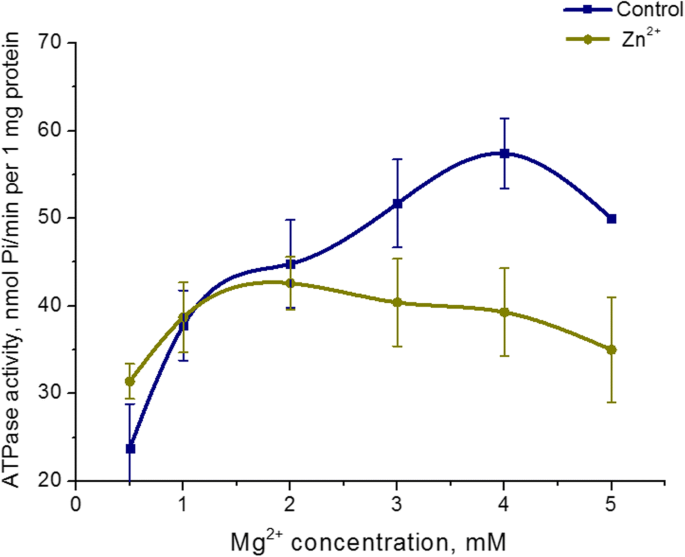
Dependencia de la actividad de la ATPasa de miosina S1 en Mg 2+ concentración en presencia de Zn 2+ 5 mM en comparación con un control (M ± SD, n =6)
Sitios de unión a Zn en Myosin S1
La simulación por computadora muestra que los cationes Zn tienen varias regiones de unión en la cabeza de miosina. Uno de ellos está ubicado en la parte inferior de la hendidura entre los subdominios superior e inferior de 50 kDa, cerca del sitio de unión de nucleótidos y directamente cerca del P-loop. Zn 2+ está coordinado con los átomos de oxígeno Glu177 (longitud de enlace 0,23 y 0,39 nm), con el átomo de oxígeno Ser178 (longitud de enlace 0,31 nm) y Arg236 (longitud de enlace 0,32 nm).
Otra región de unión a Zn se encuentra en la parte inferior del subdominio superior de 50 kDa (Leu218-Asp463, Glu605-Phe621) y cerca del conmutador 1 (Gly233-Phe246) y el bucle P. Zn 2+ puede coordinarse con el átomo de oxígeno Glu327 (longitud de enlace 0,21 nm), con un átomo de oxígeno Glu326 (longitud de enlace de 0,34 nm) y un átomo de oxígeno Asp323 (longitud de enlace 0,32 nm). El catión Zn también puede interactuar con la miosina S1 en la región que entra en contacto con el interruptor 2, interactuando con Glu 465 (0,24 nm), Asp468 (longitud de enlace 0,31 nm) y Leu653 (longitud de enlace 0,37 nm). Esta región de unión está cerca del sitio de unión de actina y la hendidura entre los subdominios superior e inferior de 50 kDa. La parte inferior de esta hendidura se encuentra en el bolsillo de unión de ATP. Estos vinculantes Zn 2+ Los dominios de miosina S1 juegan un papel esencial en la unión e hidrólisis del ATP. Estas regiones experimentan transformaciones conformacionales complejas en el proceso de transferencia de energía desde el sitio de hidrólisis de ATP a la superficie de unión de actina.
Thiacalix [4] arenes Elimina los efectos inhibidores del Zn 2+ sobre la actividad de ATPasa de miosina
Se agregaron cien micromolares de soluciones C-800 o C-798 en tampón Tris-HCl 50 mM (pH 7,2) al medio de incubación que contenía cationes Zn 5 mM para eliminar el impacto negativo de Zn 2+ sobre la actividad ATPasa de la miosina S1 del músculo liso uterino. Como control, se utilizó como actividad enzimática sin agregar zinc y / o tiacalix [4] arenos al medio de incubación. Se demostró (Fig. 5) que el compuesto C-800 no afecta la actividad ATPasa de la miosina S1 del miometrio. Aunque, el compuesto C-798 exhibe un pequeño efecto inhibidor sobre la actividad de la ATPasa de miosina S1 que probablemente esté relacionado con la extracción de una cierta cantidad de Mg 2+ [21], esencial para la unión de ATP en el centro activo y su hidrólisis, a partir del medio de incubación. No obstante, 100 μM C-798, así como C-800, eliminaron los efectos inhibidores de 5 mM Zn 2+ sobre el proceso de hidrólisis de ATP catalizada por miosina S1.
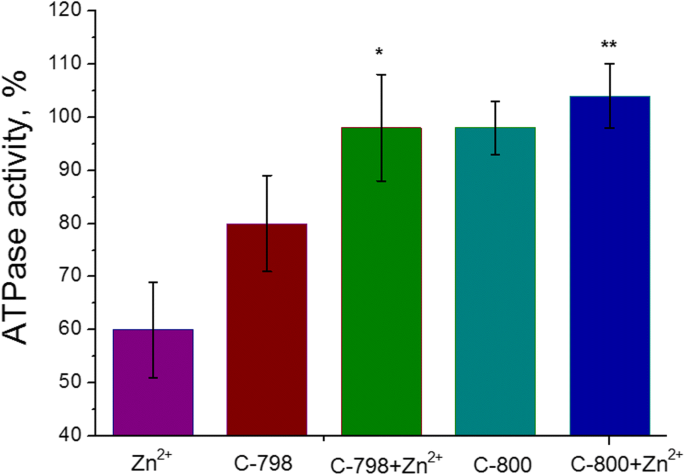
Efecto de C-798 y C-800 100 μM sobre la actividad ATPasa de miosina S1 en presencia de Zn 2+ 5 mM (M ± SD, n =5-6). El 100% es el valor de la actividad ATPasa sin la adición de catión Zn. La diferencia entre "Zn" y "Zn + C-798", así como entre los valores de "Zn" y "Zn + C-800", es estadísticamente significativa ( p <0.05) y se muestran como * y **, respectivamente
Mecanismos probables de la acción de restauración de C-798 y C-800 sobre la actividad de ATPasa de miosina S1 en presencia de Zn 2+
Uno de los mecanismos más probables de la acción restauradora de C-798 y C-800 sobre la actividad ATPasa de miosina S1 en Zn 2+ La presencia puede ser la capacidad de los tiacalix [4] arenos para unirse a los cationes Zn y, en consecuencia, excluir estos cationes del medio de incubación. Fue interesante si estos tiacalix [4] arenos pueden unirse a los cationes de zinc que ya están unidos a la miosina.
La simulación por computadora mostró que los tiacalix [4] arenos C-798 y C-800 con átomos de azufre puente entre anillos aromáticos están en la conformación de "cono" estabilizado por enlaces intrahidrógeno entre los grupos fenólicos. Se obtuvo la estructura de energía minimizada de estos cálices [4] arenos. La energía total de C-798 después de la minimización fue de 64,5 kcal / mol. La presencia de grupos ionizados en los bordes del calix [4] areno (en particular el inferior) aumenta significativamente la contribución de las interacciones electrostáticas a la energía total de la interacción huésped-huésped. También realizamos la “minimización” del C-798 — Zn 2+ complejo; su energía total fue de 83 kcal / mol.
C-798 se incrustó en la estructura de la miosina S1 que coopera con el catión Zn que previamente estaba unido a la proteína en la región del bucle P. En este caso, Zn 2+ interactúa con los átomos de oxígeno del borde inferior y el azufre de puente de C-798 (O3, 0,21 nm; S1, 0,30 nm; O2, 0,34 nm). Se muestra que Zn 2+ se desvía en cierta medida de los residuos de aminoácidos del bucle P y debilita su interacción con el átomo de oxígeno Glu177 (longitud de enlace de 0,43 nm) (Fig. 6).
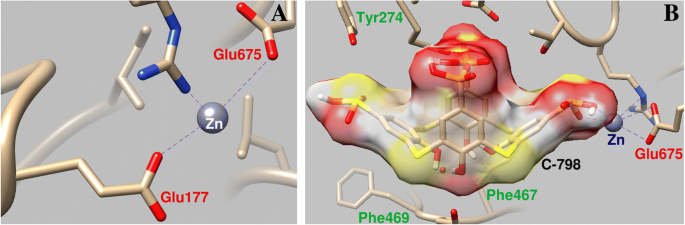
Parámetros geométricos de la interacción de Zn 2+ con la región del bucle P de la miosina S1 ( a ) y la influencia del C-798 en la cooperación del catión Zn con esta región ( b )
La fijación del C-798 en la "cavidad" de la región de unión de ATP de la miosina se produce con la participación de varios residuos de aminoácidos. En particular, la cesta hidrófoba de tiacalixareno se ha fijado por los residuos de aminoácidos aromáticos de miosina de Phe467 y Phe469; Los átomos de oxígeno cargados negativamente de tiacalixareno interactúan con los residuos de aminoácidos cargados positivamente de Arg570, Asn572 e His689.
El estudio de la influencia del C-798 en el cambio del Zn 2+ La posición durante el acoplamiento en el área cercana al sitio de unión de ATP de miosina demostró que Zn 2+ en presencia de tiacalix [4], el areno interactúa con los átomos de oxígeno del tercer grupo sulfonilo (O16–0.26 nm; O15–0.27 nm), casi no interactúa con los átomos de oxígeno Asp134 y Glu326, y la coordinación con Glu327 es mucho más débil (Longitud de acoplamiento de 0,43 nm) (Fig. 7). En este caso, el tiacalixareno se fija en la "cavidad" de la proteína con la participación de varios residuos de aminoácidos. En particular, los átomos de oxígeno cargados negativamente de los grupos tiacalixarenosulfonilo interactúan con los residuos de aminoácidos cargados positivamente de miosina de Lys188, Lys195 y Gln221.
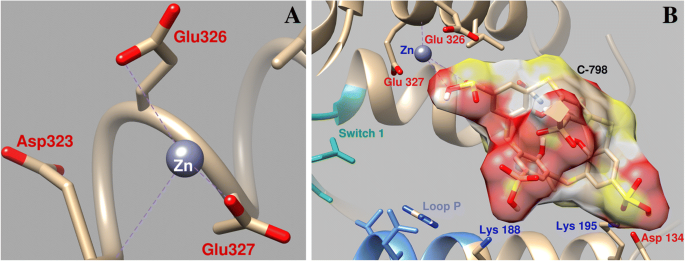
Parámetros geométricos de la interacción de Zn 2+ en el área cercana al interruptor 1 de miosina y el bucle P de la miosina S1 ( a ) y la influencia del C-798 en la cooperación de Zn 2+ con esta región ( b )
Se muestra que la esfera de energía condicional del catión Zn entra en contacto e incluso se superpone un poco con la superficie de propagación de interacciones electrostáticas debido a la presencia de átomos de oxígeno y átomos de azufre en C-798. Esto indica que el catión que se está estudiando está en interacción lo suficientemente estrecha con los átomos cargados negativamente de las coronas superior e inferior del C-798. Es probable que el tiacalixareno atraiga sobre sí mismo un Zn 2+ , como resultado de lo cual se debilita la interacción de los cationes con los residuos de aminoácidos de la enzima.
En consecuencia, los resultados del acoplamiento del C-798 en la región de miosina S1, que contiene Zn 2+ unido, indican la posibilidad de la interacción de los grupos funcionales C-798 con el catión Zn. En este caso, el enlace del catión Zn con los residuos de aminoácidos de la miosina S1 se debilitó significativamente y la distancia entre ellos aumenta. Como resultado, se puede eliminar el efecto adverso del catión Zn sobre la actividad ATPasa de la miosina.
También realizamos una simulación por computadora del efecto de calix [4] areno C-800, con acoplamiento en el área cercana a la región de unión de ATP de la miosina S1, para cambiar la geometría del catión Zn. Al mismo tiempo, Zn 2+ está en contacto con Arg236 (longitud de enlace de 0,37 nm), Glu675 (longitud de enlace de 0,41 nm) y átomos del calix funcional superior [4] residuos de areno (H26, 2,36 nm; H30, 2,96 nm; C30, 0,31 nm; O5, 3,7 nm; O16, 0,4 nm; O7, 0,48 nm; y O11, longitud de enlace de 0,51 nm). Zn 2+ interactúa con el calix [4] areno C-800, similar al C-798. El catión también se retira del sitio de unión anterior en esta región y está en contacto con Asp468 (longitud de enlace de 0,2 nm) y los átomos de la corona inferior de calixareno (C4, 1,96 nm; C14, 2,07 nm; S3, 2,16 nm; O2 , 2,26 nm; C3, 2,97 nm; C20, 3,10 nm; O4, 4,2 nm; C14, 3,0 nm; y O3, 4,1 nm).
El acoplamiento de C-798 y C-800 en la región del subfragmento 1 de miosina mostró que estos tiacalix [4] arenos podrían interactuar con los cationes Zn que se unen a los residuos de aminoácidos de la miosina cerca del sitio activo de la ATPasa. Por tanto, su efecto protector podría ser el resultado del debilitamiento de la interacción entre estos cationes y la miosina S1.
Discusión
Numerosas anomalías reproductivas femeninas son causadas por trastornos del músculo liso uterino (miometrio). Los metales pesados tienen un efecto adverso sobre la contractilidad del músculo liso uterino. El zinc de metal pesado es un elemento biogénico esencial para la mayoría de los organismos; altas dosis de este elemento son tóxicas [5]. Varias investigaciones de las concentraciones milimolares de Zn 2+ sobre los objetos vivos se describieron previamente [32]. Encontramos que el Zn 5 mM tiene el efecto inhibidor más pronunciado sobre la actividad de la ATPasa de miosina S1 del útero. Por lo tanto, los efectos adversos de los cationes Zn sobre la hidrólisis de ATP de miosina S1 se han estudiado más a fondo con esta concentración de Zn 2+ . El cálculo de los parámetros cinéticos de ATPasa de miosina S1 para ATP reveló que V máx., ATP de la actividad enzimática de la miosina en presencia de Zn 2+ 5 mM disminuyó en 1.6 veces. El valor de К m para la hidrólisis de ATP no cambia estadísticamente, aunque tiende a disminuir.
La miosina en condiciones fisiológicas es un Mg 2+ -ATPasa dependiente. El catión magnesio participa en la unión de ATP en el sitio activo de miosina, así como en la hidrólisis de ATP. El Mg 2+ se coordina en el sitio activo de la enzima con las cadenas laterales de los residuos de aminoácidos de miosina Thr-186 y Ser-237, así como con los grupos β- y γ-fosfato de la molécula de ATP con la formación de β- y γ- complejo bidentado así como con moléculas de agua activas, una de las cuales lleva a cabo un ataque nucleófilo sobre γ-fosfato ATP [33, 34]. Mg 2+ interactúa con los grupos de fósforo cargados negativamente del ATP, los polariza y, por lo tanto, facilita un ataque nucleofílico en el γ-fosfato terminal [14].
Se encontró que la actividad ATPasa de miosina S1 no es sensible a la presencia de Mg 2+ a una concentración de 5 mM de Zn 2+ en contraste con el control cuando el zinc estaba ausente en el medio de incubación [35, 36].
La actividad de la miosina ATPasa depende de la naturaleza del catión metálico y se correlaciona bien con su radio iónico. Los radios de iones Mg 2+ y Zn 2+ en las soluciones son muy similares (0,070 y 0,076 nm, respectivamente) [37]. Por lo tanto, la interacción de Zn 2+ cationes con el Mg 2+ -Es posible la unión de sitios de miosina. Por lo tanto, el Mg 2+ -los sitios de enlace pueden ser ocupados por Zn 2+ cationes en sus altas concentraciones. La actividad ATPasa de la miosina S1 en tales condiciones puede ser insensible a los cationes de magnesio. La miosina contiene dos sitios de alta afinidad para Mg 2+ y Mg 2+ unido a estos sitios tiene un papel fisiológico importante en el proceso de transducción de energía durante la contracción muscular. Todavía hay varios Mg 2+ - Sitios de unión además del sitio de ATPasa en la molécula de miosina, que difieren en la energía de unión de los iones de magnesio y su afinidad [35]. Por lo tanto, se puede suponer que Zn 2+ También puede unirse a otros sitios funcionalmente importantes de miosina S1 que afectan la unión e hidrólisis del ATP.
La simulación por computadora muestra que los cationes Zn tienen varias regiones de unión en la cabeza de miosina ubicadas cerca del sitio de unión de ATP, a saber, el bucle P y los subdominios superior e inferior de 50 kDa cambian 2. Estos Zn de unión 2+ Los dominios de miosina S1 juegan un papel esencial en la unión e hidrólisis del ATP. Estas regiones experimentan transformaciones conformacionales complejas en el proceso de transferir energía desde el sitio de hidrólisis de ATP a la superficie de unión de actina.
Los resultados del análisis obtenidos por Zn 2+ el acoplamiento en la miosina S1 indica que un papel clave en la unión de este catión a la molécula de miosina juega su interacción con grupos cargados negativamente de los residuos de aminoácidos de la enzima, en particular, Glu y Asp.
La influencia nociva de las concentraciones tóxicas de Zn 2+ Los cationes sobre la actividad ATPasa de la miosina S1 requiere la búsqueda de compuestos farmacológicos que puedan eliminar la acción de este metal. Los objetos de nuestro estudio fueron tetrahidroxitiacalix [4] areno-tetrasulfonato (C-798) y tetrahidroxitiacalix [4] areno-tetrafosfonato (C-800) que son capaces de quelar metales de transición y pesados con la formación de complejos metálicos estables (Fig. 1). La corona macrocíclica superior de C-798 y C-800 contiene cuatro grupos sulfonato aniónicos o cuatro fosfonatos, respectivamente, que proporcionan buena solubilidad en agua del tiacalixareno y adhesión a moléculas de proteína debido a contactos electrostáticos con átomos de nitrógeno cargados positivamente de fragmentos de aminoácidos [21 ].
El acoplamiento de C-798 y C-800 en la región de miosina S1 mostró que estos tiacalix [4] arenos podrían interactuar con los cationes Zn que se unen a los residuos de aminoácidos de miosina cerca del sitio activo de la ATPasa. Por tanto, su efecto protector podría ser el resultado del debilitamiento de la interacción entre estos cationes y la miosina S1. Se especuló que los resultados obtenidos podrían ser utilizados para futuras investigaciones con el objetivo de utilizar estos tiacalix [4] arenos como compuestos farmacológicos en el caso de intoxicaciones con altas concentraciones de zinc.
Conclusiones
La alta concentración (5 mM) de catión Zn inhibió la actividad de la ATPasa de miosina S1 del útero. La influencia inhibida del Zn está relacionada con una disminución de la velocidad máxima del ATP de hidrólisis catalizada por la miosina S1 en presencia de Zn 2+ 5 mM . El valor de К m para ATP no cambia estadísticamente, aunque tiende a disminuir.
El tetrahidroxitiacalix [4] areno-tetrasulfosfonato (C-798) y el tetrahidroxitiacalix [4] areno-tetrafosfonato (C-800) restauraron la actividad de la miosina S1 ATPasa al nivel de control en presencia de 5 mM de Zn 2+ .
Los cationes Zn tienen varias regiones de unión en la miosina S1 ubicadas cerca del sitio activo de la ATPasa. El acoplamiento de C-798 y C-800 en la región de miosina S1, que contiene Zn 2+ enlazado, indica la posibilidad de la interacción de estos grupos funcionales tiacalix [4] areno con cationes Zn enlazados. El enlace del catión Zn con los residuos de aminoácidos de la miosina S1 se debilitó significativamente y la distancia entre ellos aumenta. Como resultado, se puede eliminar el efecto adverso del catión Zn sobre la actividad ATPasa de la miosina.
Se asume que los resultados obtenidos podrían ser utilizados para futuras investigaciones con el objetivo de utilizar estos tiacalix [4] arenos como compuestos farmacológicos en el caso de intoxicaciones con altas concentraciones de zinc.
Métodos
Reactivos
Se utilizaron los siguientes reactivos:albúmina sérica, EGTA, EDTA, ATP, ácido ascórbico, Tris, tricina, ditiotreitol, acrilamida, (Sigma, EE. UU.), Glicina (Merck, Alemania), N, N'-metilenbisacrilamida (Acros Organics, Bélgica ) N, N, N ′, N′-tetrametilendiamina (Reanal, Hungría) y reactivos de producción nacional (grado R). Las soluciones se prepararon en agua purificada en el sistema Crystal Bio (Adrona, Letonia). La conductancia del agua fue inferior a 0,1 µS. La concentración de los cationes metálicos divalentes en solución se determinó mediante el método de Mohr.
Aislamiento del subfragmento 1 de actomiosina y miosina
La actomiosina se aisló del músculo liso uterino de cerdo mediante el método de Barany modificado como se describe en [17]. La miosina S1 se obtuvo de la actomiosina de cerdo mediante el método Suzuki modificado [24]. The purity of the samples was controlled by PAAG-SDS electrophoresis [25].
ATPase Activity Assay
ATPase activity of myosin S1 was determined in a 96-well plate at 37 °C in an incubation medium (total volume 0.1 ml) of the following composition (mM):Tris-HCl buffer (pH 7.2), 20; KCl, 100; CaCl2 , 0.01; MgCl2 , 5; and ATP, 3 (standard conditions). Protein (myosin S1) concentration was 20 μg/ml. Incubation time was 5 min. Samples containing all components of the incubation medium without myosin S1 were taken as control of non-enzyme hydrolysis of ATP. The amount of inorganic phosphate released during ATP hydrolysis reaction was determined by the Chen method [26] by the measurement of optical absorbance of the solution at 820 nm using a microplate reader μQuwant (Biotek @ Instruments, Inc., USA) and specified as Pi nmol/min per 1 mg of protein.
The Zn 2+ and thiacalix[4]arene effects on the ATPase activity of myosin S1 were studied using standard incubation medium with solutions of ZnCl2 and thiacalix[4]arenes at the corresponding concentrations. The value of ATPase activity in the absence of ZnCl2 and/or calix[4]arenes in the incubation medium was taken as 100% (control).
Kinetic and Statistical Analysis
The values of the imaginary constant of Michaelis (K m ) and maximal rate of myosin S1 ATPase for ATP (V max, ATP ) were calculated using the graph of the dependence of ATPase activity on the ATP concentration according to Lineweaver–Burk method [27]. Statistical processing of the obtained data was performed using standard methods of variation statistics. Experimental data were analyzed by using the standard software “MS Office” and “Statistica 4.5.” The statistical comparisons were performed using two-way analysis of variances (ANOVA).
Thiacalix[4]Arene Synthesis and Characterization
Tetrahydroxy-thiacalix[4]arene-tetrasulphonate and tetrahydroxy-thiacalix[4]arene-tetraphosphonate were synthesized and characterized using NMR techniques and IR spectroscopy in the Phosphoranes Chemistry Department of the Institute of Organic Chemistry, NAS of Ukraine. Infrared and NMR spectroscopy confirmed the structure of these synthesized thiacalix[4]arenes. This thiacalix[4]arenes were dissolved in water.
Computer Modeling
Computer modeling of the interaction between ligands (thiacalix[4]arenes, Zn 2+ , model bindings) and receptor (myosin S1) was performed using AutoDock software, version 4.2 [28]. We used the three-dimensional enzyme structure with the 1b7t identifier in RSCB PDB in our research [29]. Computer modeling of the thiacalix[4]arene structural peculiarities was carried out using HyperChem 7.01. Molecular dynamics calculations were performed by the MM2 method with the semi-empirical methods (CNDO).
Program AutoDockTools was used for preliminary “processing” of interacting molecules. One hundred runs of Lamarkian genetic algorithms (population size, 100; the maximal number of energy evaluations, 10 6 ) were conducted. To analyze and visualize the docking results, we used the programs Chimera [30] and Yassara [31]. Calculation of the minimal total binding energy was implemented considering Van der Waals forces, electrostatic and hydrophobic interactions, and hydrogen bonds. The optimal ligand positions in the complex “receptor-ligand” were determined according to the energy values obtained by docking software calculator for binding energy in complex “receptor-ligand.” Thus, we selected a series of complexes with the lowest total energy and then calculated the optimal geometry of the complexes and determined the most energetically preferred arrangement of the ligands in the space of myosin subfragment-1 binding domain.
Abreviaturas
- C-798:
-
Tetrahydroxythiacalix[4]arene-tetrasulfosphonate
- C-800:
-
Tetrahydroxythiacalix[4]arene-tetraphosphonate
- CNDO:
-
Complete Neglect of Differential Overlap (methods)
- K m :
-
Michaelis constant, the substrate concentration at which the reaction rate of the enzyme is half of the maximal velocity
- L50:
-
Lower 50-kDa domain of myosin
- LD50 :
-
Lethal dose is the amount of an ingested substance that kills 50% of a test sample
- MM2:
-
A class of force fields
- Myosin S1:
-
Myosin subfragment-1
- NASU:
-
National Academy of Science of Ukraine
- PDB:
-
Protein Data Bank
- P-loop:
-
Phosphate-binding loop of myosin
- RCSB:
-
Research Collaboratory for Structural Bioinformatics
- U50:
-
The upper 50-kDa domain of myosin
- V máx :
-
Maximal velocity of the enzyme
- V max, ATP :
-
V máx for ATP
Nanomateriales
- Acero galvanizado versus acero galvanizado:¿Cuál es la diferencia?
- Los efectos de COVID-19 en la fabricación
- La administración de nanopartículas de artesunato mejora la eficacia antitumoral activando la apoptosis celular mediada por mitocondrias
- Los efectos de la relación Li / Nb en la preparación y el rendimiento fotocatalítico de los compuestos Li-Nb-O
- Efectos del espesor de la bicapa en las propiedades morfológicas, ópticas y eléctricas de los nanolaminados de Al2O3 / ZnO
- Los efectos positivos de la automatización agrícola
- Cortes de energía:5 formas de prevenir los efectos negativos
- Los efectos del empuje radial en las bombas centrífugas
- Los efectos de combustión del plasma y el oxígeno/combustible
- Los efectos de los elementos de aleación comunes
- ¿Cuáles son los efectos de la actual escasez de níquel?



